文档内容
元素电离能、电负性的规范解答
1.元素的电离能
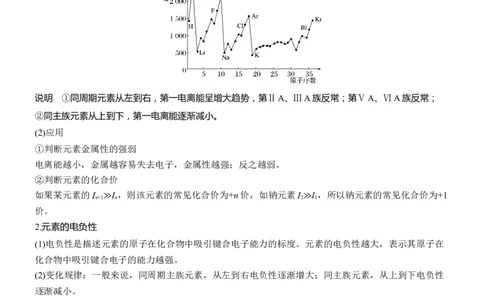
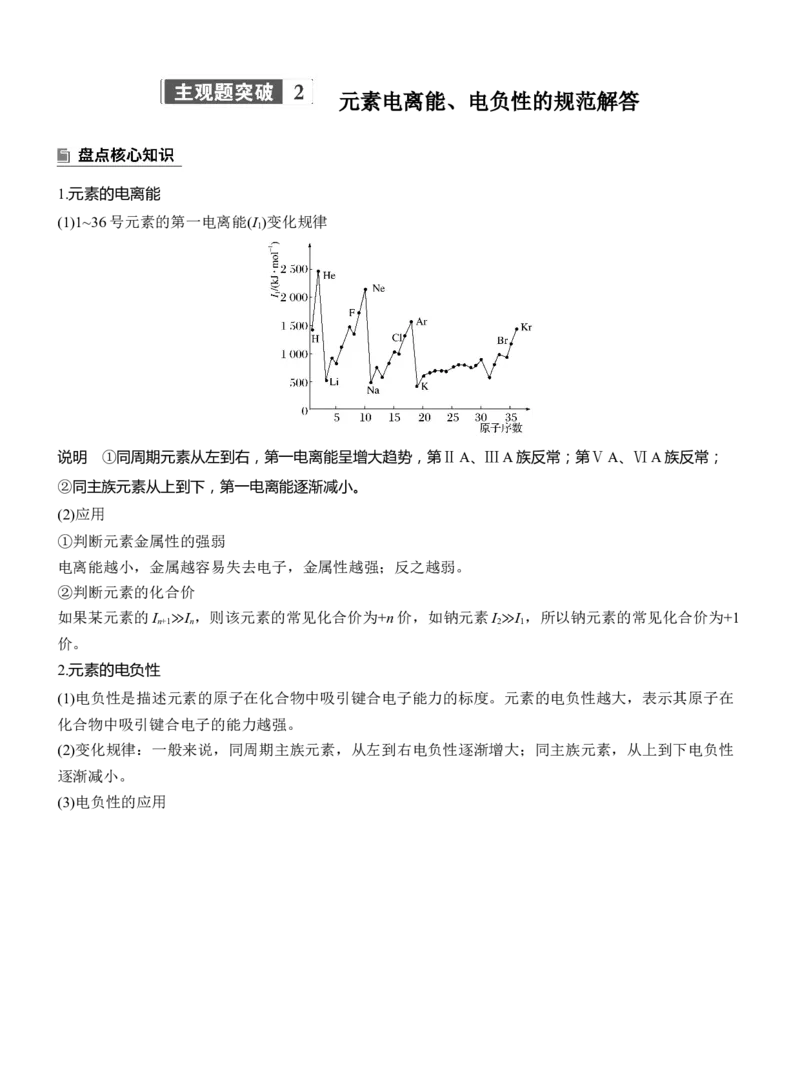
(1)1~36号元素的第一电离能(I )变化规律
1
说明 ①同周期元素从左到右,第一电离能呈增大趋势,第ⅡA、ⅢA族反常;第ⅤA、ⅥA族反常;
②同主族元素从上到下,第一电离能逐渐减小。
(2)应用
①判断元素金属性的强弱
电离能越小,金属越容易失去电子,金属性越强;反之越弱。
②判断元素的化合价
如果某元素的I I ,则该元素的常见化合价为+n价,如钠元素I I ,所以钠元素的常见化合价为+1
n+1 n 2 1
价。
≫ ≫
2.元素的电负性
(1)电负性是描述元素的原子在化合物中吸引键合电子能力的标度。元素的电负性越大,表示其原子在
化合物中吸引键合电子的能力越强。
(2)变化规律:一般来说,同周期主族元素,从左到右电负性逐渐增大;同主族元素,从上到下电负性
逐渐减小。
(3)电负性的应用1.[2023·北京,15(2)]比较S原子和O原子的第一电离能大小,从原子结构的角度说明理由: 。
2.[2023·浙江1月选考,17(2)改编]由硅原子核形成的三种微粒,电子排布式分别为:①[Ne]3s23p2、
②[Ne]3s23p1、③[Ne]3s23p14s1,则电离一个电子所需最低能量由大到小的顺序为 。
3.[2022·河北,17(1)(2)](1)基态S原子的价电子中,两种自旋状态的电子数之比为 。
(2)Cu与Zn相比,第二电离能与第一电离能差值更大的是 ,原因是 。
4.(1)[2020·全国卷Ⅲ,35(1)]H、B、N中,原子半径最大的是 。根据对角线规则,B的一些化
学性质与元素 的相似。
(2)[2021·湖南,18(2)②节选]H、C、N的电负性由大到小的顺序为 。
(3)[2021·山东,16(2)节选]O、F、Cl电负性由大到小的顺序为 。
(4)[2020·江苏,21A(2)节选]C、N、O元素的第一电离能由大到小的顺序为 。
5.[2020·全国卷Ⅰ,35(1)(2)]Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面
的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为 。
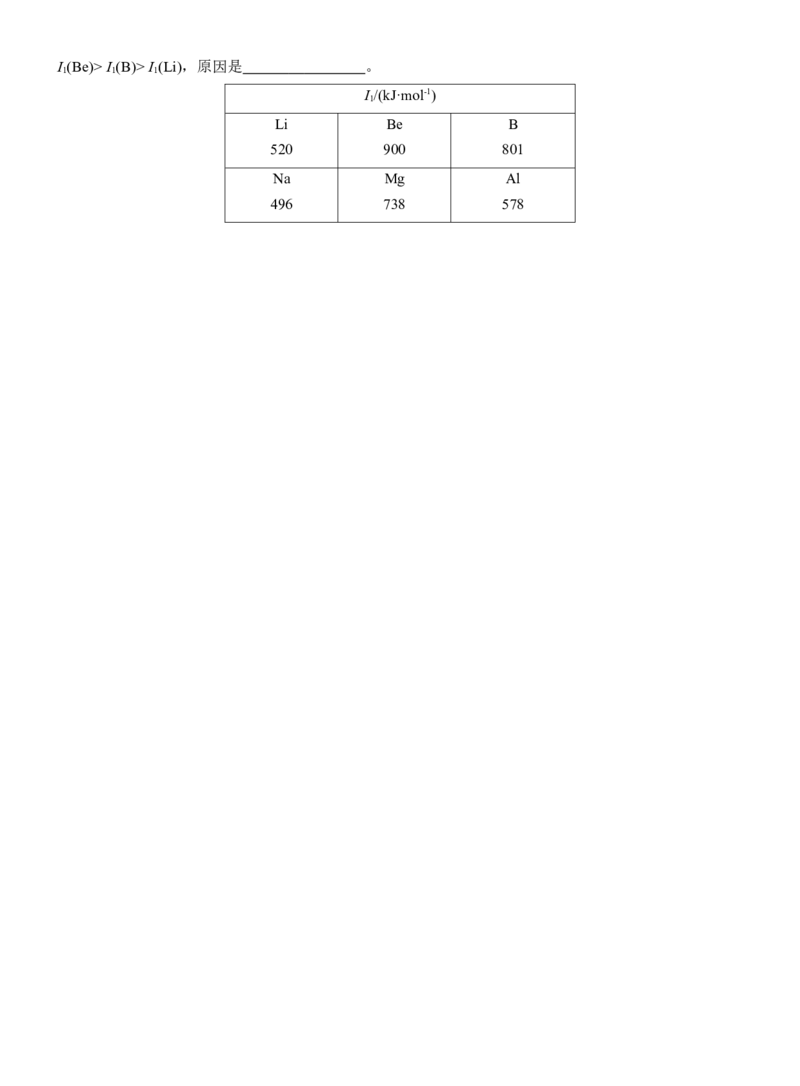
(2)Li及其周期表中相邻元素的第一电离能(I )如表所示。I (Li)> I (Na),原因是 。
1 1 1I (Be)> I (B)> I (Li),原因是 。
1 1 1
I /(kJ·mol-1)
1
Li Be B
520 900 801
Na Mg Al
496 738 578答案精析
精练高考真题
1.I (O)>I (S),氧原子半径小,原子核对最外层电子的吸引力大,不易失去一个电子
1 1
2.②>①>③
3.(1)1∶2(或2∶1) (2)Cu Cu的第一电离能比Zn的第一电离能小,但Cu失去1个电子后形成的Cu+的价
层电子排布为3d10,较难失去电子,Zn失去1个电子后形成的Zn+的价层电子排布为3d104s1,较易失去1
个电子达到稳定状态,Cu的第二电离能比Zn的第二电离能大
4.(1)B Si (2)N>C>H (3)F>O>Cl (4)N>O>C
5.(1)4∶5 (2)Na与Li同主族,Na的电子层数更多,原子半径更大,更易失电子,故第一电离能更小
Li、Be和B为同周期元素,同周期元素从左至右,第一电离能呈现增大的趋势;但由于基态Be原子的s
能级轨道处于全充满状态,能量更低更稳定,故其第一电离能大于B的
解析 (1)基态Fe2+的价层电子排布式为3d6,未成对电子数为4,基态Fe3+的价层电子排布式为3d5,未成
对电子数为5,所以两者之比为4∶5。