文档内容
常见无机物的性质、转化及应用
(一)常见无机物的性质及应用
1.常见杀菌剂、消毒剂、净水剂
性质 用途
明矾、铁盐水解生成胶体,具有吸附性 明矾作净水剂(混凝剂)
次氯酸钠是含氯消毒剂,具有氧化性 用“84”消毒液消毒
二氧化氯具有较强的氧化性 可用于自来水的杀菌消毒
漂白粉(次氯酸盐)具有强氧化性 可作杀菌消毒剂,还可作漂白剂
K FeO 是强氧化剂,还原产物铁离子水
2 4
K FeO 作新型净水剂
2 4
解生成氢氧化铁胶体
2.常见干燥剂、还原剂与食品安全
性质 用途
氮气的化学性质稳定 作食品保护气
生石灰、无水氯化钙、硅胶能吸水 可作(食品)干燥剂
P O 能与水反应 可作干燥剂(不可用于食品)
2 5
Fe、FeO具有还原性 食品的抗氧化剂
SO 既可以杀菌又具有还原性 在葡萄酒中可以微量添加
2
3.其他生产、生活中的物质
性质 用途
Al(OH) 有弱碱性 可用于治疗胃酸过多
3
NaHCO 受热分解生成CO 、能与酸反应 可用作焙制糕点的膨松剂、胃酸中和剂
3 2
明矾溶液显酸性 古代用明矾溶液清除铜镜表面的铜锈
肥皂水显碱性 作蚊虫叮咬处的清洗剂铝有还原性,与氧化铁发生铝热反应 可用于焊接铁轨、冶炼难熔金属
Na CO 水解使溶液显碱性 用热的纯碱溶液洗去油污
2 3
草木灰含碳酸钾,水解显碱性 铵态氮肥(如硫酸铵)不能和草木灰混合施用
硅是常用的半导体材料 可作太阳能电池板、电脑芯片
二氧化硅导光能力强 可作光导纤维
4HF+SiO ===2H O+SiF ↑ 用HF刻蚀玻璃
2 2 4
Al具有良好的延展性和抗腐蚀性 常用铝箔包装物品
MgO、Al O 的熔点很高 作耐高温材料
2 3
水玻璃(硅酸钠)不燃不爆 可用作耐火材料等
锌的活泼性大于铁 在海轮外壳上装若干锌块以减缓船体腐蚀
(二)常见无机物的性质与转化
1.常见的金属氧化物
化学式
颜色状态
与水作用
Na O
2
白色固体
反应生成NaOH
Na O
2 2
淡黄色固体
反应生成NaOH和O
2
MgO
白色固体
缓慢反应生成Mg(OH)
2
Al O
2 3
白色固体
不溶于水,
也不与水反应FeO
黑色粉末
Fe O
2 3
红棕色粉末
Fe O
3 4
黑色晶体
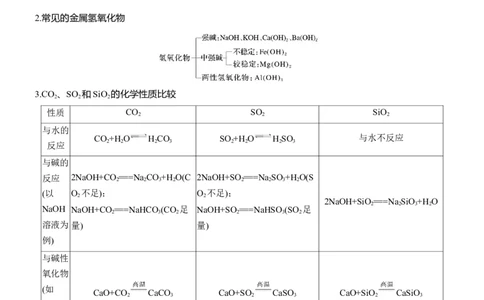
2.常见的金属氢氧化物
3.CO 、SO 和SiO 的化学性质比较
2 2 2
性质 CO SO SiO
2 2 2
与水的
CO +H O H CO SO +H O H SO 与水不反应
反应 2 2 2 3 2 2 2 3
与碱的
反应 2NaOH+CO ===Na CO +H O(C 2NaOH+SO ===Na SO +H O(S
2 2 3 2 2 2 3 2
(以 O 不足); O 不足);
2 2
2NaOH+SiO ===Na SiO +H O
2 2 3 2
NaOH NaOH+CO ===NaHCO (CO 足 NaOH+SO ===NaHSO (SO 足
2 3 2 2 3 2
溶液为量) 量)
例)
与碱性
氧化物
(如
CaO+CO CaCO CaO+SO CaSO CaO+SiO CaSiO
2 3 2 3 2 3
CaO)
反应
与
Na CO +SiO Na SiO +CO
Na CO Na CO +CO +H O===2NaHCO Na CO +SO ===Na SO +CO 2 3 2 2 3 2
2 2 3 2 2 3 2 3 2 2 3 2
↑
反应
3
2H S+SO ===3S↓+2H O,
2 2 2
与酸的
— 2HNO (稀) SiO +4HF===SiF ↑+2H O
3 2 4 2
反应
+3SO +2H O===2NO+3H SO
2 2 2 44.HCl、H S和NH 的化学性质比较
2 3
性质 HCl H S NH
2 3
水溶液显强酸性,与碱反 水溶液显弱酸性,与碱反应
水溶液显弱碱性,与酸反应生成
酸碱性 应生成盐和水,如 生成盐和水,如
盐,如NH +HCl===NH Cl
3 4
NaOH+HCl===NaCl+H O 2NaOH+H S===Na S+2H O
2 2 2 2
与活泼金属反应,表现氧
与较活泼金属反应,表现氧
氧化性 化性,如 -
化性
Fe+2HCl===FeCl +H ↑
2 2
与强氧化剂(如MnO 、 与较强的氧化剂(如O 、Cl 、
2 2 2
KClO 等)反应: 与某些金属氧化物(如CuO等)反
3
SO 等)反应:H S+Cl
还原性 2 2 2
MnO +4HCl(浓) MnCl S↓+2HCl, 应:3CuO+2NH 3Cu+N +3H O
2 2 3 2 2
+Cl ↑+2H O 2H S+SO ===3S↓+2H O
2 2 2 2 2
先生成白色沉淀,后沉淀溶解:
与
生成白色沉淀: 生成黑色沉淀: AgNO +NH +H O===AgOH↓+NH
3 3 2 4
AgNO
3
AgNO +HCl===AgCl↓+HN2AgNO +H S===Ag S↓+2HNNO 、
3 3 2 2 3
溶液
O O AgNO +3NH +H O===[Ag(NH ) ]OH
3 3 3 3 2 3 2
反应
+NH NO
4 3
考向一 物质的性质与用途
1.(2024·甘肃,3)化学与生活息息相关,下列对应关系错误的是( )
物质
性质
用途
A
次氯酸钠
氧化性
衣物漂白
B
氢气
可燃性
制作燃料电池
C
聚乳酸
生物可降解性制作一次性餐具
D
活性炭
吸附性
分解室内甲醛
2.(2024·浙江6月选考,2)下列说法不正确的是( )
A.Al(OH) 呈两性,不能用于治疗胃酸过多
3
B.Na O 能与CO 反应产生O ,可作供氧剂
2 2 2 2
C.FeO有还原性,能被氧化成Fe O
3 4
D.HNO 见光易分解,应保存在棕色试剂瓶中
3
3.(2024·北京,8)关于Na CO 和NaHCO 的下列说法中,不正确的是( )
2 3 3
A.两种物质的溶液中,所含微粒的种类相同
B.可用NaOH溶液使NaHCO 转化为Na CO
3 2 3
C.利用二者热稳定性差异,可从它们的固体混合物中除去NaHCO
3
D.室温下,二者饱和溶液的pH差约为4,主要是由于它们的溶解度差异
考向二 物质的性质与转化
4.(2023·辽宁,3)下列有关物质的工业制备反应错误的是( )
A.合成氨:N +3H 2NH
2 2 3
B.制HCl:H +Cl 2HCl
2 2
C.制粗硅:SiO +2C Si+2CO↑
2
D.冶炼镁:2MgO(熔融) 2Mg+O ↑
2
5.(2023·重庆,3)下列叙述正确的是( )
A.Mg分别与空气和氧气反应,生成的产物相同
B.SO 分别与H O和H S反应,反应的类型相同
2 2 2
C.Na O 分别与H O和CO 反应,生成的气体相同
2 2 2 2
D.浓H SO 分别与Cu和C反应,生成的酸性气体相同
2 4
6.(2024·安徽,4)下列选项中的物质能按图示路径在自然界中转化。且甲和水可以直接生成乙的是(
)
选项 甲 乙 丙A Cl NaClO NaCl
2
B SO H SO CaSO
2 2 4 4
C Fe O Fe(OH) FeCl
2 3 3 3
D CO H CO Ca(HCO )
2 2 3 3 2
7.(2024·全国甲卷,10)四瓶无色溶液NH NO 、Na CO 、Ba(OH) 、AlCl ,它们之间的反应关系如图所
4 3 2 3 2 3
示。其中a、b、c、d代表四种溶液,e和g为无色气体,f为白色沉淀。下列叙述正确的是( )
A.a呈弱碱性
B.f可溶于过量的b中C.c中通入过量的e可得到无色溶液
D.b和d反应生成的沉淀不溶于稀硝酸答案精析
精练高考真题
1.D [由于次氯酸钠有强氧化性,所以次氯酸钠可作漂白剂,用于衣物漂白,A正确;氢气是可燃气体,
能在氧气中燃烧,被氧气氧化,可制作燃料电池,B正确;聚乳酸具有生物可降解性,无毒,是高分子,
可以制作一次性餐具,C正确;活性炭有吸附性,能够有效吸附空气中的有害气体、去除异味,但无法分
解甲醛,D错误。]
2.A [Al(OH) 能够中和胃中的盐酸,因此可以用于治疗胃酸过多,A不正确;Na O 能与CO 反应生成
3 2 2 2
Na CO 和O ,故可作供氧剂,B正确;FeO中Fe元素的化合价为+2价,具有还原性,用适当的氧化剂可
2 3 2
以将其氧化成更高价态的Fe O ,C正确。]
3 4
3.D [Na CO 和NaHCO 的溶液中均存在H O、H CO
、H+、OH-、Na+、CO2- 、HCO-
,A正确;NaHCO
2 3 3 2 2 3 3 3 3
中加入NaOH溶液会发生反应:NaOH+NaHCO ===Na CO +H O,B正确;NaHCO 受热易分解,可转化为
3 2 3 2 3
Na CO ,而Na CO 热稳定性较强,利用二者热稳定性差异,可从它们的固体混合物中除去NaHCO ,C正
2 3 2 3 3
确;室温下,Na CO 和NaHCO
饱和溶液pH相差较大的主要原因是CO2- 的水解程度远大于HCO-
,D错
2 3 3 3 3
误。]
4.D [冶炼金属镁是电解熔融氯化镁,反应方程式为MgCl (熔融) Mg+Cl ↑,D错误。]
2 2
5.C [镁在空气中燃烧部分会与氮气反应生成氮化镁,A错误;SO 与H O发生化合反应生成亚硫酸,而
2 2
和H S会发生氧化还原反应生成硫单质,反应的类型不相同,B错误;Na O 分别与H O和CO 反应,生
2 2 2 2 2
成的气体均为氧气,C正确;浓H SO 与Cu反应生成二氧化硫气体,而和C反应生成二氧化碳和二氧化硫,
2 4
生成的酸性气体不相同,D错误。]
6.D [NaClO(乙)与浓盐酸反应生成NaCl(丙)、Cl 和H O,NaCl(丙)电解生成Cl (甲),Cl (甲)与水反应生成
2 2 2 2
HClO和HCl,无法直接生成NaClO(乙),故A项不符合;H SO (乙)与Ca(OH) 反应生成CaSO (丙)和水,
2 4 2 4
CaSO (丙)很稳定,加热至1 200 ℃以上分解,生成CaO、SO (甲)和O ,SO (甲)与水反应生成H SO 而不
4 2 2 2 2 3
是H SO (乙),故B项不符合;Fe(OH) (乙)与盐酸反应生成FeCl (丙)和水,FeCl (丙)不能直接转化为
2 4 3 3 3
Fe O (甲),Fe O (甲)与水不反应,不能生成Fe(OH) (乙),故C项不符合;CO (甲)与水反应生成H CO (乙),
2 3 2 3 3 2 2 3
H CO (乙)与CaCO 反应生成Ca(HCO ) (丙),Ca(HCO ) (丙)受热分解生成CO (甲),故D项符合。]
2 3 3 3 2 3 2 2
7.B [a与b反应需要加热,且产生的e为无色气体,则a和b分别为NH NO 和Ba(OH) 中的一种,产生
4 3 2
的气体e为NH ;b和c反应生成白色沉淀f,NH NO 不会与其他三种溶液产生沉淀,可确定b为Ba(OH)
3 4 3 2
溶液,a为NH NO 溶液;c与b和d反应均产生沉淀f,c应为AlCl 溶液,则d为Na CO 溶液,生成的白
4 3 3 2 3
色沉淀f为Al(OH) ,无色气体g为CO 。a为NH NO 溶液,N H+ 水解使溶液显酸性,A错误;Al(OH) 可
3 2 4 3 4 3
溶于强碱溶液,B正确;AlCl 溶液中通入NH 会生成Al(OH) 沉淀,但Al(OH) 不溶于弱碱,继续通入
3 3 3 3
NH 不能得到无色溶液,C错误;Ba(OH) 与Na CO 反应生成的BaCO 沉淀可溶于稀硝酸,D错误。]
3 2 2 3 3