文档内容
平衡体系中的有关计算
1.转化率、产率的计算公式
反应物的变化量
反应物的转化率= ×100%
反应物的起始量
生成物的实际产量
生成物的产率= ×100%
生成物的理论产量
2.分压与压强平衡常数
对于可逆反应:aA(g)+bB(g) cC(g)+dD(g),在一定温度下达到化学平衡时,若用p(A)、p(B)、
p(C)、p(D)分别表示A、B、C、D各气体的分压,用K 表示压强平衡常数,则有:
p
(1)p(C)=平衡时的总压×物质C的物质的量分数。
pc (C)·pd (D)
(2)K = 。
p pa (A)·pb (B)
3.相关反应平衡常数的相互计算
(1)同一可逆反应中,K ·K =1。
正 逆
(2)同一化学方程式中的化学计量数等倍扩大或缩小n倍,则新平衡常数K'与原平衡常数K间的关系是
K'=Kn或K'=√n K。
(3)几个可逆反应的化学方程式相加得总化学方程式,则总化学反应的平衡常数等于各分步反应平衡常
数之积。
4.速率方程、速率常数及应用
对于基元反应:aA(g)+bB(g) dD(g)+eE(g)
(1)速率方程v =k ·ca(A)·cb(B);v =k ·cd(D)·ce(E)。
正 正 逆 逆
(2)速率常数(k)是一个与温度有关,而与浓度、压强无关的量。
k
(3)基元反应的平衡常数K= 正。
k
逆
5.多平衡体系中有关平衡常数的计算技巧
(1)有关多平衡体系平衡常数的计算,如何确定多个反应相关联物质在平衡时量的多少是解题的关键点。
若用常规的三段式计算,对反应过程分析要求高,容易出错。但无论多少个反应,反应进行的程度如
何,反应前后的原子总数是不变的,因而解答这类问题可用原子守恒法,可规避对反应过程的分析。
(2)原子守恒法解题基本思路类型1 连续型多反应体系
连续平衡是指两个可逆反应有关联,第一个反应的某一生成物是第二个反应的反应物。解题时要注意
如果该物质是第一个反应的生成物,第二个反应的反应物,则在第一个反应中,该物质的初始量为0,
它的平衡量则为第二个反应中该物质的初始量(计算第二个反应的转化率尤为重要)。
例1 [2023·河北,17(1)③]氮是自然界重要元素之一,研究氮及其化合物的性质以及氮的循环利用对
解决环境和能源问题都具有重要意义。
恒温下,将1 mol空气(N 和O 的体积分数分别为0.78和0.21,其余为惰性组分)置于容积为V L的恒容
2 2
密闭容器中,假设体系中只存在如下两个反应:
ⅰ.N (g)+O (g) 2NO(g) K ΔH
2 2 1 1
ⅱ.2NO(g)+O (g) 2NO (g) K ΔH =-114 kJ·mol-1
2 2 2 2
若上述平衡体系中c(NO )=a mol·L-1,c(NO)=b mol·L-1,则c(O )= mol·L-1,K =
2 2 1
(写出含a、b、V的计算式)。
b2
0.21 2a+b
答案 - 0.78 a+b 0.21 2a+b
V 2 ( - )×( - )
V 2 V 2
解析 根据三段式:
N (g) + O (g) 2NO(g)
2 2
0.78 0.21
起始/(mol·L-1) 0
V V
a+b a+b
转化/(mol·L-1) a+b
2 2
0.78 a+b 0.21 a+b
平衡/(mol·L-1) - - a+b
V 2 V 2
2NO(g) + O (g) 2NO (g)
2 2
0.21 a+b
起始/(mol·L-1) a+b - 0
V 2
a
转化/(mol·L-1) a a
20.21 a+b a
平衡/(mol·L-1) b - - a
V 2 2
b2
0.21 2a+b c2 (NO)
c(O )=( - )mol·L-1,K = = 0.78 a+b 0.21 2a+b 。
2 V 2 1 c(N )·c(O ) ( - )×( - )
2 2 V 2 V 2
类型2 竞争反应(平行反应)
例2 CO
2
在 Cu⁃ZnO催化下,同时发生如下反应Ⅰ、Ⅱ,是解决温室效应和能源短缺的重要手段。
Ⅰ.CO (g)+3H (g) CH OH (g)+H O(g) ΔH <0
2 2 3 2 1
Ⅱ.CO (g)+H (g) CO(g)+H O(g) ΔH >0
2 2 2 2
保持温度T时,在容积不变的密闭容器中,充入一定量的CO 及H ,起始及达到平衡时,容器内各气
2 2
体物质的量及总压强如下表:
CO
2
H
2
CH OH(g)
3
CO
H O(g)
2
总压
强/kPa
起始/mol
0.5
0.9
0
0
0
p
0
平衡/mol
n
0.3
p
若反应Ⅰ、Ⅱ均达到平衡时,p =1.4p,则表中n= ;反应Ⅰ的平衡常数K = kPa-2(用含
0 p
p的式子表示)。
思路引导 利用C、H、O原子守恒计算平衡时各物质的物质的量,再求各物质的平衡分压,带入平衡常
数表达式计算。75
答案 0.2
2p2
解析 设平衡时CO 为x mol,H 为y mol,CO为z mol,根据:
2 2
C守恒:x+n+z=0.5
H守恒:2y+4n+0.3×2=0.9×2
O守恒:2x+n+0.3+z=0.5×2
0.5+0.9 1.4
由p =1.4p知, = ,
0 x+ y+n+0.3+z 1
解得:x=0.2,y=0.2,z=0.1,n=0.2。
平衡后气体总物质的量:(0.2+0.2+0.2+0.1+0.3) mol=1.0 mol。平衡后各物质的分压:CO (g):0.2p kPa,
2
H (g):0.2p kPa,CH OH (g):0.2p kPa,H O(g):0.3p kPa。
2 3 2
0.2p×0.3p 75
则反应Ⅰ的平衡常数K = kPa-2= kPa-2。
p (0.2p) 3×0.2p 2p2
1.[2024·安徽,17(2)(3)]乙烯是一种用途广泛的有机化工原料。由乙烷制乙烯的研究备受关注。回答下
列问题:
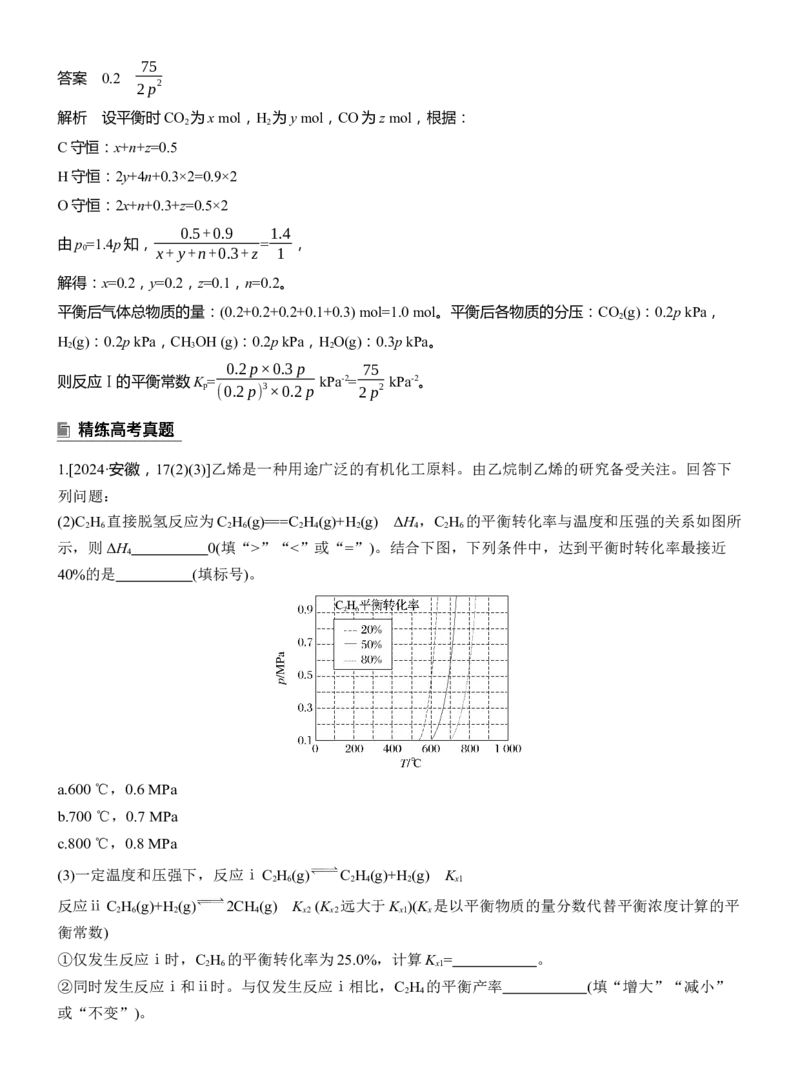
(2)C H 直接脱氢反应为C H (g)===C H (g)+H (g) ΔH ,C H 的平衡转化率与温度和压强的关系如图所
2 6 2 6 2 4 2 4 2 6
示,则ΔH 0(填“>”“<”或“=”)。结合下图,下列条件中,达到平衡时转化率最接近
4
40%的是 (填标号)。
a.600 ℃,0.6 MPa
b.700 ℃,0.7 MPa
c.800 ℃,0.8 MPa
(3)一定温度和压强下,反应ⅰC H (g) C H (g)+H (g) K
2 6 2 4 2 x1
反应ⅱC H (g)+H (g) 2CH (g) K (K 远大于K )(K 是以平衡物质的量分数代替平衡浓度计算的平
2 6 2 4 x2 x2 x1 x
衡常数)
①仅发生反应ⅰ时,C H 的平衡转化率为25.0%,计算K = 。
2 6 x1
②同时发生反应ⅰ和ⅱ时。与仅发生反应ⅰ相比,C H 的平衡产率 (填“增大”“减小”
2 4
或“不变”)。1
答案 (2)> b (3)① ②增大
15
解析 (2)由图可知,若压强相同,温度升高,C H 的平衡转化率增大,该反应为吸热反应,故ΔH >0。
2 6 4
(3)①若仅发生反应ⅰ,设初始时C H 的物质的量为1 mol,则:
2 6
C H (g) C H (g)+ H (g)
2 6 2 4 2
起始量/mol 1 0 0
转化量/mol 0.25 0.25 0.25
平衡量/mol 0.75 0.25 0.25
0.75mol
平衡时气体总物质的量为1.25 mol,C H 、C H 、H 物质的量分数分别为x(C H )= =0.6,
2 6 2 4 2 2 6 1.25mol
0.25mol x(C H )·x(H ) 0.2×0.2 1
x(C H )=x(H )= =0.2,则K = 2 4 2 = = 。②只发生反应ⅰ时,随着反应进行,
2 4 2 1.25mol x1 x(C H ) 0.6 15
2 6
体系内气体总物质的量增大,压强增大;反应ⅱ为反应前后气体体积不变的反应,由题干信息知,K 远大
x2
于K ,C H 同时发生反应ⅰ和ⅱ时,反应ⅱ进行程度远大于反应ⅰ,且反应ⅱ会消耗反应ⅰ生成的H ,
x1 2 6 2
使反应ⅰ的化学平衡正向移动,C H 的平衡产率增大。
2 4
2.[2024·新课标卷,29(3)(4)]Ni(CO) (四羰合镍,沸点43 ℃)可用于制备高纯镍,也是有机化合物羰基化
4
反应的催化剂。回答下列问题:
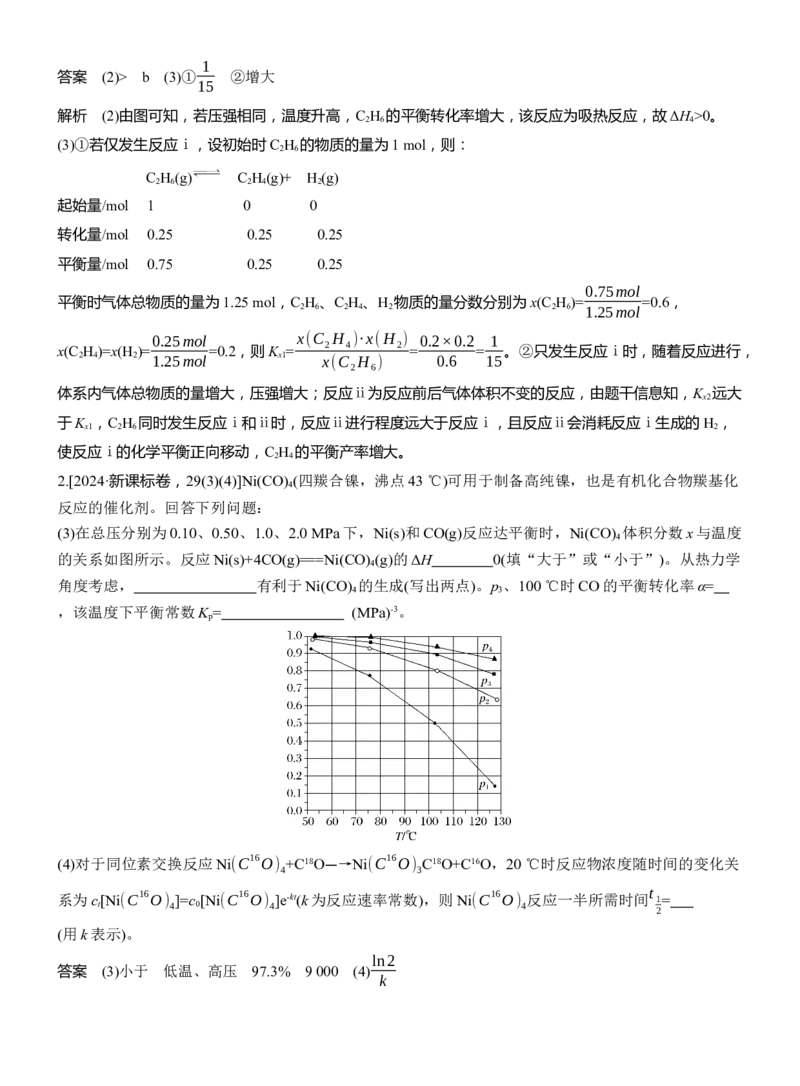
(3)在总压分别为0.10、0.50、1.0、2.0 MPa下,Ni(s)和CO(g)反应达平衡时,Ni(CO) 体积分数x与温度
4
的关系如图所示。反应Ni(s)+4CO(g)===Ni(CO) (g)的ΔH 0(填“大于”或“小于”)。从热力学
4
角度考虑, 有利于Ni(CO) 的生成(写出两点)。p 、100 ℃时CO的平衡转化率α=
4 3
,该温度下平衡常数K = (MPa)-3。
p
(4)对于同位素交换反应Ni(C16O) +C18O―→Ni(C16O) C18O+C16O,20 ℃时反应物浓度随时间的变化关
4 3
t
系为c[Ni(C16O) ]=c [Ni(C16O) ]e-kt(k为反应速率常数),则Ni(C16O) 反应一半所需时间 1=
t 4 0 4 4
2
(用k表示)。
ln2
答案 (3)小于 低温、高压 97.3% 9 000 (4)
k解析 (3)由图可知,随着温度升高,平衡时Ni(CO) 的体积分数减小,说明温度升高平衡逆向移动,因此
4
该反应的ΔH<0;该反应是反应前后气体分子数减小的放热反应,因此低温和高压均有利于Ni(CO) 的生成;
4
由上述分析知,温度相同时,增大压强平衡正向移动,对应的平衡体系中Ni(CO) 的体积分数增大,则压
4
强:p >p >p >p ,即p 对应的压强是1.0 MPa。由题图可知,p 、100 ℃条件下达到平衡时,CO和Ni(CO)
4 3 2 1 3 3 4
的物质的量分数分别为0.1、0.9,设初始投入的CO为4 mol,反应生成的Ni(CO) 为x mol,可得三段式:
4
Ni(s)+4CO(g) Ni(CO) (g)
4
起始/mol 4 0
转化/mol 4x x
平衡/mol 4-4x x
反应后总物质的量为(4-3x) mol,根据阿伏加德罗定律,其他条件相同时,气体的体积分数即为其物质的量
x 36 36
分数,因此有 =0.9,解得x= ,因此达到平衡时n (CO)=4× mol,CO的平衡转化率α=
4-3x 37 转化 37
36
4× mol
37 ×100%≈97.3%;气体的分压=总压强×该气体的物质的量分数,则该温度下的压强平衡常数K =
p
4mol
p[∋(CO) ] 0.9×p 0.9×1.0 MPa c [∋(C16O) ]
4 3 t 4
= = =9 000 (MPa)-3。(4)由题给关系式可得e-kt= ,当
p4 (CO) (0.1×p ) 4 (0.1×1.0 MPa) 4 c [∋(C16O) ]
3 0 4
Ni(C16O)
4
反应一半时
c
c t [
[
∋
∋
(
(
C
C
1
1
6
6
O
O
)
)
4 ]
]
= 1
2
,即e -kt 1
2
= 1
2
,-k t 1
2
=ln 1
2
,k t 1
2
=ln 2,则 t 1
2
= ln
k
2 。
0 4
3.[2023·湖北,19(1)(2)(3)(4)(5)]纳米碗C H 是一种奇特的碗状共轭体系。高温条件下,C H 可以由
40 10 40 10
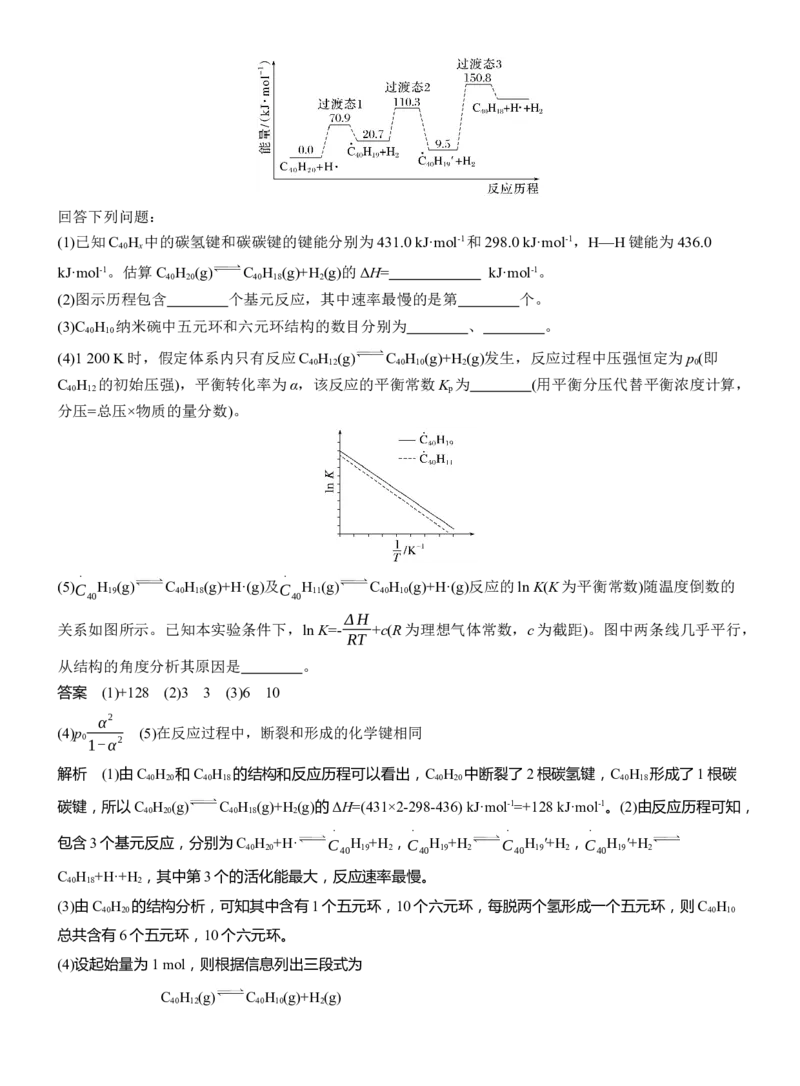
C H 分子经过连续5步氢抽提和闭环脱氢反应生成。C H (g) C H (g)+H (g)的反应机理和能量变
40 20 40 20 40 18 2
化如下:回答下列问题:
(1)已知C H 中的碳氢键和碳碳键的键能分别为431.0 kJ·mol-1和298.0 kJ·mol-1,H—H键能为436.0
40 x
kJ·mol-1。估算C H (g) C H (g)+H (g)的ΔH= kJ·mol-1。
40 20 40 18 2
(2)图示历程包含 个基元反应,其中速率最慢的是第 个。
(3)C H 纳米碗中五元环和六元环结构的数目分别为 、 。
40 10
(4)1 200 K时,假定体系内只有反应C H (g) C H (g)+H (g)发生,反应过程中压强恒定为p (即
40 12 40 10 2 0
C H 的初始压强),平衡转化率为α,该反应的平衡常数K 为 (用平衡分压代替平衡浓度计算,
40 12 p
分压=总压×物质的量分数)。
· ·
(5)C H 19 (g) C 40 H 18 (g)+H·(g)及 C H 11 (g) C 40 H 10 (g)+H·(g)反应的ln K(K为平衡常数)随温度倒数的
40 40
ΔH
关系如图所示。已知本实验条件下,ln K=- +c(R为理想气体常数,c为截距)。图中两条线几乎平行,
RT
从结构的角度分析其原因是 。
答案 (1)+128 (2)3 3 (3)6 10
α2
(4)p (5)在反应过程中,断裂和形成的化学键相同
0 1-α2
解析 (1)由C H 和C H 的结构和反应历程可以看出,C H 中断裂了2根碳氢键,C H 形成了1根碳
40 20 40 18 40 20 40 18
碳键,所以C H (g) C H (g)+H (g)的ΔH=(431×2-298-436) kJ·mol-1=+128 kJ·mol-1。(2)由反应历程可知,
40 20 40 18 2
· · · ·
包含3个基元反应,分别为C H +H· C H +H ,C H +H C H '+H ,C H '+H
40 20 40 19 2 40 19 2 40 19 2 40 19 2
C H +H·+H ,其中第3个的活化能最大,反应速率最慢。
40 18 2
(3)由C H 的结构分析,可知其中含有1个五元环,10个六元环,每脱两个氢形成一个五元环,则C H
40 20 40 10
总共含有6个五元环,10个六元环。
(4)设起始量为1 mol,则根据信息列出三段式为
C H (g) C H (g)+H (g)
40 12 40 10 2起始量/mol 1 0 0
变化量/mol α α α
平衡量/mol 1-α α α
α α
p × ×p ×
1-α α α 0 1+α 0 1+α
则p(C H )=p × ,p(C H )=p × ,p(H )=p × ,该反应的平衡常数K =
40 12 0 1+α 40 10 0 1+α 2 0 1+α p 1-α
p ×
0 1+α
α2 ΔH
=p 。(5)图中两条线几乎平行,说明斜率几乎相等,根据ln K=- +c(R为理想气体常数,c为截距)
0 1-α2 RT
可知,焓变相等,因为在反应过程中,断裂和形成的化学键相同。
题型突破练 [分值:100 分]
1.(6分)对于反应CO (g)+H (g) CO(g)+H O(g) ΔH>0,反应速率v=v -v =k p(CO )·p(H )-k
2 2 2 正 逆 正 2 2 逆
p(CO)·p(H O),其中k 、k 分别为正、逆反应速率常数,p为气体的分压(分压=总压×物质的量分数)。
2 正 逆
(1)降低温度,k -k (填“增大”“减小”或“不变”)。
正 逆
v 4
(2)在T K、101 kPa下,按照n(CO )∶n(H )=1∶1投料,CO 转化率为50%时, 正 = ,用气体分压表示的
2 2 2 v 5
逆
平衡常数K = (保留小数点后一位)。
p
答案 (1)减小 (2)0.8
解析 (1)降低温度,反应逆向进行,所以k -k 减小。
正 逆
(2)设初始n(CO )=2 mol,
2
CO (g)+H (g) CO(g)+H O(g)
2 2 2
起始/mol 2 2 0 0
转化/mol 1 1 1 1
平衡/mol 1 1 1 1
v k p(CO )·p(H ) 4 1 v k 4
正= 正× 2 2 = ,其中p(CO )=p(H )=p(CO)=p(H O)= p ,即 正 = 正 = ,平衡时v =v
v k p(CO)·p(H O) 5 2 2 2 4 总 v k 5 正
逆 逆 2 逆 逆
p(CO)·p(H O) k 4
,有k p(CO )·p(H )=k p(CO)·p(H O),则K= 2 = 正= =0.8。
逆 正 2 2 逆 2 p p(CO )·p(H ) k 5
2 2 逆
2.(9分)某化学兴趣小组模拟SO 催化氧化制备SO ,在2 L刚性容器中进行下列三组实验,数据如下:
2 3
第1组
第2组
第3组
温度/℃T
1
T
2
T
3
投料n(SO )/mol
2
1
2
4
投料n(O )/mol
2
2
2
2
SO 平衡
2
转化率(α)/%
40
50
α
(1)T ℃时平衡常数K= (保留两位有效数字)。
1
(2)若T =T ,则α (填“>”“<”或“=”)40%,结合相关数据计算,写出推理过程: 。
1 3
答案 (1)0.49
(2)< T =T 时,假设反应达到平衡时,SO 的转化率也为40%,则转化的c(SO )=0.8 mol·L-1。
3 1 2 2
2SO (g)+O (g) 2SO (g)
2 2 3
起始浓度/(mol·L-1) 2 1 0
转化浓度/(mol·L-1) 0.8 0.4 0.8
α=40%时浓度/(mol·L-1) 1.2 0.6 0.8
c2 (SO ) 0.82 20
Q= 3 = = >K,平衡逆向移动,所以SO 的平衡转化率小于40%
c2 (SO )·c(O ) 1.22×0.6 27 2
2 2
解析 (1)T ℃时SO 的平衡转化率为40%,则转化的c(SO )=0.2 mol·L-1。
1 2 2
2SO (g)+O (g) 2SO (g)
2 2 3
起始浓度/(mol·L-1) 0.5 1 0
转化浓度/(mol·L-1) 0.2 0.1 0.2
平衡浓度/(mol·L-1) 0.3 0.9 0.2
c2 (SO ) 0.22
3
K= = ≈0.49。
c2 (SO )·c(O ) 0.32×0.9
2 23.(15分)在5.0 MPa下,将5 mol CO 和16 mol H 在Cu/ZrO 催化剂作用下进行主反应:CO (g) +3H (g)
2 2 2 2 2
CH OH(g) + H O(g) ΔH =-49.3 kJ·mol-1。该合成过程还存在一个副反应:CO (g) + H (g) CO(g) +
3 2 1 2 2
CH OH或CO的量
H O(g) ΔH =+41 kJ·mol-1。平衡时CH OH和CO 选择性S[S(CH OH或CO)= 3 ×100%]
2 2 3 3 已转化CO 的总量
2
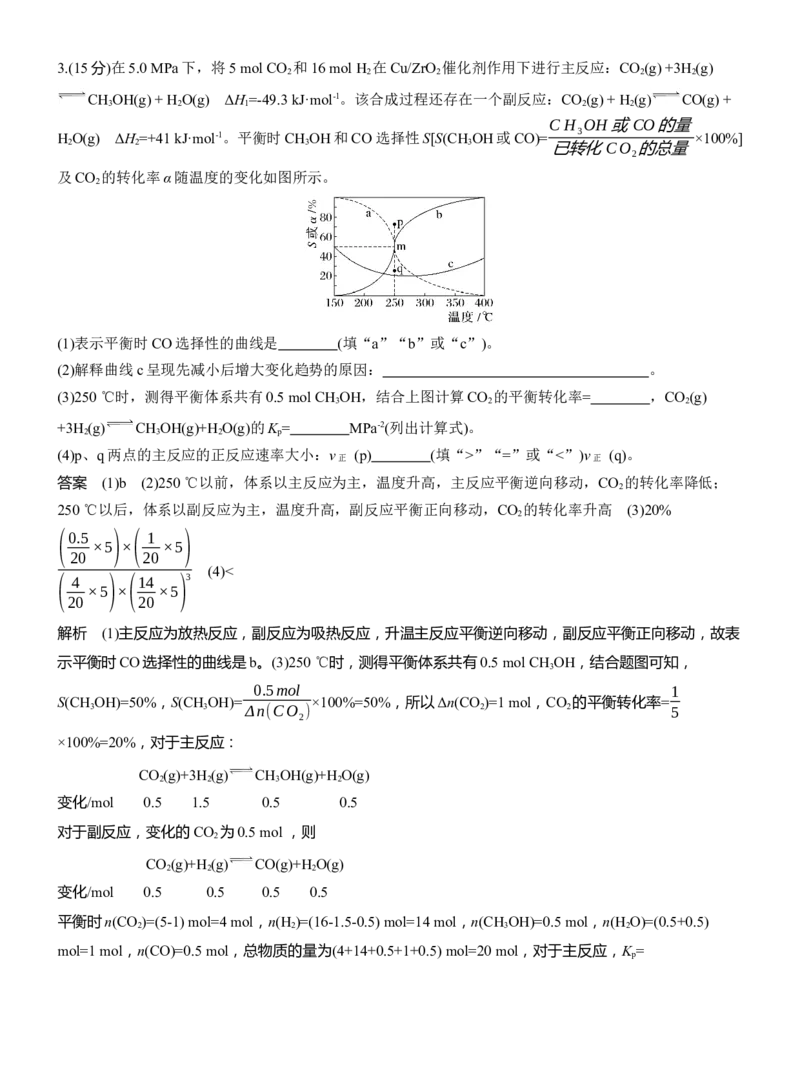
及CO 的转化率α随温度的变化如图所示。
2
(1)表示平衡时CO选择性的曲线是 (填“a”“b”或“c”)。
(2)解释曲线c呈现先减小后增大变化趋势的原因: 。
(3)250 ℃时,测得平衡体系共有0.5 mol CH OH,结合上图计算CO 的平衡转化率= ,CO (g)
3 2 2
+3H (g) CH OH(g)+H O(g)的K = MPa-2(列出计算式)。
2 3 2 p
(4)p、q两点的主反应的正反应速率大小:v (p) (填“>”“=”或“<”)v (q)。
正 正
答案 (1)b (2)250 ℃以前,体系以主反应为主,温度升高,主反应平衡逆向移动,CO 的转化率降低;
2
250 ℃以后,体系以副反应为主,温度升高,副反应平衡正向移动,CO 的转化率升高 (3)20%
2
(0.5 ) ( 1 )
×5 × ×5
20 20
(4)<
( 4 ) (14 ) 3
×5 × ×5
20 20
解析 (1)主反应为放热反应,副反应为吸热反应,升温主反应平衡逆向移动,副反应平衡正向移动,故表
示平衡时CO选择性的曲线是b。(3)250 ℃时,测得平衡体系共有0.5 mol CH OH,结合题图可知,
3
0.5mol 1
S(CH OH)=50%,S(CH OH)= ×100%=50%,所以Δn(CO )=1 mol,CO 的平衡转化率=
3 3 Δn(CO ) 2 2 5
2
×100%=20%,对于主反应:
CO (g)+3H (g) CH OH(g)+H O(g)
2 2 3 2
变化/mol 0.5 1.5 0.5 0.5
对于副反应,变化的CO 为0.5 mol ,则
2
CO (g)+H (g) CO(g)+H O(g)
2 2 2
变化/mol 0.5 0.5 0.5 0.5
平衡时n(CO )=(5-1) mol=4 mol,n(H )=(16-1.5-0.5) mol=14 mol,n(CH OH)=0.5 mol,n(H O)=(0.5+0.5)
2 2 3 2
mol=1 mol,n(CO)=0.5 mol,总物质的量为(4+14+0.5+1+0.5) mol=20 mol,对于主反应,K =
p(0.5 ) ( 1 )
×5 × ×5
20 20
MPa-2。(4)根据图像,p位于曲线a之上,q位于曲线a之下,p、q两点的主反应的正
( 4 ) (14 ) 3
×5 × ×5
20 20
反应速率大小:v (p)”“<”或“=”)v ,达到平衡时二氧化硫的转化率为 。
正 逆
(2)模仿工业上用反应2SO (g)+O (g) 2SO (g)得到硫酸,除去工业废气中的SO 。现在一容积固定为1 L
2 2 3 2
的密闭容器中进行该反应,测得如下数据:
实验组
温度/℃
起始量/mol
平衡量/mol
达平衡
所需时
间/min
SO
2
O
2
SO
3
1
550
2
1
0.5
10
2
650
10.5
0.4
4
①分析第1组和第2组实验数据,可以得出有关反应速率的结论是 。
②已知,反应中v =k c2(SO )·c(O ),v =k c2(SO ),k 、k 为速率常数。若实验组2,1 min时n(SO )=0.2
正 1 2 2 逆 2 3 1 2 3
k v
mol,则 1 = , 正 = 。
k v
2 逆
答案 (1)9 减小 > 50% (2)①温度升高,反应速率增大 ②1.48 9.472
解析 (1)设加入二氧化氮和二氧化硫的量都为1 mol,容器体积为1 L,则浓度都为1 mol·L-1,设反应消耗
了NO (g)的浓度为x mol·L-1,列出三段式:
2
NO (g)+SO (g) SO (g)+NO(g)
2 2 3
初始/(mol·L-1) 1 1 0 0
转化/(mol·L-1) x x x x
平衡/(mol·L-1) 1-x 1-x x x
x 3 0.75×0.75
达到平衡时NO和NO 的浓度之比为3∶1,即 = ,解得x=0.75,平衡常数K= =9,该反应
2 1-x 1 0.25×0.25
1×1
为放热反应,升高温度,平衡常数减小;保持温度不变,则化学平衡常数不变,Q= =1v ;根据已知列三段式:
正 逆
NO (g)+SO (g) SO (g)+NO(g)
2 2 3
初始/(mol·L-1) 1 1 1 1
转化/(mol·L-1) y y y y
平衡/(mol·L-1) 1-y 1-y 1+y 1+y
(1+ y)×(1+ y) 0.5
则K= =9,解得y=0.5,达到平衡时二氧化硫的转化率为 ×100%=50%。
(1- y)×(1- y) 1
(2)②实验组2,列三段式:
2SO (g)+O (g) 2SO (g)
2 2 3
起始/mol 1 0.5 0
转化/mol 0.4 0.2 0.4
平衡/mol 0.6 0.3 0.4
体积为1 L,平衡浓度分别为c(SO )=0.6 mol·L-1、c(O )=0.3 mol·L-1、c(SO )=0.4 mol·L-1,平衡时v
2 2 3 正
k c2 (SO ) k
1 3 1
=k c2(SO )·c(O )=v =k c2(SO )则 = ,解得 ≈1.48;实验组2,1 min时,列三段式:
1 2 2 逆 2 3 k c2 (SO )·c(O ) k
2 2 2 2
2SO (g)+O (g) 2SO (g)
2 2 3起始/mol 1 0.5 0
转化/mol 0.2 0.1 0.2
1 min时/mol 0.8 0.4 0.2
v k c2 (SO )·c(O ) k c2 (SO )·c(O ) (0.8) 2×0.4
正 1 2 2 1 2 2
= = × =1.48× =9.472。
v k c2 (SO ) k c2 (SO ) (0.2) 2
逆 2 3 2 3
5.(18分)合成氨原料气高纯氢可以由天然气、水蒸气催化重整制取,所涉及的主要反应如下:
相关反应
ΔH
物质的量分数平衡常数
反应ⅰ
CH (g)+H O(g) CO(g)+3H (g)
4 2 2
ΔH =+206 kJ·mol-1
1
K
x1
反应ⅱ
CO(g)+H O(g) CO (g)+H (g)
2 2 2
ΔH =-41 kJ·mol-1
2
K
x2
反应ⅲ
CH (g)+2H O(g) CO (g)+4H (g)
4 2 2 2
ΔH =+165 kJ·mol-1
3
K
x3
xc (C)·xd (D)
已知:反应aA(g)+bB(g) cC(g)+dD(g)的物质的量分数平衡常数K= ,其中x(A)、x(B)、
x xa (A)·xb (B)
x(C)、x(D)为各组分的物质的量分数。
K
(1)相同条件下,随着反应温度的升高,化学平衡常数K 、K 的比值( x1 ) (填“增大”“减小”
x1 x3 K
x3
或“不变”),其原因为 。
(2)T ℃时,向2 L恒容密闭容器中充入1 mol CH 和2 mol H O(g),发生上述反应ⅰ和ⅲ。测得反应达到平
4 2
衡时,容器中n(CH )=0.4 mol,n(H )=2 mol。
4 2
①T ℃时,反应中H O的平衡转化率为 。
2
②T ℃时,反应ⅰ的平衡常数K = (列出表达式,无需化简)。
x1
③若将容器的体积压缩为1 L,甲烷的平衡转化率 (填“增大”“减小”或“不变”,下同),反应
ⅲ的逆反应速率 。答案 (1)增大 根据盖斯定律可知反应ⅰ-反应ⅲ可得:CO (g)+H (g) CO(g)+H O(g),该反应ΔH=+41
2 2 2
K
kJ·mol-1,温度升高,平衡正向移动,该反应的物质的量分数平衡常数K= x1增大 (2)①40% ②
x K
x3
( 2 ) 3 0.4
×
4.2 4.2
③减小 增大
0.4 1.2
×
4.2 4.2
4+2×2-0.4×4-2×2
解析 (2)①根据H原子守恒,平衡时H O的物质的量为 mol=1.2 mol,H O的平衡
2 2 2
2-1.2
转化率为 ×100%=40%。②设平衡时反应ⅰ消耗x mol甲烷,反应 ⅲ 消耗y mol甲烷,则:
2
CH (g)+H O(g) CO(g)+3H (g)
4 2 2
变化/mol x x x 3x
CH (g)+2H O(g) CO (g)+4H (g)
4 2 2 2
变化/mol y 2y y 4y
由题意得:x+y=1-0.4=0.6,3x+4y=2,解得:x=0.4,y=0.2;则平衡时n(CH )=0.4 mol,n(H )=2 mol,
4 2
( 2 ) 3 0.4
×
4.2 4.2
n(CO)=0.4 mol,n(CO )=0.2 mol,n(H O)=1.2 mol,n(总)=4.2 mol,反应ⅰ的平衡常数K = 。
2 2 x1
0.4 1.2
×
4.2 4.2
③反应ⅰ和ⅲ正向气体分子数均增大,压缩体积,平衡均逆向移动,甲烷的平衡转化率减小;压缩体积各
物质的浓度均增大,则正、逆反应速率均增大。
6.(15分)CO 催化加氢可合成乙烯,反应为2CO (g)+6H (g) C H (g)+4H O(g) ΔH<0,在恒压密闭容器
2 2 2 2 4 2
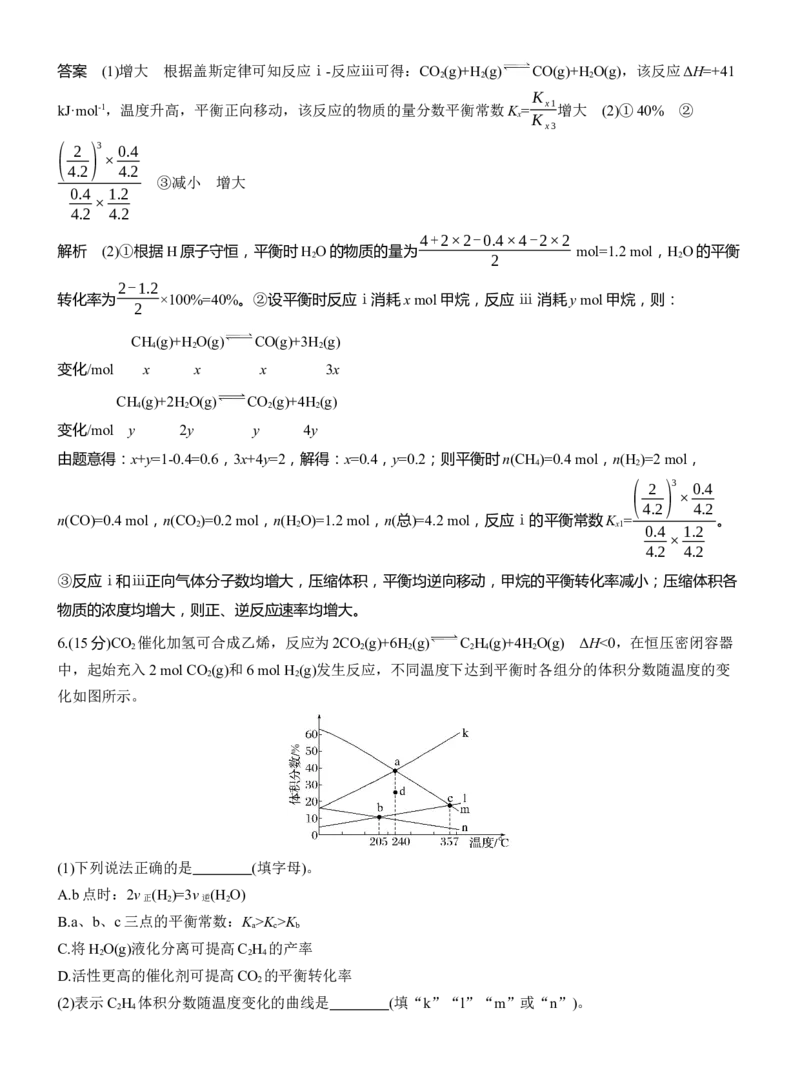
中,起始充入2 mol CO (g)和6 mol H (g)发生反应,不同温度下达到平衡时各组分的体积分数随温度的变
2 2
化如图所示。
(1)下列说法正确的是 (填字母)。
A.b点时:2v (H )=3v (H O)
正 2 逆 2
B.a、b、c三点的平衡常数:K>K>K
a c b
C.将H O(g)液化分离可提高C H 的产率
2 2 4
D.活性更高的催化剂可提高CO 的平衡转化率
2
(2)表示C H 体积分数随温度变化的曲线是 (填“k”“l”“m”或“n”)。
2 4(3)若d点表示240 ℃某时刻H 的体积分数,保持温度不变,则反应向 (填“正”或“逆”)反应方
2
向进行。
(4)205 ℃,反应达b点所用时间为t min,则此过程中用CO 表示的反应速率是 mol·min-1。若平
2
衡时b点总压为p,则平衡常数K = (列出计算式,以分压表示,分压=总压×物质的量分数)。
p
1 4
( p)×( p) 4
4 9 9
答案 (1)AC (2)n (3)逆 (4)
3t 1 1
( p) 2×( p) 6
9 3
解析 (1)由化学方程式体现的关系可知,b点时达到平衡状态,正、逆反应速率相等,则有2v (H )=3v
正 2 逆
(H O),A正确;反应为放热反应,随着温度升高,平衡逆向移动,平衡常数减小,故a、b、c三点的平衡
2
常数:K >K>K,B错误;将H O(g)液化分离,平衡正向移动,可提高C H 的产率,C正确;活性更高的
b a c 2 2 4
催化剂可提高反应速率,但是不改变CO 的平衡转化率,D错误。(2)随着温度升高,平衡逆向移动,乙烯、
2
水的体积分数减小,结合化学方程式中化学计量数可知,乙烯减小的程度小于水,故表示水体积分数随温
度变化的曲线是m,表示C H 体积分数随温度变化的曲线是n。(3)随着温度升高,平衡逆向移动,二氧化
2 4
碳、氢气的体积分数增大,结合化学方程式中化学计量数可知,二氧化碳增大的程度小于氢气,则l为二
氧化碳体积分数随温度变化曲线,k为氢气体积分数随温度变化曲线;若d点表示240 ℃某时刻H 的体积
2
分数,此时氢气的体积分数小于平衡时氢气的体积分数,保持温度不变,反应向逆反应方向进行。(4)205
℃,反应达b点所用时间为t min,设CO 转化了2a mol,可得
2
2CO (g)+6H (g) C H (g)+4H O(g)
2 2 2 4 2
起始/mol 2 6 0 0
转化/mol 2a 6a a 4a
平衡/mol 2-2a 6-6a a 4a
2
2 ×2
此时二氧化碳和乙烯体积分数相同,则2-2a=a,a= ,则此过程中用CO 表示的反应速率是3
3 2
t
4 2 2 8
mol·min-1= mol·min-1;平衡时二氧化碳、氢气、乙烯、水分别为 mol、2 mol、 mol、 mol,总的物
3t 3 3 3
1 4
( p)×( p) 4
9 9
质的量为6 mol,若平衡时b点总压为p,则平衡常数K = 。
p 1 1
( p) 2×( p) 6
9 3
7.(6分)我国科学家成功开发Pd⁃Fe/Fe
2
O
3
催化剂在低温条件下高选择性合成高纯度的乙烯,化学原理为主反应:C H (g)+H (g) C H (g) ΔH
2 2 2 2 4 1
副反应:C H (g)+2H (g) C H (g) ΔH
2 2 2 2 6 2
在密闭容器中充入1 mol C H 和2 mol H ,发生上述两个反应,测得C H 平衡转化率与温度、压强的关系
2 2 2 2 2
8 n(C H )
如图所示。在T K、20 kPa下C H 的选择性等于 [C H 选择性= 2 4 ]。p (填
0 2 4 9 2 4 n(C H )+n(C H ) 0
2 4 2 6
“>”“<”或“=”)20 kPa。T K下,主反应的平衡常数K = kPa-1(K 为用气体分压计算的平衡常
0 p p
数,气体分压等于气体总压×物质的量分数)。
答案 < 0.8
解析 主反应和副反应均为气体分子数减小的反应,增大压强,平衡正向移动,C H 的转化率升高,结合
2 2
图像可知,p <20 kPa;T K时,设平衡时C H (g)、C H (g)的物质的量分别为x mol、y mol;
0 0 2 4 2 6
C H (g)+ H (g) C H (g)
2 2 2 2 4
起始/mol 1 2 0
转化/mol x x x
平衡/mol 1-x-y 2-x-2y x
C H (g)+ 2H (g) C H (g)
2 2 2 2 6
起始/mol 1-x 2-x 0
转化/mol y 2y y
平衡/mol 1-x-y 2-x-2y y
x+ y 8
由图可知,在T K、20 kPa下C H 的平衡转化率为90%,则 ×100%=90%;C H 的选择性等于 ,则
0 2 2 1 2 4 9
x 8
= ;解得x=0.8,y=0.1;平衡时C H (g)、C H (g)、C H (g)、H (g)的物质的量分别为0.1 mol、0.1
x+ y 9 2 2 2 6 2 4 2
0.8
20×
2.0
mol、0.8 mol、1.0 mol,总物质的量为2.0 mol,则T K下,主反应的平衡常数K =
0 p 0.1 1.0
(20× )×(20× )
2.0 2.0
kPa-1=0.8 kPa-1。
n(CO )
2
8.(15分)反应CO (g)+H (g) CO(g)+H O(g) ΔH=+41.0 kJ·mol-1。在进气比 不同时,测得相应的
2 2 2 n(H )
2
CO 平衡转化率如图(各点对应的反应温度可能相同,也可能不同;各点对应的其他反应条件都相同)。
2(1)反应中CO 的平衡转化率与进气比、反应温度之间的关系是 。
2
(2)图中E和G两点对应的反应温度T 、T 的关系是 ,其原因是 。
E G
(3)A、B两点对应的反应速率v (填“<”“=”或“>”)v 。已知反应速率v =k
A B 正 正
x(CO )·x(H ),v =k x(CO)·x(H O),k为反应速率常数,x为物质的量分数,在达到平衡状态为C点的反应
2 2 逆 逆 2
v
过程(此过程为恒温)中,当CO 的转化率刚好达到60%时, 正 = 。
2 v
逆
答案 (1)反应温度相同,进气比越大,CO 的平衡转化率越小;进气比相同,反应温度越高,CO 的平衡
2 2
转化率越大(或进气比越大,反应温度越低,CO 的平衡转化率越小) (2)T =T K =K =1 (3)> 4
2 E G E G
n(CO )
2
解析 (2)在E点时 =1,CO 的平衡转化率为50%,根据三段式得
n(H ) 2
2
CO (g)+H (g) CO(g)+H O(g)
2 2 2
始/(mol·L-1) 1 1 0 0
转/(mol·L-1) 0.5 0.5 0.5 0.5
平/(mol·L-1) 0.5 0.5 0.5 0.5
c(CO)·c(H O) 0.5×0.5
2
K = = =1;
E c(CO )·c(H ) 0.5×0.5
2 2
n(CO )
2
在G点时 =1.5,CO 的平衡转化率为40%,根据三段式得
n(H ) 2
2
CO (g)+H (g) CO(g)+H O(g)
2 2 2
始/(mol·L-1) 1.5 1 0 0
转/(mol·L-1) 0.6 0.6 0.6 0.6
平/(mol·L-1) 0.9 0.4 0.6 0.6
c(CO)·c(H O) 0.6×0.6
2
K = = =1。
G c(CO )·c(H ) 0.9×0.4
2 2
平衡常数只与温度有关,平衡常数相等,温度相等,故T =T 。(3)反应CO (g)+H (g) CO(g)+H O(g)
E G 2 2 2
n(CO )
2
ΔH=+41.0 kJ·mol-1,该反应为吸热反应,当 相同时,温度高CO 转化率大,A点的转化率大于B
n(H ) 2
2
n(CO )
2
点,说明A点的温度高,故反应速率:v >v ;在C点时 =1,CO 的平衡转化率为75%,根据三段
A B n(H ) 2
2
式得
CO (g)+H (g) CO(g)+H O(g)
2 2 2
始/(mol·L-1) 1 1 0 0
转/(mol·L-1) 0.75 0.75 0.75 0.75
平/(mol·L-1) 0.25 0.25 0.75 0.75c(CO)·c(H O) 0.75×0.75
2
K= = =9,
c(CO )·c(H ) 0.25×0.25
2 2
k x(CO)·x(H O)
正 2
平衡状态时v =v ,得 = =K=9。当CO 的转化率刚好达到60%时,
正 逆 k x(CO )·x(H ) 2
逆 2 2
CO (g)+H (g) CO(g)+H O(g)
2 2 2
始/(mol·L-1) 1 1 0 0
转/(mol·L-1) 0.6 0.6 0.6 0.6
CO 转化率为60%时/(mol·L-1) 0.4 0.4 0.6 0.6
2
v k x(CO )·x(H ) 0.4×0.4
正 正 2 2
= =9× =4。
v k x(CO)·x(H O) 0.6×0.6
逆 逆 2