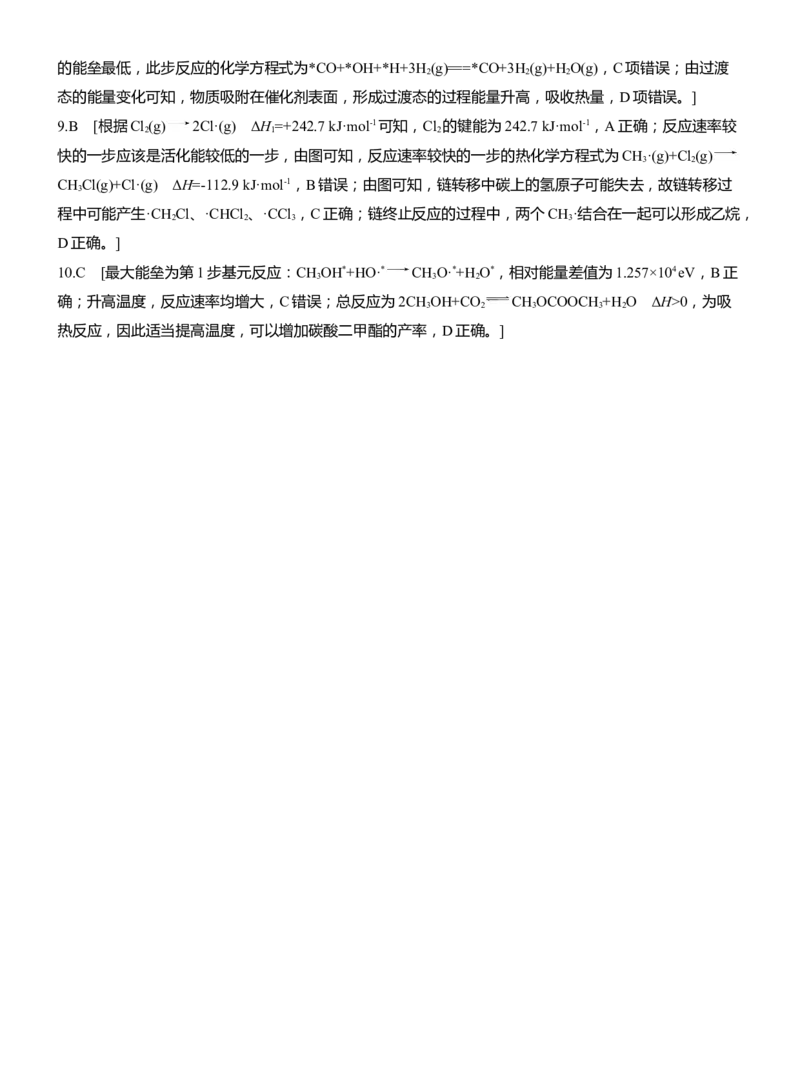文档内容
物质能量、能垒变化图像分析
(选择题1~10题,每小题5分,共50分)
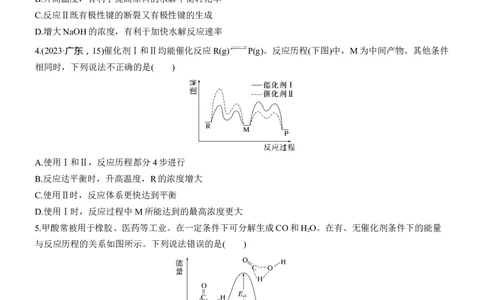
1.(2024·北京市丰台区高三练习)过渡金属氧化物离子(以MO+表示)在烃类的选择性氧化等方面应用广泛。
MO+与CH 反应的过程如图所示。
4
下列说法不正确的是( )
A.反应速率:步骤Ⅰ<步骤Ⅱ
B.CH OH分子中,键角:H—C—H>H—O—C
3
C.若MO+与CHD 反应,生成的氘代甲醇有2种
3
D.CH (g) + MO+(g)===CH OH(g) + M+(g) ΔH=E +E -E -E
4 3 2 4 1 3
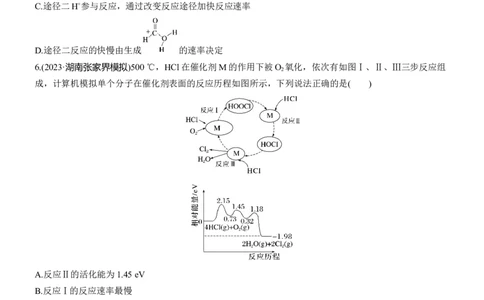
2.(2024·广东汕头高三一模)三甲胺[N(CH ) ]是重要的化工原料。我国科学家利用(CH ) NCHO(简称
3 3 3 2
DMF)在铜催化作用下转化得到N(CH ) ,如图是计算机模拟单个DMF分子在铜催化剂表面的反应历程
3 3
图(*表示物质吸附在铜催化剂上),下列说法错误的是( )
A.该反应为放热反应,降温可提高DMF的平衡转化率
B.该历程最大能垒(活化能)为1.19 eV
*
C.设法提高N(CH ) +OH*+H*===N(CH ) (g)+H O(g)的速率可以提高总反应速率
3 3 3 3 2
D.若1 mol DMF完全转化为三甲胺,则会吸收1.02N eV的能量
A
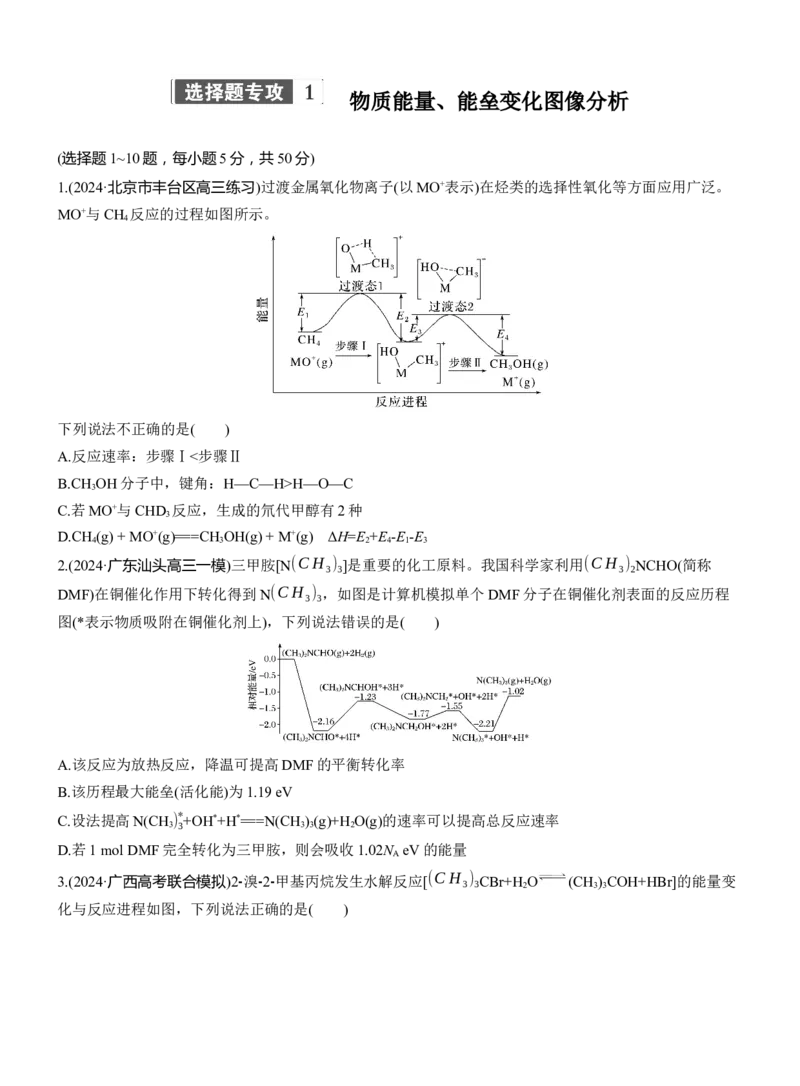
3.(2024·广西高考联合模拟)2⁃ 溴 ⁃2⁃ 甲基丙烷发生水解反应[(CH
3
)
3
CBr+H
2
O (CH
3
)
3
COH+HBr]的能量变
化与反应进程如图,下列说法正确的是( )A.水解反应的速率由反应Ⅰ决定
B.升高温度,有利于提高原料的水解平衡转化率
C.反应Ⅱ既有极性键的断裂又有极性键的生成
D.增大NaOH的浓度,有利于加快水解反应速率
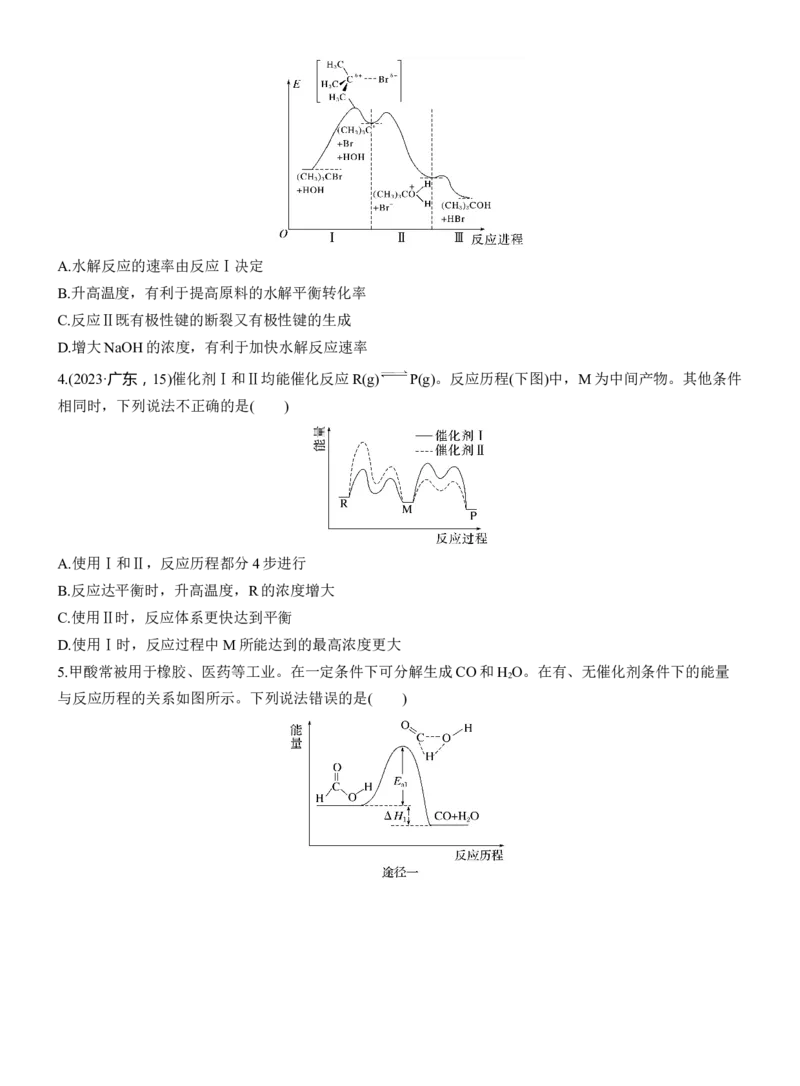
4.(2023·广东,15)催化剂Ⅰ和Ⅱ均能催化反应R(g) P(g)。反应历程(下图)中,M为中间产物。其他条件
相同时,下列说法不正确的是( )
A.使用Ⅰ和Ⅱ,反应历程都分4步进行
B.反应达平衡时,升高温度,R的浓度增大
C.使用Ⅱ时,反应体系更快达到平衡
D.使用Ⅰ时,反应过程中M所能达到的最高浓度更大
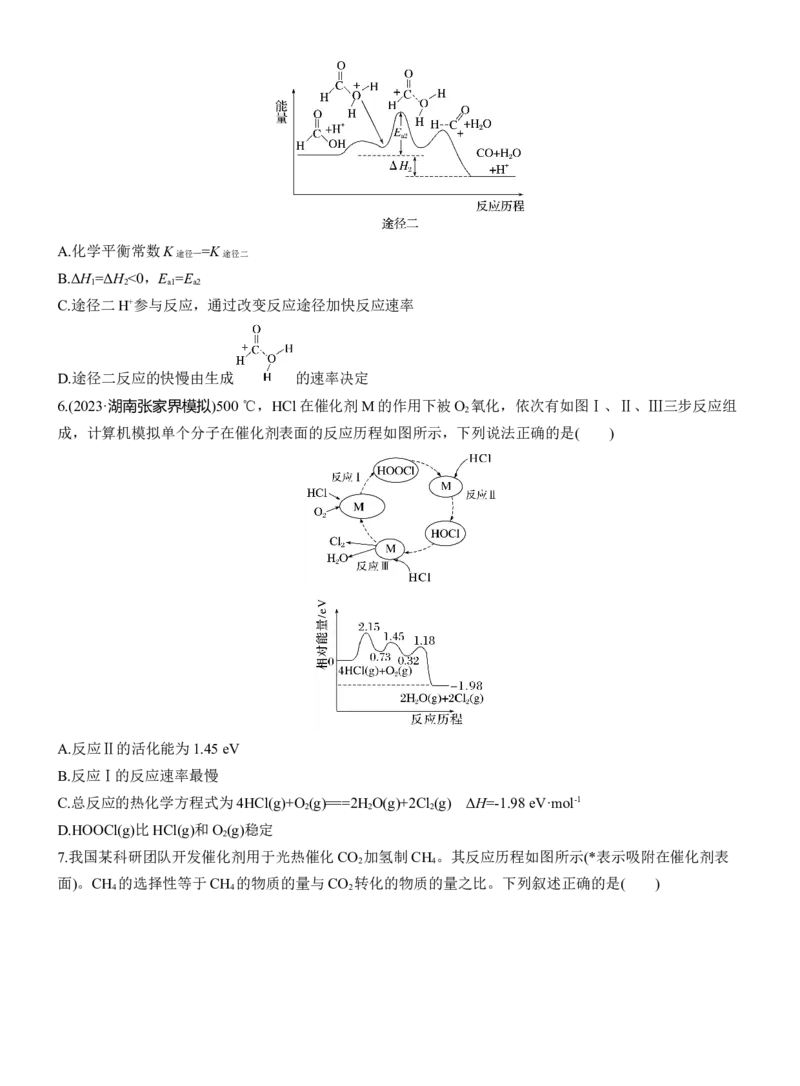
5.甲酸常被用于橡胶、医药等工业。在一定条件下可分解生成CO和H O。在有、无催化剂条件下的能量
2
与反应历程的关系如图所示。下列说法错误的是( )A.化学平衡常数K =K
途径一 途径二
B.ΔH =ΔH <0,E =E
1 2 a1 a2
C.途径二H+参与反应,通过改变反应途径加快反应速率
D.途径二反应的快慢由生成 的速率决定
6.(2023·湖南张家界模拟)500 ℃,HCl在催化剂M的作用下被O 氧化,依次有如图Ⅰ、Ⅱ、Ⅲ三步反应组
2
成,计算机模拟单个分子在催化剂表面的反应历程如图所示,下列说法正确的是( )
A.反应Ⅱ的活化能为1.45 eV
B.反应Ⅰ的反应速率最慢
C.总反应的热化学方程式为4HCl(g)+O (g)===2H O(g)+2Cl (g) ΔH=-1.98 eV·mol-1
2 2 2
D.HOOCl(g)比HCl(g)和O (g)稳定
2
7.我国某科研团队开发催化剂用于光热催化CO 加氢制CH 。其反应历程如图所示(*表示吸附在催化剂表
2 4
面)。CH 的选择性等于CH 的物质的量与CO 转化的物质的量之比。下列叙述正确的是( )
4 4 2A.在CO →CH 历程中能垒最大为0.69 eV
2 4
B.该反应历程中,CH 的选择性为100%
4
C.催化剂表面上CH 、CO脱附都会放出能量
4
D.反应历程中有极性键的断裂与形成
8.氢气可将CO 还原为甲烷:CO (g)+4H (g) CH (g)+2H O(g),科学家研究在催化剂表面上CO 与H 反
2 2 2 4 2 2 2
应的前三步历程如图所示,吸附在催化剂表面上的物种用“*”标注,TS表示过渡态。下列说法正确的是(
)
A.起始到TS1历程中发生了非极性共价键的断裂
B.前三步反应的速率取决于TS2的能垒
C.前三步历程中最小能垒步骤的化学方程式为*CO+3H (g)+H O(g) *CO+*OH+*H+3H (g)
2 2 2
D.物质吸附在催化剂表面,形成过渡态的过程会放出热量
9.甲烷与氯气在光照条件下发生取代反应的部分机理与能量变化如下:
链引发:Cl (g)―→2Cl·(g)
2
ΔH =+242.7 kJ·mol-1
1
链转移:部分反应进程与势能变化关系如图(所有物质状态为气态)……
链终止:Cl·(g)+CH ·(g)―→CH Cl(g) ΔH
3 3 2下列说法不正确的是( )
A.Cl 的键能为242.7 kJ·mol-1
2
B.链转移中反应速率较快的一步的热化学方程式为CH (g)+Cl·(g)―→CH ·(g)+HCl(g) ΔH=+7.5 kJ·mol-1
4 3
C.链转移过程中可能产生·CH Cl、·CHCl 、·CCl
2 2 3
D.链终止反应的过程中,还可能会生成少量的乙烷
10.(2023·湖南岳阳平江县高三教学质量监测)碳酸二甲酯DMC(CH OCOOCH )是一种低毒、性能优良的有
3 3
机合成中间体,科学家提出了新的合成方案(吸附在催化剂表面上的物种用*标注),反应机理如图所示。
下列说法错误的是( )
A.第2步的基元反应方程式为CH O·*+CO *―→CH OCOO·*
3 2 3
B.反应进程中最大能垒为1.257×104 eV
C.升高温度,第1步反应的正反应速率增加,第3步反应的正反应速率减小
D.适当提高温度,可以增加碳酸二甲酯的产率答案精析
1.D [步骤Ⅰ的活化能大于步骤Ⅱ,反应速率步骤Ⅰ更小,故A正确;O原子上有两个孤电子对,排斥力
较大,CH OH分子中键角:H—C—H>H—O—C,故B正确;根据反应机理可知,若MO+与CHD 反应,
3 3
生成的氘代甲醇可能为CHD OD或CD OH,共两种,故C正确;根据题图可知,总反应的ΔH=E -E +E -
2 3 1 2 3
E ,故D错误。]
4
2.D [由图可知,该反应为反应物总能量高于生成物总能量的放热反应,降低温度,平衡向正反应方向移
动,DMF的平衡转化率增大,故A正确;由图可知,该历程最大能垒(活化能)为1.19 eV,故B正确;反
应的活化能越大,反应速率越慢,总反应的速率取决于慢反应,由图可知,最大能垒(活化能)的反应的方
程式为N(CH ) * +OH*+H*===N(CH ) (g)+H O(g),故C正确;由反应物和生成物的相对能量可知,1 mol
3 3 3 3 2
DMF完全转化为三甲胺,会释放出1.02N eV的能量,故D错误。]
A
3.A [反应Ⅰ活化能最大,反应速率最慢,决定水解反应的速率,增大NaOH的浓度,消耗HBr,HBr浓
度减小,平衡正向移动,不能加快水解反应速率,A正确,D错误;反应物总能量大于生成物总能量,为
放热反应,升高温度,平衡逆向移动,导致原料平衡转化率下降,B错误;反应Ⅱ无极性键的断裂,C错
误。]
4.C [由图可知两种催化剂均出现四个波峰,所以使用Ⅰ和Ⅱ,反应历程都分4步进行,A正确;该反应
是放热反应,升高温度平衡向左移动,R的浓度增大,B正确;由图可知使用Ⅰ时反应的最高活化能小于
使用Ⅱ时反应的最高活化能,所以使用Ⅰ时反应速率更快,反应体系更快达到平衡,C错误;在前两个历
程中使用Ⅰ活化能较低反应速率较快,后两个历程中使用Ⅰ活化能较高反应速率较慢,所以使用Ⅰ时,反
应过程中M所能达到的最高浓度更大,D正确。]
5.B [化学平衡常数只与温度有关,与反应途径无关,因此两个途径下的化学平衡常数相同,故K =K
途径一
,A正确;由图可知,总反应的反应物总能量大于生成物总能量,则总反应放热,催化剂不能改变反
途径二
应热,但能降低反应的活化能,所以ΔH =ΔH <0、E >E ,B错误;由图可知,途径二中第二阶段的活化
1 2 a1 a2
能最大,则该阶段的反应速率最慢,决定着整个反应的快慢,D正确。]
6.B [反应Ⅱ的活化能为(1.45-0.73) eV=0.72 eV,A错误;反应Ⅰ的能垒最高,所以反应Ⅰ的化学反应速率
最慢,B正确;总反应的热化学方程式为4HCl(g)+O (g)===2H O(g)+2Cl (g) ΔH=-1.98N eV·mol-1,C错误;
2 2 2 A
由反应Ⅰ可知HOOCl(g)的总能量比HCl(g)和O (g)的总能量高,能量越高,物质越不稳定,D错误。]
2
7.D [由图可知,在CO →CH 历程中能垒最大的是 CO HCOO的能垒为0.77 eV,故A错误;CO 加
2 4 2 2
氢生成了副产物CO等,CH 的选择性小于100%,B项错误;由图可知 CO→CO(g) CH →CH (g)是脱
4 4 4
附过程,需要吸收能量,C项错误。]
8.A [根据图示可知,起始到TS1历程中H 分子部分变成*H,则发生了H—H非极性共价键的断裂,A项
2
正确;在前三步历程中,TS1的能垒最大,为决速反应,B项错误;从图中可知,在前三步历程中,TS3的能垒最低,此步反应的化学方程式为*CO+*OH+*H+3H (g)===*CO+3H (g)+H O(g),C项错误;由过渡
2 2 2
态的能量变化可知,物质吸附在催化剂表面,形成过渡态的过程能量升高,吸收热量,D项错误。]
9.B [根据Cl (g) 2Cl·(g) ΔH =+242.7 kJ·mol-1可知,Cl 的键能为242.7 kJ·mol-1,A正确;反应速率较
2 1 2
快的一步应该是活化能较低的一步,由图可知,反应速率较快的一步的热化学方程式为CH ·(g)+Cl (g)
3 2
CH Cl(g)+Cl·(g) ΔH=-112.9 kJ·mol-1,B错误;由图可知,链转移中碳上的氢原子可能失去,故链转移过
3
程中可能产生·CH Cl、·CHCl 、·CCl ,C正确;链终止反应的过程中,两个CH ·结合在一起可以形成乙烷,
2 2 3 3
D正确。]
10.C [最大能垒为第1步基元反应:CH OH*+HO·* CH O·*+H O*,相对能量差值为1.257×104 eV,B正
3 3 2
确;升高温度,反应速率均增大,C错误;总反应为2CH OH+CO CH OCOOCH +H O ΔH>0,为吸
3 2 3 3 2
热反应,因此适当提高温度,可以增加碳酸二甲酯的产率,D正确。]