文档内容
化学反应速率与平衡图像、图表分析
1.化学平衡与平衡转化率
(1)转化率和平衡转化率
转化率有未达到平衡的转化率和平衡转化率,在审题的时候一定要注意转化率是否为平衡转化率。
(2)转化率与温度的关系
可逆反应
的焓变ΔH
升高温度
吸热反应,
ΔH>0
未达到平衡的转化率增大
平衡转化率增大
放热反应,
ΔH<0
未达到平衡的转化率增大
平衡转化率减小
(3)增大反应物的浓度与平衡转化率的关系(其中A、B、C均为气体)
可逆
反应
改变
条件
平衡移
动方向
反应物平
衡转化率
备注
A+B
C
增大A
的浓度正向
移动
α(A)减小
α(B)增大
-
A
B+C
增大A
的浓度
正向
移动
α(A)
减小
反应物平
衡转化率
实际是考
虑压强的
影响
2A
B+C
增大A
的浓度
正向
移动
α(A)
不变
3A
B+C
增大A
的浓度
正向
移动
α(A)
增大(4)如果两气体物质的投料比按照化学计量数投料,那么无论是否达到化学平衡,两者的转化率一直相
等。
2.化学平衡常数、平衡移动方向与反应速率的关系
aA(g)+bB(g) cC(g)+dD(g)
cc (C)·cd (D) cc (C)·cd (D)
K= Q=
ca (A)·cb (B) ca (A)·cb (B)
平衡时浓度 某时刻浓度
K
{ =Q,反应处于化学平衡状态,v v
正 逆
Q,平衡向正反应方向移动,v v
正 逆
3.化学反应速率与平衡图像分析思路
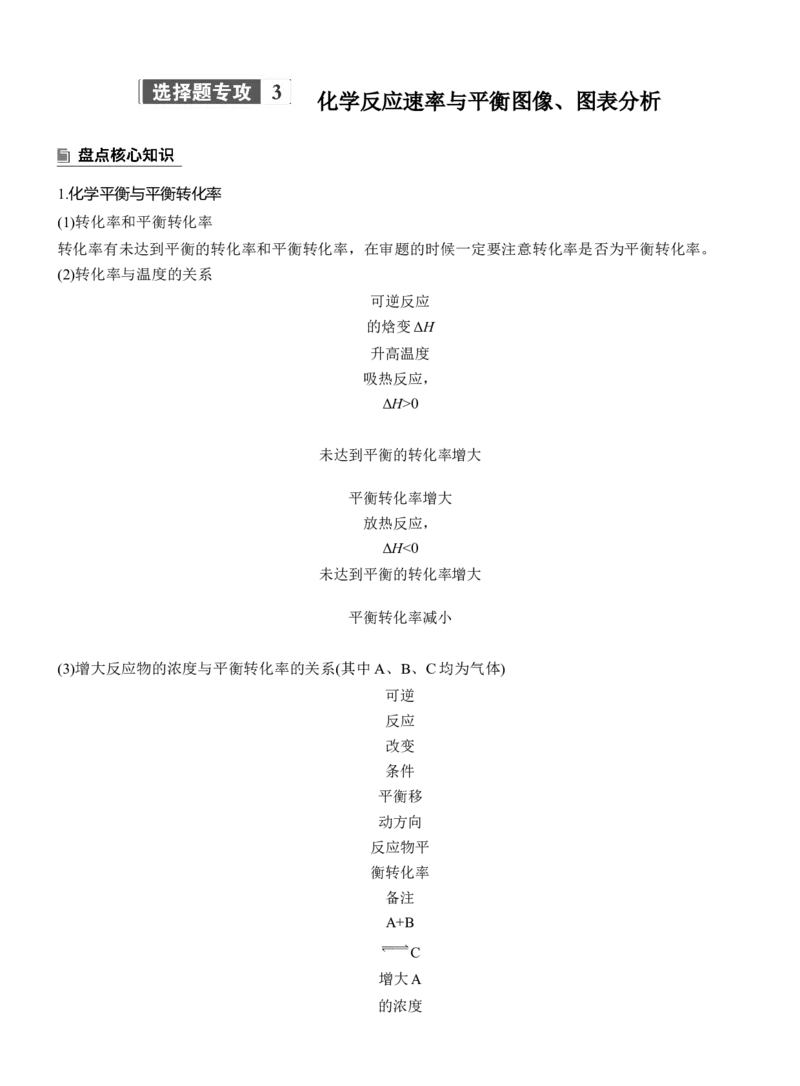
例1 (2023·河南安阳一中模拟预测) (环戊二烯)容易发生聚合反应生成二聚体,该反应为可逆反
应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法不正确的是( )
A.T ②
C.0~3 h平均速率(异山梨醇)=0.014 mol·kg-1·h-1
D.反应②加入催化剂不改变其平衡转化率
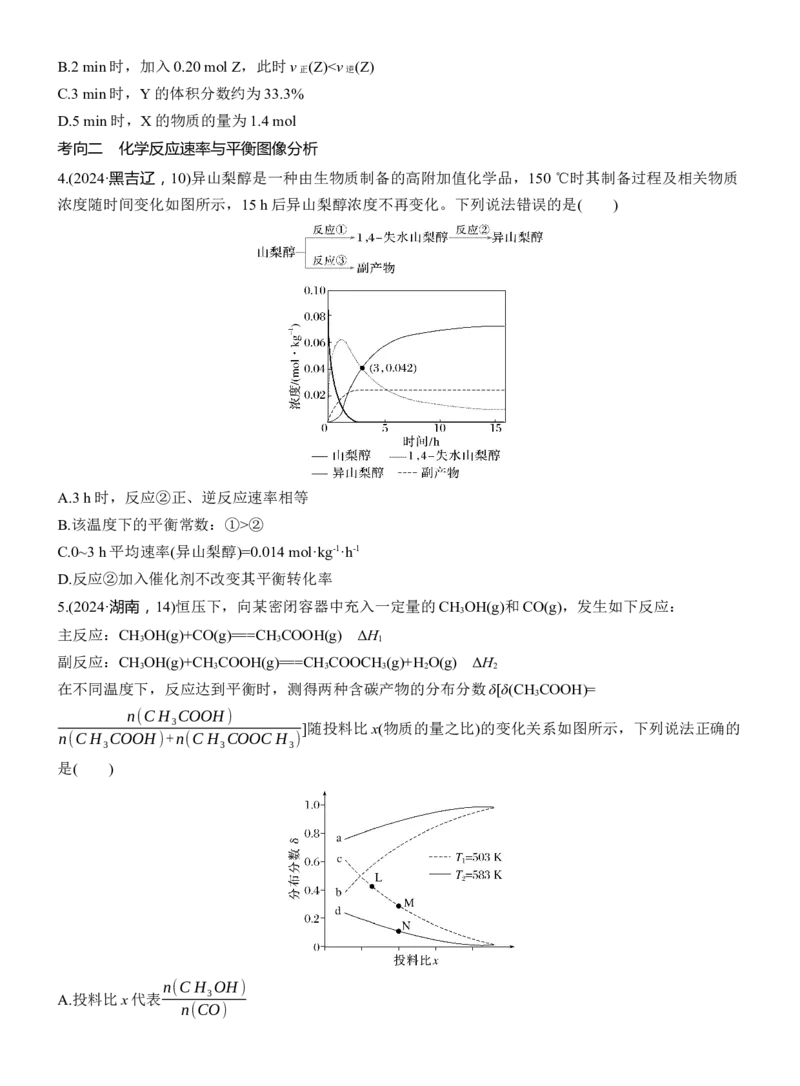
5.(2024·湖南,14)恒压下,向某密闭容器中充入一定量的CH OH(g)和CO(g),发生如下反应:
3
主反应:CH OH(g)+CO(g)===CH COOH(g) ΔH
3 3 1
副反应:CH OH(g)+CH COOH(g)===CH COOCH (g)+H O(g) ΔH
3 3 3 3 2 2
在不同温度下,反应达到平衡时,测得两种含碳产物的分布分数δ[δ(CH COOH)=
3
n(CH COOH)
3 ]随投料比x(物质的量之比)的变化关系如图所示,下列说法正确的
n(CH COOH)+n(CH COOCH )
3 3 3
是( )
n(CH OH)
A.投料比x代表 3
n(CO)B.曲线c代表乙酸的分布分数
C.ΔH <0,ΔH >0
1 2
D.L、M、N三点的平衡常数:K(L)=K(M)>K(N)
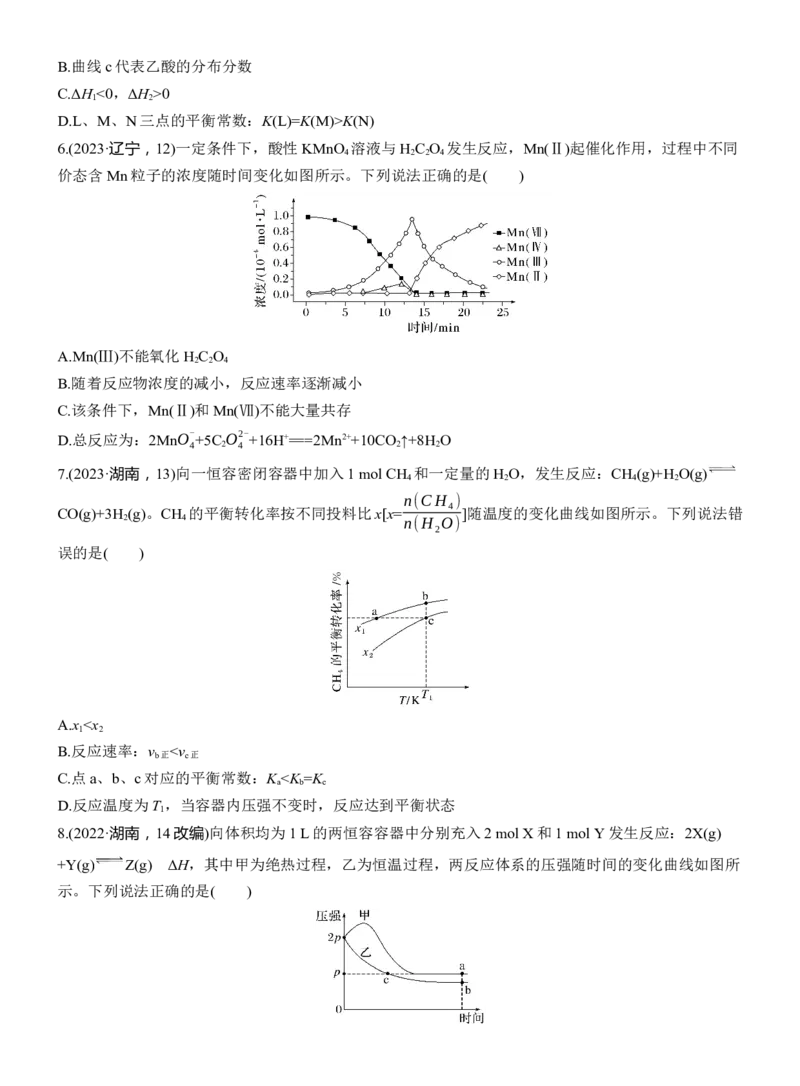
6.(2023·辽宁,12)一定条件下,酸性KMnO 溶液与H C O 发生反应,Mn(Ⅱ)起催化作用,过程中不同
4 2 2 4
价态含Mn粒子的浓度随时间变化如图所示。下列说法正确的是( )
A.Mn(Ⅲ)不能氧化H C O
2 2 4
B.随着反应物浓度的减小,反应速率逐渐减小
C.该条件下,Mn(Ⅱ)和Mn(Ⅶ)不能大量共存
D.总反应为:2MnO-
+5C
O2-
+16H+===2Mn2++10CO ↑+8H O
4 2 4 2 2
7.(2023·湖南,13)向一恒容密闭容器中加入1 mol CH 和一定量的H O,发生反应:CH (g)+H O(g)
4 2 4 2
n(CH )
CO(g)+3H (g)。CH 的平衡转化率按不同投料比x[x= 4 ]随温度的变化曲线如图所示。下列说法错
2 4 n(H O)
2
误的是( )
A.x 0
B.气体的总物质的量:n
例1 B [单位时间T 温度下,环戊二烯浓度变化大,因此速率快,则反应温度高,因此T v (Z),B错误;反
正 逆
应生成的Y与Z的物质的量之比恒等于1∶2,反应体系中只有Y和Z为气体,同温同压下,体积之比等
V(Y) 1
于物质的量之比, = ,故Y的体积分数始终约为33.3%,C正确;由B项分析可知5 min时反应处
V(Z) 2
于平衡状态,此时生成的Z为0.6 mol,则X的转化量为0.6 mol,初始X的物质的量为2.0 mol,剩余X的
物质的量为1.4 mol,D正确。]
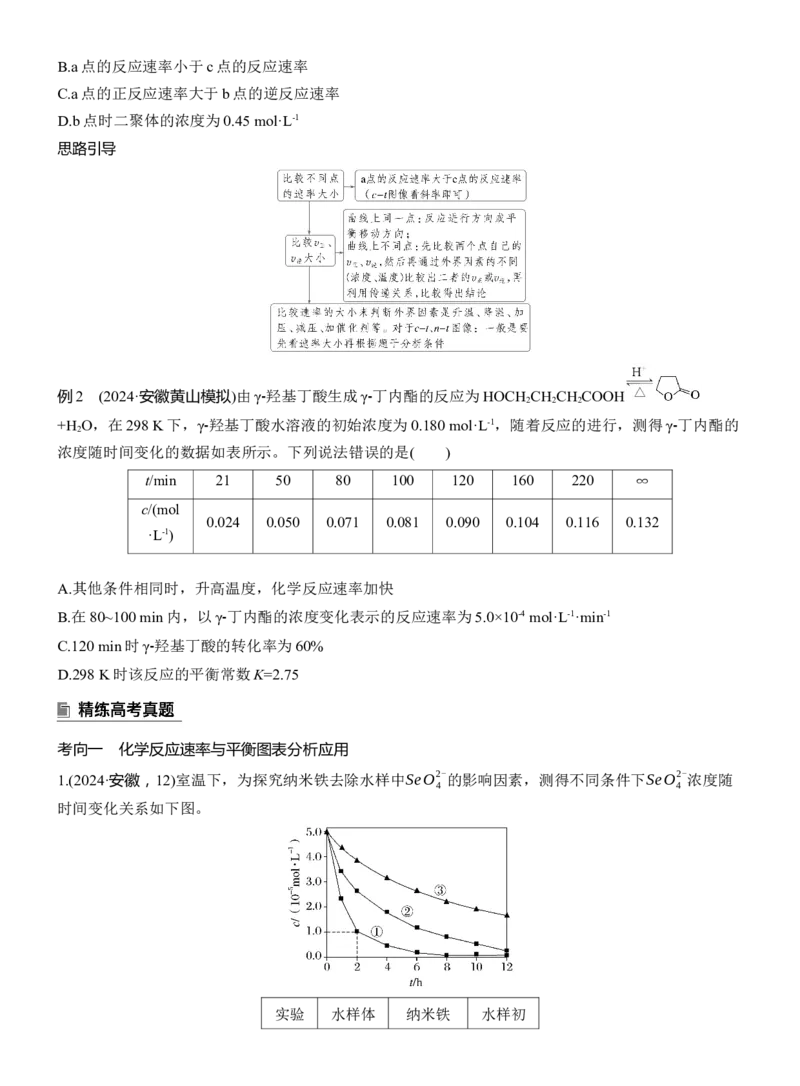
4.A [由图可知,3 h后异山梨醇浓度继续增大,15 h后异山梨醇浓度才不再变化,所以3 h时,反应②未
达到平衡状态,即正、逆反应速率不相等,故A错误;图像显示该温度下,15 h后所有物质浓度都不再变
化,且此时山梨醇转化完全,即反应充分,而1,4⁃失水山梨醇仍有剩余,即反应②正向进行程度小于反
应①,所以该温度下的平衡常数:①>②,故B正确;在0~3 h内异山梨醇的浓度变化量为0.042 mol·kg-1,
0.042mol·kg-1
所以平均速率(异山梨醇)= =0.014 mol·kg-1·h-1,故C正确;催化剂只能改变化学反应速率,
3 h
不能改变物质平衡转化率,故D正确。]
5.D [图中曲线表示的是两种含碳产物的分布分数即δ(CH COOH)、δ(CH COOCH ),结合主、副反应可知,
3 3 3
n(CO)
x代表 ,曲线a或曲线b表示CH COOH分布分数,曲线c或曲线d表示CH COOCH 分布分
n(CH OH) 3 3 3
3
n(CO)
数,故A、B错误;曲线a或曲线b表示δ(CH COOH),由图像可知,当 相同时,T >T ,T 时
3 n(CH OH) 2 1 2
3
δ(CH COOH)大于T 时,说明升高温度主反应的平衡正向移动,故ΔH >0;同理,T 时δ(CH COOCH )大
3 1 1 1 3 3
于T 时,说明升高温度副反应的平衡逆向移动,故ΔH <0,C错误;L、M、N三点对应副反应ΔH <0,且
2 2 2
T >T =T ,升高温度平衡逆向移动,故K(L)=K(M)>K(N),D正确。]
N M L
6.C [由图像可知,随着时间的推移Mn(Ⅲ)的浓度先增大后减小,说明开始反应生成Mn(Ⅲ),后Mn(Ⅲ)
被消耗生成Mn(Ⅱ),Mn(Ⅲ)能氧化H C O ,A项错误;随着反应物浓度的减小,到大约13 min时开始生
2 2 4
成Mn(Ⅱ),Mn(Ⅱ)对反应起催化作用,13 min后反应速率会增大,B项错误;由图像可知,Mn(Ⅶ)的浓度
为0后才开始生成Mn(Ⅱ),该条件下Mn(Ⅱ)和Mn(Ⅶ)不能大量共存,C项正确;H C O 为弱酸,在离子
2 2 4
方程式中不拆成离子,总反应为2MnO-
+5H C O +6H+===2Mn2++10CO ↑+8H O,D项错误。]
4 2 2 4 2 2
7.B [一定条件下,增大H O(g)的浓度,能提高CH 的转化率,即x值越小,CH 的转化率越大,则
2 4 4
x v ,故B错误;由图像可知,x一定时,温度升高CH 的平衡转化
b正 c正 4
率增大,说明正反应为吸热反应,温度升高平衡正向移动,K增大,温度相同,K不变,则点a、b、c对
应的平衡常数:K0.75,即平衡常数K>12,故C错误;根据图像可知,甲容
2
器达到平衡的时间短,温度高,所以达到平衡的速率相对乙容器的快,即v >v ,故D错误。]
a正 b正