文档内容
专题十五 盐类的水解
一、盐类的水解及其规律
1.定义:在水溶液中盐电离出来的离子跟水所电离出来的H+或 OH-结合生成弱电解质的反应,叫做盐类的
水解。
2.水解实质:盐和水发生反应生成弱电解质,使水的电离平衡被破坏,从而建立新的平衡的过程。
3.水解特点:①只有弱酸的阴离子或弱碱的阳离子才能与H+或OH-结合生成弱电解质。
②盐类水解使水的电离平衡发生移动,促进水的电离,使水电离出的c(OH-)≠c(H+)并使溶液呈酸性或碱性。
③盐类水解反应是酸碱中和反应的逆反应。水解是微弱的程度很小,故水解产物极少,盐溶液的酸碱性极
弱,用“ ”号。
④盐类水解是吸热反应。
4.盐类的水解规律:有弱才水解、无弱不水解、越弱越水解、谁强显谁性、双弱具体定。
具体为:
(1)正盐溶液:①强酸弱碱盐呈酸性;②强碱弱酸盐呈碱性;
③强酸强碱盐呈中性;④弱酸弱碱盐不一定。
如 NH CN CH COONH NH F
4 3 4 4
碱性 中性 酸性
取决于弱酸弱碱 相对强弱
(2)酸式盐
①若只有电离而无水解,则呈酸性(如NaHSO);
4
②若既有电离又有水解,取决于两者相对大小;
电离程度>水解程度,呈酸性;电离程度<水解程度,呈碱性
强碱弱酸式盐的电离和水解,如HPO 及其三种阴离子随溶液pH变化可相互转化:
3 4
pH值增大
HPO H PO - HPO 2- PO 3-
3 4 2 4 4 4
pH减小
③常见酸式盐溶液的酸碱性碱性:NaHCO 、NaHS、NaHPO
3 2 4
酸性:NaHSO、NaHC O、NaH PO
3 2 4 2 4
【注意】比较盐类水解程度的相对大小
(1)盐对应的弱酸(或弱碱)越弱,水解程度越大。
(2)同种弱酸(或弱碱)的盐溶液浓度越小,水解程度越大。
(3)相同条件下的水解程度:正盐>相应酸式盐,如CO>HCO。
(4)相互促进水解的盐>单独水解的盐>水解相互抑制的盐。如NH的水解:
(NH )CO>(NH)SO >(NH)Fe(SO )。
4 2 3 4 2 4 4 2 4 2
(5)温度越高,盐的水解程度越大。
二、盐类水解的影响因素及应用
1.探究影响盐类水解平衡的因素
(1)内因:盐类本身的性质是影响盐类水解的内在因素,也是主要因素。组成盐的酸或碱越弱,盐的水
解程度越大,其盐溶液的酸性或碱性就越强。
(2)外界条件:
①温度:盐的水解是吸热反应,升高温度,水解程度增大。
②浓度:加入水,溶液浓度减小,使平衡向正反应方向移动,水解程度增大。
③外加相关离子:盐类水解后,溶液会呈现不同的酸碱性。外加酸或碱,可以促进或抑制盐的水解。如在
配制FeCl 溶液时常加入少量盐酸来抑制FeCl 水解。
3 3
【小结】影响盐类水解的因素
溶液中离
因素 水解平衡 水解程度
子的浓度
温度 升高 右移 增大 增大
增大 右移 减小 增大
浓度
减小
右移 增大 减小
(稀释)
促进弱酸阴离子的水解,使其水解程度增大;抑制弱碱阳离子的
酸
外加 水解,使其水解程度减小
酸、
碱 抑制弱酸阴离子的水解,使其水解程度减小;促进弱碱阳离子的
碱
水解,使其水解程度增大
加能水解的盐
小结:强酸弱碱盐:加强酸抑制水解,加强碱促进水解;强碱弱酸盐:加强酸促进水解,加强碱抑制水解。
2.水解原理的应用
下列有关问题与盐的水解有关的是①②③④⑤⑥。
①NH Cl与ZnCl 溶液可作焊接金属时的除锈剂
4 2
②NaHCO 与Al (SO ) 两种溶液可作泡沫灭火剂
3 2 4 3
③草木灰与铵态氮肥不能混合施用
④实验室中盛放NaCO 溶液的试剂瓶不能用磨口玻璃塞
2 3
⑤加热蒸干CuCl 溶液得到Cu(OH) 固体
2 2
⑥要除去CuCl 溶液中混有的Fe2+,可先通入氧化剂Cl,再调节溶液的pH
2 2
三、把握三种守恒,明确等量关系
(1)电荷守恒
电解质溶液必须保持电中性,即阴离子所带负电荷总数一定等于阳离子所带正电荷总数。
(2)元素质量守恒
变化前后某种元素的原子个数守恒。
①单一元素守恒,如1 mol NH 通入水中形成氨水,就有n(NH )+n(NH ·H O)+n(NH)=1 mol,即氮元素
3 3 3 2
守恒。
②两元素守恒,如NaHCO 溶液中,c(Na+)=c(H CO)+c(HCO)+c(CO),即钠元素与碳元素守恒。
3 2 3
(3)质子守恒
电解质溶液中,由于电离、水解等过程的发生,往往存在质子(H+)的转移,转移过程中质子数量保持不变,
称为质子守恒。
四、比较电解质溶液中粒子浓度相对大小
1. 解题思路2. 溶液中粒子浓度的三个守恒关系
(1)电荷守恒:指在电解质的水溶液中,阳离子的所带总电荷数与阴离子的所带总电荷数必须相等。因为溶
液总是呈电中性的。
如在NaCO 溶液中存在Na+、CO2-、H+、OH-、HCO -,它们存在如下关
2 3 3 3
系: c(Na+)+c(H+)=2c(CO 2-)+c(HCO-)+c(OH-)。
3 3
(2)物料守恒(原子守恒):指一个平衡体系中,某一组分的总浓度一定等于它所离解成的多种微粒的平衡
浓度之和,也就是变化前后某种元素的原子个数守恒。
例如:c mol·L-1的NaCO 溶液的物料守恒,可以根据溶液中存在的平衡关系:
2 3
在NaCO 溶液的物料守恒:c(Na+)=2 c(CO2-)+2c(HCO-)+2c(H CO)
2 3 3 3 2 3
(3)质子守恒
即HO电离的H+和OH-浓度相等。指溶液中得到质子的物质的量应该与失去质子的物质的量相等。如
2
在NaCO 溶液中水电离出OH-和H+,其中水电离出的H+以H+、HCO -、HCO 三种形式存在于溶液中,则有
2 3 3 2 3
c(OH-)=c(H+)+c(HCO -)+2c(H CO)(由电荷守恒式减去物料守恒式也可求出质子守恒式)。
3 2 3规律小结 盐溶液的配制与保存注意事项
(1)强酸弱碱盐:配制FeCl 、SnCl 、Fe (SO ) 溶液时,常加入少量相应酸来抑制弱碱阳离子的水解。
3 2 2 4 3
(2)强碱弱酸盐:配制NaCO 溶液时,常加入少量相应的碱来抑制弱酸根离子的水解。
2 3
(3)Na CO 溶液、NaHCO 溶液等由于水解使溶液呈碱性,故不能用带玻璃塞的玻璃瓶来盛。又如:
2 3 3
NaF溶液保存时不能用玻璃容器装,因F-+HO HF+OH-,生成的氢氟酸会与玻璃的成分之一二氧
2
化硅反应,长时间会漏液。常用塑料或铅制容器装NaF溶液或氢氟酸。
1.【2022年辽宁卷】甘氨酸 是人体必需氨基酸之一、在 时, 、
和 的分布分数【如 】与溶液 关系如
图。下列说法错误的是
A.甘氨酸具有两性
B.曲线c代表
C. 的平衡常数
D.
2.(2021·广东真题)鸟嘌呤( )是一种有机弱碱,可与盐酸反应生成盐酸盐(用 表示)。已知 水
溶液呈酸性,下列叙述正确的是
A. 水溶液的B. 水溶液加水稀释, 升高
C. 在水中的电离方程式为:
D. 水溶液中:
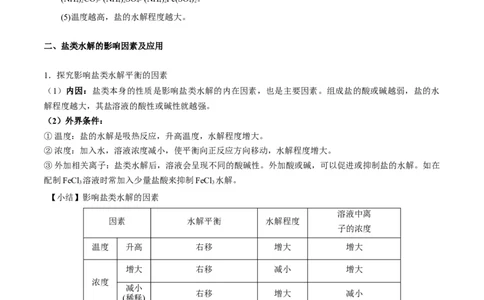
3.(2021·山东真题)赖氨酸[H N+(CH)CH(NH)COO-,用HR表示]是人体必需氨基酸,其盐酸盐
3 2 4 2
(H RCl )在水溶液中存在如下平衡:HR2+ HR+ HR R-。向一定浓度的HRCl 溶液中滴
3 2 3 2 3 2
加NaOH溶液,溶液中HR2+、HR+、HR和R-的分布系数δ(x)随pH变化如图所示。已知δ(x)=
3 2
,下列表述正确的是
A. >
B.M点,c(Cl-) +c(OH-)+c(R-)=2c(H R+)+c(Na+)+c(H+)
2
C.O点,pH=
D.P点,c(Na+)>c(Cl-)>c(OH-)>c(H+)
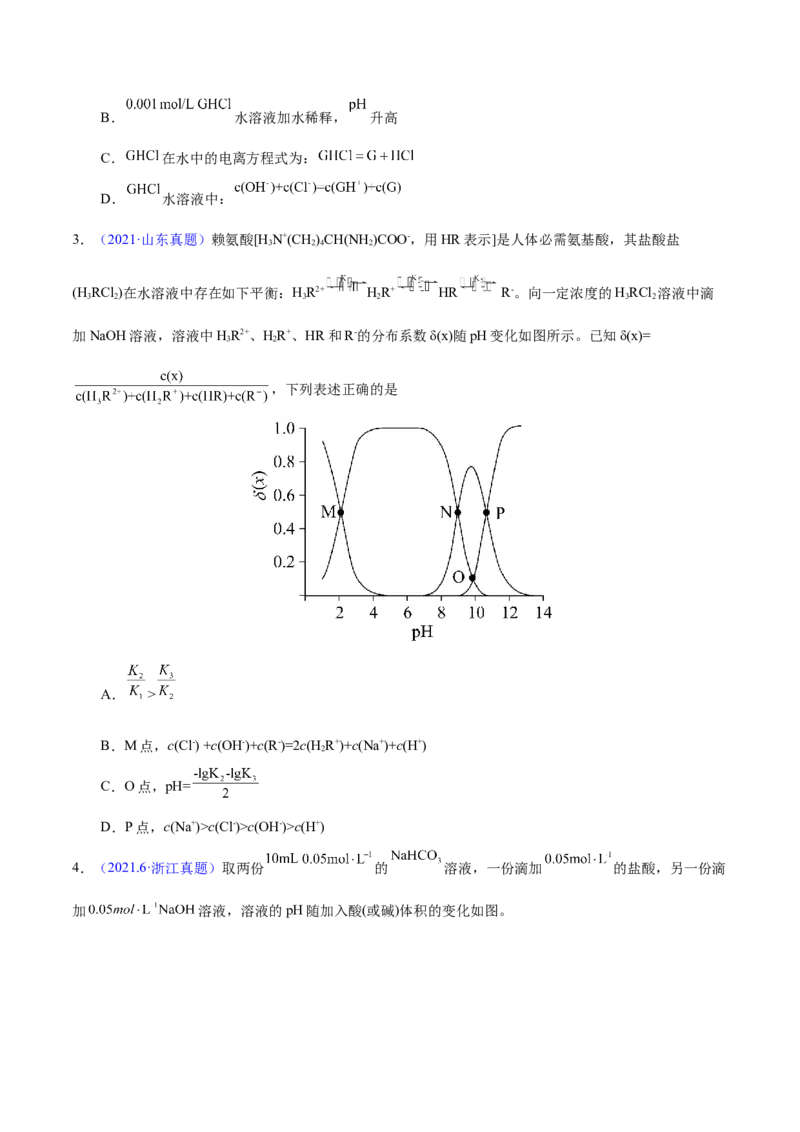
4.(2021.6·浙江真题)取两份 的 溶液,一份滴加 的盐酸,另一份滴
加 溶液,溶液的pH随加入酸(或碱)体积的变化如图。下列说法不正确的是
A.由a点可知: 溶液中 的水解程度大于电离程度
B. 过程中: 逐渐减小
C. 过程中:
D.令c点的 ,e点的 ,则
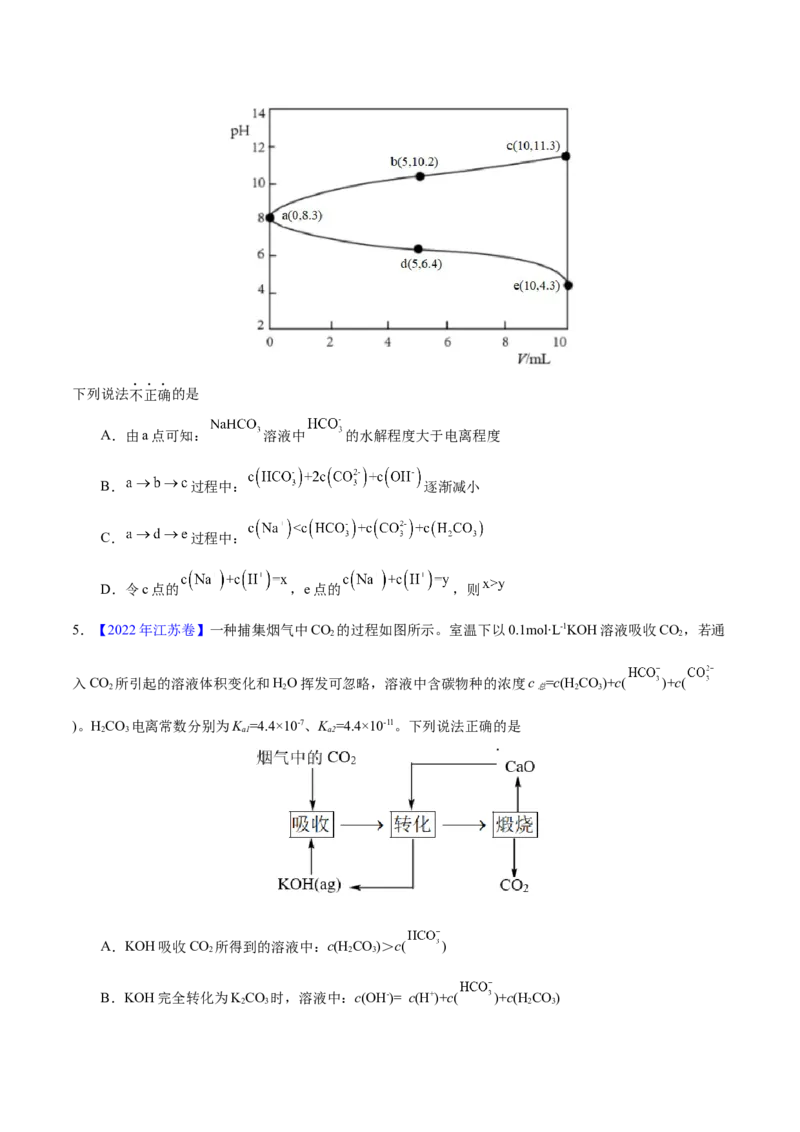
5.【2022年江苏卷】一种捕集烟气中CO 的过程如图所示。室温下以0.1mol∙L-1KOH溶液吸收CO,若通
2 2
入CO 所引起的溶液体积变化和HO挥发可忽略,溶液中含碳物种的浓度c =c(H CO)+c( )+c(
2 2 总 2 3
)。HCO 电离常数分别为K =4.4×10-7、K =4.4×10-11。下列说法正确的是
2 3 a1 a2
A.KOH吸收CO 所得到的溶液中:c(H CO)>c( )
2 2 3
B.KOH完全转化为KCO 时,溶液中:c(OH-)= c(H+)+c( )+c(H CO)
2 3 2 3C.KOH溶液吸收CO,c =0.1mol∙L-1溶液中:c(H CO)>c( )
2 总 2 3
D.如图所示的“吸收”“转化”过程中,溶液的温度下降
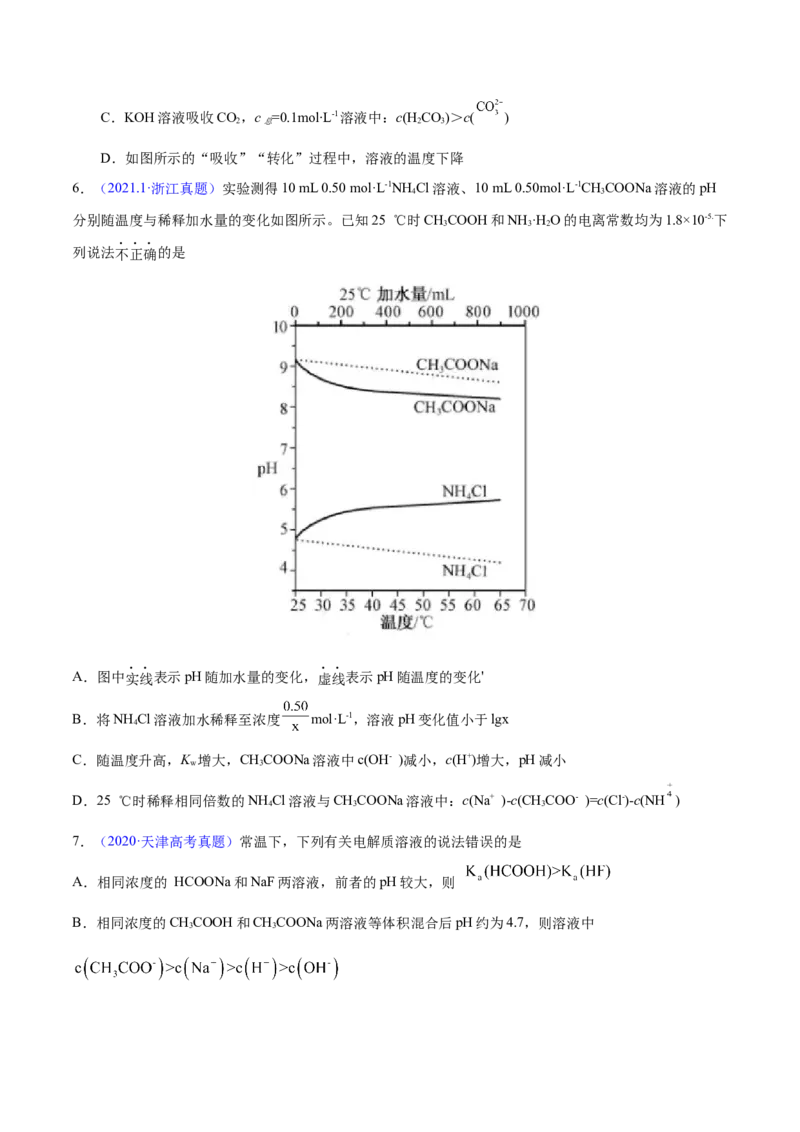
6.(2021.1·浙江真题)实验测得10 mL 0.50 mol·L-1NH Cl溶液、10 mL 0.50mol·L-1CHCOONa溶液的pH
4 3
分别随温度与稀释加水量的变化如图所示。已知25 ℃时CHCOOH和NH ·H O的电离常数均为1.8×10-5.下
3 3 2
列说法不正确的是
A.图中实线表示pH随加水量的变化,虚线表示pH随温度的变化'
B.将NH Cl溶液加水稀释至浓度 mol·L-1,溶液pH变化值小于lgx
4
C.随温度升高,K 增大,CHCOONa溶液中c(OH- )减小,c(H+)增大,pH减小
w 3
D.25 ℃时稀释相同倍数的NH Cl溶液与CHCOONa溶液中:c(Na+ )-c(CHCOO- )=c(Cl-)-c(NH )
4 3 3
7.(2020·天津高考真题)常温下,下列有关电解质溶液的说法错误的是
A.相同浓度的 HCOONa和NaF两溶液,前者的pH较大,则
B.相同浓度的CHCOOH和CHCOONa两溶液等体积混合后pH约为4.7,则溶液中
3 3C.FeS溶于稀硫酸,而CuS不溶于稀硫酸,则
D.在 溶液中,
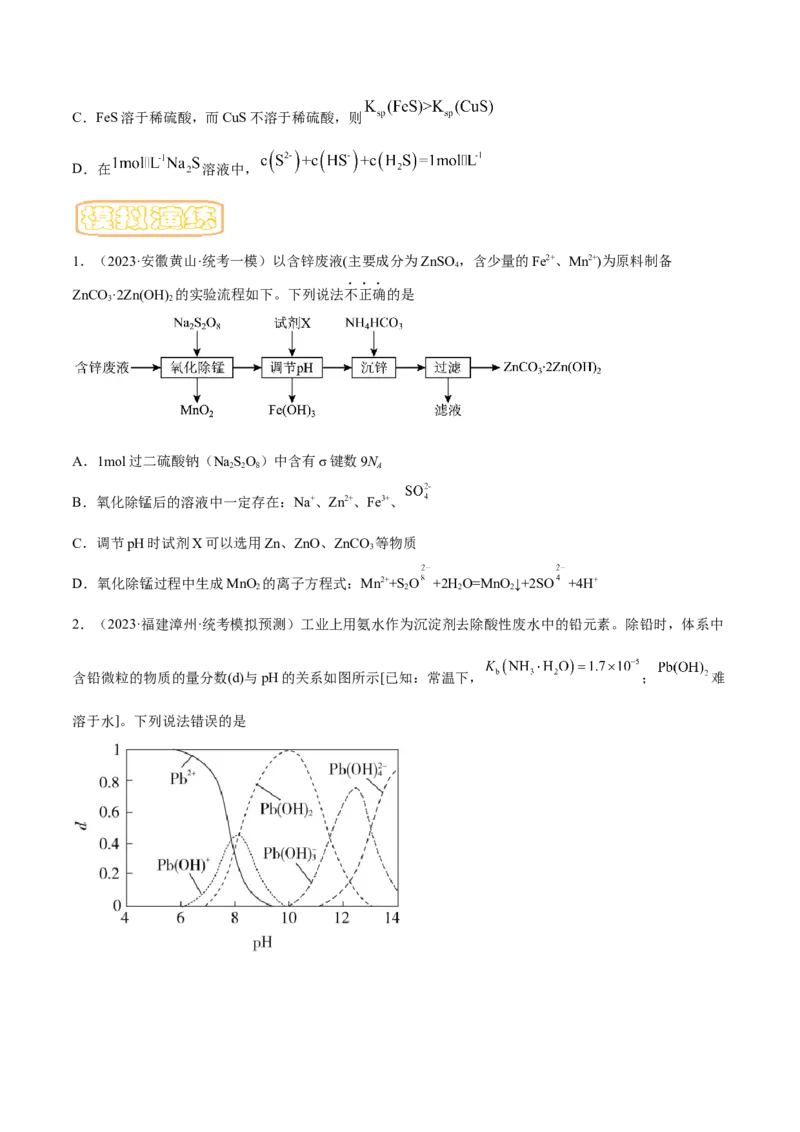
1.(2023·安徽黄山·统考一模)以含锌废液(主要成分为ZnSO,含少量的Fe2+、Mn2+)为原料制备
4
ZnCO ·2Zn(OH) 的实验流程如下。下列说法不正确的是
3 2
A.1mol过二硫酸钠(NaSO)中含有σ键数9N
2 2 8 A
B.氧化除锰后的溶液中一定存在:Na+、Zn2+、Fe3+、
C.调节pH时试剂X可以选用Zn、ZnO、ZnCO 等物质
3
D.氧化除锰过程中生成MnO 的离子方程式:Mn2++S O +2H O=MnO ↓+2SO +4H+
2 2 2 2
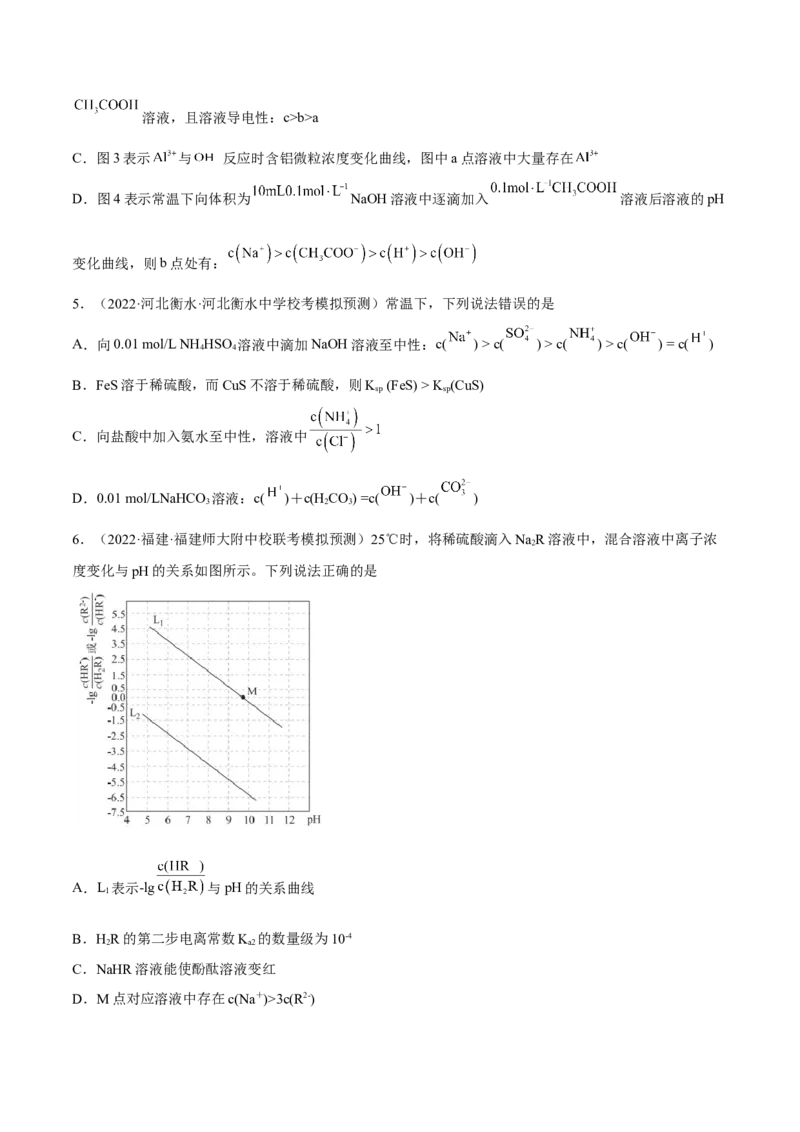
2.(2023·福建漳州·统考模拟预测)工业上用氨水作为沉淀剂去除酸性废水中的铅元素。除铅时,体系中
含铅微粒的物质的量分数(d)与pH的关系如图所示[已知:常温下, ; 难
溶于水]。下列说法错误的是A. 时, 与氨水反应生成 ,溶液中
B. 时,
C. 时, 物质的量分数最大,除铅效果最好
D. 时, 转化为 的离子方程式为
3.(2023·广东清远·清新一中校考模拟预测)下列叙述中正确的是
A.室温下,向浓度为 弱酸HA溶液中,滴加同浓度的NaOH溶液,溶液的pH与 的
差为定值
B.常温下, HSeO 的电离方程式: , ,浓度均为 的
2 4
① 溶液、② 溶液、③ 溶液, 由大到小的顺序为③>②>①
C.同浓度的 溶液和盐酸,加水稀释相同倍数时 相等
D.将硫化氢气体通入硫酸铜溶液中,不能发生反应 (已知:室温下,氢硫酸两级电
离常数分别为 、 , )
4.(2023·湖南邵阳·统考一模)根据下列各图曲线表征的信息,得出的结论正确的是
A.由图1得出若要除去 溶液中的 ,可采用向溶液中加入适量CuO,调节溶液的pH至4左右
B.图2表示用水稀释pH相同的盐酸和 溶液时,溶液的pH变化曲线,其中I表示盐酸,II表示溶液,且溶液导电性:c>b>a
C.图3表示 与 反应时含铝微粒浓度变化曲线,图中a点溶液中大量存在
D.图4表示常温下向体积为 NaOH溶液中逐滴加入 溶液后溶液的pH
变化曲线,则b点处有:
5.(2022·河北衡水·河北衡水中学校考模拟预测)常温下,下列说法错误的是
A.向0.01 mol/L NH HSO 溶液中滴加NaOH溶液至中性:c( ) > c( ) > c( ) > c( ) = c( )
4 4
B.FeS溶于稀硫酸,而CuS不溶于稀硫酸,则K (FeS) > K (CuS)
sp sp
C.向盐酸中加入氨水至中性,溶液中
D.0.01 mol/LNaHCO 溶液:c( )+c(HCO) =c( )+c( )
3 2 3
6.(2022·福建·福建师大附中校联考模拟预测)25℃时,将稀硫酸滴入NaR溶液中,混合溶液中离子浓
2
度变化与pH的关系如图所示。下列说法正确的是
A.L 表示-lg 与pH的关系曲线
1
B.HR的第二步电离常数K 的数量级为10-4
2 a2
C.NaHR溶液能使酚酞溶液变红
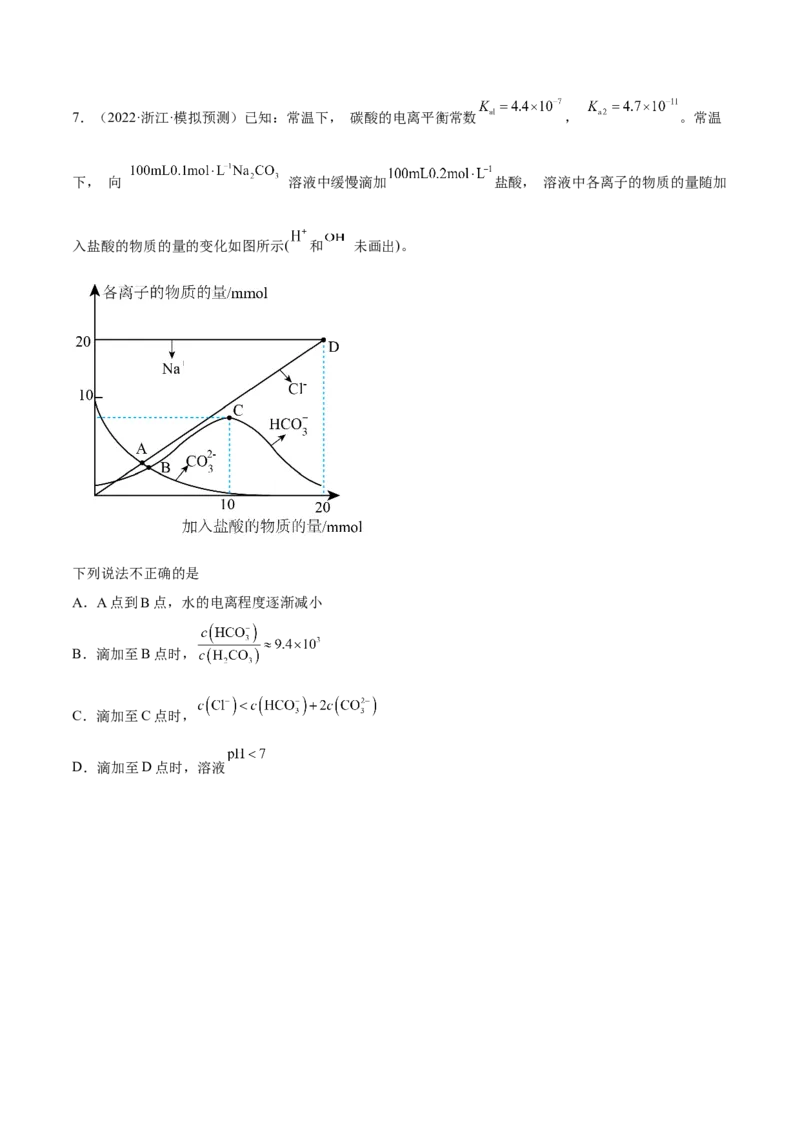
D.M点对应溶液中存在c(Na+)>3c(R2-)7.(2022·浙江·模拟预测)已知:常温下, 碳酸的电离平衡常数 , 。常温
下, 向 溶液中缓慢滴加 盐酸, 溶液中各离子的物质的量随加
入盐酸的物质的量的变化如图所示( 和 未画出)。
下列说法不正确的是
A.A点到B点,水的电离程度逐渐减小
B.滴加至B点时,
C.滴加至C点时,
D.滴加至D点时,溶液