文档内容
专题十四 弱电解质的电离
一、定义及特征
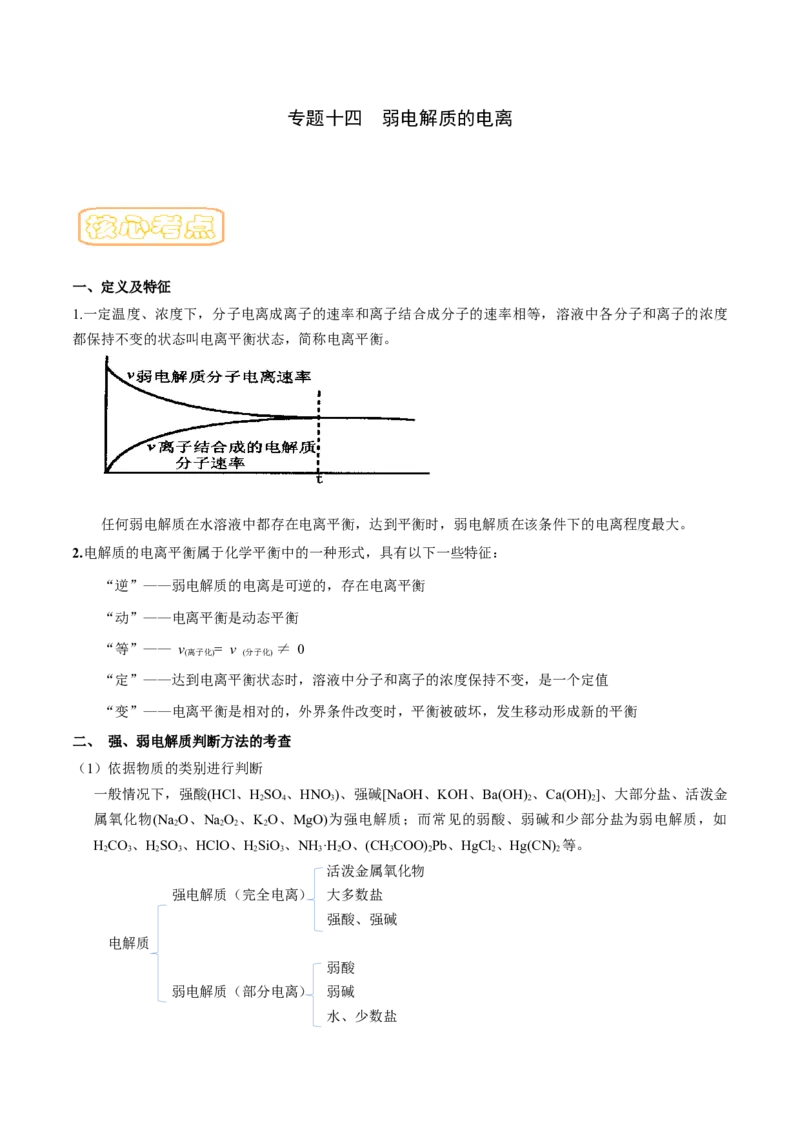
1.一定温度、浓度下,分子电离成离子的速率和离子结合成分子的速率相等,溶液中各分子和离子的浓度
都保持不变的状态叫电离平衡状态,简称电离平衡。
任何弱电解质在水溶液中都存在电离平衡,达到平衡时,弱电解质在该条件下的电离程度最大。
2.电解质的电离平衡属于化学平衡中的一种形式,具有以下一些特征:
“逆”——弱电解质的电离是可逆的,存在电离平衡
“动”——电离平衡是动态平衡
“等”—— v = v ≠ 0
(离子化) (分子化)
“定”——达到电离平衡状态时,溶液中分子和离子的浓度保持不变,是一个定值
“变”——电离平衡是相对的,外界条件改变时,平衡被破坏,发生移动形成新的平衡
二、 强、弱电解质判断方法的考查
(1)依据物质的类别进行判断
一般情况下,强酸(HCl、HSO 、HNO)、强碱[NaOH、KOH、Ba(OH) 、Ca(OH) ]、大部分盐、活泼金
2 4 3 2 2
属氧化物(Na O、NaO 、KO、MgO)为强电解质;而常见的弱酸、弱碱和少部分盐为弱电解质,如
2 2 2 2
HCO、HSO 、HClO、HSiO、NH ·H O、(CHCOO) Pb、HgCl 、Hg(CN) 等。
2 3 2 3 2 3 3 2 3 2 2 2
活泼金属氧化物
强电解质(完全电离) 大多数盐
强酸、强碱
电解质
弱酸
弱电解质(部分电离) 弱碱
水、少数盐(2)依据强、弱电解质的定义或弱电解质电离平衡的移动规律进行判断
①在相同温度、相同浓度下,进行导电性对比实验,如 HCl 与 CHCOOH,CHCOOH 导电性,则
3 3
CHCOOH为弱电解质。
3
②在相同温度、相同浓度下,比较反应速率的快慢,如将锌粒投入等浓度的 HCl与CHCOOH中,则
3
CHCOOH反应慢,为弱电解质。
3
③浓度与pH的关系,浓度均为0.01 mol·L-1的HCl与CHCOOH,pH =2而CHCOOH的pH>2,为弱电解
3 HCl 3
质。
④利用盐类的水解,测定对应盐的酸碱性,如CHCOONa 溶液呈碱性,则证明CHCOOH 是弱酸。
3 3
⑤根据同离子效应的实验证明存在电离平衡,如:浓度均为 0.01 mol·L-1的HCl与CHCOOH,分别加入
3
固体NaCl、CHCOONa后,HCl的pH不变,CHCOOH的pH变大。
3 3
⑥稀释前后的pH 与稀释倍数的变化关系,如将pH=2 的酸稀释1000 倍,若pH=5,为强酸,pH<5,则
为弱酸。
三、与电离度结合的考查
当弱电解质在溶液里达到电离平衡时,溶液中已经电离的电解质分子数占原来总分子数(包括已电离
的和未电离的)的百分数叫做电离度。反映了弱电解质电离程度的相对强弱,常用α表示。
α= ×100%
例如:一元弱酸、弱碱电离度的计算。设c为一元弱酸、一元弱碱的物质的量浓度。
C(H+
)
一元弱酸:HA H++A-,α= ×100%,c(H+)=c·α
C
C(H+
)
一元弱碱:BOH B++OH-,α= ×100%,c(OH-)=c·α
C
四、外界条件对弱电解质电离平衡的影响
(1)温度: 升高温度,由于电离过程吸热,平衡向电离方向移动,电离程度增大。
(2)浓度: 加水稀释,使弱电解质的浓度减小,电离平衡向电离的方向移动,电离程度增大。因为溶液浓
度越小,离子相互碰撞结合成分子的机会越小,弱电解质的电离程度就越大,所以,稀释溶液会促进弱电
解质的电离。
例如:在醋酸的电离平衡 CHCOOH CH COO-+H+
3 3
①加水稀释,平衡向正向移动,电离程度变大,但c(CHCOOH)、c(H+)、c(CHCOO-)变小;
3 3
②加入少量冰醋酸,平衡向正向移动,c(CHCOOH)、c(H+)、c(CHCOO-)均增大但电离程度小;
3 3
(3)外加相关物质(同离子效应)
例如:0.1 mol/L的CHCOOH溶液 CHCOOH CH COO-+ H+
3 3 3向其中加入CHCOONa固体,溶液中c(CHCOO-)增大,CHCOOH的电离平衡逆向移动,电离程度减小,
3 3 3
c(H+)减小,pH增大。
五、电离平衡常数的考查
弱电解质的电离是一个可逆过程,在一定条件下达到电离平衡时,溶液中弱电解质电离生成的各种离
子平衡浓度的乘积,与溶液中未电离分子的平衡浓度的比值是一个常数,叫做该弱电解质的电离平衡常数,
简称电离常数。弱酸在水中的电离常数通常用K 表示,弱碱的电离常数用K 表示。
a b
如CHCOOH CHCOO-+H+, c(CH COOH− )c(H+ )
3 3 K = 3
a c(CH COOH)
3
说明:(1)电离平衡常数只用于弱电解质的计算。
(2)电离平衡常数只与温度有关,与浓度无关。因电离过程是吸热过程,故它随温度的升高而增大。
(3)电离平衡常数是表征了弱电解质的电离能力大小,也是弱酸、弱碱是否达到平衡状态的标志。
六、比较溶液导电性强弱、pH等综合考查
(1)强弱电解质与溶解度的关系
强电解质的溶解度不一定大,弱电解质的溶解度不一定小。比如: CaCO 属于强电解质,但是溶解度很
3
小;CHCOOH 属于弱电解质,但是溶解度比较大。
3
(2)强弱电解质与导电性的关系
强电解质溶液的导电能力不一定强,弱电解质溶液的导电能力也不一定弱。导电能力的强弱要看溶液中
离子浓度的大小和离子所带电荷的多少,离子浓度大的,所带电荷多的,导电性强。如果某强电解质溶液
浓度很小,那么它的导电性可以很弱(AgCl);而某弱电解质虽然电离程度小,但浓度较大时,该溶液的
导电能力也可以较强(CHCOOH)。
3
七、同浓度(或PH)强弱电解质的比较
(1)相同体积、相同物质的量浓度的比较,比如:一元强酸(HCl)和一元弱酸(CHCOOH)
3
酸的浓度 C(H+) pH 开始与金 中和碱的 与活泼金
属反应的 能力 属反应产
速率 生H 的量
2
一元强酸 相同 大 小 大 相同 相同
一元弱酸 小 大 小
(2)相同体积、相同pH的比较,比如:一元强酸(HCl)和一元弱酸(CHCOOH)
3
酸的浓度 C(H+) pH 开始与金 中和碱的 与活泼金
属反应的 能力 属反应产
速率 生H 的量
2
一元强酸 小 相同 相同 相同 小 小一元弱酸 大 大 大
1.【2022年湖北卷】根据酸碱质子理论,给出质子 的物质是酸,给出质子的能力越强,酸性越强。
已知: , ,下列酸性强弱顺序正确的是
A. B.
C. D.
【答案】D
【解析】根据复分解反应的规律,强酸能制得弱酸,根据酸碱质子理论,给出质子 的物质是酸,则反
应 中,酸性: ,反应 中,
酸性: ,故酸性: ,答案选D。
2.【2022年海南卷】NaClO溶液具有漂白能力,已知25℃时,K=(HClO)=4.0×10-8。下列关于NaClO溶
a
液说法正确的是
A.0.01mol/L溶液中,c(ClO-)<0.01mol/L
B.长期露置在空气中,释放Cl,漂白能力减弱
2
C.通入过量SO ,反应的离子方程式为SO +ClO-+H O=HSO +HClO
2 2 2
D.25℃,pH=7.0的NaClO和HClO的混合溶液中,c(HClO)>c(ClO-)=c(Na+)
【答案】AD
【解析】A.NaClO溶液中ClO-会水解,故0.01mol/L NaClO溶液中c(ClO-)<0.01mol/L,A正确;B.次氯
酸钠溶液中的ClO-会发生水解生成HClO,HClO长期露置在空气中会分解,为HCl和O,不会释放
2
Cl,B错误;C.将过量的SO 通入NaClO溶液中,SO 被氧化:SO +ClO−+H O=Cl-+ +2H+,C错
2 2 2 2 2
误;D.25℃,pH=7.0的NaClO和HClO的混合溶液中,存在电荷守恒:c(ClO-)+c(OH-)=c(H+)+c(Na+),则c(ClO-)=c(Na+),又c(HClO)>c(ClO-),所以c(HClO)>c(ClO-)=c(Na+),D正确;答案选
AD。
3.【2022年全国乙卷】常温下,一元酸 的 。在某体系中, 与 离子不能穿过隔
膜,未电离的 可自由穿过该膜(如图所示)。
设溶液中 ,当达到平衡时,下列叙述正确的是
A.溶液Ⅰ中
B.溶液Ⅱ中的HA的电离度 为
C.溶液Ⅰ和Ⅱ中的 不相等
D.溶液Ⅰ和Ⅱ中的 之比为
【答案】B
【解析】A.常温下溶液I的pH=7.0,则溶液I中c(H+)=c(OH-)=1×10-7mol/L,c(H+)<c(OH-)+c(A-),A错误;
B.常温下溶液II的pH=1.0,溶液中c(H+)=0.1mol/L,K = =1.0×10-3,c (HA)=c(HA)+c(A-),
a 总
则 =1.0×10-3,解得 = ,B正确;C.根据题意,未电离的HA可自由穿过隔膜,故
溶液I和II中的c(HA)相等,C错误;D.常温下溶液I的pH=7.0,溶液I中c(H+)=1×10-7mol/L,K =
a
=1.0×10-3,c (HA)=c(HA)+c(A-), =1.0×10-3,溶液I中c
总 总(HA)=(104+1)c(HA),溶液II的pH=1.0,溶液II中c(H+)=0.1mol/L,K = =1.0×10-3,c
a 总
(HA)=c(HA)+c(A-), =1.0×10-3,溶液II中c (HA)=1.01c(HA),未电离的HA可自由穿
总
过隔膜,故溶液I和II中的c(HA)相等,溶液I和II中c (HA)之比为
总
[(104+1)c(HA)]∶[1.01c(HA)]=(104+1)∶1.01≈104,D错误;
4.【2022年6月浙江卷】关于反应 ,达到平衡后,
下列说法不正确的是
A.升高温度,氯水中的 减小
B.氯水中加入少量醋酸钠固体,上述平衡正向移动, 增大
C.取氯水稀释, 增大
D.取两份氯水,分别滴加 溶液和淀粉KI溶液,若前者有白色沉淀,后者溶液变蓝色,可以
证明上述反应存在限度
【答案】D
【解析】A.HClO受热易分解,升高温度,HClO分解,平衡正向移动,c(HClO)减小,A正确;B.氯水
中加入少量醋酸钠固体,醋酸根离子和氢离子结合生成醋酸分子,氢离子浓度减小,平衡正向移动,
c(HClO)增大,B正确;C.氯水稀释,平衡正向移动,而c(HClO)和c(Cl-)均减小,但HClO本身也存在电
离平衡HClO⇌H++ClO-,稀释促进了HClO的电离,使c(HClO)减少更多,因此 增大,C正确;
D.氯水中加硝酸银产生白色沉淀,证明溶液中有氯离子,氯水中加淀粉碘化钾溶液,溶液变蓝,证明生
成了碘单质,溶液中有强氧化性的物质,而氯气和次氯酸都有强氧化性,不能证明反应物和生成物共存,
即不能证明上述反应存在限度,D错误;答案选D。
5.【2022年6月浙江卷】 时,苯酚 的 ,下列说法正确的是
A.相同温度下,等 的 和 溶液中,B.将浓度均为 的 和 溶液加热,两种溶液的 均变大
C. 时, 溶液与 溶液混合,测得 ,则此时溶液中
D. 时, 的 溶液中加少量 固体,水的电离程度变小
【答案】C
【解析】A.醋酸的酸性大于苯酚,则醋酸根离子的水解程度较小,则相同温度下,等pH的C HONa和
6 5
CHCOONa溶液中c(C HO-)