文档内容
专题突破(二) 整合有效信息书写化学(离子)方程式
高考试题中信息型化学(或离子)方程式的书写以氧化还原反应为主,此类问题提供新流
程、新成果、新技术、新反应等信息,考查考生提取、加工和整合信息的能力,对学科能力多维
度、多层次的考查,促进考生的批判性、缜密性和系统性思维品质的形成,形成自主学习和终
身学习的意识和能力。解答此类问题的思维模板如下:
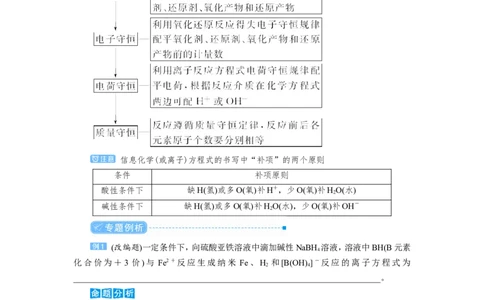
信息化学(或离子)方程式的书写中“补项”的两个原则
条件 补项原则
酸性条件下 缺H(氢)或多O(氧)补H+,少O(氧)补HO(水)
2
碱性条件下 缺H(氢)或多O(氧)补HO(水),少O(氧)补OH-
2
(改编题)一定条件下,向硫酸亚铁溶液中滴加碱性NaBH 溶液,溶液中BH(B元素
4
化合价为+3 价)与 Fe2+反应生成纳米 Fe、H 和[B(OH) ]-反应的离子方程式为
2 4
________________________________________________________________________。
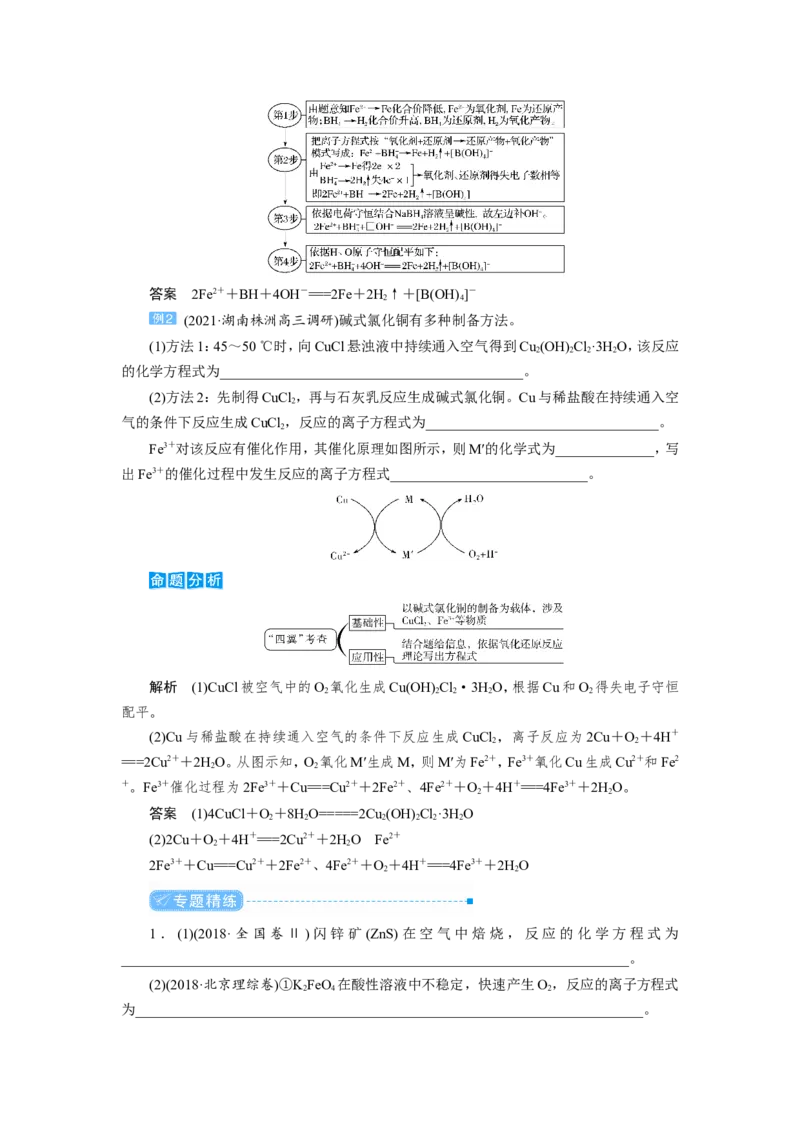
解析 结合题给信息,分四步书写离子方程式:答案 2Fe2++BH+4OH-===2Fe+2H↑+[B(OH) ]-
2 4
(2021·湖南株洲高三调研)碱式氯化铜有多种制备方法。
(1)方法1:45~50 ℃时,向CuCl悬浊液中持续通入空气得到Cu (OH) Cl·3H O,该反应
2 2 2 2
的化学方程式为___________________________________________。
(2)方法2:先制得CuCl ,再与石灰乳反应生成碱式氯化铜。Cu与稀盐酸在持续通入空
2
气的条件下反应生成CuCl ,反应的离子方程式为_________________________________。
2
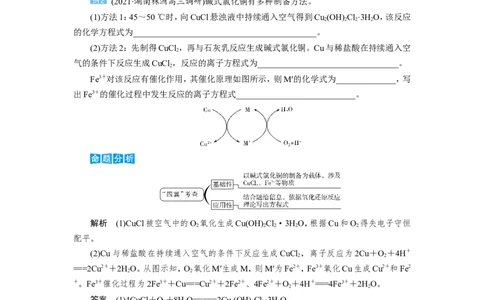
Fe3+对该反应有催化作用,其催化原理如图所示,则M′的化学式为______________,写
出Fe3+的催化过程中发生反应的离子方程式____________________________。
解析 (1)CuCl被空气中的O 氧化生成Cu(OH) Cl·3HO,根据Cu和O 得失电子守恒
2 2 2 2 2
配平。
(2)Cu与稀盐酸在持续通入空气的条件下反应生成CuCl ,离子反应为2Cu+O +4H+
2 2
===2Cu2++2HO。从图示知,O 氧化M′生成M,则M′为Fe2+,Fe3+氧化Cu生成Cu2+和Fe2
2 2
+。Fe3+催化过程为2Fe3++Cu===Cu2++2Fe2+、4Fe2++O+4H+===4Fe3++2HO。
2 2
答案 (1)4CuCl+O+8HO=====2Cu (OH) Cl·3H O
2 2 2 2 2 2
(2)2Cu+O+4H+===2Cu2++2HO Fe2+
2 2
2Fe3++Cu===Cu2++2Fe2+、4Fe2++O+4H+===4Fe3++2HO
2 2
1.(1)(2018·全国卷Ⅱ)闪锌矿(ZnS)在空气中焙烧,反应的化学方程式为
________________________________________________________________________。
(2)(2018·北京理综卷)①KFeO 在酸性溶液中不稳定,快速产生O,反应的离子方程式
2 4 2
为________________________________________________________________________。② 实 验 室 用 KMnO 与 浓 盐 酸 反 应 制 取 Cl , 反 应 的 方 程 式 是
4 2
________________________________________________________________________。
(3)(2018·天津理综卷)向浆状Mg(OH) 中通入SO ,使其转化为稳定的Mg化合物,该反
2 2
应的化学方程式为
________________________________________________________________________。
答案 (1)2ZnS+3O=====2ZnO+2SO
2 2
(2)①4FeO+20H+===4Fe3++3O↑+10HO
2 2
②2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO
4 2 2 2
(3)2Mg(OH) +2SO +O===2MgSO +2HO
2 2 2 4 2
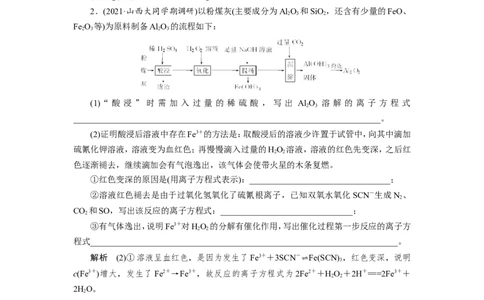
2.(2021·山西大同学期调研)以粉煤灰(主要成分为Al O 和SiO ,还含有少量的FeO、
2 3 2
Fe O 等)为原料制备Al O 的流程如下:
2 3 2 3
(1)“ 酸 浸 ” 时 需 加 入 过 量 的 稀 硫 酸 , 写 出 Al O 溶 解 的 离 子 方 程 式
2 3
________________________________________________________________________。
(2)证明酸浸后溶液中存在Fe3+的方法是:取酸浸后的溶液少许置于试管中,向其中滴加
硫氰化钾溶液,溶液变为血红色;再慢慢滴入过量的HO 溶液,溶液的红色先变深,之后红
2 2
色逐渐褪去,继续滴加会有气泡逸出,该气体会使带火星的木条复燃。
①红色变深的原因是(用离子方程式表示):_________________________________;
②溶液红色褪去是由于过氧化氢氧化了硫氰根离子,已知双氧水氧化SCN-生成N 、
2
CO 和SO,写出该反应的离子方程式:_______________________________;
2
③有气体逸出,说明Fe3+对HO 的分解有催化作用,写出催化过程第一步反应的离子方
2 2
程式________________________________________________________________________。
解析 (2)①溶液呈血红色,是因为发生了Fe3++3SCN- ⇌Fe(SCN)
3
,红色变深,说明
c(Fe3+)增大,发生了Fe2+→Fe3+,故反应的离子方程式为2Fe2++HO +2H+===2Fe3++
2 2
2HO。
2
③催化作用中Fe3+一定要参与反应,故Fe3+在第一步反应中应作氧化剂,发生2Fe3++
HO===2Fe2++O↑+2H+;第二步重新生成Fe3+,发生2Fe2++2H++HO===2Fe3++
2 2 2 2 2
2HO。
2
答案 (1)AlO+6H+===2Al3++3HO
2 3 2
(2)①2Fe2++H
2
O
2
+2H+===2Fe3++2H
2
O、Fe3++3SCN- ⇌Fe(SCN)
3
②2SCN-+11HO===2CO ↑+N↑+2H++10HO+2SO
2 2 2 2 2
③2Fe3++HO===2Fe2++O↑+2H+
2 2 2
章末综合检测(二) 化学物质及其变化一、选择题:本题包括10个小题,每个小题只有一个选项符合题意。
1.(2021·黑龙江哈尔滨三中检测)下列有关物质分类或归类中,正确的是( )
A.混合物:石灰石、盐酸、聚乙烯
B.化合物:CaCl 、胆矾、HD
2
C.电解质:硫酸、冰醋酸、酒精
D.同位素:1HO、2HO、3HO
A [HD是单质,B错误。酒精是非电解质,C错误。同位素是同种元素的不同质量之间
的互称,D错误。]
2.(2021·河南信阳调研)下列各组物质按照纯净物、混合物、强电解质、弱电解质和非电
解质顺序排列的是( )
A.氯水 水煤气 硫酸 醋酸 干冰
B.冰醋酸 福尔马林 硫酸钡 次氯酸 乙醇
C.单甘油酯 混甘油酯 水玻璃 氢硫酸 三氧化硫
D.胆矾 漂白粉 氯化钾 氢氟酸 氯气
B [氯水是氯气的水溶液,属于混合物,A项错误;油脂、水玻璃都是混合物,C项错误;
氯气是单质,既不是电解质也不是非电解质,D项错误。]
3.(2021·重庆巴蜀中学月考)下列离子能大量共存的是( )
A.某弱碱溶液中:AlO、HCO、Na+、Cl-
B.与Al反应放出H 的溶液中:Fe2+、K+、NO、SO
2
C.c(Fe3+)=1 mol/L的溶液中:Na+、NH、SCN-、SO
D.无色透明溶液中:K+、Cu2+、Cl-、NO
D [溶液中AlO、HCO发生反应:AlO+HCO+HO===Al(OH) ↓+CO,不能大量共存,
2 3
A项错误;与Al反应放出H 的溶液可能呈强酸性或强碱性,若为强碱性,Fe2+与OH-不能大
2
量共存,若为强酸性,Fe2+、NO、H+发生氧化还原反应而不能大量共存,B项错误;Fe3+与
SCN-反应生成Fe(SCN) 而不能大量共存,C项错误。]
3
4.(2021·湖南株洲高三调研)已知反应P +3NaOH+3HO===3NaHPO
4 2 2 2
+PH ↑,产物PH 中P的化合价为-3价。下列说法正确的是( )
3 3
A.1 mol P 分子中含有P—P的物质的量为4 mol
4
B.31 g P 中所含的电子数为5×6.02×1023
4
C.反应中还原剂和氧化剂的物质的量之比为1∶3
D.反应生成2.24 L(标准状况)PH ,转移的电子数为0.3×6.02×1023
3
D [1个P 分子含6个P—P键,则1 mol P 分子含有6 mol P—P键,A项错误;1个P
4 4 4
分子含有 60 个电子,31 g P 为 0.25 mol,则含有电子数为 0.25×60×6.02×1023=
4
15×6.02×1023,B项错误;作还原剂的P 被氧化为NaH PO ,作氧化剂的P 被还原为PH ,二
4 2 2 4 3
者的物质的量之比为3∶1,C项错误;反应生成标准状况下2.24 L PH 为0.1 mol,转移电子
3
数为0.1×3×6.02×1023个,D项正确。]5.(2021·四川成都七中检测)能正确表示下列反应的离子方程式是( )
A.向次氯酸钠溶液中通入足量 SO 气体:ClO-+SO +HO===HClO+HSO
2 2 2
B.0.1 mol/L NH Al(SO ) 溶液与 0.2 mol/L Ba(OH) 溶液等体积混合:Al3++2SO+
4 4 2 2
2Ba2++4OH-===2BaSO +AlO+2HO
4 2
C.用浓盐酸酸化的KMnO 溶液与HO 反应,证明HO 具有还原性:2MnO+6H++
4 2 2 2 2
5HO===2Mn2++5O↑+8HO
2 2 2 2
D.Fe O 溶于过量氢碘酸溶液中:Fe O+6H++2I-===2Fe2++I+3HO
2 3 2 3 2 2
D [NaClO溶液中通入足量 SO 气体,发生氧化还原反应,生成NaCl和HSO ,A项错
2 2 4
误;两溶液等体积混合,二者的物质的量比为1∶1,反应生成Al(OH) 、NH ·HO和BaSO,
3 3 2 4
B项错误;KMnO 溶液具有强氧化性,可将Cl-氧化生成Cl,而MnO被还原为Mn2+,溶液褪
4 2
色,故不能用浓盐酸酸化高锰酸钾溶液,C项错误;HI是强酸,且具有较强还原性,Fe O 溶液
2 3
与过量HI溶液反应,生成FeI、I 和HO,D项正确。]
2 2 2
6.(2021·河南洛阳一中检测)某研究小组对离子方程式xR2++yH++O===mR3++nHO
2 2
的分析研究,下列说法中错误的是( )
A.根据电荷守恒,得出x与y的和一定等于m
B.根据原子守恒,得出x和m的数值一定相等
C.根据电子得失守恒,得出x=4的结论
D.根据氧化还原反应关系得出:R2+是还原剂,O 是氧化剂,R3+是氧化产物,HO是还
2 2
原产物
A [据电荷守恒可得:2x+y=3m,A项错误。据R原子守恒可知,x=m,B项正确。R由
+2价变为+3价,O由0价变为-2价,据得失电子守恒推知,x=4,C项正确。R元素化合价
升高,则R2+是还原剂,R3+是氧化产物;O元素化合价降低,则O 是氧化剂,HO是还原产物,
2 2
D项正确。]
7.(2021·河南省部分重点校联考)下列解释实验操作中的现象所写的离子方程式错误的
是( )
实验操作及现象 离子方程式
过量SO 通入滴有酚酞的NaOH
2
A SO +OH-===HSO
2
溶液中,溶液变为无色
FeCl 与KSCN的混合溶液中通 2Fe2++Cl===2Fe3++2Cl-、
2 2
B
入少量Cl,溶液变红色 Fe3++3SCN- Fe(SCN)
2 3
往红色Cu O中滴入稀硫酸,溶液
2
C Cu O+2H+===Cu2++Cu+HO
2 2
变蓝,有紫红色不溶物产生
SO 通入Ba(NO ) 溶液中,产生白
2 3 2
D Ba2++SO +HO===BaSO ↓+2H+
2 2 3
色沉淀
D [SO 通入Ba(NO ) 溶液中,发生氧化还原反应,产生的白色沉淀是BaSO,正确应为
2 3 2 4
3Ba2++3SO +2NO+2HO===3BaSO ↓+2NO↑+4H+,D项错误。]
2 2 4
8.(2021·黑龙江哈师大附中检测)将几滴KSCN(SCN-是“类卤离子”)溶液加入含有Fe3+的酸性溶液中,溶液变成红色。将该红色溶液分为两份:①一份中加入适量KMnO 溶液,
4
红色褪去;②另一份中通入SO 红色也褪去。下列推测肯定不正确的是( )
2
A.SCN-在适当条件下可失去电子被氧化为(SCN)
2
B.①中红色褪去的原因是KMnO 将SCN-氧化
4
C.②中红色褪去的原因是SO 将Fe3+还原为Fe2+
2
D.②中红色褪去的原因是SO 将SCN-还原
2
D [SCN-是“类卤离子”,其性质与卤素离子相似,加入KMnO 溶液后,可能被氧化生
4
成(SCN) ,溶液的红色褪去,A、B项正确;SO 具有还原性,可能将Fe3+还原为Fe2+而使溶液
2 2
红色褪去,C项正确;SO 和SCN-都具有还原性,二者不发生反应,D项错误。]
2
9.(2021·湖北武汉联考)在ZrO催化作用下CO与NO的循环反应路径如图所示,下列
2 2
叙述错误的是( )
A.ZrO是反应中间产物
2
B.反应过程中Zr的成键数目未改变
C.ZrO转化为ZrO的氧化剂是NO
2 2 2
D.催化循环的总反应为CO+NO=====N+CO
2 2 2
B [由图可知,ZrO转化为ZrO,又重新生成ZrO,故ZrO是反应中间产物,A项正确;
2 2 2 2
ZrO中Zr形成4个共价键,ZrO中的1个Zr原子形成4个共价键,另一个Zr原子形成3个
2 2
共价键,B项错误;由图可知,ZrO与NO反应生成N 和ZrO,氧化剂是NO,C项正确;整
2 2 2 2 2
个催化循环过程中,ZrO是催化剂,CO和NO反应生成N 和CO,D项正确。]
2 2 2 2
10.(2021·河南洛阳一中检测)某同学设计完成了以下两个实验:
①向盛有KI溶液的试管中加入少许CCl 后滴加氯水,CCl 层变成紫色。继续向试管中
4 4
滴加氯水,振荡,CCl 层会逐渐变浅,最后变成无色(生成了HIO )。
4 3
②向盛有KBr溶液的试管中加入少许CCl 后滴加氯水,CCl 层变成红棕色。继续向试管
4 4
中滴加氯水,振荡,CCl 层的颜色没有变化。
4
下列说法不正确的是( )
A.实验①生成HIO 时发生的反应为:I+5Cl+6HO===2HIO+10HCl
3 2 2 2 3
B.实验②中当CCl 层变成红棕色时可通过分液的方法获得Br 的CCl 溶液
4 2 4
C.由上述实验得出Cl、Br 、I 的氧化性由强到弱的顺序是:Cl>Br >I
2 2 2 2 2 2
D.由上述实验得出Cl、HIO 、HBrO 氧化性由强到弱的顺序是:HBrO >Cl>HIO
2 3 3 3 2 3
C [实验①中I-被Cl 氧化生成I,继续滴加氯水后,I 被过量氯水氧化生成HIO ,溶液
2 2 2 3褪色,A项正确;②中CCl 层变成红棕色,是生成的Br 溶于CCl 形成,通过分液可获得Br
4 2 4 2
的CCl 溶液,B项正确;由①可得Cl 的氧化性强于Br ,由②可得Cl 的氧化性强于I,但不
4 2 2 2 2
能判断Br 、I 的氧化性,C项错误;过量氯水可将I 氧化生成HIO ,则氧化性:Cl>HIO ;实
2 2 2 3 2 3
验②中红棕色溶液加入过量氯水,CCl 层的颜色没有变化,说明Cl 不能将Br 氧化生成
4 2 2
HBrO ,则氧化性:HBrO >Cl,D项正确。]
3 3 2
二、非选择题:本题包括2小题。
11.(2021·河南郑州一中检测)氟及其化合物在生产生活中被广泛应用,造福人类。
(1)氟在元素周期表中的位置是____________________________________。
(2)氢氟酸具有刻蚀玻璃的特性,写出该反应的化学方程式______________________。
(3)四氟肼(N F)用作高能燃料的氧化剂,1 mol NF 分子中含有的共价键数目是
2 4 2 4
________N 。NF 气体可用 Fe3+氧化二氟胺(HNF )制得,写出该反应的离子方程式
A 2 4 2
________________________________________________________________________。
(4)六氟化铀(UF )是铀的稳定气态化合物,用作核燃料,由UO 制取UF 的三步反应原
6 3 8 6
理如下:① UO +H―→UO +HO(未配平) ② UO +4HF===UF +2HO ③ UF +
3 8 2 2 2 2 4 2 4
F===UF 则下列说法正确的是________。
2 6
A.反应①②③都是氧化还原反应
B.反应③中U元素被氧化
C.反应①中氧化剂和还原剂的物质的量之比为2∶1
解析 (3)N F 气体被Fe3+氧化生成HNF ,Fe3+则被还原为Fe2+,结合守恒规律写出离
2 4 2
子方程式:2HNF +2Fe3+===N F↑+2Fe2++2H+。
2 2 4
(4)反应②中各元素化合价均未变化,不是氧化还原反应,A项错误;反应③中U元素由
+4价升高到+6价,则U元素被氧化,B项正确;反应①配平可得:UO+2H===3UO+
3 8 2 2
2HO,
2
UO 是氧化剂,H 是还原剂,二者的物质的量之比为1∶2,C项正确。
3 8 2
答案 (1)第二周期第ⅦA族
(2)SiO+4HF===SiF ↑+2HO
2 4 2
(3)5 2HNF +2Fe3+===N F↑+2Fe2++2H+
2 2 4
(4)B
12.以辉铜矿(主要成分为Cu S,含少量SiO)为原料制备硝酸铜的流程如图所示:
2 2
(1)写出“浸取”过程中Cu S溶解时发生反应的离子方程式______________________。
2
(2)恒温“浸取”的过程中发现铜元素的浸取速率先增大后减少,有研究指出CuCl 是该
2
反应的催化剂,该过程的反应原理可用化学方程式表示为:
①Cu S+2CuCl ===4CuCl+S;
2 2② ________________________________________________________________________
。
(3)向滤液M中加入(或通入)________(填字母),可得到一种可循环利用的物质。
a.铁 b.氯气 c.高锰酸钾 d.氯化氢
(4)辉铜矿可由黄铜矿(主要成分为CuFeS)通过电化学反应转变而成,有关转化见图,转
2
化时转移0.2 mol电子,生成Cu S________ mol。
2
解析 (1)辉铜矿主要成分为Cu S,“浸取”时加入FeCl 溶液,Cu S被氧化生成Cu2+、
2 3 2
S,Fe3+被还原生成Fe2+,结合守恒规律写出离子方程式:Cu S+4Fe3+===2Cu2++4Fe2++S。
2
(2)根据催化剂的作用机理,①中CuCl 参与反应生成CuCl,②中CuCl被氧化生成
2
CuCl ,反应机理为CuCl+FeCl ===CuCl +FeCl 。
2 3 2 2
(3)“置换”过程中加入Fe,所得滤液M中含有Fe2+,通入Cl 可将Fe2+氧化生成Fe3+,
2
得到FeCl 溶液,可用于“浸取”步骤,重复使用。
3
(4)该反应中,Cu被氧化为Cu S,Cu元素由0价升高到+1价,CuFeS 被还原为Cu S,
2 2 2
Cu元素由+2价降低到+1价。据得失电子守恒可知,转移0.2 mol电子时,Cu被氧化得到
0.1 mol Cu S,CuFeS 被还原得到0.1 mol Cu S,故共生成0.2 mol Cu S。
2 2 2 2
答案 (1)Cu S+4Fe3+===2Cu2++4Fe2++S
2
(2)CuCl+FeCl ===CuCl +FeCl
3 2 2
(3)b (4)0.2