文档内容
专题突破卷 03 金属及其化合物
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.“神八”与“天宫一号”的成功对接,标志着中国的航空铝材处于世界领先的行列。下列关于铝合金
的说法中错误的是
A.铝合金是一种混合物,它比纯铝的硬度大
B.高温铝液易被氧化,铝合金应在熔剂层覆盖下熔炼
C.镁铝合金耐腐蚀,但能被烧碱(NaOH)腐蚀
D.镁铝合金在盐酸中无法溶解
2.下列关于Fe、Cu、Mg、Al四种金属元素的说法中不正确的是
A.四种元素的单质只有三种能和盐酸反应,生成相应的盐和氢气
B.制备AlCl 、FeCl 、CuCl 均不能采用将溶液直接蒸干的方法
3 3 2
C.将Mg棒和Al棒作为原电池的两个电极插入NaOH溶液中,Mg棒上发生氧化反应
D.铁锈的主要成分是氧化铁,铜锈的主要成分是碱式碳酸铜
3.下列反应的离子方程式正确的是
A.铁钉放入硫酸铜溶液中:
B.硫酸铜溶液与Ca(OH) 溶液混合:
2
C.钠与水反应:
D.氧化铁与稀盐酸混合:
4.金属及其化合物的转化关系是化学学习的重要内容之一。下列各组物质的转化不能全部通过一步反应
直接完成的是
A.Al→Al O→Al(OH) →AlCl B.Na→NaOH→Na CO→NaCl
2 3 3 3 2 3
C.Mg→MgCl →Mg(OH) →MgSO D.Fe→FeCl →Fe(OH) →Fe(OH)
2 2 4 2 2 3
5.将一小块钠投入如图所示的烧杯中,下列有关说法正确的是
资料收集整理【淘宝店铺:向阳百分百】A.钠块只在煤油中游动,并放出气体
B.钠块只在水层游动,钠块熔化,水层变红色
C.在CCl 和水层交界处上下跳动,钠块熔化,水层变红
4
D.在水层和煤油层交界处上下跳动,钠块熔化,水层变红
6.金属材料在日常生活以及生产中有着广泛的应用。下列关于金属的一些说法不正确的是
A.合金的性质与其组成金属的性质不完全相同
B.灼烧孔雀石[Cu (OH) CO]和焦炭混合物制铜也属于还原法
2 2 3
C.金属冶炼的本质是金属阳离子得到电子变成金属原子
D.工业上金属Mg、Cu都是用热还原法制得的
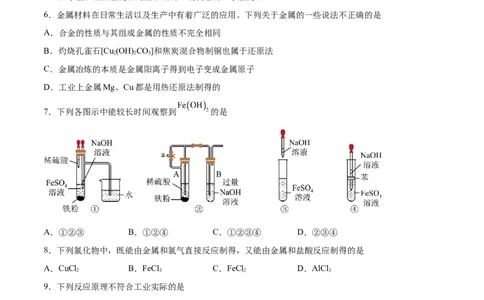
7.下列各图示中能较长时间观察到 的是
A.①②③ B.①②④ C.①②③④ D.②③④
8.下列氯化物中,既能由金属和氯气直接反应制得,又能由金属和盐酸反应制得的是
A.CuCl B.FeCl C.FeCl D.AlCl
2 3 2 3
9.下列反应原理不符合工业实际的是
A.2Ag O 4Ag+O↑ B.4Al+3MnO 3Mn+2Al O
2 2 2 2 3
C.2MgO 2Mg+O↑ D.2CuO+C 2Cu+CO ↑
2 2
10.关于物质的相关用途,下列说法错误的是
A. 可用于潜水艇中作供氧剂 B. 可用于制作红色油漆或涂料
资料收集整理【淘宝店铺:向阳百分百】C.小苏打可用于治疗胃溃疡 D.氧化铝可用于耐火材料
11.探究铁及其化合物的性质,下列方案设计、现象和结论都正确的是
实验方案 现象 结论
A 往 溶液中加入 片 短时间内无明显现象 的氧化能力比 弱
往 溶液中滴加 溶液,再加 溶液先变成血红色后
B 与 的反应不可逆
无明显变化
入少量 固体
将食品脱氧剂样品中的还原铁粉溶于盐
C 溶液呈浅绿色 食品脱氧剂样品中没有 价铁
酸,滴加 溶液
向沸水中逐滴加5~6滴饱和 溶液,持 溶液先变成红褐色再 先水解得 再聚集成
D
续煮沸 析出沉淀 沉淀
A.A B.B C.C D.D
12.以下关于铜跟浓、稀HNO 反应的说法中错误的是
3
A.1mol浓HNO 被还原转移2mol电子
3
B.Cu与浓HNO 反应剧烈,故氧化性浓HNO 强于稀HNO
3 3 3
C.Cu与浓、稀HNO 反应都不需加热
3
D.生成等量的Cu(NO ),消耗浓HNO 的量多
3 2 3
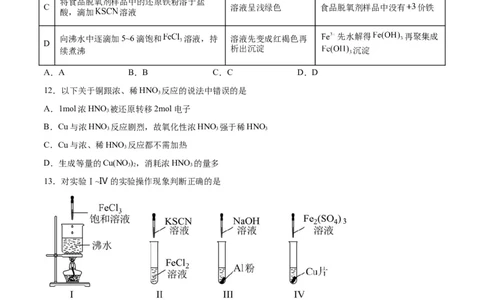
13.对实验Ⅰ~Ⅳ的实验操作现象判断正确的是
A.实验Ⅰ:制得 胶体,产生红褐色沉淀
B.实验Ⅱ:溶液颜色变红
C.实验Ⅲ:放出大量气体
D.实验Ⅳ:铜片表面有黑色固体生成
14.下列说法正确的是
A.铝、铁、铜相比较,铜元素在自然界中的含量最低、铁元素含量最高
资料收集整理【淘宝店铺:向阳百分百】B.A1 O、MgO可用作高温材料,二氧化硅是生产光纤制品的基本原料
2 3
C.工业上采用电解熔融态A1 O、MgO的方法冶炼Al、Mg
2 3
D.用纯碱制玻璃、用铁矿石炼铁、用氨制碳酸铵都会产生温室气体
15.工业上用铝土矿(主要成分为Al O,含Fe O 杂质)为原料冶炼铝的工艺流程如下:
2 3 2 3
下列叙述正确的是
A.按上述流程,试剂X可以是氢氧化钠溶液,也可以是盐酸
B.反应①过滤后所得沉淀为氧化铁
C.图中所有的转化反应都不是氧化还原反应
D.反应②的离子方程式为2AlO-+CO+3HO=2Al(OH) ↓+CO2-
2 2 2 3 3
二、填空题(本题包括4小题,共55分)
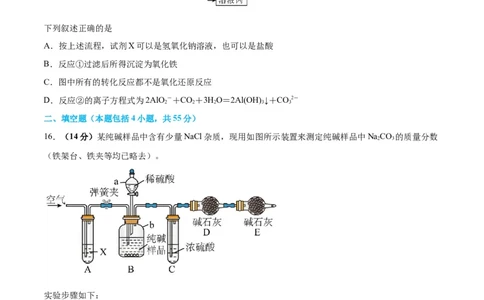
16.(14分)某纯碱样品中含有少量NaCl杂质,现用如图所示装置来测定纯碱样品中NaCO 的质量分数
2 3
(铁架台、铁夹等均已略去)。
实验步骤如下:
①按如图所示连接装置,并检查气密性;
②准确称得盛有碱石灰的干燥管D的质量为80.20;
③准确称得20.00g纯碱样品放入容器b中;
④打开分液漏斗a的旋塞,缓缓滴入稀硫酸至不再产生气泡;
⑤打开弹簧夹,往试管A中缓缓鼓入一定量空气;
⑥熟后称得干燥管D的总质量为86.36g;
⑦重复步骤⑤和⑥的操作,直到干燥管D的质量不变,且其质量为86.80g。
资料收集整理【淘宝店铺:向阳百分百】试回答:
(1)装置B中发生反应的化学方程式为 。
(2)装置A中试剂X应选用足量的 (填标号)。
A.饱和NaCl溶液 B.浓HSO
2 4
D.NaOH溶液 C.NaHCO 溶液
3
(3)①装置C的作用: 。②装置E的作用: 。
(4)如果将分液漏斗中的稀硫酸换成浓度相同的盐酸,则会导致测定结果 (填“偏大”“偏小”或
“不变”,下同);若没有操作⑤⑦,则会导致测定结果 。
(5)该纯碱样品中NaCO 的质量分数为 。
2 3
17.(14分)铝、铁、铜及其化合物在日常生活中应用广泛,根据下列事实回答问题。
(1)铝土矿的主要成分是氧化铝,写出铝土矿与稀硫酸反应的离子方程式: 。
(2)铁矿石主要分为赤铁矿和磁铁矿。写出赤铁矿主要成分的化学式: 。磁铁矿与铝粉在一定条件
下发生铝热反应,写出反应的化学方程式: 。
(3)现有一定浓度的FeCl 溶液,检验溶液是否变质的方法是取少量溶液,向其中加入几滴KSCN溶液,如
2
果溶液 ,证明溶液变质。
(4)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为 。
(5)向新制的FeCl 溶液中滴加氢氧化钠溶液,可以观察到的现象为 。
2
(6)Cu不活泼,通常情况下不与稀硫酸反应,但向Cu和稀硫酸的混合物中通入O 后,溶液很快变蓝色,试
2
写出该反应的离子方程式: 。
18.(18分)铁在人体中以Fe2+和Fe3+的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含
二价铁离子的铁盐,如硫酸亚铁(FeSO )。
4
(1)人体中经常进行转化 Fe2+ Fe3+,A反应中Fe2+作 剂,B反应中Fe3+作 剂。
(2)新配制的FeCl 溶液应加入 以防止FeCl 转化为FeCl ,要除去FeCl 溶液中少量的FeCl 杂质,可
2 2 3 3 2
向其中通入适量的 。
(3)在制作印刷电路板的过程中常利用铜与氯化铁溶液的反应。反应的离子方程式为 。
(4)为消除废气中的Cl 对环境的污染,将废气通过含有铁粉的FeCl 溶液,即可有效地除去Cl,这一处理
2 2 2
过程可用两个离子方程式表示为2Fe2++Cl=2Fe3++2Cl- 和 ;处理过程中需定期添加的原料是
2
。
(5)某同学为检验某未知溶液中是否为FeCl 溶液,采取如下实验方案加以验证: 取少许未知试液于试管中
2
资料收集整理【淘宝店铺:向阳百分百】溶液呈红色(证明含有FeCl ),你认为此方案 (填“合理”或“不合理”),若不合
2
理,如何改进: 。
19.(10分)工业上通常以铝土矿(主要成分为Al O,含有少量Fe O、SiO 等杂质)为原料制备无水氯化
2 3 2 3 2
铝:2Al O+6Cl===4AlCl +3O。
2 3 2 3 2
回答以下问题:
(1)为促进反应的进行,实际生产中需加入焦炭,其原因是 。
(2)加入焦炭后的化学反应可表示为Al O+C+Cl AlCl +X↑,则气体X可能是
2 3 2 3
。
(3)在提纯AlCl 粗产品时,需加入少量铝粉,可使熔点较低的FeCl 转化为熔点较高的FeCl ,从而避免在
3 3 2
AlCl 中混入铁的氯化物。该反应的化学方程式为 。
3
(4)以铝土矿为原料可以通过以下途径提纯氧化铝:
①写出滤液甲中溶质的化学式: 。
②写出滤液乙中加入过量氨水得到Al(OH) 的离子方程式: 。
3
资料收集整理【淘宝店铺:向阳百分百】