文档内容
专题讲座(四)反应速率、平衡图像题解题策略
1.反应 经历两步:① ;② 。反应体系中 、 、 的浓度c随时间t的变化曲
线如图所示。下列说法不正确的是( )
A.a为 随t的变化曲线
B. 时,
C. 时, 的消耗速率大于生成速率
D. 后,
【答案】D
【解析】由题中信息可知,反应 经历两步:① ;② 。因此,图中呈不断减小趋势
的a线为X的浓度 随时间 的变化曲线,呈不断增加趋势的线为Z的浓度 随时间 的变化曲线,先增加
后减小的线为Y的浓度 随时间 的变化曲线。X是唯一的反应物,随着反应的发生,其浓度不断减小,
因此,由图可知, 为 随 的变化曲线,A正确;由图可知,分别代表3种不同物质的曲线相交于
时刻,因此, 时 ,B正确;由图中信息可知, 时刻以后,Y的浓度仍在不断减
小,说明 时刻反应两步仍在向正反应方向发生,而且反应①生成Y的速率小于反应②消耗Y的速率,即
时 的消耗速率大于生成速率,C正确;由图可知, 时刻反应①完成,X完全转化为Y,若无反应②
发生,则 ,由于反应② 的发生, 时刻Y浓度的变化量为 ,变化量之比等于化学计量数之比,所以Z的浓度的变化量为 ,这种关系在 后仍成立, 因此,D不正确。综
上所述,本题选D。
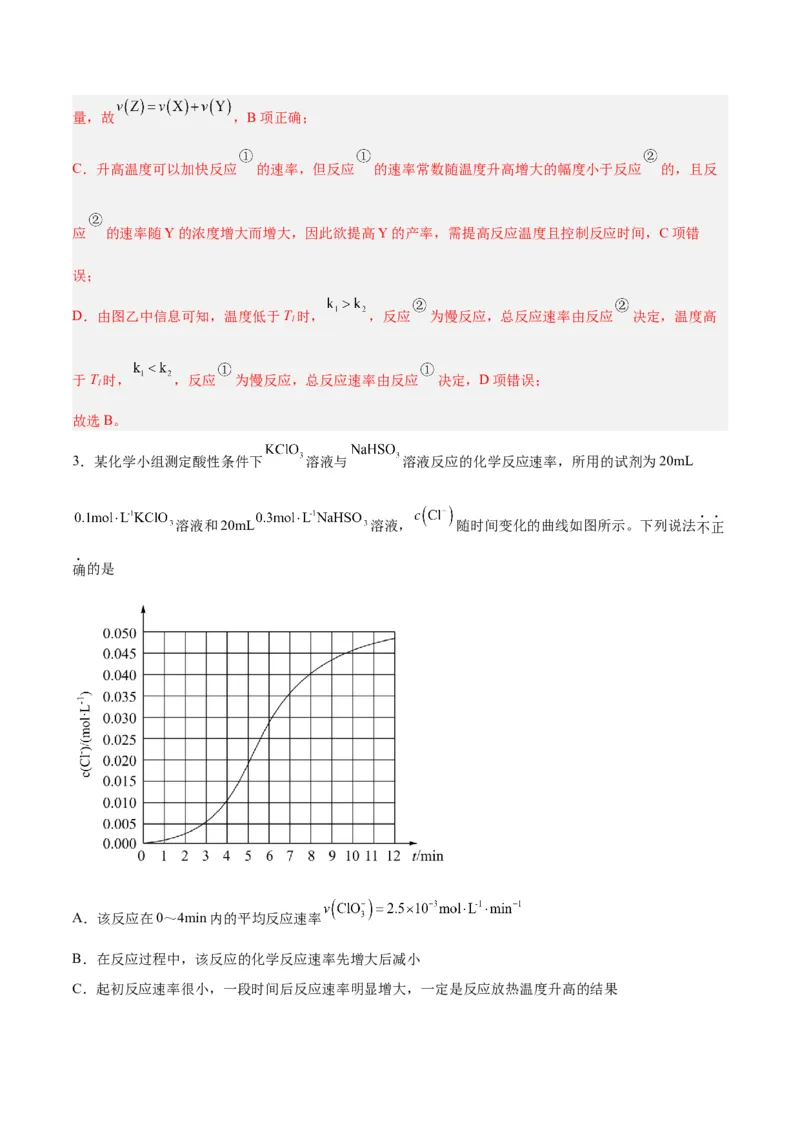
2.恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为 ; 。反应
的速率 ,反应 的速率 ,式中 、 为速率常数。图甲为该体系中 、 、 浓
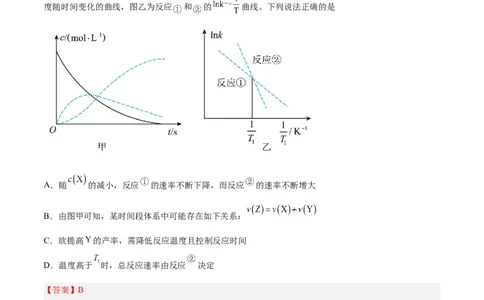
度随时间变化的曲线,图乙为反应 和 的 曲线。下列说法正确的是
A.随 的减小,反应 的速率不断下降,而反应 的速率不断增大
B.由图甲可知,某时间段体系中可能存在如下关系:
C.欲提高 的产率,需降低反应温度且控制反应时间
D.温度高于 时,总反应速率由反应 决定
【答案】B
【解析】A.由图甲中信息可知,随 的减小, 先增大后减小, 增大,故反应 的速率随
的减小而减小,反应 的速率先增大后减小,A项错误;
B.由图甲可知,依据反应关系,在Y的浓度达到最大值之前,单位时间内X的减少量等于Y和Z的增加
量,因此 ,在Y的浓度达到最大值之后,单位时间内Z的增加量等于Y和X的减少量,故 ,B项正确;
C.升高温度可以加快反应 的速率,但反应 的速率常数随温度升高增大的幅度小于反应 的,且反
应 的速率随Y的浓度增大而增大,因此欲提高Y的产率,需提高反应温度且控制反应时间,C项错
误;
D.由图乙中信息可知,温度低于T 时, ,反应 为慢反应,总反应速率由反应 决定,温度高
1
于T 时, ,反应 为慢反应,总反应速率由反应 决定,D项错误;
1
故选B。
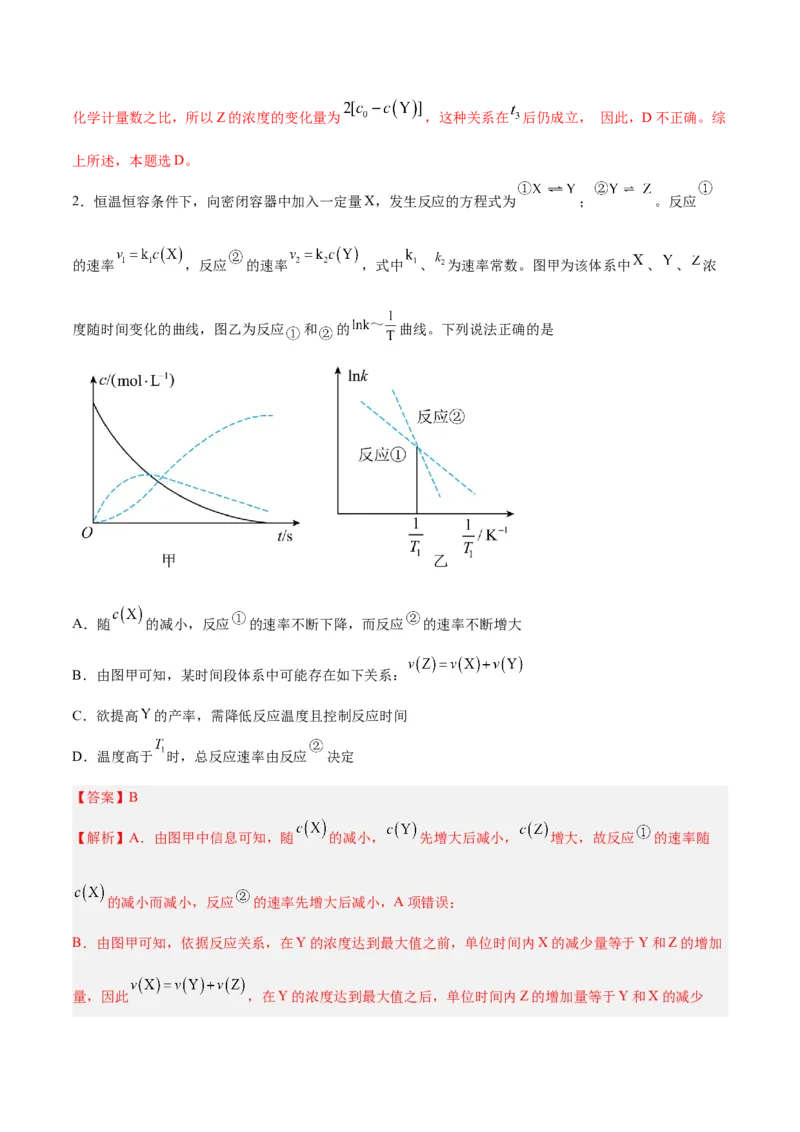
3.某化学小组测定酸性条件下 溶液与 溶液反应的化学反应速率,所用的试剂为20mL
溶液和20mL 溶液, 随时间变化的曲线如图所示。下列说法不正
确的是
A.该反应在0~4min内的平均反应速率
B.在反应过程中,该反应的化学反应速率先增大后减小
C.起初反应速率很小,一段时间后反应速率明显增大,一定是反应放热温度升高的结果D.该反应的离子方程式为
【答案】C
【解析】A.由题图中数据可知,该反应在0~4min内的平均反应速率
, ,A正确;
B.由题图可知,该反应的化学反应速率先增大后减小,B正确;
C.起初反应速率很小,一段时间后反应速率明显增大,可能是因为反应放热使体系温度升高,也可能是
因为生成的离子对反应有催化作用等,C错误;
D.根据得失电子守恒、原子守恒和电荷守恒,可得该反应的离子方程式为
,D正确;故答案为:C。
4.一定量的 和足量碳在刚性密闭容器中发生反应 , 随时间变化如
图。下列说法错误的是
A.
B.b点的正反应速率大于逆反应速率
C.c点正反应速率一定大于a点正反应速率
D.c点时向容器中再充入少量 ,反应速率增大
【答案】C
【解析】A.“先拐先平”,根据图像可知 ,故A正确;
B.b点后CO 的浓度继续减小,可知反应正向进行,正反应速率大于逆反应速率,故B正确;
2
C.c点温度高,a点反应物浓度大,所以c点正反应速率不一定大于a点正反应速率,故C错误;D.c点时向容器中再充入少量 ,反应物浓度增大,反应速率增大,故D正确;选C。
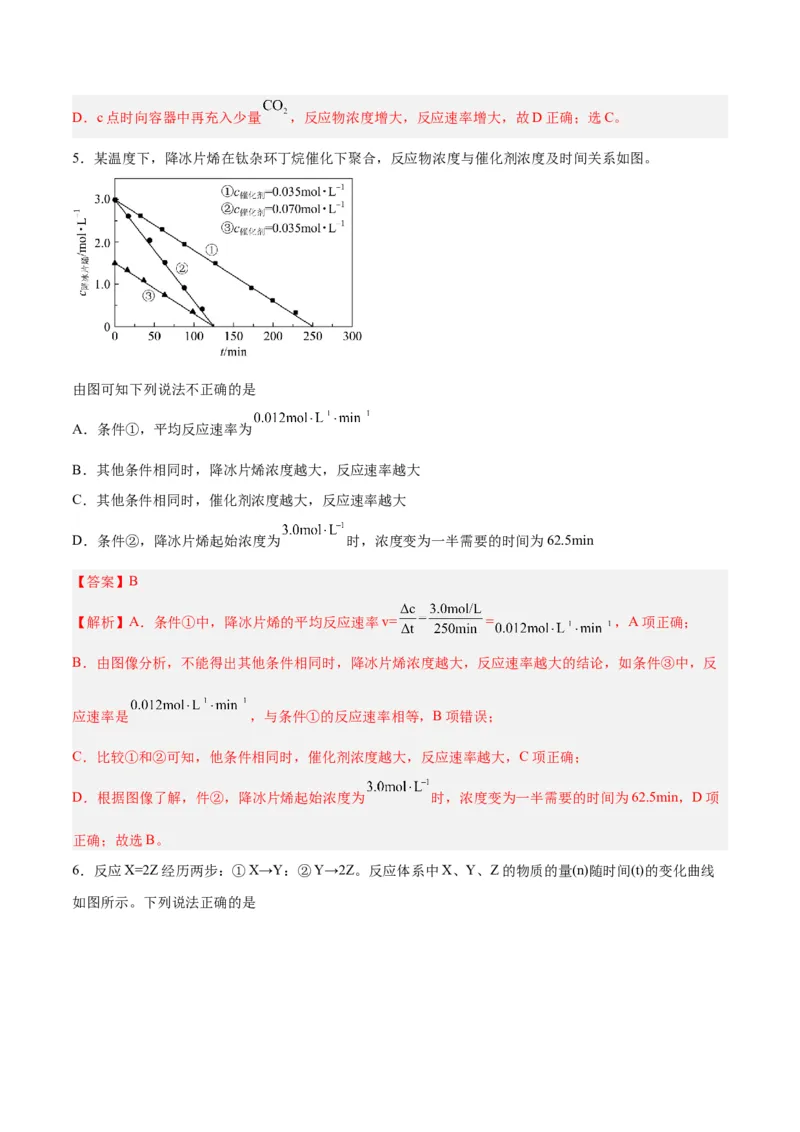
5.某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度与催化剂浓度及时间关系如图。
由图可知下列说法不正确的是
A.条件①,平均反应速率为
B.其他条件相同时,降冰片烯浓度越大,反应速率越大
C.其他条件相同时,催化剂浓度越大,反应速率越大
D.条件②,降冰片烯起始浓度为 时,浓度变为一半需要的时间为62.5min
【答案】B
【解析】A.条件①中,降冰片烯的平均反应速率v= = ,A项正确;
B.由图像分析,不能得出其他条件相同时,降冰片烯浓度越大,反应速率越大的结论,如条件③中,反
应速率是 ,与条件①的反应速率相等,B项错误;
C.比较①和②可知,他条件相同时,催化剂浓度越大,反应速率越大,C项正确;
D.根据图像了解,件②,降冰片烯起始浓度为 时,浓度变为一半需要的时间为62.5min,D项
正确;故选B。
6.反应X=2Z经历两步:①X→Y:②Y→2Z。反应体系中X、Y、Z的物质的量(n)随时间(t)的变化曲线
如图所示。下列说法正确的是A.曲线c为n(Z)随t的变化曲线
B.0~t 时间段内,反应速率v(X)=v(Y)=v(Z)
1
C.t 时,Y的消耗速率大于生成速率
2
D.t 时,n(Z)=2n -n(Y)
3 0
【答案】C
【分析】反应X=2Z经历两步:①X→Y:②Y→2Z,则X的物质的量随时间逐渐减小,Z的物质的量随时
间逐渐增大,Y的物质的量随时间先增大后减小,X、Y、Z分别对应曲线a、c、b。
【解析】A.根据分析可知,曲线c为n(Y)随t的变化曲线,A错误;
B.观察图可知,0-t 时间段内,X的消耗量大于Y和Z的生成量,则v(X)>v(Y)=v(Z),B错误;
1
C.t 时刻,Y的物质的量呈现下降的趋势,说明其消耗速率大于生成速率,C正确;
2
D.根据反应, , ,由图可知,
t 时n(X)=0,则n= ,则n(Z)=2n -2n(Y),D错误;故选C。
3 0 0
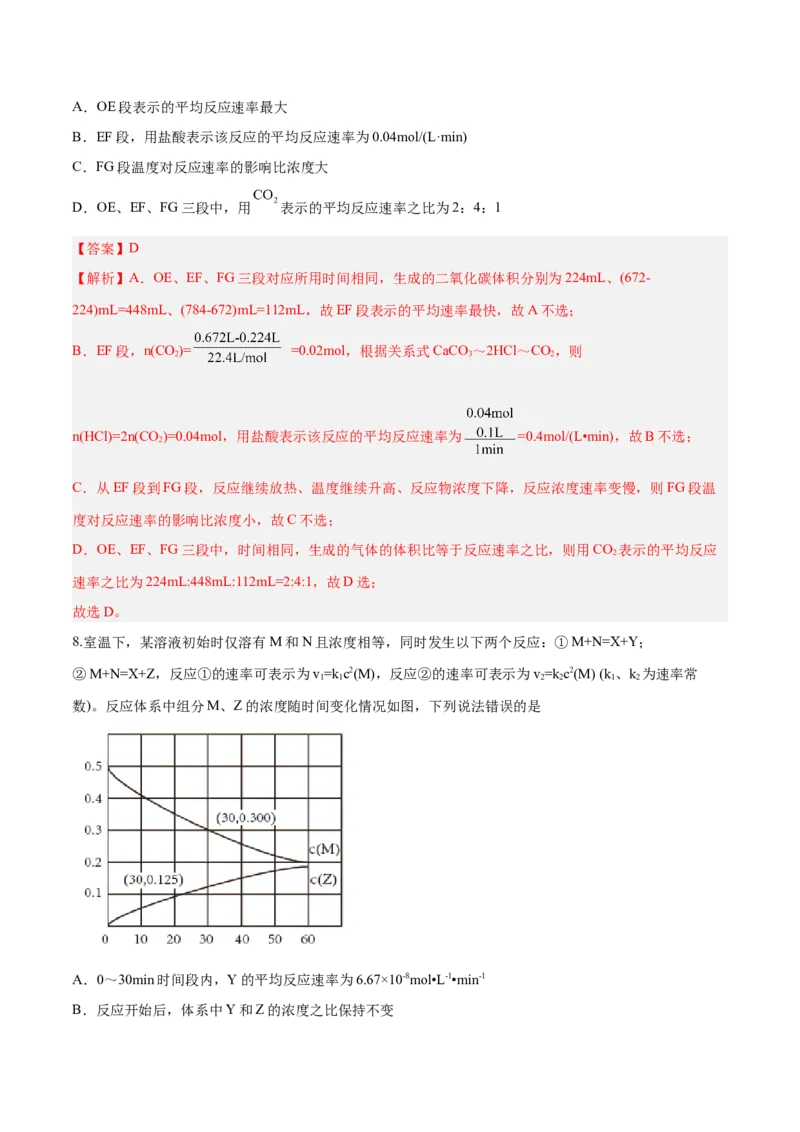
7.用纯净的 固体与100mL稀盐酸反应制取 。实验过程记录如图所示( 的体积已折算为标准
状况下的体积,溶液体积变化忽略不计),下列说法中正确的是A.OE段表示的平均反应速率最大
B.EF段,用盐酸表示该反应的平均反应速率为0.04mol/(L·min)
C.FG段温度对反应速率的影响比浓度大
D.OE、EF、FG三段中,用 表示的平均反应速率之比为2:4:1
【答案】D
【解析】A.OE、EF、FG三段对应所用时间相同,生成的二氧化碳体积分别为224mL、(672-
224)mL=448mL、(784-672)mL=112mL,故EF段表示的平均速率最快,故A不选;
B.EF段,n(CO)= =0.02mol,根据关系式CaCO ~2HCl~CO,则
2 3 2
n(HCl)=2n(CO )=0.04mol,用盐酸表示该反应的平均反应速率为 =0.4mol/(L•min),故B不选;
2
C.从EF段到FG段,反应继续放热、温度继续升高、反应物浓度下降,反应浓度速率变慢,则FG段温
度对反应速率的影响比浓度小,故C不选;
D.OE、EF、FG三段中,时间相同,生成的气体的体积比等于反应速率之比,则用CO 表示的平均反应
2
速率之比为224mL:448mL:112mL=2:4:1,故D选;
故选D。
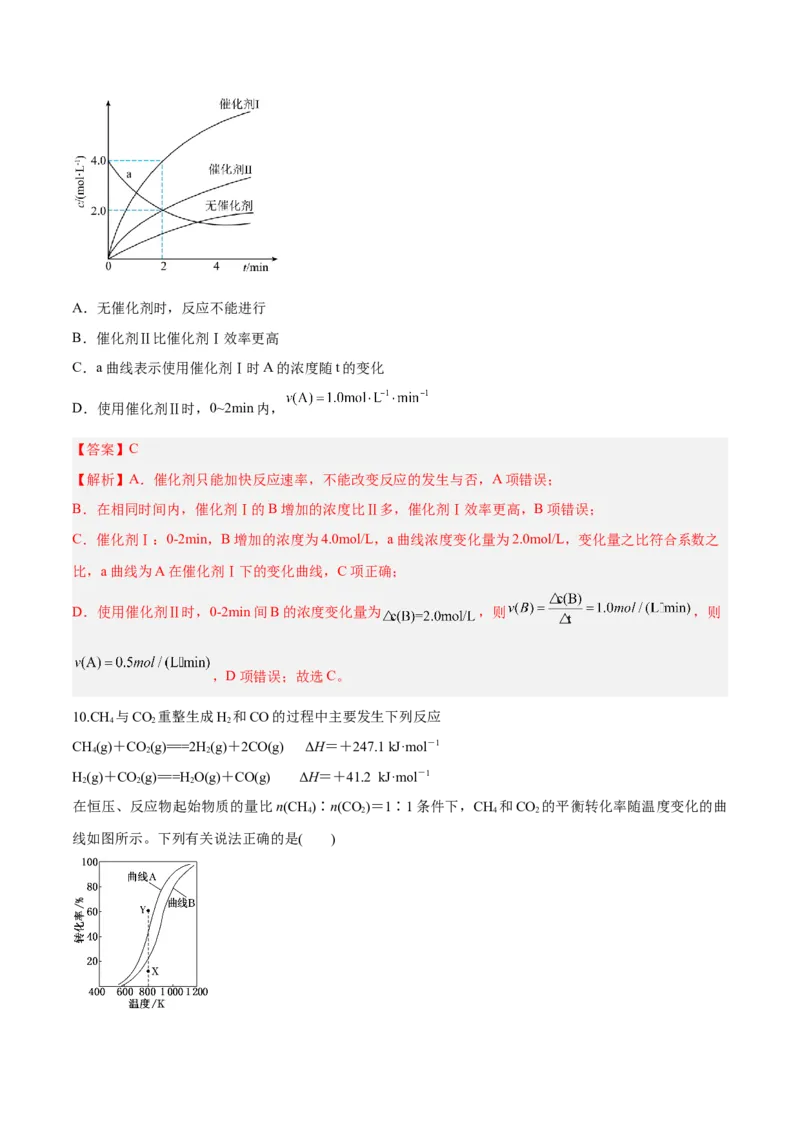
8.室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:①M+N=X+Y;
②M+N=X+Z,反应①的速率可表示为v=kc2(M),反应②的速率可表示为v=kc2(M) (k 、k 为速率常
1 1 2 2 1 2
数)。反应体系中组分M、Z的浓度随时间变化情况如图,下列说法错误的是
A.0~30min时间段内,Y的平均反应速率为6.67×10-8mol•L-1•min-1
B.反应开始后,体系中Y和Z的浓度之比保持不变C.如果反应能进行到底,反应结束时62.5%的M转化为Z
D.反应①的活化能比反应②的活化能大
【答案】A
【解析】由图中数据可知, 时,M、Z的浓度分别为0.300 和0.125 ,则M的变
化量为0.5 -0.300 =0.200 ,其中转化为Y的变化量为0.200 -0.125
=0.075 。因此, 时间段内,Y的平均反应速率为
,A说法不正确;由题中信息可知,反应①和反应②的速率之比为 ,Y和Z分别为反
应①和反应②的产物,且两者与M的化学计量数相同(化学计量数均为1),因此反应开始后,体系中Y
和Z的浓度之比等于 ,由于k、k 为速率常数,故该比值保持不变,B说法正确; 结合A、B的分析
1 2
可知因此反应开始后,在相同的时间内体系中Y和Z的浓度之比等于 =0.6,因此,如果反应能进行到
底,反应结束时有 的M转化为Z,即 的M转化为Z,C说法正确;由以上分析可知,在相同的
时间内生成Z较多、生成Y较少,因此,反应①的化学反应速率较小,在同一体系中,活化能较小的化学
反应速率较快,故反应①的活化能比反应②的活化能大,D说法正确。综上所述,相关说法不正确的只有
A,故本题选A。
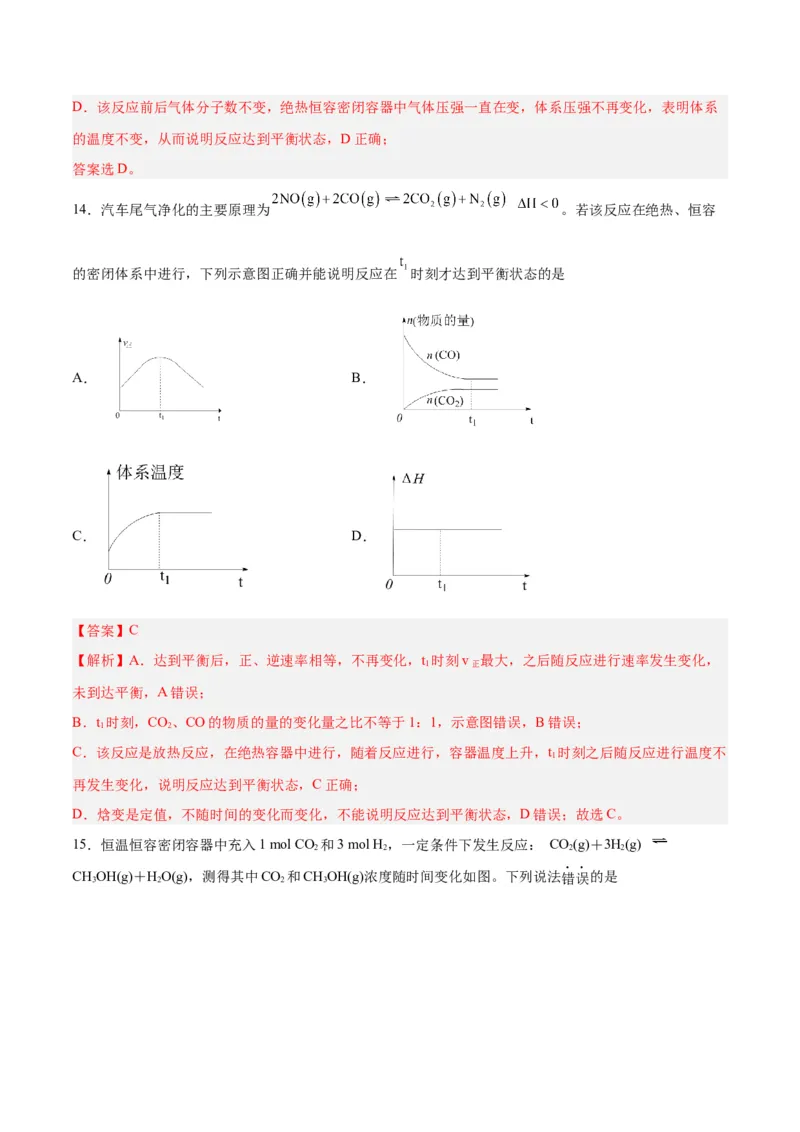
9.在相同条件下研究催化剂Ⅰ、Ⅱ对反应 的影响,各物质浓度c随反应时间t的部分变化曲
线如图所示。下列说法正确的是A.无催化剂时,反应不能进行
B.催化剂Ⅱ比催化剂Ⅰ效率更高
C.a曲线表示使用催化剂Ⅰ时A的浓度随t的变化
D.使用催化剂Ⅱ时,0~2min内,
【答案】C
【解析】A.催化剂只能加快反应速率,不能改变反应的发生与否,A项错误;
B.在相同时间内,催化剂Ⅰ的B增加的浓度比Ⅱ多,催化剂Ⅰ效率更高,B项错误;
C.催化剂Ⅰ:0-2min,B增加的浓度为4.0mol/L,a曲线浓度变化量为2.0mol/L,变化量之比符合系数之
比,a曲线为A在催化剂Ⅰ下的变化曲线,C项正确;
D.使用催化剂Ⅱ时,0-2min间B的浓度变化量为 ,则 ,则
,D项错误;故选C。
10.CH 与CO 重整生成H 和CO的过程中主要发生下列反应
4 2 2
CH(g)+CO(g)===2H (g)+2CO(g) ΔH=+247.1 kJ·mol-1
4 2 2
H(g)+CO(g)===H O(g)+CO(g) ΔH=+41.2 kJ·mol-1
2 2 2
在恒压、反应物起始物质的量比n(CH)∶n(CO)=1∶1条件下,CH 和CO 的平衡转化率随温度变化的曲
4 2 4 2
线如图所示。下列有关说法正确的是( )A.升高温度、增大压强均有利于提高CH 的平衡转化率
4
B.曲线A表示CH 的平衡转化率随温度的变化
4
C.相同条件下,改用高效催化剂能使曲线A和曲线B相重叠
D.恒压、800 K、n(CH)∶n(CO)=1∶1条件下,反应至CH 转化率达到X点的值,改变除温度外的特定
4 2 4
条件继续反应,CH 转化率能达到Y点的值
4
【答案】D
【解析】升高温度有利于题干中第一个反应正向进行,有利于提高CH 的平衡转化率,但增大压强有利于
4
题干中第一个反应逆向进行,不利于提高CH 的平衡转化率,A项错误;由题述反应及起始反应物的物质
4
的量比可知,平衡时CO 的转化率比CH 的高,则曲线B表示CH 的平衡转化率随温度的变化,B项错
2 4 4
误;使用催化剂只能加快化学反应速率,对化学平衡无影响,即曲线 A和曲线B不能相重叠,C项错误;
恒压、800 K、n(CH)∶n(CO)=1∶1条件下,反应至CH 转化率达到X点的值时,通过增大n(CO)或减小压
4 2 4 2
强继续反应,可以使CH 的转化率从X点提高到Y点,D项正确。
4
11.工业上可以利用水煤气( 、 )合成二甲醚( ),同时生成 。合成过程中,主要发生三个
反应, ℃时,有关反应及相关数据如下。
保持原料气组成、压强、反应时间等因素不变,进行实验,测得 转化率随温度变化曲线如下图。下列
说法不正确的是
A. ℃时,水煤气合成二甲醚的热化学方程式:B. ℃时,增大压强、加入催化剂均可提高 的平衡转化率
C.220℃~240℃时,温度升高反应速率加快, 转化率升高
D.温度高于240℃时,温度升高 转化率降低的原因可能是平衡逆向移动
【答案】B
【解析】A.已知: ℃时,有关反应及相关数据如下
①
②
③
由盖斯定律可知,2×①+②+③得反应 ,则其焓变为
,A正确;
B.加入催化剂可以加快反应速率,但是不能改变物质的平衡转化率,B错误;
C.升高温度反应速率加快,2由图可知,20℃~240℃时,温度升高反应速率加快,且 转化率升高,C
正确;
D.反应均为放热反应,温度高于240℃时,温度升高导致平衡逆向移动,使得 转化率降低,D正确;
故选B。
12.观察图:对合成氨反应中,下列叙述错误的是
A.开始反应时,正反应速率最大,逆反应速率为零
B.随着反应的进行,正反应速率逐渐减小,逆反应速率逐渐增大
C.反应到达t 时,正反应速率与逆反应速率相等,反应停止
1D.反应在t 之后,正反应速率与逆反应速率相等,反应达到化学平衡状态
1
【答案】C
【解析】A.反应开始时,反应物的浓度最大,正反应速率最大,生成物的浓度为零,逆反应速率为零,
故A正确;
B.随着反应的进行,反应物的浓度降低,则正反应速率逐渐减小,生成物的浓度增大,则逆反应速率逐
渐增大,故B正确;
C.反应到达t 时,正反应速率与逆反应速率相等,但都不为零,反应没有停止,故C错误;
1
D.反应在t 之后,正反应速率与逆反应速率相等,但都不为零,达到化学平衡状态,故D正确;
1
故选C。
13.向绝热恒容密闭容器中通入A和B,在一定条件下发生反应 ,正反应速率
随时间的变化关系如图所示,下列结论正确的是
A.气体A的浓度:a点小于b点
B.若 ,则气体C的生成量:ab段大于bc段
C.c点时:
D.体系压强不再变化,说明反应达到平衡状态
【答案】D
【解析】A.随着反应的进行,反应物气体 的浓度不断减小,故气体 的浓度: 点大于 点, 错
误;
B.在 段,正反应速率不断增大,则单位时间内气体 的生成量不断增多,故若 ,则气体
的生成量: 段小于 段,B错误;
C.化学反应达到平衡状态时,正反应速率不再变化,而c点时,正反应速率开始减少,说明反应没有达
到平衡状态,则 ,C错误;D.该反应前后气体分子数不变,绝热恒容密闭容器中气体压强一直在变,体系压强不再变化,表明体系
的温度不变,从而说明反应达到平衡状态,D正确;
答案选D。
14.汽车尾气净化的主要原理为 。若该反应在绝热、恒容
的密闭体系中进行,下列示意图正确并能说明反应在 时刻才达到平衡状态的是
A. B.
C. D.
【答案】C
【解析】A.达到平衡后,正、逆速率相等,不再变化,t 时刻v 最大,之后随反应进行速率发生变化,
1 正
未到达平衡,A错误;
B.t 时刻,CO、CO的物质的量的变化量之比不等于1:1,示意图错误,B错误;
1 2
C.该反应是放热反应,在绝热容器中进行,随着反应进行,容器温度上升,t 时刻之后随反应进行温度不
1
再发生变化,说明反应达到平衡状态,C正确;
D.焓变是定值,不随时间的变化而变化,不能说明反应达到平衡状态,D错误;故选C。
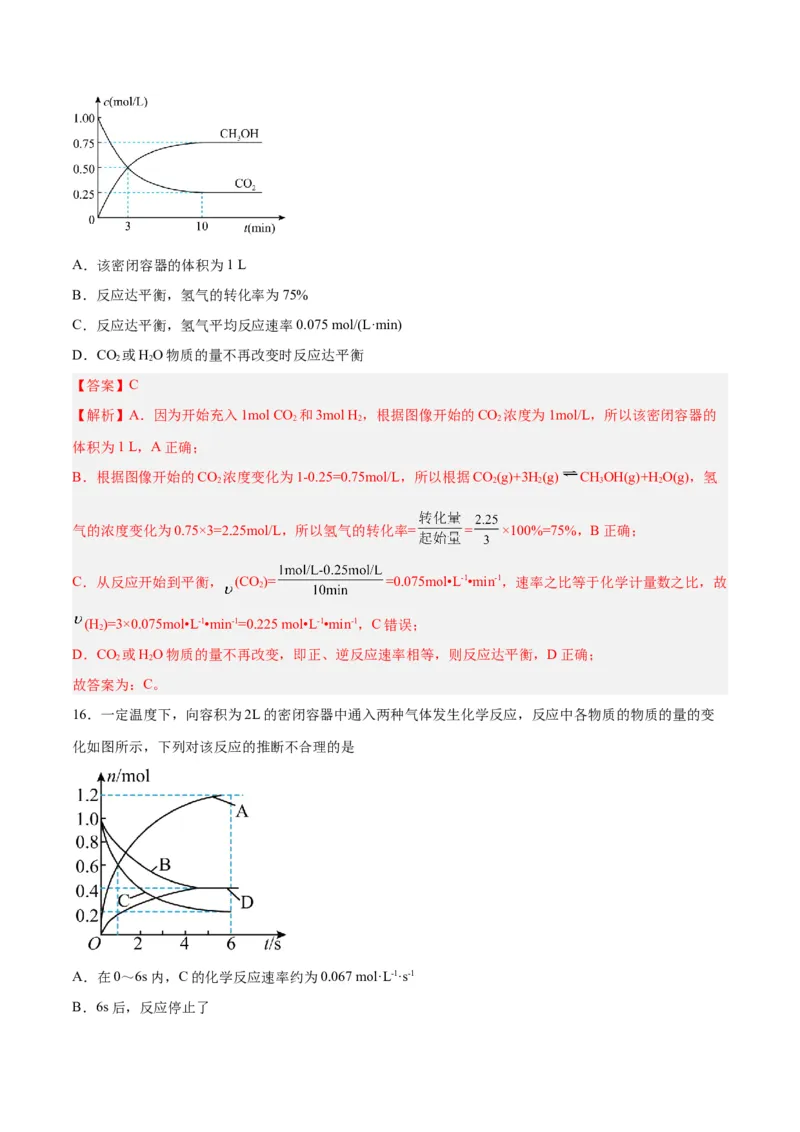
15.恒温恒容密闭容器中充入1 mol CO 和3 mol H ,一定条件下发生反应: CO(g)+3H(g)
2 2 2 2
CHOH(g)+HO(g),测得其中CO 和CHOH(g)浓度随时间变化如图。下列说法错误的是
3 2 2 3A.该密闭容器的体积为1 L
B.反应达平衡,氢气的转化率为75%
C.反应达平衡,氢气平均反应速率0.075 mol/(L·min)
D.CO 或HO物质的量不再改变时反应达平衡
2 2
【答案】C
【解析】A.因为开始充入1mol CO 和3mol H,根据图像开始的CO 浓度为1mol/L,所以该密闭容器的
2 2 2
体积为1 L,A正确;
B.根据图像开始的CO 浓度变化为1-0.25=0.75mol/L,所以根据CO(g)+3H(g) CHOH(g)+H O(g),氢
2 2 2 3 2
气的浓度变化为0.75×3=2.25mol/L,所以氢气的转化率= = ×100%=75%,B正确;
C.从反应开始到平衡, (CO)= =0.075mol•L-1•min-1,速率之比等于化学计量数之比,故
2
(H )=3×0.075mol•L-1•min-1=0.225 mol•L-1•min-1,C错误;
2
D.CO 或HO物质的量不再改变,即正、逆反应速率相等,则反应达平衡,D正确;
2 2
故答案为:C。
16.一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量的变
化如图所示,下列对该反应的推断不合理的是
A.在0~6s内,C的化学反应速率约为0.067 mol·L-1·s-1
B.6s后,反应停止了C.该反应的化学方程式为3B+4C 6A+2D
D.在0~4s内,v(A)=3v(D) ⇌
【答案】B
【解析】A.在0~6s内,C的化学反应速率约为 ,A正确;
B.6s后,反应达平衡,正、逆反应速率相等但不等于零,反应没有停止,只是达到动态平衡,B错误;
C.由图中信息可知,0~6s内B、C物质的量分别减小0.6mol、0.8mol,A、D物质的量分别增加1.2mol、
0.4mol,所以B、C、A、D系数比为3∶4∶6∶2,该反应的化学方程式为3B+4C 6A+2D,C正确;
D.在0~4s内,用不同物质表示表示反应速率,速率比等于方程式系数比,⇌v(A)=3v(D),D正确;
故答案选B。
17.若在绝热、恒容的密闭容器中充入一定量的SO Cl(g)和SCl (g),发生反应: SO Cl(g)+SCl (g)
2 2 2 2 2 2
2SOCl (g),下列示意图能说明t 时刻反应达到平衡状态的是
2 1
A.a和c B.b和d C.c和d D.b和c
【答案】B
【解析】由图像可知正反应是放热反应,a中t 时刻正反应速率在减小,说明反应没有达到平衡;b中反应
1
放热,温度升高压强增大,当压强不变时说明反应达到平衡;c中两种物质的浓度保持不变时说明达到平
衡,所以此时并没有达到平衡;d中所示反应物的转化率不再变化说明达到平衡,B正确;
故选B。
18.已知X(g)和Y(g)可以相互转化:2X(g) Y(g) ΔH<0。现将一定量X(g)和Y(g)的混合气体通入一体积
为1 L的恒温密闭容器中,反应物及生成物⇌的浓度随时间变化的关系如图所示。则下列说法不正确的是A.若混合气体的压强不变,则说明反应已达化学平衡状态
B.a、b、c、d四个点表示的反应体系中,表示化学反应处于平衡状态的只有b点
C.25~30 min内用X表示的平均化学反应速率是0.08 mol·L-1·min-1
D.反应进行至25 min时,曲线发生变化的原因是增加Y的浓度
【答案】D
【分析】根据图示可知Y是反应物,X是生成物,在0-10 min内该反应达到平衡状态,相同时间内反应物
浓度变化量 n(Y)=(0.6- 0.4) mol/L=0.2 mol/L,生成物浓度变化量 n(X)=(0.6-0.2)mol/L=0.4 mol/L,反应物
和生成物计△量数之比等于其浓度变化量之比=0.2 mol/L:0.4 mol/L△=l:2,反应方程式为:Y(g) 2X(g),
然后根据用不同物质表示的反应速率关系及影响因素分析。
【解析】A.恒温恒容条件下,混合气体压强与气体物质的量成正比,该反应前后气体计量数之和减小,
则气体压强减小,则如果混合气体压强不变时,正、逆反应速率相等,反应体系达到平衡状态,A正确;
B.各物质的物质的量浓度不变时该反应达到平衡状态,根据图知,只有b点各物质的物质的量浓度不
变,反应达到平衡状态,B正确;
C.25 ~ 30 min内用X表示的平均化学反应速率v(X)= ,C正确;
D.25 min时,X的物质的量浓度增大、Y的物质的量浓度不变,所以改变的条件是增大X的浓度,D错
误;
故合理选项是D。
19.近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长。因此,将氯化氢
转化为氯气的技术成为科学研究的热点。回答下列问题:
(1)Deacon发明的直接氧化法为:4HCl(g)+O(g)===2Cl(g)+2HO(g)。如图为刚性容器中,进料浓度比
2 2 2
c(HCl)∶c(O )分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系:
2可知反应平衡常数K(300 ℃)______K(400 ℃)(填“大于”或“小于”)。设HCl初始浓度为c ,根据进料
0
浓度比c(HCl)∶c(O )=1∶1的数据计算K(400 ℃)=______(列出计算式)。按化学计量比进料可以保持反
2
应物高转化率,同时降低产物分离的能耗。进料浓度比 c(HCl)∶c(O )过低、过高的不利影响分别是
2
________、________。
(3)在一定温度的条件下,进一步提高HCl的转化率的方法是___________________________。(写出2种)
【答案】(1)大于 O 和Cl 分离能耗较高 HCl转化率较低 (3)增加反应体系压强、及时除去产物
2 2
【解析】(1)由题给HCl平衡转化率随温度变化的关系图可知,随温度升高,HCl平衡转化率降低,则此反
应为放热反应,温度越高,平衡常数越小,即K(300 ℃)大于K(400 ℃)。结合题图可知,c(HCl)∶c(O )=
2
1∶1、400 ℃时HCl的平衡转化率为84%,列出三段式:
4HCl(g) + O(g) === 2Cl(g)+2HO(g)
2 2 2
起始 c c 0 0
0 0
转化 0.84c 0.21c 0.42c 0.42c
0 0 0 0
平衡 (1-0.84)c (1-0.21)c 0.42c 0.42c
0 0 0 0
则K(400 ℃)==;进料浓度比c(HCl)∶c(O )过低会使O 和Cl 分离的能耗较高,过高则会造成HCl转化
2 2 2
率较低。(3)题述反应是气体体积减小的反应,增大反应体系压强可使反应正向移动,提高HCl的转化率,
及时分离出产物也能提高HCl的转化率。
20.近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:
(1)反应Ⅱ:3SO (g)+2HO(g)===2H SO (l)+S(s) ΔH=-254 kJ·mol-1
2 2 2 4
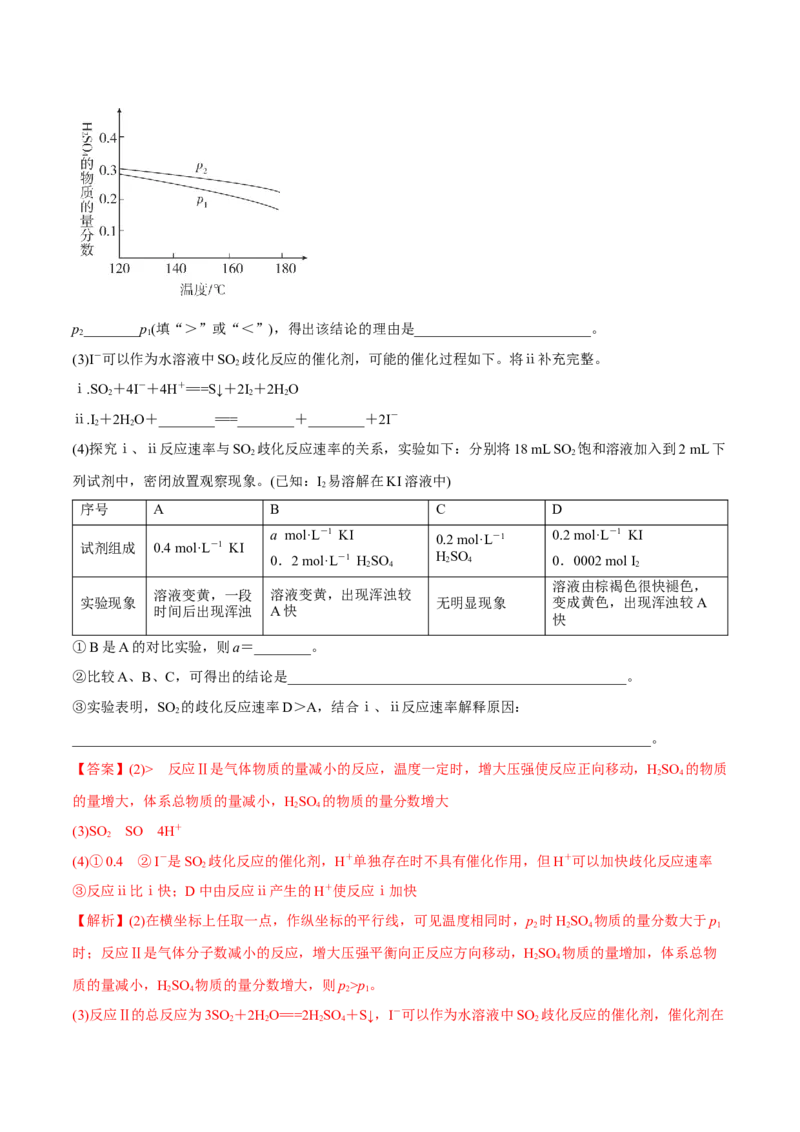
(2)对反应Ⅱ,在某一投料比时,两种压强下,HSO 在平衡体系中物质的量分数随温度的变化关系如图所
2 4
示。p________p(填“>”或“<”),得出该结论的理由是_________________________。
2 1
(3)I-可以作为水溶液中SO 歧化反应的催化剂,可能的催化过程如下。将ⅱ补充完整。
2
ⅰ.SO+4I-+4H+===S↓+2I+2HO
2 2 2
ⅱ.I+2HO+________===________+________+2I-
2 2
(4)探究ⅰ、ⅱ反应速率与SO 歧化反应速率的关系,实验如下:分别将18 mL SO 饱和溶液加入到2 mL下
2 2
列试剂中,密闭放置观察现象。(已知:I 易溶解在KI溶液中)
2
序号 A B C D
a mol·L-1 KI 0.2 mol·L-1 0.2 mol·L-1 KI
试剂组成 0.4 mol·L-1 KI
0.2 mol·L-1 HSO H 2 SO 4 0.0002 mol I
2 4 2
溶液由棕褐色很快褪色,
溶液变黄,一段 溶液变黄,出现浑浊较
实验现象 无明显现象 变成黄色,出现浑浊较A
时间后出现浑浊 A快
快
①B是A的对比实验,则a=________。
②比较A、B、C,可得出的结论是________________________________________________。
③实验表明,SO 的歧化反应速率D>A,结合ⅰ、ⅱ反应速率解释原因:
2
__________________________________________________________________________________。
【答案】(2)> 反应Ⅱ是气体物质的量减小的反应,温度一定时,增大压强使反应正向移动,HSO 的物质
2 4
的量增大,体系总物质的量减小,HSO 的物质的量分数增大
2 4
(3)SO SO 4H+
2
(4)①0.4 ②I-是SO 歧化反应的催化剂,H+单独存在时不具有催化作用,但H+可以加快歧化反应速率
2
③反应ⅱ比ⅰ快;D中由反应ⅱ产生的H+使反应ⅰ加快
【解析】(2)在横坐标上任取一点,作纵坐标的平行线,可见温度相同时,p 时HSO 物质的量分数大于p
2 2 4 1
时;反应Ⅱ是气体分子数减小的反应,增大压强平衡向正反应方向移动,HSO 物质的量增加,体系总物
2 4
质的量减小,HSO 物质的量分数增大,则p>p。
2 4 2 1
(3)反应Ⅱ的总反应为3SO +2HO===2H SO +S↓,I-可以作为水溶液中SO 歧化反应的催化剂,催化剂在
2 2 2 4 2反应前后质量和化学性质不变,(总反应-反应ⅰ)÷2得反应ⅱ的离子方程式为I+2HO+SO ===4H++SO
2 2 2
+2I-。
(4)①B是A的对比实验,采用控制变量法,B比A多加了0.2 mol·L-1 HSO ,A与B中KI浓度应相等,
2 4
则a=0.4。
②对比A与B,加入H+可以加快SO 歧化反应的速率;对比B与C,单独H+不能催化SO 的歧化反应;
2 2
比较A、B、C,可得出的结论是:I-是SO 歧化反应的催化剂,H+单独存在时不具有催化作用,但H+可
2
以加快歧化反应速率。
③对比D和A,D中加入KI的浓度小于A,D中多加了I,反应ⅰ消耗H+和I-,反应ⅱ中消耗I,D中
2 2
“溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快”,反应速率D>A,由此可见,反应ⅱ比反应ⅰ速
率快,反应ⅱ产生H+使c(H+)增大,从而使反应ⅰ加快。