文档内容
主题五 物质的结构与性质测试(一)
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Na-23 K-39 Cr-52 Mn-55
第Ⅰ卷(选择题 共45分)
一、选择题(本题共15个小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合
题目要求的)
1.下列有关描述及化学用语的表示方法正确的是( )
A.As原子的简化电子排布式为[Ar]3s23p3
B.KCI形成过程:
C.基态Mg原子的核外电子排布图为
D.Se在周期中属于p区元素,Zn属于ds区元素
【答案】D
【解析】A项,As的原子序数为33,属于主族元素,由构造原理可知电子排布为
1s22s22p63s23p63d104s24p3,所以As原子的简化电子排布式为:[Ar]3d104s24p3,A错误;B项,KCl形成过程
为 ,B错误;C项,基态Mg原子的核外电子排布式为:1s22s22p63s2,所以核外
电子轨道表示式: ,C错误;D项,Se的价电子为4s24p4,最后填充4p电子,
为p区元素,Zn的价电子构型为3d104s2,属于ds区元素,D正确;故选D。
2.下列化学术语正确的是( )
A. 的电子式: B.AlCl 的结构式:
3
C.Cr原子的价电子排布图: D.葡萄糖的实验式:CHO
2
【答案】D【解析】A项,氢化钠的电子式为 ,A项错误;B项,AlCl 的结构式 ,B项
3
错误;C项,Cr原子的价电子排布图 ,C项错误;D项,葡萄糖的分子式
C H O,实验室为CHO,D项正确;故选D。
06 12 6 2
3.已知X、Y是短周期的两种元素,下列相关结论一定正确的是( )
选项 条件 结论
A 若原子半径:X>Y 则原子序数:XY
a
【答案】D
【解析】A项,同周期主族元素,核电荷数越大,原子半径越小,若X、Y同周期,原子半径:
X>Y,则原子序数:XY,可知X的周期数大于Y,即
原子序数X>Y,A项错误;B项,金属元素与非金属元素之间可能形成共价键,如AlCl 是共价化合物,
3
Al与Cl形成的是共价键,B项错误;C项,SO 分子中中心原子S是sp2杂化,则VSEPR模型为平面三角
2
形,C项错误;D项,电负性大的元素得电子能力强,在化合物中显负价,化合物中X显负价,则元素的
电负性:X>Y,D项正确。
4.N、 P、 As、 Sb是周期表中ⅤA族元素。下列说法正确的是( )
7 15 33 51
A.电负性大小: B.氢化物沸点高低:AsH >PH >NH
3 3 3
C.酸性强弱:HNO>HPO >HAsO D.ⅤA族元素单质的晶体类型相同
3 3 4 3 4
【答案】C
【解析】A项,N、P、As为同主族元素,从上到下非金属性依次减弱,则电负性大小:,A不正确;B项,由于NH 分子间能形成氢键,增大了分子间的作用力,使其沸
3
点升高,所以氢化物沸点高低:NH >AsH >PH ,B不正确;C项,N、P、As为同主族元素,从上到下
3 3 3
非金属性依次减弱,则最高价氧化物的水化物的酸性依次减弱,从而得出酸性强弱:HNO>HPO >
3 3 4
HAsO ,C正确;D项,ⅤA族元素单质中,N、P、As的单质晶体类型相同,都为分子晶体,但Sb为金
3 4
属,其晶体为金属晶体,D不正确;故选C。
5.NF 是一种优良的蚀刻气体。HF、F 均可用于制备NF ,F 制备NF 的反应为4NH +3F
3 2 3 2 3 3 2
NF +3NHF.K(HF)=6.3×10−4,K(NH ·H O)=1.8×10−5。下列说法正确的是( )
3 4 a b 3 2
A.中子数为10的氟原子: F B.HF的电子式:
C.NF 的空间构型为平面正三角形 D.第一电离能:I(F)>I(N)>I(O)
3 1 1 1
【答案】D
【解析】A项,中子数为10的氟原子的质量数为10+9=19,符号为 F,A错误;B项,HF为共价化
合物,电子式为 ,B错误;C项,NF 的价层电子对数为 =4,含一对孤电子对,空间构型为
3
三角锥形,C错误;D项,同周期自左至右第一电离能呈增大趋势,但N原子的2p能级轨道半满,更稳定,
第一电离能大于相邻元素,所以I(F)>I(N)>I(O),D正确;故选D。
1 1 1
6.光气(COCl )是一种重要的有机中间体。可用反应CHCl +H O=COCl ↑+HCl+H O制备光气。下列
2 3 2 2 2 2
叙述错误的是( )
A.CHCl 为极性分子
3
B.电负性:O>Cl>C
C.基态Cl原子的价电子轨道表示式:
D.COCl 中碳原子的杂化类型为sp3杂化
2
【答案】D
【解析】A项,CH 为非极性分子,3个H被Cl代替得到的CHCl 为极性分子,A正确;B项,非金
4 3
属性越强,电负性越大,故电负性:O>Cl>C,B正确;C项,Cl元素为17号元素,原子核外有17个电子,
所以核外电子排布式为:1s22s22p63s23p5,价电子轨道表示式: ,C正确;D项,COCl
2中含有碳氧双键,碳原子为sp2杂化,D错误;故选D。
7.CHOH、NH 和(CH)NNH 均为常见的燃料,关于这三者的结构与性质,下列说法错误的是(
3 2 4 3 2 2
)
A.CHOH的电子式为 B.NH 空间结构为平面形
3 2 4
C.CHOH、NH 和(CH)NNH 都易溶于水 D.CHOH和(CH)NNH中C、O、N杂化方式均
3 2 4 3 2 2 3 3 2
相同
【答案】B
【解析】A项,甲醇可看成是甲烷中的一个氢原子被羟基取代得到的,CHOH的电子式为 ,
3
A正确;B项,NH 中N原子的杂化方式为sp3,不是平面形,B错误;C项,CHOH、NH 和(CH)NNH
2 4 3 2 4 3 2 2
都能和水分子形成氢键,都易溶于水,C正确;D项,CHOH为四面体结构,-OH结构类似于水的结构,
3
(CH)NNH 的结构简式为 ,两者分子中C、O、N杂化方式均为sp3,D正确;故选B。
3 2 2
8.已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y
元素原子的最外层2p轨道上有2个未成对电子。X与Y可形成化合物XY,2元素可形成负一价离子。下
2 3
列说法正确的是( )
A.X元素基态原子的电子排布式为
B.X元素是第4周期第VA族元素
C.Y元素原子的轨道表示式为
D.Z元素的单质Z 在氧气中不能燃烧
2
【答案】B
【解析】X元素原子的4p轨道上有3个未成对电子,推知原子序数为33号,是As元素;Y元素原子
的最外层2p轨道上有2个未成对电子,推知原子序数为8,是O元素;已知X、Y和Z三种元素的原子序
数之和等于42,推知Z的原子序数为1,是氢元素;X与Y形成的化合物XY 是As O。A项,由分析知
2 3 2 3X为As,As元素基态原子的电子排布式为 ,故A项错误;B项,As元素是第4周期第
ⅤA族元素,故B正确;C项,由分析知Y为氧元素,不是碳元素,而 是碳元素原
子的轨道表示式,故C错误;D项,由分析知Z为氢元素,H 能在O 中燃烧,故D错误;故选B。
2 2
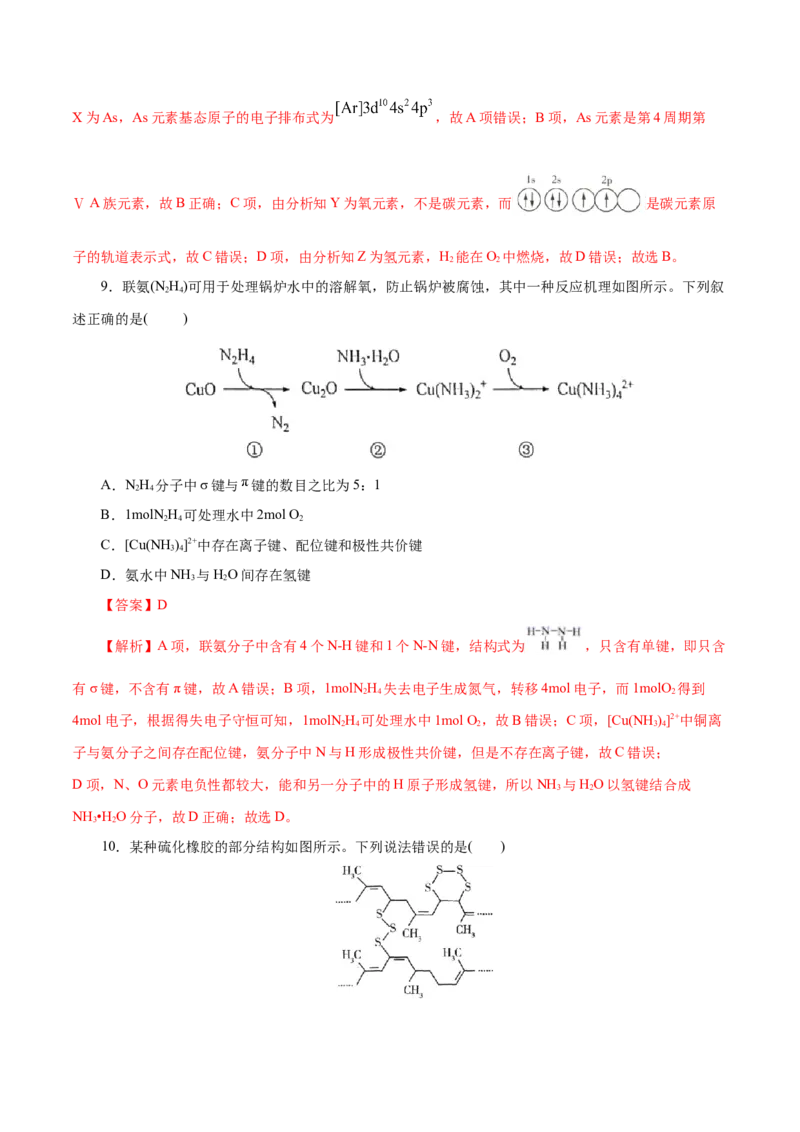
9.联氨(NH)可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,其中一种反应机理如图所示。下列叙
2 4
述正确的是( )
A.NH 分子中σ键与 键的数目之比为5:1
2 4
B.1molN H 可处理水中2mol O
2 4 2
C.[Cu(NH )]2+中存在离子键、配位键和极性共价键
3 4
D.氨水中NH 与HO间存在氢键
3 2
【答案】D
【解析】A项,联氨分子中含有4个N-H键和1个N-N键,结构式为 ,只含有单键,即只含
有σ键,不含有π键,故A错误;B项,1molN H 失去电子生成氮气,转移4mol电子,而1molO 得到
2 4 2
4mol电子,根据得失电子守恒可知,1molN H 可处理水中1mol O,故B错误;C项,[Cu(NH )]2+中铜离
2 4 2 3 4
子与氨分子之间存在配位键,氨分子中N与H形成极性共价键,但是不存在离子键,故C错误;
D项,N、O元素电负性都较大,能和另一分子中的H原子形成氢键,所以NH 与HO以氢键结合成
3 2
NH •H O分子,故D正确;故选D。
3 2
10.某种硫化橡胶的部分结构如图所示。下列说法错误的是( )A.图中元素位于s区和p区的种数之比为1:2
B.基态硫原子和碳原子最高能级电子云轮廓图均为哑铃形
C.图中的硫原子和碳原子共有两种杂化方式
D.图示结构中含有σ键、π键和氢键等作用力
【答案】D
【解析】A项,位于s区的元素有H元素,位于p区的元素有C、S元素,则图中元素位于s区和p区
的种数之比为1:2,A正确;B项,p能级的电子电子云轮廓图为哑铃形,s能级的电子电子云轮廓图为球
形,基态S原子最高能级为3p能级、基态C原子最高能级为2p能级,所以电子云轮廓图都是哑铃形,B
正确;C项,连接双键的碳原子采用sp2杂化,价层电子对数是4的碳原子、硫原子采用sp3杂化,所以
C、S原子共有两种杂化方式,C正确;D项,图中不存在氢键,存在σ键、π键,D错误;故选D。
11.冠醚能与碱金属离子作用,并随环的大小不同而与不同的金属离子作用。12-冠-4与K+作用而不
与Na+、Li+作用;18-冠-6与K+作用(如图),但不与Li+或Na+作用。下列说法正确的是( )
A.18-冠-6与K+作用,不与Li+或Na+作用,这反映了超分子的“自组装”的特征
B.18-冠-6中O原子与K+间存在离子键
C.18-冠-6中C和O的杂化轨道类型不同
D.冠醚能与碱金属离子形成的晶体属于离子晶体
【答案】D
【解析】A项,18-冠-6与K+作用,不与Li+或Na+作用,这反映了超分子的“分子识别”的特征,A
错误;B项,离子键是由阴、阳离子间形成的,18-冠-6为分子,分子中的O以O原子形式存在,所以18-
冠-6中O原子与K+间不存在离子键,B错误;C项,18-冠-6中C和O的价层电子对数均为4,杂化轨道类
型均为sp3杂化,杂化轨道类型相同,C错误;D项,冠醚能与碱金属离子形成晶体,碱金属离子是阳离子,
故所得到的晶体里还有阴离子,则冠醚能与碱金属离子形成的晶体属于离子晶体,D正确;故选D。
12.六硝基合钴酸钾{K [Co(NO )]}是一种黄色难溶物。检验K+或Co2+的反应原理如下:
3 2 6
CoCl+NaNO +KCl+HCl→K[Co(NO )]↓+NO↑+NaCl+H O(未配平)。下列说法错误的是( )
2 2 3 2 6 2
A.将上述反应设计成原电池,正极产物为NOB.配合物K[Co(NO )]中配位原子是氧原子
3 2 6
C.基态Co原子的价层电子中,成对电子数与未成对电子数之比为2:1
D.上述反应的离子方程式为CoCl+7NO -+3K++2H+=K[Co(NO )]↓+NO↑+HO
2 2 3 2 6 2
【答案】B
【解析】A.原电池正极得到电子,CoCl+NaNO +KCl+HCl→K[Co(NO )]↓+NO↑+NaCl+H O,该反应
2 2 3 2 6 2
中亚硝酸根得到电子生成NO,设计成原电池,正极产物为NO,故A正确;B项,氮原子电负性小于氧原
子,配合物K[Co(NO )]中配位原子是氮原子,Co提供空轨道,故B错误;C项,基态Co原子的价层电
3 2 6
子中,价层电子排布图为: ,成对电子数与未成对电子数之比为2:1,故C正确;D
项,上述反应的离子方程式为CoCl+7NO -+3K++2H+=K[Co(NO )]↓+NO↑+HO,故D正确;故选B。
2 2 3 2 6 2
13.前四周期的元素X、Y、Z、Q、W的原子序数依次增大,基态X原子的半径是所有原子中最小的,
Y与X可形成室温下XY、XY 两种无色液体,基态Z原子的M电子层上p轨道为半充满状态,Y、Q同
2 2 2
主族,W原子的价层电子排布式为 ,下列说法不正确的是
A.电负性:Z<Q<Y
B.简单离子半径:Z>Q>Y>Z
C.同周期中第一电离能比Q大的元素有1种
D. 三种元素形成的某些化合物,可存在于某些使用后的碱性电池中
【答案】C
【解析】五种前四周期的元素X、Y、Z、Q、W的原子序数依次增大,其中基态X原子的半径是所有
原子中最小的,则X为H元素;Y与X可形成室温下XY、XY 两种无色液体,则Y为O,基态Z原子的
2 2 2
M电子层上P轨道为半充满状态,其外围电子排布式为3s23p3,故Z为P元素;W原子的特征电子构型为
3d54s2,则W为Mn元素;Y、Q同主族,由Y为O元素,故Q为S元素。A项,由分析可知,Y、Z、Q
分别为O、P、S,根据同一周期从左往右电负性依次增大,同一主族从上往下电负性依次减小,故电负性
O>S>P即Z<Q<Y,A正确;B项,X、Y、Z、Q分别为H、O、P、S,根据电子层数越多半径越大,
电子层数相同,核电荷数越大,半径越小可知,简单离子半径P3->S2->O2->H+即Z>Q>Y>Z,B正确;
C项,Q为S,根据同一周期从左往右元素的第一电离能呈增大趋势,ⅡA与ⅢA、ⅤA与ⅥA反常,故
同周期中第一电离能比Q大的元素有P、Cl、Ar等3种,C错误;D项,X、Y、W分别为H、O、Mn三
种元素形成的某些化合物,如MnOOH可存在于某些使用后的碱性电池中,D正确;故选C。14.W、X、Y、Z、N是原子序数依次增大的五种短周期元素,W基态原子只有一种自旋取向,X的
最高正化合价与最低负化合价代数和为零,Y位于第二周期,基态原子的s能级电子总数与p能级电子总
数相等,Z基态原子的价电子中,在不同形状原子轨道运动中的电子数相等,N的简单离子半径是同周期
元素简单离子中最大的。下列说法不正确的是( )
A.Y的第一电离能一定低于同周期相邻元素
B.由W、X、Y、N四种元素中的任意两种形成的化合物只有极性共价键
C.由W、X、Y三种元素形成的化合物可能有成千上万种
D.最简单氢化物的稳定性: Z<Y
【答案】B
【解析】W、X、Y、Z、N是原子序数依次增大的五种短周期元素,W基态原子只有一种自旋取向,
说明W中只有1个电子,为H元素;X的最高正化合价与最低负化合价代数和为零,X为第IVA族元素,
X为C元素;Y位于第二周期,基态原子的s能级电子总数与p能级电子总数相等,Y的电子排布式为
1s22s22p4,为O元素;Z基态原子的价电子中,在不同形状原子轨道运动中的电子数相等,则Z的价电子
排布式为3s23p2,为Si元素,N的简单离子半径是同周期元素简单离子中最大的,N为P元素。A项,F对
最外层电子的吸引力比O强,N原子核外电子处于半满的较稳定状态,故第一电离能均高于 O,故A正确;
B项,H和O构成的化合物HO 中存在非极性共价键,故B错误;C项,由H、C、O三种元素形成的有
2 2
机化合物可能有成千上万种,故 C正确;D项,非金属性:O>Si,则最简单氢化物的稳定性:HO>
2
SiH,故D正确;故选B。
4
15.(CHNH )PbI 具有较高的光电转接效率,在太阳能电池領域具有重要的应用价值。(CHNH )PbI
3 3 3 3 3 3
的立方晶格结构如图所示,下列说法错误的是( )
A.CHNH +中N原子的杂化轨道类型为sp3
3 3
B.CHNH +中存在配位键
3 3C.甲基的供电子能力强于氢原子,则接受质子能力:CH)NH >(CH)NH
3 2 2 3 2
D.晶胞中B(灰色球)代表Pb2+,则每个晶胞中含有 的数目为3
【答案】C
【解析】由立方晶格结构可推知每个晶胞中A的个数=8× =1,C的个数=6× =3,B的个数为1,对
比化学式(CHNH )PbI 可知C为I-,B为中心原子,则B为Pb2+,A为CHNH +。A项,CHNH +的电子式
3 3 3 3 3 3 3
为 ,N有4个σ键,杂化方式为sp3杂化,A正确;B项,CHNH +中N提供孤电子对,
3 3
H提供空轨道,形成一个配位键,B正确;C项,甲基的供电子能力强于氢原子,则(CH)NH中含有两个
3 2
甲基,接受质子能力较强,即接受质子能力:(CH)NH <(CH)NH,C错误;D项,由分析可知晶胞中
3 2 2 3 2
B(灰色球)代表Pb2+,则每个晶胞中含有I-的数目为3,D正确;故选C。
第II卷(非选择题 共55分)
二、填空题(本题共4小题,共55分)
16.(13分)我国在商代或更早就掌握了冶炼铜的技术。以黄铜矿为原料冶炼铜涉及多个反应,其中一
个反应为8CuFeS+21O 8Cu+4FeO+2Fe O+16SO。
2 2 2 3 2
(1)基态Cu+的电子排布式为_______,从原子结构角度上解释,高温下CuO能转化为Cu O的原因是
2
_______。铜、铁两类原子核外电子运动状态相差_______种。
(2) SO、SO 、SO 2-、SO 2-四种含硫微粒中,中心原子为sp3杂化的是_______,属于极性分子的是
2 3 3 4
_______,空间构型为平面三角形的微粒是_______。
(3) FeO、Fe O 的熔点是下列两个值中的一个: , ,则两种氧化物的品体类型都是
2 3
_______, 是_______的熔点。
(4) CuFeS 晶胞结构如图1所示。晶胞中 的投影位置如图2所示。以晶胞参数为单位长度建立的坐
2
标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1的坐标分数为 ,则
原子2的分数坐标为_______;该晶体的密度为ρg· cm-3,则阿伏加德罗常数N =_______ mol-1 (用含ρ、a
A
的代数式表示)。【答案】(1)1 s22s22p63s23p63d10或 [Ar]3d10(1分)
Cu+的价电子排布式为全充满的3d10,处于较稳定状态,Cu2+的价电子排布式为3d9,较不稳定(2分)
3(1分)
(2) SO 2-、SO 2-(1分) SO (1分) SO (1分)
3 4 2 3
(3)离子晶体(1分) FeO(1分)
(4) (2分) (2分)
【解析】(1)Cu元素是29号元素,基态Cu+的电子排布式为1s22s22p63s23p63d10或[Ar]3d10,从原子结构
角度上解释,高温下CuO能转化为Cu O的原因是:Cu+的价电子排布式为全充满的3d10,处于较稳定状态,
2
Cu2+的价电子排布式为3d9,较不稳定,故高温下氧化铜可转化为更稳定的氧化亚铜。原子核外一个电子均
对应一种运动状态,铜原子比铁原子多3个电子,故铜原子多3种运动状态。(2)SO 中心原子孤电子对数=
2
、价层电子对数=2+1=3,故为sp2杂化、空间构型为V形、则其正负电荷中心不重叠,为极性
分子;SO 中心原子孤电子对数= 、价层电子对数=3+0=3,故为sp2杂化、空间构型为平面正三
3
角形、则其正负电荷中心重叠,为非极性分子;SO 2-离子中,中心原子S的孤电子对数= 、
3
价层电子对数=3+1=4,故为sp3杂化、空间构型为三角锥形;SO 2-离子中,中心原子S原子的孤电子对为
4
,价层电子对个数=4+0=4 ,所以中心原子为 sp3 杂化,其空间构型为正四面体;综上,
SO 、SO 、SO 2-、SO 2-四种含硫微粒中,中心原子为 sp3 杂化的是SO 2-、SO 2-,属于极性分子的是
2 3 3 4 3 4
SO ,空间构型为平面三角形的微粒是SO 。(3)两种物质的熔点都比较高,因此两种氧化物的晶体类型都
2 3
是离子晶体。由于氧化铁中Fe3+带三个单位正电荷,而氧化亚铁中Fe2+带两个单位正电荷,因此氧化铁中离子键强与氧化亚铁中的离子键,因此氧化亚铁的熔点较低,则1360℃是FeO的熔点。(4)由图1可知原子
2位于最右侧面上,沿x轴方向居中,沿z轴方向位于 处,结合原子1的分数坐标可知,原子2的坐标为
分数坐标为 ;由图知,S原子位于晶胞内部,共有8个硫原子,结合化学式可知一个晶胞内含有4
个Fe原子、4个Cu原子, 1个晶胞质量为 ,晶胞的体积为:2a3×10-30cm3,该晶体的密度为
,则 =2a3×10-30cm3×ρg· cm-3,则阿伏加德罗常数 (用含ρ、a的代数式
表示)。
17.(14分)镁、铜、硼及其化合物在医药、国防、材料领域应用广泛。请回答下列问题:
(1)铜是重要的金属材料铜属于元素周期表中的___________区元素,与铜同周期且基态原子最外层未
成对电子数与基态铜原子相同的元素有___________种。
(2)镁元素是人体必需的微量元素,其中起作用的是Mg2+。碱性条件下,检验Mg2+是否存在的化合物
被称为“试镁灵”,其结构简式如图所示,其组成元素中第一电离能由大到小的顺序为___________(用元素
符号表示),分子中N原子的杂类型为___________。
(3)氨硼烷(H BNH )是一种安全、高效的储氢材料,可由反应3CH+2B NH+6H O=3CO+6H BNH 制
3 3 4 3 3 6 2 2 3 3
得。
①HBNH 的结构与乙烷相似,HBNH 中存在配位键,提供孤电子对形成配位键的原子是
3 3 3 3
___________(填元素符号)。
②CO 的空间构型为___________,HO的键角小于CH 的键角,原因为___________。
2 2 4
(4)一种由Mg2+、N3-、F-组成的化合物的立方晶胞如图所示:①该化合物的化学式为___________, 的配位数为___________。
②Mg2+填充在由阴离子构成的八面体空隙中,则八面体空隙的填充率为___________%。
③若距离最近的两个Mg2+的核间距为apmN 表示阿伏加德罗常数的值,则晶胞密度为___________ g·
A
cm-3。
【答案】(1)ds(1分) 4(1分) (2)N>O>H>C(1分) sp2(1分)
(3)N(1分) 直线(1分) H O中的O原子和CH 中的C原子的杂化方式相同,但O原子上有2个
2 4
孤电子对,孤电子对与键合电子对之间的斥力比成键电子对之间的斥力大,导致水的键角变小(2分)
(4) ①Mg NF (2分) 6(1分) ②75(1分) ③ (2分)
3 3
【解析】(1)Cu属于ds区元素,与Cu同周期且基态原子最外层未成对电子数与Cu相同的元素有K、
Cr、Ga、Br,共4种;(2)“试镁灵”中由H、C、N、O\四种元素组成,第一电离能由大到小的顺序为N>O
>H>C;分子中氮氮双键和硝基中的氮原子均为sp2杂化;(3)①HBNH 的结构与乙烷相似,结构为
3 3
HB←NH ,B原子提供空轨道,N原子提供孤对电子;②CO 的空间构型为直线;HO中的O原子和CH
3 3 2 2 4
中的C原子的杂化方式相同,但O原子上有2个孤电子对,孤电子对与键合电子对之间的斥力大于成键电
子对之间的斥力,故水的键角小于甲烷的键角;(4)①根据均摊法可知,1个晶胞中含有3个Mg2+、1个N3-
和3个F-,故该化合物的化学式为MgNF ;由晶胞结构可知N3-的配位数为6;②晶胞中由阴离子构成的八
3 3
面体空隙有4个,3个Mg2+填充在八面体空隙中,八面体空隙的填充率为75%;③若距离最近的两个
Mg2+间距为apm,则晶胞边长为 ,晶胞密度为 。
18.(14分)Ge、GaAs、CdTe、CdSe等均为重要的半导体材料,在电子、材料等领域应用广泛。回答
下列问题:
(1)Ge基态原子核外电子排布式为[Ar]_______。
(2)第四周期主族元素中,第一电离能介于Ga、As之间的元素是_______(填元素符号)。
(3)碲的化合物TeO 、TeO 、HTe三种物质中,HTe的中心原子杂化类型为_______,分子构型为V形
2 3 2 2的是_______
(4)GaCl 熔点为77.9℃,气体在270℃左右以二聚体存在,GaCl 二聚体的结构式为_______。GaF 熔
3 3 3
点为1000℃,GaCl 熔点低于GaF 的原因是_______。
3 3
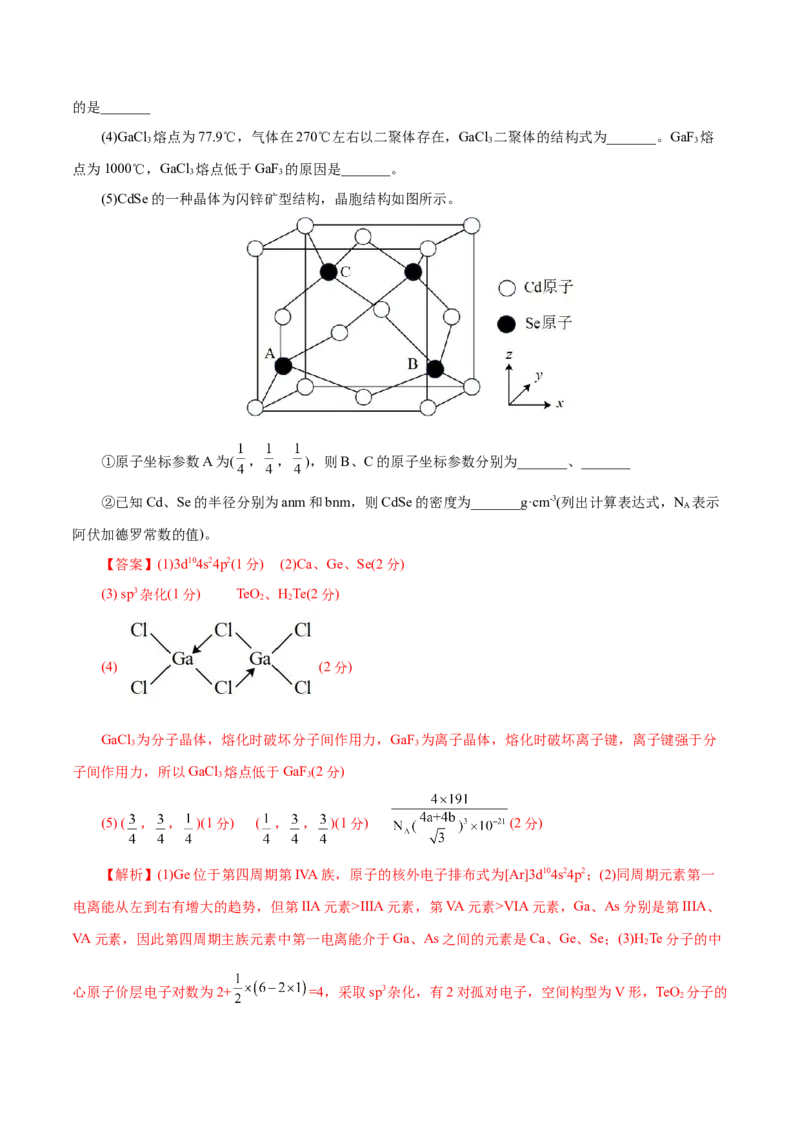
(5)CdSe的一种晶体为闪锌矿型结构,晶胞结构如图所示。
①原子坐标参数A为( , , ),则B、C的原子坐标参数分别为_______、_______
②已知Cd、Se的半径分别为anm和bnm,则CdSe的密度为_______g·cm-3(列出计算表达式,N 表示
A
阿伏加德罗常数的值)。
【答案】(1)3d104s24p2(1分) (2)Ca、Ge、Se(2分)
(3) sp3杂化(1分) TeO 、HTe(2分)
2 2
(4) (2分)
GaCl 为分子晶体,熔化时破坏分子间作用力,GaF 为离子晶体,熔化时破坏离子键,离子键强于分
3 3
子间作用力,所以GaCl 熔点低于GaF (2分)
3 3
(5) ( , , )(1分) ( , , )(1分) (2分)
【解析】(1)Ge位于第四周期第IVA族,原子的核外电子排布式为[Ar]3d104s24p2;(2)同周期元素第一
电离能从左到右有增大的趋势,但第IIA元素>IIIA元素,第VA元素>VIA元素,Ga、As分别是第IIIA、
VA元素,因此第四周期主族元素中第一电离能介于Ga、As之间的元素是Ca、Ge、Se;(3)H Te分子的中
2
心原子价层电子对数为2+ =4,采取sp3杂化,有2对孤对电子,空间构型为V形,TeO 分子的
2中心原子价层电子对数为2+ =3,有1对孤对电子,空间构型为V形,TeO 分子的中心原子价
3
层电子对数为3+ =3,无孤对电子,空间构型为平面三角形。(4)GaCl 二聚体的结构式为
3
。GaCl 为分子晶体,熔化时破坏分子间作用力,GaF 为离子晶体,熔化时破
3 3
坏离子键,离子键强于分子间作用力,所以GaCl 熔点低于GaF ;(5)①由晶胞结构示意图可知,A、B、C
3 3
三个原子分别位于八个小立方体中三个立方体的体心上,类似于金刚石的晶胞,根据相对位置,可知B、
C原子的坐标参数分别为( , , )、( , , );②该晶胞中所含有的Cd原子个数为8× +6×
=4,Se原子位于晶胞内部,有4个,晶胞参数为 nm,则其密度为 g·cm-3。
19.(14分)硅及其化合物在生产生活中有广泛应用。根据所学知识,回答下列问题:
(1)三甲基卤硅烷【(CH)SiX,X为Cl、Br、I】是重要的化工原料。
3 3
①氯元素基态原子的价电子排布式为__________;按照核外电子排布对元素周期表分区,溴元素位于
__________区;基态硅原子中有___________种运动状态不同的电子。
②Br、I的第一电离能的大小关系:I(Br)__ _________I (I)(填“大于”“小于”或“等于”)。
1 1
③常温下,(CH)SiI中Si—I键比(CH)SiCl中Si—Cl键易断裂的原因是__________________。
3 3 3 3
(2)(CH )SiCl可作为下列有机合成反应的催化剂。
3 3
①1个有机物A分子中采取sp2杂化的碳原子有____个。
②有机物B的沸点低于对羟基苯甲醛( )的沸点,其原因是___________。③CH CN中σ键与π键的个数比为___________。
3
(3)一种钛硅碳新型材料可用作高铁车体与供电网的连接材料。该材料的晶胞属于六方晶系(a、b方向
的夹角为120°,c方向垂直于a、b方向,棱长a+b≠c),如图甲所示;晶胞中碳原子的投影位置如图乙所示。
①该钛硅碳新型材料的化学式为___________。
②已知该新型材料的密度为4.51g•cm-3,且a、b的长度均为307pm,阿伏加德罗常数的值用N 表示,
A
则c的长度为___________pm (列出计算式)。
【答案】(1) ①3s23p5(1分) p(1分) 14(1分)
②大于(1分) ③I原子半径比Cl的原子半径大,导致Si-I键键能较小,较易断裂;而Si-Cl键键能较
大,较不易断裂(2分)
(2) ①7(1分) ②邻羟基苯甲醛主要形成分子内氢键,而对羟基苯甲醛只能形成分子间氢键,所以后者
的熔点高于前者(2分) ③5:2(1分)
(3) ①TiSiC (2分) ② (2分)
3 2
【解析】(1)①Cl原子核外有17个电子,核外电子排布式为[Ne] 3s23p5,价电子为3s23p5;溴原子的价
电子为4s24p5,属于p区;硅原子核外有14个电子,每个电子的运动状态各不相同,即有14种运动状态不
同的电子;②同主族自上而下第一电离能减小,所以I(Br)大于I(I);③I原子半径比Cl的原子半径大,导
1 1
致Si-I键键能较小,较易断裂;而Si-Cl键键能较大,较不易断裂;(2)①苯环上的碳原子以及碳氧双键中
的碳原子为sp2杂化,共有7个;②B为邻羟基苯甲醛,羟基与醛基距离较近,主要形成分子内氢键,而
对羟基苯甲醛只能形成分子间氢键,分子间氢键可以增大熔点,所以后者的熔点高于前者;③单键均为σ
键,碳氮三键中有一个σ键、两个π键,所以σ键与π键的个数比为5:2;(3)①根据均摊法,Ti原子的个数为8× +4× +4=6,Si原子的个数为8× =2,C原子的个数为4,Ti、Si、C原子的个数比为6:2:
4=3:1:2,所以化学式为Ti SiC ;②晶胞的质量为 g= g,密度为4.51g•cm-3,所以晶
3 2
胞的体积为 cm3= pm,底面为边长307pm的菱形,则底面积为 ×3072pm3,所以c
的长度为 pm。