文档内容
绝密★启用前
2025 年高考考前信息必刷卷 04(江苏专用)
化 学
考情速递
高考·新动向:图表信息深度整合:试卷中大量采用流程图(如第14、16题)、结构简式图(如第
10、15题)及实验装置图(如第3、9题),要求学生快速提取关键信息并关联化学原理。例如第17
题通过电解原理图考查电极反应分析,体现了对图像解析能力的强化。
跨学科融合趋势:题目注重物理、化学交叉应用,如第9题将电化学与废水处理结合,涉及能量转化
与离子迁移;第17题通过乙烯与SO₂反应机理图,要求理解催化循环中的电子转移与物质转化,体现
学科综合素养。
高考·新考法:知识融合型设问:第12题结合HS的多步电离与沉淀溶解平衡,要求学生综合运用电离
2
常数、电荷守恒与物料守恒分析离子浓度关系;第7题通过判断反应方程式的正误,融合物质性质
(如浓盐酸的强氧化性)与反应条件(如无水乙醇的作用),考查细节理解与综合应用能力。
系统性思维考查:工艺流程题(如第14、16题)要求分析多步操作(焙烧、酸浸、过滤、电解)的化
学原理及条件控制(如pH调节、温度影响),需学生串联知识点并解决实际问题。
高考·新情境:热点情境聚焦:环保(如Cr(Ⅵ)还原处理、SO₂资源化)、新能源(废水提铀同步产
电)、药物合成(利喘贝制备)等前沿领域将成为命题重点,需关注技术原理与化学知识的结合。
命题·大预测:能力导向强化:图像分析、实验设计及定量计算(如第14题锰氧化物化学式的确定)的
考查力度将进一步增强,需加强学生从数据到结论的逻辑推导训练。
学科交叉深化:电化学与工业流程(如第9、17题)、有机合成与反应机理(如第15题)的融合命题
可能增多,需培养跨模块知识整合能力。
今后将更注重真实情境下的问题解决能力,通过图表分析、跨学科融合及热点应用,全面考查学生的
核心素养。备考需强化图像解析训练,关注科技前沿案例,并加强综合性实验与工艺流程题的实战演
练。
(考试时间:90分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 P 31 S 32 K 39
一、选择题:本题共13小题,每小题3分,共39分。每小题只有一个选项符合题目要求。
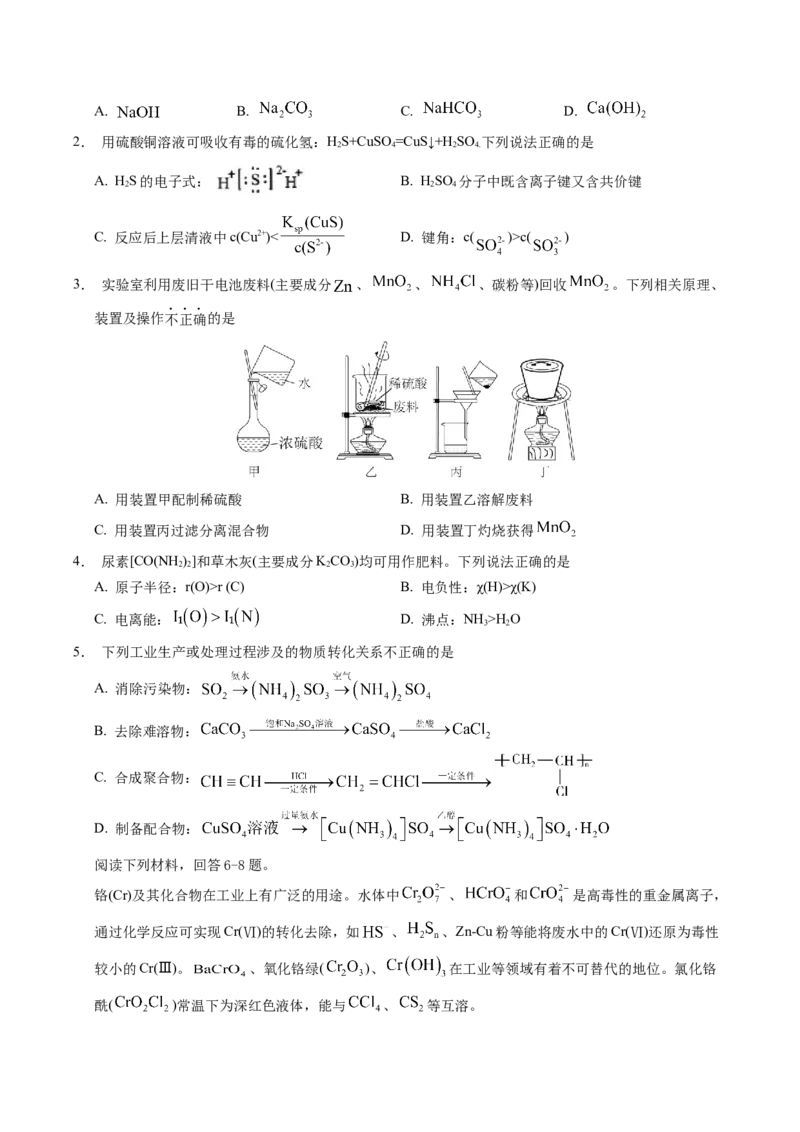
1. 侯德榜发明的侯氏制碱法造福了全人类。侯氏制碱法中的“碱”指的是A. B. C. D.
2. 用硫酸铜溶液可吸收有毒的硫化氢:HS+CuSO=CuS↓+H SO 下列说法正确的是
2 4 2 4.
A. HS的电子式: B. HSO 分子中既含离子键又含共价键
2 2 4
C. 反应后上层清液中c(Cu2+)< D. 键角:c( )>c( )
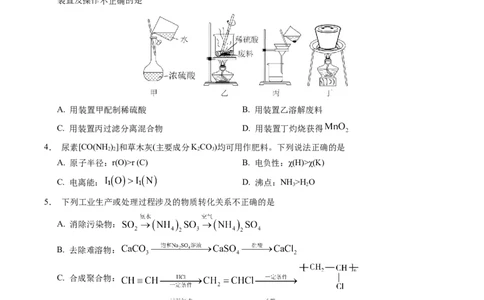
3. 实验室利用废旧干电池废料(主要成分 、 、 、碳粉等)回收 。下列相关原理、
装置及操作不正确的是
A. 用装置甲配制稀硫酸 B. 用装置乙溶解废料
C. 用装置丙过滤分离混合物 D. 用装置丁灼烧获得
4. 尿素[CO(NH)]和草木灰(主要成分KCO)均可用作肥料。下列说法正确的是
2 2 2 3
A. 原子半径:r(O)>r (C) B. 电负性:χ(H)>χ(K)
C. 电离能: D. 沸点:NH >H O
3 2
5. 下列工业生产或处理过程涉及的物质转化关系不正确的是
A. 消除污染物:
B. 去除难溶物:
C. 合成聚合物:
D. 制备配合物:
阅读下列材料,回答6-8题。
铬(Cr)及其化合物在工业上有广泛的用途。水体中 、 和 是高毒性的重金属离子,
通过化学反应可实现Cr(Ⅵ)的转化去除,如 、 、Zn-Cu粉等能将废水中的Cr(Ⅵ)还原为毒性
较小的Cr(Ⅲ)。 、氧化铬绿( )、 在工业等领域有着不可替代的地位。氯化铬
酰( )常温下为深红色液体,能与 、 等互溶。6. 下列说法正确的是
A. 空间构型为直线形 B. 中C原子采用 杂化
C. Cr(Ⅲ)的外围电子排布式为 D. 为分子晶体
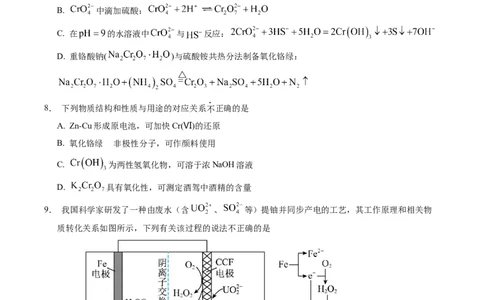
7. 下列化学反应表示错误的是
A. 与过量浓盐酸和无水乙醇混合制备 :
B. 中滴加硫酸:
C. 在 的水溶液中 与 反应:
D. 重铬酸钠( )与硫酸铵共热分法制备氧化铬绿:
8. 下列物质结构和性质与用途的对应关系不正确的是
A. Zn-Cu形成原电池,可加快Cr(Ⅵ)的还原
B. 氧化铬绿 为非极性分子,可作颜料使用
C. 为两性氢氧化物,可溶于浓NaOH溶液
D. 具有氧化性,可测定酒驾中酒精的含量
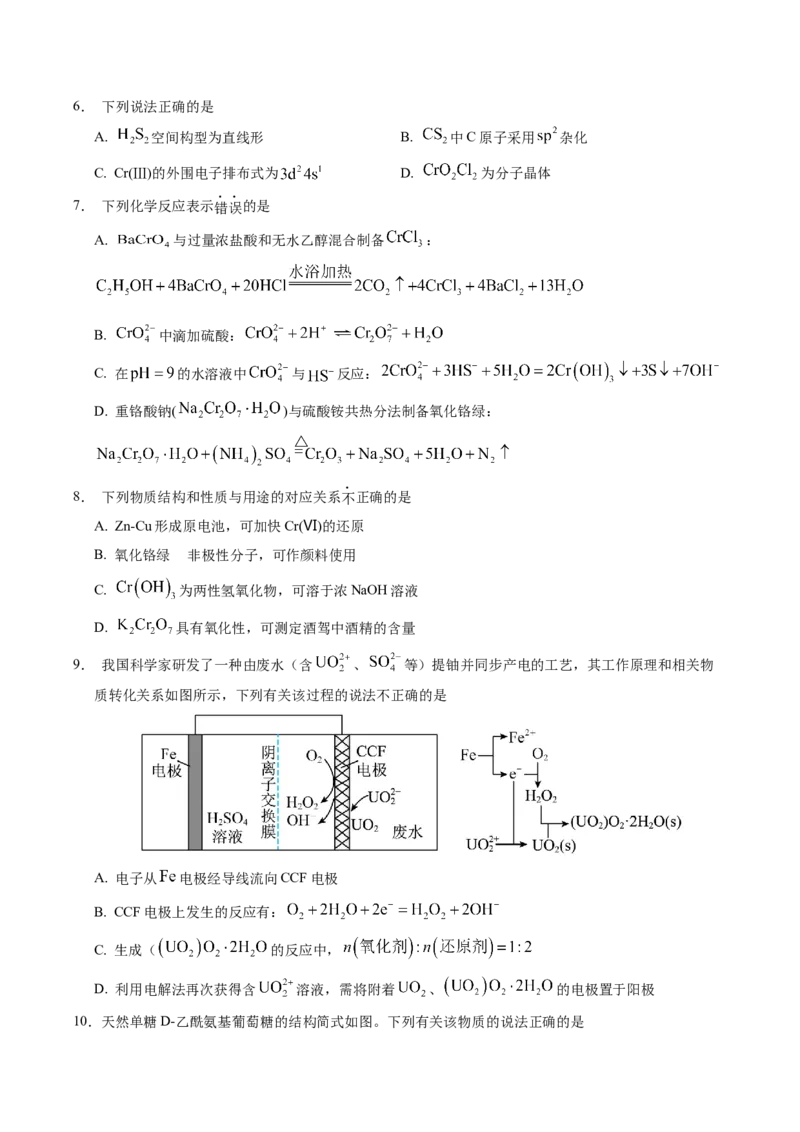
9. 我国科学家研发了一种由废水(含 、 等)提铀并同步产电的工艺,其工作原理和相关物
质转化关系如图所示,下列有关该过程的说法不正确的是
A. 电子从 电极经导线流向CCF电极
B. CCF电极上发生的反应有:
C. 生成( 的反应中,
D. 利用电解法再次获得含 溶液,需将附着 、 的电极置于阳极
10.天然单糖D-乙酰氨基葡萄糖的结构简式如图。下列有关该物质的说法正确的是A. 分子式为 B. 与葡萄糖互为同系物
C. 能发生缩聚反应 D. 分子中含3个手性碳原子
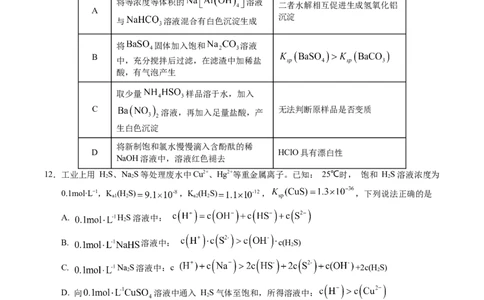
11.室温下,根据下列实验过程及现象,能验证相应实验结论的是
选项 实验过程及现象 实验结论
将等浓度等体积的 溶液
二者水解相互促进生成氢氧化铝
A
沉淀
与 溶液混合有白色沉淀生成
将 固体加入饱和 溶液
B
中,充分搅拌后过滤,在滤渣中加稀盐
酸,有气泡产生
取少量 样品溶于水,加入
C 无法判断原样品是否变质
溶液,再加入足量盐酸,产
生白色沉淀
将新制饱和氯水慢慢滴入含酚酞的稀
D HClO具有漂白性
NaOH溶液中,溶液红色褪去
12.工业上用 HS、NaS等处理废水中Cu2+、Hg2+等重金属离子。已知: 25℃时, 饱和 HS溶液浓度为
2 2 2
0.1mol∙L−1,K (H S) ,K (H S) , ,下列说法正确的是
a1 2 a2 2
A. HS溶液中:
2
B. 溶液中: c(HS)
2
C. NaS溶液中:c +2c(H S)
2 2
D. 向 溶液中通入 HS气体至饱和,所得溶液中:
2
13.甲醇-水催化重整可获得,其主要反应如下:
I:CHOH(g)+H O(g) CO(g)+3H(g) H=+49.4kJ/mol
3 2 2 2
II:CHOH(g) CO(g)+2H(g) H =+92kJ/mol
3 2
在1.01×105Pa下,将等体积的CHOH和HO的混合气体以一定流速通过装有催化剂的反应管,
3 2
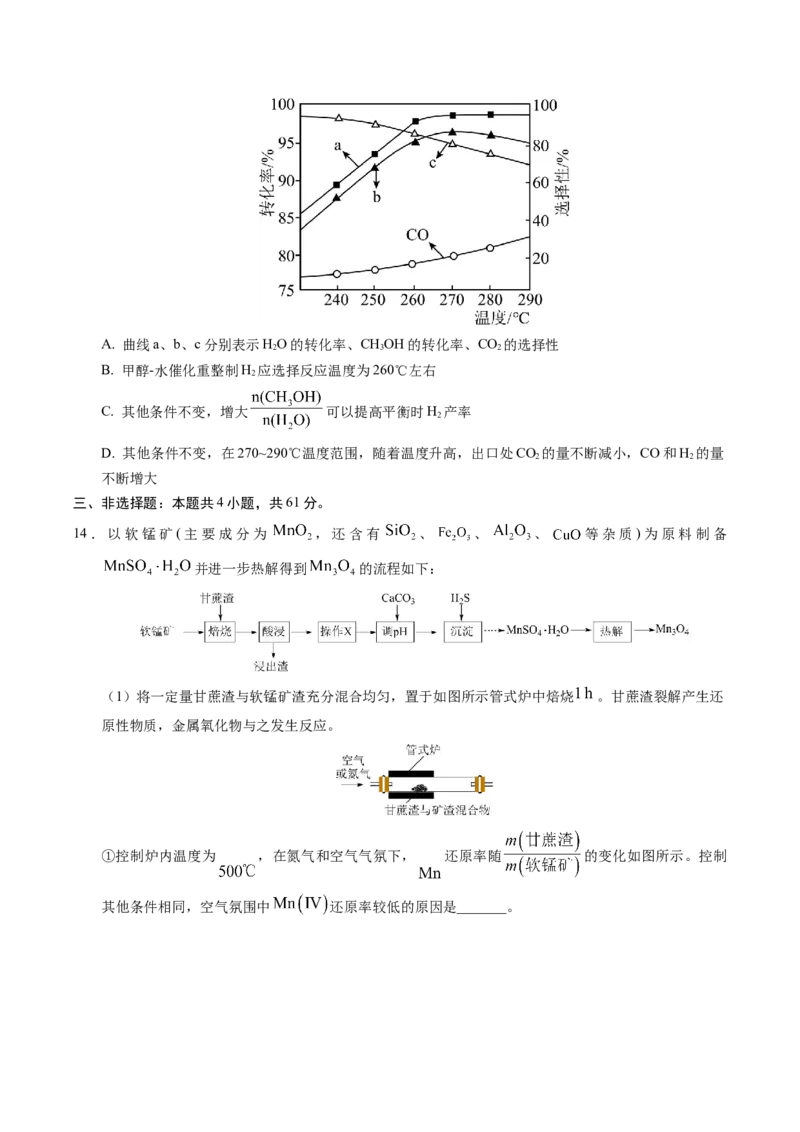
CHOH、HO的转化率及CO、CO 的选择性随温度变化情况如图所示。CO的选择性=
3 2 2
×100%]。下列说法正确的是A. 曲线a、b、c分别表示HO的转化率、CHOH的转化率、CO 的选择性
2 3 2
B. 甲醇-水催化重整制H 应选择反应温度为260℃左右
2
C. 其他条件不变,增大 可以提高平衡时H 产率
2
D. 其他条件不变,在270~290℃温度范围,随着温度升高,出口处CO 的量不断减小,CO和H 的量
2 2
不断增大
三、非选择题:本题共4小题,共61分。
14.以软锰矿(主要成分为 ,还含有 、 、 、 等杂质)为原料制备
并进一步热解得到 的流程如下:
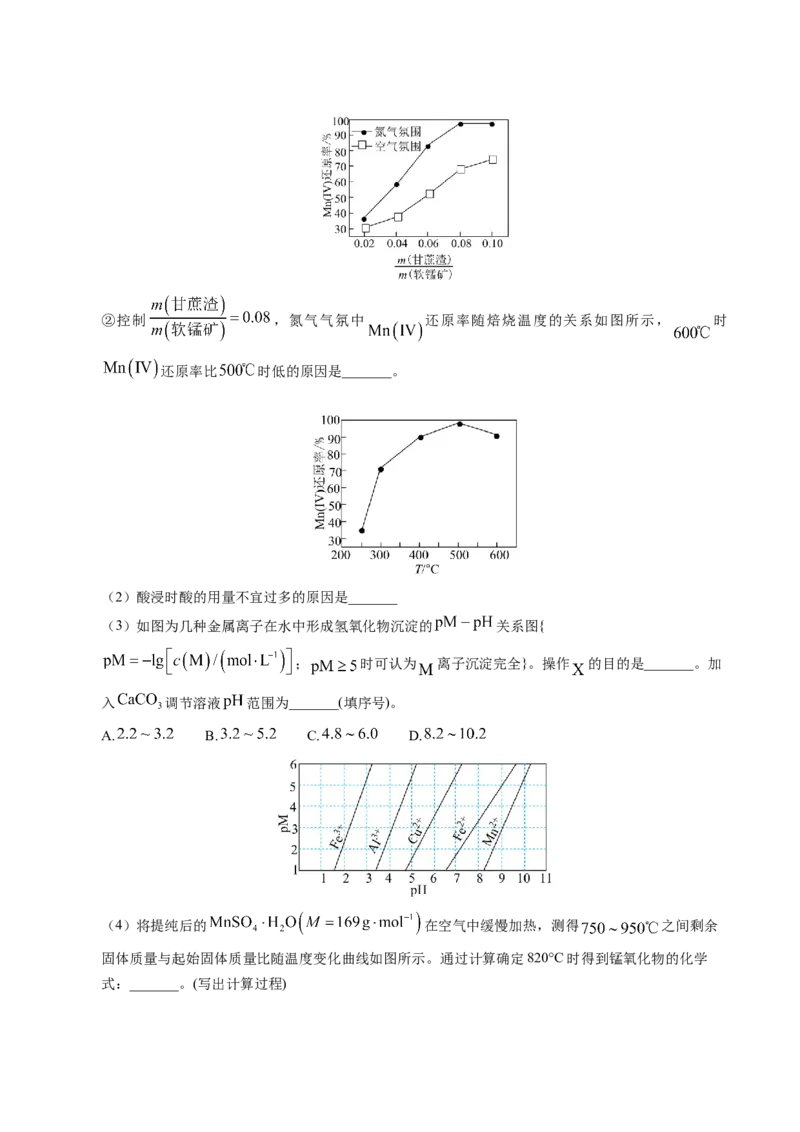
(1)将一定量甘蔗渣与软锰矿渣充分混合均匀,置于如图所示管式炉中焙烧 。甘蔗渣裂解产生还
原性物质,金属氧化物与之发生反应。
①控制炉内温度为 ,在氮气和空气气氛下, 还原率随 的变化如图所示。控制
其他条件相同,空气氛围中 还原率较低的原因是_______。②控制 ,氮气气氛中 还原率随焙烧温度的关系如图所示, 时
还原率比 时低的原因是_______。
(2)酸浸时酸的用量不宜过多的原因是_______
(3)如图为几种金属离子在水中形成氢氧化物沉淀的 关系图{
; 时可认为 离子沉淀完全}。操作 的目的是_______。加
入 调节溶液 范围为_______(填序号)。
A. B. C. D.
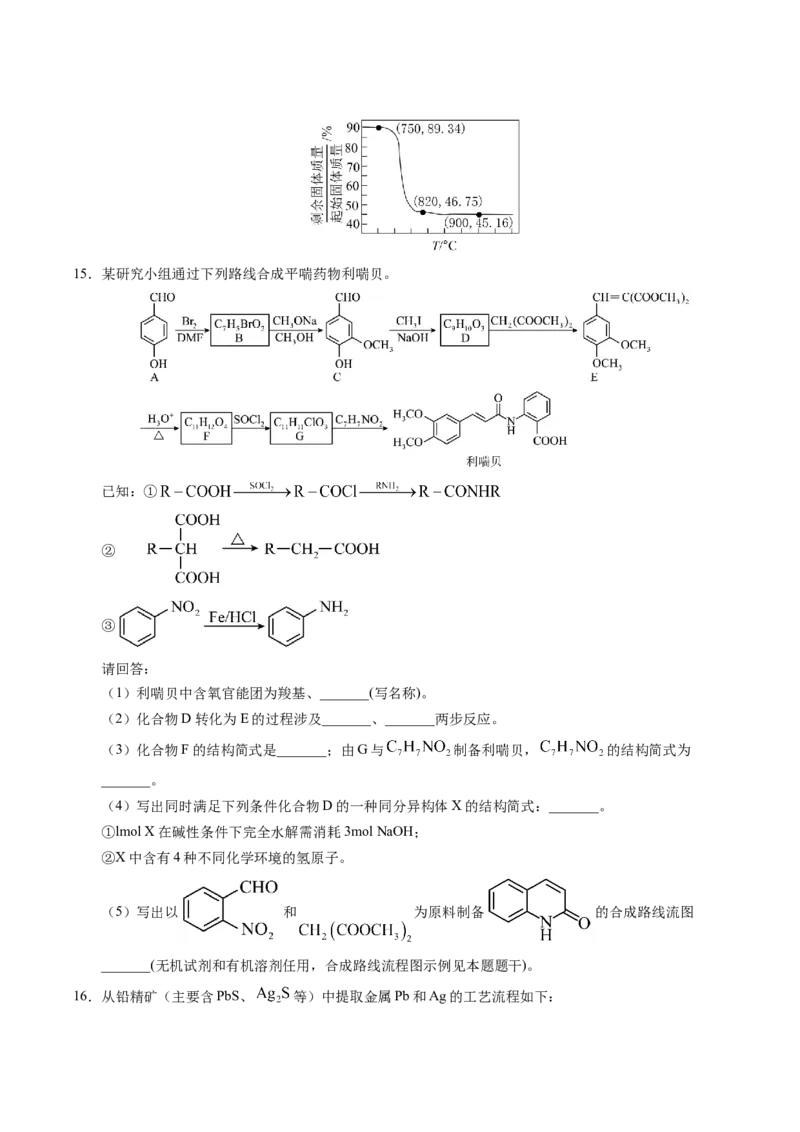
(4)将提纯后的 在空气中缓慢加热,测得 之间剩余
固体质量与起始固体质量比随温度变化曲线如图所示。通过计算确定820°C时得到锰氧化物的化学
式:_______。(写出计算过程)15.某研究小组通过下列路线合成平喘药物利喘贝。
已知:①
②
③
请回答:
(1)利喘贝中含氧官能团为羧基、_______(写名称)。
(2)化合物D转化为E的过程涉及_______、_______两步反应。
(3)化合物F的结构简式是_______;由G与 制备利喘贝, 的结构简式为
_______。
(4)写出同时满足下列条件化合物D的一种同分异构体X的结构简式:_______。
①lmol X在碱性条件下完全水解需消耗3mol NaOH;
②X中含有4种不同化学环境的氢原子。
(5)写出以 和 为原料制备 的合成路线流图
_______(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
16.从铅精矿(主要含PbS、 等)中提取金属Pb和Ag的工艺流程如下:(1)“热浸”时,难溶的PbS和 转化为 和 及单质硫。
①写出 转化为 的离子方程式:__________。
②浸取液中盐酸的浓度不宜过大,除防止“热浸”时HCl挥发外,另一目的是防止产生__________(填
化学式)。
(2)“过滤Ⅰ”得到的滤液经“稀释、冷却”得到 沉淀,再经“过滤Ⅱ”将 沉淀分离。
沉淀反复用饱和食盐水“热溶”,所得溶液经“电解Ⅰ”可获得金属Pb。
①“过滤Ⅰ”得到的滤液经“稀释”可得到 沉淀,其原因是__________。
②“电解Ⅰ”的阳极产物用“尾液”吸收所得的吸收液,可直接用于此工艺中的__________(填题干工艺
流程方框中的操作名称),从而实现循环利用。
(3)“还原”中加入铅精矿的目的是__________。
(4)经“置换”得到的富银铅泥主要为金属Pb和Ag的混合物。
①“置换”中可选用的试剂X为__________(填序号)。
A.Al B.Zn C.Pb D.Ag
②补充完整运用电解原理分离金属Pb和Ag的实验方案:将富银铅泥压实制成块状,__________。
17.用烟气中SO 制S是一种重要的脱硫技术。
2
(1)用电解法将 SO 转化为S的原理如图所示。
2
电极a表面的电极反应式为___________。随稀硫酸的浓度增大,SO 转化率先增大后减小的可能原因
2
为___________。
(2)利用乙烯与 SO 反应制S的机理如图所示,Cu⁺的基态核外电子排布式___________,此过程总
2
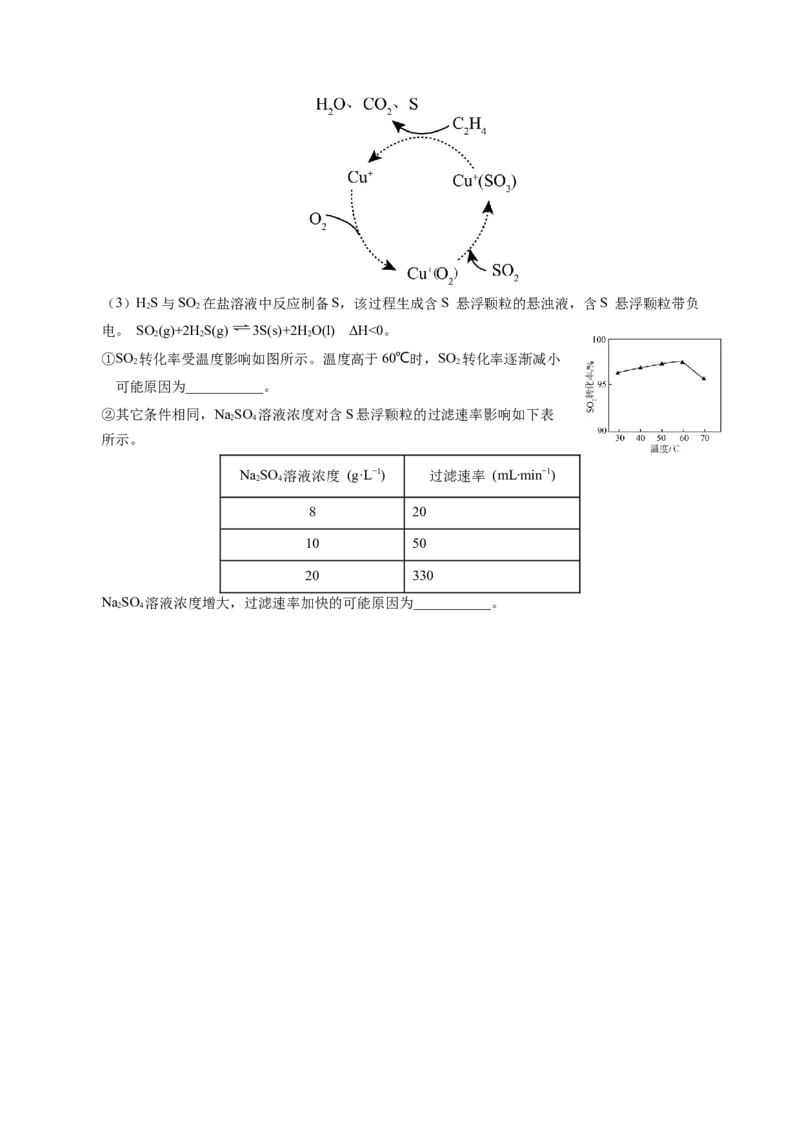
反应的化学方程式为___________。(3)HS与SO 在盐溶液中反应制备S,该过程生成含S 悬浮颗粒的悬浊液,含S 悬浮颗粒带负
2 2
电。 SO (g)+2HS(g) 3S(s)+2H O(l) ΔH<0。
2 2 2
①SO 转化率受温度影响如图所示。温度高于60℃时,SO 转化率逐渐减小
2 2
的可能原因为___________。
②其它条件相同,NaSO 溶液浓度对含S悬浮颗粒的过滤速率影响如下表
2 4
所示。
NaSO 溶液浓度 (g·L−1) 过滤速率 (mL∙min−1)
2 4
8 20
10 50
20 330
NaSO 溶液浓度增大,过滤速率加快的可能原因为___________。
2 4