文档内容
微专题28 有关工艺流程和实验探究方程式的书写
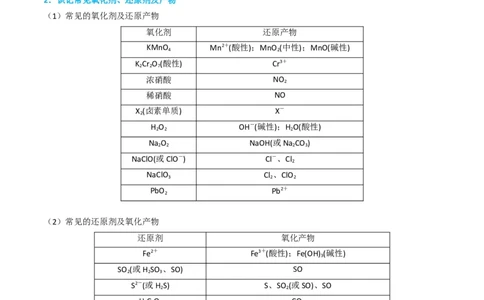
1.(2023·全国·统考高考真题)LiMn O 作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO ,
2 4 3
含有少量Si、Fe、Ni、Al等元素)制备LiMn O 的流程如下:
2 4
已知:K [Fe(OH) ]=2.8×10-39,K [Al(OH) ]=1.3×10-33,K [Ni(OH) ]=5.5×10-16。
sp 3 sp 3 sp 2
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为 。为提高溶矿速率,可采取的措施 (举1例)。
(2)加入少量MnO 的作用是 。不宜使用H O 替代MnO ,原因是 。
2 2 2 2
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)= mol·L-1;用石灰乳调节至pH≈7,除去的金属
离子是 。
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有 。
(5)在电解槽中,发生电解反应的离子方程式为 。随着电解反应进行,为保持电解液成分稳定,应
不断 。电解废液可在反应器中循环利用。(6)煅烧窑中,生成LiMn O 反应的化学方程式是 。
2 4
2.(2023·全国·统考高考真题) 是一种压电材料。以 为原料,采用下列路线可制备粉状
。
回答下列问题:
(1)“焙烧”步骤中碳粉的主要作用是 。
(2)“焙烧”后固体产物有 、易溶于水的 和微溶于水的 。“浸取”时主要反应的离子方程式为
。
(3)“酸化”步骤应选用的酸是 (填标号)。
a.稀硫酸 b.浓硫酸 c.盐酸 d.磷酸
(4)如果焙烧后的产物直接用酸浸取,是否可行? ,其原因是 。
(5)“沉淀”步骤中生成 的化学方程式为 。
(6)“热分解”生成粉状钛酸钡,产生的 。
一、工艺流程和实验探究中的氧化还原方程式的书写方法
1.①细读题干寻找提纯对象,结合工艺流程示意图分析被提纯元素的存在形式及杂质的去除情况。
②细读题干寻找实验目的,通读题目中从实验步骤中了解操作步骤,结合装置分析实验过程,与实验
目的相对应。
2.确定未知反应的反应物和生成物,根据题意分析溶液环境,配平氧化还原方程式。
3.配平步骤:
第1步:根据题干信息或流程图,判断氧化剂、还原剂、氧化产物、还原产物。第2步:按“氧化剂+还原剂——氧化产物+还原产物”写出方程式,根据得失电子守恒对方程式进行配平。
第3步:根据电荷守恒和反应物的酸碱性,在方程式左边或右边补充H+、OH-或H O等。
2
第4步:根据质量守恒配平反应方程式。
一、工艺流程中的化学反应类型
化学反应最常见的考试形式为新情景方程式的书写,要求能够根据反应类型寻找对应的反应规律,最常见
的是溶液中的反应(离子反应),主要有四类反应:
(1)普通的复分解反应 (2)氧化还原反应
(3)配位(络合)反应 (4)双水解反应
二、化工流程中新情景方程式的书写思路
首先根据题给材料中的信息写出部分反应物和生成物的化学式,再根据反应前后元素化合价有无变化判断
反应类型:
1.元素化合价无变化则为非氧化还原反应,遵循质量守恒定律。
2.元素化合价有变化则为氧化还原反应,除遵循质量守恒外,还要遵循得失电子守恒规律。最后根据题
目要求写出化学方程式或离子方程式(需要遵循 电荷守恒规律)即可。
三、非氧化还原反应方程式的书写
非氧化还原反应主要包括三类:(1)普通的复分解反应 (2)配位(络合)反应 (3)双水解反应
1.普通的复分解反应发生的条件:
①产生水等弱电解质 ②产生难溶电解质 ③产生挥发性物质等
弱电解质、难溶弱电解质、难溶物可以引申出强酸制弱酸、沉淀转化等规律,也可以用平衡常数理解(热
力学基础)。
2.常见的配位(络合)反应
(1) AgNO + NH .H O =AgOH(沉淀)+ NH NO
3 3 2 4 3
AgOH + 2NH .H O = Ag(NH ) OH + 2H O (制银氨络合反应)
3 2 3 2 2
(2) CuSO + 2NH .H O = Cu(OH) (沉淀)+ (NH ) SO
4 3 2 2 4 2 4
Cu(OH) + 4NH .H O = [Cu(NH ) ](OH) + 4H O (制铜氨络离子)
2 3 2 3 4 2 2
(3)常见的络合物
[Ag(NH ) ]OH、[Cu(NH ) ](OH) 、[Fe(SCN) ] 、[Cu(NH ) ]SO 、K [Fe(CN) ]、Fe [Fe(CN) ] 、Na AlF
3 2 3 4 2 3 3 4 4 3 6 3 6 2 3 6
3.双水解反应Al3+、Fe3+、Mg2+与AlO、HCO、CO 、S2-等会发生双水解反应。
四、氧化还原反应方程式的书写
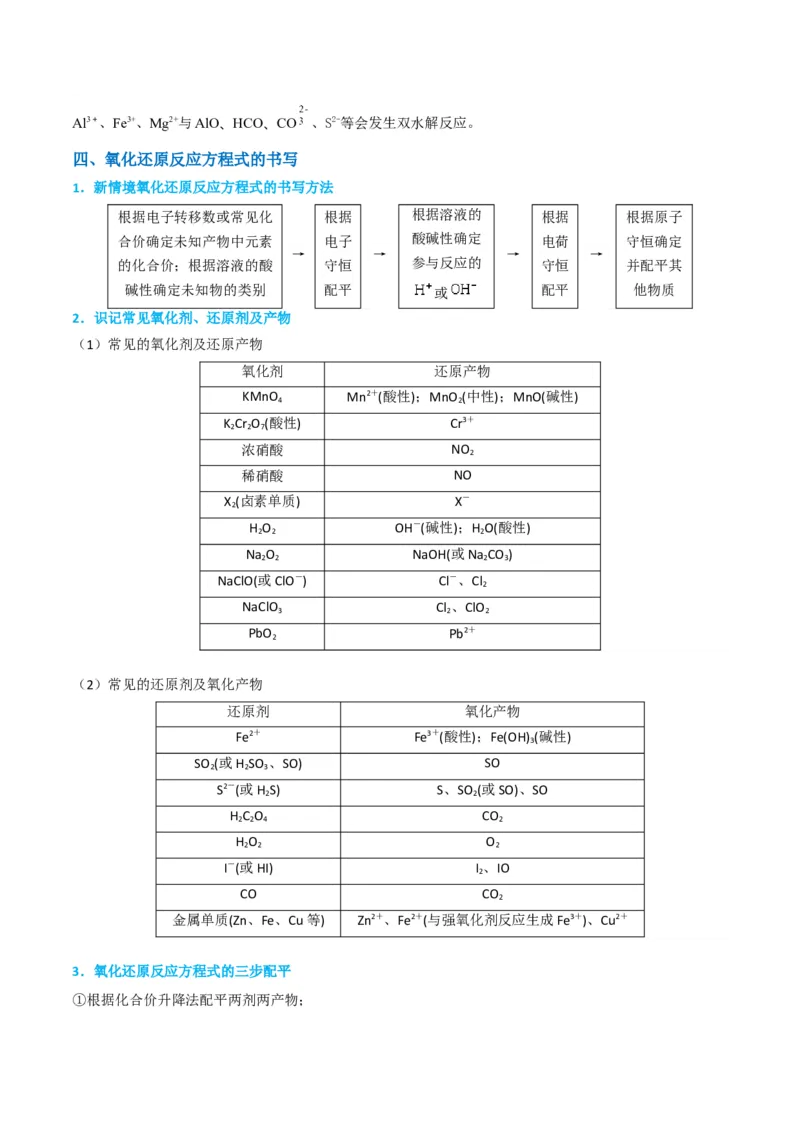
1.新情境氧化还原反应方程式的书写方法
根据电子转移数或常见化 根据 根据溶液的 根据 根据原子
合价确定未知产物中元素 电子 酸碱性确定 电荷 守恒确定
→ → → →
的化合价;根据溶液的酸 守恒 参与反应的 守恒 并配平其
碱性确定未知物的类别 配平 或 配平 他物质
2.识记常见氧化剂、还原剂及产物
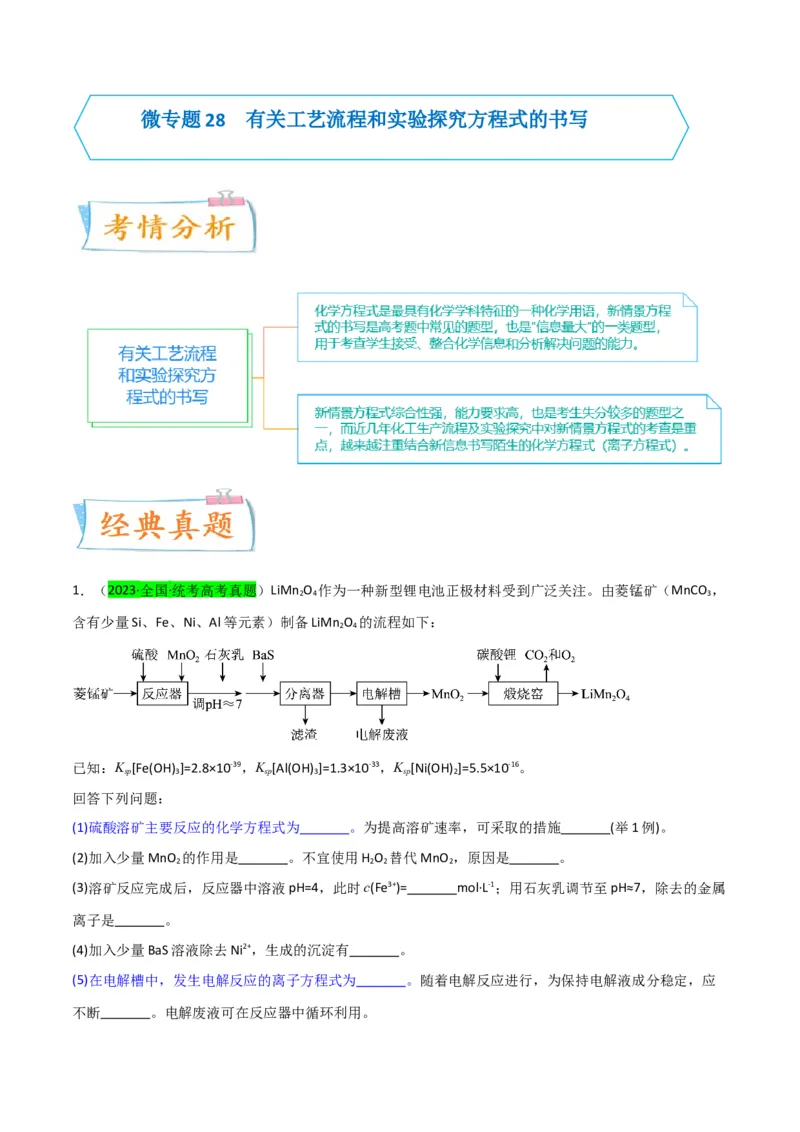
(1)常见的氧化剂及还原产物
氧化剂 还原产物
KMnO Mn2+(酸性);MnO (中性);MnO(碱性)
4 2
K Cr O (酸性) Cr3+
2 2 7
浓硝酸 NO
2
稀硝酸 NO
X (卤素单质) X-
2
H O OH-(碱性);H O(酸性)
2 2 2
Na O NaOH(或Na CO )
2 2 2 3
NaClO(或ClO-) Cl-、Cl
2
NaClO Cl 、ClO
3 2 2
PbO Pb2+
2
(2)常见的还原剂及氧化产物
还原剂 氧化产物
Fe2+ Fe3+(酸性);Fe(OH) (碱性)
3
SO (或H SO 、SO) SO
2 2 3
S2-(或H S) S、SO (或SO)、SO
2 2
H C O CO
2 2 4 2
H O O
2 2 2
I-(或HI) I 、IO
2
CO CO
2
金属单质(Zn、Fe、Cu等) Zn2+、Fe2+(与强氧化剂反应生成Fe3+)、Cu2+
3.氧化还原反应方程式的三步配平
①根据化合价升降法配平两剂两产物;②根据电荷守恒补充 H+和 OH-;
③根据原子守恒补充 H O 并配平所有原子。
2
4.“补缺”的技巧
缺项化学方程式的配平:配平化学方程式时,有时要用H+、OH-、H O来使化学方程式两边电荷及原子守
2
恒,总的原则是酸性溶液中不能出现OH-,碱性溶液中不能出现H+,具体方法如下:
酸性环境 碱性环境
反应物中少氧 左边加H O,右边加H+ 左边加OH-,右边加H O
2 2
反应物中多氧 左边加H+,右边加H O 左边加H O,右边加OH-
2 2
五、掌握氧化还原反应的常用规律
1.(2023·全国·统考高考真题)铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要
杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:已知:最高价铬酸根在酸性介质中以Cr O 存在,在碱性介质中以CrO 存在。
2
回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为 (填化学式)。
(2)水浸渣中主要有SiO 和 。
2
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是 。
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO 和MgNH PO 的形式沉淀,该步需要控制溶液的pH≈9以达到
3 4 4
最好的除杂效果,若pH<9时,会导致 ;pH>9时,会导致 。
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到V O 沉淀,V O 在pH<1时,溶解为VO 或VO3+在碱性条
2 5 2 5
件下,溶解为VO 或VO ,上述性质说明V O 具有 (填标号)。
2 5
A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na S O )溶液,反应的离子方程式为 。
2 2 5
2.(2021·江苏卷)超酸是一类比纯硫酸更强的酸,在石油重整中用作高效催化剂。某实验小组对超酸
HSbF 的制备及性质进行了探究。由三氯化锑(SbCl )制备HSbF 的反应如下: 、
6 3 6
SbCl +6HF=HSbF +5HCl。制备SbCl 的初始实验装置如图(毛细管连通大气,减压时可吸人极少量空气,防止
5 6 5
液体暴沸;夹持、加热及搅拌装置略):
相关性质如表:
物质 熔点 沸点 性质
SbCl 73.4℃ 220.3℃ 极易水解
3SbCl 3.5℃ 140℃分解79℃/2.9kPa 极易水解
5
回答下列问题:
(1)实验小组在由SbCl 制备HSbF 时,没有选择玻璃仪器,其原因为___。(写化学反应方程式)
5 6
(2)为更好地理解超酸的强酸性,实验小组查阅相关资料了解到:弱酸在强酸性溶剂中表现出碱的性质,如
冰醋酸与纯硫酸之间的化学反应方程式为CH COOH+H SO =[CH C(OH) ]+[HSO ]-。以此类推,H SO 与HSbF 之
3 2 4 3 2 4 2 4 6
间的化学反应方程式为___。
(3)实验小组在探究实验中发现蜡烛可以溶解于HSbF 中,同时放出氢气。已知烷烃分子中碳氢键的活性大
6
小顺序为:甲基(—CH )<亚甲基(—CH —)<次甲基( )。写出2—甲基丙烷与HSbF 反应的离子方程式
3 2 6
___。
3.(2021·北京卷)用如图方法回收废旧CPU中的单质Au(金),Ag和Cu。
已知:①浓硝酸不能单独将Au溶解。②HAuCl =H++AuCl
4
(1)酸溶后经____操作,将混合物分离。
(2)浓、稀HNO 均可作酸溶试剂。溶解等量的Cu消耗HNO 的物质的量不同,写出消耗HNO 物质的量少的
3 3 3
反应的化学方程式:____。
(3)HNO -NaCl与王水[V(浓硝酸):V(浓盐酸)=1:3溶金原理相同。
3
①将溶金反应的化学方程式补充完整:
Au+____NaCl+____HNO =HAuCl +____+____+____NaNO
3 4 3
②关于溶金的下列说法正确的是____。
A.用到了HNO 的氧化性
3
B.王水中浓盐酸的主要作用是增强溶液的酸性
C.用浓盐酸与NaNO 也可使Au溶解
31.(2023·北京·统考高考真题)以银锰精矿(主要含 、 、 )和氧化锰矿(主要含 )为原料
联合提取银和锰的一种流程示意图如下。
已知:酸性条件下, 的氧化性强于 。
(1) “浸锰”过程是在 溶液中使矿石中的锰元素浸出,同时去除 ,有利于后续银的浸出:矿石中
的银以 的形式残留于浸锰渣中。
①“浸锰”过程中,发生反应 ,则可推断: (填“>”或“<”)
。
②在 溶液中,银锰精矿中的 和氧化锰矿中的 发生反应,则浸锰液中主要的金属阳离子有
。
(2) “浸银”时,使用过量 和 的混合液作为浸出剂,将 中的银以 形式浸出。
①将“浸银”反应的离子方程式补充完整: 。
②结合平衡移动原理,解释浸出剂中 的作用: 。
(3) “沉银”过程中需要过量的铁粉作为还原剂。
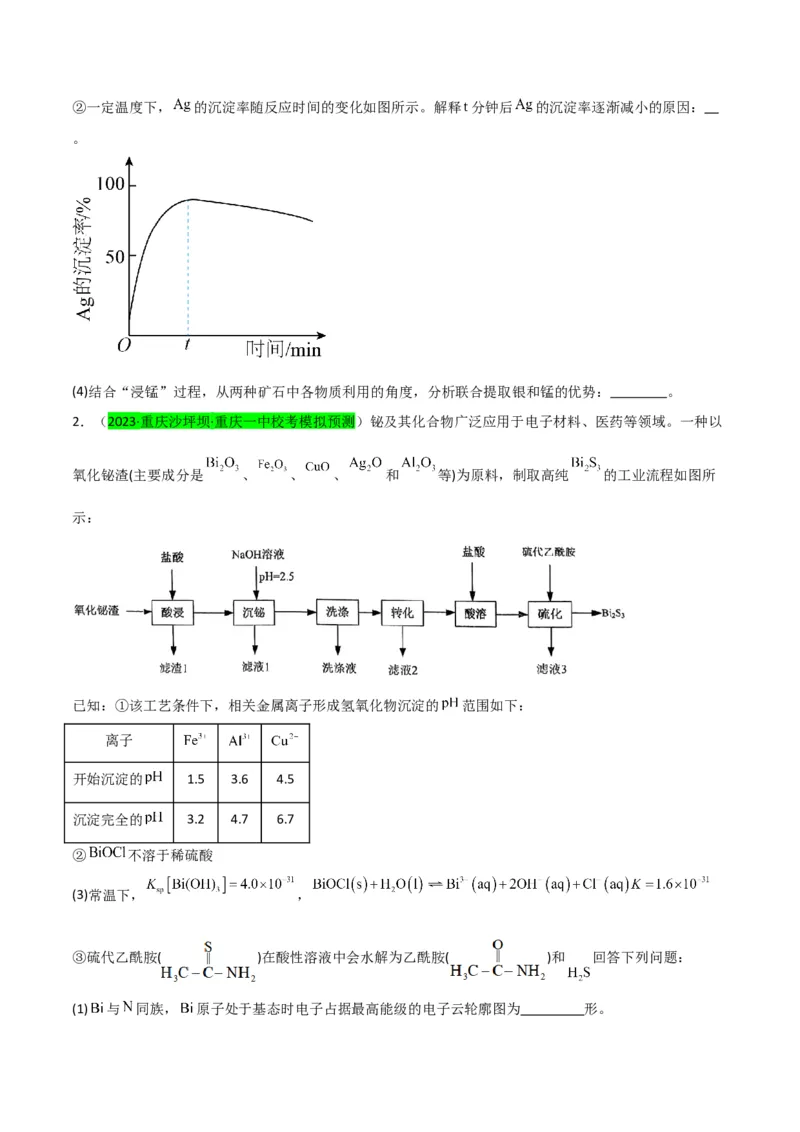
①该步反应的离子方程式有 。②一定温度下, 的沉淀率随反应时间的变化如图所示。解释 分钟后 的沉淀率逐渐减小的原因:
。
(4)结合“浸锰”过程,从两种矿石中各物质利用的角度,分析联合提取银和锰的优势: 。
2.(2023·重庆沙坪坝·重庆一中校考模拟预测)铋及其化合物广泛应用于电子材料、医药等领域。一种以
氧化铋渣(主要成分是 、 、 、 和 等)为原料,制取高纯 的工业流程如图所
示:
已知:①该工艺条件下,相关金属离子形成氢氧化物沉淀的 范围如下:
离子
开始沉淀的 1.5 3.6 4.5
沉淀完全的 3.2 4.7 6.7
② 不溶于稀硫酸
(3)常温下, ,
③硫代乙酰胺( )在酸性溶液中会水解为乙酰胺( )和 回答下列问题:
(1) 与 同族, 原子处于基态时电子占据最高能级的电子云轮廓图为 形。(2)“滤渣1”的主要成分为 (填化学式)。
(3)“沉铋”时, 转化为 沉淀。往“滤液1”中加入铁粉,可回收其中的 金属。
(4)“洗涤”时先用水洗,再用稀硫酸洗涤。用稀硫酸洗涤的目的是 。
(5)“转化”分两步进行:
第一步,用 溶液将 转化为 。常温下,当该过程达到平衡状态时,测得溶液的 ,
则此时溶液中 ;
第二步 受热分解为 。
(6)“酸溶”工序通常会加入过量的盐酸,其作用为:①充分溶出 ;② 。
(7)从“滤液3”中分离出乙酰胺以后,可返回“酸溶”或“酸浸”工序中循环使用,则“硫化”过程的化学
方程式为 。
3.(2023·广东汕头·金山中学校考三模)钒的用途十分广泛,有金属“维生素”之称。以含钒石煤(主要成
分为 、 ,杂质有 、 及 、 、 等化合物)制备单质钒的工艺流程如图所示。
已知:
①该工艺条件下,溶液中金属离子开始沉淀时和完全沉淀时的 如下表所示:
金属离子
开始沉淀时 1.9 7.0 3.0 8.1
完全沉底时 3.2 9.0 4.7 10.1
② , , 远大于 。
回答下列问题:
(1)为了提高“焙烧”效率,可采取的措施有 、
(2)“焙烧”时, 、 都转化为 ,写出 转化为 的化学方程式为(3)“水浸”加入 调节溶液的 为8.5,可完全除去的金属离子有 ,部分除去的金属离
子有 。“水浸”加入过量 不能使 完全转化为 ,原因是 。
(4)“离子交换”与“洗脱”可表示为 ( 为强碱性阴离子交换树脂,
为 在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用
(5)“沉钒”过程析出 晶体,需要加入过量 ,目的是 。
(6)钒的某种氧化物的晶胞结构如图所示,晶胞的长、宽、高分别是apm、bpm、cpm,阿伏加德罗常数的
值为 ,则该晶体的密度为 (用含a、b、c、 的代数式表示)。
4.(2023·北京顺义·北京市顺义区第一中学校考模拟预测)钛白粉学名二氧化钛(TiO )是性能最佳、应用最
2
广、用量最大的白色颜料。钛铁矿(FeTiO )中往往含有Fe O 、MgO、CaO、Al O 、SiO 等杂质。一种硫酸法
3 2 3 2 3 2
钛白粉生产工艺如图:
已知:
①酸解后,钛主要以 形式存在。强电解质 在溶液中仅能电离出 和一种阳离子。
② 不溶于水和稀酸。
(1)写出基态Ti原子的价层电子排布式 。(2)磨矿的目的是 。
(3)滤渣①的主要成分是 。
(4)酸解过程中,写出 发生反应的化学方程式 。
(5)还原过程中,加入铁粉的目的是还原体系中的 。为探究最佳反应条件,某实验室做如下尝试:
①在其它条件不变的情况下。体系中Fe(Ⅲ)含量随pH变化如图,试分析在pH介于4~6之间时,Fe(Ⅲ)含
量基本保持不变的原因: 。
②保持其它条件不变的情况下,体系中Fe(Ⅲ)含量随温度变化如图,55℃后,Fe(Ⅲ)含量增大的原因是因为
温度升高, 易被体系中的 氧化,写出反应的离子方程式 。
(6)水解过程是硫酸法制钛白工艺中的重要一步:
①水解过程中得到沉淀③的离子方程式为 。
②一定量 的存在有利于水解工艺的进行,因此在水解之前,先要测定钛液中 的含量。实验室常用
酸性高锰酸钾溶液进行滴定,用离子方程式表示其原理 。
5.(2021·全国乙卷)磁选后的炼铁高钛炉渣,主要成分有 、 、 、 、 以及少量
的 。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。该工艺条件下,有关金属离子开始沉淀和沉淀完全的 见下表
金属离子
开始沉淀的 2.2 3.5 9.5 12.4
沉淀完全 的
3.2 4.7 11.1 13.8
回答下列问题:
(1)“焙烧”中, 、 几乎不发生反应, 、 、 、 转化为相应的硫酸盐,写出
转化为 的化学方程式_______。
(2)“水浸”后“滤液”的 约为2.0,在“分步沉淀”时用氨水逐步调节 至11.6,依次析出的金属离子
是_______。
(3)“母液①"中 浓度为_______ 。
(4)“水浸渣”在160℃“酸溶”最适合的酸是_______。“酸溶渣”的成分是_______、_______。
(5)“酸溶”后,将溶液适当稀释并加热, 水解析出 沉淀,该反应的离子方程式是_______。
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得_______,循环利用。
6.(2021·河北卷)绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相
氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,
实现了Cr—Fe—Al—Mg的深度利用和Na+内循环。工艺流程如图:回答下列问题:
(1)高温连续氧化工序中被氧化的元素是_______(填元素符号)。
(2)工序①的名称为__。
(3)滤渣I的主要成分是__(填化学式)。
(4)工序③中发生反应的离子方程式为_______。
(5)物质V可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为__,可代替NaOH的
化学试剂还有_______(填化学式)。
(6)热解工序产生的混合气体最适宜返回工序_______(填“①”或“②”或“③”或“④”)参与内循环。
(7)工序④溶液中的铝元素恰好完全转化为沉淀的pH为__。(通常认为溶液中离子浓度小于10-5mol•L-1为沉
淀完全;A1(OH) +OH- Al(OH) :K=100.63,K =10-14,K [A1(OH) ]=10-33)
3 w sp 3
⇌
7.(2023·山东·统考高考真题)三氯甲硅烷 是制取高纯硅的重要原料,常温下为无色液体,沸点
为 ,熔点为 ,易水解。实验室根据反应 ,利用如下装置制备
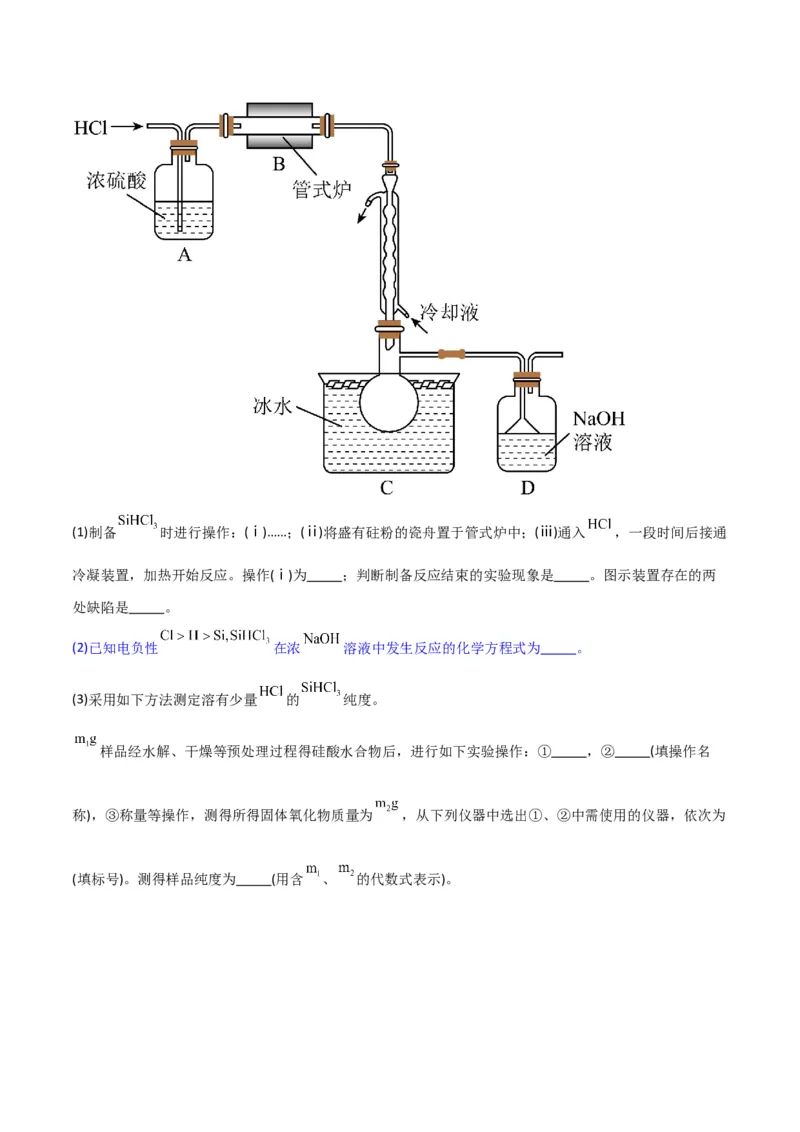
粗品(加热及夹持装置略)。回答下列问题:(1)制备 时进行操作:(ⅰ)……;(ⅱ)将盛有砫粉的瓷舟置于管式炉中;(ⅲ)通入 ,一段时间后接通
冷凝装置,加热开始反应。操作(ⅰ)为 ;判断制备反应结束的实验现象是 。图示装置存在的两
处缺陷是 。
(2)已知电负性 在浓 溶液中发生反应的化学方程式为 。
(3)采用如下方法测定溶有少量 的 纯度。
样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:① ,② (填操作名
称),③称量等操作,测得所得固体氧化物质量为 ,从下列仪器中选出①、②中需使用的仪器,依次为
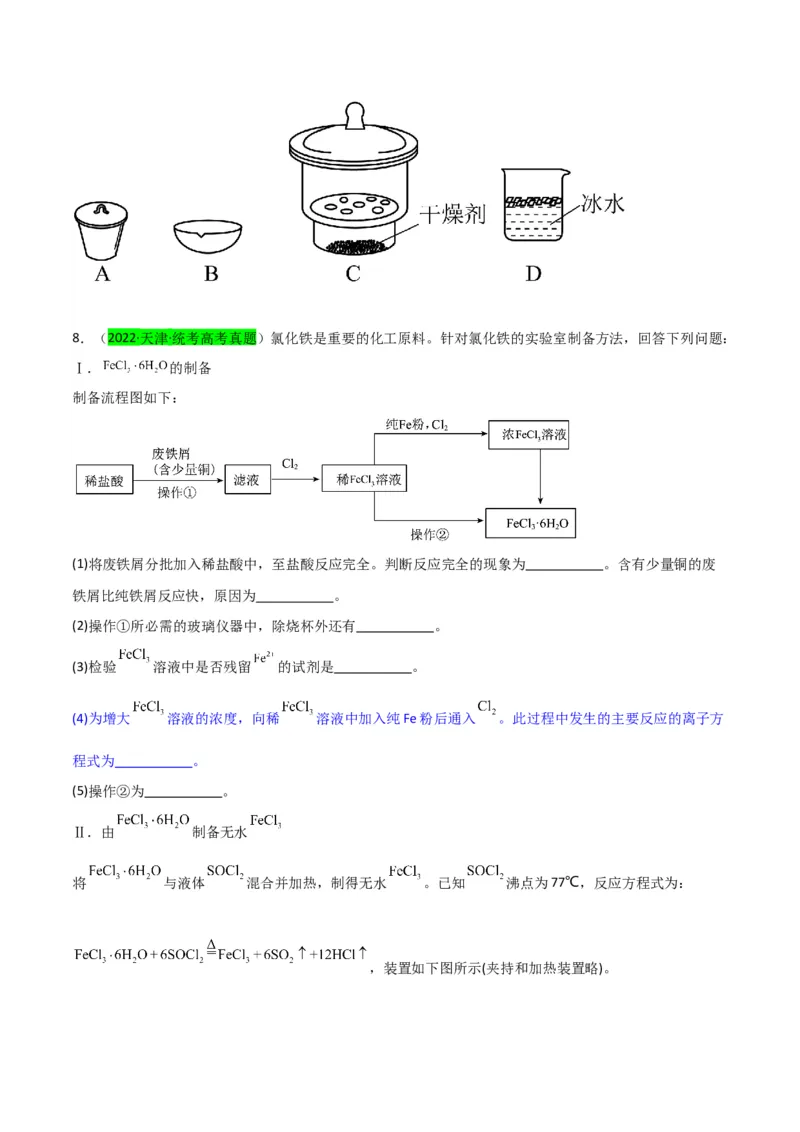
(填标号)。测得样品纯度为 (用含 、 的代数式表示)。8.(2022·天津·统考高考真题)氯化铁是重要的化工原料。针对氯化铁的实验室制备方法,回答下列问题:
Ⅰ. 的制备
制备流程图如下:
(1)将废铁屑分批加入稀盐酸中,至盐酸反应完全。判断反应完全的现象为 。含有少量铜的废
铁屑比纯铁屑反应快,原因为 。
(2)操作①所必需的玻璃仪器中,除烧杯外还有 。
(3)检验 溶液中是否残留 的试剂是 。
(4)为增大 溶液的浓度,向稀 溶液中加入纯Fe粉后通入 。此过程中发生的主要反应的离子方
程式为 。
(5)操作②为 。
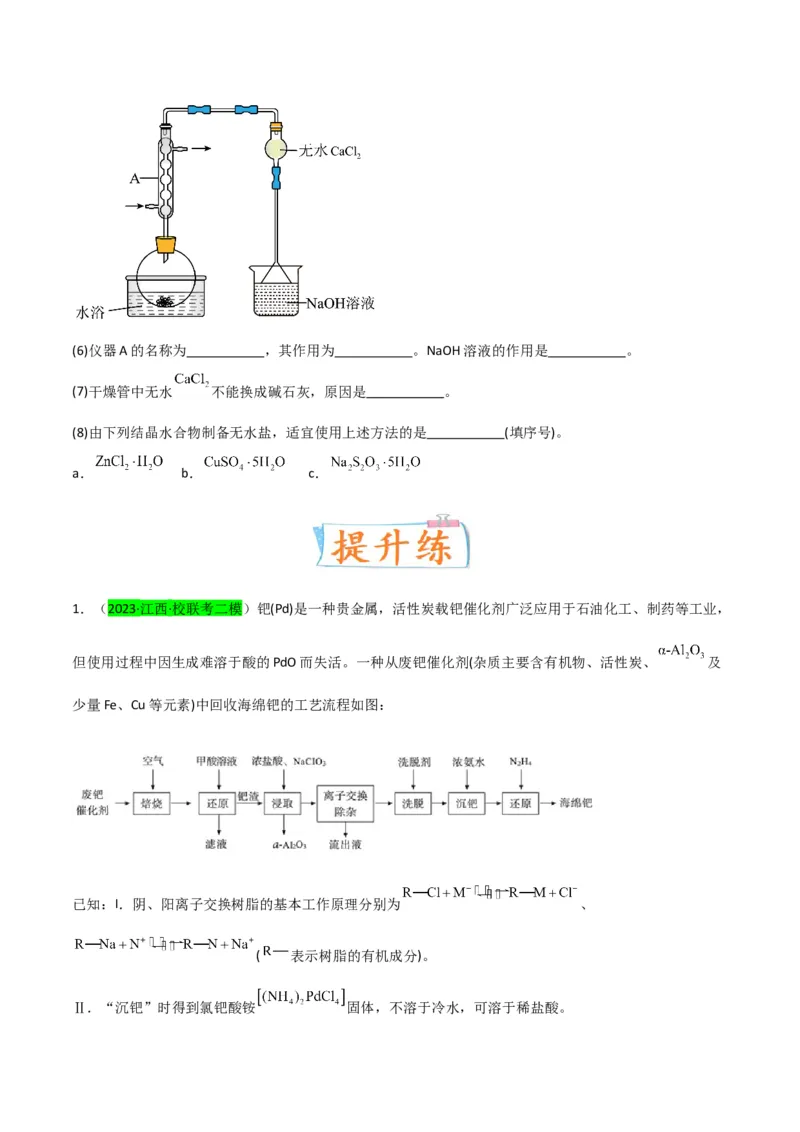
Ⅱ.由 制备无水
将 与液体 混合并加热,制得无水 。已知 沸点为77℃,反应方程式为:
,装置如下图所示(夹持和加热装置略)。(6)仪器A的名称为 ,其作用为 。NaOH溶液的作用是 。
(7)干燥管中无水 不能换成碱石灰,原因是 。
(8)由下列结晶水合物制备无水盐,适宜使用上述方法的是 (填序号)。
a. b. c.
1.(2023·江西·校联考二模)钯(Pd)是一种贵金属,活性炭载钯催化剂广泛应用于石油化工、制药等工业,
但使用过程中因生成难溶于酸的PdO而失活。一种从废钯催化剂(杂质主要含有机物、活性炭、 及
少量Fe、Cu等元素)中回收海绵钯的工艺流程如图:
已知:I.阴、阳离子交换树脂的基本工作原理分别为 、
( 表示树脂的有机成分)。
Ⅱ.“沉钯”时得到氯钯酸铵 固体,不溶于冷水,可溶于稀盐酸。请回答下列问题:
(1)进行“焙烧”的目的是 。
(2)“浸取”时,加入 有利于Pd的溶解,生成的四氯合钯(Ⅱ)酸( )为二元强酸。加入浓盐酸
和 后主要反应的离子方程式: 。
(3)“离子交换除杂”应使用 (填“阳离子”或“阴离子”)树脂。
(4)“还原”过程 转化为 ,在反应器出口处器壁内侧有白色晶体生成,该过程发生的化学方程式为
,且该反应的副产物可循环利用至 环节(填环节名称)。
(5)研究表明有些过渡金属型氢化物能高效的储存和输送氢能源,如LaH 、TiH ,已知标准状况下,1体
2.76 1.73
积的钯粉大约可吸附896体积的氢气(钯粉的密度为10.64g·cm-3,相对原子质量为106.4),试写出钯(Pd)的
氢化物的化学式 。在第二步还原过程中,也可用 代替N H 进行热还原,但消耗的H 质量比理论
2 4 2
值略高,其原因是 。
2.(2023·云南·校联考二模)六水合氯化镍(NiCl ·6H O)常用于电镀、陶瓷等工业。某实验室以镍矿渣(主要
2 2
含NiS、CuS、FeS)制备六水合氯化镍晶体,设计流程如图所示:
已知: K (NiS)= 1.07×10-21, K (CuS)= 1.27×10-26。
sp sp
回答下列问题:
(1)①写出“酸溶”时,NiS发生反应的离子方程式: 。
②“酸溶”时,为减少生产过程对大气的污染,通常还需通入过量的 (填气体名称)。
(2)试剂a应选用下列物质中的_______(填标号)。
A.NaOH B.Ni(OH)
2
C.Na CO D.Ni(NO )
2 3 3 2
(3)“除铜”过程发生反应的离子方程式是 ,若要求溶液中Cu2+浓度小于1×10-5mol/L,则应控制溶液
中Ni2+浓度 。(结果保留两位小数)
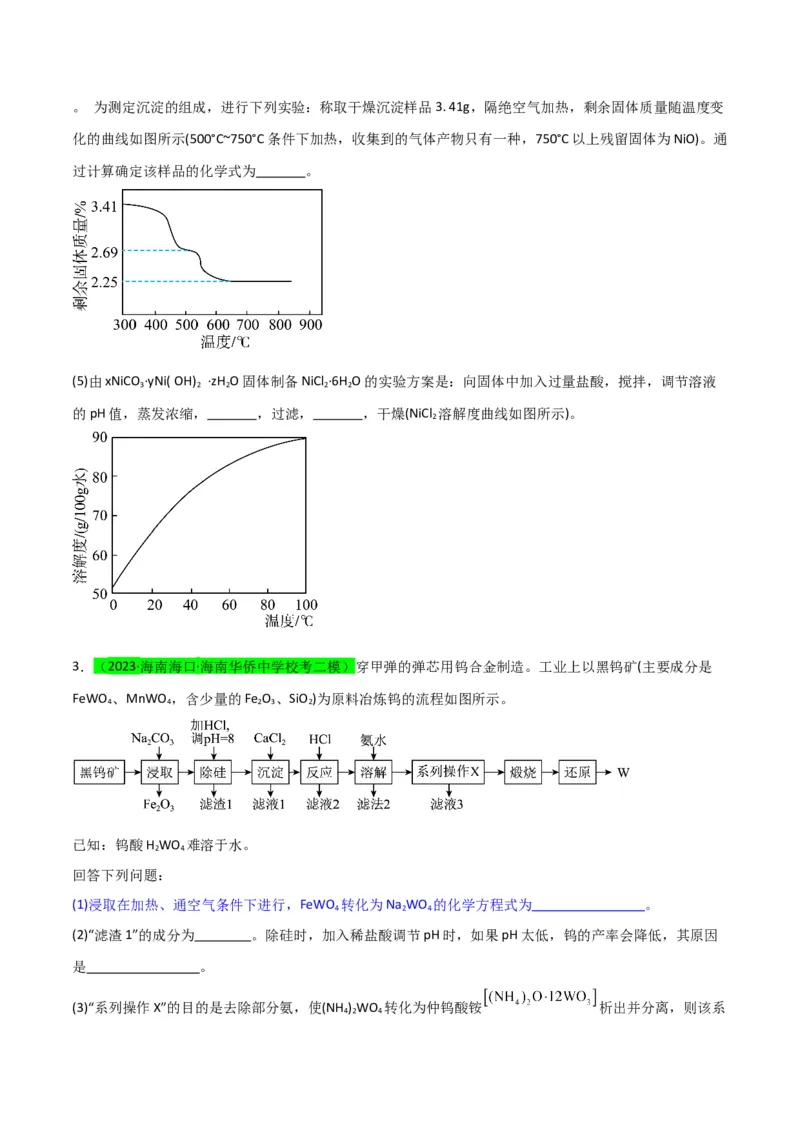
(4)“沉镍”所得沉淀有多种组成,可表示为xNiCO ·yNi( OH) ·zH O,若试剂b为纯净物,试剂b可以是
3 2 2。 为测定沉淀的组成,进行下列实验:称取干燥沉淀样品3. 41g,隔绝空气加热,剩余固体质量随温度变
化的曲线如图所示(500°C~750°C条件下加热,收集到的气体产物只有一种,750°C以上残留固体为NiO)。通
过计算确定该样品的化学式为 。
(5)由xNiCO ·yNi( OH) ·zH O固体制备NiCl ·6H O的实验方案是:向固体中加入过量盐酸,搅拌,调节溶液
3 2 2 2 2
的pH值,蒸发浓缩, ,过滤, ,干燥(NiCl 溶解度曲线如图所示)。
2
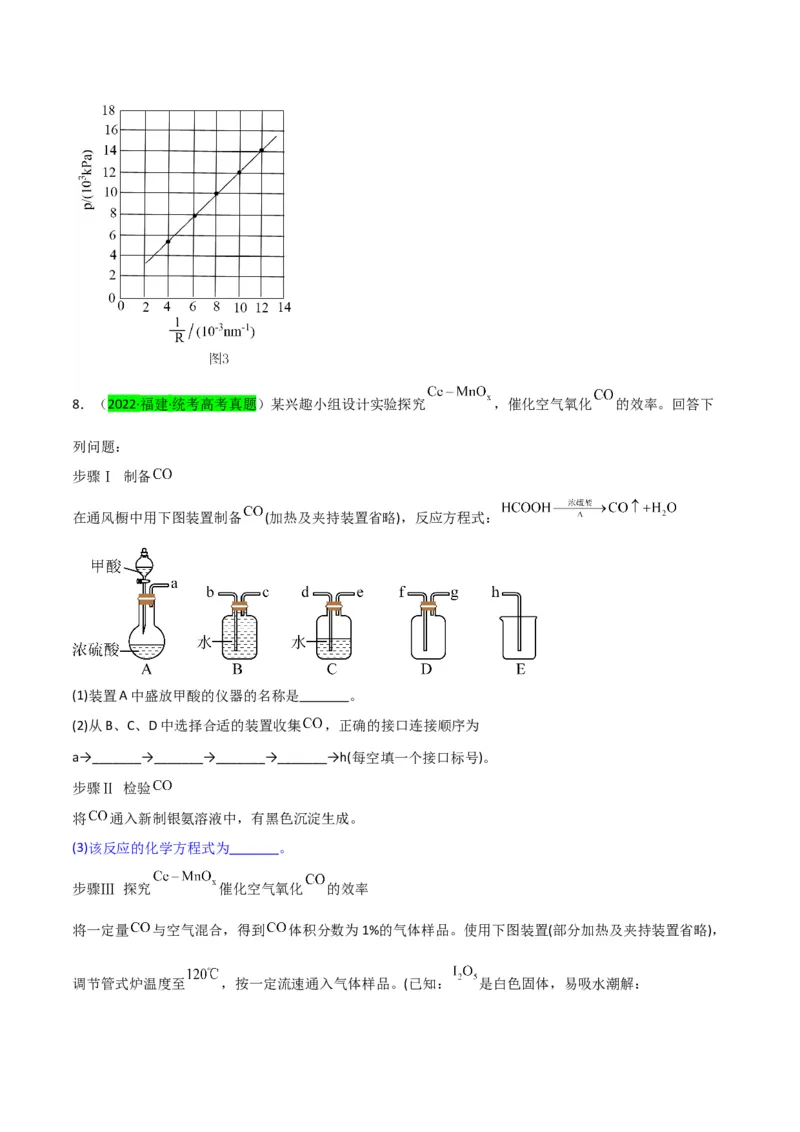
3.(2023·海南海口·海南华侨中学校考二模)穿甲弹的弹芯用钨合金制造。工业上以黑钨矿(主要成分是
FeWO 、MnWO ,含少量的Fe O 、SiO )为原料冶炼钨的流程如图所示。
4 4 2 3 2
已知:钨酸H WO 难溶于水。
2 4
回答下列问题:
(1)浸取在加热、通空气条件下进行,FeWO 转化为Na WO 的化学方程式为 。
4 2 4
(2)“滤渣1”的成分为 。除硅时,加入稀盐酸调节pH时,如果pH太低,钨的产率会降低,其原因
是 。
(3)“系列操作X”的目的是去除部分氨,使(NH ) WO 转化为仲钨酸铵 析出并分离,则该系
4 2 4列操作是 。
(4)已知:含大量钨酸钙固体的溶液中存在 。 时,
,当温度升高至 时, ,则 (填“ ”“ ”或“ ”)0。
4.(2023·陕西商洛·统考三模)固体电解质LATP的化学式为Li Al Ti (PO ) ,某研究人员以钛铁矿精粉
1.4 0.4 1.6 4 3
(主要成分为FeTiO ,含少量Al O ,SiO )为原料合成LATP的工艺流程如图所示。
3 2 3 2
请回答下列问题:
(1)LATP中钛的化合价为 价。
(2)“粉碎”的目的是 ,为了达到这一目的,还可以采用的措施有 (答一条即可)。
(3)“碱浸”的目的是除去 (填化学式)。
(4)“碱浸”时加入适当过量的NaOH溶液,“酸浸”时加入适当过量的稀硫酸,且NaOH溶液和稀硫酸均不
宜过量太多,其主要原因是 。
(5)“沉钛”时生成Ti (PO ) 的化学方程式为 。
3 4 4
(6)本实验洗涤Ti (PO ) 时采用如图所示装置,该装置为抽滤装置,其原理是用抽气泵使吸滤瓶中的压强降
3 4 4
低,达到快速固液分离的目的。其中“安全瓶”的作用是 。
(7)常温下,Ti (PO ) 的K =a,当溶液中c(Ti4+)≤1.0×10-5mol·L-1时可认为Ti4+沉淀完全,则“沉钛”时,溶液
3 4 4 sp
中c( )最低为 mol·L-1。5.(2023·山东潍坊·统考三模) 可用于油漆颜料及羊毛处理。工业上以高铁铬铁矿(主要成分为
,含 、 、 等杂质)为原料生产 和金属Al的工艺流程如图。
已知:
I.“焙烧”过程中, 反应转化为
Ⅱ.若溶液中相关离子的物质的量浓度为c,则常温时,lgc与溶液pH的关系如图所示。
Ⅲ. (黄色) (橙色) 。
回答下列问题:
(1)“焙烧”时, 发生反应的化学方程式为 。
(2)“水浸”后滤渣主要成分为 (填化学式);“调pH”时通入的“气体X”是 。
(3)常温下,图像上M点对应的溶液 。
(4)用稀硫酸进行“酸浸”,调节溶液pH的最大值为 。“沉铝”后
的母液Ⅱ的主要成分为 。(5)加入 “析铬”时, 被还原的离子方程式为 。
6.(2023·湖南邵阳·统考三模)金属钒主要用于冶炼特种钢,被誉为“合金的维生素”。人们在化工实践
中,以富钒炉渣(其中的钒以FeO•V O 、V O 等形式存在,还有少量的SiO 、Al O 等)为原料提取金属钒的
2 3 2 5 2 2 3
工艺流程如图所示:
提示:①钒有多种价态,其中+5价最稳定;
②V O 在碱性条件下可转化为VO 。
2 5
(1)可加快“高温氧化”速率的措施有 (填一条)。
(2)“气体X”和“气体Y”的化学式分别为 、 。
(3)“沉硅、沉铝”中得到含铝沉淀的离子方程式为 。
(4)写出“高温氧化”过程中发生反应的化学方程式 。
(5)写出“热解”时的化学方程式 。
(6)在“高温还原”反应中,氧化钙最终转化为 (写化学式)。
(7)已知:25℃时,NH •H O的电离平衡常数K =1.8×10-5,H CO 的电离平衡常数K =4.3×10-7,K =5.6×10-11,
3 2 b 2 3 a1 a2
判断NH HCO 溶液呈 (填“酸性”“碱性”或“中性”)。
4 3
7.(2022·重庆·统考高考真题)研究小组以无水甲苯为溶剂,PCl (易水解)和NaN 为反应物制备米球状红
5 3
磷。该红磷可提高钠离子电池的性能。
(1)甲苯干燥和收集的回流装置如图1所示(夹持及加热装置略)。以二苯甲酮为指示剂,无水时体系呈蓝色。①存贮时,Na应保存在 中。
②冷凝水的进口是 (填“a”或“b”)。
③用Na干燥甲苯的原理是 (用化学方程式表示)。
④回流过程中,除水时打开的活塞是 ;体系变蓝后,改变开关状态收集甲苯。
(2)纳米球状红磷的制备装置如图2所示(搅拌和加热装置略)。
①在Ar气保护下,反应物在A装置中混匀后转入B装置,于280℃加热12小时,反应物完全反应。其化学
反应方程式为 。用Ar气赶走空气的目的是 。
②经冷却、离心分离和洗涤得到产品,洗涤时先后使用乙醇和水,依次洗去的物质是 和 。
③所得纳米球状红磷的平均半径R与B装置中气体产物的压强p的关系如图3所示。欲控制合成R=125nm
的红磷,气体产物的压强为 kPa,需NaN 的物质的量为 mol(保留3位小数)。已知:p=a×n,其
3
中a=2.5×105kPa•mol-1,n为气体产物的物质的量。8.(2022·福建·统考高考真题)某兴趣小组设计实验探究 ,催化空气氧化 的效率。回答下
列问题:
步骤Ⅰ 制备
在通风橱中用下图装置制备 (加热及夹持装置省略),反应方程式:
(1)装置A中盛放甲酸的仪器的名称是 。
(2)从B、C、D中选择合适的装置收集 ,正确的接口连接顺序为
a→_______→_______→_______→_______→h(每空填一个接口标号)。
步骤Ⅱ 检验
将 通入新制银氨溶液中,有黑色沉淀生成。
(3)该反应的化学方程式为 。
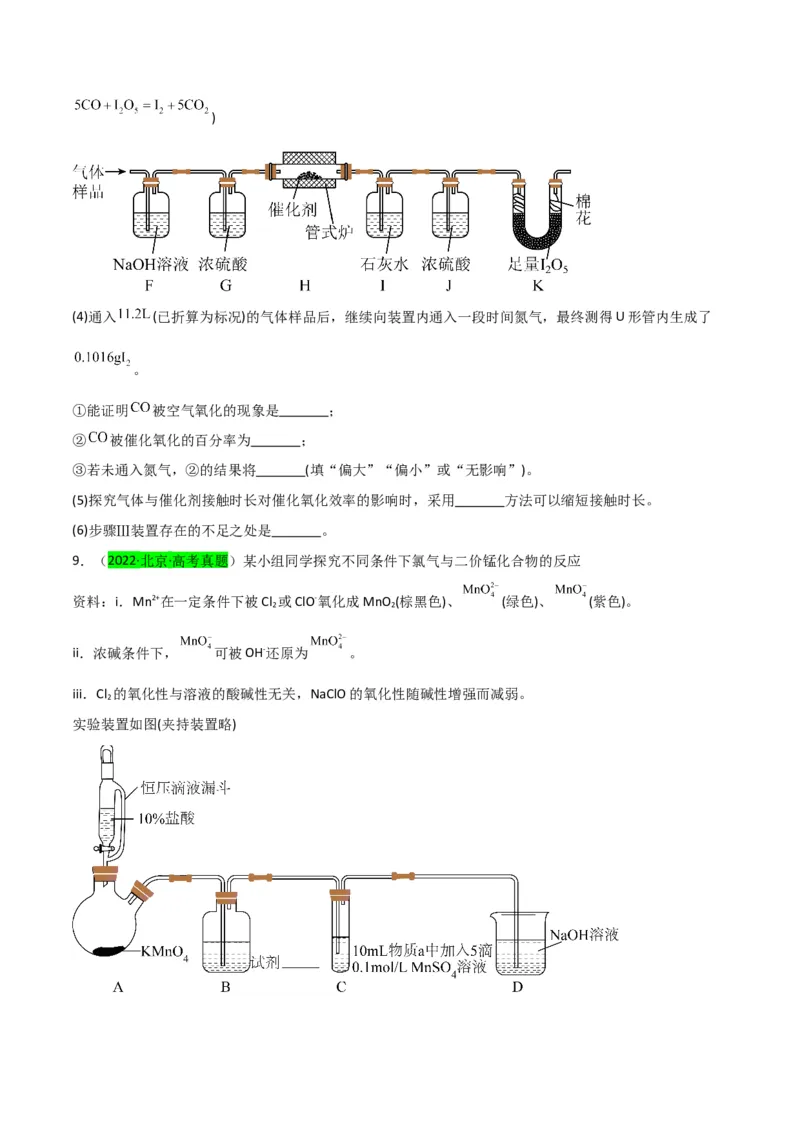
步骤Ⅲ 探究 催化空气氧化 的效率
将一定量 与空气混合,得到 体积分数为1%的气体样品。使用下图装置(部分加热及夹持装置省略),
调节管式炉温度至 ,按一定流速通入气体样品。(已知: 是白色固体,易吸水潮解:)
(4)通入 (已折算为标况)的气体样品后,继续向装置内通入一段时间氮气,最终测得U形管内生成了
。
①能证明 被空气氧化的现象是 ;
② 被催化氧化的百分率为 ;
③若未通入氮气,②的结果将 (填“偏大”“偏小”或“无影响”)。
(5)探究气体与催化剂接触时长对催化氧化效率的影响时,采用 方法可以缩短接触时长。
(6)步骤Ⅲ装置存在的不足之处是 。
9.(2022·北京·高考真题)某小组同学探究不同条件下氯气与二价锰化合物的反应
资料:i.Mn2+在一定条件下被Cl 或ClO-氧化成MnO (棕黑色)、 (绿色)、 (紫色)。
2 2
ii.浓碱条件下, 可被OH-还原为 。
iii.Cl 的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
2
实验装置如图(夹持装置略)C中实验现象
序
物质a
号
通入Cl 前 通入Cl 后
2 2
I 水 得到无色溶液 产生棕黑色沉淀,且放置后不发生变化
产生白色沉淀,在空气中缓慢变成棕 棕黑色沉淀增多,放置后溶液变为紫色,
II 5%NaOH溶液
黑色沉淀 仍有沉淀
40%NaOH 溶 产生白色沉淀,在空气中缓慢变成棕 棕黑色沉淀增多,放置后溶液变为紫色,
III
液 黑色沉淀 仍有沉淀
(1)B中试剂是 。
(2)通入Cl 前,II、III中沉淀由白色变为黑色的化学方程式为 。
2
(3)对比实验I、II通入Cl 后的实验现象,对于二价锰化合物还原性的认识是 。
2
(4)根据资料ii,III中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入Cl 导致溶液的碱性减弱。
2
原因二:可能是氧化剂过量,氧化剂将 氧化为 。
①化学方程式表示可能导致溶液碱性减弱的原因 ,但通过实验测定溶液的碱性变化很小。
②取III中放置后的1 mL悬浊液,加入4 mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶
液紫色变为绿色的离子方程式为 ,溶液绿色缓慢加深,原因是MnO 被 (填“化学
2
式”)氧化,可证明III的悬浊液中氧化剂过量;
③取II中放置后的1 mL悬浊液,加入4 mL水,溶液紫色缓慢加深,发生的反应是 。
④从反应速率的角度,分析实验III未得到绿色溶液的可能原因 。