文档内容
第 25 讲 碳、硅 无机非金属材料
[复习目标] 1.了解碳、硅及其化合物的组成和成键特点。2.了解碳、硅两种元素单质及其
重要化合物的性质及应用,能用化学方程式表示其主要化学性质。3.了解无机非金属材料的
组成、分类及其应用价值。
考点一 碳族元素 碳
1.碳族元素
(1)碳、硅、锗、锡、铅均属于第ⅣA族元素,又称碳族元素,其价层电子排布式为 n s 2 n p 2 。
(2)碳单质的存在形式有金刚石、石墨、无定形碳、足球烯,它们互为同素异形体。
2.金刚石、石墨、C 的物理性质
60
金刚石 石墨 C
60
晶体类型 共价晶体 混合型晶体 分子晶体
熔点高,硬度小,
物理性质 熔点高,硬度大,不导电 熔点低,不导电
能导电
钻石制作,切割工具,钻探 做电极、润滑剂、 广泛应用于超导、医
主要用途
机的钻头等 铅笔芯 学领域
3.CO 在自然界中的循环
2
(1)CO 的主要来源:大量含碳燃料的燃烧。(2)自然界消耗CO 的主要反应:
2 2
①溶于江水、海水中:CO+HOHCO;
2 2 2 3
②光合作用将CO 转化为O;
2 2
③岩石的风化:CaCO +HO+CO===Ca(HCO )。
3 2 2 3 2
1.金刚石、石墨、C 都是由碳元素组成的单质( )
60
2.水墨画可长久保存不变色是因为在常温下碳的化学性质不活泼( )
3.二氧化碳能使紫色石蕊溶液变红,说明二氧化碳具有酸性( )
4.低碳环保中的“碳”是指二氧化碳( )
5.石墨转变为金刚石的反应属于氧化还原反应( )
6.向空气中排放二氧化碳会形成酸雨( )7.向CaCl 溶液中通入CO 气体,溶液变浑浊,继续通入CO 至过量,浑浊消失( )
2 2 2
8.向氨化的饱和食盐水中通入足量的CO 气体,会析出晶体( )
2
答案 1.√ 2.√ 3.× 4.√ 5.× 6.× 7.× 8.√
1.中国力争在2030年前实现碳达峰、2060年前实现碳中和,关于碳及其化合物,下列说
法不正确的是( )
A.金刚石和石墨是碳元素的两种不同单质,二者互称为同素异形体
B.在100 kPa时,1 mol石墨转变为金刚石要吸收1.895 kJ的热量,故金刚石比石墨稳定
C.考古时常用于测定文物年代的是碳元素的一种核素C,该核素的中子数为8
D.引起温室效应的气体之一CO 中含极性共价键
2
答案 B
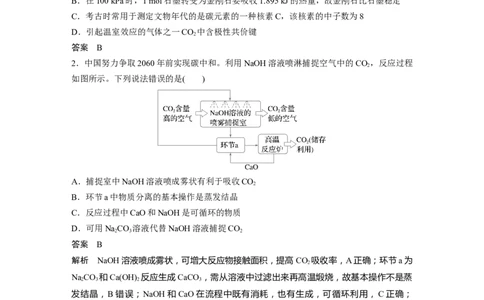
2.中国努力争取2060年前实现碳中和。利用NaOH溶液喷淋捕捉空气中的CO ,反应过程
2
如图所示。下列说法错误的是( )
A.捕捉室中NaOH溶液喷成雾状有利于吸收CO
2
B.环节a中物质分离的基本操作是蒸发结晶
C.反应过程中CaO和NaOH是可循环的物质
D.可用NaCO 溶液代替NaOH溶液捕捉CO
2 3 2
答案 B
解析 NaOH溶液喷成雾状,可增大反应物接触面积,提高CO 吸收率,A正确;环节a为
2
NaCO 和Ca(OH) 反应生成CaCO ,需从溶液中过滤出来再高温煅烧,故基本操作不是蒸
2 3 2 3
发结晶,B错误;NaOH和CaO在流程中既有消耗,也有生成,可循环利用,C正确;
NaCO 溶液可以和CO 反应,因此可用NaCO 溶液代替NaOH溶液,D正确。
2 3 2 2 3
考点二 硅及其重要化合物
1.硅的存在
自然界中硅元素仅有化合态,在地壳中含量仅次于氧,主要以氧化物和硅酸盐的形式存在。2.硅单质
(1)常温下不活泼,一般不与其他物质反应,但可以与氟、氢氟酸、碱反应。
反应的化学方程式分别为
与F:Si+2F===SiF;
2 2 4
与HF:Si+4HF===SiF↑+2H↑;
4 2
与NaOH:Si+2NaOH+HO===NaSiO+2H↑。
2 2 3 2
(2)在加热的条件下可以与氧气、氯气等反应。
(3)粗硅的制取:SiO+2C=====Si(粗)+2CO↑。
2
(4)硅单质的用途
①良好的半导体材料;②硅太阳能电池;③计算机芯片。
3.二氧化硅
(1)物理性质:硬度大,熔、沸点高,常温下为固体,不溶于水。
(2)化学性质
SiO 为酸性氧化物,是硅酸的酸酐。
2
①SiO 可以与碱反应,生成硅酸盐,如与氢氧化钠溶液反应的化学方程式为 SiO +
2 2
2NaOH===NaSiO+HO。
2 3 2
②在高温条件下可以与碳酸盐反应,如与碳酸钙反应的化学方程式为 SiO +
2
CaCO =====CaSiO +CO↑。
3 3 2
③在高温条件下,能够与碱性氧化物反应,如与氧化钙反应的化学方程式为 SiO +
2
CaO=====CaSiO 。
3
④常温下与氢氟酸反应的化学方程式为SiO+4HF===SiF↑+2HO,可用于刻蚀玻璃。
2 4 2
(3)用途:光导纤维、光学仪器、电子部件。
4.硅酸(H SiO)
2 3
5.硅酸盐
(1)硅酸盐是由硅、氧和金属组成的化合物的总称,是构成地壳岩石的主要成分。
(2)硅酸钠:硅酸钠溶液俗称水玻璃,溶液呈碱性,是无色黏稠液体,常用于制备黏合剂、
防腐剂、耐火材料。
(3)硅酸盐写成氧化物形式的顺序:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水,不同氧化物间以“·”隔开。
如,石棉(CaMg Si O )用氧化物的形式表示为CaO·3MgO·4SiO 。
3 4 12 2
1.晶体硅熔点高、硬度大,故可用于制作半导体材料( )
2.非金属性:C>Si,则热稳定性:CH>SiH( )
4 4
3.SiO 是酸性氧化物,可溶于强碱(NaOH),不溶于任何酸( )
2
4.硅酸钠的水溶液俗称“水玻璃”,是一种建筑行业常用的黏合剂( )
5.SiO 能与HF反应,因此可用HF刻蚀玻璃( )
2
6.向NaSiO 溶液中逐滴加入稀盐酸制备硅酸凝胶( )
2 3
7.石英是良好的半导体材料,可以制成光电池,将光能直接转化成电能( )
8.工业上制取粗硅的反应是SiO+C=====Si+CO↑( )
2 2
9.因为高温时二氧化硅与碳酸钠反应放出二氧化碳,所以硅酸酸性比碳酸强( )
答案 1.× 2.√ 3.× 4.√ 5.√ 6.√ 7.× 8.× 9.×
一、硅及其重要化合物转化关系落实
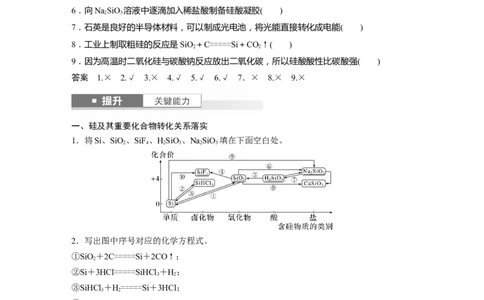
1.将Si、SiO、SiF、HSiO、NaSiO 填在下面空白处。
2 4 2 3 2 3
2.写出图中序号对应的化学方程式。
①SiO+2C=====Si+2CO↑;
2
②Si+3HCl=====SiHCl +H;
3 2
③SiHCl +H=====Si+3HCl;
3 2
④SiO+4HF===SiF↑+2HO;
2 4 2
⑤HSiO=====HO+SiO;
2 3 2 2
⑥SiO+2NaOH===NaSiO+HO(或SiO+NaCO=====NaSiO+CO↑);
2 2 3 2 2 2 3 2 3 2
⑦NaSiO+CO+HO===NaCO+HSiO↓(或NaSiO+2HCl===2NaCl+HSiO↓);
2 3 2 2 2 3 2 3 2 3 2 3
⑧SiO+CaO=====CaSiO (或SiO+CaCO =====CaSiO +CO↑);
2 3 2 3 3 2
⑨Si+2NaOH+HO===NaSiO+2H↑。
2 2 3 2
二、工业制取高纯硅问题分析
3.清华大学等重点高校为解决中国“芯”——半导体芯片,成立了“芯片学院”。某小组
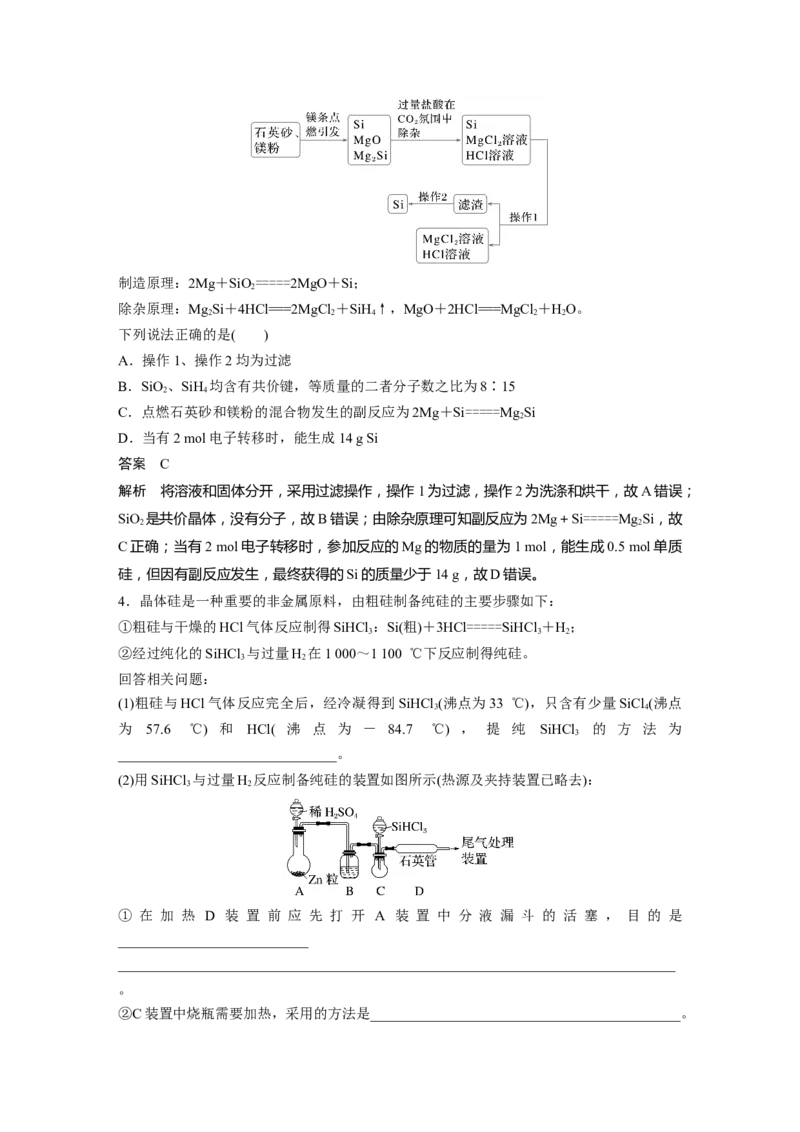
拟在实验室制造硅,其流程如图:制造原理:2Mg+SiO=====2MgO+Si;
2
除杂原理:MgSi+4HCl===2MgCl +SiH↑,MgO+2HCl===MgCl +HO。
2 2 4 2 2
下列说法正确的是( )
A.操作1、操作2均为过滤
B.SiO、SiH 均含有共价键,等质量的二者分子数之比为8∶15
2 4
C.点燃石英砂和镁粉的混合物发生的副反应为2Mg+Si=====MgSi
2
D.当有2 mol电子转移时,能生成14 g Si
答案 C
解析 将溶液和固体分开,采用过滤操作,操作1为过滤,操作2为洗涤和烘干,故A错误;
SiO 是共价晶体,没有分子,故B错误;由除杂原理可知副反应为2Mg+Si=====MgSi,故
2 2
C正确;当有2 mol电子转移时,参加反应的Mg的物质的量为1 mol,能生成0.5 mol单质
硅,但因有副反应发生,最终获得的Si的质量少于14 g,故D错误。
4.晶体硅是一种重要的非金属原料,由粗硅制备纯硅的主要步骤如下:
①粗硅与干燥的HCl气体反应制得SiHCl :Si(粗)+3HCl=====SiHCl +H;
3 3 2
②经过纯化的SiHCl 与过量H 在1 000~1 100 ℃下反应制得纯硅。
3 2
回答相关问题:
(1)粗硅与HCl气体反应完全后,经冷凝得到SiHCl (沸点为33 ℃),只含有少量SiCl (沸点
3 4
为 57.6 ℃) 和 HCl( 沸 点 为 - 84.7 ℃) , 提 纯 SiHCl 的 方 法 为
3
_______________________________。
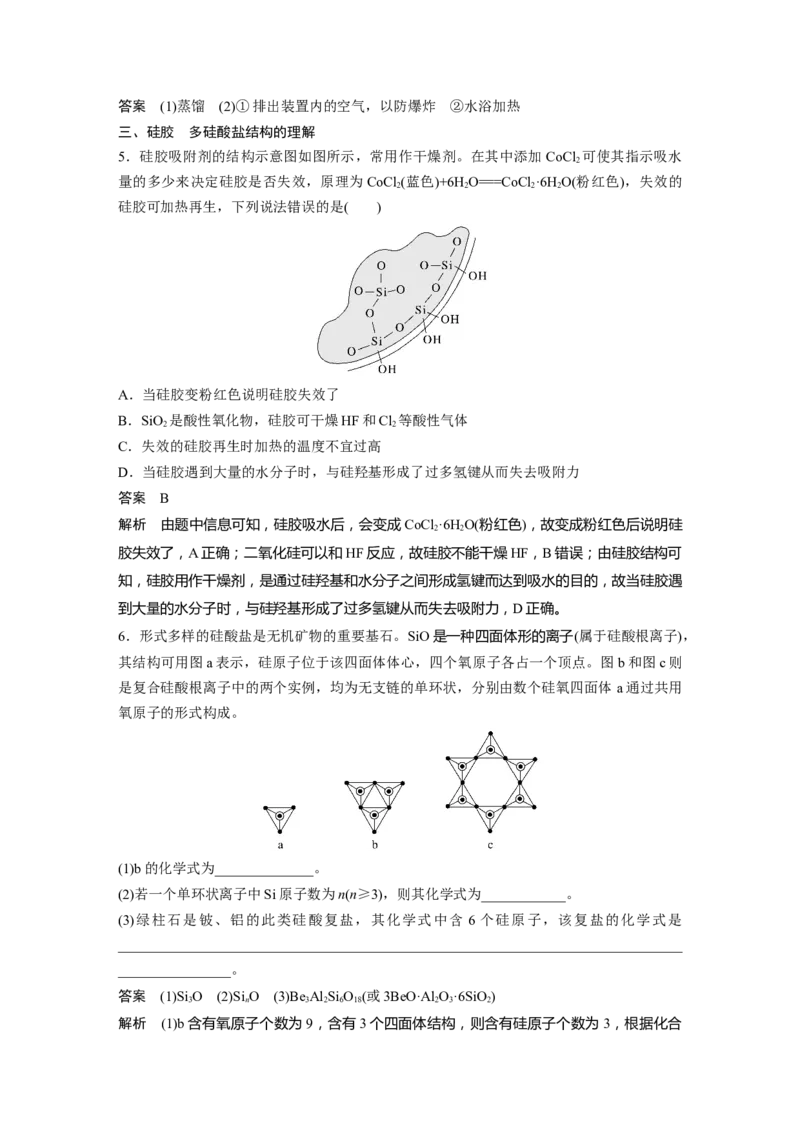
(2)用SiHCl 与过量H 反应制备纯硅的装置如图所示(热源及夹持装置已略去):
3 2
① 在 加 热 D 装 置 前 应 先 打 开 A 装 置 中 分 液 漏 斗 的 活 塞 , 目 的 是
___________________________
_______________________________________________________________________________
。
②C装置中烧瓶需要加热,采用的方法是____________________________________________。答案 (1)蒸馏 (2)①排出装置内的空气,以防爆炸 ②水浴加热
三、硅胶 多硅酸盐结构的理解
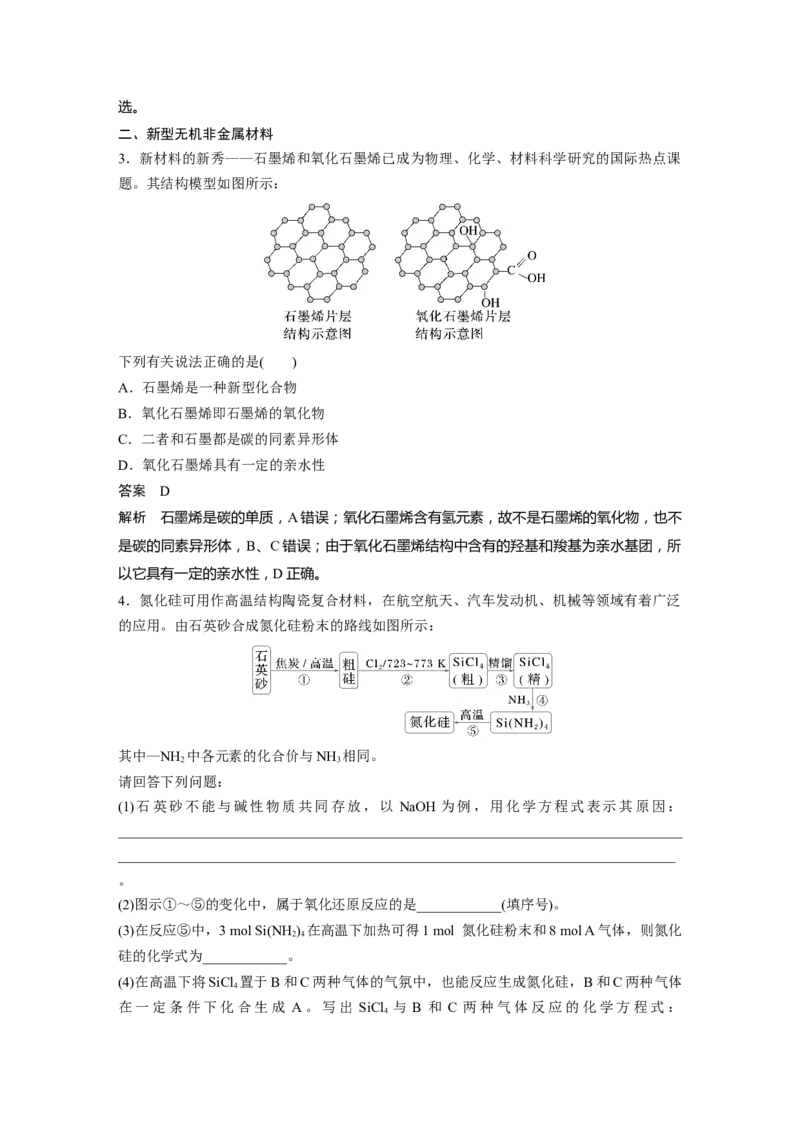
5.硅胶吸附剂的结构示意图如图所示,常用作干燥剂。在其中添加CoCl 可使其指示吸水
2
量的多少来决定硅胶是否失效,原理为CoCl (蓝色)+6H O===CoCl ·6H O(粉红色),失效的
2 2 2 2
硅胶可加热再生,下列说法错误的是( )
A.当硅胶变粉红色说明硅胶失效了
B.SiO 是酸性氧化物,硅胶可干燥HF和Cl 等酸性气体
2 2
C.失效的硅胶再生时加热的温度不宜过高
D.当硅胶遇到大量的水分子时,与硅羟基形成了过多氢键从而失去吸附力
答案 B
解析 由题中信息可知,硅胶吸水后,会变成CoCl ·6H O(粉红色),故变成粉红色后说明硅
2 2
胶失效了,A正确;二氧化硅可以和HF反应,故硅胶不能干燥HF,B错误;由硅胶结构可
知,硅胶用作干燥剂,是通过硅羟基和水分子之间形成氢键而达到吸水的目的,故当硅胶遇
到大量的水分子时,与硅羟基形成了过多氢键从而失去吸附力,D正确。
6.形式多样的硅酸盐是无机矿物的重要基石。SiO是一种四面体形的离子(属于硅酸根离子),
其结构可用图a表示,硅原子位于该四面体体心,四个氧原子各占一个顶点。图b和图c则
是复合硅酸根离子中的两个实例,均为无支链的单环状,分别由数个硅氧四面体 a通过共用
氧原子的形式构成。
(1)b的化学式为______________。
(2)若一个单环状离子中Si原子数为n(n≥3),则其化学式为____________。
(3)绿柱石是铍、铝的此类硅酸复盐,其化学式中含 6 个硅原子,该复盐的化学式是
________________________________________________________________________________
________________。
答案 (1)Si O (2)Si O (3)Be Al Si O (或3BeO·Al O·6SiO)
3 n 3 2 6 18 2 3 2
解析 (1)b含有氧原子个数为9,含有3个四面体结构,则含有硅原子个数为3,根据化合物中Si的化合价为+4、氧元素化合价为-2可知,b的化学式为Si O。(2)c中含有6个四面
3
体结构,所以含有6个Si原子,含有的氧原子数为18,含有氧原子数比6个硅酸根离子少6
个O,带有的电荷为6×(-2)=-12;根据图示可知:若一个单环状离子中Si原子数为
n(n≥3),则含有n个四面体结构,含有的氧原子比n个硅酸根离子恰好少n个O原子,即含
有n个Si,则含有3n个O,带有的负电荷为n×(-2)=-2n,其化学式为Si O。 (3)根据
n
Si O可知,含有6个硅原子,该硅酸盐所带的负电荷为-12,设铍的个数为x,铝的个数为
n
y,则2x+3y=12,讨论可得x=3、y=2,其化学式为Be Al Si O 或3BeO·Al O·6SiO。
3 2 6 18 2 3 2
考点三 无机非金属材料
1.传统无机非金属材料——常见硅酸盐材料
硅酸盐材料 水泥 普通玻璃 陶瓷
生产原料 石灰石、黏土 纯碱、石灰石、石英砂 黏土
主要设备 水泥回转窑 玻璃窑 陶瓷窑
玻 璃 生 产 中 的 两 个 重 要 反 应 : NaCO + SiO=====NaSiO + CO ↑ ; CaCO +
2 3 2 2 3 2 3
SiO=====CaSiO + CO ↑。
2 3 2
2.新型无机非金属材料
(1)高温结构陶瓷,如SiC、BN、Si N、Al O 等。
3 4 2 3
(2)碳纳米材料
①类型:富勒烯、碳纳米管、石墨烯等。
②用途:在能源、信息、医药等领域有广阔的应用前景。
(3)特殊功能的含硅材料
①碳化硅为共价晶体,具有类似金刚石的结构,可用作磨料。
②含硅元素4%的硅钢具有导磁性。
1.沙子和黏土的主要成分均为硅酸盐( )
2.碳化硅俗称金刚砂,它可用于高温结构陶瓷的制作( )
3.压电陶瓷能实现机械能与电能的相互转化( )
4.石墨烯的电阻率低,热导率也低( )
5.冰壶主材料花岗岩属于无机非金属材料(2022·辽宁,1A)( )
答案 1.× 2.√ 3.√ 4.× 5.√一、传统无机非金属材料
1.水玻璃(Na SiO 溶液)广泛应用于耐火材料、洗涤剂生产等领域,是一种重要的工业原料。
2 3
如图是用稻壳灰(SiO:65%~70%、C:30%~35%)制取水玻璃的工艺流程:
2
下列说法正确的是( )
A.原材料稻壳灰价格低廉,且副产品活性炭有较高的经济价值
B.操作A与操作B完全相同
C.该流程中硅元素的化合价发生改变
D.反应器中发生的反应为氧化还原反应
答案 A
解析 B项,操作A为过滤,操作B为蒸发浓缩,是两种不同的操作,错误;C项,二氧化
硅中硅元素的化合价是+4价,硅酸钠中硅元素的化合价也是+4价,所以该流程中硅元素
的化合价没有发生改变,错误;D项,反应器中发生的反应为SiO +2NaOH===NaSiO +
2 2 3
HO,此反应没有元素化合价的变化,属于非氧化还原反应,错误。
2
2.世博会中国馆——“东方之冠”由钢筋、混凝土、7 000多块铝板和1 200多块玻璃等建
成。
(1)铝板易被烧碱腐蚀,玻璃易被氢氟酸腐蚀,原因分别为_____________________________、
________________________________________________________________________________
(用化学方程式表示)。
(2)生产硅酸盐水泥和普通玻璃都需要用到的主要原料是____________________。制备普通
玻璃的主要反应的化学方程式为________________________________(任写一个)。
(3)石英玻璃化学稳定性强、膨胀系数小,是一种特殊玻璃,石英玻璃的主要成分是
________(填化学式)。
(4)要将NaOH高温熔化,下列坩埚中可选用的是________(填字母)。
A.普通玻璃坩埚 B.石英玻璃坩埚
C.氧化铝坩埚 D.铁坩埚
答案 (1)2Al+2NaOH+2HO===2NaAlO +3H↑ SiO+4HF===SiF↑+2HO
2 2 2 2 4 2
(2)石灰石 SiO+NaCO=====NaSiO+CO↑(或SiO+CaCO =====CaSiO +CO↑)
2 2 3 2 3 2 2 3 3 2
(3)SiO (4)D
2
解析 (4)普通玻璃坩埚和石英玻璃坩埚中的二氧化硅能够与熔融的氢氧化钠反应,故A、B
不选;氧化铝能够与熔融的氢氧化钠反应,故 C不选;铁与熔融的氢氧化钠不反应,故D选。
二、新型无机非金属材料
3.新材料的新秀——石墨烯和氧化石墨烯已成为物理、化学、材料科学研究的国际热点课
题。其结构模型如图所示:
下列有关说法正确的是( )
A.石墨烯是一种新型化合物
B.氧化石墨烯即石墨烯的氧化物
C.二者和石墨都是碳的同素异形体
D.氧化石墨烯具有一定的亲水性
答案 D
解析 石墨烯是碳的单质,A错误;氧化石墨烯含有氢元素,故不是石墨烯的氧化物,也不
是碳的同素异形体,B、C错误;由于氧化石墨烯结构中含有的羟基和羧基为亲水基团,所
以它具有一定的亲水性,D正确。
4.氮化硅可用作高温结构陶瓷复合材料,在航空航天、汽车发动机、机械等领域有着广泛
的应用。由石英砂合成氮化硅粉末的路线如图所示:
其中—NH 中各元素的化合价与NH 相同。
2 3
请回答下列问题:
(1)石英砂不能与碱性物质共同存放,以 NaOH 为例,用化学方程式表示其原因:
________________________________________________________________________________
_______________________________________________________________________________
。
(2)图示①~⑤的变化中,属于氧化还原反应的是____________(填序号)。
(3)在反应⑤中,3 mol Si(NH ) 在高温下加热可得1 mol 氮化硅粉末和8 mol A气体,则氮化
2 4
硅的化学式为____________。
(4)在高温下将SiCl 置于B和C两种气体的气氛中,也能反应生成氮化硅,B和C两种气体
4
在一定条件下化合生成 A。写出 SiCl 与 B 和 C 两种气体反应的化学方程式:
4_______________
_______________________________________________________________________________
。
答案 (1)SiO+2NaOH===NaSiO+HO
2 2 3 2
(2)①② (3)Si N
3 4
(4)3SiCl +2N+6H=====Si N+12HCl
4 2 2 3 4
解析 (3)氮化硅的化学式可通过题目信息运用质量守恒定律求得:3Si(NH )=====Si N +
2 4 3 4
8NH ↑。(4)结合题给信息,SiCl 与N、H 反应可得到Si N 和HCl。
3 4 2 2 3 4
1.正误判断,正确的打“√”,错误的打“×”。
(1)晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维(2022·浙江6月选考,8A)(
)
(2)用焦炭和石英砂制取粗硅,SiO 可制作光导纤维(2022·广东,12A)( )
2
(3)石灰石是制造玻璃和水泥的主要原料之一(2022·湖南,2D)( )
(4)火炬“飞扬”使用的碳纤维属于有机高分子材料(2022·辽宁,1B)( )
答案 (1)× (2)√ (3)√ (4)×
2.(2021·海南,1)2020年9月22日,中国向全世界宣布,努力争取2060年前实现碳中和。
下列措施不利于大气中CO 减少的是( )
2
A.用氨水捕集废气中的CO,将其转化为氮肥
2
B.大力推广使用风能、水能、氢能等清洁能源
C.大力推广使用干冰实现人工增雨,缓解旱情
D.通过植树造林,利用光合作用吸收大气中的CO
2
答案 C
解析 氨水能与酸性氧化物二氧化碳反应生成碳酸铵或碳酸氢铵,则用氨水捕集废气中的二
氧化碳,将其转化为氮肥有利于大气中二氧化碳的减少,故 A不符合题意;大力推广使用
风能、水能、氢能等清洁能源可以减少化石能源的使用,从而减少二氧化碳气体的排放,故
B不符合题意;大力推广使用干冰实现人工增雨,会增加大气中二氧化碳的量,不利于大气
中二氧化碳的减少,故C符合题意;通过植树造林,利用光合作用吸收大气中的二氧化碳,
有利于大气中二氧化碳的减少,故D不符合题意。
课时精练
1.“九秋风露越窑开,夺得千峰翠色来”是赞誉越窑秘色青瓷的诗句,描绘了我国古代精美的青瓷工艺品。玻璃、水泥和陶瓷均为硅酸盐制品,下列有关说法正确的是( )
A.玻璃是人类最早使用的硅酸盐制品
B.制水泥的原料为纯碱、石灰石和石英
C.硅酸盐制品的性质稳定、熔点较高
D.陶瓷的烧制过程为物理变化
答案 C
解析 陶瓷是人类最早使用的硅酸盐制品,A项错误;纯碱、石灰石和石英是制普通玻璃的
原料,而制水泥的原料是黏土和石灰石,B项错误。
2.(2019·全国卷Ⅰ,7)陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学
有着密切的关系。下列说法错误的是( )
A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁
B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成
C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐
D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点
答案 A
解析 “雨过天晴云破处”所描述的瓷器青色与氧化亚铁有关,而氧化铁显红棕色,A项错
误;秦兵马俑是陶制品,由黏土经高温烧结而成,B项正确;陶瓷以黏土为原料,经高温烧
制而成,属于人造材料,主要成分是硅酸盐,C项正确;陶瓷主要成分是硅酸盐,硅酸盐中
硅元素化合价处于最高价,化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点,D项正确。
3.下列关于硅的说法不正确的是( )
A.硅是非金属元素,它的单质是灰黑色、有金属光泽的固体
B.硅的导电性能介于导体和绝缘体之间,是良好的半导体材料
C.硅的化学性质不活泼,常温下不与任何物质发生反应
D.加热到一定温度时,硅能与氯气、氧气等非金属反应
答案 C
解析 晶体硅的结构与金刚石类似,它是灰黑色、有金属光泽的非金属固体,故 A正确;
硅常温下能和HF溶液、氢氧化钠溶液反应,故C错误;在加热时,硅能与氧气或氯气反应
生成二氧化硅或四氯化硅,故D正确。
4.(2021·湖北,1)“碳中和”有利于全球气候改善。下列有关CO 的说法错误的是( )
2
A.CO 是V形的极性分子
2
B.CO 可催化还原为甲酸
2
C.CO 晶体可用于人工增雨
2
D.CO 是侯氏制碱法的原料之一
2
答案 A
解析 CO 中C采取sp杂化,空间结构为直线形,CO 是非极性分子,A项错误;CO 在电
2 2 2催化下与氢气反应可以降低碳的化合价,生成一系列化合物,如 CH 、CH===CH 、
4 2 2
CHOH、HCOOH等,B项正确;干冰气化时吸收大量热量,使水蒸气液化而增雨,C项正
3
确 ; 侯 氏 制 碱 法 的 化 学 反 应 原 理 是 NaCl + NH + CO + HO===NaHCO ↓ +
3 2 2 3
NH Cl,2NaHCO =====NaCO+CO↑+HO,D项正确。
4 3 2 3 2 2
5.硅是构成无机非金属材料的一种主要元素,下列有关硅及其化合物的叙述错误的是(
)
A.氮化硅陶瓷是一种高温结构陶瓷,其化学式为Si N
3 4
B.高纯硅可以制成计算机、通信设备等的芯片
C.硅可以用来生产新型无机非金属材料——光导纤维
D.二氧化硅为立体网状结构,每个硅原子结合4个氧原子
答案 C
解析 光导纤维的主要成分是二氧化硅,属于新型无机非金属材料,故C错误;二氧化硅
为共价晶体,为立体网状结构,其晶体中每个硅原子结合4个氧原子,每个氧原子结合2个
硅原子,硅原子和氧原子个数之比为1∶2,故D正确。
6.下列关于二氧化硅的说法正确的是( )
A.二氧化硅是酸性氧化物,因此能与水反应生成硅酸
B.二氧化硅制成的光导纤维,由于导电能力强而被用于制造光缆
C.二氧化硅能与碳酸钠固体在高温时发生反应
D.用二氧化硅制取单质硅时,当生成2.24 L气体(标准状况)时,得到2.8 g硅
答案 C
解析 二氧化硅是酸性氧化物,但是二氧化硅不溶于水,与水不反应,故 A错误;二氧化
硅制成的光导纤维,由于其良好的光学特性而被用于制造光缆,故B错误;在高温时,二
氧化硅能够与碳酸钠固体反应生成硅酸钠和二氧化碳,故 C正确;由化学方程式SiO +
2
2C=====Si+2CO↑可知,当生成2.24 L(标准状况)即0.1 mol气体时,得到0.05 mol 即1.4 g
硅,故D错误。
7.在20世纪90年代末,科学家发现碳有新的单质形态C 存在。后来人们又相继得到了
60
C 、C 、C 、C 、C 等另外一些球碳分子。21世纪初,科学家又发现了管状碳分子和洋
70 76 84 90 94
葱状碳分子,大大丰富了碳元素单质的家族。下列有关碳元素单质的说法错误的是( )
A.金刚石和石墨的熔点肯定比C 高
60
B.熔点:C <C <C
60 70 90
C.球碳分子、管状碳分子和洋葱状碳分子都不能与O 发生反应
2
D.金刚石以非分子形式的粒子存在,属于共价晶体;C 、C 、管状碳分子和洋葱状碳分
60 70子以分子形式的粒子存在,属于分子晶体;这些碳单质互为同素异形体
答案 C
解析 金刚石属于共价晶体,石墨属于混合型晶体,C 属于分子晶体,因此金刚石和石墨
60
的熔点肯定比C 高,故A正确;分子晶体的相对分子质量越大,熔点越高,因此熔点:C
60 60
<C <C ,故B正确。
70 90
8.二氧化硅广泛存在于自然界中,在日常生活、生产、科研及新型材料等方面有着重要的
用途。a~e是对①~⑤反应中SiO 所表现的化学性质或作用进行的判断,其中正确的是(
2
)
①SiO+2NaOH===NaSiO+HO
2 2 3 2
②SiO+2C=====Si+2CO↑
2
③SiO+4HF===SiF↑+2HO
2 4 2
④NaCO+SiO=====NaSiO+CO↑
2 3 2 2 3 2
⑤SiO+3C=====SiC+2CO↑
2
a.反应①中SiO 作为玻璃的成分被消耗,用于刻蚀玻璃
2
b.反应②中SiO 表现出氧化性
2
c.反应③中SiO 表现了酸性氧化物的通性
2
d.反应④符合用难挥发性的酸酐制取易挥发性的酸酐的原理
e.反应⑤中SiO 未参加氧化还原反应
2
A.ace B.bde C.cde D.ab
答案 B
解析 通常用氢氟酸来刻蚀玻璃,与之对应的反应是③,a、c判断错误;反应②是一个置
换反应,其中二氧化硅被还原,表现出氧化性,b判断正确;反应④用难挥发的二氧化硅制
取易挥发的二氧化碳,d判断正确;反应⑤中碳的化合价由0价变为-4价和+2价,硅的化
合价和氧的化合价都没有改变,因此二氧化硅没有参加氧化还原反应,e判断正确。
9.纯二氧化硅可用下列流程制得。下列说法不正确的是( )
A.X可用作木材防火剂
B.步骤Ⅱ的反应是NaSiO+HSO ===HSiO↓+ NaSO
2 3 2 4 2 3 2 4
C.步骤Ⅱ中的稀硫酸可用CO 来代替
2
D.SiO 既能与NaOH溶液反应,又能与氢氟酸反应,所以SiO 是两性氧化物
2 2
答案 D
解析 碳酸、硫酸的酸性都强于硅酸,能够与硅酸钠溶液反应生成硅酸,C正确;SiO 既能
2
和NaOH溶液反应又能和氢氟酸反应,但与氢氟酸反应的生成物不是盐,所以二氧化硅不
是两性氧化物,而是酸性氧化物,D不正确。
10.由粗硅制备硅烷(SiH)的基本流程如图所示:
4已知:反应Ⅰ的化学方程式为Si+3HCl=====SiHCl +X,反应Ⅱ的化学方程式为SiHCl +
3 3
Y=====Si+3HCl。下列说法不正确的是( )
A.X和Y为同一种物质
B.SiH 的稳定性比NH 弱
4 3
C.流程中的4个反应有3个属于氧化还原反应
D.反应Ⅳ中SiH、NH 两种气体在常温、常压下体积比为4∶1
4 3
答案 D
解析 根据题给反应Ⅰ、Ⅱ的化学方程式和原子守恒可得,X为H,Y为H,X、Y为同一
2 2
种物质,A正确;非金属性越强,简单氢化物的稳定性越强,非金属性:N>Si,则简单氢
化物的稳定性:NH >SiH ,B正确;根据图示可知,流程中的反应Ⅰ、Ⅱ、Ⅲ均属于氧化还
3 4
原反应,反应Ⅳ为非氧化还原反应,C 正确;由反应Ⅳ的化学方程式 MgSi+
2
4NH Cl===SiH↑+4NH ↑+2MgCl 可知,SiH 、NH 两种气体在常温、常压下体积比为
4 4 3 2 4 3
1∶4,D错误。
11.科学家最新研制的利用氯化氢和氢气生产高纯硅的工艺流程如图所示:
容器①中进行的反应为①Si(粗)+3HCl(g)=====SiHCl (l)+H(g);容器②中进行的反应为
3 2
②SiHCl +H=====Si(纯)+3HCl。下列说法不正确的是( )
3 2
A.该工艺流程的优点是部分反应物可循环使用
B.①和②互为可逆反应
C.该流程中需要隔绝空气
D.粗硅制备不能通过SiO――→SiCl ――→Si实现
2 4
答案 B
解析 A项,反应②中生成的HCl在反应①中循环利用,反应①中生成的H 在反应②中循
2
环利用,正确;B项,反应①与反应②的反应温度不同,不是可逆反应,错误;C项,高温
条件下,Si、SiHCl 、H 都与O 反应,故需隔绝空气,正确;D项,SiO 不与HCl(aq)反应,
3 2 2 2
不能通过上述途径制硅,正确。
12.Ag催化刻蚀Si晶片的反应原理示意图如图,刻蚀溶液由一定浓度的HF和HO 混合而成,
2 2
刻蚀时间为2~16 min,由Ag薄膜覆盖的硅晶片部分逐渐被刻蚀掉,剩余部分就形成了硅
纳米线。下列说法不正确的是( )A.Ag薄膜附近随着反应的进行,pH逐渐减小
B.Si极发生的反应为Si+2HO-4e-===SiO+4H+,SiO+6HF===HSiF+2HO
2 2 2 2 6 2
C.该刻蚀的总反应可表示为Si+6HF+2HO===HSiF+4HO
2 2 2 6 2
D.该刻蚀过程是由微小的Si、Ag、HF和HO 的原电池组成
2 2
答案 A
解析 根据图示可知:在Ag薄膜附近发生反应:2H++2e-+HO===2HO,所以随着反应
2 2 2
的进行,c(H+)减小,故pH逐渐增大,A错误;根据图示可知:在Si电极上,Si失去电子
与 HF 结合形成 HSiF 和 H+,反应方程式为 Si+2HO-4e-===SiO +4H+,SiO +
2 6 2 2 2
6HF===HSiF +2HO,B正确;由Ag、Si极发生的电极反应及电子转移数目相等,可知总
2 6 2
反应方程式为Si+6HF+2HO===HSiF +4HO,C正确;根据上述分析可知:在Ag电极
2 2 2 6 2
上得到电子,在Si电极上失去电子,电解质溶液为HF和HO ,它们形成闭合回路,实现
2 2
了化学能向电能的转化,即构成了原电池,D正确。
13.(2023·河北邢台高三校联考)硅的提纯是电子工业一项十分重要的工作,可用粗硅与干燥
的HCl气体反应制SiHCl (其中含有BCl 、SiCl ),SiHCl 与过量H 在1 000~1 100 ℃反应
3 3 4 3 2
制得纯硅。有关物质的物理性质见下表:
物质 SiCl BCl SiHCl
4 3 3
沸点/℃ 57.6 12.5 33.0
熔点/℃ -70.0 -107 -127
回答下列问题:
(1)基态Si原子核外电子共有________种运动状态;粗硅与HCl反应完全后的混合物冷却到
标准状况,可通过________(填操作名称)提纯得到SiHCl 。
3
(2)已知在有HF存在的条件下,硅可以和浓硝酸反应生成六氟合硅酸,该反应的化学方程式
为______________________________________________________________________。
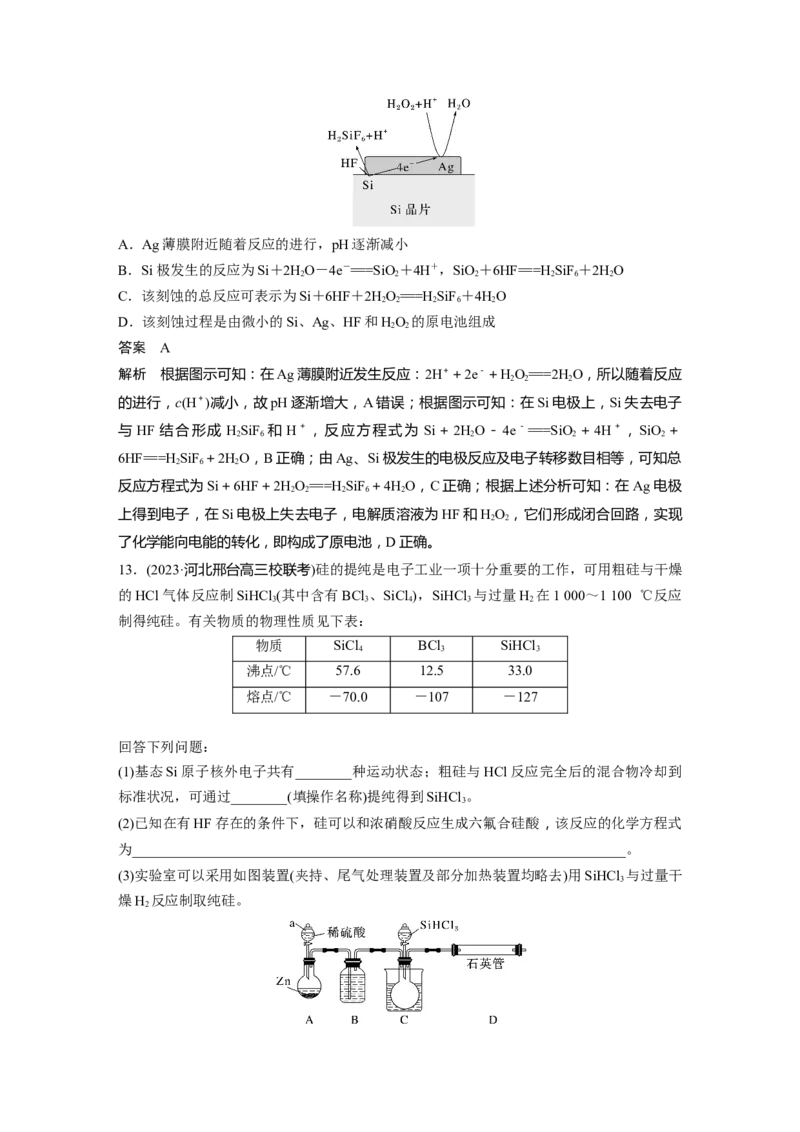
(3)实验室可以采用如图装置(夹持、尾气处理装置及部分加热装置均略去)用SiHCl 与过量干
3
燥H 反应制取纯硅。
2①仪器a的名称为__________,装置B中的试剂为________。
② 将 装 置 C 水 浴 加 热 , 该 加 热 方 式 的 优 点 是
___________________________________________
_______________________________________________________________________________
。
③为保证实验安全,加热装置 D 前必须完成的操作是:ⅰ.检验装置的气密性;ⅱ.
_____________________________________________________________________________
_______________________________________________________________________________
,
该装置中发生反应的化学方程式为__________________________________________________
_______________________________________________________________________________
。
答案 (1)14 蒸馏 (2)Si+4HNO(浓)+6HF===HSiF+4NO ↑+4HO
3 2 6 2 2
(3)①分液漏斗 浓硫酸 ②加热均匀,便于控制温度使SiHCl 汽化 ③检验氢气的纯度(或
3
先滴加稀硫酸,产生氢气,排尽装置中的空气) SiHCl +H==========Si+3HCl
3 2