文档内容
第 11 讲 碳酸钠和碳酸氢钠 钠及其化合物的相互转化
[复习目标] 1.通过比较掌握 NaCO 、NaHCO 的性质,能从不同角度鉴别 NaCO 和
2 3 3 2 3
NaHCO ,会分析NaCO 、NaHCO 含量测定的思维方法。2.熟练掌握钠及其重要化合物的
3 2 3 3
转化关系及应用。
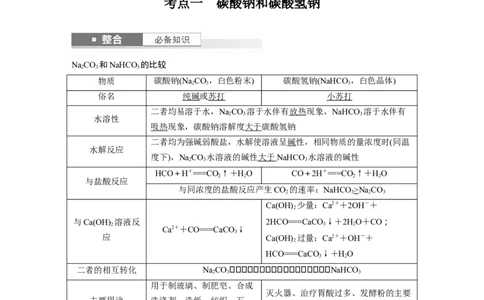
考点一 碳酸钠和碳酸氢钠
NaCO 和NaHCO 的比较
2 3 3
物质 碳酸钠(Na CO,白色粉末) 碳酸氢钠(NaHCO ,白色晶体)
2 3 3
俗名 纯碱或苏打 小苏打
二者均易溶于水,NaCO 溶于水伴有放热现象,NaHCO 溶于水伴有
2 3 3
水溶性
吸热现象,碳酸钠溶解度大于碳酸氢钠
二者均为强碱弱酸盐,水解使溶液呈碱性,相同物质的量浓度时(同温
水解反应
度下),NaCO 水溶液的碱性大于 NaHCO 水溶液的碱性
2 3 3
HCO+H+===CO↑+HO CO+2H+===CO↑+HO
2 2 2 2
与盐酸反应
与同浓度的盐酸反应产生CO 的速率:NaHCO >NaCO
2 3 2 3
Ca(OH) 少量:Ca2++2OH-+
2
与Ca(OH) 溶液反 2HCO===CaCO ↓+2HO+CO;
2 3 2
Ca2++CO===CaCO ↓
3
应 Ca(OH) 过量:Ca2++OH-+
2
HCO===CaCO ↓+HO
3 2
二者的相互转化 NaCONaHCO
2 3 3
用于制玻璃、制肥皂、合成
灭火器、治疗胃酸过多、发酵粉的主要
主要用途 洗涤剂、造纸、纺织、石
成分之一
油、冶金等工业中
1.碳酸钠、碳酸氢钠都能与盐酸、氢氧化钠溶液反应( )
2.用热碱水清除炊具上残留的油污,没有发生化学反应( )
3.Al (SO ) 和小苏打反应可用作泡沫灭火器灭火( )
2 4 3
4.向饱和NaCO 溶液中通入CO,有NaHCO 晶体析出( )
2 3 2 35.将稀盐酸滴入碳酸钠与氢氧化钠的混合溶液中,立即产生气泡( )
6.用酚酞溶液可鉴别饱和食盐水和饱和碳酸钠溶液( )
7.苏打是面包发酵粉的主要成分之一( )
8.相同温度下,溶解度:小苏打<苏打,热稳定性:NaCO>NaHCO( )
2 3 3
答案 1.× 2.× 3.√ 4.√ 5.× 6.√ 7.× 8.√
一、NaCO、NaHCO 的转化与除杂
2 3 3
1.选择适当的试剂或方法除去杂质,并完成转化的化学方程式,“[ ]”内为杂质。
(1)Na CO(s)[NaHCO ] :
2 3 3
_________________________________________________________,
______________________________________________________________________________。
(2)NaHCO (aq)[Na CO] :
3 2 3
________________________________________________________,
______________________________________________________________________________。
(3)Na CO(aq)[NaHCO ] :
2 3 3
_________________________________________________________,
______________________________________________________________________________。
答案 (1)充分灼烧至恒重 2NaHCO =====NaCO+HO+CO↑
3 2 3 2 2
(2)通入足量CO NaCO+HO+CO===2NaHCO
2 2 3 2 2 3
(3)滴加适量NaOH 溶液 NaHCO +NaOH===NaCO+HO
3 2 3 2
二、NaCO、NaHCO 的鉴别
2 3 3
2.多角度鉴别NaCO 与NaHCO 的基本方法
2 3 3
(1)固体的鉴别用加热法:产生使澄清石灰水变浑浊的气体的是NaHCO 固体。
3
(2)气体法
(3)测pH法
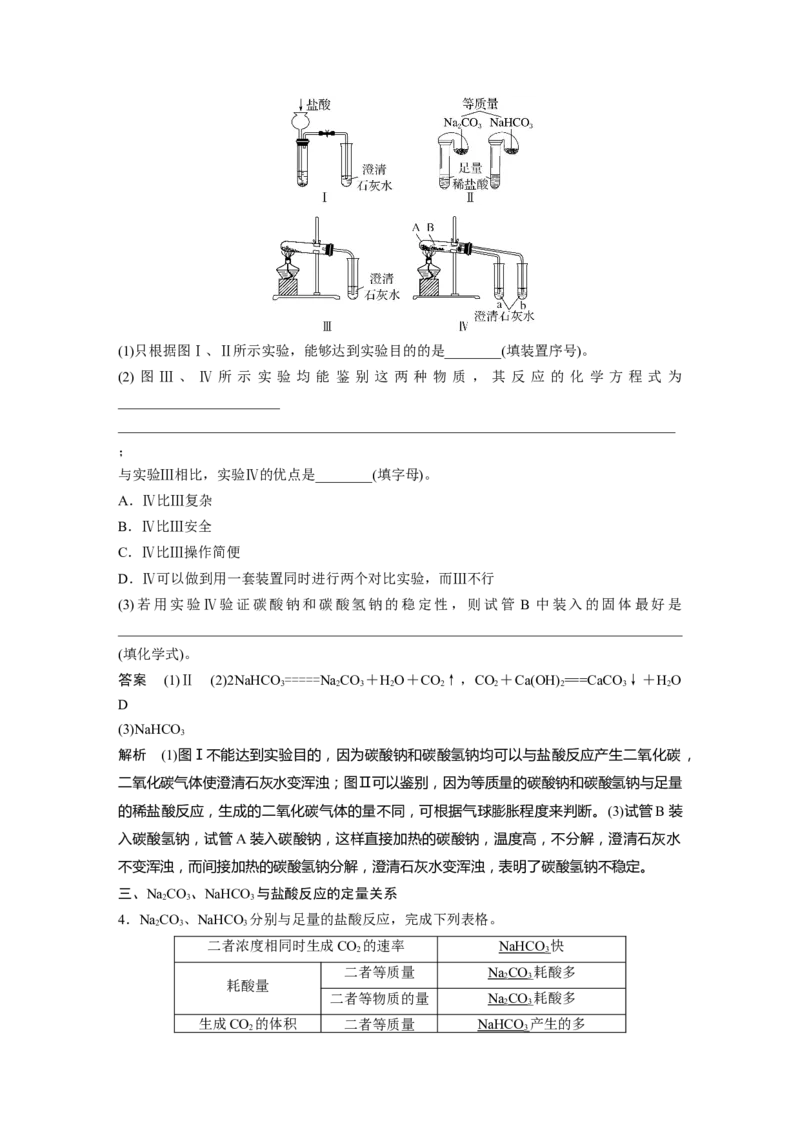
3.某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实
验,如图Ⅰ~Ⅳ所示。(1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是________(填装置序号)。
(2) 图 Ⅲ 、 Ⅳ 所 示 实 验 均 能 鉴 别 这 两 种 物 质 , 其 反 应 的 化 学 方 程 式 为
_______________________
_______________________________________________________________________________
;
与实验Ⅲ相比,实验Ⅳ的优点是________(填字母)。
A.Ⅳ比Ⅲ复杂
B.Ⅳ比Ⅲ安全
C.Ⅳ比Ⅲ操作简便
D.Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
(3)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管 B 中装入的固体最好是
________________________________________________________________________________
(填化学式)。
答案 (1)Ⅱ (2)2NaHCO =====NaCO +HO+CO↑,CO +Ca(OH) ===CaCO ↓+HO
3 2 3 2 2 2 2 3 2
D
(3)NaHCO
3
解析 (1)图Ⅰ不能达到实验目的,因为碳酸钠和碳酸氢钠均可以与盐酸反应产生二氧化碳,
二氧化碳气体使澄清石灰水变浑浊;图Ⅱ可以鉴别,因为等质量的碳酸钠和碳酸氢钠与足量
的稀盐酸反应,生成的二氧化碳气体的量不同,可根据气球膨胀程度来判断。(3)试管B装
入碳酸氢钠,试管A装入碳酸钠,这样直接加热的碳酸钠,温度高,不分解,澄清石灰水
不变浑浊,而间接加热的碳酸氢钠分解,澄清石灰水变浑浊,表明了碳酸氢钠不稳定。
三、NaCO、NaHCO 与盐酸反应的定量关系
2 3 3
4.NaCO、NaHCO 分别与足量的盐酸反应,完成下列表格。
2 3 3
二者浓度相同时生成CO 的速率 NaHCO 快
2 3
二者等质量 NaCO 耗酸多
2 3
耗酸量
二者等物质的量 NaCO 耗酸多
2 3
生成CO 的体积 二者等质量 NaHCO 产生的多
2 3二者等物质的量 相等
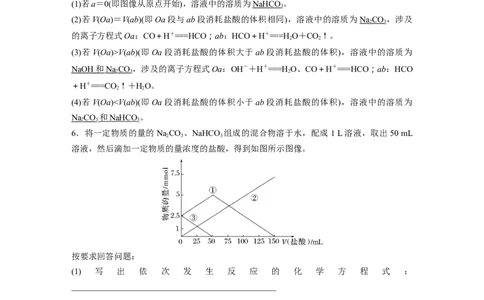
5.向含NaOH、NaCO 、NaHCO 其中一种或两种的溶液中滴加某浓度的盐酸,生成 CO
2 3 3 2
的体积(标准状况)与加入盐酸的体积的关系如图所示。依据图像特点判断溶液溶质的成分:
(1)若a=0(即图像从原点开始),溶液中的溶质为NaHCO 。
3
(2)若V(Oa)=V(ab)(即Oa段与ab段消耗盐酸的体积相同),溶液中的溶质为NaCO ,涉及
2 3
的离子方程式Oa:CO+H+===HCO;ab:HCO+H+===HO+CO↑。
2 2
(3)若V(Oa)>V(ab)(即Oa段消耗盐酸的体积大于ab段消耗盐酸的体积),溶液中的溶质为
NaOH 和 Na CO ,涉及的离子方程式Oa:OH-+H+===HO、CO+H+===HCO;ab:HCO
2 3 2
+H+===CO↑+HO。
2 2
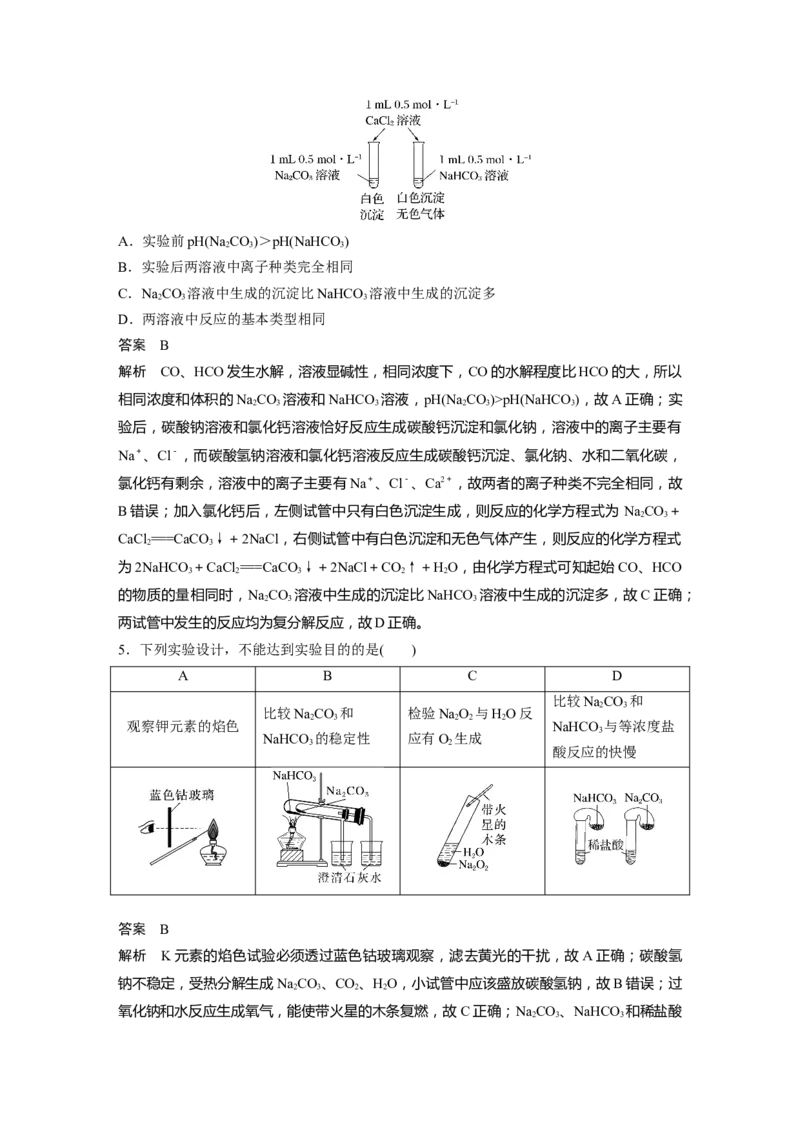
(4)若V(Oa)pH(NaHCO ),故A正确;实
2 3 3 2 3 3
验后,碳酸钠溶液和氯化钙溶液恰好反应生成碳酸钙沉淀和氯化钠,溶液中的离子主要有
Na+、Cl-,而碳酸氢钠溶液和氯化钙溶液反应生成碳酸钙沉淀、氯化钠、水和二氧化碳,
氯化钙有剩余,溶液中的离子主要有Na+、Cl-、Ca2+,故两者的离子种类不完全相同,故
B错误;加入氯化钙后,左侧试管中只有白色沉淀生成,则反应的化学方程式为 NaCO +
2 3
CaCl ===CaCO ↓+2NaCl,右侧试管中有白色沉淀和无色气体产生,则反应的化学方程式
2 3
为2NaHCO +CaCl ===CaCO ↓+2NaCl+CO↑+HO,由化学方程式可知起始CO、HCO
3 2 3 2 2
的物质的量相同时,NaCO 溶液中生成的沉淀比NaHCO 溶液中生成的沉淀多,故C正确;
2 3 3
两试管中发生的反应均为复分解反应,故D正确。
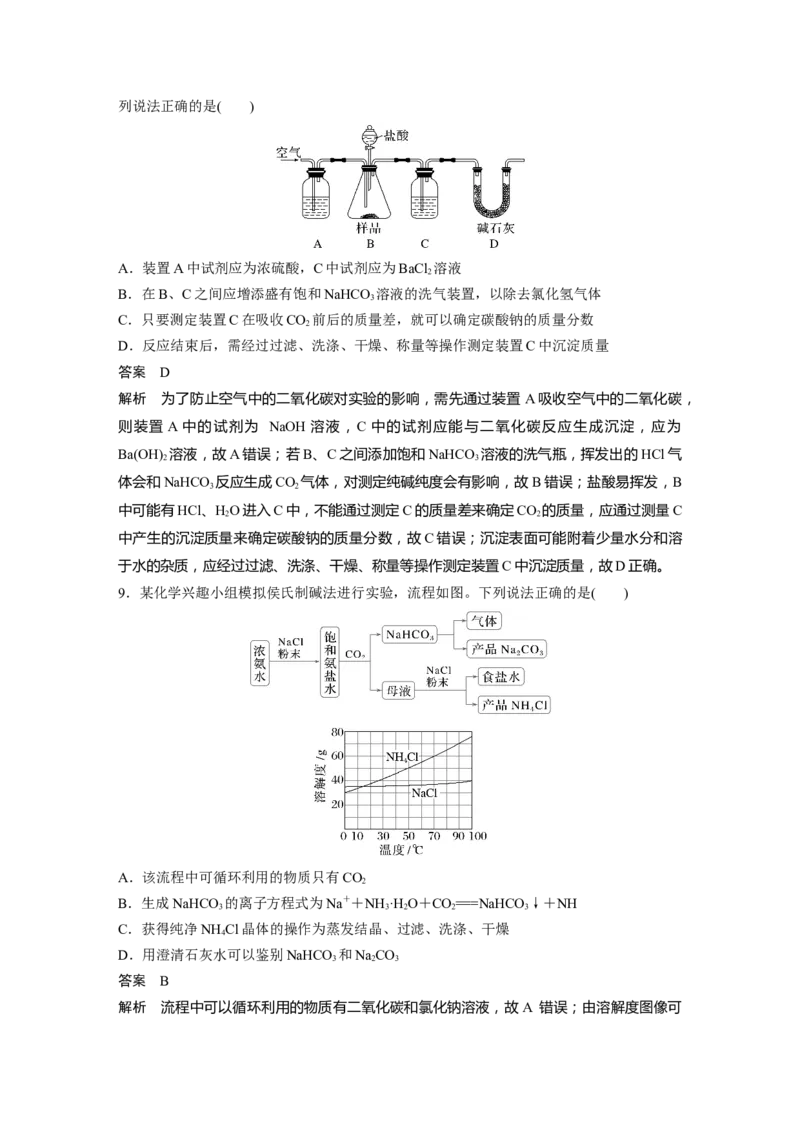
5.下列实验设计,不能达到实验目的的是( )
A B C D
比较NaCO 和
2 3
比较NaCO 和 检验NaO 与HO反
2 3 2 2 2
观察钾元素的焰色 NaHCO 与等浓度盐
3
NaHCO 的稳定性 应有O 生成
3 2
酸反应的快慢
答案 B
解析 K元素的焰色试验必须透过蓝色钴玻璃观察,滤去黄光的干扰,故A正确;碳酸氢
钠不稳定,受热分解生成NaCO 、CO 、HO,小试管中应该盛放碳酸氢钠,故B错误;过
2 3 2 2
氧化钠和水反应生成氧气,能使带火星的木条复燃,故 C正确;NaCO、NaHCO 和稀盐酸
2 3 3反应生成气泡的快慢不同,从而可以比较NaHCO 和NaCO 与盐酸反应的快慢,故D正确。
3 2 3
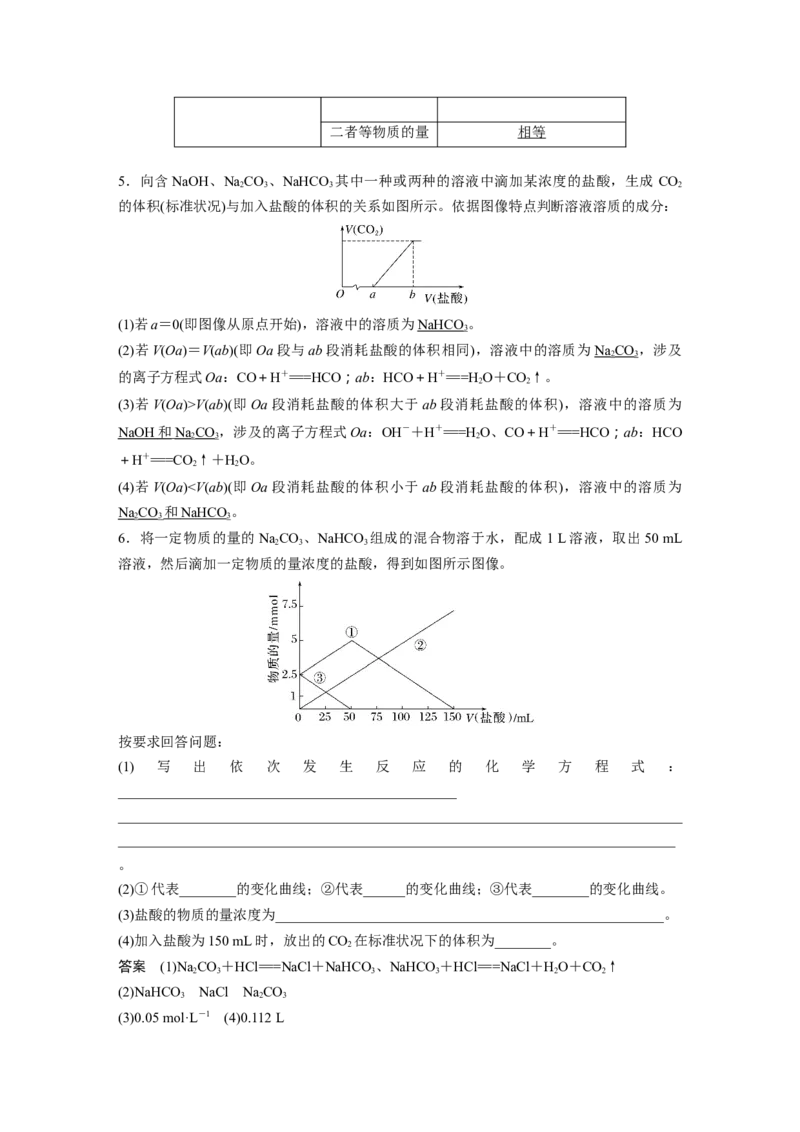
6.为精确测定工业纯碱中碳酸钠的质量分数(含少量NaCl),准确称量W g样品进行实验,
下列实验方法所对应的实验方案和测量数据合理的是( )
选项 实验方法 实验方案 测量数据
将样品配成100 mL溶液,取10 mL,加入
A 滴定法 消耗盐酸的体积
酚酞,用标准盐酸滴定
将样品与盐酸反应,生成的气体全部被碱石
B 量气法 碱石灰增加的质量
灰吸收
将样品放入烧瓶中,置于电子天平上,加入
C 重量法 减少的质量
足量盐酸
将样品与盐酸反应,气体通过排水量气装置
D 量气法 排出水的体积
量气
答案 A
解析 用酚酞作指示剂时,NaCO 与盐酸发生反应,依据消耗盐酸的量可以计算出样品中
2 3
NaCO 的量,进而确定样品中NaCO 的质量分数,A项正确;测量碱石灰增重的方法是重
2 3 2 3
量法而不是量气法且碱石灰吸收的是CO 和HO,无法计算,B项错误;因盐酸的质量未知,
2 2
且CO 挥发带出水蒸气,无法通过重量法测量NaCO 的质量,C项错误;因部分CO 能溶
2 2 3 2
解到水里,与水反应生成HCO,故排出水的体积并不是CO 的体积,D项错误。
2 3 2
7.以不同类别物质间的转化为线索,认识钠及其化合物。
下列分析不正确的是( )
A.反应③表明CO 具有酸性氧化物的性质
2
B.反应④说明NaHCO 的热稳定性强于NaCO
3 2 3
C.反应⑤⑥可用于潜水艇中氧气的供给
D.上述转化中发生的反应有分解反应、化合反应、置换反应
答案 B
解析 二氧化碳与氢氧化钠反应生成碳酸钠和水,则反应③表明CO 具有酸性氧化物的性质,
2
故 A 正确;碳酸氢钠受热分解生成碳酸钠,则反应④说明 NaCO 的热稳定性强于
2 3
NaHCO ,故B错误;过氧化钠与水、二氧化碳反应生成氧气,可用于潜水艇中氧气的供给,
3
故C正确;④是分解反应,①是化合反应,②是置换反应,故D正确。
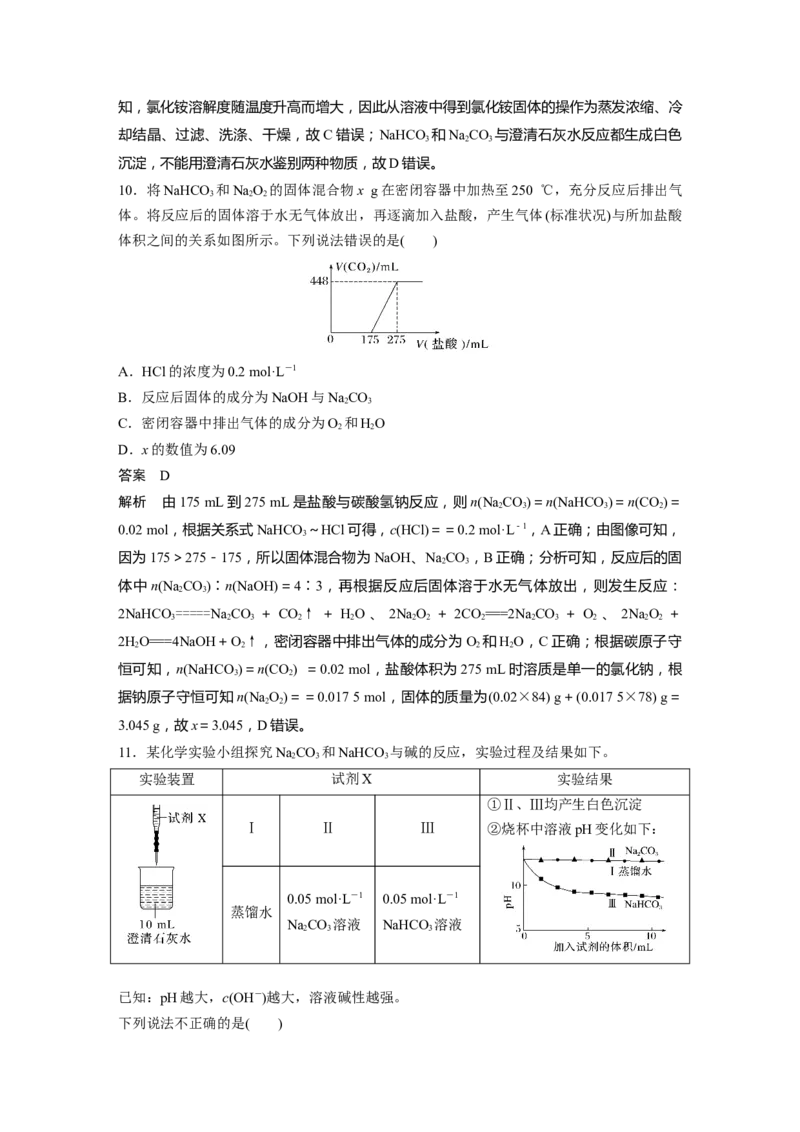
8.实验室可通过沉淀重量法测定样品纯度,按如图装置测定纯碱(含少量NaCl)的纯度,下列说法正确的是( )
A.装置A中试剂应为浓硫酸,C中试剂应为BaCl 溶液
2
B.在B、C之间应增添盛有饱和NaHCO 溶液的洗气装置,以除去氯化氢气体
3
C.只要测定装置C在吸收CO 前后的质量差,就可以确定碳酸钠的质量分数
2
D.反应结束后,需经过过滤、洗涤、干燥、称量等操作测定装置C中沉淀质量
答案 D
解析 为了防止空气中的二氧化碳对实验的影响,需先通过装置 A吸收空气中的二氧化碳,
则装置 A 中的试剂为 NaOH 溶液,C 中的试剂应能与二氧化碳反应生成沉淀,应为
Ba(OH) 溶液,故A错误;若B、C之间添加饱和NaHCO 溶液的洗气瓶,挥发出的HCl气
2 3
体会和NaHCO 反应生成CO 气体,对测定纯碱纯度会有影响,故B错误;盐酸易挥发,B
3 2
中可能有HCl、HO进入C中,不能通过测定C的质量差来确定CO 的质量,应通过测量C
2 2
中产生的沉淀质量来确定碳酸钠的质量分数,故C错误;沉淀表面可能附着少量水分和溶
于水的杂质,应经过过滤、洗涤、干燥、称量等操作测定装置C中沉淀质量,故D正确。
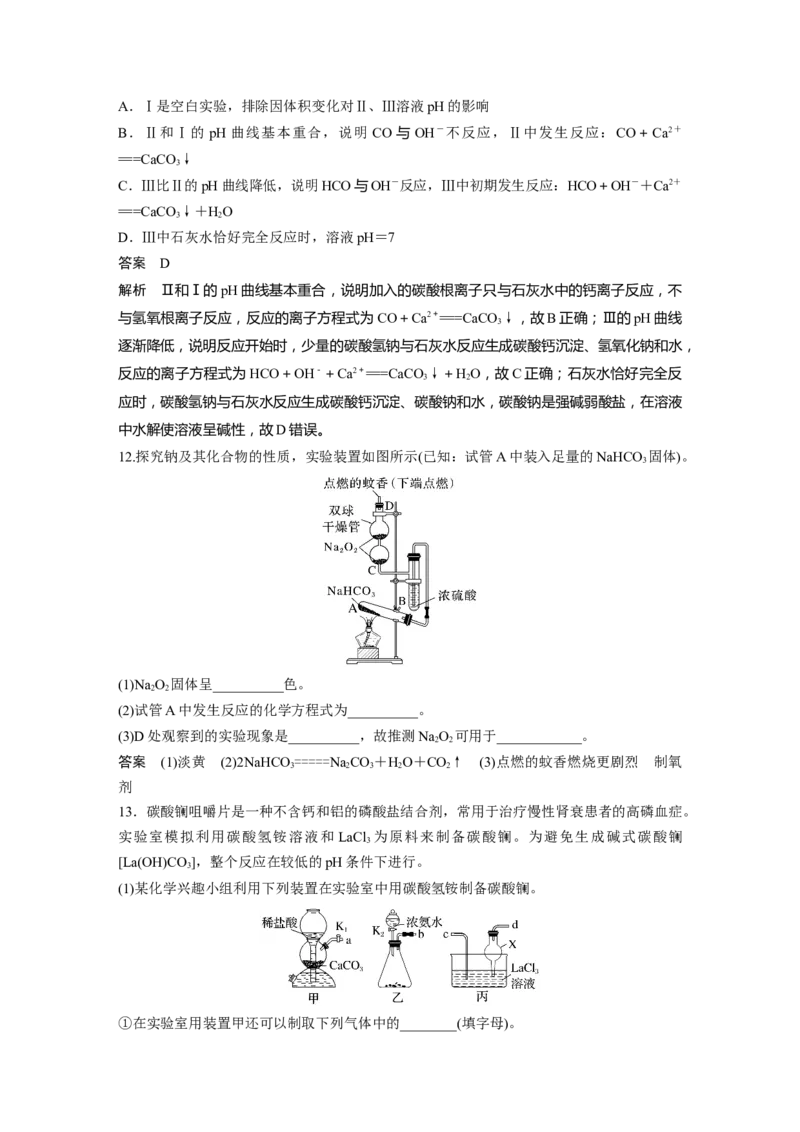
9.某化学兴趣小组模拟侯氏制碱法进行实验,流程如图。下列说法正确的是( )
A.该流程中可循环利用的物质只有CO
2
B.生成NaHCO 的离子方程式为Na++NH ·H O+CO===NaHCO ↓+NH
3 3 2 2 3
C.获得纯净NH Cl晶体的操作为蒸发结晶、过滤、洗涤、干燥
4
D.用澄清石灰水可以鉴别NaHCO 和NaCO
3 2 3
答案 B
解析 流程中可以循环利用的物质有二氧化碳和氯化钠溶液,故A 错误;由溶解度图像可知,氯化铵溶解度随温度升高而增大,因此从溶液中得到氯化铵固体的操作为蒸发浓缩、冷
却结晶、过滤、洗涤、干燥,故C错误;NaHCO 和NaCO 与澄清石灰水反应都生成白色
3 2 3
沉淀,不能用澄清石灰水鉴别两种物质,故D错误。
10.将NaHCO 和NaO 的固体混合物x g在密闭容器中加热至250 ℃,充分反应后排出气
3 2 2
体。将反应后的固体溶于水无气体放出,再逐滴加入盐酸,产生气体(标准状况)与所加盐酸
体积之间的关系如图所示。下列说法错误的是( )
A.HCl的浓度为0.2 mol·L-1
B.反应后固体的成分为NaOH与NaCO
2 3
C.密闭容器中排出气体的成分为O 和HO
2 2
D.x的数值为6.09
答案 D
解析 由175 mL到275 mL是盐酸与碳酸氢钠反应,则n(Na CO)=n(NaHCO )=n(CO)=
2 3 3 2
0.02 mol,根据关系式NaHCO ~HCl可得,c(HCl)==0.2 mol·L-1,A正确;由图像可知,
3
因为175>275-175,所以固体混合物为NaOH、NaCO ,B正确;分析可知,反应后的固
2 3
体中n(Na CO)∶n(NaOH)=4∶3,再根据反应后固体溶于水无气体放出,则发生反应:
2 3
2NaHCO =====NaCO + CO↑ + HO 、 2NaO + 2CO===2NaCO + O 、 2NaO +
3 2 3 2 2 2 2 2 2 3 2 2 2
2HO===4NaOH+O↑,密闭容器中排出气体的成分为O 和HO,C正确;根据碳原子守
2 2 2 2
恒可知,n(NaHCO )=n(CO) =0.02 mol,盐酸体积为275 mL时溶质是单一的氯化钠,根
3 2
据钠原子守恒可知n(Na O)==0.017 5 mol,固体的质量为(0.02×84) g+(0.017 5×78) g=
2 2
3.045 g,故x=3.045,D错误。
11.某化学实验小组探究NaCO 和NaHCO 与碱的反应,实验过程及结果如下。
2 3 3
实验装置 试剂X 实验结果
①Ⅱ、Ⅲ均产生白色沉淀
Ⅰ Ⅱ Ⅲ ②烧杯中溶液pH变化如下:
0.05 mol·L-1 0.05 mol·L-1
蒸馏水
NaCO 溶液 NaHCO 溶液
2 3 3
已知:pH越大,c(OH-)越大,溶液碱性越强。
下列说法不正确的是( )A.Ⅰ是空白实验,排除因体积变化对Ⅱ、Ⅲ溶液pH的影响
B.Ⅱ和Ⅰ的 pH 曲线基本重合,说明 CO 与 OH-不反应,Ⅱ中发生反应:CO+Ca2+
===CaCO ↓
3
C.Ⅲ比Ⅱ的pH曲线降低,说明HCO与OH-反应,Ⅲ中初期发生反应:HCO+OH-+Ca2+
===CaCO ↓+HO
3 2
D.Ⅲ中石灰水恰好完全反应时,溶液pH=7
答案 D
解析 Ⅱ和Ⅰ的pH曲线基本重合,说明加入的碳酸根离子只与石灰水中的钙离子反应,不
与氢氧根离子反应,反应的离子方程式为CO+Ca2+===CaCO ↓,故B正确;Ⅲ的pH曲线
3
逐渐降低,说明反应开始时,少量的碳酸氢钠与石灰水反应生成碳酸钙沉淀、氢氧化钠和水,
反应的离子方程式为HCO+OH-+Ca2+===CaCO ↓+HO,故C正确;石灰水恰好完全反
3 2
应时,碳酸氢钠与石灰水反应生成碳酸钙沉淀、碳酸钠和水,碳酸钠是强碱弱酸盐,在溶液
中水解使溶液呈碱性,故D错误。
12.探究钠及其化合物的性质,实验装置如图所示(已知:试管A中装入足量的NaHCO 固体)。
3
(1)Na O 固体呈__________色。
2 2
(2)试管A中发生反应的化学方程式为__________。
(3)D处观察到的实验现象是__________,故推测NaO 可用于____________。
2 2
答案 (1)淡黄 (2)2NaHCO =====NaCO +HO+CO↑ (3)点燃的蚊香燃烧更剧烈 制氧
3 2 3 2 2
剂
13.碳酸镧咀嚼片是一种不含钙和铝的磷酸盐结合剂,常用于治疗慢性肾衰患者的高磷血症。
实验室模拟利用碳酸氢铵溶液和 LaCl 为原料来制备碳酸镧。为避免生成碱式碳酸镧
3
[La(OH)CO ],整个反应在较低的pH条件下进行。
3
(1)某化学兴趣小组利用下列装置在实验室中用碳酸氢铵制备碳酸镧。
①在实验室用装置甲还可以制取下列气体中的________(填字母)。A.O B.Cl C.H D.NO E.SO F.C H G.C H
2 2 2 2 2 2 2 4
②仪器X的作用是________。
③ 实 验 中 应 先 打 开 K , 再 打 开 K , 原 因 是
2 1
_____________________________________________
_______________________________________________________________________________
。
④为保证碳酸镧的纯度,实验过程中需要注意的问题有_____________________________(答
一条即可)。
(2)碳酸钠或碳酸氢钠与氯化镧反应均可生成碳酸镧。
① 为 了 高 磷 血 症 患 者 的 安 全 , 通 常 选 用 碳 酸 氢 钠 溶 液 , 优 点 是
____________________________
___________________________________________________________________(答一条即可)。
②NaHCO 与LaCl 反应过程中会发生两个平行反应,其离子方程式为A._________________
3 3
和B.H++HCO===CO↑+HO。
2 2
答案 (1)①CD ②防倒吸 ③NH 在水中溶解度大,而 CO 在水中溶解度小,先通入
3 2
NH ,可提高CO 利用率 ④控制氨气(或CO)的通入量
3 2 2
(2)① 碳 酸 氢 钠 溶 液 碱 性 相 对 较 弱 , 可 防 止 生 成 碱 式 碳 酸 镧 ② 2La3 + +
3HCO===La(CO)↓+3H+
2 3 3
解析 (1)②仪器X为球形干燥管,从d口通入的是极易溶于水的氨气,倒置的球形干燥管
能防倒吸。③氨气是极易溶于水的气体,而二氧化碳气体在水中溶解度小,实验中先通入氨
气形成碱性溶液后,再通入二氧化碳,能够增大二氧化碳的溶解量,有利于碳酸氢根离子的
生成,则实验中应先打开K ,再打开K 。④由题意可知,为避免生成碱式碳酸镧,整个反
2 1
应在较低的pH条件下进行,则为保证碳酸镧的纯度,实验过程中应控制氨气或二氧化碳的
通入量,防止生成碱式碳酸镧,影响产品纯度。(2)①相对于碳酸钠溶液而言,碳酸氢钠在
溶液中的水解程度小于碳酸钠,溶液的碱性较弱,可防止生成碱式碳酸镧。
14.某化学兴趣小组的同学为测定某NaCO 和NaCl的固体混合物样品中NaCO 的质量分
2 3 2 3
数进行了以下实验。回答下列问题:
(1)甲同学用图 1 所示装置测定 CO 的质量。实验时稀硫酸与样品中的________(填
2
“NaCO”或“NaCl”)发生反应,仪器b的名称是________,洗气瓶c中盛装的是浓硫酸,
2 3
作 用 是
_______________________________________________________________________________
_______________________________________________________________________________。
(2)乙同学用图2所示装置,取一定质量的样品(m g)和足量稀硫酸反应进行实验,完成样品
中NaCO 质量分数的测定。
2 3
①实验前,检查该装置气密性的方法是先打开活塞a,向仪器b中注入水至其下端玻璃管中
形成一段水柱,再将针筒活塞向内推压,若仪器b下端玻璃管中的________________,则装
置气密性良好。
②在实验完成时,能直接测得的数据是CO 的________(填“体积”或“质量”)。
2
(3)丙同学用下图所示方法和步骤进行实验。
①操作Ⅰ涉及的实验名称有________、洗涤;操作Ⅱ涉及的实验名称有干燥、________。
②丙同学测得样品中NaCO 的质量分数为__________________________________________。
2 3
答案 (1)Na CO 分液漏斗 除去CO 中的水蒸气 (2)①液面上升 ②体积
2 3 2
(3)①过滤 称量 ②×100%
解析 (2)①将针筒活塞向内推压,增大了容器中的压强,若仪器b下端玻璃管中的液面上
升,则装置气密性良好。②CO 是气体,故能直接测得的数据是 CO 的体积。(3)根据
2 2
NaCO +Ba(OH) ===BaCO ↓+2NaOH,n(Na CO)=n(BaCO)= mol,所以NaCO 的质量
2 3 2 3 2 3 3 2 3
分数为×100%。