文档内容
第 71 讲 简单实验方案的设计与评价
[复习目标] 掌握简单实验方案设计与评价解题的一般思路。
1.一般解题思路
2.解题基本原则
(1)科学性原则
设计实验的科学性是指设计实验的原理正确、程序合理、方法得当。如鉴别 BaSO 和BaSO
3 4
沉淀是否溶于酸时,如果选用HNO 等具有氧化性的酸就不符合科学性原则。
3
(2)安全性原则
设计实验时应尽量避免选择有毒、有害的化学药品;尽量避免设计具有危险性的实验操作,
并且对实验中可能存在的安全隐患采取必要的措施,如装置气密性的检查、可燃性气体的检
验、蒸馏操作中在蒸馏的液体中放入沸石等。
(3)可行性原则
可行性原则是指实验设计应切实可行,具备可操作性,也就是说所选用的化学药品、实验仪
器和实验方法等在中学实验室中能够进行。一、物质检验类实验方案的评价
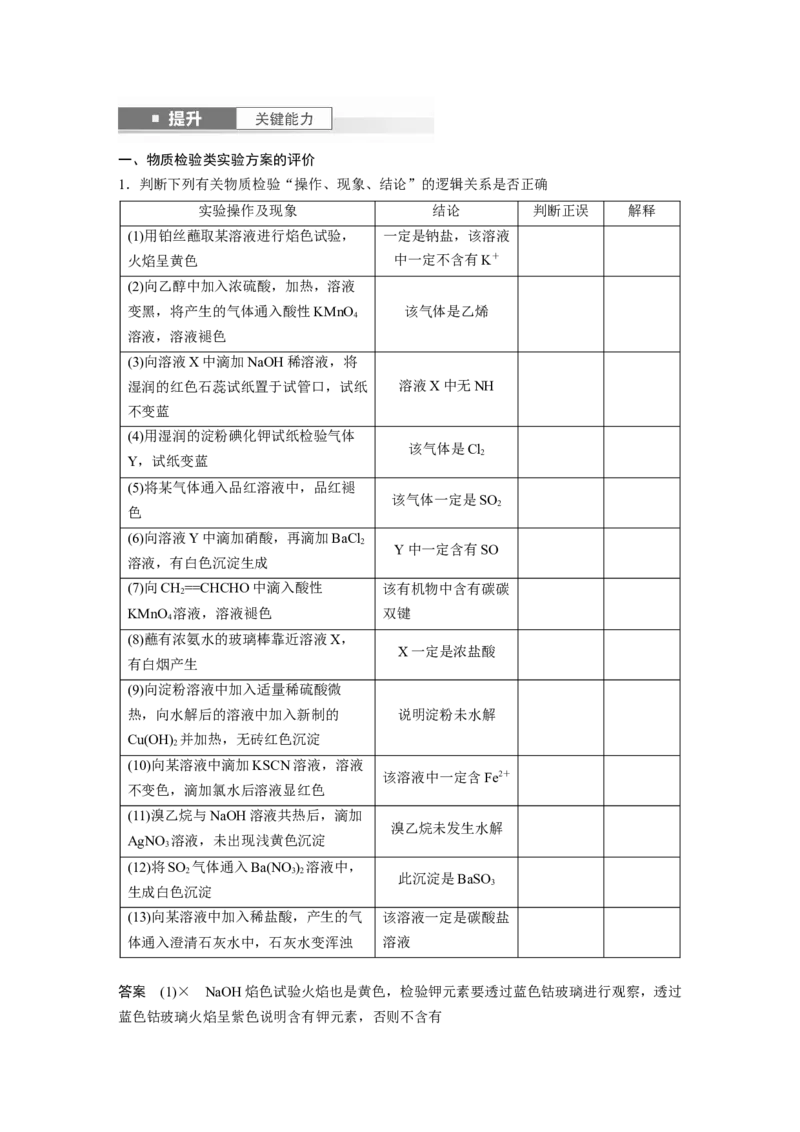
1.判断下列有关物质检验“操作、现象、结论”的逻辑关系是否正确
实验操作及现象 结论 判断正误 解释
(1)用铂丝蘸取某溶液进行焰色试验, 一定是钠盐,该溶液
火焰呈黄色 中一定不含有K+
(2)向乙醇中加入浓硫酸,加热,溶液
变黑,将产生的气体通入酸性KMnO 该气体是乙烯
4
溶液,溶液褪色
(3)向溶液X中滴加NaOH稀溶液,将
湿润的红色石蕊试纸置于试管口,试纸 溶液X中无NH
不变蓝
(4)用湿润的淀粉碘化钾试纸检验气体
该气体是Cl
2
Y,试纸变蓝
(5)将某气体通入品红溶液中,品红褪
该气体一定是SO
2
色
(6)向溶液Y中滴加硝酸,再滴加BaCl
2
Y中一定含有SO
溶液,有白色沉淀生成
(7)向CH==CHCHO中滴入酸性 该有机物中含有碳碳
2
KMnO 溶液,溶液褪色 双键
4
(8)蘸有浓氨水的玻璃棒靠近溶液X,
X一定是浓盐酸
有白烟产生
(9)向淀粉溶液中加入适量稀硫酸微
热,向水解后的溶液中加入新制的 说明淀粉未水解
Cu(OH) 并加热,无砖红色沉淀
2
(10)向某溶液中滴加KSCN溶液,溶液
该溶液中一定含Fe2+
不变色,滴加氯水后溶液显红色
(11)溴乙烷与NaOH溶液共热后,滴加
溴乙烷未发生水解
AgNO 溶液,未出现浅黄色沉淀
3
(12)将SO 气体通入Ba(NO ) 溶液中,
2 3 2
此沉淀是BaSO
3
生成白色沉淀
(13)向某溶液中加入稀盐酸,产生的气 该溶液一定是碳酸盐
体通入澄清石灰水中,石灰水变浑浊 溶液
答案 (1)× NaOH焰色试验火焰也是黄色,检验钾元素要透过蓝色钴玻璃进行观察,透过
蓝色钴玻璃火焰呈紫色说明含有钾元素,否则不含有(2)× 未反应的乙醇,生成的乙烯、SO 都能使酸性KMnO 溶液褪色
2 4
(3)× NH 极易溶于水,在溶液中加入NaOH稀溶液,生成的氨水浓度小,不加热时 NH
3 3
不会逸出
(4)× 淀粉碘化钾试纸检验的是具有强氧化性的气体,Y可能是Cl ,也可能是O 、NO 等
2 3 2
气体
(5)× O、Cl 也能使品红溶液褪色
3 2
(6)× 若溶液Y中含有SO,滴加硝酸时能被氧化成SO,加入BaCl 也会有白色沉淀产生
2
(7)× 碳碳双键和醛基都能使酸性高锰酸钾溶液褪色,故用KMnO 溶液无法证明分子中含
4
有碳碳双键
(8)× 只要是挥发性的浓酸遇蘸有浓氨水的玻璃棒都能产生白烟,浓盐酸、浓硝酸都符合
(9)× 稀硫酸在淀粉水解实验中作催化剂,在未中和硫酸的情况下加入的新制的 Cu(OH)
2
会与硫酸反应生成CuSO ,在加热时得不到沉淀,应该先加氢氧化钠中和硫酸后再加新制的
4
Cu(OH)
2
(10)√ Fe2+的检验方法正确
(11)× NaOH与AgNO 溶液反应生成的AgOH极不稳定,分解生成棕褐色的氧化银,干扰
3
溴离子的检验,应该先加稀硝酸中和NaOH后再加AgNO 溶液
3
(12)× HSO 是中强酸,电离出的H+与溶液中的NO能将SO氧化成SO,故该白色沉淀是
2 3
BaSO
4
(13)× 碳酸氢盐、亚硫酸盐、亚硫酸氢盐溶液也有相同现象
二、原理或性质探究类实验方案分析评价
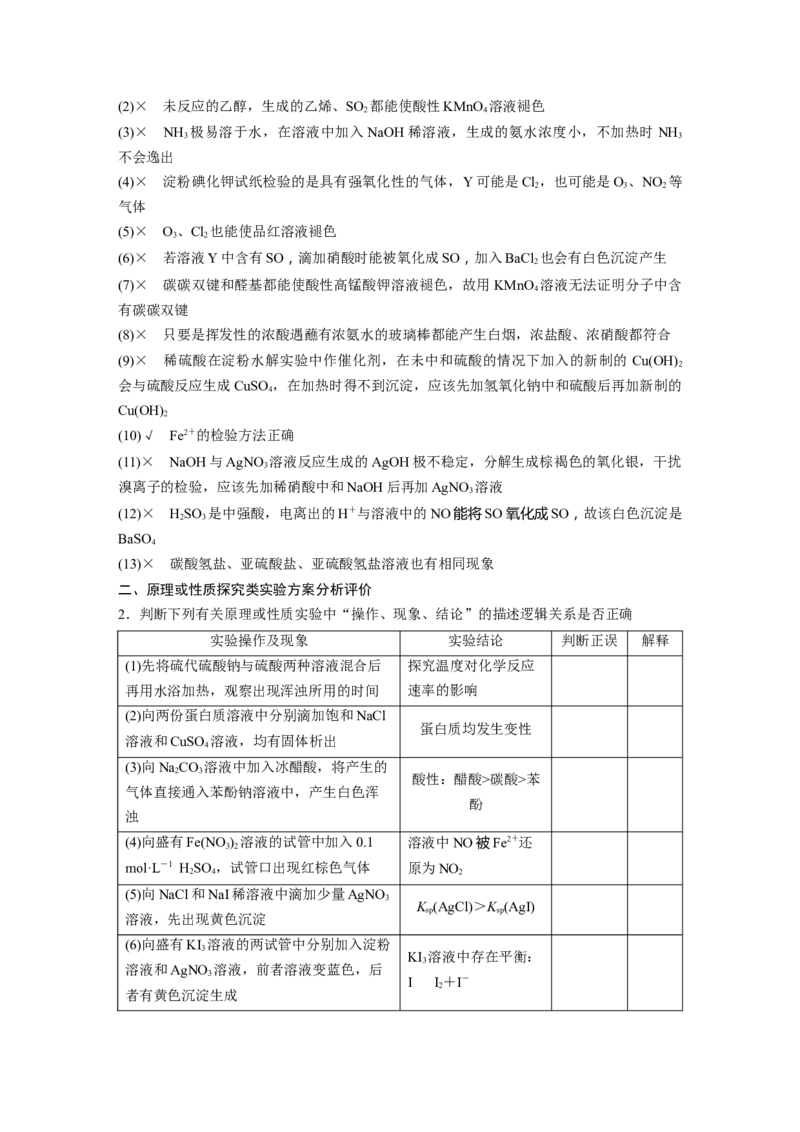
2.判断下列有关原理或性质实验中“操作、现象、结论”的描述逻辑关系是否正确
实验操作及现象 实验结论 判断正误 解释
(1)先将硫代硫酸钠与硫酸两种溶液混合后 探究温度对化学反应
再用水浴加热,观察出现浑浊所用的时间 速率的影响
(2)向两份蛋白质溶液中分别滴加饱和NaCl
蛋白质均发生变性
溶液和CuSO 溶液,均有固体析出
4
(3)向NaCO 溶液中加入冰醋酸,将产生的
2 3
酸性:醋酸>碳酸>苯
气体直接通入苯酚钠溶液中,产生白色浑
酚
浊
(4)向盛有Fe(NO ) 溶液的试管中加入0.1 溶液中NO被Fe2+还
3 2
mol·L-1 HSO ,试管口出现红棕色气体 原为NO
2 4 2
(5)向NaCl和NaI稀溶液中滴加少量AgNO
3
K (AgCl)>K (AgI)
sp sp
溶液,先出现黄色沉淀
(6)向盛有KI 溶液的两试管中分别加入淀粉
3
KI 溶液中存在平衡:
3
溶液和AgNO 溶液,前者溶液变蓝色,后
3
II+I-
2
者有黄色沉淀生成HS-水解程度大于其
(7)向NaHS溶液中滴入酚酞,溶液变红色
电离程度
答案 (1)× 探究温度对化学反应速率的影响,要先将混合液加热到所需要的温度后再混
合,若先混合则会发生反应,影响实验的判断,且需设置对照实验
(2)× 向蛋白质溶液中加入饱和氯化钠溶液发生盐析
(3)× 醋酸具有挥发性,生成的CO 气体中混有挥发出的醋酸,苯酚钠溶液变浑浊可能是
2
因为CO,也可能是因为醋酸,无法比较碳酸与苯酚的酸性强弱
2
(4)× 还原产物是NO,在试管口被氧化为NO
2
(5)× NaCl和NaI溶液的浓度未知,无法比较K 大小
sp
(6)√ 使淀粉溶液显蓝色的一定是I,与AgNO 反应生成黄色沉淀的是I-,所以KI 溶液中
2 3 3
存在I 和I-,故可推知I存在平衡
2
(7)√ HS-水解生成OH-:HS-+HOHS+OH-,HS-电离生成H+:HS-S2-+H
2 2
+,溶液呈碱性,说明HS-的水解程度大于其电离程度
1.(2022·江苏,11)室温下,下列实验探究方案不能达到探究目的的是( )
选项 探究方案 探究目的
向盛有FeSO 溶液的试管中滴加几滴KSCN溶液,振
4
A Fe2+具有还原性
荡,再滴加几滴新制氯水,观察溶液颜色变化
向盛有SO 水溶液的试管中滴加几滴品红溶液,振
2
B SO 具有漂白性
2
荡,加热试管,观察溶液颜色变化
向盛有淀粉-KI溶液的试管中滴加几滴溴水,振荡,
C Br 的氧化性比I 的强
2 2
观察溶液颜色变化
D 用pH计测量醋酸、盐酸的pH,比较溶液pH大小 CHCOOH是弱电解质
3
答案 D
解析 向盛有FeSO 溶液的试管中滴加几滴KSCN溶液,无现象,振荡,再滴加几滴新制氯
4
水,溶液变为红色,亚铁离子被新制氯水氧化,说明 Fe2+具有还原性,A正确;SO 具有漂
2
白性,可以和有色物质结合为无色物质,但不稳定,加热易分解,又恢复原来的颜色,B正
确;向盛有淀粉-KI溶液的试管中滴加几滴溴水,振荡,溶液变为蓝色,说明 Br 的氧化性
2
比I 的强,C正确;用pH计测量醋酸、盐酸的pH来证明CHCOOH是弱电解质时,需要测
2 3
量物质的量浓度相同的醋酸和盐酸,D错误。
2.(2022·辽宁,13)下列实验能达到目的的是( )
实验目的 实验方法或操作酸碱中和滴定的同时,用温度传感器采集
A 测定中和反应的反应热
锥形瓶内溶液的温度
量取同体积不同浓度的NaClO溶液,分别
B 探究浓度对化学反应速率的影响 加入等体积等浓度的NaSO 溶液,对比现
2 3
象
将NaCO 溶液与BaCl 溶液混合,反应后
2 3 2
C 判断反应后Ba2+是否沉淀完全
静置,向上层清液中再加1滴NaCO 溶液
2 3
D 检验淀粉是否发生了水解 向淀粉水解液中加入碘水
答案 C
解析 酸碱中和滴定操作中没有很好的保温措施,热量损失较多,不能用于测定中和反应的
反应热,A错误;NaClO和NaSO 反应无明显现象,无法根据现象探究浓度对化学反应速
2 3
率的影响,B错误;若有浑浊产生,则说明Ba2+没有沉淀完全,反之,则沉淀完全,C正确;
检验淀粉是否发生了水解,应检验是否有淀粉的水解产物(葡萄糖)存在,可用银氨溶液或新
制的氢氧化铜检验,D错误。
3.根据实验目的,下列实验及现象、结论都正确的是( )
选项 实验目的 实验及现象 结论
A.(2022·全国甲 检验铁锈中是否 将铁锈溶于浓盐酸,滴入KMnO 铁锈中含有二
4
卷,13B) 含有二价铁 溶液,紫色褪去 价铁
取少量待测样品溶于蒸馏水,加
B.(2021·浙江6 探究NaSO 固
2 3
入足量稀盐酸,再加入足量 样品已经变质
月选考,25D) 体样品是否变质
BaCl 溶液,有白色沉淀产生
2
C.(2022·全国甲 检验乙醇中是否 向乙醇中加入一小粒金属钠,产
乙醇中含有水
卷,13D) 含有水 生无色气体
向X溶液中滴加几滴新制氯水,
D.(2019·江苏, 检验X溶液中 X溶液中一定
振荡,再加入少量KSCN溶液,
13A) 是否含有Fe2+ 含有Fe2+
溶液变为红色
答案 B
解析 浓盐酸也能与KMnO 发生反应,使溶液紫色褪去,A错误;加入稀盐酸,亚硫酸根
4
离子会转化为二氧化硫气体,加入氯化钡生成的沉淀只能是硫酸钡沉淀,可以说明样品已经
变质,B正确;乙醇和水均会与金属钠发生反应生成氢气,C错误;先滴加氯水,再加入
KSCN溶液,溶液变红,说明加入KSCN溶液前溶液中存在Fe3+,但不能确定Fe3+是否由
Fe2+氧化而来,故D错误。
4.(2022·全国乙卷,10)由实验操作和现象,可得出相应正确结论的是( )选项 实验操作 现象 结论
向NaBr溶液中滴加过量
A 氯水,再加入淀粉-KI溶 先变橙色,后变蓝色 氧化性:Cl>Br >I
2 2 2
液
向蔗糖溶液中滴加稀硫
B 酸,水浴加热,加入新制 无砖红色沉淀 蔗糖未发生水解
的Cu(OH) 悬浊液
2
石蜡油加强热,将产生的
C 溶液由红棕色变无色 气体中含有不饱和烃
气体通入Br 的CCl 溶液
2 4
加热试管中的聚氯乙烯薄 试管口湿润的蓝色石
D 氯乙烯加聚是可逆反应
膜碎片 蕊试纸变红
答案 C
解析 过量的氯水可以将碘离子氧化为碘单质,无法证明溴单质的氧化性强于碘单质,A错
误;向蔗糖溶液中滴加稀硫酸,水浴加热后,应先加入氢氧化钠溶液使体系呈碱性,再加新
制氢氧化铜悬浊液检验,若不加氢氧化钠,未反应的稀硫酸会和新制的氢氧化铜反应,则不
会产生砖红色沉淀,不能说明蔗糖未发生水解,B错误;聚氯乙烯加强热会发生焦化、分解
反应,产生能使湿润的蓝色石蕊试纸变红的气体,说明产生了氯化氢,与氯乙烯加聚反应条
件不同,不能说明氯乙烯加聚是可逆反应,D错误。
课时精练
1.(2023·浙江1月选考,16)探究铁及其化合物的性质,下列方案设计、现象和结论都正确
的是( )
选项 实验方案 现象 结论
短时间内无明显
A 向FeCl 溶液中加入Zn片 Fe2+的氧化能力比Zn2+弱
2
现象
往Fe (SO ) 溶液中滴加KSCN 溶液先变成红色 Fe3+与SCN-的反应不可
2 4 3
B
溶液,再加入少量KSO 固体 后无明显变化 逆
2 4
将食品脱氧剂样品中的还原铁 食品脱氧剂样品中没有+3
C 溶液呈浅绿色
粉溶于盐酸,滴加KSCN溶液 价铁
Fe3+先水解得Fe(OH) 胶
3
向沸水中逐滴滴加5~6滴饱和 溶液先变成红褐
D 体,再聚集成Fe(OH) 沉
3
FeCl 溶液,持续煮沸 色再析出沉淀
3
淀答案 D
解析 FeCl 溶液中加入Zn片,Fe2++Zn===Fe+Zn2+,溶液由浅绿色变为无色,Fe2+的氧
2
化能力比Zn2+强,A错误;溶液变成红色的原因为Fe3++3SCN-Fe(SCN) ,与SO和K+
3
无关,B错误;Fe3+可能先与单质铁反应生成Fe2+,则溶液呈浅绿色,C错误;向沸水中逐
滴滴加饱和氯化铁溶液,制取Fe(OH) 胶体,继续加热则胶体因聚沉变为沉淀,D正确。
3
2.(2021·湖南,3)下列实验设计不能达到实验目的的是( )
实验目的 实验设计
取少量待测液,滴加KSCN溶液,观察溶液
A 检验溶液中FeSO 是否被氧化
4
颜色变化
气体依次通过盛有饱和NaCl溶液、浓HSO
2 4
B 净化实验室制备的Cl
2
的洗气瓶
将待测液滴在湿润的pH试纸上,与标准比
C 测定NaOH溶液的pH
色卡对照
D 工业酒精制备无水乙醇 工业酒精中加生石灰,蒸馏
答案 C
解析 若Fe2+被氧化为Fe3+,Fe3+能与SCN-生成Fe(SCN) ,溶液变成红色,能达到实验目
3
的,故A不符合题意;实验室用浓盐酸和二氧化锰加热制氯气,先用饱和食盐水除去混有
的氯化氢,再通过盛有浓硫酸的洗气瓶干燥,能达到实验目的,故 B不符合题意;用pH试
纸测定NaOH溶液的pH,不能润湿pH试纸,否则会因浓度减小而影响测定结果,不能达
到实验目的,故C符合题意;制取无水乙醇时,通常把工业酒精和新制的生石灰混合,加
热蒸馏,能达到实验目的,故D不符合题意。
3.(2021·辽宁,9)由下列实验操作及现象能得出相应结论的是( )
实验操作 现象 结论
向KBr、KI混合溶液中依次加入少量氯水 溶液分层,下 氧化性:
A
和CCl ,振荡,静置 层呈紫红色 Cl>Br >I
4 2 2 2
B 在火焰上灼烧搅拌过某无色溶液的玻璃棒 火焰出现黄色 溶液中含Na元素
用pH计测定pH:
HCO 酸性弱于
2 3
C ①NaHCO 溶液 pH:①>②
3
CHCOOH
3
②CHCOONa溶液
3
把水滴入盛有少量NaO 的试管中,立即
2 2
D 木条复燃 反应生成了O
2
把带火星木条放在试管口
答案 D解析 根据实验操作和现象,说明反应产生I,发生反应:2KI+Cl===2KCl+I,证明氧化
2 2 2
性:Cl>I ,Br >I ,但不能比较Br 与Cl 的氧化性强弱,A错误;玻璃中含有Na元素,因
2 2 2 2 2 2
此灼烧时火焰呈黄色,不能证明溶液中含Na元素,B错误;应该采用对照方法进行实验,
但两种溶液的浓度未知,盐的种类也不同,因此不能通过测定溶液的pH来判断HCO 、
2 3
CHCOOH的酸性强弱,C错误;氧气有助燃性,木条复燃,可以证明NaO 与水反应产生
3 2 2
了O,D正确。
2
4.(2023·哈尔滨三中校考模拟)化学实验源于生活。下列实验方案设计、现象与结论均正确
的是( )
选项 目的 方案设计 现象与结论
取少量菠菜叶剪碎研磨后加水搅
若溶液变红,说明
A 检验菠菜中的铁元素 拌,取上层清液于试管中,加入
菠菜中含有铁元素
稀硝酸后再加入KSCN溶液
将几根未燃过的火柴头浸入水 若有白色沉淀产
检验火柴头中是否含
B 中,稍后取少量溶液于试管中, 生,说明火柴头中
有氯元素(ClO)
加入稀HNO、AgNO 溶液 含有氯元素
3 3
溶液颜色不变,说
检验食盐中是否含有
C 向某食盐溶液中滴加淀粉溶液 明该食盐属于无碘
碘元素
盐
一段时间后鸡皮变
检验鸡皮中是否含有 取一小块鸡皮于表面皿上,将几
D 黄,说明鸡皮中含
脂肪 滴浓硝酸滴到鸡皮上
有脂肪
答案 A
解析 亚铁离子被硝酸氧化为铁离子,铁离子能使KSCN溶液变红色,若溶液变红,说明
菠菜中含有铁元素,故A符合题意;溶液中氯酸根离子不能和银离子反应生成氯化银沉淀,
故B不符合题意;碘单质能使淀粉溶液变蓝色,溶液颜色不变,说明该食盐不含碘单质,
不能说明不含碘元素,故C不符合题意;某些蛋白质遇浓硝酸变黄色,一段时间后鸡皮变
黄,说明鸡皮中含有蛋白质,故D不符合题意。
5.(2023·湖南衡阳校联考模拟)实验是化学研究的重要方法。下列实验设计能达到实验目的
的是( )
选项 实验目的 实验设计
用洁净的铂丝蘸取该溶液,在酒精灯
A 检验NaCl溶液中是否存在KCl杂质
外焰上灼烧,观察火焰是否出现紫色
B 检验敞口放置的NaOH溶液是否变质 取样,滴加酚酞试液,观察颜色
将混合气体通入盛有硫酸铜溶液的洗
C 除去乙炔气体中的硫化氢
气瓶中配制100 mL 1.00 mol·L-1 称取4.0 g NaOH固体溶解在100 mL
D
NaOH溶液 容量瓶中,再定容、摇匀
答案 C
解析 观察钾元素的焰色需要透过蓝色钴玻璃,故 A不符合题意;硫酸铜溶液可吸收硫化
氢而不吸收乙炔,从而能达到除杂的目的,故C符合题意;容量瓶不能直接溶解物质,故D
不符合题意。
6.(2023·江苏南通统考模拟)室温下,下列实验探究方案能达到探究目的的是( )
选项 探究方案 探究目的
向盛有少量酸性KCr O 溶液的试管中滴加足量乙
2 2 7
A 乙醇具有还原性
醇,充分振荡,观察溶液颜色变化
B 用铂丝蘸取某溶液进行焰色试验,观察火焰颜色 溶液中存在NaCO
2 3
C 将SO 通入酸性高锰酸钾溶液中,观察溶液颜色变化 SO 具有漂白性
2 2
将中间裹有锌皮的铁钉放在滴有酚酞的饱和NaCl溶
D 铁钉能发生吸氧腐蚀
液中,一段时间后观察铁钉周围溶液颜色变化
答案 A
解析 向盛有少量酸性KCr O 溶液的试管中滴加足量乙醇,充分振荡,若溶液由橙色变为
2 2 7
绿色,说明KCr O 被还原为Cr3+,则乙醇表现还原性,故A符合题意;焰色试验只能确定
2 2 7
金属元素是否存在,不能确定具体物质,故B不符合题意;锌比铁活泼,形成原电池时Zn
作负极,Fe作正极,铁钉不被腐蚀,故D不符合题意。
7.(2024·南昌模拟)下列方案设计、现象和结论不正确的是( )
选项 目的 方案设计 现象和结论
将去除氧化膜的铝片放入浓硝
探究铝在浓硝酸 铝片表面未见紫红色固
酸中,片刻后取出,立即用水
A 中会形成致密氧 体,说明铝片表面已形成
洗净,并快速放入硫酸铜溶液
化膜 致密的氧化膜
中
探究Fe2+、Br- 向FeBr 溶液中加入少量氯水, 若CCl 层无色,则Fe2+的
2 4
B
的还原性强弱 再加CCl 萃取 还原性强于Br-
4
取适量HO 溶液于试管中,滴 若产生的气体使带火星的
2 2
比较HO 和Fe3+
C 2 2 入Fe (SO ) 溶液,振荡,观察 木条复燃,说明Fe3+的氧
2 4 3
的氧化性强弱
现象 化性强于HO
2 2
若沸水中溶液颜色比冷水
探究温度对Fe3+ 向25 mL冷水和沸水中分别滴
D 中溶液颜色深,则说明升
水解程度的影响 入5滴饱和FeCl 溶液
3 温能促进Fe3+水解答案 C
解析 铝片表面形成致密氧化膜后,与铜离子不反应,故 A正确;CCl 层无色,说明氯气
4
未与溴离子反应,而是与亚铁离子反应,故B正确;产生的气体使带火星的木条复燃,可
能是铁离子的催化作用使双氧水分解,故C错误。
8.(2023·合肥统考一模)下列由实验操作和现象可得出正确结论的是( )
选项 实验操作和现象 结论
向鸡蛋清中加入饱和(NH )SO 溶液,有
4 2 4
A (NH )SO 使蛋白质变性
4 2 4
白色沉淀产生
向某溶液中滴加稀硫酸,将产生的气体
B 该溶液中可能含有SO
通入品红溶液,品红褪色
向Mg(OH) 悬浊液中加浓NH Cl溶液, 铵根离子水解显酸性,中和OH-,
2 4
C
沉淀溶解 促进反应
向0.1 mol·L-1HO 溶液中滴加0.1 mol·L
2 2
D HO 具有氧化性
2 2
-1KMnO 溶液,溶液褪色
4
答案 B
解析 硫酸铵溶液能使蛋白质发生盐析而不是变性,A错误;亚硫酸根离子和酸反应会生成
使品红褪色的二氧化硫气体,故该溶液中可能含有SO,B正确;高锰酸钾发生还原反应为
氧化剂,过氧化氢发生氧化反应体现还原性,D错误。
9.(2023·郑州统考一模)下列实验中,所采取的实验方法与对应实验原理都正确的是( )
选项 实验目的 实验方法 实验原理
分离乙酸乙酯和 乙酸乙酯和乙醇的密度
A 用分液漏斗分液
乙醇 不同
除去CO 中少量 SO 能与NaHCO 反应生
2 2 3
B 用饱和NaHCO 溶液洗气
3
的SO 成CO
2 2
检验溶液中的 滴加稀盐酸,产生无色无味且能 CO+2H+===HO+
2
C
CO 使澄清石灰水变浑浊的气体 CO↑
2
将混有HCl的Cl 通过饱和食盐
2
D 得到纯净的Cl HCl极易溶于水
2
水
答案 B
解析 乙酸乙酯和乙醇互溶,不能采取分液的方法分离,A错误;加入稀盐酸,产生无色无
味且能使澄清石灰水变浑浊的气体,不能说明溶液中一定含有CO,也可能含有HCO,C错
误;将混有HCl的Cl 通过饱和食盐水,可以除去HCl,但是Cl 中还会混有水蒸气,得不
2 2
到纯净的Cl,D错误。
2
10.(2023·陕西渭南统考一模)下列实验操作能达到实验目的的是( )选项 实验目的 操作
取5 mL 0.1 mol·L-1KI溶液于试管中,加入1 mL
探究KI与FeCl 反应的限
3
A 0.1 mol·L-1FeCl 溶液,充分反应后滴入5滴
3
度
15%KSCN溶液
证明Cu和浓HSO 反应生 向少量铜与浓HSO 反应后的溶液中慢慢加水,
2 4 2 4
B
成CuSO 溶液变蓝
4
证明木炭在加热时能与浓
C 将灼热的木炭加入浓硝酸中,有红棕色气体产生
硝酸发生反应
向试管中依次加入浓硫酸、乙醇、乙酸和碎瓷
D 实验室制备乙酸乙酯 片,加热,蒸出的乙酸乙酯用饱和碳酸钠溶液收
集
答案 A
解析 反应中碘离子过量,充分反应后滴入5滴15% KSCN溶液,若溶液变红色,说明KI
与FeCl 的反应存在限度,故A符合题意;不能向浓硫酸中加水,会产生危险,应将反应后
3
的溶液加入水中,故B不符合题意;浓硝酸受热也会分解产生二氧化氮气体,故 C不符合
题意;浓硫酸溶解放出大量的热,应先加入乙醇,再沿器壁慢慢加入浓硫酸、乙酸,故D
不符合题意。
11.(2023·辽宁葫芦岛统考模拟预测)根据下列实验操作和现象所得出的结论正确的是( )
选项 实验操作 实验现象 实验结论
向盛有饱和NaSO 溶液的试 溶液变浑浊且有气
2 2 3
A 生成了S和HS
2
管中滴加稀盐酸 泡逸出
向饱和食盐水中通入氨气至饱
B 溶液变浑浊 析出了NaHCO
3
和后,再通入过量二氧化碳
加热无水乙醇和浓HSO 的混
2 4
乙醇发生消去反应生成
C 合液至170 ℃,将气体通入 红色褪去
了乙烯
酸性KMnO 溶液
4
铜片不断溶解,而
铁片与铜片同导线相连,放入 铜单质的还原性强于铁
D 铁片表面无明显变
盛有浓硝酸的烧杯中 单质
化
答案 B
解析 向NaSO 溶液中滴加稀盐酸发生的反应为NaSO +2HCl===2NaCl+HO+S↓+
2 2 3 2 2 3 2
SO ↑,可观察到溶液变浑浊且有气体生成,但生成的气体是SO ,故A错误;饱和食盐水
2 2
中含有较多的 Na+,通入氨气至饱和后,再通入二氧化碳后产生较多的 HCO,析出
NaHCO 晶体,故B正确;加热无水乙醇和浓HSO 的混合液至170 ℃,产生的乙烯气体中
3 2 4含有挥发出的乙醇,而乙烯、乙醇都能使酸性KMnO 溶液褪色,因此酸性KMnO 溶液褪色
4 4
不能说明乙醇发生了消去反应,故C错误。
12.(2023·山东菏泽统考一模)下列实验操作能达到相应实验目的的是( )
选项 实验目的 实验操作
用洁净的玻璃棒蘸取少许“84”消毒液滴在pH
A 测定“84”消毒液的pH
试纸上
向2 mL 1 mol·L-1 NaOH溶液中加入2 mL 1
验证Mg(OH) 可以转化为 mol·
2
B
Fe(OH) L-1 MgCl 溶液,产生白色沉淀,再加入几滴1
3 2
mol·L-1 FeCl 溶液
3
取少量固体溶于蒸馏水,滴加少量稀硫酸,再滴
C 检验Fe(NO ) 固体是否变质
3 2
入KSCN溶液,振荡,观察溶液颜色变化
向NaHCO 溶液中滴加足量稀盐酸,观察有无气
3
D 验证氯的非金属性强于碳
体产生
答案 B
解析 “84”消毒液的有效成分是次氯酸钠,具有漂白性,能使pH试纸褪色,所以不能用
pH试纸测定“84”消毒液的pH,应该用pH计,故A不符合题意;加入稀硫酸后,溶液中
含有氢离子和硝酸根离子,相当于含有硝酸,硝酸能将亚铁离子氧化为铁离子,故C不符
合题意;盐酸为无氧酸,由碳酸、盐酸的酸性强弱不能比较 C、Cl的非金属性强弱,故D
不符合题意。