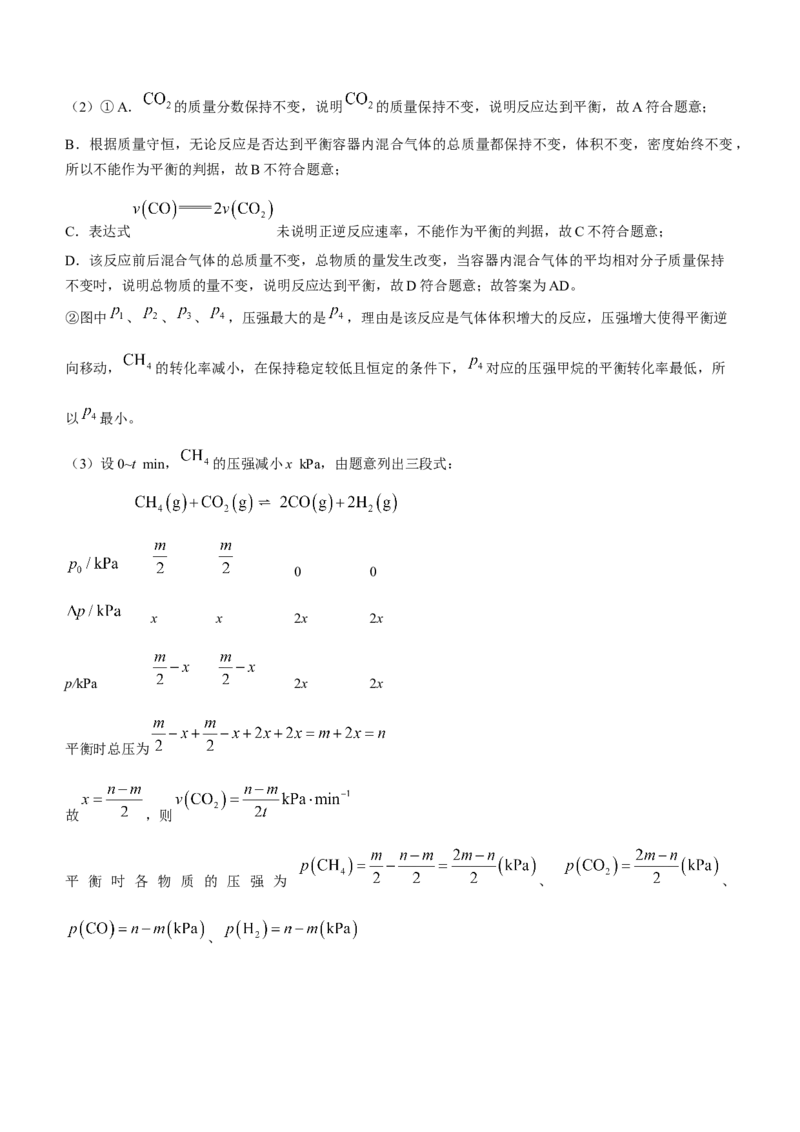文档内容
江淮十校2023届高三第一次联考
化学试题
2022.9
可能用到的相对原子质量:H—1 O—16 Ba—137 S—32 C1—35.5
一、选择题(本大题共16小题,每小题3分,共48分。每小题只有一项符合题目要求。)
1.下列诗词解读不正确的是( )
A.“芳菲夕雾起,暮色满房栊”,雾有丁达尔效应是因为胶粒对光有散射作用
B.“淘金岂假披沙得,不触波澜犹费力”,利用金与沙子的密度关系来达到分离目的
C.“编钟曾氏奏传奇,后母戊鼎树丰碑”,纯铜比青铜硬度大,熔点低
D.“肉芝石耳不足数,醋芼鱼皮真倚墙”,陈醋里的醋酸是弱电解质
2.下列各项表述正确的是( )
A. 和 均只含一种化学键 B. 的电子式为
C.KCl、 、 均为离子化合物 D. 的电子式可表示为
3.下列离子方程式对事实的表述正确的是( )
A.向碘化亚铁溶液中滴加少量稀硝酸:
B.向NaClO溶液中通入少量 :
C.向重水中加入 :
D.向硫代硫酸钠溶液中加入过量稀盐酸:
4.布洛芬是一种解热镇痛药,其结构如下。关于布洛芬,下列说法不正确的是( )
A.分子式为
B.能使酸性高锰酸钾溶液褪色C.1mol布洛芬最多可与4mol 发生加成反应
D.布洛芬分子中所有碳原子不可能共面
5.下列各组离子在指定的溶液中,一定能大量共存的是( )
A.澄清透明的溶液中: 、 、 、
B.能使酚酞变红的溶液中: 、 、 、
C.常温下,由水电离的 的溶液中: 、 、 、
D.无色溶液中: 、 、 、
6.某工业度水中含有大量的 和 ,都可以在碱性条件下被次氨酸钠氧化:反应①
,反应② ,再进行一系列操作,回收锰和铬,以沾到回收利用
且降低污染的目的。下列说法不正确的是( )
A.在氧化处理过程中用 代替NaClO效果更好
B.反应①中氧化剂与还原剂的物质的量之比为1:1
C.反应②为
D.在酸性条件下 转化为 不是氧化还原反应
7.随着工业的需要和制碱原料的改变,纯碱生产技术得到迅速的发展。世界最早工业生产碳酸钠的反应为
,下列说法正确的是( )
A.0.1mol 含有的离子总数为
B.1mol 中含有的质子数为
C.1mol/L 溶液中含有的钠离子个数为
D.反应生成0.1mol CaS转移电子的数目为
8.研究表明,采用新型铁改性的镍金属陶瓷作电极,可以增强对氨利用的催化活性,提高质子陶瓷燃料电池
的性能,工作原理如右图。下列说法正确的是( )A.Ni金属陶瓷电极作正极
B.电池工作时,电子经固体电解质向正极移动
C.负极的电极反应式为
D.标准状况下消耗22.4L氨气转移6mol
9.下列关于反应热的说法正确的是( )
A.a.
b.
若a、b反应放热,则
B.已知 ,则甲烷的燃烧热为
C. ,则常温下 比 更稳定
D. ,恒温恒压下达平衡后加入X,上述反应 增大
10.工业上以卤水(富含 )为原料用高分子树脂提取碘的工艺流程如图。下列说法不正确的是( )
A.“氧化1”过程既可以用氯气,也可以用过氧化氢溶液B.“解脱”可以用亚硫酸钠将碘单质还原为 ,离子方程式为
C.用高分子树脂“吸附”,再“解脱”是为了便于分离富集碘元素
D.“提纯”过程包括萃取分液、蒸馏得到粗产品,再利用升华法纯化
11.一学习小组探究 与 能否反应产生 。已知 固体易升华,其蒸气为黄色。实验装置
如下图,下列说法不正确的是( )
A.加热前需要先通氮气,排尽空气,并检查装置的气密性
B,加热一段时间后,装置A中产生黄色气体,说明反应生成了氯气
C.从安全角度出发,应在装置A、B之间应添加冷凝装置,防止堵塞导管
D.除了氯气外,升华的 、未除尽的 都可使B中溶液变蓝
12.X、Y、Z、M、Q是元素周期表中前20号主族元素,且原子序数依次增大。其中X、Y、Z、Q在不同的
周期,且Y、Z、Q三种元素最高价氧化物对应的水化物两两皆能反应,X、Y的最外层电子数之和等于M的
最外层电子数,下列说法正确的是( )
A.原子半径
B.Z和Q元素的单质均可通过电解其熔融态的氯化物得到
C.M的氧化物在标准状况下均为气体
D.Y的简单氢化物可作制冷剂
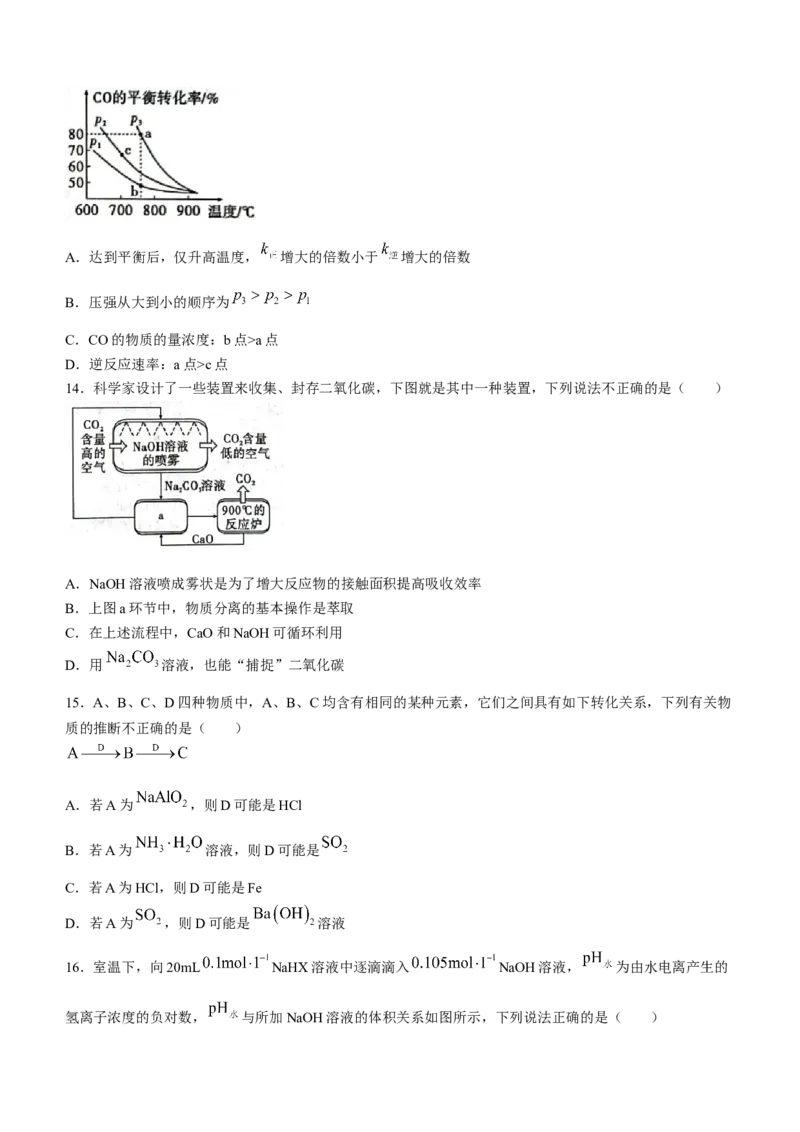
13.在密闭容器中充入1mol CO和1mol NO,在一定条件下发生反应:
,测得CO的平衡转化率与温度及压强的关系如图所示。实验测得, 、
( 、 速率常数,只与温度有关),下列说法不正确的是( )A.达到平衡后,仅升高温度, 增大的倍数小于 增大的倍数
B.压强从大到小的顺序为
C.CO的物质的量浓度:b点>a点
D.逆反应速率:a点>c点
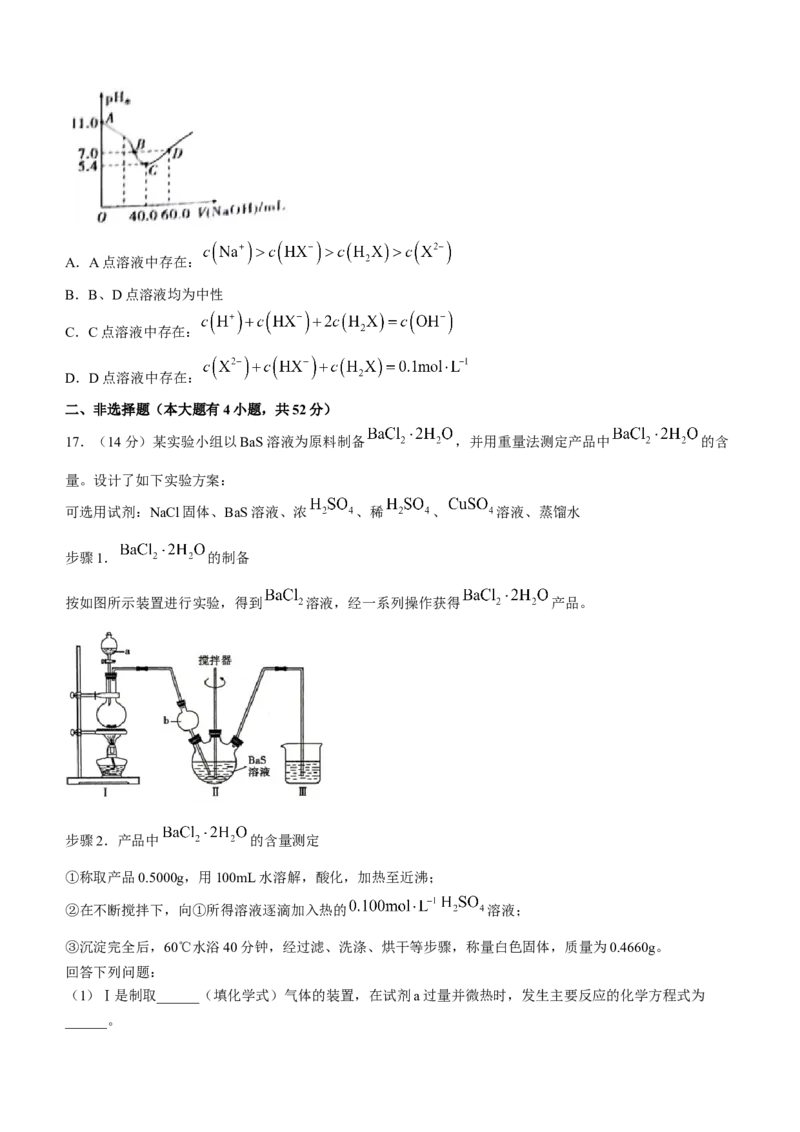
14.科学家设计了一些装置来收集、封存二氧化碳,下图就是其中一种装置,下列说法不正确的是( )
A.NaOH溶液喷成雾状是为了增大反应物的接触面积提高吸收效率
B.上图a环节中,物质分离的基本操作是萃取
C.在上述流程中,CaO和NaOH可循环利用
D.用 溶液,也能“捕捉”二氧化碳
15.A、B、C、D四种物质中,A、B、C均含有相同的某种元素,它们之间具有如下转化关系,下列有关物
质的推断不正确的是( )
A.若A为 ,则D可能是HCl
B.若A为 溶液,则D可能是
C.若A为HCl,则D可能是Fe
D.若A为 ,则D可能是 溶液
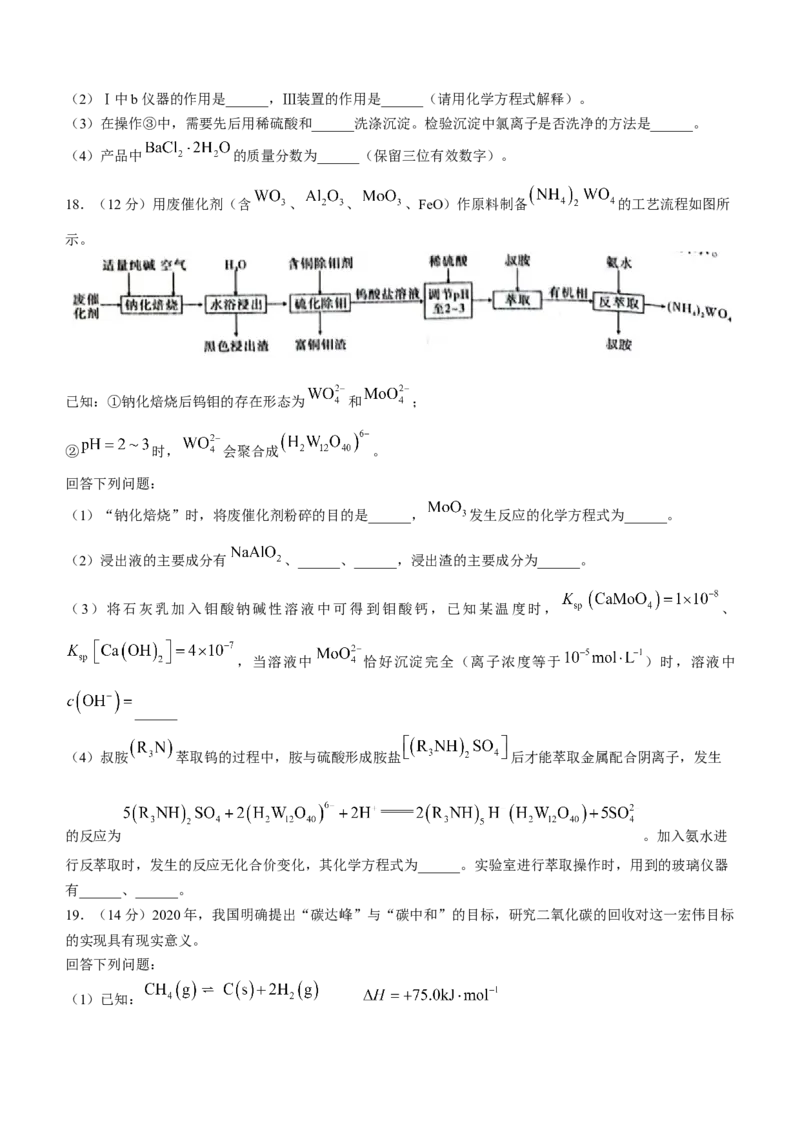
16.室温下,向20mL NaHX溶液中逐滴滴入 NaOH溶液, 为由水电离产生的
氢离子浓度的负对数, 与所加NaOH溶液的体积关系如图所示,下列说法正确的是( )A.A点溶液中存在:
B.B、D点溶液均为中性
C.C点溶液中存在:
D.D点溶液中存在:
二、非选择题(本大题有4小题,共52分)
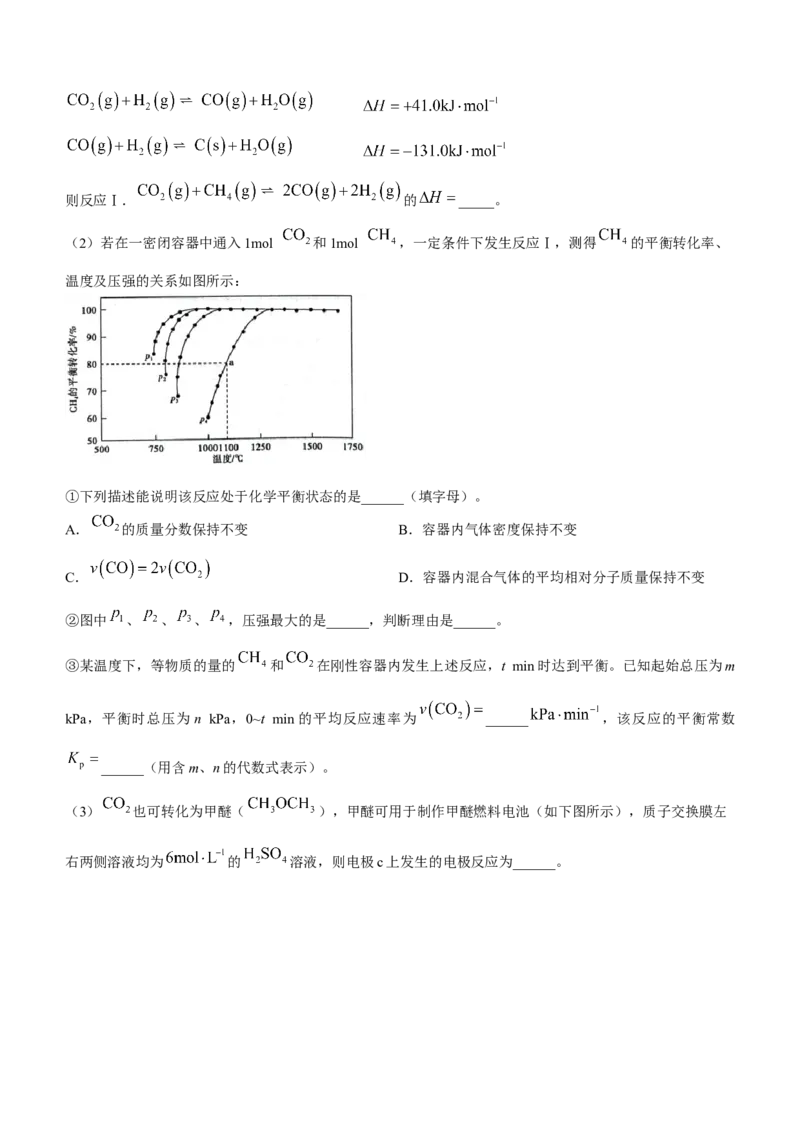
17.(14分)某实验小组以BaS溶液为原料制备 ,并用重量法测定产品中 的含
量。设计了如下实验方案:
可选用试剂:NaCl固体、BaS溶液、浓 、稀 、 溶液、蒸馏水
步骤1. 的制备
按如图所示装置进行实验,得到 溶液,经一系列操作获得 产品。
步骤2.产品中 的含量测定
①称取产品0.5000g,用100mL水溶解,酸化,加热至近沸;
②在不断搅拌下,向①所得溶液逐滴加入热的 溶液;
③沉淀完全后,60℃水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为0.4660g。
回答下列问题:
(1)Ⅰ是制取______(填化学式)气体的装置,在试剂a过量并微热时,发生主要反应的化学方程式为
______。(2)Ⅰ中b仪器的作用是______,Ⅲ装置的作用是______(请用化学方程式解释)。
(3)在操作③中,需要先后用稀硫酸和______洗涤沉淀。检验沉淀中氯离子是否洗净的方法是______。
(4)产品中 的质量分数为______(保留三位有效数字)。
18.(12分)用废催化剂(含 、 、 、FeO)作原料制备 的工艺流程如图所
示。
已知:①钠化焙烧后钨钼的存在形态为 和 ;
② 时, 会聚合成 。
回答下列问题:
(1)“钠化焙烧”时,将废催化剂粉碎的目的是______, 发生反应的化学方程式为______。
(2)浸出液的主要成分有 、______、______,浸出渣的主要成分为______。
(3)将石灰乳加入钼酸钠碱性溶液中可得到钼酸钙,已知某温度时, 、
,当溶液中 恰好沉淀完全(离子浓度等于 )时,溶液中
______
(4)叔胺 萃取钨的过程中,胺与硫酸形成胺盐 后才能萃取金属配合阴离子,发生
的反应为 。加入氨水进
行反萃取时,发生的反应无化合价变化,其化学方程式为______。实验室进行萃取操作时,用到的玻璃仪器
有______、______。
19.(14分)2020年,我国明确提出“碳达峰”与“碳中和”的目标,研究二氧化碳的回收对这一宏伟目标
的实现具有现实意义。
回答下列问题:
(1)已知:则反应Ⅰ. 的 _____。
(2)若在一密闭容器中通入1mol 和1mol ,一定条件下发生反应Ⅰ,测得 的平衡转化率、
温度及压强的关系如图所示:
①下列描述能说明该反应处于化学平衡状态的是______(填字母)。
A. 的质量分数保持不变 B.容器内气体密度保持不变
C. D.容器内混合气体的平均相对分子质量保持不变
②图中 、 、 、 ,压强最大的是______,判断理由是______。
③某温度下,等物质的量的 和 在刚性容器内发生上述反应,t min时达到平衡。已知起始总压为m
kPa,平衡时总压为n kPa,0~t min的平均反应速率为 ______ ,该反应的平衡常数
______(用含m、n的代数式表示)。
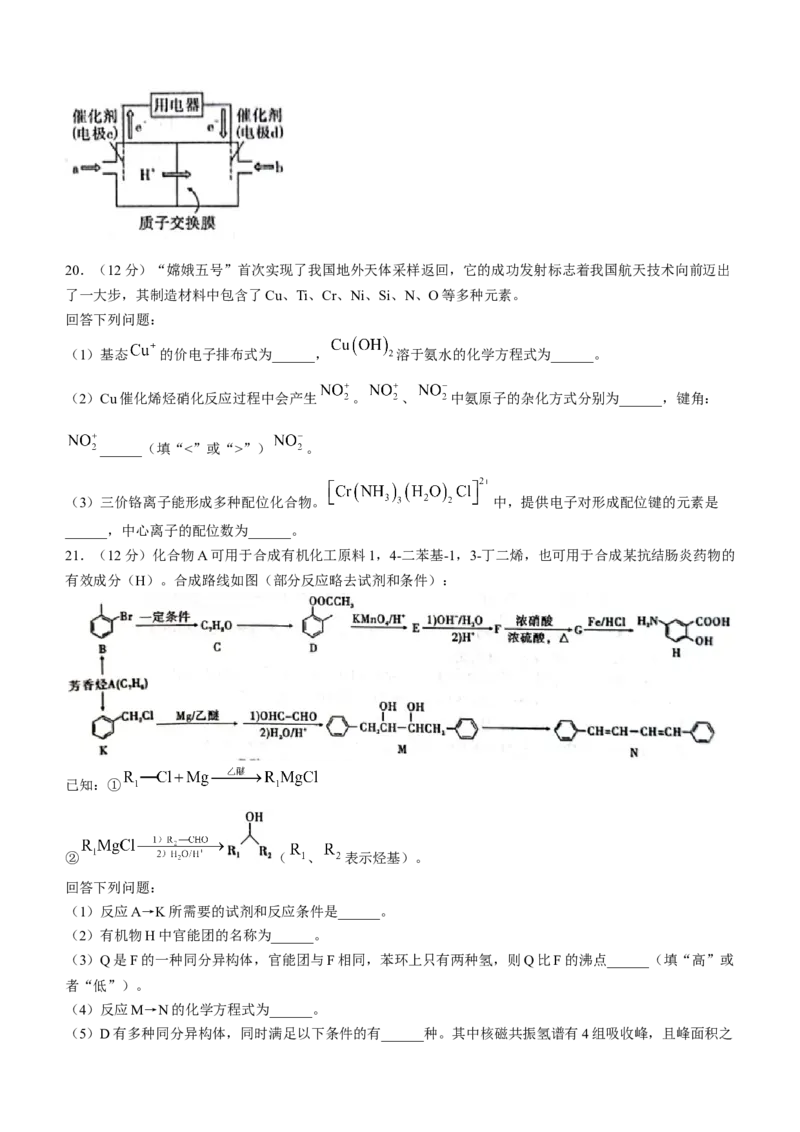
(3) 也可转化为甲醚( ),甲醚可用于制作甲醚燃料电池(如下图所示),质子交换膜左
右两侧溶液均为 的 溶液,则电极c上发生的电极反应为______。20.(12分)“嫦娥五号”首次实现了我国地外天体采样返回,它的成功发射标志着我国航天技术向前迈出
了一大步,其制造材料中包含了Cu、Ti、Cr、Ni、Si、N、O等多种元素。
回答下列问题:
(1)基态 的价电子排布式为______, 溶于氨水的化学方程式为______。
(2)Cu催化烯烃硝化反应过程中会产生 。 、 中氨原子的杂化方式分别为______,键角:
______(填“<”或“>”) 。
(3)三价铬离子能形成多种配位化合物。 中,提供电子对形成配位键的元素是
______,中心离子的配位数为______。
21.(12分)化合物A可用于合成有机化工原料1,4-二苯基-1,3-丁二烯,也可用于合成某抗结肠炎药物的
有效成分(H)。合成路线如图(部分反应略去试剂和条件):
已知:①
② ( 、 表示烃基)。
回答下列问题:
(1)反应A→K所需要的试剂和反应条件是______。
(2)有机物H中官能团的名称为______。
(3)Q是F的一种同分异构体,官能团与F相同,苯环上只有两种氢,则Q比F的沸点______(填“高”或
者“低”)。
(4)反应M→N的化学方程式为______。
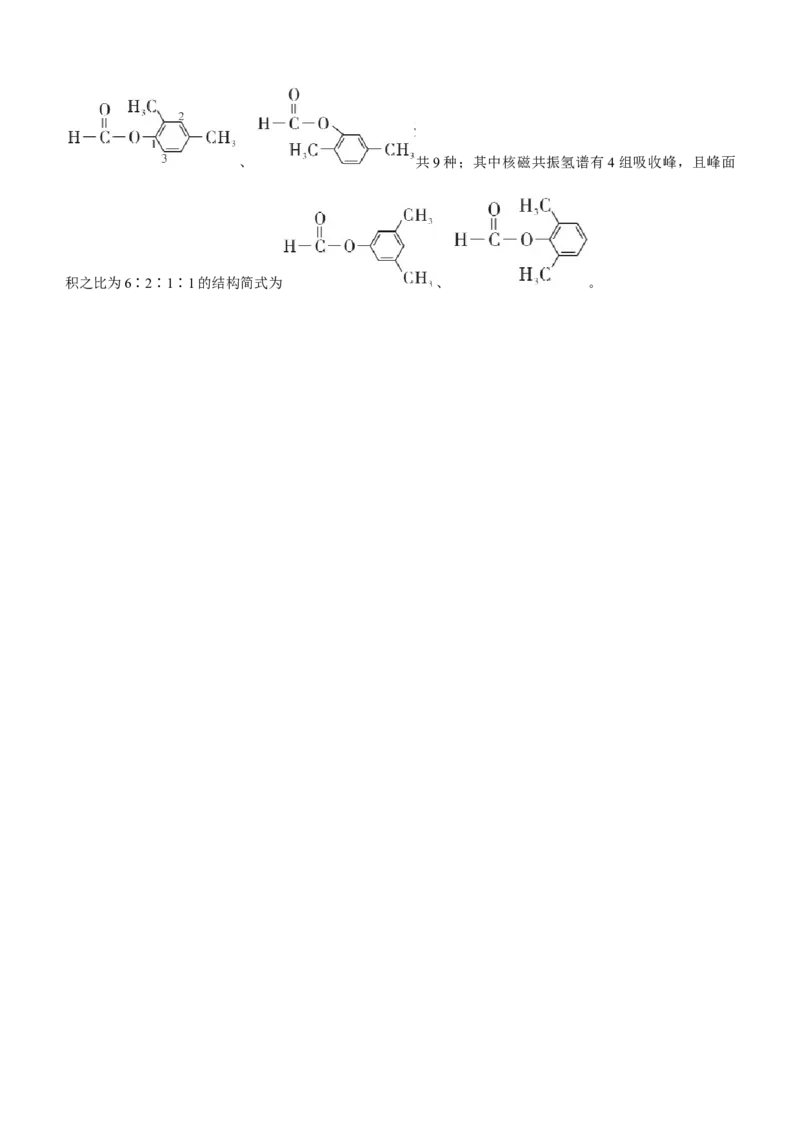
(5)D有多种同分异构体,同时满足以下条件的有______种。其中核磁共振氢谱有4组吸收峰,且峰面积之比为6∶2∶1∶1的结构简式为______(任写一种)。
①1mol该有机物能与2mol氢氧化钠溶液反应 ②能发生银镜反应
江淮十校2023届高三第一次联考
化学试题参考答案、提示及评分细则
一、选择题(本大题共16小题,每小题3分,共48分。每小题只有一项符合题目要求。)
题号 1 2 3 4 5 6 7 8
选项 C B D C B A D C
题号 9 10 11 12 13 14 15 16
选项 A B B D C B C C
1.答案C
A.雾是胶体,有丁达尔效应
B.金的密度大于沙
C.合金比金属单质硬度大
D.醋酸是弱电解质
2.答案B
A中 还含有共价键,B正确,C中 是共价化合物,D中 的电子式为 。
3.答案D
A.稀 少量,还原性: ,应该 先反应
B. 少量, 过量,∴ 与 不共存
C. 发生歧化反应, 中的O来自于
D.正确
4.答案C
A.正确,B.苯环上连烷基可使 褪色,C.与3mol 加成,D.正确。
5.答案B
A.酸性条件下, 可以氧化
B.碱性条件下,这些离子可大量共存
C.酸性条件下, 不能大量共存,碱性条件下, 不能大量共存
D. 是蓝色的
6.答案AA. 催化 分解,且 氧化性弱于 。
7.答案D
A中离子总数为 ,B中1mol 中有质子数 ,C未给体积,D正确。
8.答案C
A.电极a是 转化为 ,故失 为负极;
B.电子只在外中路中传输,固体电解质甲是质子移动;
C.正确;
D.由C可知,转移3mol 。
9.答案A
A.A(g)变为A(s)需放热,故反应a放热更多, 更小,A正确;
B.该反应生成气态水,燃烧热指生成液态水,D错误;
C.物质能量越低越稳定,C错误;
D.方程式不变,且是恒温条件,故 不变,D错误。
10.答案B
A.双氧水也能把碘离子氧化为单质碘,且不引入新杂质,“氧化1”可以用 溶液代替
B.“解脱”过程发生的反应为
C.由于海水中碘离子的含量较低,因此“吸附”、“解脱”的目的是富集碘元素
D.“萃取分液”后得到的是含有单质碘的有机层,需要进一步蒸馏才能得到单质碘,再升小华获得单质碘
11.答案B
A.有气体参加的反应或制取气体的反应在实验前要检查装置的气密性,为防止空气成分对实验的干扰;
B. 升华后产生的气体也为黄色;
C.对于易升华的物质要注意采取安全措施;
D.空气中的 、 、 都有氧化性,均可将KI氧化为 并使淀粉溶液变为蓝色。
12.答案D
X、Y、Z、Q不同周期且Y、Z、Q三种元素最高价氧化物对应水化物两两能反应,∴X为H,Y为N,Z为
Al,Q为K或者Ca,M为S元素。
A.原子半径: ;
B.Z为Al,Al单质是通过电解熔融 得到的;C.M为S, 标况下为固态;
D.Y为N,氢化物为 。
13.答案C
A.升温,CO的转化率减小,所以该反应的
B.在同一温度下, 时CO的转化率最大, 时CO的转化率最小,且p增大,CO的转化率增大,所以
C.a点时压强为 ,b点压强为 , ,∴浓度:b点 (3)N、O、Cl 6
【解析】(1)基态 的价电子排布式为 , 溶于氨水生成氢氧化四氨合铜,故化学方程式
为 。
(2)键角: 中N原子的价层电子对数为2,N原子为 杂化,键角为180°, 的价层电子对数为
3,N原子为 杂化,键角约为120°,故键角: 。
(4)配位化合物 的中心离子是 ,其提供空轨道,配体 中的N原子和
中的O原子提供电子对形成配位键,该配合物中 也是配体,推断 也提供了电子对参与形成配位
键; 、 、 均是配体,则中心离子的配位数为6。
21.【答案】(每空2分,共12分)
(1)氯气、光照 (2)酚羟基、羧基、氨基 (3)高
(4)
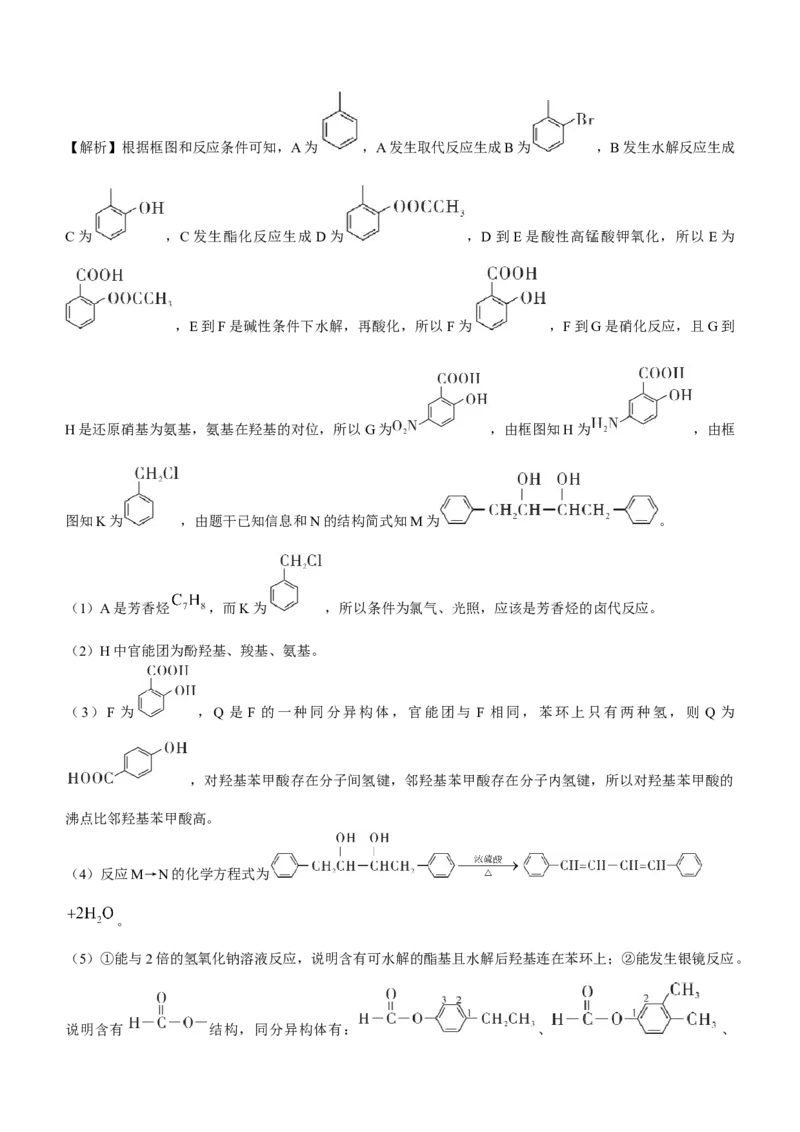
(5)9 、 (任写一个即可)【解析】根据框图和反应条件可知,A为 ,A发生取代反应生成B为 ,B发生水解反应生成
C为 ,C发生酯化反应生成 D为 ,D到E是酸性高锰酸钾氧化,所以 E为
,E到F是碱性条件下水解,再酸化,所以F为 ,F到G是硝化反应,且G到
H是还原硝基为氨基,氨基在羟基的对位,所以G为 ,由框图知H为 ,由框
图知K为 ,由题干已知信息和N的结构简式知M为 。
(1)A是芳香烃 ,而K为 ,所以条件为氯气、光照,应该是芳香烃的卤代反应。
(2)H中官能团为酚羟基、羧基、氨基。
(3)F 为 ,Q 是 F 的一种同分异构体,官能团与 F 相同,苯环上只有两种氢,则 Q 为
,对羟基苯甲酸存在分子间氢键,邻羟基苯甲酸存在分子内氢键,所以对羟基苯甲酸的
沸点比邻羟基苯甲酸高。
(4)反应M→N的化学方程式为
。
(5)①能与2倍的氢氧化钠溶液反应,说明含有可水解的酯基且水解后羟基连在苯环上;②能发生银镜反应。
说明含有 结构,同分异构体有: 、 、、 共9种;其中核磁共振氢谱有4组吸收峰,且峰面
积之比为6∶2∶1∶1的结构简式为 、 。下载最新免费模拟卷,到公众号:一枚试卷君