文档内容
高三化学试题
可能用到的相对原子质量:
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项符合题目要求。
1. 化学与生活密切相关。下列说法正确的是
A. “爆竹声中一岁除”,点燃爆竹后,硫燃烧生成三氧化硫
B. “半江瑟瑟(碧绿色)半江红”描述的是丁达尔效应
C. 对运输过程中的鲜花喷洒高锰酸钾稀溶液可达到保鲜的目的
D. 用米汤检验加碘食盐中的碘酸钾
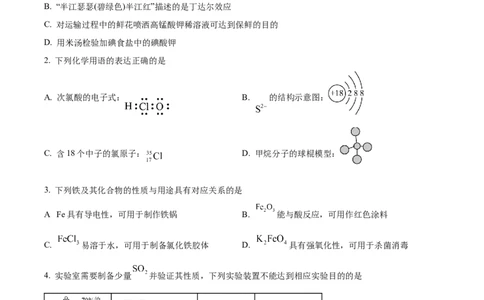
2. 下列化学用语的表达正确的是
A. 次氯酸的电子式: B. 的结构示意图:
C. 含18个中子的氯原子: D. 甲烷分子的球棍模型:
3. 下列铁及其化合物的性质与用途具有对应关系的是
.
A Fe具有导电性,可用于制作铁锅 B. 能与酸反应,可用作红色涂料
C. 易溶于水,可用于制备氯化铁胶体 D. 具有强氧化性,可用于杀菌消毒
4. 实验室需要制备少量 并验证其性质,下列实验装置不能达到相应实验目的的是
A.制取 B.验证 的还原性 C.收集 D.吸收
A. A B. B C. C D. D的
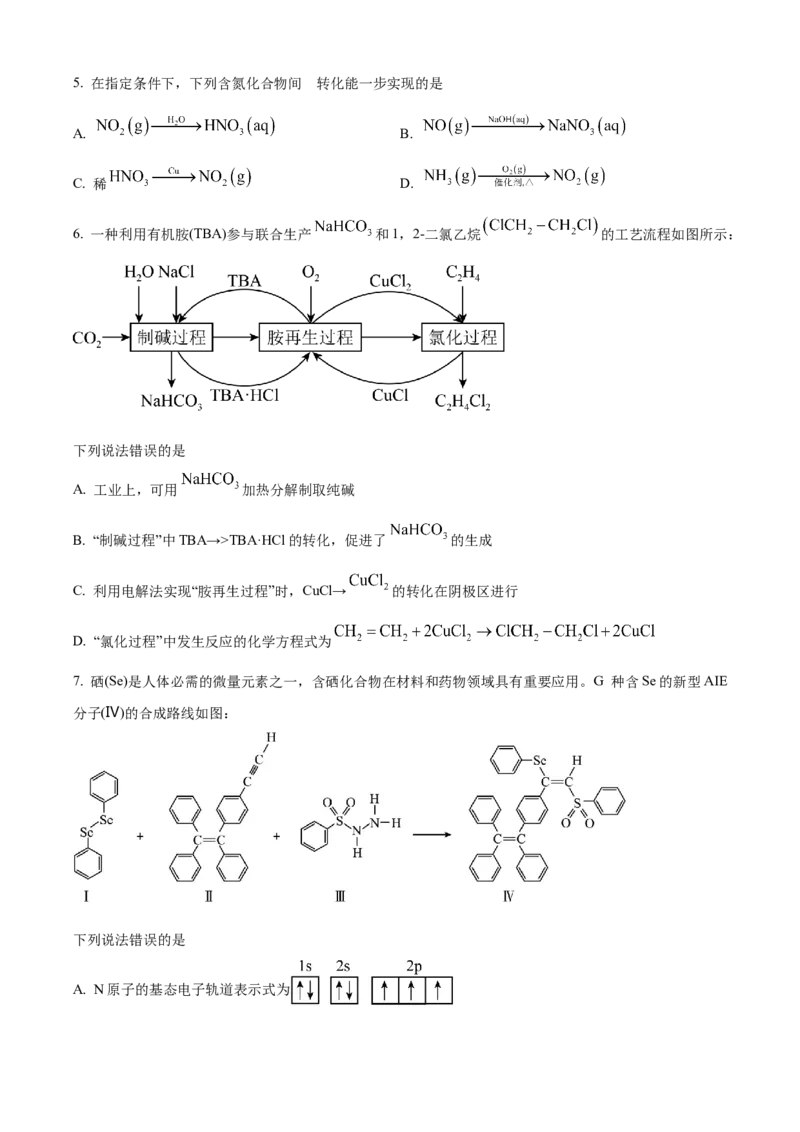
5. 在指定条件下,下列含氮化合物间 转化能一步实现的是
A. B.
C. 稀 D.
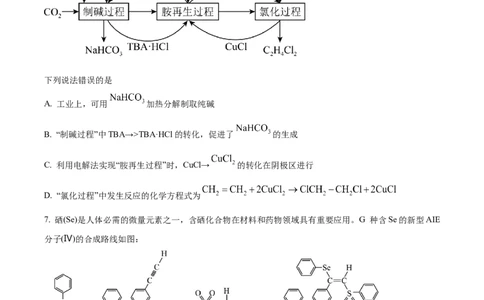
6. 一种利用有机胺(TBA)参与联合生产 和1,2-二氯乙烷 的工艺流程如图所示:
下列说法错误的是
A. 工业上,可用 加热分解制取纯碱
B. “制碱过程”中TBA→>TBA·HCl的转化,促进了 的生成
C. 利用电解法实现“胺再生过程”时,CuCl→ 的转化在阴极区进行
D. “氯化过程”中发生反应的化学方程式为
7. 硒(Se)是人体必需的微量元素之一,含硒化合物在材料和药物领域具有重要应用。G 种含Se的新型AIE
分子(Ⅳ)的合成路线如图:
下列说法错误的是
A. N原子的基态电子轨道表示式为B. 0.1mol I中共含2.5mol 键
C. Ⅱ中碳原子的杂化轨道类型为 、sp
D. Ⅲ中N、O、S的电负性:O>S>N
8. 现有四种短周期原子序数依次增大的主族元素A、B、C、D,A的一种单质被称为“足球分子”,B的原
子半径在短周期中最大,C元素的原子最外层电子数是最内层的3倍。下列说法正确的是
A. 简单离子半径:D>C>B
B. 上述四种元素分别与氧元素形成的氧化物均至少有两种
C. 最简单氢化物的稳定性:C>D>A
D. 氧化物对应水化物的酸性:D>C>A
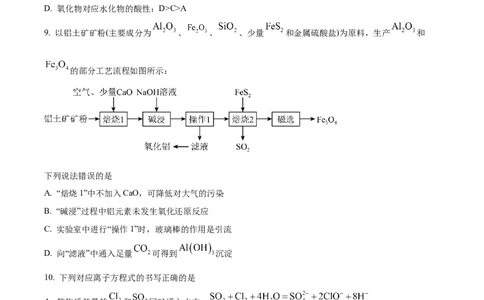
9. 以铝土矿矿粉(主要成分为 、 、 、少量 和金属硫酸盐)为原料,生产 和
的部分工艺流程如图所示:
下列说法错误的是
A. “焙烧1”中不加入CaO,可降低对大气的污染
B. “碱浸”过程中铝元素未发生氧化还原反应
C. 实验室中进行“操作1”时,玻璃棒的作用是引流
D. 向“滤液”中通入足量 可得到 沉淀
10. 下列对应离子方程式的书写正确的是
A. 等物质的量的 和 同时通入水中:
B. 向 中滴加足量的稀硝酸:
C. 向 溶液中滴加少量的 溶液:D. 向 溶液中滴加少量NaOH溶液:
11. 类推是学习化学的一种重要手段。下列根据相应客观事实得出的类推结论正确的是
选
客观事实 类推结论
项
A 将铜片加入足量稀硝酸中,铜片会被溶解 将铜片加入足量稀盐酸中,铜片也会被溶解
B 铁在氯气中燃烧的产物为 铁在溴蒸气中燃烧的产物为
向 溶液中滴加过量的NaOH溶液,最终有 向 溶液中滴加过量的氨水,最终也有
C
沉淀生成 沉淀生成
D 将 通入 溶液中无明显现象 将 通入 溶液中也无明显现象
A. A B. B C. C D. D
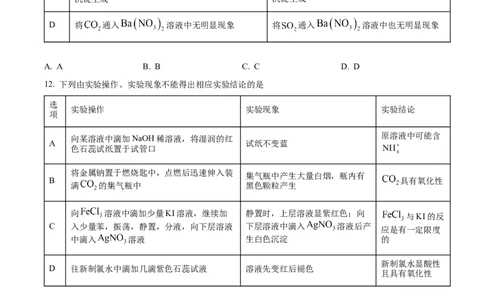
12. 下列由实验操作、实验现象不能得出相应实验结论的是
选
实验操作 实验现象 实验结论
项
原溶液中可能含
向某溶液中滴加NaOH稀溶液,将湿润的红
A 试纸不变蓝
色石蕊试纸置于试管口
将金属钠置于燃烧匙中,点燃后迅速伸入装
集气瓶中产生大量白烟,瓶内有
B 具有氧化性
满 的集气瓶中 黑色颗粒产生
向 溶液中滴加少量KI溶液,继续加 静置时,上层溶液显紫红色;向
与KI的反
C 入少量苯,振荡,静置,分液,向下层溶液 下层溶液中滴入 溶液后产
应是有一定限度
中滴入 溶液 生白色沉淀 的
新制氯水显酸性
D 往新制氯水中滴加几滴紫色石蕊试液 溶液先变红后褪色
且具有氧化性
A. A B. B C. C D. D
13. 设 为阿伏加德罗常数的值。下列说法正确的是
A. 4.4g由 和 组成的混合气体中含有的原子总数为
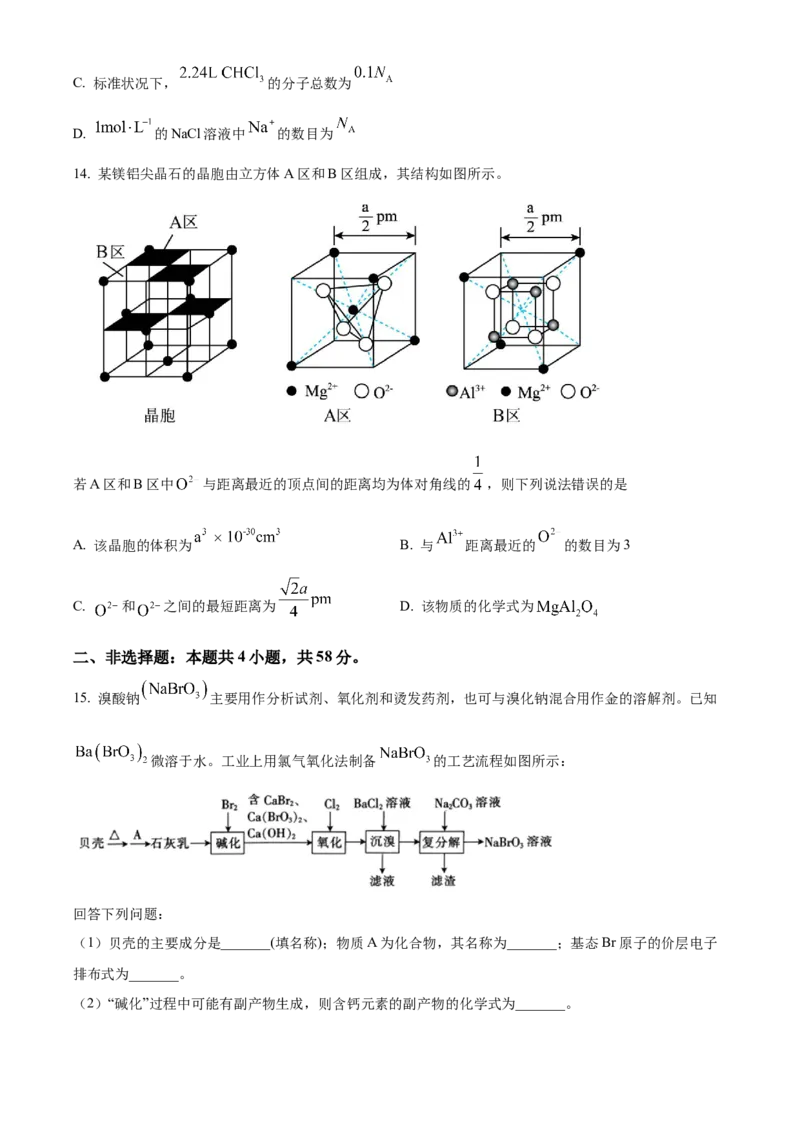
B. 中含有的共价键总数为C. 标准状况下, 的分子总数为
D. 的NaCl溶液中 的数目为
14. 某镁铝尖晶石的晶胞由立方体A区和B区组成,其结构如图所示。
若A区和B区中 与距离最近的顶点间的距离均为体对角线的 ,则下列说法错误的是
A. 该晶胞的体积为 B. 与 距离最近的 的数目为3
C. 和 之间的最短距离为 D. 该物质的化学式为
二、非选择题:本题共4小题,共58分。
15. 溴酸钠 主要用作分析试剂、氧化剂和烫发药剂,也可与溴化钠混合用作金的溶解剂。已知
微溶于水。工业上用氯气氧化法制备 的工艺流程如图所示:
回答下列问题:
(1)贝壳的主要成分是_______(填名称);物质A为化合物,其名称为_______;基态Br原子的价层电子
排布式为_______。
(2)“碱化”过程中可能有副产物生成,则含钙元素的副产物的化学式为_______。(3)此工艺流程中涉及过滤操作,该操作的原理是_______。
(4)“氧化”时,生成 反应的化学方程式为_______;将氯气通入石灰乳中可制得漂白粉,但通
入石灰水中不能制得漂白粉,分析其原因:_______(用文字描述)。
(5)“复分解”时,“滤渣”的化学式为_______,复分解反应能发生的原因是_______。
16. 水合草酸铝酸钾晶体是一种化工原料,其晶体组成可表示为 (相对分子质量
为462)。某化学兴趣小组设计实验制备水合草酸铝酸钾晶体并探究其性质。
.
I制备水合草酸铝酸钾晶体:
步骤1:将 溶液和 溶液混合,完全反应后过滤,
分离出生成的 沉淀,并用水洗涤2~3次。
步骤2:称取 和 ,并用100mL水溶解得到溶液,再向所得溶
液中加入步骤1得到的 沉淀,煮沸、浓缩,趁热过滤得到固体,将固体加入乙醇和水的体积比为
1∶1的混合溶液中,过滤,用无水乙醇洗涤2~3次,得水合草酸铝酸钾晶体。
(1)若步骤1中的NaOH溶液用氨水代替,则发生反应的离子方程式为_______。
(2)水合草酸铝酸钾在水中的溶解度_______(填“大于”或“小于”)其在乙醇中的溶解度。
II.确定水合草酸铝酸钾晶体的组成:称取2.31g水合草酸铝酸钾晶体,进行热重分析,测得的固体失重率
如表1所示。
表1
阶段 温度变化范围/℃ 残留固体组成 固体失重率
1 47~340 11.69%
2 340~533 32.47%
已知:固体失重率 %,其中 为原始固体的质量, 为某温度下剩余固体的质量。
(3)c=_______;水合草酸铝酸钾晶体的化学式为_______。
(4)阶段2发生反应的化学方程式为_______。
III..测定某混合物中 的百分含量(设混合物中其他组分均不与酸性 溶液
反应)。已知:酸性 溶液可将 氧化并放出 ,测定上述混合物中 的百
分含量时,可用酸性 标准溶液进行滴定。
(5)滴定时,酸性 溶液不能用碱式滴定管盛装的原因是_______;滴定过程中发生反应的离子方
程式为_______。
(6)取10.0g产物配成100mL溶液,从中取出20mL于锥形瓶中,用 的酸性 溶液滴
定至终点,重复滴定4次,消耗酸性 溶液的体积如表2所示。
表2
滴定次数 第一次 第二次 第三次 第四次
消耗酸性 溶液的体积/mL 24.02 23.98 24.00 22.08
则该混合物中 的质量分数为_______。
17. 将二氧化碳转化为高附加值碳基燃料有利于实现碳中和。
已知:① ;
② ;
③ 。
的
(1)相关化学键 键能数据如表所示。
化学键 H—H H—O C—H
键能 436 802 463 x
则 _______ ,x=_______。
(2)某温度下,将 和 充入容积可变的密闭容器中发生反应(设仅发生反应①和
反应②),保持体系压强为P 反应起始时气体总体积为V L,平衡体系中 、 的物质的量分
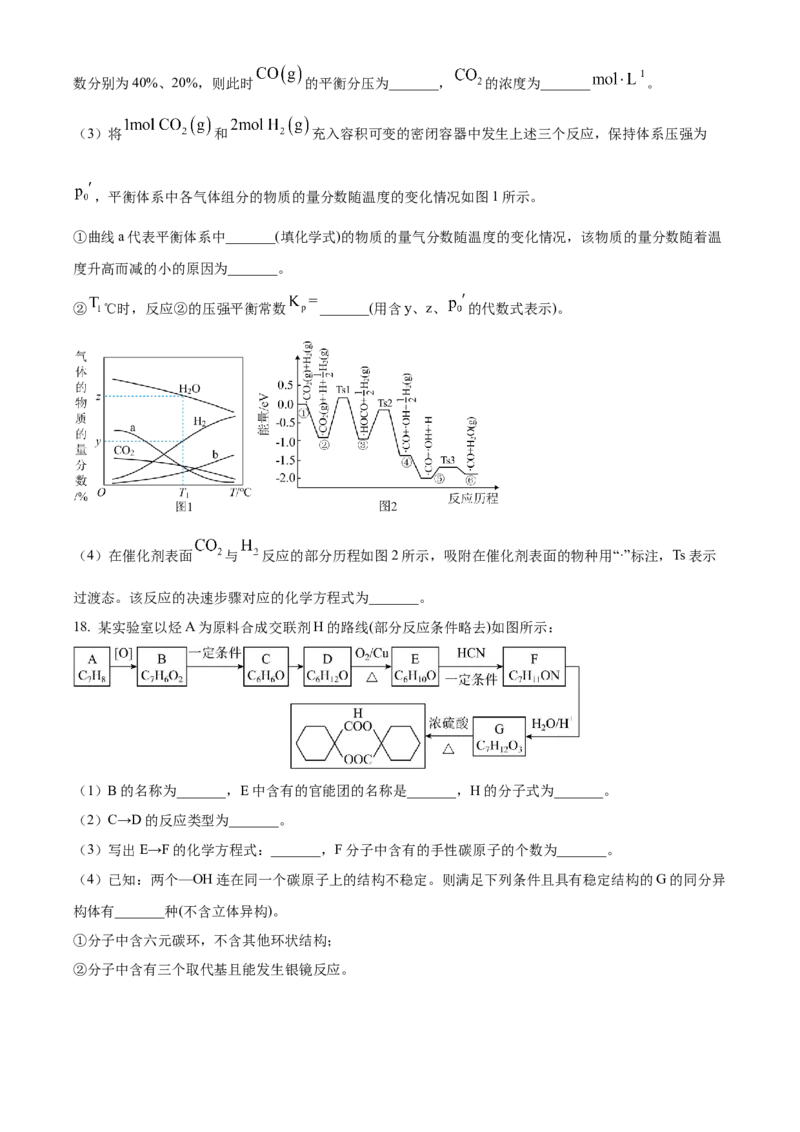
0数分别为40%、20%,则此时 的平衡分压为_______, 的浓度为_______ 。
(3)将 和 充入容积可变的密闭容器中发生上述三个反应,保持体系压强为
,平衡体系中各气体组分的物质的量分数随温度的变化情况如图1所示。
①曲线a代表平衡体系中_______(填化学式)的物质的量气分数随温度的变化情况,该物质的量分数随着温
度升高而减的小的原因为_______。
② ℃时,反应②的压强平衡常数 _______(用含y、z、 的代数式表示)。
(4)在催化剂表面 与 反应的部分历程如图2所示,吸附在催化剂表面的物种用“·”标注,Ts表示
过渡态。该反应的决速步骤对应的化学方程式为_______。
18. 某实验室以烃A为原料合成交联剂H的路线(部分反应条件略去)如图所示:
(1)B的名称为_______,E中含有的官能团的名称是_______,H的分子式为_______。
(2)C→D的反应类型为_______。
(3)写出E→F的化学方程式:_______,F分子中含有的手性碳原子的个数为_______。
(4)已知:两个—OH连在同一个碳原子上的结构不稳定。则满足下列条件且具有稳定结构的G的同分异
构体有_______种(不含立体异构)。
①分子中含六元碳环,不含其他环状结构;
②分子中含有三个取代基且能发生银镜反应。(5)参照题干中的合成路线,设计以苯乙酮( )和甲醇为主要原料制备 的合成路
线_______ (无机试剂任选)。高三化学试题
可能用到的相对原子质量:
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项符合题目要求。
【1题答案】
【答案】C
【2题答案】
【答案】C
【3题答案】
【答案】D
【4题答案】
【答案】D
【5题答案】
【答案】A
【6题答案】
【答案】C
【7题答案】
【答案】D
【8题答案】
【答案】B
【9题答案】
【答案】A
【10题答案】
【答案】D
【11题答案】
【答案】B
【12题答案】
【答案】C
【13题答案】
【答案】A【14题答案】
【答案】B
二、非选择题:本题共4小题,共58分。
【15题答案】
【答案】(1) ①. 碳酸钙 ②. 水 ③.
(2)
(3)利用不同种物质在同一溶剂中溶解能力的不同来进行分离
(4) ①. ②. 石灰水中
浓度过小,而石灰乳中 浓度较大
(5) ①. ②. 相同温度下, 的溶解度小于反应物 的溶解度
【16题答案】
【答案】(1)
(2)大于 (3) ①. 3 ②.
(4)
( 5 ) ① . 酸 性 溶 液 具 有 酸 性 和 强 氧 化 性 , 会 腐 蚀 橡 皮 管 ② .
(6)46.2%
【17题答案】
【答案】(1) ①. ②. 415
(2) ①. ②.
的
(3) ①. ②. 反应② ,反应③的 ,升高温度反应②平衡左移,反应③平衡右移, 的物质的量分数减小 ③.
(4) 或
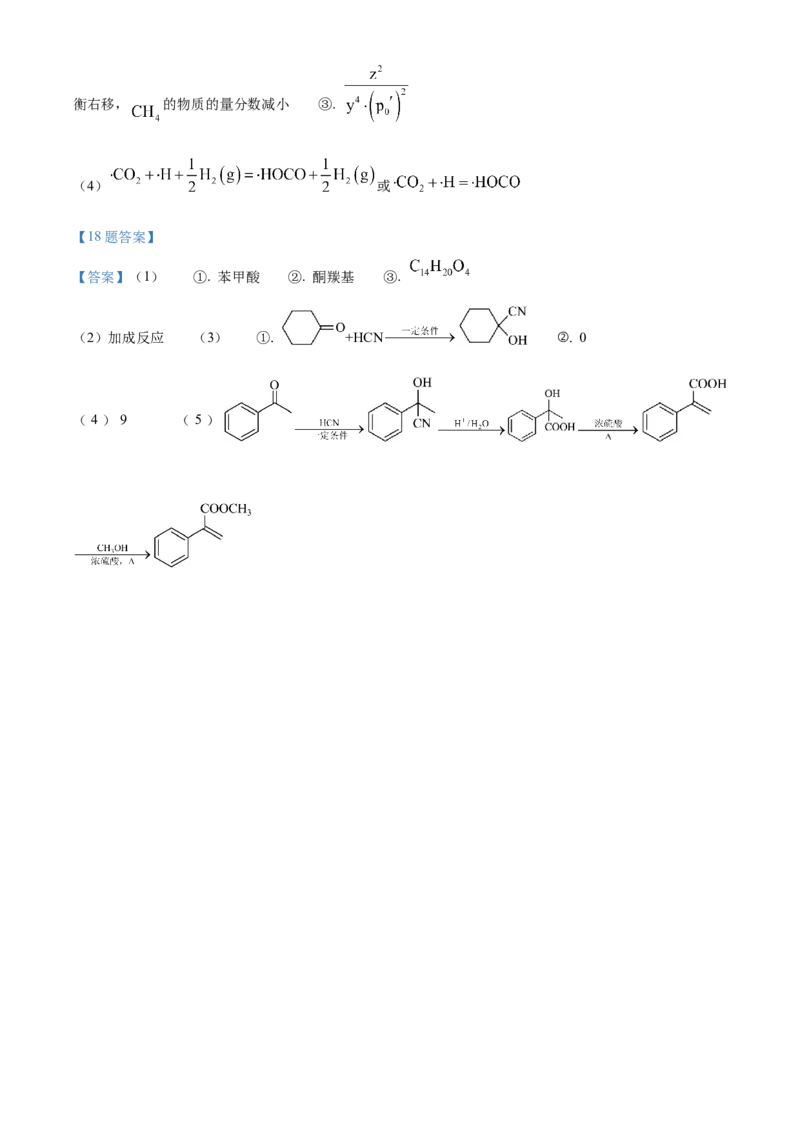
【18题答案】
【答案】(1) ①. 苯甲酸 ②. 酮羰基 ③.
(2)加成反应 (3) ①. +HCN ②. 0
( 4 ) 9 ( 5 )