文档内容
微专题32 化学工艺流程题-----核心反应与条件控制
化学工艺流程题是将化工生产中的生产流程用框图形式表示出来,并根据生产流程中有
关的化学知识步步设问,是无机框图的创新。它以现代工业生产为基础,与化工生产成
本、产品提纯、环境保护等相融合,考查物质的制备、检验、分离提纯等基本实验原理
在化工生产中的实际应用,要求考生依据流程图分析原理,紧扣信息,抓住关键、准确
答题。这类试题具有较强的实用性和综合性,是高考化学命题的常考题型。
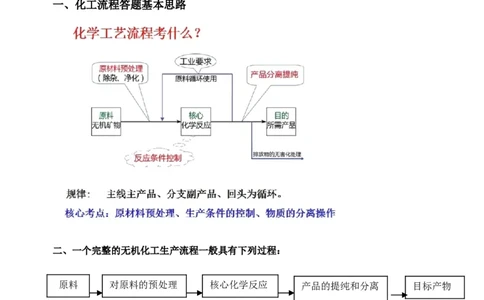
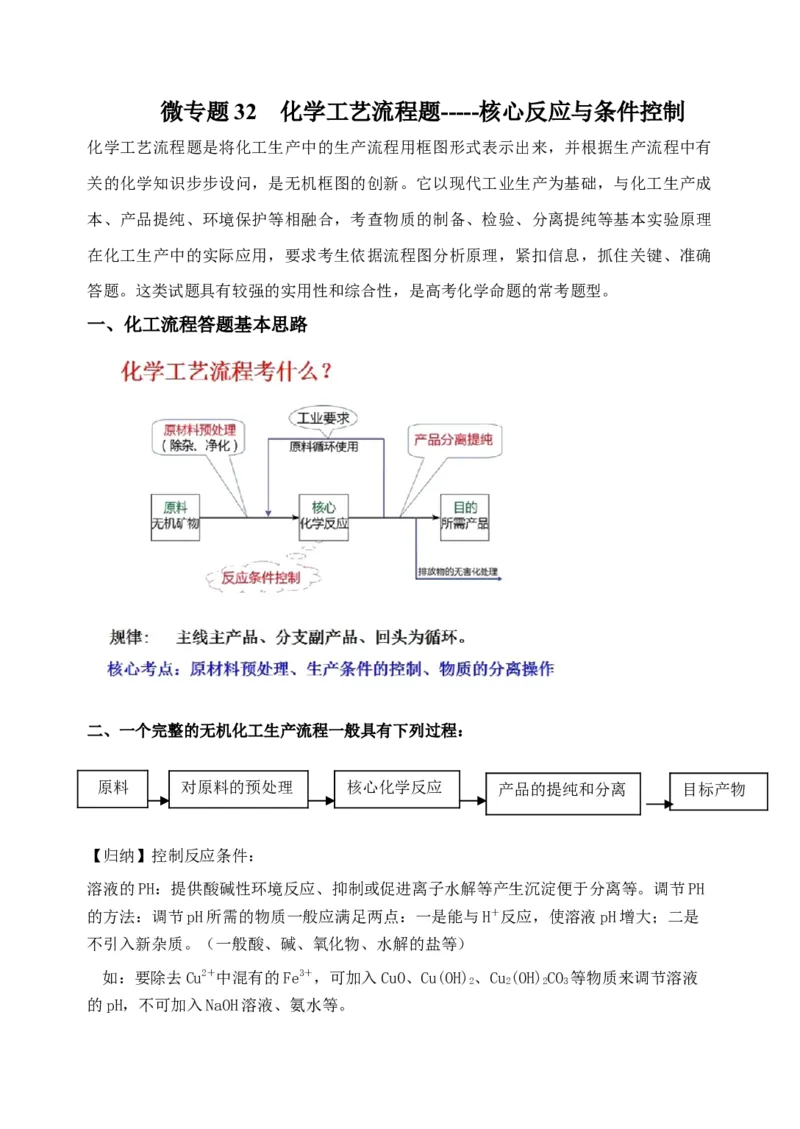
一、化工流程答题基本思路
二、一个完整的无机化工生产流程一般具有下列过程:
原料 对原料的预处理 核心化学反应 产品的提纯和分离 目标产物
【归纳】控制反应条件:
溶液的PH:提供酸碱性环境反应、抑制或促进离子水解等产生沉淀便于分离等。调节PH
的方法:调节pH所需的物质一般应满足两点:一是能与H+反应,使溶液pH增大;二是
不引入新杂质。(一般酸、碱、氧化物、水解的盐等)
如:要除去Cu2+中混有的Fe3+,可加入CuO、Cu(OH)、Cu(OH)CO 等物质来调节溶液
2 2 2 3
的pH,不可加入NaOH溶液、氨水等。温度:升温----加快反应(溶解)速率;促进平衡向吸热方向移动;去除热稳定性差的
物质或易升华的物质。
降温----防止物质分解,挥发;使平衡向放热方向移动;使高沸点的物质液化,使其
与其他物质分离;降低溶解度,减少损失。
控温-----水浴、沙浴、油浴-----受热均匀,便于控制温度。温度太高---速率太快;
物质可能分解、挥发、水解;催化剂可能中毒;发生副反应等。温度太低----速
率可能太慢;催化剂活性不高;物质转化率、产率不高等。
氧化剂(还原剂)(电化学):生产目标(过程)产物或去除某些离子。
其他条件:浓度、压强、催化剂、隔绝空气等。
【典例精析】
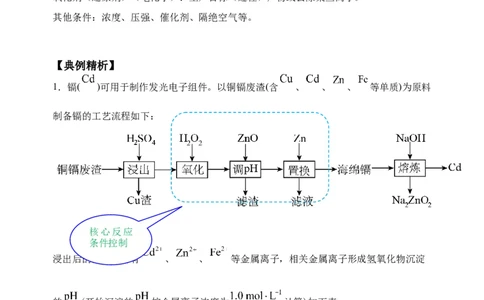
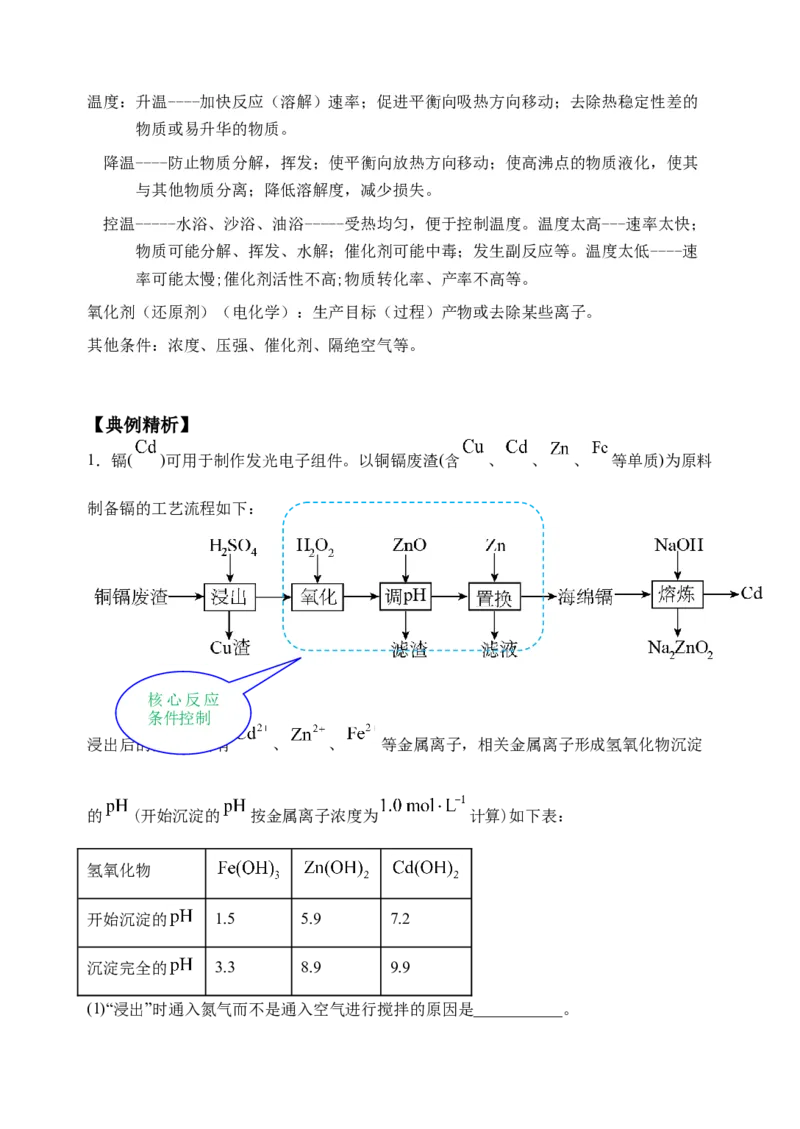
1.镉( )可用于制作发光电子组件。以铜镉废渣(含 、 、 、 等单质)为原料
制备镉的工艺流程如下:
核心反应
条件控制
浸出后的溶液中含有 、 、 等金属离子,相关金属离子形成氢氧化物沉淀
的 (开始沉淀的 按金属离子浓度为 计算)如下表:
氢氧化物
开始沉淀的 1.5 5.9 7.2
沉淀完全的 3.3 8.9 9.9
(1)“浸出”时通入氮气而不是通入空气进行搅拌的原因是___________。(2)“氧化”时发生反应的离子方程式为___________。 也能氧化 ,工业生产中
不选用 的原因是___________。
(3)“调 ”时控制溶液 在3.3~5.9之间,“滤渣”的主要成分是___________(填化学式)。
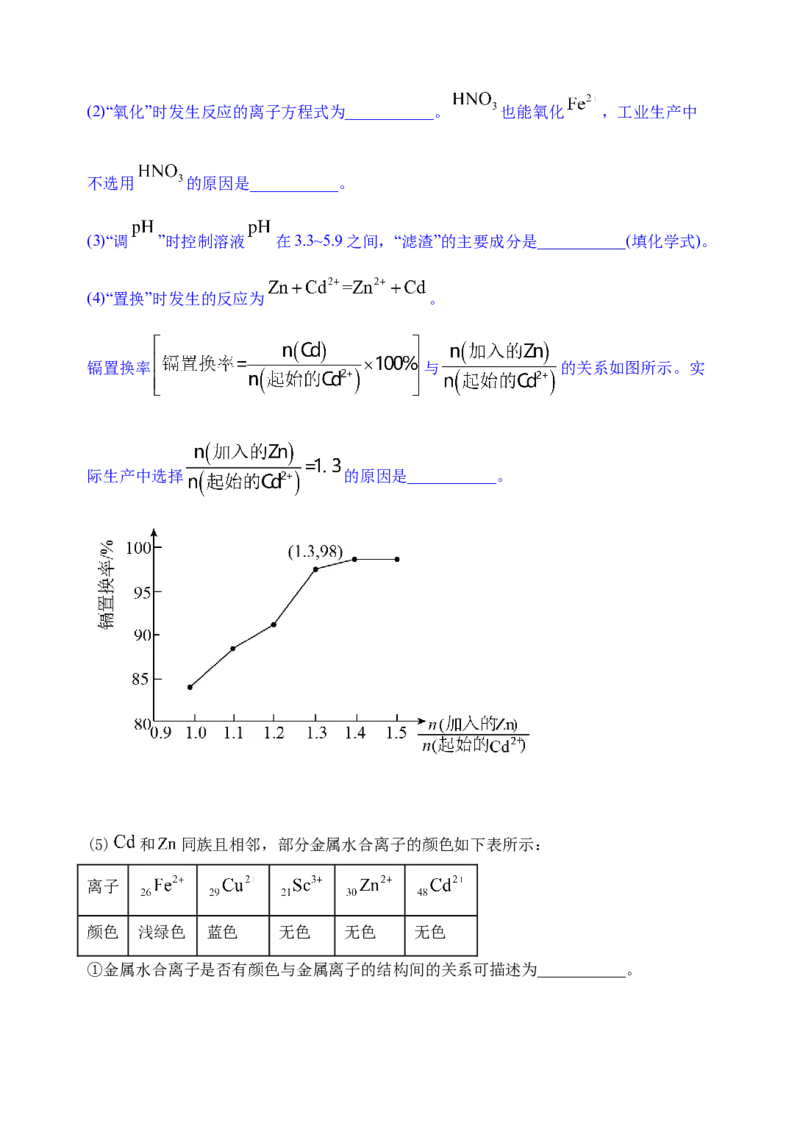
(4)“置换”时发生的反应为 。
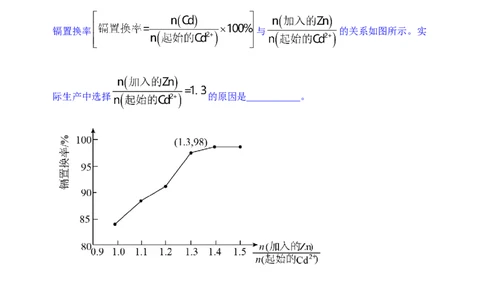
镉置换率 与 的关系如图所示。实
际生产中选择 的原因是___________。
(5) 和 同族且相邻,部分金属水合离子的颜色如下表所示:
离子
颜色 浅绿色 蓝色 无色 无色 无色
①金属水合离子是否有颜色与金属离子的结构间的关系可描述为___________。②硫酸酸化的硫酸铁溶液中铁元素以 形式存在而使溶液呈浅紫色,向其中
滴入几滴 溶液,因生成 、 等离子而
使溶液呈红色,能发生上述反应的原因是___________。
【专题精练】
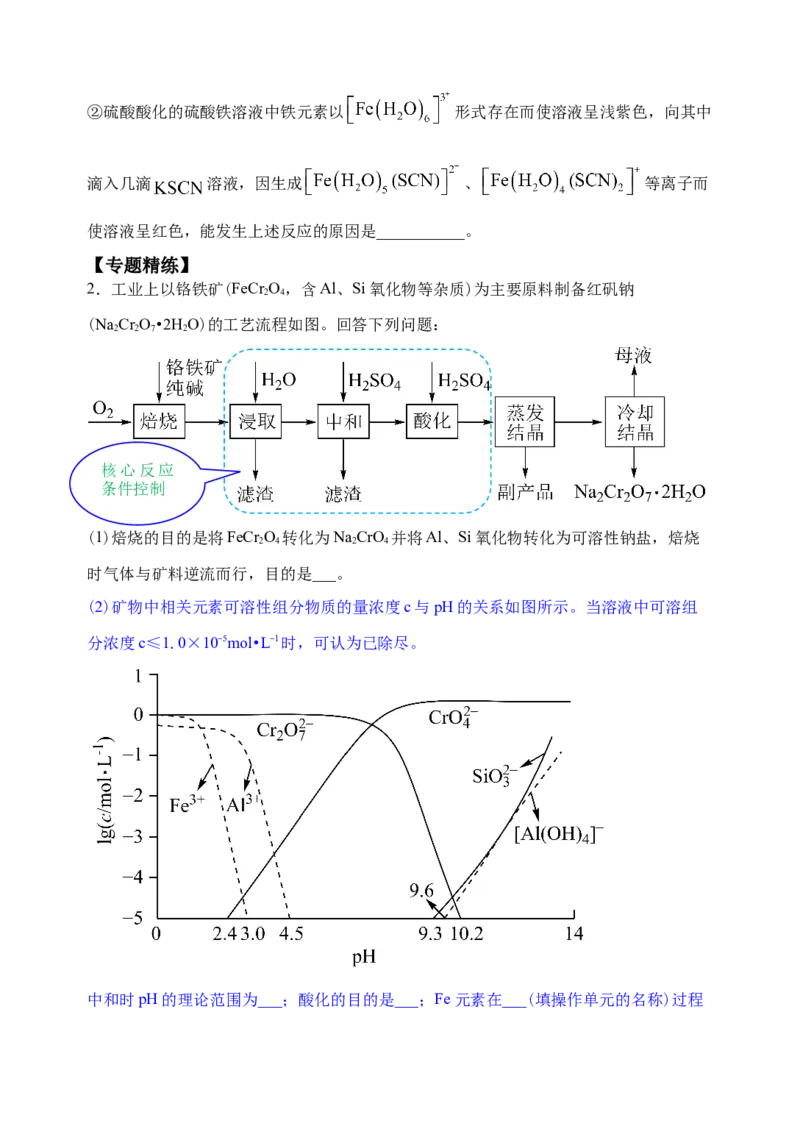
2.工业上以铬铁矿(FeCr O,含Al、Si氧化物等杂质)为主要原料制备红矾钠
2 4
(NaCr O•2HO)的工艺流程如图。回答下列问题:
2 2 7 2
核心反应
条件控制
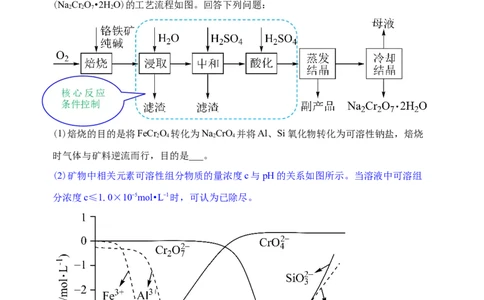
(1)焙烧的目的是将FeCr O 转化为NaCrO 并将Al、Si氧化物转化为可溶性钠盐,焙烧
2 4 2 4
时气体与矿料逆流而行,目的是___。
(2)矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图所示。当溶液中可溶组
分浓度c≤1.0×10-5mol•L-1时,可认为已除尽。
中和时pH的理论范围为___;酸化的目的是___;Fe元素在___(填操作单元的名称)过程中除去。
(3)蒸发结晶时,过度蒸发将导致___;冷却结晶所得母液中,除NaCr O 外,可在上述
2 2 7
流程中循环利用的物质还有____。
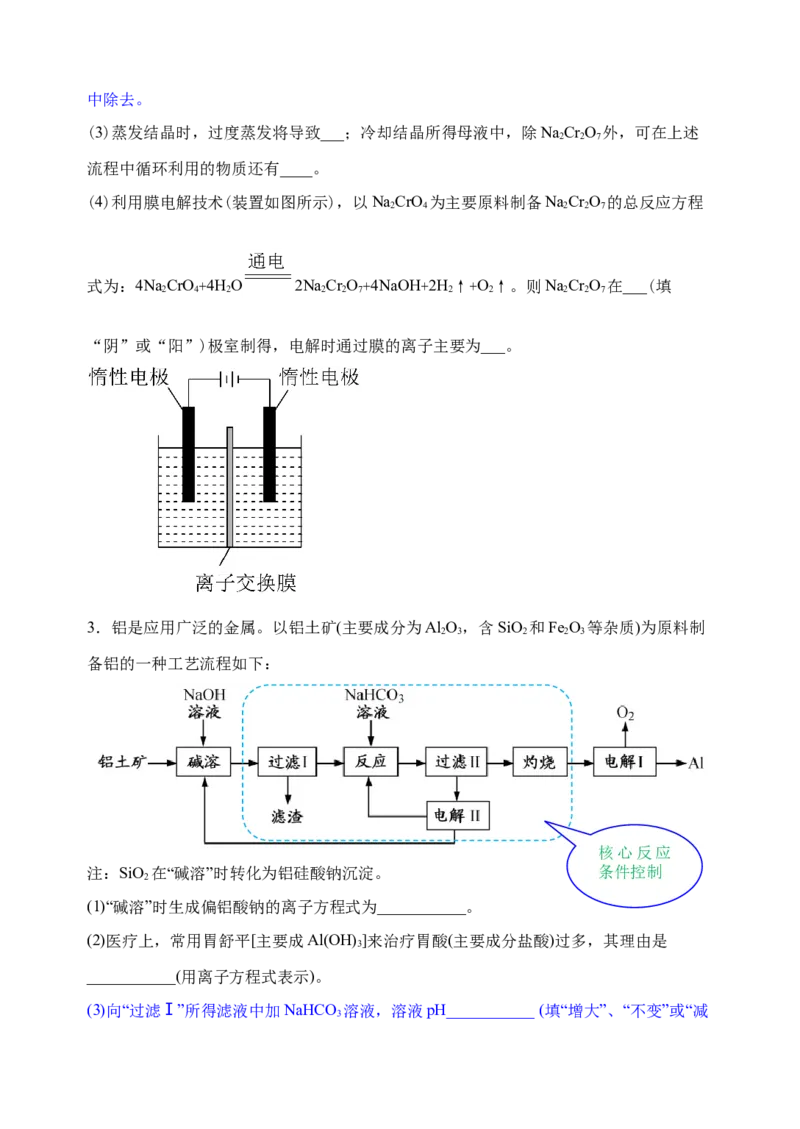
(4)利用膜电解技术(装置如图所示),以NaCrO 为主要原料制备NaCr O 的总反应方程
2 4 2 2 7
式为:4NaCrO+4HO 2NaCr O+4NaOH+2H↑+O↑。则NaCr O 在___(填
2 4 2 2 2 7 2 2 2 2 7
“阴”或“阳”)极室制得,电解时通过膜的离子主要为___。
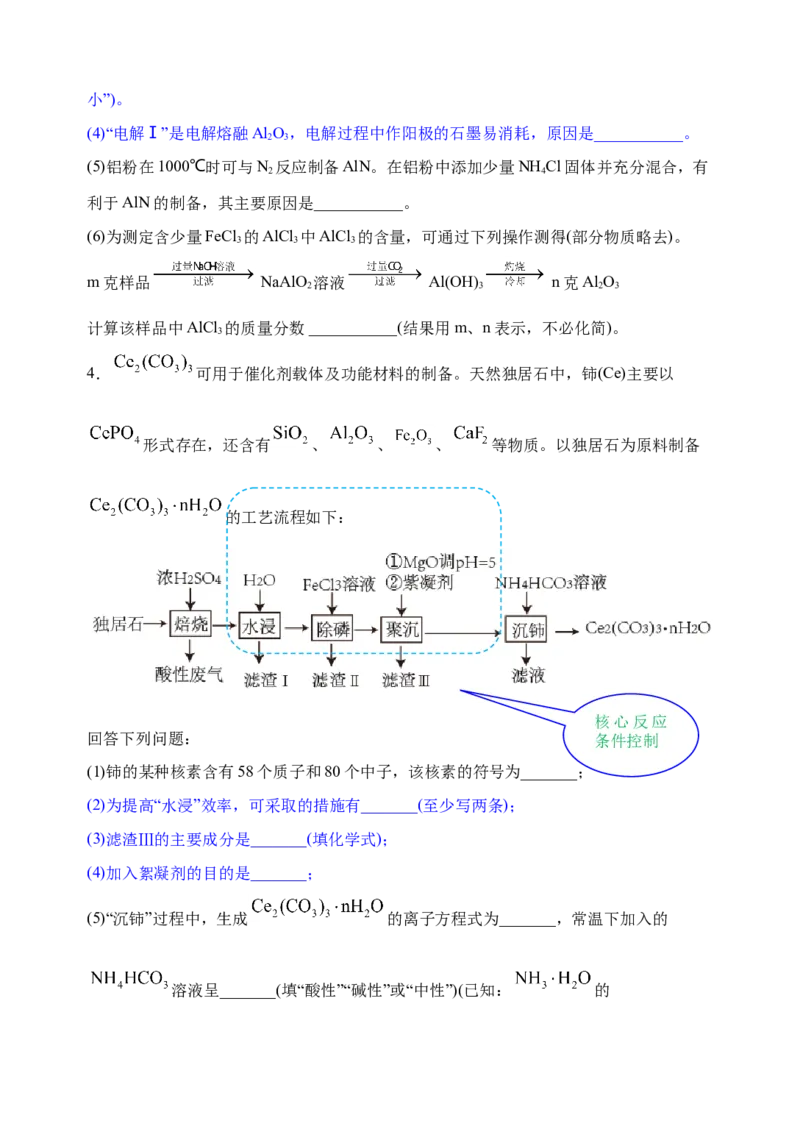
3.铝是应用广泛的金属。以铝土矿(主要成分为Al O,含SiO 和Fe O 等杂质)为原料制
2 3 2 2 3
备铝的一种工艺流程如下:
核心反应
注:SiO 在“碱溶”时转化为铝硅酸钠沉淀。 条件控制
2
(1)“碱溶”时生成偏铝酸钠的离子方程式为___________。
(2)医疗上,常用胃舒平[主要成Al(OH) ]来治疗胃酸(主要成分盐酸)过多,其理由是
3
___________(用离子方程式表示)。
(3)向“过滤Ⅰ”所得滤液中加NaHCO 溶液,溶液pH___________ (填“增大”、“不变”或“减
3小”)。
(4)“电解Ⅰ”是电解熔融Al O,电解过程中作阳极的石墨易消耗,原因是___________。
2 3
(5)铝粉在1000℃时可与N 反应制备AlN。在铝粉中添加少量NH Cl固体并充分混合,有
2 4
利于AlN的制备,其主要原因是___________。
(6)为测定含少量FeCl 的AlCl 中AlCl 的含量,可通过下列操作测得(部分物质略去)。
3 3 3
m克样品 NaAlO 溶液 Al(OH) n克Al O
2 3 2 3
计算该样品中AlCl 的质量分数 ___________(结果用m、n表示,不必化简)。
3
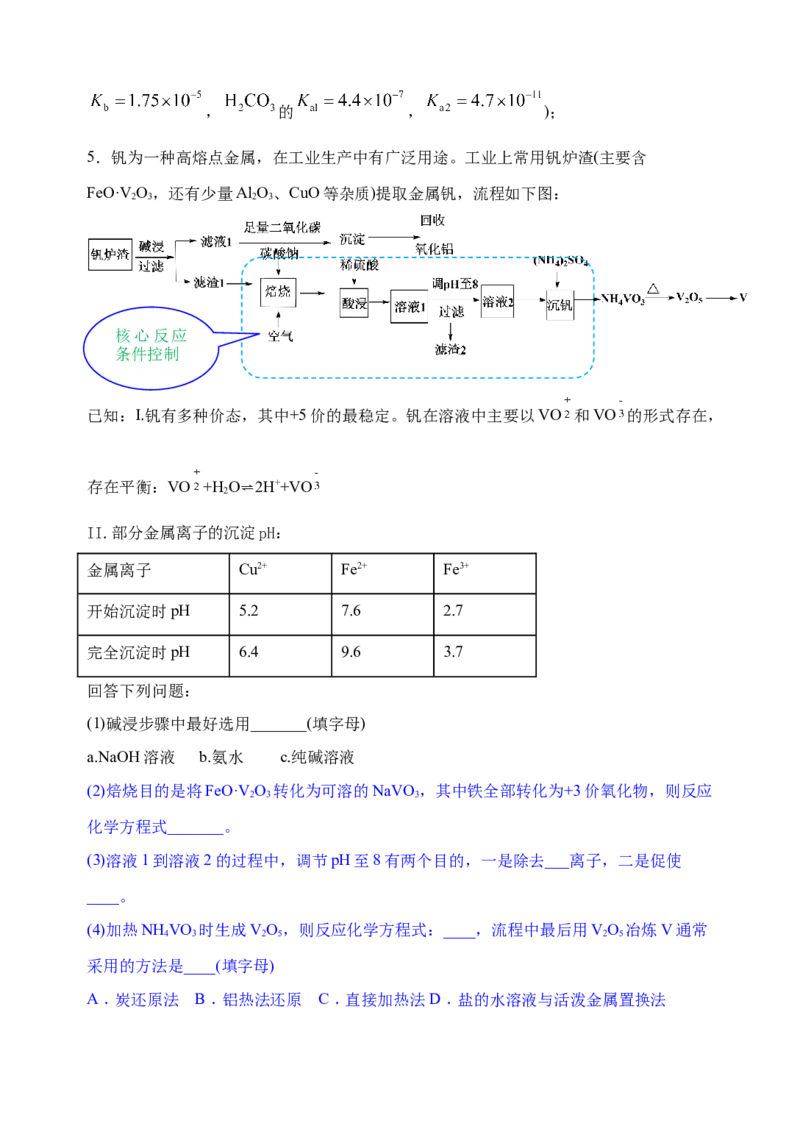
4. 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以
形式存在,还含有 、 、 、 等物质。以独居石为原料制备
的工艺流程如下:
核心反应
回答下列问题: 条件控制
(1)铈的某种核素含有58个质子和80个中子,该核素的符号为_______;
(2)为提高“水浸”效率,可采取的措施有_______(至少写两条);
(3)滤渣Ⅲ的主要成分是_______(填化学式);
(4)加入絮凝剂的目的是_______;
(5)“沉铈”过程中,生成 的离子方程式为_______,常温下加入的
溶液呈_______(填“酸性”“碱性”或“中性”)(已知: 的, 的 , );
5.钒为一种高熔点金属,在工业生产中有广泛用途。工业上常用钒炉渣(主要含
FeO·V O,还有少量Al O、CuO等杂质)提取金属钒,流程如下图:
2 3 2 3
核心反应
条件控制
已知:I.钒有多种价态,其中+5价的最稳定。钒在溶液中主要以VO 和VO 的形式存在,
存在平衡:VO +H
2
O⇌2H++VO
II.部分金属离子的沉淀pH:
金属离子 Cu2+ Fe2+ Fe3+
开始沉淀时pH 5.2 7.6 2.7
完全沉淀时pH 6.4 9.6 3.7
回答下列问题:
(1)碱浸步骤中最好选用_______(填字母)
a.NaOH溶液 b.氨水 c.纯碱溶液
(2)焙烧目的是将FeO·V O 转化为可溶的NaVO ,其中铁全部转化为+3价氧化物,则反应
2 3 3
化学方程式_______。
(3)溶液1到溶液2的过程中,调节pH至8有两个目的,一是除去___离子,二是促使
____。
(4)加热NH VO 时生成VO,则反应化学方程式:____,流程中最后用VO 冶炼V通常
4 3 2 5 2 5
采用的方法是____(填字母)
A.炭还原法 B.铝热法还原 C.直接加热法 D.盐的水溶液与活泼金属置换法(5)全钒液流电池工作原理如图:
已知各种含钒离子的颜色如下:VO 黄色、VO2+蓝色、V3+绿色、V2+紫色
①全钒液流电池放电时V2+发生氧化反应,该电池放电时总反应式是_______。
②当完成储能时,阳极区溶液的颜色是_______。