文档内容
微专题31 化学工艺流程题-----原料的预处理
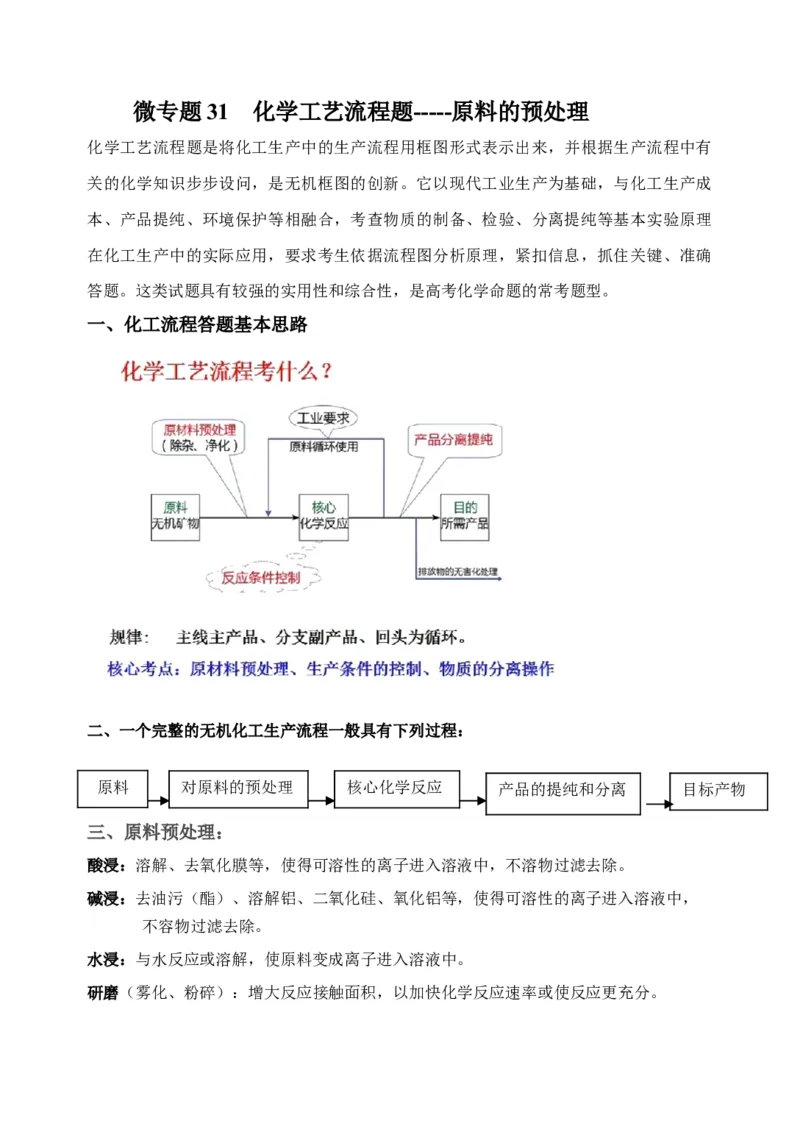
化学工艺流程题是将化工生产中的生产流程用框图形式表示出来,并根据生产流程中有
关的化学知识步步设问,是无机框图的创新。它以现代工业生产为基础,与化工生产成
本、产品提纯、环境保护等相融合,考查物质的制备、检验、分离提纯等基本实验原理
在化工生产中的实际应用,要求考生依据流程图分析原理,紧扣信息,抓住关键、准确
答题。这类试题具有较强的实用性和综合性,是高考化学命题的常考题型。
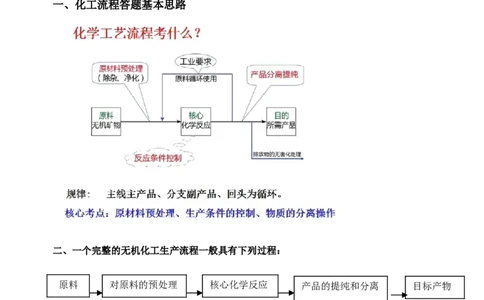
一、化工流程答题基本思路
二、一个完整的无机化工生产流程一般具有下列过程:
原料 对原料的预处理 核心化学反应 产品的提纯和分离 目标产物
三、原料预处理:
酸浸:溶解、去氧化膜等,使得可溶性的离子进入溶液中,不溶物过滤去除。
碱浸:去油污(酯)、溶解铝、二氧化硅、氧化铝等,使得可溶性的离子进入溶液中,
不容物过滤去除。
水浸:与水反应或溶解,使原料变成离子进入溶液中。
研磨(雾化、粉碎):增大反应接触面积,以加快化学反应速率或使反应更充分。灼烧(焙烧、煅烧):使物质高温分解或者氧化去除杂质、改变物质结构,使物质能溶
解。如从海带中提取碘时的灼烧就是为了除去可燃性杂质。如煅烧高岭土。
加入其他物质:如有机物醇、四氯化碳、无机盐等----反应、溶解。
四、原料预处理过程中常考知识点:
1.增大原料浸出率(离子在溶液中的含量多少)的措施:搅拌、适当升高温度、延长浸
出时间、增大浸出液的浓度、固体粉碎增大接触面积
2.提高固体的焙烧效率方法:增加氧气的量、固体充分粉碎、逆流焙烧、适当升温等。
3.加热的目的:加快反应速率或促进平衡向某个方向(一般是有利于生成物生成的方
向)移动
【典例精析】
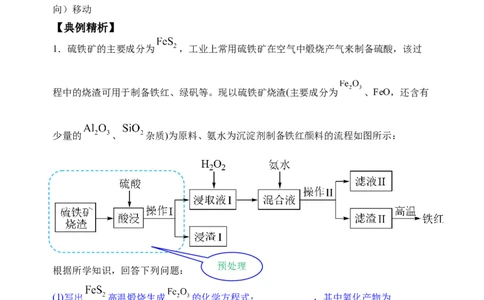
1.硫铁矿的主要成分为 ,工业上常用硫铁矿在空气中煅烧产气来制备硫酸,该过
程中的烧渣可用于制备铁红、绿矾等。现以硫铁矿烧渣(主要成分为 、FeO,还含有
少量的 、 杂质)为原料、氨水为沉淀剂制备铁红颜料的流程如图所示:
预处理
根据所学知识,回答下列问题:
(1)写出 高温煅烧生成 的化学方程式:___________,其中氧化产物为
___________(填化学式)。
(2)“浸取液Ⅰ”中加入 的目的是___________,发生反应的离子方程式为
___________。
(3)“操作Ⅰ”的名称为___________。(4)在加入氨水沉淀时,调节pH可使得 沉淀而 不沉淀。“滤液Ⅱ”中溶质的主
要成分为___________(填化学式)。写出获得“滤渣Ⅱ”的离子方程式:___________。
【答案】(1) 、 (2) 作氧化剂,氧化
(3) 过滤 (4) 、
(多写 不扣分)
【分析】
硫铁矿烧渣(主要成分为 Fe O、FeO,还含有少量的 Al O、 SiO 杂质)经过酸浸后
2 3 2 3 2
Fe O、FeO和 Al O 溶解,SiO 在硫酸中不能溶解,过滤将难溶物除去,用 HO 将浸取
2 3 2 3 2 2 2
液Ⅰ中的 Fe2+氧化成Fe3+,继续加入氨水,调节pH可使得 Fe3+沉淀而 Al3+ 不沉淀,过滤
分离得到 Fe(OH) ,煅烧得到铁红,据此分析答题。
3
【详解】
(1) FeS 在高温煅烧时,铁元素生成 Fe O,硫元素生成SO ,发生的化学方程式为:
2 2 3 2
;硫元素和铁元素化合价均升高,得到氧化产物,氧
化产物为: Fe O、 SO ;
2 3 2
(2)硫铁矿烧渣中含有Fe2+,用HO 将Fe2+氧化成Fe3+,便于下一步用氨水使Fe3+沉淀;发
2 2
生的离子方程式为: ;
(3)硫酸酸浸溶解Fe O、FeO和Al O,SiO 在硫酸中不能溶解,过滤将难溶物除去,故
2 3 2 3 2
操作Ⅰ为过滤;
(4) 酸浸之后溶液中含有:Al (SO )、Fe (SO )、FeSO ,若硫酸过量,还有剩余的
2 4 3 2 4 3 4
HSO 。加入HO 将Fe2+氧化成Fe3+,加入氨水沉淀时,调节pH可使得Fe3+沉淀而Al3+不
2 4 2 2沉淀,溶液中剩余溶质主要为(NH )SO 、Al (SO );滤渣Ⅱ为Fe(OH) ,氨水沉淀Fe3+所
4 2 4 2 4 3 3
得,离子方程式为: 。
【专题精练】
2.铝是应用广泛的金属。以铝土矿(主要成分为Al O,含SiO 和Fe O 等杂质)为原料制
2 3 2 2 3
备铝的一种工艺流程如下:
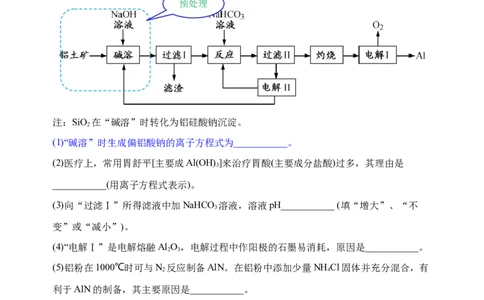
预处理
注:SiO 在“碱溶”时转化为铝硅酸钠沉淀。
2
(1)“碱溶”时生成偏铝酸钠的离子方程式为___________。
(2)医疗上,常用胃舒平[主要成Al(OH) ]来治疗胃酸(主要成分盐酸)过多,其理由是
3
___________(用离子方程式表示)。
(3)向“过滤Ⅰ”所得滤液中加NaHCO 溶液,溶液pH___________ (填“增大”、“不
3
变”或“减小”)。
(4)“电解Ⅰ”是电解熔融Al O,电解过程中作阳极的石墨易消耗,原因是___________。
2 3
(5)铝粉在1000℃时可与N 反应制备AlN。在铝粉中添加少量NH Cl固体并充分混合,有
2 4
利于AlN的制备,其主要原因是___________。
(6)为测定含少量FeCl 的AlCl 中AlCl 的含量,可通过下列操作测得(部分物质略去)。
3 3 3
m克样品 NaAlO 溶液 Al(OH) n克Al O
2 3 2 3
计算该样品中AlCl 的质量分数 ___________(结果用m、n表示,不必化简)。
3
【答案】(1)AlO+2OH−=2AlO +H O (2) Al(OH) +3H+ =2Al3++ 3H O (3) 减小 (4) 石墨
2 3 2 3 2
电极被阳极上产生的O 氧化 (5) NHCl分解产生的HCl能够破坏Al表面的Al O 薄膜
2 4 2 3(6) 或 或
【分析】
以铝土矿(主要成分为Al O,含SiO 和Fe O 等杂质)为原料制备铝,由流程可知,加
2 3 2 2 3
NaOH溶解时Fe O 不反应,由信息可知SiO 在“碱溶”时转化为铝硅酸钠沉淀,过滤得
2 3 2
到的滤渣为Fe O、铝硅酸钠,然后加入碳酸氢钠与NaAlO 反应生成Al(OH) 沉淀和碳酸
2 3 2 3
钠溶液,过滤II得到Al(OH) ,灼烧生成氧化铝,电解I为电解氧化铝生成Al和氧气,电
3
解II为电解NaCO 溶液,阴极得到NaHCO 、阳极得到NaOH,循环利用。
2 3 3
【详解】
(1)碱溶时氧化铝和NaOH溶液反应得到偏铝酸钠和水,离子方程式为Al O+2OH−=2AlO
2 3
+H O;
2
(2)Al(OH) 可以和盐酸反应生成可溶性盐氯化铝和水,离子方程式为Al(OH) +3H+ =2Al3++
3 3
3HO;
2
(3)根据分析,向“过滤Ⅰ”所得滤液中加NaHCO 溶液,NaAlO 和残留的NaOH反应生
3 2
成Al(OH) 沉淀和碳酸钠溶液,碱性为OH->AlO >CO ,所以溶液碱性减弱,pH减
3
小;
(4)电极熔融Al O 时,阳极阳离子被氧化生成氧气,石墨电极被阳极上产生的O 氧化,
2 3 2
从而被损耗;
(5)铵盐受热易分解,高温条件下NH Cl分解产生的HCl能够破坏Al表面的Al O 薄膜,
4 2 3
有利于AlN的制备;
(6)根据元素守恒可知样品中n(AlCl )=2n(Al O) mol,所以AlCl 的质量分数为
3 2 3 3×100%= 或 或
。
3.硫酸铜晶体(CuSO ·5H O)是铜盐中重要的无机化工原料,广泛应用于农业、电镀、饲
4 2
料添加剂、催化剂、石油、选矿、油漆等行业。
I.采用孔雀石[主要成分CuCO·Cu(OH) ]、硫酸(70%)、氨水为原料制取硫酸铜晶体。其工
3 2
艺流程如图: 预处理
已知:(1)硫酸铜晶体易溶于水,难溶于乙醇。
(2)硫酸铜晶体在102℃时失水成CuSO ·3H O,在113℃时失水成CuSO ·H O,在258℃时
4 2 4 2
失水成CuSO 。
4
请回答下列问题:
(1)已知氨浸时发生的反应为CuCO·Cu(OH) +8NH·H O=[Cu(NH )](OH) CO+8H O,蒸
3 2 3 2 3 4 2 2 3 2
氨时得到的固体呈黑色。孔雀石经过氨浸、蒸氨操作目的是:___。
(2)下列说法正确的是___。
A.步骤I,高温可提高浸取率
B.预处理时用破碎机将孔雀石破碎成粒子直径<1mm,其目的是提高反应速率和浸取率
C.步骤III,蒸氨出来的气体有污染,需要净化处理,经吸收净化所得的溶液可作化肥
D.步骤IV,固液分离操作可采用常压过滤,也可采用减压过滤
(3)步骤IV为一系列的操作:①使晶体从溶液中析出,可采取的方式有___(写出两条)。
②减压过滤后,洗涤沉淀可能需要用到以下操作:
a.加入水至浸没沉淀物;b.加入乙醇至浸没沉淀物;c.洗涤剂缓慢通过沉淀物;d.洗涤剂快
速通过沉淀物;e.关小水龙头;f.开大水龙头;g.重复2-3次。
请选出正确的操作并排序 → → →f→ 。___。
③晶体中所含结晶水可通过重量分析法测定,主要步骤有:a.称量b.置于烘箱中脱结晶水
c.冷却d.称量e.重复b~d至恒重f.计算。步骤e的目的是___。
④若测得结晶水的含量偏低,则杂质可能是___。
II.采用金属铜单质制备硫酸铜晶体
(4)某兴趣小组查阅资料得知:Cu+CuCl =2CuCl,4CuCl+O +2H O=2[Cu(OH) ·CuCl ],
2 2 2 2 2
[Cu(OH) ·CuCl ]+H SO =CuSO+CuCl +2H O。现设计如下实验来制备硫酸铜晶体,装置
2 2 2 4 4 2 2
及相关物质溶解度随温度变化如图:
向铜和稀硫酸的混合物中加入氯化铜溶液,利用二连球鼓入空气,将铜溶解,当三颈烧
瓶中呈乳状浑浊液时,滴加浓硫酸。装置中存在一处缺陷是___;最后可以利用重结晶的
方法纯化硫酸铜晶体的原因为___。
【答案】(1)除去孔雀石中的杂质,获得纯净的氧化铜 (2) BCD (3) ①蒸发浓缩至表层
出现晶膜、冷却结晶;加入适量无水乙醇 ② ebcg ③ 检验晶体中的结晶水是否已全
部失去或确保晶体中的结晶水已全部失去 ④ CuSO •3H O或CuSO •H O或CuSO (4)
4 2 4 2 4
三颈烧瓶形成密闭体系,空气很难鼓入 氯化铜的溶解度在常温下比硫酸铜晶体大得
多,且氯化铜的溶解度随温度的变化程度不大
【分析】由题给流程可知,孔雀石经粉碎预处理后,加入氨水氨浸时,CuCO·Cu(OH) 溶于氨水转
3 2
化为[Cu(NH )](OH) CO,过滤得到含有[Cu(NH )](OH) CO 的滤液和沉淀;滤液经蒸氨,
3 4 2 2 3 3 4 2 2 3
[Cu(NH )](OH) CO 受热分解生成二氧化碳、氨气、氧化铜和水,向氧化铜固体中加入
3 4 2 2 3
70%硫酸,氧化铜溶解得到硫酸铜浸出液,向浸出液中加入适量无水乙醇降低硫酸铜的溶
解度,经蒸发浓缩至表层出现晶膜、冷却结晶,过滤或减压过滤,用无水乙醇洗涤沉淀,
干燥得到硫酸铜晶体。
【详解】
(1)由分析可知,孔雀石经过氨浸、蒸氨可以达到除去孔雀石中的杂质,获得纯净的氧化
铜的目的,故答案为:除去孔雀石中的杂质,获得纯净的氧化铜;
(2)A.由分析可知,若步骤I时采用高温,氨水会受热挥发,反应生成
[Cu(NH )](OH) CO 会受热分解生成氧化铜,使浸取率降低,故错误;
3 4 2 2 3
B.预处理时用破碎机将孔雀石破碎成粒子直径<1mm,可以增大反应物的接触面积,使
反应更加充分,加快反应速率,提高浸取率,故正确;
C.步骤III,蒸氨出来的氨气直接排出,会污染空气,若用一定浓度的硫酸溶液吸收净化,
可以防止污染空气,所得的硫酸铵溶液可作化肥,故正确;
D.步骤IV时,采用常压过滤或减压过滤都可以得到硫酸铜晶体,故正确;
BCD正确,故答案为:BCD;
(3) ①由分析可知,可以向浸出液中加入适量无水乙醇降低硫酸铜的溶解度,经蒸发浓缩
至表层出现晶膜、冷却结晶析出硫酸铜晶体,故答案为:蒸发浓缩至表层出现晶膜、冷
却结晶;加入适量无水乙醇;
②减压过滤后,洗涤沉淀时,先关小水龙头,加入乙醇至浸没沉淀物,使洗涤剂缓慢通
过沉淀物,将晶体表面的杂质洗涤干净,然后开大水龙头,加入乙醇至浸没沉淀物,使
洗涤剂快速通过沉淀物,减少晶体因溶解造成损失,并重复操作2-3次,则减压过滤后,
洗涤沉淀的正确操作为e→b→c→f→g,故答案为:ebcg;
③晶体中所含结晶水可通过重量分析法测定时,重复置于烘箱中脱结晶水、冷却、称量
的操作可以确保晶体中的结晶水已全部失去,减少测定结晶水含量的误差,故答案为:
检验晶体中的结晶水是否已全部失去或确保晶体中的结晶水已全部失去;④若晶体中含有CuSO •3H O或CuSO •H O或CuSO 杂质,会导致测得结晶水的含量偏
4 2 4 2 4
低,故答案为:CuSO •3H O或CuSO •H O或CuSO ;
4 2 4 2 4
(4)由实验装置图可知,该装置的缺陷为三颈烧瓶为密闭体系,不能起到平衡气压的作用,
不利于空气鼓入;由溶解度曲线可知,氯化铜的溶解度在常温下比硫酸铜晶体大得多,
且氯化铜的溶解度随温度的变化程度不大,可以利用重结晶的方法纯化硫酸铜晶体,故
答案为:三颈烧瓶形成密闭体系,空气很难鼓入;氯化铜的溶解度在常温下比硫酸铜晶
体大得多,且氯化铜的溶解度随温度的变化程度不大。
4.对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝( )、钼( )、镍(
预处理
)等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:25℃时, 的 , ;
; ;该工艺中, 时,溶液
中 元素以 的形态存在。
(1)“焙烧”中,有 生成,其中 元素的化合价为_______。
(2)“沉铝”中,生成的沉淀 为_______。(3)“沉钼”中, 为7.0。
①生成 的离子方程式为_______。
②若条件控制不当, 也会沉淀。为避免 中混入 沉淀,溶液中
_______(列出算式)时,应停止加入 溶液。
(4)①滤液Ⅲ中,主要存在的钠盐有 和 , 为_______。
②往滤液Ⅲ中添加适量 固体后,通入足量_______(填化学式)气体,再通入足量
,可析出 。
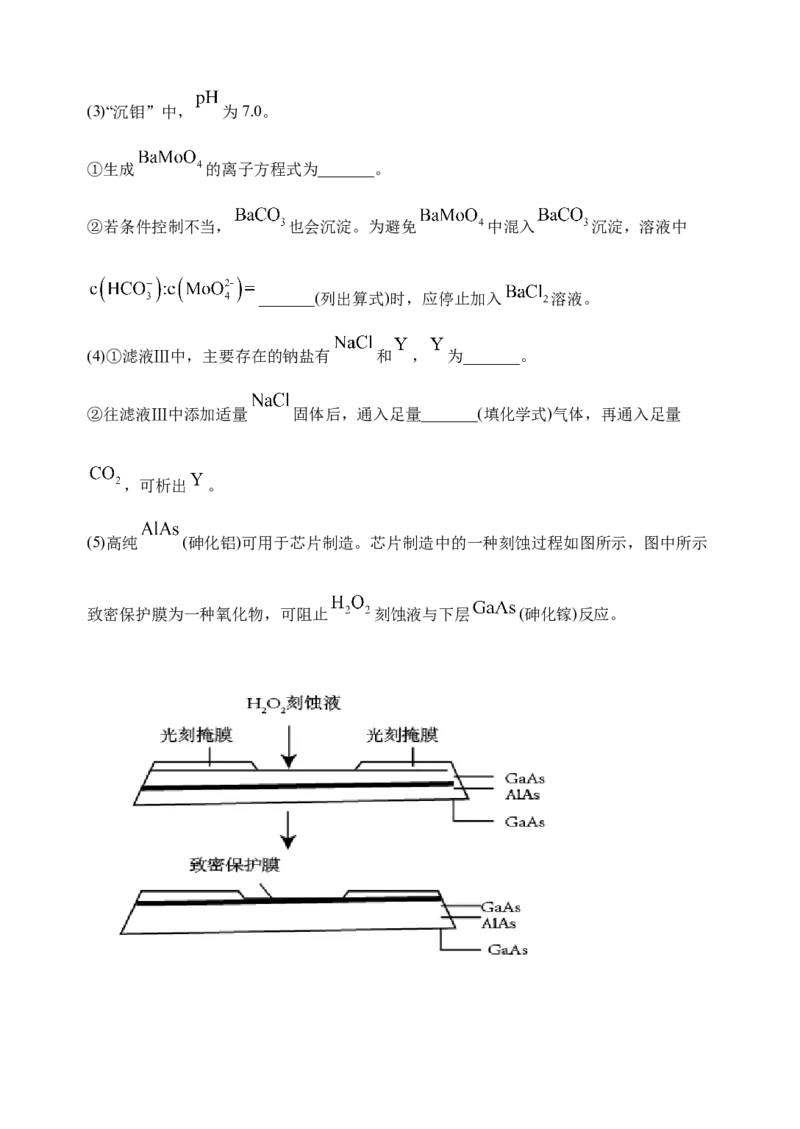
(5)高纯 (砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示
致密保护膜为一种氧化物,可阻止 刻蚀液与下层 (砷化镓)反应。①该氧化物为_______。
②已知: 和 同族, 和 同族。在 与上层 的反应中, 元素的化
合价变为+5价,则该反应的氧化剂与还原剂物质的量之比为_______。
【答案】(1)+6 (2) (3) + = ↓
(4) (5)
【分析】
由题中信息可知,废催化剂与氢氧化钠一起焙烧后,铝和钼都发生了反应分别转化为偏
铝酸钠和钼酸钠,经水浸、过滤,分离出含镍的固体滤渣,滤液I中加入过量的二氧化碳,
偏铝酸钠转化为氢氧化铝沉淀,过滤得到的沉淀X为氢氧化铝,滤液II中加入适量的氯
化钡溶液沉钼后,过滤得到钼酸钡。
【详解】
(1)“焙烧”中,有 生成,其中Na和O的化合价为+1和-2,根据化合价的
代数和为0可知, 元素的化合价为+6。
(2)“沉铝”中,偏铝酸钠转化为氢氧化铝,因此,生成的沉淀 为 。
(3)①滤液II中含有钼酸钠,加入氯化钡溶液后生成 沉淀,该反应的离子方
程式为 + = ↓。
②若开始生成 沉淀,则体系中恰好建立如下平衡:
,该反应的化学平衡常数为。为避免
中混入 沉淀,必须满足 ,由于
“沉钼”中 为7.0, ,所以溶液中
时,开始生成 沉淀, 因此,
时,
应停止加入 溶液。
(4)①滤液I中加入过量的二氧化碳,偏铝酸钠转化为氢氧化铝沉淀,同时生成碳酸氢
钠,过滤得到的滤液II中含有碳酸氢钠和钼酸钠。滤液II中加入适量的氯化钡溶液沉钼
后,因此,过滤得到的滤液Ⅲ中,主要存在的钠盐有 和 ,故 为
。
②根据侯氏制碱法的原理可知,往滤液Ⅲ中添加适量 固体后,通入足量 ,再
通入足量 ,可析出 。
(5)①由题中信息可知,致密的保护膜为一种氧化物,是由 与 反应生成的,联想到金属铝表面容易形成致密的氧化膜可知,该氧化物为 。
②由 和 同族、 和 同族可知, 中显+3价(其最高价)、 显-3价。
在 与上层 的反应中, 元素的化合价变为+5价,其化合价升高了8,
元素被氧化,则该反应的氧化剂为 ,还原剂为 。 中的O元素为-1价,
其作为氧化剂时,O元素要被还原到-2价,每个 参加反应会使化合价降低2,根据
氧化还原反应中元素化合价升高的总数值等于化合价降低的总数值可知,该反应的氧化
剂与还原剂物质的量之比为 。
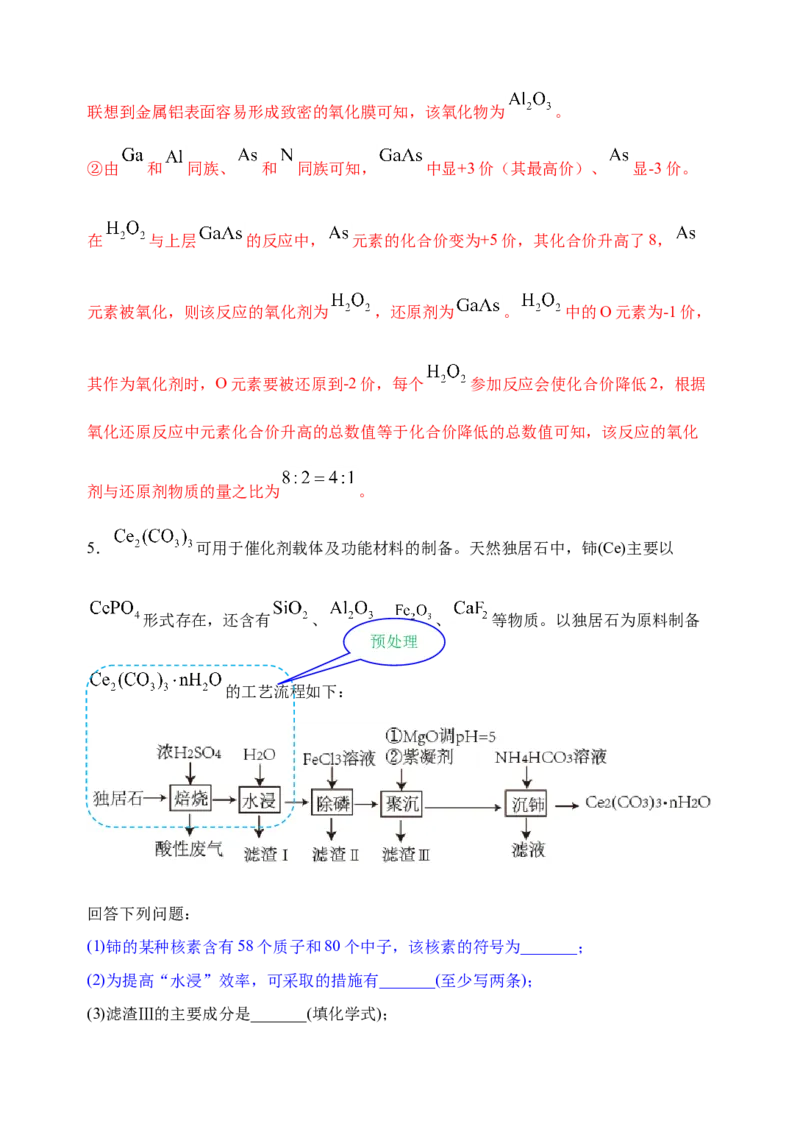
5. 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以
形式存在,还含有 、 、 、 等物质。以独居石为原料制备
预处理
的工艺流程如下:
回答下列问题:
(1)铈的某种核素含有58个质子和80个中子,该核素的符号为_______;
(2)为提高“水浸”效率,可采取的措施有_______(至少写两条);
(3)滤渣Ⅲ的主要成分是_______(填化学式);(4)加入絮凝剂的目的是_______;
(5)“沉铈”过程中,生成 的离子方程式为_______,常温下加入的
溶液呈_______(填“酸性”“碱性”或“中性”)(已知: 的
, 的 , );
(6)滤渣Ⅱ的主要成分为 ,在高温条件下, 、葡萄糖( )和
可制备电极材料 ,同时生成 和 ,该反应的化学方程式为_______
【答案】(1) (2) 适当升高温度,将独居石粉碎等 (3) Al(OH) (4) 促使铝离子沉
3
淀 (5) ↑ 碱性 (6)6
+ +12 =12 +6CO↑+6H O+6CO↑
2 2
【分析】
焙烧浓硫酸和独居石的混合物、水浸, 转化为Ce (SO ) 和HPO , 与硫酸不
2 4 3 3 4
反应, 转化为Al (SO ), 转化为Fe (SO ), 转化为CaSO 和HF,酸性
2 4 3 2 4 3 4
废气含HF;后过滤,滤渣Ⅰ为 和磷酸钙、FePO ,滤液主要含HPO ,Ce (SO ),
4 3 4 2 4 3
Al (SO ),Fe (SO ),加氯化铁溶液除磷,滤渣Ⅱ为FePO ;聚沉将铁离子、铝离子转化
2 4 3 2 4 3 4
为沉淀,过滤除去,滤渣Ⅲ主要为氢氧化铝,还含氢氧化铁;加碳酸氢铵沉铈得
Ce (CO)·nH O。
2 3 3 2
【详解】(1)铈的某种核素含有58个质子和80个中子,则质量数为58+80=138,该核素的符号为
;
(2)为提高“水浸”效率,可采取的措施有适当升高温度,将独居石粉碎等;
(3)结合流程可知,滤渣Ⅲ的主要成分是Al(OH) ;
3
(4)加入絮凝剂的目的是促使铝离子沉淀;
(5)用碳酸氢铵“沉铈”,则结合原子守恒、电荷守恒可知生成 的离子
方程式为 ↑;铵根离子的水解常
数K( )= ≈5.7×10-10,碳酸氢根的水解常数K( )==
h h
≈2.3×10-8,则K( )