文档内容
微专题突破2 氧化还原反应 离子反应
古之立大事者,不惟有超世之才,亦必有坚忍不拔之志。——苏轼
目标定位
1.理解氧化还原反应规律并能应用有关规律解决问题。
2.根据离子的性质(酸碱性、氧化性、还原性、水解性、配合性),能准确书写离子方程式并能判断所给
离子方程式的正误。
3.能根据题目要求检验溶液中存在的离子。
教学重点难点
1.电子守恒的应用。
2.离子方程式判断及离子的检验。
教学方法
讨论、归纳
教学过程
【规律点和易错点】
孙猴子七十二般变化,都逃不出你的手心
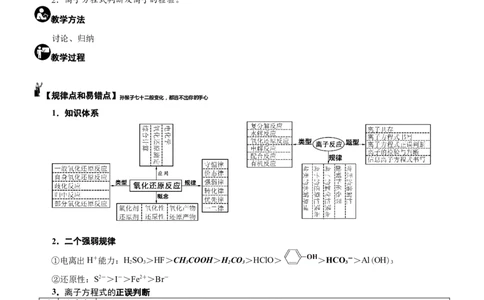
1.知识体系
2.二个强弱规律
①电离出H+能力:HSO >HF>CHCOOH>HCO>HClO> >HCO ->Al(OH)
2 3 3 2 3 3 3
②还原性:S2->I->Fe2+>Br-
3.离子方程式的正误判断
① 合事实 离子反应要符合客观事实,不可臆造产物及反应
化学式与离子符号使用正确合理,该“拆”或不该“拆”要分清。易溶且易电离的物质即可
② 式正确 溶性的强电解质包括强酸、强碱、大多数的可溶性盐(不包括配盐),应写以实际参加反应
的离子的符号;非电解质、难溶物、气体、单质、氧化物等一律写化学式
③ 号实际 “=”、“ ”、“→”、“↑”、“↓”等符号符合实际
④ 三守恒 两边原子数、电荷数、电子得失数目必须守恒
⑤ 明类型 分清类型,注意少量、过量等
⑥ 细检查 结合书写离子方程式过程中易出现的错误,细心检查
4.两种方法配平过量或少量SO 与NaClO反应的离子方程式
2
将少量的物质系数定为1,然后再将其中的离子完全参加反应,根据所需离子的量从而确定另一种
物质需要多少。如:
方法一 则SO (少量)+ClO-+HO=SO 2-+Cl-+2H+,又由于H++ClO-=
若SO 少量 2 2 4
2 HClO,所以SO 少量时,SO (少量)+3ClO-+HO=SO 2-+Cl-+2HClO
2 2 2 4
若ClO-少量 则有ClO-(少量)+SO +HO=SO 2-+Cl-+2H+
2 2 4微专题突破2 氧化还原反应 离子反应 问题的态度:问则少;辩则明
利用转移电子数守恒,写出一个“基准”离子反应式,再利用过量物质中的离子与“基准”离子
方程式中的产物离子是否共存,进行书写。如 SO 与NaClO反应:先利用转移电子数相等,确
2
定:ClO-+SO +HO=SO 2-+Cl-+2H+
2 2 4
方法二 过量的SO 不与“基准”反应产物中的任何微粒反应,则该离子方程式可表
若SO 过量 2
2 示SO 过量
2
过量的次氯酸根继续发生:H++ClO-=HClO,则离子方程式应为3ClO-
若ClO-过量
(过量)+SO +HO=SO 2-+Cl-+2HClO
2 2 4
考考
(2024·江苏卷节选)氢能是理想清洁能源,氢能产业链由制氢、储氢和用氢组成。
利用铁及其氧化物循环制氢,原理如图所示。反应器Ⅰ中化合价发生改变的元素有_____________;含CO
和H 各1 mol的混合气体通过该方法制氢,理论上可获得_______mol H。
2 2
【答案】C、H、Fe
【解析】反应器I中参与反应的物质有CO、H、Fe O,产物有CO、HO、Fe,发生反应3CO+FeO=
2 2 3 2 2 2 3
2Fe+3CO、3H+FeO=2Fe+3HO化合价发生改变的元素有C、H、Fe;CO、H 各1 mol参与上述反应,
2 2 2 3 2 2
各生成 mol Fe,共生成 mol Fe, mol Fe在反应器Ⅱ中发生反应3Fe+4HO(g)=Fe O+4H,则 mol Fe参
2 3 4 2
加反应生成的n(H)=n(Fe)×= mol×= mol,共生成 mol H₂。
2
【问题解决1】
1.已知在酸性溶液中,Fe O易转化为Fe2+:Fe O+2e-+8H+=2Fe2++4HO。
2 2 2
有KMnO 、NaCO 、Cu O、Fe (SO ) 四种物质中的一种能使上述还原过程发生,写出该氧化还原反应的
4 2 3 2 2 4 3
离子方程式并配平:_______________________________________________。
【答案】Fe O+Cu O+10H+=2Fe2++2Cu2++5HO
2 2 2
2.(2025·南通市如东县期初考)MnCO 在空气中,一段时间后会生成MnO(OH),写出该反应的化学
3 2
方程式___________________________________________________。
【答案】2MnCO+O+2HO=2MnO(OH)+2CO
3 2 2 2 2
【解析】MnCO 在空气中一段时间后,与空气中的氧气和水反应,生成MnO(OH),故方程式为:
3 2
2MnCO+O+2HO=2MnO(OH)+2CO
3 2 2 2 2
氧化还原反应规律及应用
规律 内容 应用
元素处于最高价只有氧化性,最低价只有还原性,
价态律 判断元素的氧化性、还原性
中间价态既有氧化性,又有还原性
强氧化性的氧化剂与强还原性的还原剂反应, 判断反应能否进行
强弱律
生成弱还原性的还原产物和弱氧化性的氧化产物
比较微粒的氧化性或还原性强弱
优先律 多种氧化剂遇一种还原剂时,氧化性最强的先反应 判断反应先后顺序
判断氧化还原反应能否发生、电子转移情
转化律 同一元素的不同价态间反应,其价态只靠拢不交叉
况
一二律 一个氧化还原反应可拆分为氧化与还原两个半反应 书写电极反应式
守恒律 氧化还原反应中得失电子数相等 配平、相关计算
考点精练
1.(2023·山东)一种制备Cu O的工艺路线如图所示,反应Ⅱ所得溶液pH在3~4之间,反应Ⅲ需及时
2
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找补加NaOH以保持反应在pH=5条件下进行。常温下,HSO 的电离平衡常数K =1.3×10-2,K =6.3×10-
2 3 a1 a2
8。
下列说法正确的是
A.反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应
B.低温真空蒸发主要目的是防止NaHSO 被氧化
3
C.溶液Y可循环用于反应Ⅱ所在操作单元吸收气体Ⅰ
D.若Cu O产量不变,参与反应Ⅲ的X与CuSO 物质的量之比增大时,需补加NaOH的量减少
2 4
【答案】CD
【解析】铜和浓硫酸反应(反应Ⅰ)生成二氧化硫气体(气体Ⅰ)和硫酸铜,生成的二氧化硫气体与碳酸钠反
应(反应Ⅱ),所得溶液 pH在3~4之间,溶液显酸性,根据 HSO 的电离平衡常数 K =1.3×10-2,K =
2 3 a1 a2
6.3×10-8,可知NaHSO 溶液显酸性(电离大于水解),则反应Ⅱ所得溶液成分是NaHSO ,调节溶液pH值至
3 3
11,使NaHSO 转化为NaSO ,低温真空蒸发(防止NaSO 被氧化),故固液分离得到NaSO 晶体和NaSO 溶
3 2 3 2 3 2 3 2 3
液,NaSO 和CuSO 反应的离子方程式是SO2-+2Cu2++2HO=SO 2-+Cu O↓+4H+,反应过程中酸性越来
2 3 4 3 2 4 2
越强,使NaSO 转化成SO 气体,总反应方程式是2CuSO +3NaSO =Cu O+2SO ↑+3NaSO ,需及时补加
2 3 2 4 2 3 2 2 2 4
NaOH以保持反应在pH=5条件下进行,据此分析解答。
A项,反应Ⅰ是铜和浓硫酸反应生成SO 、CuSO 和HO,是氧化还原反应,反应Ⅱ是SO 和碳酸钠溶液反
2 4 2 2
应生成NaHSO 和CO ,是非氧化还原反应,反应Ⅲ是NaSO 和CuSO 反应生成Cu O、NaSO 和SO ,是氧化
3 2 2 3 4 2 2 4 2
还原反应,错误;B项,低温真空蒸发主要目的是防止NaSO 被氧化,而不是NaHSO ,错误;C项,溶液Y
2 3 3
含NaSO ,可循环用于反应Ⅱ的操作单元吸收SO 气体(气体Ⅰ),正确;D项,制取Cu O总反应方程式是
2 3 2 2
2CuSO +3NaSO =Cu O↓+2SO ↑+3NaSO ,化合物 X 为 NaSO ,若 Cu O 产量不变,增大时,多的
4 2 3 2 2 2 4 2 3 2
NaSO 会消耗氢离子,为控制反应pH=5,可减少NaOH的量,正确。
2 3
2.(2022·山东)在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的是
A.含N分子参与的反应一定有电子转移
B.由NO生成HONO的反应历程有2种
C.增大NO的量,C H 的平衡转化率不变
3 8
D.当主要发生包含②的历程时,最终生成的水减少
【答案】D
【解析】A项,根据反应机理图知,含N分子发生的反应有NO+·OOH=NO +·OH、NO+NO +HO
2 2 2
=2HONO、NO +·C H =C H +HONO、HONO=NO+·OH,含N分子NO、NO 、HONO中N元素的
2 3 7 3 6 2
化合价依次为+2价、+4价、+3价,上述反应中均有元素化合价的升降,都为氧化还原反应,一定有电子转
移,正确;B项,根据图示,由NO生成HONO的反应历程有2种,正确;C项,NO是催化剂,增大NO的量,
C H 的平衡转化率不变,正确;D项,无论反应历程如何,在NO催化下丙烷与O 反应制备丙烯的总反应都为
3 8 2
2C H+O N\s\up 4()2C H+2HO,当主要发生包含②的历程时,最终生成的水不变,错误。
3 8 2 O 3 6 2
3.(2024·北京卷)可采用Deacon催化氧化法将工业副产物 制成Cl,实现氯资源的再利用。反应的
2
热化学方程式:4HCl(g)+O(g)=====2Cl(g)+2HO(g) ∆H=-114.4 kJ·mol-1。下图所示为该法的一种催
2 2 2
化机理。微专题突破2 氧化还原反应 离子反应 问题的态度:问则少;辩则明
下列说法不正确的是
A.Y为反应物HCl,W为生成物HO
2
B.反应制得1 mol Cl,须投入2 mol CuO
2
C.升高反应温度,HCl被O 氧化制Cl 的反应平衡常数减小
2 2
D.图中转化涉及的反应中有两个属于氧化还原反应
【答案】B
【解析】由该反应的热化学方程式可知,该反应涉及的主要物质有HCl、O、CuO、Cl、HO;CuO与Y
2 2 2
反应生成Cu(OH)Cl,则Y为HCl;Cu(OH)Cl分解生成W和Cu OCl ,则W为HO;CuCl 分解为X和
2 2 2 2
CuCl,则X为Cl;CuCl和Z反应生成Cu OCl ,则Z为O;综上所述,X、Y、Z、W依次是Cl、HCl、O、
2 2 2 2 2 2
HO。
2
A项,由分析可知,Y为反应物HCl,W为生成物HO,正确;B项,CuO在反应中作催化剂,会不断循
2
环,适量即可,错误;C项,总反应为放热反应,其他条件一定,升温平衡逆向移动,平衡常数减小,正确;D
项,图中涉及的两个氧化还原反应是CuCl — \s\up 0()CuCl和CuCl— \s\up 0()Cu OCl ,正确。
2 → → 2 2
【问题解决2】
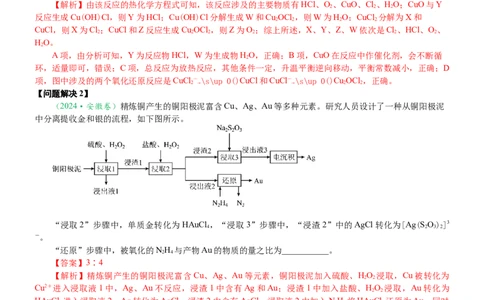
(2024·安徽卷)精炼铜产生的铜阳极泥富含Cu、Ag、Au等多种元素。研究人员设计了一种从铜阳极泥
中分离提收金和银的流程,如下图所示。
“浸取2”步骤中,单质金转化为HAuCl ,“浸取3”步骤中,“浸渣2”中的AgCl转化为[Ag(SO)]3
4 2 3 2
-。
“还原”步骤中,被氧化的NH 与产物Au的物质的量之比为___________。
2 4
【答案】3∶4
【解析】精炼铜产生的铜阳极泥富含Cu、Ag、Au等元素,铜阳极泥加入硫酸、HO 浸取,Cu被转化为
2 2
Cu2+进入浸取液1中,Ag、Au不反应,浸渣1中含有Ag和Au;浸渣1中加入盐酸、HO 浸取,Au转化为
2 2
HAuCl 进入浸取液2,Ag转化为AgCl,浸渣2中含有AgCl;浸取液2中加入NH 将HAuCl 还原为Au,同时
4 2 4 4
NH 被氧化为N ;浸渣2中加入NaSO ,将AgCl转化为[Ag(SO)]3-,得到浸出液3,利用电沉积法将
2 4 2 2 2 3 2 3 2
[Ag(SO)]3-还原为Ag。
2 3 2
还原步骤中,HAuCl 被还原为Au,Au化合价由+3价变为0价,一个HAuCl 转移3个电子,NH 被氧化
4 4 2 4
为N ,N的化合价由-2价变为0价,一个NH 转移4个电子,根据得失电子守恒,被氧化的NH 与产物Au
2 2 4 2 4
的物质的量之比为3∶4。
或HAuCl 4 得 -— 3 — e\s\up 4()Au、N 2 H 4 失 -— 2 — e\s\up 4()N 2 ,由得失电子数目守恒可知,n(HAuCl 4 )×3=n(N 2 H 4 )×4,
n(NH)∶n(HAuCl )=3∶4。
2 4 4
电子守恒原理
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找写两式 氧化剂+ne\s\up 4()还原产物、还原剂-me\s\up 4()氧化产物
-—— -——
列等式 n(氧化剂)×化合价变化值×变价原子数=n(还原剂)×化合价变化值×变价原子数
考点精练
1.(2024·南通市如皋市高三上学期开学考)以绿矾(FeSO •7HO)为原料,可以制取铁铬氧体
4 2
Cr Fe O (Cr为+3价)。制取的方法如下:向含1 mol CrO2-的溶液中,加入10 mol FeSO •7HO,充分反应
2 20 27 4 4 2
后向溶液中边通入空气边滴加NaOH溶液,反应后过滤得到铁铬氧体。反应共消耗O 的物质的量为__________。
2
【答案】0.25 mol
【解析】根据化合物中各元素化合价代数和为0,Cr Fe O 中Cr元素+3价,则Fe元素平均化合价为+
2 20 27
2.4价;若1 mol CrO2-与10 mol FeSO •7HO混合,充分反应后可得到Cr Fe O 物质的量为 mol,则1 mol
4 4 2 2 20 27
CrO2-得到3 mol电子,10 mol FeSO •7HO失去4 mol电子,根据得失电子守恒,氧气得到1 mol电子,故
4 4 2
反应共消耗O 的物质的量:0.25 mol。
2
或:CrO2-得3e\s\up 4()Cr3+,Fe2+失0.\s\up 4()Cr Fe O 、O 得4e\s\up 4()Cr Fe O ,由得失电子数目守恒可知,
4 -—— 4e- 2 20 27 2-—— 2 20 27
n(CrO2-)×3+n(O)×4=n(Fe)×0.4,1 mol×3+n(O)×4=10 mol×0.4,n(O)=0.25 mol。
4 2 2 2
2.(2024·无锡上学期期中)在pH=2的废水中,Cr(VI)主要以HCrO -和Cr O2-的形式存在,选用还原
4 2 7
剂FeSO 处理此废水,生成Fe Cr(OH) 沉淀,Fe2+还原Cr O2-时,两者物质的量之比为________。实际投入
4 3 12 2 7
FeSO 的量需大于上述计算值的可能原因是_________________________________________________________。
4
【答案】6∶1 Fe2+具有还原性,在酸性条件下能被溶液中的溶解氧氧化
【解析】在pH=2的废水中,Cr(VI)主要以HCrO -和Cr O2-的形式存在,选用还原剂FeSO 处理此废水,
4 2 7 4
生成Fe Cr(OH) 沉淀,Fe2+还原Cr O2-时,Fe2+变为Fe3+、Cr由+6价变为+3价,根据电子守恒可知,
3 12 2 7
n(Fe2+)=6n(Cr O2-),故两者物质的量之比为6∶1,由于Fe2+具有还原性,在酸性条件下能被溶液中的溶解
2 7
氧化,则实际投入FeSO 的量需大于上述计算值,故答案为:6∶1;Fe2+具有还原性,在酸性条件下能被溶液
4
中的溶解的氧氧化。
3.(2023·海安实验中学)硫酸盐还原菌(SRB)常存在于水体中,会腐蚀许多金属及合金。一种Fe合金
在硫酸盐还原菌存在条件下腐蚀的机理如图所示。已知:溶液中的 S2-会完全转化为FeS,则Fe腐蚀后生成
Fe(OH) 和FeS的物质的量之比为__________。
2
【答案】3∶1
【解析】反应可简单表示为Fe+SO―→Fe(OH)+FeS,设Fe(OH)、FeS物质的量分别为x、y,根据得失
2 2
电子守恒,得2x+2y=8y,x∶y=3∶1。
4.(2024·连云港上学期调研一)为测定某NiC O•2HO产品的纯度,现进行如下实验:准确取2.400 g
2 4 2
样品,用足量硫酸溶解后,加水稀释到250 mL,取25.00 mL所配溶液于锥形瓶中,加入12.00 mL 0.0500
mol·L-1标准KMnO 溶液,振荡使其充分反应;向反应后的溶液滴加0.0300 mol·L-1的(NH )Fe(SO ) 标准溶
4 4 2 4 2
液与过量的KMnO 反应,恰好完全反应时消耗(NH )Fe(SO ) 标准溶液体积为20.00 mL,计算NiC O•2HO
4 4 2 4 2 2 4 2
产品的纯度___________(写出计算过程,杂质不参与反应),实验过程中反应如下:
H++C O2-+MnO -——Mn2++CO↑+HO(未配平);H++Fe2++MnO -——Mn2++Fe3+↑+HO(未配
2 4 4 2 2 4 2
平)。Ni相对原子质量为59。
【答案】91.5%
【解析】MnO -得5e\s\up 4()Mn2+、C O2-失2e\s\up 4()CO ,Fe2+失e-\s\up 4()Fe3+,n(MnO -)×5=n(C O2-)×2
4 -—— 2 4 -—— 2 ——→ 4 2 4
+n(Fe2+)×1,由得失电子数目守恒可知,在25.00 mL中:0.0500 mol·L-1×0.012 L×5=n(C O2-)×2+
2 4
0.0300 mol·L-1×0.020 L×1,n(C O2-)=0.0012 mol,250 mL溶液中二水草酸镍的物质的量为0.012 mol,则
2 4
产品的纯度为×100%=91.5%,故答案为:91.5%。
【问题解决3】微专题突破2 氧化还原反应 离子反应 问题的态度:问则少;辩则明
有关反应 离子方程式
1 NO 与水的反应 3NO +HO=2H++2NO -+2NO
2 2 2 3
2 Fe(OH) 胶体的制备 Fe3++3HO====Fe(OH)(胶体)+3H+
3 2 3
3 硫化钠的水解 S2-+HO HS-+OH-
2
4 过量CO 通入饱和碳酸钠溶液中 2Na++CO32-+CO+HO=2NaHCO ↓
2 2 2 3
5 少量CO 通入苯酚钠溶液中 CO+C HO-+HO— \s\up 0()C HO+HCO -
2 2 6 5 6 2 → 6 6 6 3
6 用惰性电极电解氯化镁溶液 Mg2++2Cl-+2HO====Mg(OH)+H↑+Cl↑
2 2 2 2
离子方程式的书写
书写后务必做到四检查:
①配平(特别关注:电荷守恒);②反应条件(如加热、催化剂、通电等);③符号使用:↑、↓、
(重点关注);④产物有无失真(注意溶液的酸碱性、试剂的用量)。
考点精练
有关反应 离子方程式
酸性高锰酸钾溶液检验Fe3+溶液中是
① 5Fe2++MnO -+8H+=5Fe3++Mn2++4HO
否含有Fe2+(不含Cl-) 4 2
①________________________________________________
②________________________________________________
② FeCl 与NaSO 溶液反应的可能性
3 2 3 2Fe3++3SO2-+3HO=2Fe(OH)↓+3SO ↑
3 2 3 2
2Fe3++SO2-+HO=2Fe2++SO 2-+2H+
3 2 4
③ NaCO 溶液中通入过量SO CO2-+2SO +HO=2HSO -+CO
2 3 2 3 2 2 3 2
④ 溴乙烷发生消去反应 C HBr+OH-Δ—\s\up 4()CH=CH↑+NaBr+HO
2 5 —→ 2 2 2
⑤ FeSO 溶液中加入HO 产生沉淀 2Fe2++HO+4HO=2Fe(OH)↓+4H+
4 2 2 2 2 2 3
在强碱性溶液中,次氯酸 钠与
⑥ 3ClO-+2Fe(OH)+4OH-=2FeO2-+3Cl-+5HO
Fe(OH) 反应生成NaFeO 3 4 2
3 2 4
【问题解决4】
① (2025·扬州开学考)工业废液中通入HS除Hg2+:S2-+Hg2+=HgS↓ 错
2
② (2024·浙江1月卷)硫化钠溶液在空气中氧化变质:2S2-+O+4H+=2S↓+2HO 错
2 2
(2024•南通市海安市上学期开学考)SO 通入少量氨水中的离子方程式为:NH ·HO+SO =
③ 2 3 2 2 对
NH+HSO -
3
④ (2024·江苏南通二模)Cu O与稀硫酸反应:Cu O+2H+=2Cu2++HO 错
2 2 2
(2024·江苏南通二模)黄铜(CuFeS)用Fe (SO ) 溶液浸泡后生成单质硫:CuFeS +4Fe3+=
⑤ 2 2 4 3 2 对
5Fe2++Cu2++2S
⑥
(2025·扬州开学考)饱和Na
2
CO
3
溶液分批浸取重晶石:CO
3
2-+BaSO
4
(s) BaCO
3
(s)+SO
4
2-
对
(2024·南通市如皋市高三上学期开学考)向小苏打溶液中滴加过量Ca(OH) 溶液时反应的离子
⑦ 2 错
方程式为2HCO -+2OH-+Ca2+=CaCO↓+CO2-+2HO
3 3 3 2
【解析】①HS是弱酸,在离子方程式中保留化学式,工业废液中通入 HS除Hg2+,反应的离子方程式为
2 2
HS+Hg2+=HgS↓+2H+,错误;②硫化钠强碱弱酸盐,溶液呈碱性,在空气中氧化变质:2S2-+O +2HO
2 2 2
=2S↓+4OH-,错误;③SO 通入少量氨水,反应生成亚硫酸氢铵,其反应的离子方程式为:NH ·HO+
2 3 2
SO =NH+HSO -,正确;④Cu O与稀硫酸发生歧化反应,离子方程式为:Cu O+2H+=Cu2++Cu+HO,
2 3 2 2 2
错误;⑤Fe (SO ) 溶液和CuFeS 反应,生成Fe2+和单质S,离子方程式为:CuFeS +4Fe3+=5Fe2++Cu2++
2 4 3 2 2
2S,正确;⑥重晶石即BaSO 与饱和NaCO 溶液反应生成碳酸钡和硫酸钠,离子方程式为CO2-+BaSO(s)
4 2 3 3 4
BaCO (s)+SO 2-,正确;⑦向小苏打溶液中滴加过量Ca(OH) 溶液,则小苏打少量,则正确的离子方程
3 4 2
式为HCO -+OH-+Ca2+=CaCO↓+HO,错误。
3 3 2
离子方程式正误判断的一般思路
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找考点精练
1.(2024·淮安市高三上学期开学考)对于下列实验,能正确描述其反应的离子方程式的是
A.向BaCl 溶液中通入SO :Ba2++HO+SO =BaSO↓+2H+
2 2 2 2 3
B.硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++HS↑
2
C.同浓度同体积NH HSO 溶液与NaOH溶液混合:NH+OH-=NH ·HO
4 4 3 2
D.用NaSO 溶液吸收少量Cl:3SO2-+Cl+HO=2HSO -+2Cl-+SO 2-
2 3 2 3 2 2 3 4
【答案】D
【解析】A项,亚硫酸属于弱酸,盐酸属于强酸,因此向氯化钡溶液中通入SO ,不发生反应,错误;B项,
2
硝酸具有强氧化性,能将Fe2+、HS氧化,错误;C项,NH HSO 在水溶液中电离出NH、H+、SO 2--,H+先
2 4 4 4
与OH-反应,两种溶液浓度相同,体积相同,则只发生H++OH-=HO,错误;D项,氯气具有强氧化性,
2
发生Cl+SO2-+HO=SO 2-+2Cl-+2H+,因为亚硫酸钠过量,因此生成H+与SO2-发生生成HSO -,即总
2 3 2 4 3 3
反应为3SO2-+Cl+HO=2HSO -+2Cl-+SO 2-,正确。
3 2 2 3 4
2.(2024·江苏南京模拟预测)下列反应表示正确的是
A.HClO在水中见光分解:HClO+HO=O↑+H++Cl-
2 2
B.惰性电极电解氯化镁溶液:2Cl-+2HO====2OH-+Cl↑+H ↑
2 2 2
C.NaClO碱性溶液与Fe(OH) 反应:3ClO-+4OH-+2Fe(OH)=2FeO2-+3Cl-+5HO
3 3 4 2
D.Ca(ClO) 溶液中通入SO :Ca2++2ClO+SO +HO=CaSO↓+2HClO
2 2 2 2 3
【答案】C
【解析】A项,HClO在水中见光分解,正确的离子方程式为2HClO====O↑+2H++2Cl-,错误;B项,
2
惰性电极电解氯化镁溶液生成氢氧化镁沉淀,正确的离子方程式为Mg2++2Cl-+2HO====Mg(OH)↓+Cl↑
2 2 2
+H↑,错误;C项,NaClO氧化Fe(OH) 生成FeO2-,自身被还原为氯离子,离子方程式正确,正确;D项,
2 3 4
Ca(ClO) 溶液中通入SO 会发生氧化还原反应生成硫酸钙,正确的离子方程式为Ca2++ClO-+SO +HO=
2 2 2 2
CaSO↓+Cl-+2H+,错误。
4
【问题解决5】
1.(2023·江阴期末)因为NaSO 具有还原性,导致产品中不可避免地存在NaSO ,检验其中是否含有
2 2 5 2 4
SO的方法是__________________________________________________________________________________。
【答案】先加入足量盐酸,再加入氯化钡溶液,若生成白色沉淀,则说明含有SO,反之,则不含有SO。
2.(2024·江苏卷)贵金属银应用广泛。Ag与稀HNO 制得AgNO,常用于循环处理高氯废水。
3 3
(2)还原AgCl。在AgCl沉淀中埋入铁圈并压实,加入足量0.5 mol·L-1盐酸后静置,充分反应得到Ag。
①铁将AgCl转化为单质Ag的化学方程式为Fe+2AgCl=FeCl +2Ag。
2
③为判断AgCl是否完全转化,补充完整实验方案:取出铁圈,搅拌均匀,取少量混合物过滤,_________
_________________________________________________________________________________________________
[实验中必须使用的试剂和设备:稀HNO、AgNO 溶液,通风设备]。
3 3
【答案】洗涤,向最后一次洗涤液中滴加硝酸银溶液,确保氯离子洗净,开启通风设备,向滤渣中加入足微专题突破2 氧化还原反应 离子反应 问题的态度:问则少;辩则明
量稀HNO,搅拌,若固体完全溶解,则AgCl完全转化,若固体未完全溶解,则AgCl未完全转化
3
【解析】判断AgCl是否完全转化,即检验混合物中是否含有AgCl,若AgCl完全转化,则剩余固体全部为
银,可完全溶于稀硝酸,若AgCl未完全转化,剩余AgCl不能溶于稀硝酸,则可用稀硝酸检验,稀硝酸参与反
应可能会产生氮氧化物,反应需在通风设备中进行,反应后的溶液中存在氯离子,若未将滤渣洗净,氯离子会
干扰实验,所以首先需要检验氯离子是否洗净,实验方案为:取出铁圈,搅拌均匀,取少量混合物过滤,洗涤,
向最后一次洗涤液中滴加AgNO 溶液,确保氯离子洗净,打开通风设备,向洗涤干净的滤渣中加入足量稀
3
HNO,搅拌,若固体完全溶解,则AgCl完全转化,若固体未完全溶解,则AgCl未完全转化。
3
离子的检验
方法 ①沉淀法——X-、SO 2-、Fe2+ ②气体法——CO2-、SO2-、NH ③显色法——X-、Fe3+、Fe2+
4 3 3
格式 操作 现象 结论(少许溶液或滤液于试管中,加入××溶液,若有××现象,则有××离子)
操作:NH需加热;试剂加入顺序:显色法检验Fe2+须先加氯水;SO 2-检验先加盐酸后加BaCl 溶液
注意 4 2
检验Fe3+中有无Fe2+:用铁氰化钾溶液
考点精练
1.(2024·南通一模)α-FeOOH在环境保护等领域有广泛应用。
在80℃下,向(NH )Fe(SO ) 溶液中边搅拌边分批加入NaClO 固体,同时滴加NaOH溶液,使溶液pH控
4 2 4 2 3
制在4~4.5之间。一段时间后,过滤、洗涤得α-FeOOH固体。
为检验(NH )Fe(SO ) 已被完全氧化,某同学向过滤所得滤液中滴加酸性KMnO 溶液,该设计方案不合理
4 2 4 2 4
的理由是___________________________________________________________________________________。
【答案】滤液中的Cl-能使酸性KMnO 溶液褪色,干扰Fe2+的检验
4
【解析】NaClO 被还原后生成NaCl,滤液中的Cl-能使酸性KMnO 溶液褪色,干扰Fe2+的检验,则该设
3 4
计方案不合理;故答案为:滤液中的Cl−能使酸性KMnO 溶液褪色,干扰Fe2+的检验。
4
2.(2024·南通一模)制备酸性乙炔银并测定其组成。将乙炔通入硝酸银溶液中可制得酸性乙炔银。反应
原理为C H+(n+2)AgNO=Ag C •nAgNO↓+2HNO。
2 2 3 2 2 3 3
将过滤所得滤渣置于小烧杯中,利用丙酮反复多次冲洗沉淀。检验滤渣已经洗净的实验方案是
_______________________________________________________________________________________________。
【答案】将最后一次洗涤液倒入少量的蒸馏水中,用pH试纸检测溶液pH,若溶液呈中性,则沉淀已洗涤
干净
【解析】当沉淀中不再含有硝酸时,沉淀则洗净,所以可以通过检查洗涤液中是否含有氢离子来判断,方
法是:将最后一次洗涤液倒入少量的蒸馏水中,用pH试纸检测溶液pH,若溶液呈中性,则沉淀已洗涤干净
3.(2024·南通市如皋二模)沸石分子筛可用于气体、重金属离子的吸附或去除。工业上以粉煤灰(主要
含SiO 和3Al O•2SiO,还含有少量CaO、Fe O 和有机物)为原料制取某种沸石分子筛 (Na Al O •27HO)
2 2 3 2 2 3 12 12 48 2
的过程如下:
粉煤灰— \s\up 0()— \s\up 0()— \s\up 0()滤渣— \s\up 0()— \s\up 0()— \s\up 0()沸石分子筛
→ → → → → →
已知:粉煤灰中的硅、铝化合物煅烧时不发生反应,且难溶于酸。
(1)将粉煤灰在空气中煅烧的目的是__________________________________。
(2)“酸浸”的操作是向“煅烧”后的固体混合物中加入足量的盐酸,充分搅拌后过滤。检验“酸浸”操
作是否达到目的的方法是___________________________________________________________________________
__________________________________________________。
【答案】(1)除去粉煤灰中的有机物 (2)取少量过滤后的固体,加入适量盐酸,充分搅拌后滴加几滴
KSCN溶液,无红色现象则说明“酸浸”操作已达到目的
成功体验
1.(2024·新课标卷)对于下列过程中发生的化学反应,相应离子方程式正确的是
A.试管壁上的银镜用稀硝酸清洗:Ag+2H++NO -=Ag++NO ↑+2HO
3 2 2
B.工业废水中的Pb2+用FeS去除:Pb2++S2-=PbS↓
8
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找C.海水提溴过程中将溴吹入SO 吸收塔:Br +SO +2H=2Br-+SO 2-+4H+
2 2 2 2 4
D.用草酸标准溶液测定高锰酸钾溶液的浓度:2MnO -+5C O2-+16H+=2Mn2++10CO↑+8HO
4 2 4 2 2
【答案】C
【解析】A项,试管壁上的银镜用稀硝酸清洗,银溶于稀硝酸生成硝酸银和一氧化氮气体,该反应的离子
方程式为3Ag+4H++NO -=3Ag++NO↑+2HO,不正确;B项,由于PbS的溶解度远远小于FeS,因此,
3 2
工业废水中的Pb2+用FeS去除,该反应的离子方程式为Pb2++HS=PbS↓+Fe2+,不正确;C项,海水提溴过
2
程中将溴吹入SO 吸收塔,SO 在水溶液中将Br 还原为Br-,该反应的离子方程式为Br +SO +2H=2Br-+
2 2 2 2 2 2
SO 2-+4H+,正确;D项,用草酸标准溶液测定高锰酸钾溶液的浓度,HC O 被氧化为CO,HC O 属于弱酸,
4 2 2 4 2 2 2 4
该反应的离子方程式为2MnO -+5HC O+6H+=2Mn2++10CO↑+8HO,不正确。
4 2 2 4 2 2
2.(2024·贵州卷)下列离子方程式书写错误的是
A.用氢氟酸雕刻玻璃:SiO +4H++4F-=SiF↑+2HO
2 4 2
B.用绿矾(FeSO •7HO)处理酸性废水中的Cr O2-:6Fe2++Cr O2-+14H+=6Fe3++2Cr3++7HO
4 2 2 7 2 7 2
C.用泡沫灭火器灭火的原理:Al3++3HCO -=Al(OH)↓+3CO↑
3 3 2
D.工业电解饱和食盐水制烧碱和氯气:2Cl-+2HO====2OH-+H↑+Cl↑
2 2 2
【答案】A
【解析】A项,氟化氢是弱酸,不能拆写成离子,用氢氟酸雕刻玻璃:SiO +4HF=SiF↑+2HO,错误;
2 4 2
B项,用绿矾(FeSO •7HO)处理酸性废水中的Cr O2-,生成铬离子和铁离子,6Fe2++Cr O2-+14H+=6Fe3+
4 2 2 7 2 7
+2Cr3++7HO,正确;C项,泡沫灭火器灭火的原理,铝离子、碳酸氢根水解反应完全生成氢氧化铝沉淀和二
2
氧化碳:Al3++3HCO -=Al(OH)↓+3CO↑,正确;D项,工业电解饱和食盐水生成烧碱、氯气和氢气:
3 3 2
2Cl-+2HO====2OH-+H↑+Cl↑,正确。
2 2 2
3.(2023·湖南卷)下列有关电极方程式或离子方程式错误的是
A.碱性锌锰电池的正极反应:MnO +HO+e-=MnO(OH)+OH-
2 2
B.铅酸蓄电池充电时的阳极反应:Pb2++2HO-2e-=PbO +4H+
2 2
C.K[Fe(CN)]溶液滴入FeCl 溶液中:K++Fe2++[Fe(CN)]3-=KFe[Fe(CN)]↓
3 6 2 6 6
D.TiCl 加入水中:TiCl +(x+2)HO=TiO·xHO↓+4H++4Cl-
4 4 2 2 2
【答案】B
【解析】A项,碱性锌锰电池放电时正极得到电子生成MnO(OH),电极方程式为MnO +HO+e-=
2 2
MnO(OH)+OH-,正确;B项,铅酸电池在充电时阳极失电子,其电极式为:PbSO -2e-+2HO=PbO +4H
4 2 2
++SO 2-,错误;C项,K[Fe(CN)]用来鉴别Fe2+生成滕氏蓝沉淀,反应的离子方程式为K++Fe2++
4 3 6
[Fe(CN)]3-=KFe[Fe(CN)]↓,正确;D项,TiCl 容易与水反应发生水解,反应的离子方程式为TiCl +(x+
6 6 4 4
2)HO=TiO·xHO↓+4H++4Cl-,正确。
2 2 2
4.(2024·江苏南京市、盐城市一模)实验室以菱锰矿(含MnCO 及少量Fe、Si的氧化物等)为原料制备
3
高纯MnCO 和MnO 的流程如下图所示。
3 3 4
(1)该流程中可循环使用的物质有___________。
(2)“沉铁”过程需加氨水调节溶液pH,使溶液中Fe3+转化为Fe(OH) 沉淀同时得到MnSO 溶液。检验
3 4
MnSO 溶液中是否含有Fe3+的实验方法是____________________________________________________________
4
___________________________________________________________________________。
【答案】(1)NH 或氨水、(NH )SO (2)取少量MnSO 溶液于试管中,向其中滴加KSCN溶液{或
3 4 2 4 4
K[Fe(CN)]溶液},若溶液不变红(或没有蓝色沉淀),则溶液中无Fe3+(其他答案合理也可)
4 6
【解析】(1)根据流程可知,碳酸锰与硫酸铵反应生成硫酸锰、氨气和二氧化碳,氨可用于后续调节溶液
的pH沉铁;加水溶解后,得到含硫酸锰溶液,再加入氨水调节pH除去铁,MnSO 溶液与氨水充分反应,过滤
4
得到硫酸锰溶液,同时得到硫酸铵,可循环使用的物质有NH 或氨水、(NH )SO ;(2)铁离子遇到KSCN变
3 4 2 4
红,则检验MnSO 溶液中是否含有Fe3+的实验方法是:取少量MnSO 溶液于试管中,向其中滴加KSCN溶液
4 4微专题突破2 氧化还原反应 离子反应 问题的态度:问则少;辩则明
{或K[Fe(CN)]溶液},若溶液不变红(或没有蓝色沉淀),则溶液中无Fe3+(其他答案合理也可)。
4 6
5.(2024·连云港上学期调研一)水体中的Cr O2-、HCrO -、SO 2-是高毒性的重金属离子,可用
2 7 4 4
Cr(Ⅵ)表示。处理含Cr(Ⅵ)废水的方法有沉淀法、还原法等。
(2)纳米铁粉还原法:纳米铁粉可将水体中Cr(Ⅵ)还原为Cr3+,再通过调节溶液pH,可使Cr3+转化为
Cr(OH) 沉淀而被除去。
3
①在氮气气氛保护下,向一定量的FeCl 溶液中逐滴加入一定量的NaBH 溶液,可制得纳米铁粉,反应
2 4
的离子方程式为2BH-+Fe2++6HO=Fe↓+2B(OH)↓+7H ↑,已知电负性χ(H)>χ(B),每生成1 mol纳
4 2 3 2
米铁粉,被Fe2+氧化的NaBH 的物质的量为___________。
4
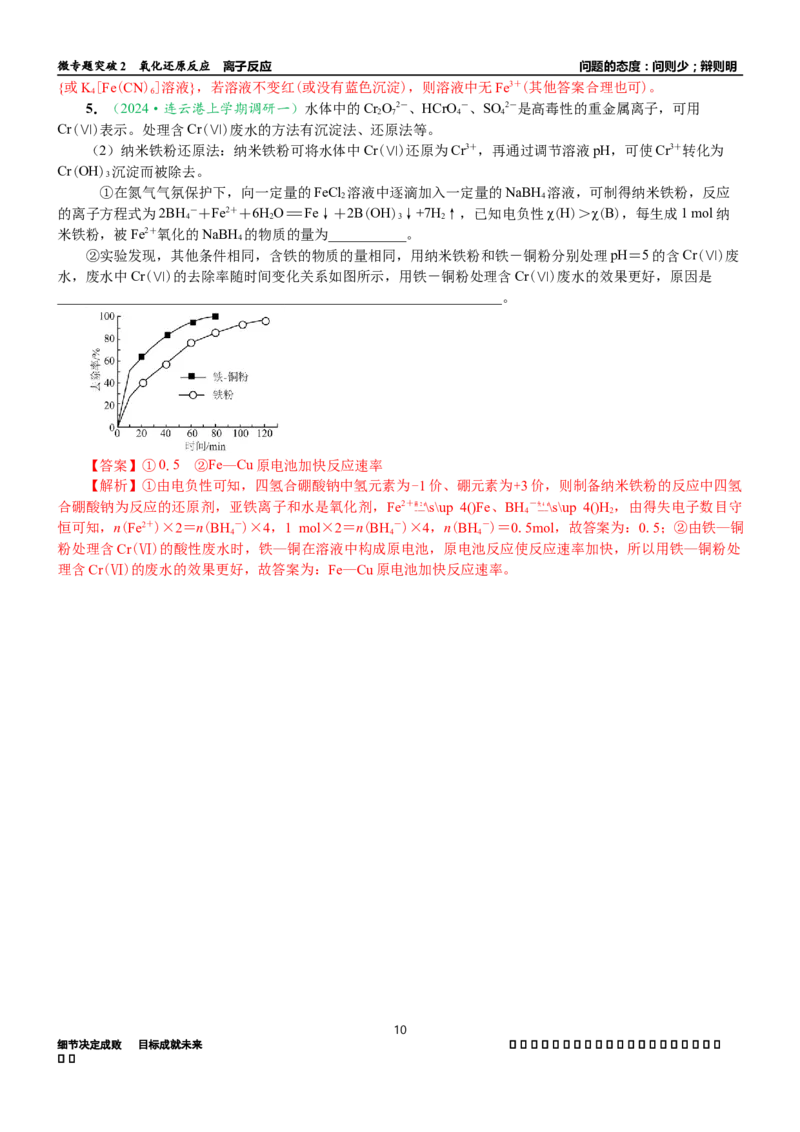
②实验发现,其他条件相同,含铁的物质的量相同,用纳米铁粉和铁-铜粉分别处理pH=5的含Cr(Ⅵ)废
水,废水中Cr(Ⅵ)的去除率随时间变化关系如图所示,用铁-铜粉处理含Cr(Ⅵ)废水的效果更好,原因是
_______________________________________________________________。
【答案】①0.5 ②Fe—Cu原电池加快反应速率
【解析】①由电负性可知,四氢合硼酸钠中氢元素为-1价、硼元素为+3价,则制备纳米铁粉的反应中四氢
合硼酸钠为反应的还原剂,亚铁离子和水是氧化剂,Fe2+得2e\s\up 4()Fe、BH -失4e\s\up 4()H ,由得失电子数目守
-—— 4 -—— 2
恒可知,n(Fe2+)×2=n(BH-)×4,1 mol×2=n(BH-)×4,n(BH-)=0.5mol,故答案为:0.5;②由铁—铜
4 4 4
粉处理含Cr(Ⅵ)的酸性废水时,铁—铜在溶液中构成原电池,原电池反应使反应速率加快,所以用铁—铜粉处
理含Cr(Ⅵ)的废水的效果更好,故答案为:Fe—Cu原电池加快反应速率。
10
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找