文档内容
微专题突破8 化学反应速率与化学平衡二
一、选择题
1.(2024·南通市海门市第一次调研)硝化法制硫酸的主要反应为:NO (g)+SO (g)=SO (g)+
2 2 3
NO(g) ∆H=+41.8 kJ·mol-1。SO 和SO 都是酸性氧化物,是制备硫酸的中间产物。有关反应NO (g)
2 3 2
+SO (g)=SO (g)+NO(g) ∆H=+41.8 kJ·mol-1,下列说法正确的
2 3
A.该反应中反应物的总能量低于生成物的总能量
B.反应达平衡后,分离出少量SO ,正反应速率加快
3
C.其他条件不变,平衡后继续充入NO ,平衡常数将减小
2
D.该反应中消耗22.4 L·mol-1 LNO ,转移电子的数目为2×6.02×1023
2
2.(2024·徐州上学期期中)汽车安装尾气净化装置也可除去NO,反应方程式为2NO (g)+
x 2
4CO(g) N(g)+4CO(g),关于反应2NO (g)+4CO(g) N(g)+4CO(g),下列说法正确的是
2 2 2 2 2
A.该反应的∆S>0
B.选择合适的催化剂,可以使NO 完全转化成N
2 2
C.及时移除N、CO,正反应速率增大,平衡向正反应方向移动
2 2
D.上述反应中每生成0.1 mol N,转移电子的数目约为0.8×6.02×1023
2
3.(2025·江苏苏州市开学考)以Cu-Zn-Al O 作催化剂发生如下反应:2CHCHO(g)+HO(g)
2 3 3 2
C HOH(g)+CHCOOH(g) ∆H<0,下列说法正确的是
2 5 3
A.该反应的∆S>0
B.该反应的平衡常数K=
C.催化剂Cu-Zn-Al O 能降低该反应的活化能
2 3
D.该反应中每消耗1 mol CHCHO,转移电子数约为2×6.02×1023
3
4.(2024·连云港上学期调研一)氨催化氧化的方程式为4NH (g)+5O(g) 4NO(g)+6HO(g)
3 2 2
∆H=-904.8 kJ·mol-1 。下列说法正确的是
A.该反应的∆S<0
B.反应平衡常数K=
C.每消耗1 mol O,反应共转移4 mol电子
2
D.平衡后升高温度,正反应速率堿小、逆反应速率增大
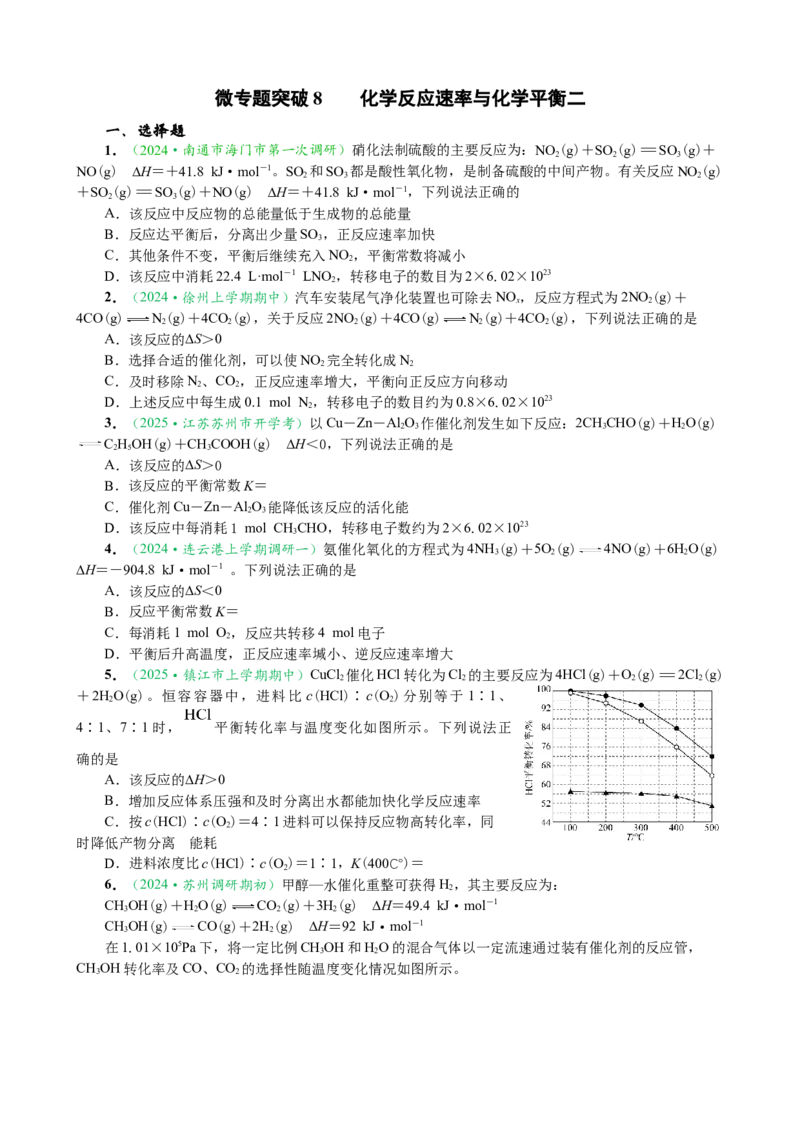
5.(2025·镇江市上学期期中)CuCl 催化HCl转化为Cl 的主要反应为4HCl(g)+O(g)=2Cl(g)
2 2 2 2
+2HO(g)。恒容容器中,进料比 c(HCl)∶c(O)分别等于 1∶1、
2 2
4∶1、7∶1时, 平衡转化率与温度变化如图所示。下列说法正
确的是
A.该反应的∆H>0
B.增加反应体系压强和及时分离出水都能加快化学反应速率
C.按c(HCl)∶c(O)=4∶1进料可以保持反应物高转化率,同
2
时降低产物分离 的能耗
D.进料浓度比c(HCl)∶c(O)=1∶1,K(400℃)=
2
6.(2024·苏州调研期初)甲醇—水催化重整可获得H,其主要反应为:
2
CHOH(g)+HO(g) CO(g)+3H(g) ∆H=49.4 kJ·mol-1
3 2 2 2
CHOH(g) CO(g)+2H(g) ∆H=92 kJ·mol-1
3 2
在1.01×105Pa下,将一定比例CHOH和HO的混合气体以一定流速通过装有催化剂的反应管,
3 2
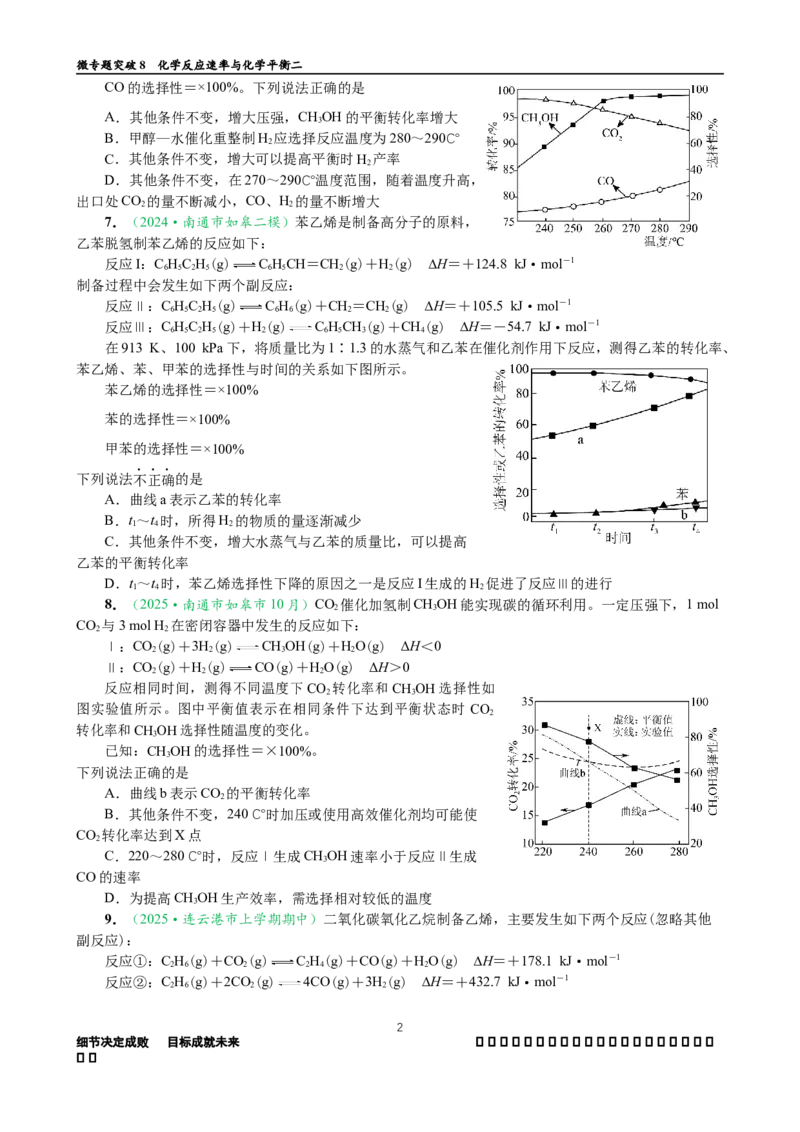
CHOH转化率及CO、CO 的选择性随温度变化情况如图所示。
3 2微专题突破8 化学反应速率与化学平衡二
CO的选择性=×100%。下列说法正确的是
A.其他条件不变,增大压强,CHOH的平衡转化率增大
3
B.甲醇—水催化重整制H 应选择反应温度为280~290℃
2
C.其他条件不变,增大可以提高平衡时H 产率
2
D.其他条件不变,在270~290℃温度范围,随着温度升高,
出口处CO 的量不断减小,CO、H 的量不断增大
2 2
7.(2024·南通市如皋二模)苯乙烯是制备高分子的原料,
乙苯脱氢制苯乙烯的反应如下:
反应I:C HC H(g) C HCH=CH(g)+H(g) ∆H=+124.8 kJ·mol-1
6 5 2 5 6 5 2 2
制备过程中会发生如下两个副反应:
反应Ⅱ:C HC H(g) C H(g)+CH=CH(g) ∆H=+105.5 kJ·mol-1
6 5 2 5 6 6 2 2
反应Ⅲ:C HC H(g)+H(g) C HCH(g)+CH(g) ∆H=-54.7 kJ·mol-1
6 5 2 5 2 6 5 3 4
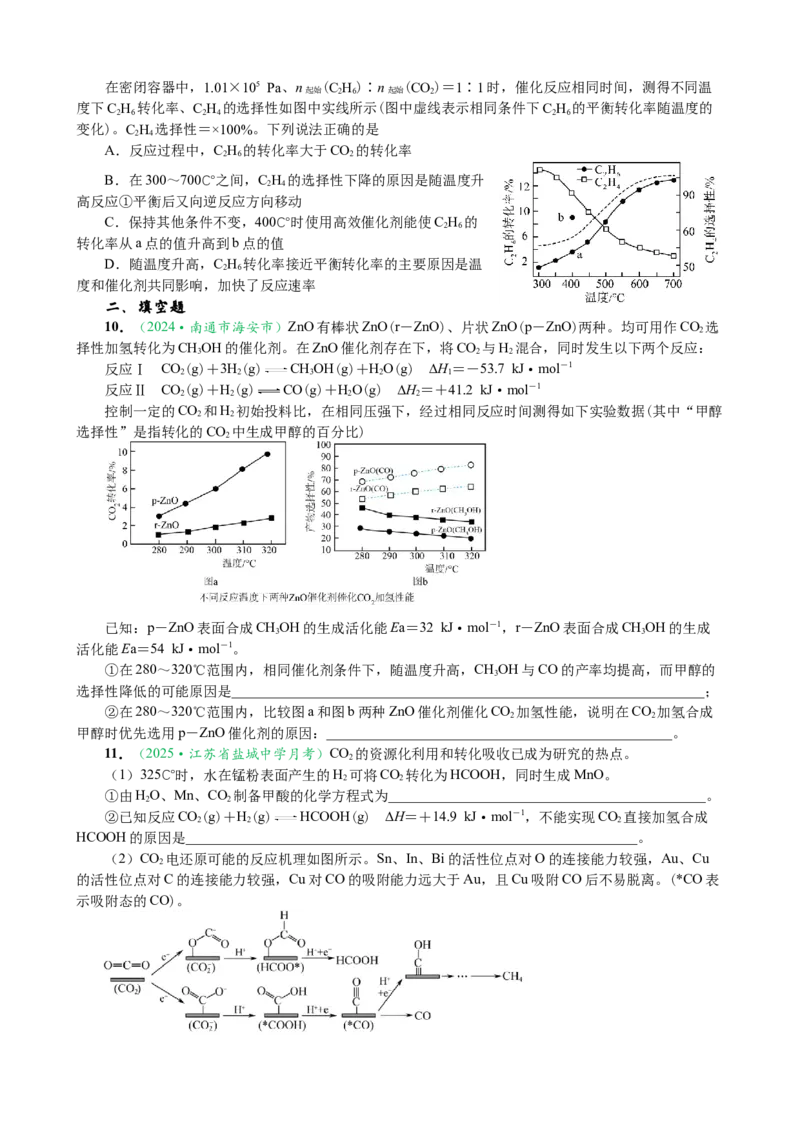
在913 K、100 kPa下,将质量比为1∶1.3的水蒸气和乙苯在催化剂作用下反应,测得乙苯的转化率、
苯乙烯、苯、甲苯的选择性与时间的关系如下图所示。
苯乙烯的选择性=×100%
苯的选择性=×100%
甲苯的选择性=×100%
下列说法不正确的是
A.曲线a表示乙苯的转化率
B.t~t 时,所得H 的物质的量逐渐减少
1 4 2
C.其他条件不变,增大水蒸气与乙苯的质量比,可以提高
乙苯的平衡转化率
D.t~t 时,苯乙烯选择性下降的原因之一是反应I生成的H 促进了反应Ⅲ的进行
1 4 2
8.(2025·南通市如皋市10月)CO 催化加氢制CHOH能实现碳的循环利用。一定压强下,1 mol
2 3
CO 与3 mol H 在密闭容器中发生的反应如下:
2 2
Ⅰ:CO(g)+3H(g) CHOH(g)+HO(g) ΔH<0
2 2 3 2
Ⅱ:CO(g)+H(g) CO(g)+HO(g) ΔH>0
2 2 2
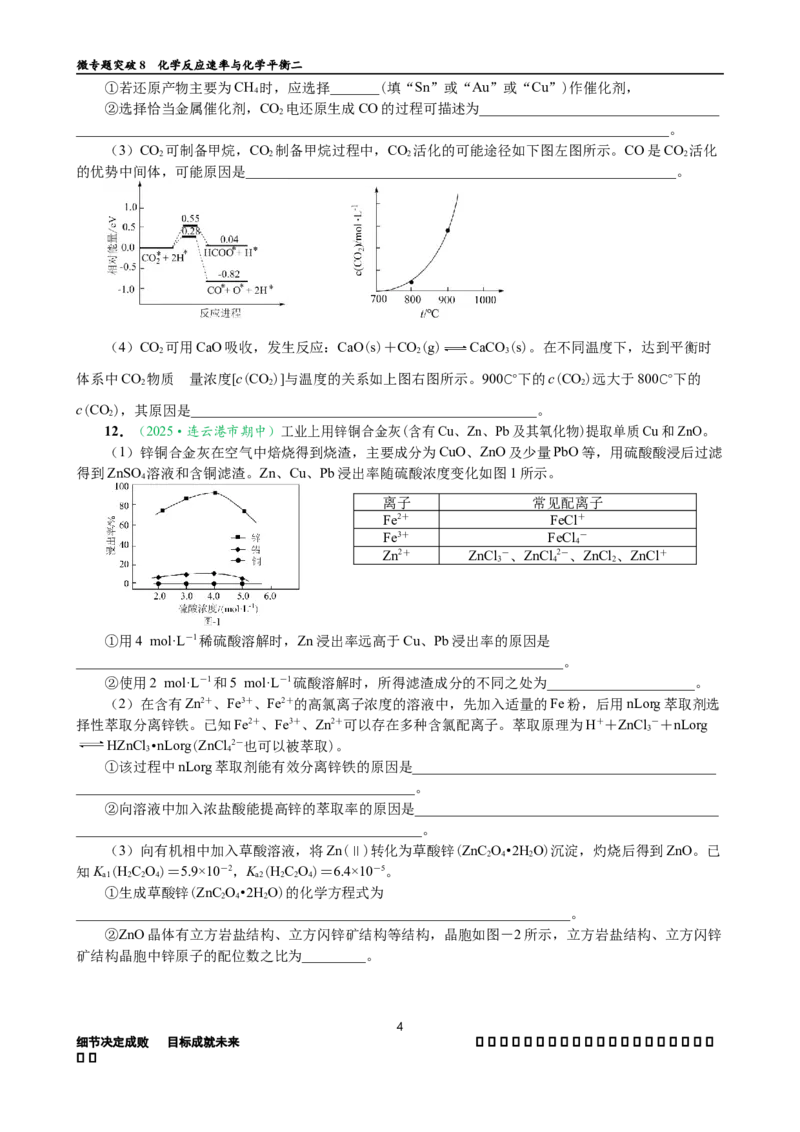
反应相同时间,测得不同温度下 CO 转化率和CHOH选择性如
2 3
图实验值所示。图中平衡值表示在相同条件下达到平衡状态时 CO
2
转化率和CHOH选择性随温度的变化。
3
已知:CHOH的选择性=×100%。
3
下列说法正确的是
A.曲线b表示CO 的平衡转化率
2
B.其他条件不变,240 ℃时加压或使用高效催化剂均可能使
CO 转化率达到X点
2
C.220~280 ℃时,反应Ⅰ生成CHOH速率小于反应Ⅱ生成
3
CO的速率
D.为提高CHOH生产效率,需选择相对较低的温度
3
9.(2025·连云港市上学期期中)二氧化碳氧化乙烷制备乙烯,主要发生如下两个反应(忽略其他
副反应):
反应①:C H(g)+CO(g) C H(g)+CO(g)+HO(g) ∆H=+178.1 kJ·mol-1
2 6 2 2 4 2
反应②:C H(g)+2CO(g) 4CO(g)+3H(g) ∆H=+432.7 kJ·mol-1
2 6 2 2
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找在密闭容器中,1.01×105 Pa、n (C H)∶n (CO)=1∶1时,催化反应相同时间,测得不同温
起始 2 6 起始 2
度下C H 转化率、C H 的选择性如图中实线所示(图中虚线表示相同条件下C H 的平衡转化率随温度的
2 6 2 4 2 6
变化)。C H 选择性=×100%。下列说法正确的是
2 4
A.反应过程中,C H 的转化率大于CO 的转化率
2 6 2
B.在300~700℃之间,C H 的选择性下降的原因是随温度升
2 4
高反应①平衡后又向逆反应方向移动
C.保持其他条件不变,400℃时使用高效催化剂能使C H 的
2 6
转化率从a点的值升高到b点的值
D.随温度升高,C H 转化率接近平衡转化率的主要原因是温
2 6
度和催化剂共同影响,加快了反应速率
二、填空题
10.(2024·南通市海安市)ZnO有棒状ZnO(r-ZnO)、片状ZnO(p-ZnO)两种。均可用作CO 选
2
择性加氢转化为CHOH的催化剂。在ZnO催化剂存在下,将CO 与H 混合,同时发生以下两个反应:
3 2 2
反应Ⅰ CO(g)+3H(g) CHOH(g)+HO(g) ∆H=-53.7 kJ·mol-1
2 2 3 2 1
反应Ⅱ CO(g)+H(g) CO(g)+HO(g) ∆H=+41.2 kJ·mol-1
2 2 2 2
控制一定的CO 和H 初始投料比,在相同压强下,经过相同反应时间测得如下实验数据(其中“甲醇
2 2
选择性”是指转化的CO 中生成甲醇的百分比)
2
已知:p-ZnO表面合成CHOH的生成活化能Ea=32 kJ·mol-1,r-ZnO表面合成CHOH的生成
3 3
活化能Ea=54 kJ·mol-1。
①在280~320℃范围内,相同催化剂条件下,随温度升高,CHOH与CO的产率均提高,而甲醇的
3
选择性降低的可能原因是___________________________________________________________________;
②在280~320℃范围内,比较图a和图b两种ZnO催化剂催化CO 加氢性能,说明在CO 加氢合成
2 2
甲醇时优先选用p-ZnO催化剂的原因:_________________________________________________。
11.(2025·江苏省盐城中学月考)CO 的资源化利用和转化吸收已成为研究的热点。
2
(1)325℃时,水在锰粉表面产生的H 可将CO 转化为HCOOH,同时生成MnO。
2 2
①由HO、Mn、CO 制备甲酸的化学方程式为_____________________________________________。
2 2
②已知反应CO(g)+H(g) HCOOH(g) ∆H=+14.9 kJ·mol-1,不能实现CO 直接加氢合成
2 2 2
HCOOH的原因是________________________________________________________________。
(2)CO 电还原可能的反应机理如图所示。Sn、In、Bi的活性位点对O的连接能力较强,Au、Cu
2
的活性位点对C的连接能力较强,Cu对CO的吸附能力远大于Au,且Cu吸附CO后不易脱离。(*CO表
示吸附态的CO)。微专题突破8 化学反应速率与化学平衡二
①若还原产物主要为CH 时,应选择_______(填“Sn”或“Au”或“Cu”)作催化剂,
4
②选择恰当金属催化剂,CO 电还原生成CO的过程可描述为__________________________________
2
____________________________________________________________________________________。
(3)CO 可制备甲烷,CO 制备甲烷过程中,CO 活化的可能途径如下图左图所示。CO是CO 活化
2 2 2 2
的优势中间体,可能原因是_____________________________________________________________。
(4)CO 可用CaO吸收,发生反应:CaO(s)+CO(g) CaCO(s)。在不同温度下,达到平衡时
2 2 3
的
体系中CO 物质 量浓度[c(CO)]与温度的关系如上图右图所示。900℃下的c(CO)远大于800℃下的
2 2 2
c(CO),其原因是_________________________________________________。
2
12.(2025·连云港市期中)工业上用锌铜合金灰(含有Cu、Zn、Pb及其氧化物)提取单质Cu和ZnO。
(1)锌铜合金灰在空气中焙烧得到烧渣,主要成分为CuO、ZnO及少量PbO等,用硫酸酸浸后过滤
得到ZnSO 溶液和含铜滤渣。Zn、Cu、Pb浸出率随硫酸浓度变化如图1所示。
4
离子 常见配离子
Fe2+ FeCl+
Fe3+ FeCl -
4
Zn2+ ZnCl-、ZnCl2-、ZnCl、ZnCl+
3 4 2
①用4 mol·L-1稀硫酸溶解时,Zn浸出率远高于Cu、Pb浸出率的原因是
_____________________________________________________________________。
②使用2 mol·L-1和5 mol·L-1硫酸溶解时,所得滤渣成分的不同之处为_____________________。
(2)在含有Zn2+、Fe3+、Fe2+的高氯离子浓度的溶液中,先加入适量的Fe粉,后用nLorg萃取剂选
择性萃取分离锌铁。已知Fe2+、Fe3+、Zn2+可以存在多种含氯配离子。萃取原理为H++ZnCl-+nLorg
3
HZnCl •nLorg(ZnCl2-也可以被萃取)。
3 4
①该过程中nLorg萃取剂能有效分离锌铁的原因是___________________________________________
________________________________________________。
②向溶液中加入浓盐酸能提高锌的萃取率的原因是___________________________________________
_________________________________________________。
(3)向有机相中加入草酸溶液,将Zn(Ⅱ)转化为草酸锌(ZnC O•2HO)沉淀,灼烧后得到ZnO。已
2 4 2
知K (HC O)=5.9×10-2,K (HC O)=6.4×10-5。
a1 2 2 4 a2 2 2 4
①生成草酸锌(ZnC O•2HO)的化学方程式为
2 4 2
______________________________________________________________________。
②ZnO晶体有立方岩盐结构、立方闪锌矿结构等结构,晶胞如图-2所示,立方岩盐结构、立方闪锌
矿结构晶胞中锌原子的配位数之比为_________。
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找