文档内容
微专题突破13 化学基础实验考点透视
离开化学实验室,我的心脏就无法跳动。——维勒
目标定位
1.能判断所给装置是否符合实验要求。
2.能判断有关实验操作、结论或相关解释是否正确。
3.能综合运用化学实验原理和方法,设计实验方案解决简单的化学问题,能对实验方案、实验过程和实验
结果进行分析和评价。
【规律点和易错点】
孙猴子七十二般变化,都逃不出你的手心
1.题型特点
以常见气体制取、重要物质(包括有机化合物)的制备装置,实验基本操作(如萃取与分液、沉淀洗涤、
广泛pH试纸使用)、化学反应原理(如化学平衡、原电池、电解)及元素化合物的性质为素材,考查学生对
实验操作的熟悉程度和实验原理的应用能力,关注化学实验操作的真实性。重现率由高到低分别为:物质的分
离与提纯、物质的检验与鉴别、溶液的配制与气体的制备、仪器(包括试纸等用品)的使用与试剂的保存、重
要课本实验操作步骤与相关的细节等。
2.考查意图
虽然每年高考试题所涉及的化学实验基本操作、原理表述、方案设计是不同的,但考查学生“掌握化学实
验的基本方法和技能”的本质不会变,因此要学生加强运用“科学性、简约性、安全性”等原则解决实际化学
实验问题的能力。
3.表格型的实验评价
考情分析:是高考实验题的主流题型,判断结论的正误或其中几方面的一致性、准确性等进行评价。
考查角度:表格型实验评价主要围绕——物质检验、性质的验证、原理的探究、实验操作、现象、结论、
实验仪器和药品的选择等。
考考位位位
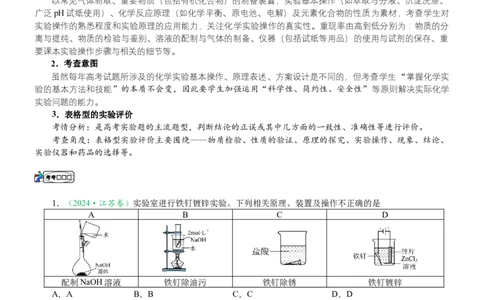
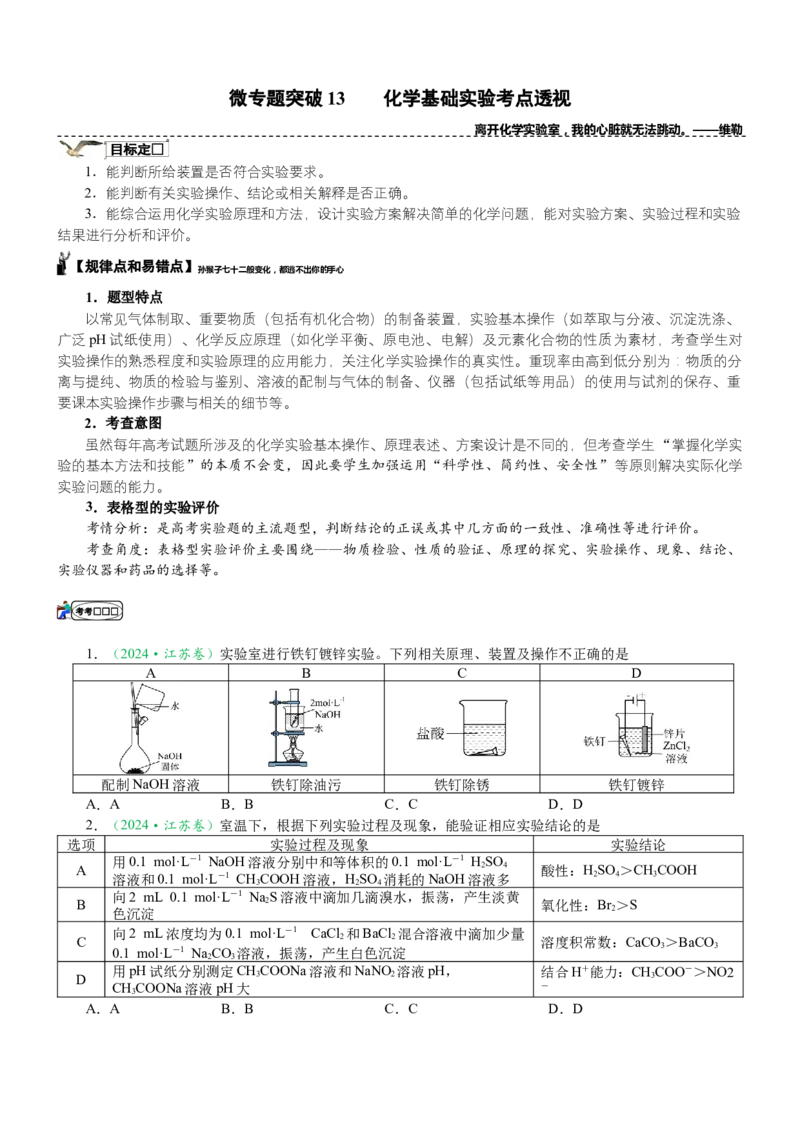
1.(2024·江苏卷)实验室进行铁钉镀锌实验。下列相关原理、装置及操作不正确的是
A B C D
配制NaOH溶液 铁钉除油污 铁钉除锈 铁钉镀锌
A.A B.B C.C D.D
2.(2024·江苏卷)室温下,根据下列实验过程及现象,能验证相应实验结论的是
选项 实验过程及现象 实验结论
用0.1 mol·L-1 NaOH溶液分别中和等体积的0.1 mol·L-1 HSO
A 2 4 酸性:HSO >CHCOOH
溶液和0.1 mol·L-1 CHCOOH溶液,HSO 消耗的NaOH溶液多 2 4 3
3 2 4
向2 mL 0.1 mol·L-1 NaS溶液中滴加几滴溴水,振荡,产生淡黄
B 2 氧化性:Br >S
色沉淀 2
向2 mL浓度均为0.1 mol·L-1 C的aCl 和BaCl 混合溶液中滴加少量
C 2 2 溶度积常数:CaCO>BaCO
0.1 mol·L-1 NaCO 溶液,振荡,产生白色沉淀 3 3
2 3
用pH试纸分别测定CHCOONa溶液和NaNO 溶液pH, 结合H+能力:CHCOO->NO2
D 3 2 3
CHCOONa溶液pH大 -
3
A.A B.B C.C D.D微专题突破13 化学基础实验考点透视 问题的态度:问则少;辩则明
【问题解决1】
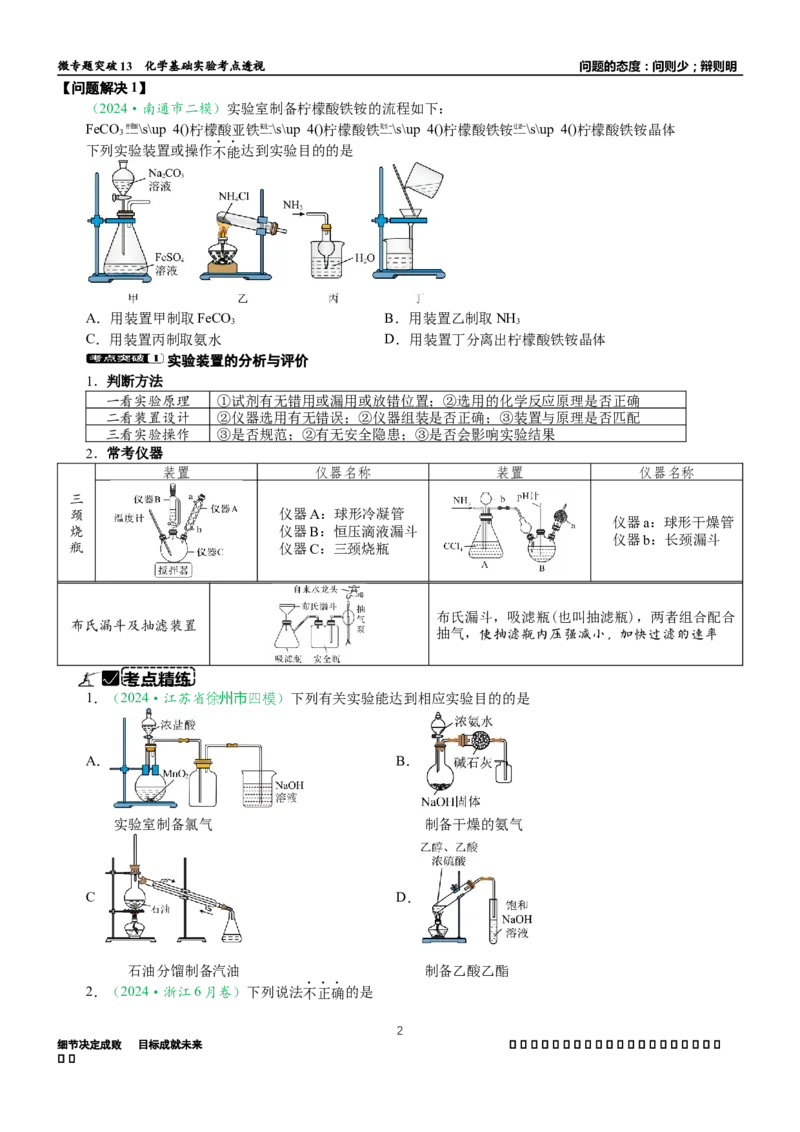
(2024·南通市二模)实验室制备柠檬酸铁铵的流程如下:
FeCO 柠檬酸\s\up 4()柠檬酸亚铁氧化—\s\up 4()柠檬酸铁氨水—\s\up 4()柠檬酸铁铵过滤—\s\up 4()柠檬酸铁铵晶体
3——— ——— ——— ———
下列实验装置或操作不能达到实验目的的是
A.用装置甲制取FeCO B.用装置乙制取NH
3 3
C.用装置丙制取氨水 D.用装置丁分离出柠檬酸铁铵晶体
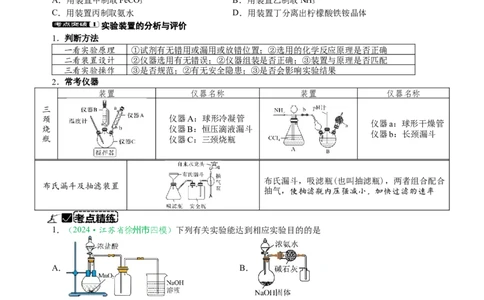
实验装置的分析与评价
1.判断方法
一看实验原理 ①试剂有无错用或漏用或放错位置;②选用的化学反应原理是否正确
二看装置设计 ②仪器选用有无错误;②仪器组装是否正确;③装置与原理是否匹配
三看实验操作 ③是否规范;②有无安全隐患;③是否会影响实验结果
2.常考仪器
装置 仪器名称 装置 仪器名称
三
颈 仪器A:球形冷凝管
仪器a:球形干燥管
烧 仪器B:恒压滴液漏斗
仪器b:长颈漏斗
瓶 仪器C:三颈烧瓶
布氏漏斗,吸滤瓶(也叫抽滤瓶),两者组合配合
布氏漏斗及抽滤装置
抽气,使抽滤瓶内压强减小,加快过滤的速率
考点精练
1.(2024·江苏省徐州市四模)下列有关实验能达到相应实验目的的是
A. B.
实验室制备氯气 制备干燥的氨气
C D.
.
石油分馏制备汽油 制备乙酸乙酯
2.(2024·浙江6月卷)下列说法不正确的是
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
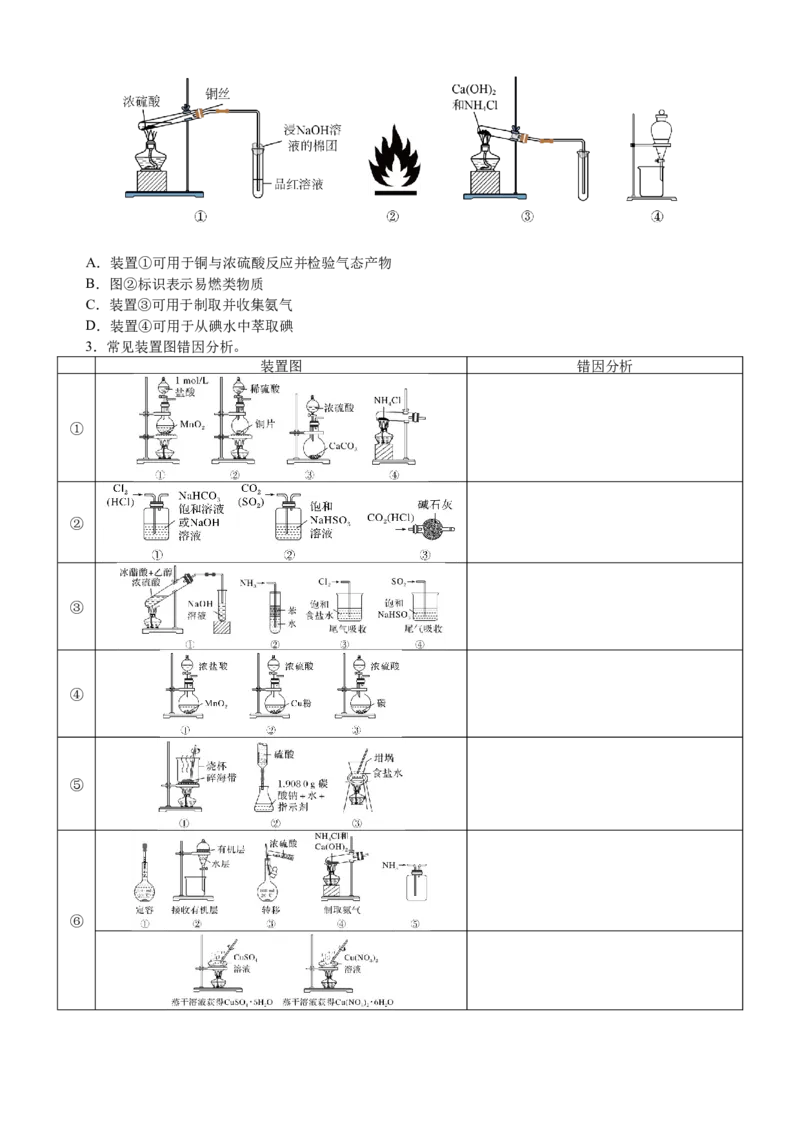
找找A.装置①可用于铜与浓硫酸反应并检验气态产物
B.图②标识表示易燃类物质
C.装置③可用于制取并收集氨气
D.装置④可用于从碘水中萃取碘
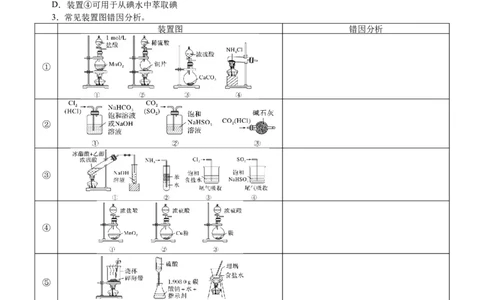
3.常见装置图错因分析。
装置图 错因分析
①
②
③
④
⑤
⑥微专题突破13 化学基础实验考点透视 问题的态度:问则少;辩则明
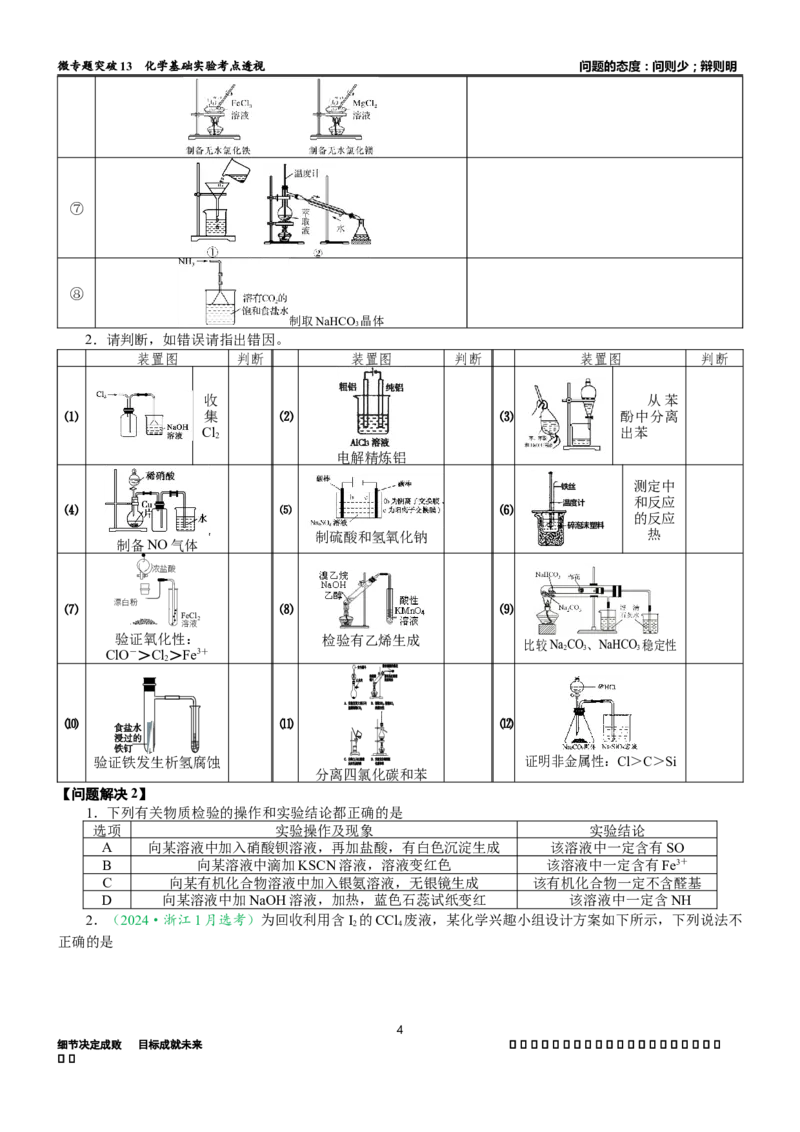
⑦
⑧
制取NaHCO 晶体
3
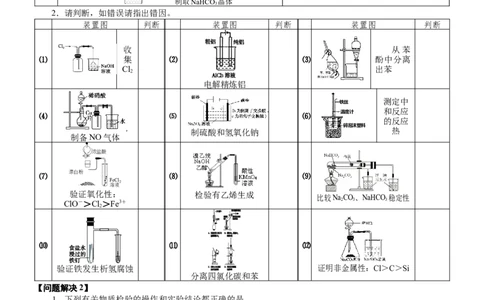
2.请判断,如错误请指出错因。
装置图 判断 装置图 判断 装置图 判断
收 从苯
⑴ 集 ⑵ ⑶ 酚中分离
Cl 出苯
2
电解精炼铝
测定中
铁丝
和反应
⑷ ⑸ ⑹ 温度计
的反应
碎泡沫塑料
制硫酸和氢氧化钠 热
制备NO气体
浓盐酸
⑺ 漂白粉 ⑻ ⑼
FeCl2
溶液
验证氧化性: 检验有乙烯生成
比较NaCO、NaHCO 稳定性
ClO->Cl>Fe3+ 2 3 3
2
⑽ ⑾ ⑿
验证铁发生析氢腐蚀 证明非金属性:Cl>C>Si
分离四氯化碳和苯
【问题解决2】
1.下列有关物质检验的操作和实验结论都正确的是
选项 实验操作及现象 实验结论
A 向某溶液中加入硝酸钡溶液,再加盐酸,有白色沉淀生成 该溶液中一定含有SO
B 向某溶液中滴加KSCN溶液,溶液变红色 该溶液中一定含有Fe3+
C 向某有机化合物溶液中加入银氨溶液,无银镜生成 该有机化合物一定不含醛基
D 向某溶液中加NaOH溶液,加热,蓝色石蕊试纸变红 该溶液中一定含NH
2.(2024·浙江1月选考)为回收利用含I 的CCl 废液,某化学兴趣小组设计方案如下所示,下列说法不
2 4
正确的是
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找A.步骤Ⅰ中,加入足量NaCO 溶液充分反应后,上下两层均为无色
2 3
B.步骤Ⅰ中,分液时从分液漏斗下口放出溶液A
C.试剂X可用硫酸
D.粗I 可用升华法进一步提纯
2
离子、官能团检验与物质分离提纯
1.离子、官能团检验
SO 2 须用________酸化 须________ 须用________________
4 NH K+
-
水解液须用_____酸化 水解液须用__________ 先 加 _________ , 再 加
—X 糖水解产物 Fe2+
______
Fe2+、Cl-共存,检Fe2+ 不能用KMnO 溶液,须用K[Fe(CN)]溶液
4 3 6
碳碳双键、醛基共存,检醛基 不能用溴水,须用溴的四氯化碳溶液
2.分离提纯
(1)试剂的选择:不和被提纯物质反应;除杂试剂稍过量,最后多余的除杂试剂须除去。
(2)分离操作
实验操作 设问 答题指导 常考归纳
蒸发浓缩与结晶是盐溶液分离的常用手段 减压蒸发的目的:降低蒸发温
蒸发
蒸发浓缩至有晶膜出现,停止加热 度,可防止所制备的物质分解
趁热过滤的目的:保持过滤温
一般“沉淀”或结晶之后的分离方法是
过滤 度,防止温度降低后某些溶质析
“过滤”
出
一般
一般“萃取”之后的分离方法是“分
操作
分液 液”;先将下层液体从分液漏斗下口放 分离互不相溶的两种液体
出,再将上层液体从分液漏斗上口倒出
蒸馏时,注意所制备物质的沸
一般“分液”之后的分离方法是干燥、蒸
蒸馏 点,以确定收集何种温度下的馏
馏
分
回流冷凝 目的:减少易挥发物质的损失 提高反应物的转化率
常见离子检验:
①检验SO:先加稀盐酸酸化,
方法:静置,在上层清液中再加入原沉淀
证明沉淀 后加氯化钡溶液;
试剂,当不再产生沉淀时,说明已经沉淀
是否完全 ②检验Cl-:先加稀硝酸酸化,
完全
后加硝酸银溶液;
③检验Fe3+:加硫氰化钾溶液
消除其他试剂、实验操作等因素
空白实验 目的:对比实验,做对照
实验 引起的误差
技巧 ①向过滤器中加入洗涤液至完全
沉淀物(或晶体)的洗涤:
浸没沉淀(或晶体),待洗涤液自
①对于易溶于水的晶体,可以用其饱
然流下后,重复洗涤2~3次;
晶体洗涤 和溶液洗涤;
②用乙醇洗涤无机盐晶体的原
②对于可溶于水的晶体,可以用乙醇
因:减少晶体溶解损失,同时乙
等有机溶剂洗涤
醇易挥发,利于产品快速干燥
方法:取少许最后一次洗涤滤液于一支洁
证明晶体 证明晶体洗涤干净的实质:检验
净的试管中,加入某种特定沉淀试剂,若
是否洗涤干净 特定离子
不再产生沉淀,则证明已经洗涤干净
考点精练
1.下表中的实验操作能达到实验目的或得出相应结论的是_____________
选项 实验目的或结论 实验操作
① 除去FeCl 溶液中混有的FeCl 加入过量铁粉,过滤
2 3微专题突破13 化学基础实验考点透视 问题的态度:问则少;辩则明
② 检验溶液中一定有I- 向某溶液中滴加氯水和四氯化碳,振荡、静置,下层溶液呈紫色
取少量 Fe(NO ) 试样加水溶解,加稀硫酸酸化,滴加 KSCN 溶
③ 检验Fe(NO ) 试样已经变质 3 2
3 2 液,溶液变为血红色
④ 溶液中一定含有Na+,无K+ 用洁净的Pt丝蘸取某溶液进行焰色反应,火焰呈黄色
⑤ 检验氯化亚铁溶液中的Fe2+ 向氯化亚铁溶液中滴加酸性高锰酸钾溶液
将少量某物质滴加到新制的氢氧化铜悬浊液中,加热后有红色沉淀
⑥ 证明某物质一定是醛
生成
向淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入新制的
⑦ 验证淀粉已水解
氢氧化铜悬浊液并加热
⑧ 除去CuCl 溶液中少量FeCl 向溶液中加入足量Cu(OH) 粉末,搅拌一段时间后过滤
2 3 2
⑨ 得到较纯净的乙酸乙酯 向混有乙酸和乙醇的乙酸乙酯的混合物中,加入浓硫酸
⑩ 除去苯中的溴 加苯酚过滤
2.有关离子检验的实验设计
实验操作及现象 实验结论 判断正误 解释
①用铂丝蘸取某溶液进行焰色试 一定是钠盐溶液,
验,火焰呈黄色 该溶液中一定不含K+
②向溶液X中滴加NaOH稀溶液,
将湿润的红色石蕊试纸置于试管 溶液X中一定不含NH
口,试纸不变蓝
③向溶液 Y 中滴加硝酸,再滴加
溶液Y中一定含有SO
BaCl 溶液,有白色沉淀生成
2
④向溶液Z中滴加KSCN溶液,溶
溶液Z中一定含有Fe2+
液不变色,滴加氯水后溶液显红色
3.(2024·广东卷)提纯2.0 g苯甲酸粗品(含少量NaCl和泥沙)的过程如下。其中,操作X为
A.加热蒸馏 B.加水稀释
C.冷却结晶 D.萃取分液
【问题解决3】
下列实验操作及现象与预期实验目的或实验结论不一致的是____________
选项 实验操作 实验目的或结论
① 向盐酸中滴加水玻璃,用激光笔照射,有丁达尔现象 说明有硅酸胶体生成
② 向饱和FeCl 溶液中滴加过量氨水 制取Fe(OH) 胶体
3 3
取酸雨试样,加入10% HO 溶液,再加入BaCl 溶液,有白色
③ 2 2 2 该酸雨试样中一定含有HSO
沉淀 2 3
将打磨过的Al片投到一定浓度的CuCl 溶液,出现气泡并有固 Al 与 CuCl 溶液反应,生成了 H
④ 2 2 2
体生成,过滤,向固体中加入过量的氨水,固体部分溶解 和Cu(OH)
2
⑤ 向包有NaO 的脱脂棉滴少量水,脱脂棉燃烧 NaO 与HO反应放热并有O 生成
2 2 2 2 2 2
⑥ 在新制的氯水中加入碳酸钙粉末,充分搅拌后,过滤 提高氯水中HClO的浓度
配制SnCl 溶液时,先将SnCl 溶于适量稀盐酸,再用蒸馏水稀 抑制Sn2+水解,并防止Sn2+被氧
⑦ 2 2
释,最后在试剂瓶中加入少量的锡粒 化为Sn4+
证明升高温度能促进 CHCOONa
⑧ 向CHCOONa溶液中滴入酚酞溶液,加热 3
3 水解
将铁粉放入稀HNO 中充分反应后,滴入KSCN溶液无明显现
⑨ 3 稀HNO 不能将Fe氧化成Fe3+
象 3
⑩ 将SO 气通入水中,测定其水溶液的导电性 判断SO 是否是电解质
2 2
测定物质的量浓度相等的磷酸、硫酸溶液的pH 比较磷、硫的非金属性强弱
微型实验方案设计与评价
操作、现象与结论一致性判断表格类实验题解题程序
① 原理 如用酸比较元素非金属性,酸须是最高价含氧酸
② 浓度 设陷点:应在同浓度条件下进行比较。如物质的酸性比较:
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找①酸性强弱比较:可通过强酸制弱酸、测定同浓度溶液导电能力或pH等方法来比较
②弱酸酸式盐的电离程度与水解程度比较:可通过测定同浓度溶液的酸碱性的方法来比
较
③ 用量 是少量还是多量
④ 关系 前后的关系是否一致
考点精练
1.(2024·扬州市高三下学期开学考)室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
选项 实验操作和现象 结论
向20%蔗糖溶液中加入少量稀HSO ,加热;再加入银氨溶液,无
A 2 4 蔗糖未发生水解反应
明显现象
B 向淀粉-KI溶液中滴加氯水,溶液变蓝色 氯水中含有HClO
用pH试纸测得:0.1 mol·L-1 CHCOOH溶液与0.1 mol·L-1 HCN
C 3 K(CHCOOH)>K(HCN)
溶液的pH分别为3、5 a 3 a
取少量待检验溶液,向其中加入少量双氧水,再滴加几滴KSCN溶
D 待检验溶液中含有Fe2+
液,溶液变为红色
A.A B.B C.C D.D
2.探究电解质强弱
探究方案 探究目的 判断正误 解释
①室温下,用pH计测量醋酸溶液、盐酸的
CHCOOH是弱电解质
pH,比较溶液pH大小 3
②室温下,用pH试纸测得:CHCOONa溶 HNO 电离出H+的能力比
3 2
液的pH约为9,NaNO 溶液的pH约为8 CHCOOH强
2 3
③室温下,用pH计测量浓度均为0.1 mol·L
比较酸性:醋酸>碳酸
-1醋酸钠溶液、碳酸钠溶液的pH
特别提醒 应该比较同温度、同浓度、同类型的电解质
3.通过实验现象判断酸性强弱
实验操作及现象 实验结论 判断正误 解释
①向NaCO 溶液中加入冰醋酸,将产生的 酸性:
2 3
气体直接通入苯酚钠溶液中,溶液变浑浊 醋酸>碳酸>苯酚
②分别向盛有0.1 mol·L-1醋酸和饱和硼酸
酸性:醋酸>
溶液的试管中滴加等浓度NaCO 溶液,前
2 3 碳酸>硼酸
者产生无色气泡,后者无明显现象
③向石灰石中加入醋酸,将产生的气体直 酸性:醋酸>
接通入硅酸钠溶液中,溶液变浑浊 碳酸>硅酸
特别提醒 挥发性酸(盐酸、硝酸、醋酸等)会干扰酸性强弱的比较
4.溶度积常数[K 的大小比较]
sp
实验操作及现象 实验结论 判断 解释
①在硫酸钡沉淀中加入浓碳酸钠溶液,充分搅 K (BaCO )<
sp 3
拌后,取沉淀(洗净)放入盐酸中,有气泡产生 K (BaSO)
sp 4
②向0.1 mol·L-1 MgSO 溶液滴入NaOH溶液
4 K [Cu(OH)]<
至不再有沉淀产生,再滴加0.1 mol·L-1 CuSO sp 2
4 K [Mg(OH)]
溶液,先有白色沉淀生成后变为浅蓝色沉淀 sp 2
③向10 mL 0.2 mol·L-1 NaOH溶液中滴入2滴
0.1 mol·L-1 MgCl 溶液,产生白色沉淀后,再 K [Mg(OH)]
2 sp 2
滴加2滴0.1 mol·L-1 FeCl 溶液,有红褐色沉 >K [Fe(OH) ]
3 sp 3
淀生成
④室温下,向浓度均为0.1 mol·L-1的BaCl 和
2 K (BaSO)<
CaCl 混合溶液中滴加NaSO 溶液,出现白色 sp 4
2 2 4 K (CaSO)
沉淀 sp 4
⑤在2 mL 0.1 mol·L-1 Na S溶液中先滴入几滴
2 K (CuS)<
0.1 mol·L-1 ZnSO 溶液,有白色沉淀生成,再 sp
4 K (ZnS)
滴入0.1 mol·L-1 CuSO 溶液有黑色沉淀生成 sp
4
①要看清楚沉淀是直接生成的,还是由其他沉淀转化而来的,若是直接生成的,则无法
特别提醒 比较K 的大小;②生成沉淀的颜色要不同,否则无法比较 K 的大小;③若往沉淀中加入浓
sp sp
溶液或饱和溶液,则无法比较K 的大小。
sp微专题突破13 化学基础实验考点透视 问题的态度:问则少;辩则明
5.探究氧化性、还原性强弱
实验操作及现象 实验结论 判断正误 解释
①将Fe(NO ) 样品溶于稀硫酸,滴加 Fe(NO ) 晶体
3 2 3 2
KSCN溶液,溶液变红 已氧化变质
②向盛有Fe(NO ) 溶液的试管中加入
3 2 溶液中NO
0.1 mol·L-1 HSO 溶液,试管口出现
2 4 被Fe2+还原为NO
红棕色气体 2
③向FeCl 溶液中滴加氯水,溶液颜 说明氯水中
2
色变成棕黄色 含有HClO
④将硫酸酸化的HO 滴入Fe(NO )
2 2 3 2 氧化性:HO>Fe3+
溶液中,溶液变黄色 2 2
⑤向0.1 mol·L-1 HO 溶液中滴加
2 2 HO 具有氧化性
0.1 mol·L-1 KMnO 溶液,溶液褪色 2 2
4
⑥向某黄色溶液中加入淀粉碘化钾溶
溶液中含Br
液,溶液呈蓝色 2
⑦将SO 气体通入Ba(NO ) 溶液中,
2 3 2 此沉淀是BaSO
生成白色沉淀 3
⑧将 SO 、SO 气体通入 BaCl 溶液 此沉淀是BaSO、
3 2 2 3
中,生成白色沉淀 BaSO
4
①向含有NO的盐溶液中加入酸后,会有强氧化性
②溶液中含有多种氧化剂时,无法判断具体是哪种氧化剂起作用
特别提醒
③一般稀硝酸的还原产物为NO,但容器口会看到红棕色气体
④过氧化氢与强氧化剂(如KMnO 溶液)反应时,过氧化氢作还原剂
4
6.有关SO 的漂白性、还原性和酸性氧化物性质的判断
2
实验操作及现象 实验结论 判断正误 解释
①将某气体通入品红溶液中,品红溶液褪色 该气体一定是SO
2
②将SO 通入溴水(或碘水或酸性高锰酸钾
2 SO 有漂白性
溶液)中,溶液褪色 2
③将SO 通入滴有酚酞的NaOH溶液中,溶
2 SO 具有漂白性
液红色褪去 2
④将SO 通入紫色石蕊试液中,溶液先变红 SO 具有酸性和漂
2 2
后褪色 白性
①在反应中,若SO 作还原剂,则体现还原性;②SO 与碱(或水)反应,体现酸性氧化物的
2 2
特别提醒 性质;③在反应中,若SO 没有体现还原性和酸性氧化物的性质,但能使溶液(如品红溶液)褪
2
色,则体现漂白性;④SO 能使紫色石蕊试液变红,但不能使其褪色。
2
7.蛋白质的盐析和变性
实验操作及现象 实验结论 判断正误 解释
①向蛋白质溶液中分别滴加饱和NaCl溶
蛋白质均发生变性
液和饱和CuSO 溶液,均有固体析出
4
②向鸡蛋清溶液中分别加入饱和硫酸
蛋白质均发生盐析
铵、硫酸钾溶液,均有固体析出
③向鸡蛋清溶液中加入几滴醋酸铅溶
蛋白质发生盐析
液,产生白色沉淀
盐析——NaCl、NaSO 、KSO 、NH Cl、(NH )SO 等溶液
特别提醒 2 4 2 4 4 4 2 4
变性——CuSO 溶液、醋酸铅溶液、HgCl 溶液、福尔马林溶液等
4 2
8.物质制备、产物证明
实验操作及现象 实验结论 判断正误
①向无水乙醇中加入浓硫酸,加热至170 ℃,将产生的气体通入
说明生成乙烯气体
酸性KMnO 溶液,红色褪去
4
②将铜丝灼烧至表面变黑,伸入盛有某有机物的试管中,铜丝恢说明该有机物中含有醇羟基或
复亮红色 羧基
③向FeCl 溶液中滴加氯水,溶液颜色变成棕黄色 说明氯水中含有HClO
2
8
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找④向某黄色溶液中加入淀粉碘化钾溶液,溶液呈蓝色 说明溶液中含Br
2
⑤将SO 、SO 气体通入BaCl 溶液中,生成白色沉淀 此沉淀是BaSO、BaSO
3 2 2 3 4
⑥将某气体通入品红溶液中,品红溶液褪色 该气体一定是SO
2
⑦将红热的木炭加入浓硝酸中,产生红棕色气体 说明碳与浓HNO 反应生成NO
3 2
⑧向补铁口服液中滴加几滴酸性KMnO 溶液,紫色褪去 说明补铁口服液中有Fe2+
4
⑨蘸有浓氨水的玻璃棒靠近溶液X,有白烟产生 溶液X一定是浓盐酸
⑩将某铁的氧化物用稀盐酸溶解,再滴入 2滴酸性KMnO 溶
4 证明该氧化物中一定含有Fe2+
液,溶液褪色
9.物质性质
实验操作及现象 实验结论 判断正误
①向溶有SO 的BaCl 溶液中加入Fe(NO ) 溶液,有白色沉淀生成 说明NO -具有强氧化性
2 2 3 3 3
②向FeBr 溶液中加入足量HO,生成大量气泡 该过程中FeBr 作催化剂
3 2 2 3
③用玻璃棒蘸取浓硫酸滴在纸上,纸变黑 浓硫酸具有脱水性
④向2 mL 1 mol·L-1硼酸溶液中加入1 mL 1 mol·L-1碳酸钠溶液,
硼酸与碳酸钠没有反应
溶液无明显变化
10.反应原理
实验操作及现象 实验结论 判断正误
①取 5 mL 0.1 mol·L-1 KI 溶液于试管中,加入 1 mL 0.1
mol·L-1 FeCl 溶液,充分反应滴入5滴15% KSCN溶液, KI与FeCl 的反应有一定限度
3 3
溶液变红色
②向两支盛有KI 溶液的试管中分别滴加淀粉溶液和 AgNO KI 溶液中存平衡:I - I-+
3 3 3 3
溶液,前者溶液变蓝、后者有黄色沉淀生成 I
2
HCO -的水解程度大于电离程
③常温下,测量NaHCO 溶液的pH,pH>7 3
3 度
④将25℃ 0.1 mol·L-1 Na SO 溶液加热到40℃,用传感器测 确定NaSO 的水解平衡逆向移
2 3 2 3
定溶液pH的变化,发现温度升高,溶液的pH逐渐减小 动
【问题解决4】
(2024·南京市二模)室温下,探究0.1 mol·L-1 NH Fe(SO ) 溶液的性质。下列实验方案能达到探究目的
4 4 2
的是
选项 探究目的 实验方案
向2 mL NH Fe(SO ) 溶液中滴加几滴0.1 mol·L-1 NaOH溶液,将湿润
4 4 2
A 验证溶液中含有NH
的红色石蕊试纸靠近试管口,观察试纸颜色变化
向2 mL NH Fe(SO ) 溶液中滴加几滴新制氯水,再滴加KSCN溶液,观
B 溶液中是否含有Fe2+ 4 4 2
察溶液的颜色变化
用玻璃棒蘸取2 mL NH Fe(SO ) 溶液滴在干燥的广泛pH试纸上,将试纸
C NH是否发生水解 4 4 2
显色的颜色与标准比色卡比较
向2 mL NH Fe(SO ) 溶液中滴加几滴0.1 mol·L-1 KI溶液,再滴加淀粉
D Fe3+是否具有氧化性 4 4 2
溶液,观察溶液颜色变化
A.A B.B C.C D.D
物质性质的探究
一、题干给出物质的性质如溶液的pH、化学性质等,判断选项说法是否正确。
二、指定性质,判断设计的实验是否正确。
考点精练
1.(2024·苏锡常镇一模)探究NaClO溶液的性质,下列实验方案能达到探究目的的是
选项 探究目的 实验方案
用洁净的铂丝蘸取少量NaClO溶液,在酒精灯上灼烧,透过蓝色
A 检验NaClO溶液中的Na+
钴玻璃观察火焰颜色微专题突破13 化学基础实验考点透视 问题的态度:问则少;辩则明
B 检验NaClO溶液的氧化性 将NaClO溶液滴加到淀粉KI溶液中,观察溶液颜色变化
用洁净的玻璃棒蘸取NaClO溶液滴在pH试纸上,待变色后与标
C 检验NaClO溶液的pH
准比色卡比对
将少量NaClO溶液与FeCl 充分反应后,滴加硝酸酸化的硝酸银
D 检验NaClO溶液的还原产物 2
溶液,观察沉淀产生情况
A.A B.B C.C D.D
2.(2023·江苏南通一模)室温下,取四根打磨后形状大小相同的镁条,通过下列实验探究镁在溶液中的
反应。
实验1 将镁条放入滴有酚酞的蒸馏水中,无明显现象,加热溶液,镁条表面产生气泡,溶液逐渐变红
实验2 将镁条放入滴有酚酞的1 mol·L-1 NH Cl溶液中,产生气泡,溶液逐渐变红
4
实验3 将镁条放入滴有酚酞的1 mol·L-1 CHCOONH 溶液(pH≈7),产生气泡,溶液逐渐变红
3 4
实验4 将镁条放入滴有酚酞的1 mol·L-1 NaCl溶液中,产生气泡,溶液逐渐变红
下列基于相应实验现象得出的结论不正确的是
A.实验1加热时发生反应的化学方程式为Mg+2HO====Mg(OH)+H↑
2 2 2
B.实验2反应后的溶液中存在:c(Cl-)<2c(Mg2+)+c(NH)
C.实验3产生的气体中可能含NH
3
D.实验1和实验4表明Cl-对Mg与HO反应有催化作用
2
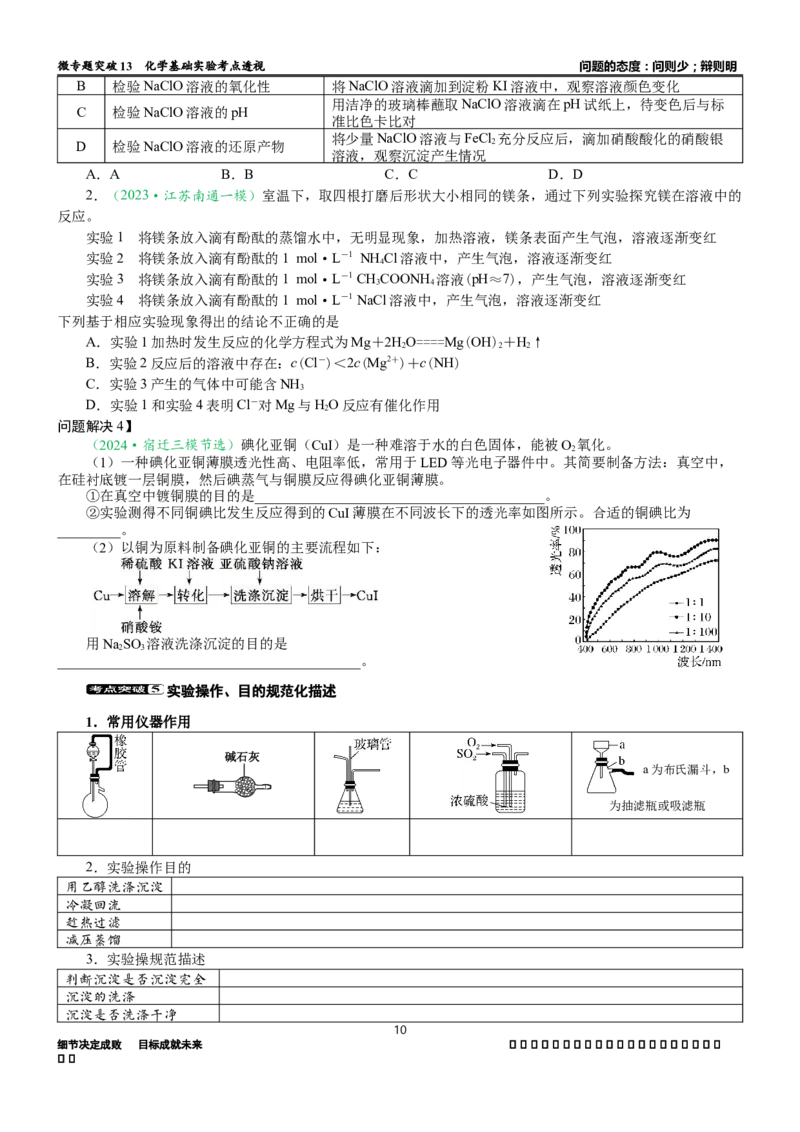
问题解决4】
(2024·宿迁三模节选)碘化亚铜(CuI)是一种难溶于水的白色固体,能被O 氧化。
2
(1)一种碘化亚铜薄膜透光性高、电阻率低,常用于LED等光电子器件中。其简要制备方法:真空中,
在硅衬底镀一层铜膜,然后碘蒸气与铜膜反应得碘化亚铜薄膜。
①在真空中镀铜膜的目的是_________________________________________。
②实验测得不同铜碘比发生反应得到的CuI薄膜在不同波长下的透光率如图所示。合适的铜碘比为
_________。
(2)以铜为原料制备碘化亚铜的主要流程如下:
用NaSO 溶液洗涤沉淀的目的是
2 3
___________________________________________。
实验操作、目的规范化描述
1.常用仪器作用
a为布氏漏斗,b
为抽滤瓶或吸滤瓶
2.实验操作目的
用乙醇洗涤沉淀
冷凝回流
趁热过滤
减压蒸馏
3.实验操规范描述
判断沉淀是否沉淀完全
沉淀的洗涤
沉淀是否洗涤干净
10
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找离子检验
考点精练
(2024·南京期末节选)实验室以菱锰矿(含MnCO 及少量Fe、Si的氧化物等)为原料制备高纯MnCO
3 3
和MnO 的流程如图所示。
3 4
(1)该流程中可循环使用的物质有________________________________。
(2)“沉铁”过程需加氨水调节溶液pH,使溶液中Fe3+ 转化为Fe(OH) 沉淀,同时得到MnSO 溶液。检
3 4
验MnSO 溶液中是否含有Fe3+的实验方法是________________________________________________________
4
____________________________________________________________________________________。
(3)制取MnCO 。在如图所示的实验装置中,搅拌下使一定量的MnSO 溶液与氨水-
3 4
NH HCO 混合溶液充分反应。
4 3
①滴液漏斗中添加的试剂是____________________________________。
②混合溶液中氨水的作用是
____________________________________________________________。
成功体验
1.(2024·南通市如皋2月)氨用于生产硝酸、铵盐、纯碱、配合物等,液氮可以和金属钠反应产生
H。实验室利用下列装置进行氨气或氨水的有关实验,能够达到实验目的的是
2
A.制取NH B.干燥NH
3 3
C.收集NH D.制[Cu(NH )](OH) 溶液
3 3 4 2
2.(2024·泰州市期中)某化学兴趣小组拟探究碳与浓HSO 反应,并检验气体产物。下列说法正确的是
2 4
A.用装置甲进行碳与浓HSO 反应
2 4
B.将检验过CO 后的气体再通入装置丁中检验产物HO
2 2
C.将反应产生的气体通入装置丙,可直接检验产物SO
2
D.将反应产生的气体通入装置乙,可直接检验产物CO
2
3.(2025·江苏苏州市开学考)下列实验探究方案能达到探究目的的是
选项 探究方案 探究目的
向淀粉溶液中加适量20% H SO 溶液,加热,冷却后加新制Cu(OH) 悬浊
A 2 4 2 淀粉发生水解
液,加热,观察溶液变化微专题突破13 化学基础实验考点透视 问题的态度:问则少;辩则明
B 向NaCl、NaI的混合稀溶液中滴入少量稀AgNO 溶液,观察产生沉淀颜色 K (AgCl)>K (AgI)
3 sp sp
C 用pH计测定等浓度盐酸和HI溶液的pH Cl的非金属性比I强
向含有FeSO 溶液的试管中滴加几滴KSCN溶液,振荡,再滴加几滴新制
D 4 Fe2+具有还原性
氯水,观察溶液颜色变化
A.A B.B C.C D.D
4.(2024·浙江省宁波市上学期模拟)探究硫及其化合物的性质,下列实验方案、现象和结论都正确的是
实验方案 现象 结论
向NaSO 溶液和盐酸反应后的溶液中加
A 2 2 3 溶液变红 说明盐酸已经过量
入紫色石蕊试液
分别测定浓度均为0.1 mol·L-1的 不能说明水解常数(K ):
B 前者pH小于后者 h
CHCOONH 和NaSO 溶液的pH K (CHCOO-)>K (HSO -)
3 4 2 3 h 3 h 3
向稀硫酸中加入铜粉,再加入少量硝酸钾 开始无明显现象,加入
C 硝酸钾起催化作用
固体 硝酸钾后溶液变蓝
先有白色沉淀生成,滴 先生成BaSO 沉淀,后被氧
D 将SO 通入BaCl 溶液中,然后滴加氯水 3
2 2 加氯水后沉淀不溶解 化为BaSO
4
A.A B.B C.C D.D
5.(2024·江苏南京市、盐城市一模)室温下,探究0.1 mol·L-1 NaHCO 溶液的性质。下列实验方案能
3
达到探究目的的是
选项 探究目的 实验方案
向2 mL 0.1 mol·L-1 NaHCO 溶液中加入一小块钠,观察溶液中是否有
A HCO -是否发生电离 3
3 气泡产生
用干燥洁净玻璃棒蘸取0.1 mol·L-1 NaHCO 溶液,点在干燥的pH试纸
B HCO -是否发生水解 3
3 上,测出溶液的pH
取一支洁净的铂丝,蘸取0.1 mol·L-1 NaHCO 溶液后在煤气灯上灼
C 溶液中是否存在Na+ 3
烧,透过蓝色钴玻璃观察火焰颜色
向2 mL 0.1 mol·L-1 NaHCO 溶液中滴入几滴澄清石灰水,观察溶液
D 溶液中是否存在CO2- 3
3 是否变浑浊
A.A B.B C.C D.D
6.下列对实验现象及操作的解释合理的是__________________
选项 实验操作 解释或结论
① KI淀粉溶液中滴入氯水变蓝,再通入SO ,褪色 SO 具有漂白性
2 2
② 配制FeCl 溶液时需加入少量盐酸 盐酸能抑制Fe3+的水解
3
向Cu与稀HNO 反应后的溶液中,滴加稀盐酸,再次产生NO
③ 3 HCl有强氧化性
气体
④ 在瓷坩埚中熔化氢氧化钠固体后进行测量 测定熔融氢氧化钠的导电性
⑤ 同浓度时NaSO 的碱性强于NaCO 溶液 非金属性硫大于碳
2 3 2 3
⑥ 向HI溶液中加Ag单质,能产生H Ag的金属活动性排在H之前
2
⑦ NaHCO 溶液与NaAlO 溶液混合产生白色沉淀 结合H+的能力:CO<AlO
3 2
在有镀层的铁片上,用刀刻一槽,在槽上滴入少量0.1 mol·L
⑧ 可能是镀锡的马口铁片
-1盐酸,2 h后滴入KSCN溶液,无红色出现
⑨ 向盛有足量Zn和稀硫酸的试管中滴加少量硫酸铜溶液 形成锌铜原电池,使反应速率加快
⑩ HPO +2NaOH(足量)=NaHPO +2HO HPO 属于二元酸
3 3 2 3 2 3 3
pH均为1的盐酸、醋酸溶液分别用蒸馏水稀释m倍、n倍后的
⑪ m<n
pH相同
⑫ 向裂化汽油中加入酸性高锰酸钾溶液,振荡,紫色褪去 说明汽油中含有甲苯等苯的同系物
⑬ 鸡蛋清溶液遇乙酸铅溶液会产生沉淀 蛋白质发生盐析
⑭ 将苯和浓硝酸混合后加热 实验室制备硝基苯
⑮ SO 通入硝酸钡溶液出现白色沉淀 BaSO 不溶于强酸
2 3
⑯ 向次氯酸溶液中滴加少量碳酸钠溶液无气泡产生 结合H+的能力:ClO-<CO32-
12
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找