文档内容
易错专题 04 离子反应和氧化还原反应
聚焦易错点:
►易错点一 离子方程式的正误判断
►易错点二 氧化反应方程式的配平和计算
典例精讲
易错点一 离子方程式的正误判断
【易错典例】
例1下列离子方程式书写正确的是:( )
A.NaHSO 溶液与Ba(OH) 溶液反应至中性: H++SO 2—+Ba2++OH— = BaSO ↓+H O
4 2 4 4 2
B.足量的溴化亚铁和少量的氯气反应:2Fe2++4Br-+3Cl =3Fe3++2Br +6Cl-
2 2
C.钢铁发生吸氧腐蚀的正极反应式:O + 4e- +2H O =4OH—
2 2
D.用铁作电极电解饱和食盐水:2Cl-+2H O Cl ↑+H ↑+2OH-
2 2 2
【解析】A、NaHSO 溶液与Ba(OH) 溶液反应至中性,H+与OH‾恰好完全反应,离子方程式为:2H++SO2‾+Ba2+
4 2 4
+2OH‾=BaSO ↓+2HO,错误;B、Fe2+还原性大于Br‾,所以通入少量Cl ,Cl 书写氧化Fe2+,离子方程式为:
4 2 2 2
2Fe2++Cl=2Fe3++2Cl‾,错误;C、钢铁发生吸氧腐蚀时,正极O 得电子,反应式为:O + 4e- +2HO =4OH
2 2 2 2
—,正确;D、用铁作电极电解饱和食盐水,阳极上 Fe 失去电子,离子方程式为:Fe+2HO
2
Fe(OH)↓+H↑,错误。答案:C
2 2
【解题必备】
确书写及判断离子方程式的关键点
注意反应环境
审清题意
注意操作顺序
注意反应物之间量的关系
易溶强电解质拆,弱电解质、难溶物不拆
微溶物清拆浊不拆
化学式拆写
单质、氧化物不拆
浓硫酸不拆,浓盐酸、浓硝酸拆
分析量不同时的产物
反应产物
分析是否漏掉同步反应分析变价元素的产物
原子是否守恒
方程式三守恒 电荷是否守恒
电子转移是否守恒
【变式突破】
1.(2023年福建福州市高三期末) 下列离子方程式的书写正确的是( )
A.水玻璃中通人过量二氧化碳:Na SiO +CO +H O =2Na++CO 2-+H SiO ↓
2 3 2 2 3 2 3
B.Na 0 加入H 180中:2Na O +2H 18O=4Na++4OH-+18O ↑
2 2 2 2 2 2 2
C.硅与氢氟酸的反应:Si+4H++4F-=SiF ↑+2H ↑
4 2
D.过量C0 通入氢氧化钙溶液中:CO +OH-=HCO -
2 2 3
【解析】A.通入过量的CO 生成碳酸氢盐,离子方程式为SiO2—+2CO+2HO=2HCO-+HSiO↓,A错误;
2 3 2 2 3 2 3
B.在NaO 与水的反应中,水既不是氧化剂,也不是还原剂,离子方程式为2NaO+2H18O=4Na++418OH-
2 2 2 2 2
+O↑,B错误;C.氢氟酸是弱酸,写化学式,应该为Si+4HF=SiF↑+2H↑,C错误。答案:D
2 4 2
2.(2024·吉林白山·二模)下列离子方程式书写正确的是( )
A.将过量SO 气体通入NaClO溶液中:SO +HO+ClO-=SO +Cl-+2H+
2 2 2
B.电解氯化镁溶液:2Cl-+2HO 2OH-+H↑+Cl↑
2 2 2
C.NaHCO 溶液水解:HCO +HO=CO +HO+
3 2 3
D.同浓度同体积的NH HSO 溶液与NaOH溶液混合:NH +OH-=NH·HO
4 4 3 2
A【解析】A.将过量SO 气体通入NaClO溶液中,发生氧化还原反应,离子方程式为SO+HO+ClO-=SO
2 2 2
+Cl-+2H+,故A正确;
B.电解氯化镁溶液生成的氢氧化镁是沉淀,离子方程式为Mg2++2Cl- +2HO H↑+Cl↑+Mg(OH)↓,故
2 2 2 2
B错误;
C.NaHCO 溶液水解生成碳酸和氢氧根,离子方程式为HCO +HO=HCO+OH-,故C错误;
3 2 2 3D.由于NHHSO 电离的H+、NH 中H+结合OH-的能力强于NH ,所以同浓度同体积的NHHSO 溶液与NaOH溶
4 4 4 4
液混合,反应的离子方程式为H++OH-=HO,故D错误。
2
易错点二 氧化还原方程式配平和计算
【易错典例】
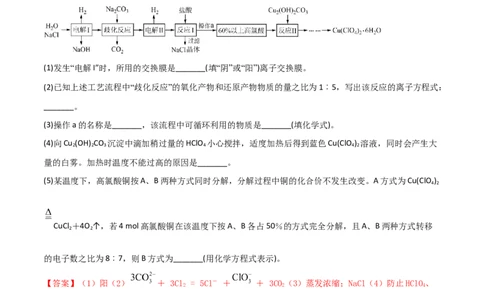
例2高氯酸铜易溶于水,在130 ℃时会发生分解反应,是一种燃烧催化剂。HClO 是易挥发的发烟液体,
4
温度高于130 ℃易爆炸。以食盐等为原料制备高氯酸铜晶体[Cu(ClO ) ·6H O]的一种工艺流程如图:
4 2 2
(1)发生“电解I”时,所用的交换膜是_______(填“阴”或“阳”)离子交换膜。
(2)已知上述工艺流程中“歧化反应”的氧化产物和还原产物物质的量之比为1︰5,写出该反应的离子方程式:
_______。
(3)操作a的名称是_______,该流程中可循环利用的物质是_______(填化学式)。
(4)向Cu (OH) CO 沉淀中滴加稍过量的HClO 小心搅拌,适度加热后得到蓝色Cu(ClO ) 溶液,同时会产生大
2 2 3 4 4 2
量的白雾。加热时温度不能过高的原因是_______。
(5)某温度下,高氯酸铜按A、B两种方式同时分解,分解过程中铜的化合价不发生改变。A方式为Cu(ClO )
4 2
CuCl +4O ↑,若4 mol高氯酸铜在该温度下按A、B各占50%的方式完全分解,且A、B两种方式转移
2 2
的电子数之比为8︰7,则B方式为_______(用化学方程式表示)。
【答案】(1)阳(2) + 3Cl = 5Cl- + + 3CO(3)蒸发浓缩;NaCl(4)防止HClO、
2 2 4
Cu(ClO) 分解(5)2Cu(ClO) 2CuO + 7O↑ + 2Cl↑
4 2 4 2 2 2
【解析】电解饱和食盐水得到氢气、氯气和NaOH溶液,得到的氯气和碳酸钠发生歧化反应生成氯化钠、氯
酸钠和二氧化碳,再电解氯酸钠溶液,阴极得到氢气,阳极得到高氯酸钠,向高氯酸钠溶液中加入盐酸生
成氯化钠和高氯酸,过滤,将滤液蒸发浓缩得到60%以上的高氯酸,向高氯酸中加入碱式碳酸铜并不断搅
拌,加热时温度不能太高,防止高氯酸铜分解和高氯酸挥发或爆炸,经过一系列过程得到高氯酸铜。(1)电解饱和食盐水采用阳离子交换膜,允许阳离子钠离子通过。
(2)由氧化产物和还原产物物质的量之比为1∶5,假设分别为1mol和5mol,还原产物为NaCl,得到5mol
电子,因此氧化产物1mol,每个Cl化合价应该升高5个即+5价氯,其氧化产物为 ,根据歧化反应
即图中信息得到 + 3Cl = 5Cl- + + 3CO;
2 2
(3)电解NaClO 溶液,阴极得到氢气,阳极得到NaClO,加盐酸反应生成HClO 和NaCl,过滤得到NaCl晶
3 4 4
体,滤液为HClO,从HClO 溶液60%的HClO,则操作a的名称是蒸发浓缩,在过滤时得到NaCl,因此该流
4 4 4
程中可循环利用的物质是NaCl。
(4)根据题中信息可知HClO、Cu(ClO) 都具有高温分解性,所以不能温度过高;故答案为:防止HClO、
4 4 2 4
Cu(ClO) 分解。
4 2
(5)4 mol高氯酸铜分解,有2mol按方程式发生Cu(ClO) CuCl+4O↑分解,共转移32mol e-,所以
4 2 2 2
B中方式转移28mol e-,由于铜化合价不变,则有4个氯由+7降到0价,氧升高,有14个氧由−2升高到
0价,配平方程式为即2Cu(ClO) 2CuO+7O↑+2Cl↑;故答案为:2Cu(ClO)
4 2 2 2 4 2
2CuO + 7O↑ + 2Cl↑。
2 2
【解题必备】
1.氧化还原反应方程式的配平
(1)配平原则:电子守恒、原子守恒、电荷守恒
(2)配平步骤(以高锰酸钾和浓盐酸反应制氯气为例):①标出化合价变化了的元素的化合价。②根据元素存
在的实际形式调整发生了氧化还原反应的物质的系数,使之成1︰1的关系。③调整系数,使化合价升降总
数相等。④根据化合价升降总数相等确定发生氧化还原反应的物质的化学计量数。⑤利用元素守恒,用观
察法配平没有参加氧化还原反应的其他物质的系数。⑥检查方程式两边各原子的个数是否相等,离子方程
式还要检查方程式两边的离子所带的电荷数是否相等。
2.信息型氧化还原反应方程式的书写:信息型氧化还原反应方程式的书写涉及元素化合价的变化。虽参加
反应的物质比较陌生,但可依据氧化还原的得失电子守恒思想,写出主要反应物和产物,再根据溶液的性
质,补上适当的反应物或生成物。具体步骤如下:根据氧化还原顺序规律确定氧化性最强的为氧化剂,还
原性最强的为还原剂;根据化合价规律及题给信息和已知元素化合物性质确定相应的还原产物、氧化产物;根据氧化还原反应的守恒规律确定氧化剂、还原剂、还原产物、氧化产物的相应化学计量数;根据溶液的
酸碱性,通过在反应方程式的两端添加H+或OH-的形式使方程式两端的电荷守恒;根据原子守恒,通过在
反应方程式两端添加HO(或其他小分子)使方程式两端的原子守恒。
2
3.氧化还原反应计算:氧化还原反应计算应首先找出氧化剂、还原剂及其物质的量以及每摩尔氧化剂、还
原剂得失电子的物质的量,然后根据得失电子守恒列出等式:氧化剂的物质的量×每摩尔氧化剂得电子数
=还原剂的物质的量×每摩尔还原剂失电子数。利用这一等式,解氧化还原反应计算题,可化难为易,化
繁为简。守恒思想是我们常用解答计算题的重要方法,也是将问题化繁为简的重要手段,我们平时常涉及
到的守恒有电荷守恒、电子守恒、原子守恒。而利用电子守恒思想求解氧化还原问题又是高考重要题型,
解答此类题目应首先找出氧化剂、还原剂及对应的还原产物和氧化产物;再确定一个原子或离子得失电子
数,列出等式关系,对于多步连续进行的氧化还原反应,只要中间各步反应过程中没有损耗,可直接找出
起始物和最终产物,删去中间产物,建立二者之间的电子守恒关系,快速求解。氧化还原反应计算得具体
步骤是:找出氧化剂、还原剂及相应的还原产物和氧化产物;确定一个原子或离子得失电子数(注意化学
式中的原子个数);根据题中物质的物质的量和得失电子守恒列出等式;对于多步连续进行的氧化还原反
应,只要中间各步反应过程中没有损耗,可直接找出起始物和最终产物,删去中间产物,建立二者之间的
电子守恒关系,快速求解。
【变式突破】
3. (1)准确称取所制备的氯化亚铜样品m g,将其置于过量的FeCl 溶液中,待样品完全溶解后,加入适量
3
稀硫酸,用a mol·L-1的KCrO 溶液滴定到终点,消耗KCrO 溶液b mL,反应中CrO2-被还原为Cr3+。
2 2 7 2 2 7 2 7
样品中CuCl的质量分数为________。
(2)水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO 和碱性KI溶液,生成MnO(OH) 沉淀,密
4 2
封静置,加入适量稀HSO,待MnO(OH) 与I-完全反应生成Mn2+和I 后,以淀粉作指示剂,用NaSO 标准
2 4 2 2 2 2 3
溶液滴定至终点,测定过程中物质的转化关系如下:O――→MnO(OH)――→I――→SO2-。O 将Mn2+氧化
2 2 2 4 6 2
成MnO(OH) 的离子方程式:______________。取加过一定量CaO·8HO的池塘水样100.00 mL,按上述方
2 2 2
法测定水样的溶解氧,消耗0.010 00 mol·L-1 NaSO 标准溶液13.50 mL。该水样中的溶解氧_______(以
2 2 3
mg·L-1表示)。
(3)某铁的氧化物(FeO)1.52 g溶于足量盐酸中,向所得溶液中通入标准状况下112 mL Cl ,恰好将Fe2+
x 2
完全氧化。x值为________。
(4)联氨(又称肼,NH ,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。实验室中可用次氯酸钠
2 4
溶液与氨反应制备联氨,反应的化学方程式为__________。联氨是一种常用的还原剂。向装有少量AgBr的
试管中加入联氨溶液,观察到的现象是___。联氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论
上1 kg的联氨可除去水中溶解的O________kg;与使用NaSO 处理水中溶解的O 相比,联氨的优点是
2 2 3 2
__________。
【答案】(1) 0.597ab÷m×100%(2)2Mn2++O +4OH-===2MnO(OH)↓ 10.80(3)0.8(4)2NH +NaClO===NH +
2 2 3 2 4NaCl+HO 固体逐渐变黑,并有气泡产生 1 NH 的用量少,不产生其他杂质(还原产物为N 和HO,而
2 2 4 2 2
NaSO 产生NaSO)
2 3 2 4
【解析】(1)反应的离子方程式:CrO2-+14H++6Cu+===6Cu2++2Cr3++7HO,由题意可知n(CrO2-)=a
2 7 2 2 7
mol·L-1×b×10-3 L,结合方程式化学计量数可得n(Cu+)=6ab×10-3mol,则样品中CuCl的质量分数
为×100%=%。(2)反应中Mn由+2价升至+4价,O由0价降至-2价,根据Mn和O得失电子守恒配平反应,
并用OH-平衡电荷反应的离子方程式为:2Mn2++O +4OH-===2MnO(OH)↓。找出反应之间的关系:n(O)~
2 2 2
n[MnO(OH)]~n(I)~n(SO),根据NaSO 的消耗量,可计算出水样中的溶解氧。 (3)FeO与盐酸和Cl 反
2 2 2 2 2 3 x 2
应的总离子方程式为:FeO+2H++Cl===xFe3++(3x-2)Cl-+HO,由题意得56x+16:=1.52 g:0.005
x 2 2
mol,解得x=0.80。(4)由题意可知,次氯酸钠是强氧化剂,氨是还原剂,氮元素由-3价升高到-2价,
失去1个电子,生成联氨,氯元素由+1价降低到-1价,得到2个电子,生成稳定的氯化钠,则反应的化
学方程式为2NH +NaClO===NH +NaCl+HO。由题意可知,联氨是还原剂,AgBr是氧化剂,两者反应时,
3 2 4 2
AgBr中银元素由+1价降低到0价,生成的单质银或银粉覆盖在淡黄色的溴化银固体表面,联氨中氮元素
由-2价升高到0价,生成氮气,反应的化学方程式为 NH +4AgBr ===N↑+4Ag+4HBr(可能还发生反应
2 4 2
NH +HBr===NHBr),因此可观察到淡黄色固体逐渐变黑,并有气泡产生。由 NH +O===N +2HO可知,1
2 4 2 5 2 4 2 2 2
mol联氨可除去1 mol O ,又因为M(NH)=M(O),m=n·M,1 kg 联氨可除去O 的质量为1 kg;用亚硫
2 2 4 2 2
酸钠处理水中溶解氧的原理为2NaSO +O===2NaSO ,处理等物质的量的O 时,消耗联氨的物质的量仅为
2 3 2 2 4 2
消耗亚硫酸钠的物质的量的一半,且联氨与氧气反应的产物为N 和HO,而亚硫酸钠与氧气反应的产物为
2 2
NaSO。
2 4
4. 硫酸亚铁是生产钛白粉的副产品,可用于制磷酸铁(FePO )、氧化铁黑(Fe O )。
4 3 4
(1)以硫酸亚铁溶液为原料制取磷酸铁的过程为:向硫酸亚铁溶液中加入磷酸和氨水,在搅拌的条件下加入
双氧水,在70~75℃范围内反应,有白色FePO ·3H O沉淀析出。将沉淀过滤、洗涤、干燥得磷酸铁。
4 2
①写出该过程中由硫酸亚铁制取FePO ·3H O的化学方程式:______。
4 2
②该过程中温度不能过高,过高会使得FePO ·3H O产率变低,原因是______。
4 2
(2)一种以铁粉、硫酸亚铁溶液为原料制取氧化铁黑的示意图如图所示。
①写出转化Ⅱ反应的离子方程式:______。
②转化Ⅱ中的O 来自于空气,反应中通入空气不能过量,过量会使所得产品中含有红色的杂质,该杂质是
2______。
【答案】(1)①2FeSO+2HPO+4NH·HO+HO 2FePO·3HO↓+2(NH)SO②温度过高会导致
4 3 4 3 2 2 2 4 2 4 2 4
HO 分解、氨水挥发 (2)①6Fe2++6HO+O=2FeO+12H+②FeO[或Fe(OH)]
2 2 2 2 3 4 2 3 3
【解析】(1)①根据题意,硫酸亚铁、磷酸、氨水和双氧水在70~75℃下反应生成FePO·3HO沉淀,反应
4 2
的化学方程式为:2FeSO+2HPO+4NH·HO+HO 2FePO·3HO↓+2(NH)SO;
4 3 4 3 2 2 2 4 2 4 2 4
②温度过高会导致过氧化氢分解,同时在高温下氨水中的氨分子会从溶液中溢出,降低FePO·3HO的产
4 2
率;
(2)①根据转化的示意图,FeSO 溶液与O 反应生成FeO,反应的化学方程式为
4 2 3 4
6FeSO+6HO+O=2FeO+6HSO,反应的离子方程式为6Fe2++6HO+O=2FeO+12H+;
4 2 2 3 4 2 4 2 2 3 4
②根据题目,若得到的产品中含有红色的杂质,该杂质含有Fe元素,则该杂质可能为FeO[或Fe(OH)]。
2 3 3
考点精练
1.(2024·浙江杭州·二模)下列方程式的书写,不正确的是
A. 溶液暴露在空气中:
B.铅酸蓄电池放电的负极反应:
C.葡萄糖与新制氢氧化铜反应:
D.煅烧黄铁矿制
2.(2024·浙江嘉兴·二模)高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理,制备的一种方法其原理: ,下列说法不正确的是
A. Fe3+是还原剂 B.H O既不是还原产物也不是氧化产物
2
C.生成 ,转移 电子 D.氧化产物与还原产物的物质的量之比为
3.(2024·湖南益阳·三模)今年春晚长沙分会场的焰火璀璨夺目,燃放烟花时发生反应:
,同时在火药中会加入 等物质。下列说法正
确的是
A.该反应中,氧化产物与还原产物物质的量之比为
B.每生成 ,被S氧化的C的物质的量为
C.火药中的 均不参与化学反应
D.燃放烟花对环境没有污染
4.(2024·浙江嘉兴·二模)下列化学反应与方程式不相符的是
A.向银氨溶液中加入过量盐酸:
B. 溶液中加入 产生沉淀:
C.将二氧化硫通入氢硫酸中产生黄色沉淀:
D.乙醇与 酸性溶液反应:
5.(2024·安徽黄山·二模)下列有关离子方程式书写正确的是
A.侯氏制碱法中制备NaHCO :NH +CO +H O=HCO +NH
3 3 2 2
B.酸性条件下催化电解 制 的阴极电极反应式为:2CO +12e−+12H+=CH CH OH+3H O
2 3 2 2
C.向苯酚钠溶液中通入少量二氧化碳:
D.碳酸铵与氢氧化钙溶液反应:CO +Ca2+=CaCO ↓
3
6.(2024·贵州贵阳·一模)下列离子方程式书写正确的是A.用高锰酸钾溶液滴定草酸:
B.电解饱和食盐水:
C.向 溶液中加入足量稀硝酸:
D.将足量 通入 溶液中:
7.(2024·湖南益阳·三模)下列反应的离子方程式正确的是
A.电解饱和的 溶液:
B.漂粉精的制备:
C.乙醛的银镜反应:
D.向胆矾溶液中加入过量的浓氨水:
8.(2024·湖南常德·一模) 是应用最广的卤素间化合物,是一种很好的溶剂,其熔点、沸点分别为
8.8℃、127℃。常温下,它能与水发生反应: 。设阿伏加德罗常数
值为 。下列说法正确的是
A.标准状况下,22.4L的 中含 键数为
B.当反应中转移电子数为 时,可产生1mol
C.将反应生成的1mol 溶于水,所得溶液中含溴的微粒总数小于
D.若有5mol水参与反应,则有2mol 被氧化
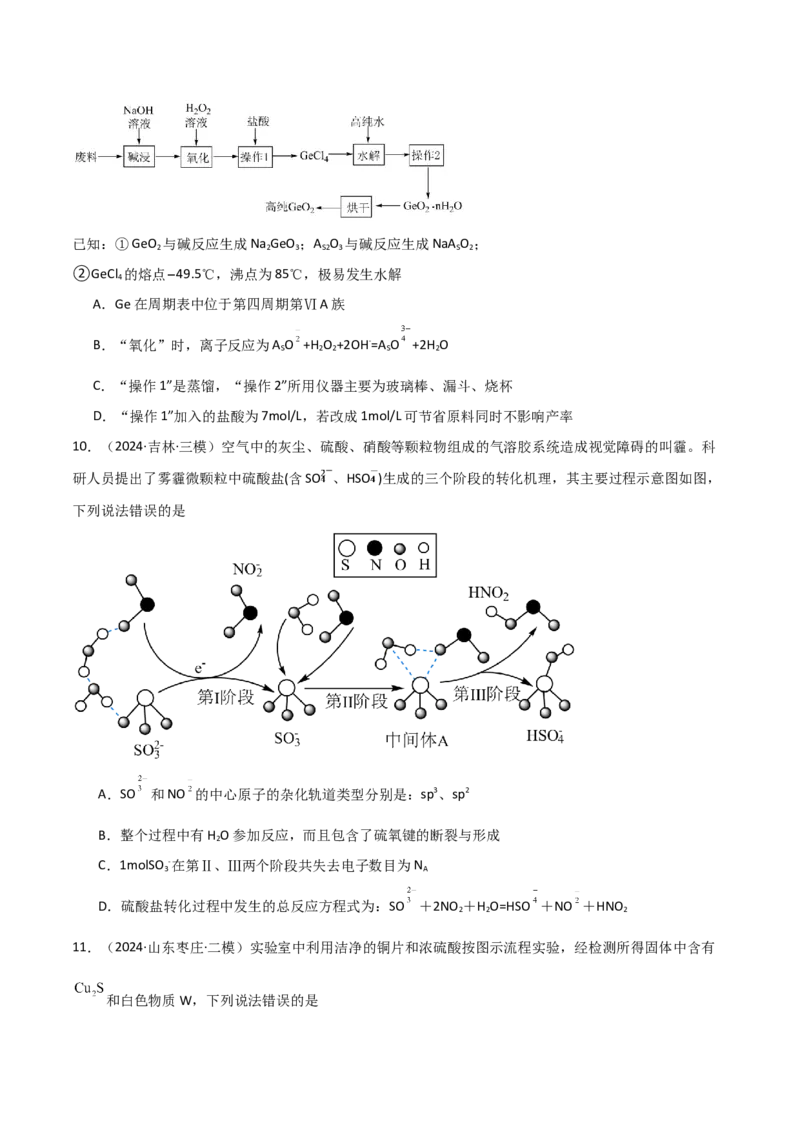
9.(2024·吉林·三模)二氧化锗常用作有机反应的催化剂以及制备半导体的原料。某大型化工厂提纯二氧
化锗废料(主要含GeO 、A O )的工艺如图,下列有关说法正确的是
2 S2 3已知:①GeO 与碱反应生成Na GeO ;A O 与碱反应生成NaAO ;
2 2 3 S2 3 S 2
②GeCl 的熔点−49.5℃,沸点为85℃,极易发生水解
4
A.Ge在周期表中位于第四周期第ⅥA族
B.“氧化”时,离子反应为AO +H O +2OH-=AO +2H O
S 2 2 S 2
C.“操作1”是蒸馏,“操作2”所用仪器主要为玻璃棒、漏斗、烧杯
D.“操作1”加入的盐酸为7mol/L,若改成1mol/L可节省原料同时不影响产率
10.(2024·吉林·三模)空气中的灰尘、硫酸、硝酸等颗粒物组成的气溶胶系统造成视觉障碍的叫霾。科
研人员提出了雾霾微颗粒中硫酸盐(含SO 、HSO )生成的三个阶段的转化机理,其主要过程示意图如图,
下列说法错误的是
A.SO 和NO 的中心原子的杂化轨道类型分别是:sp3、sp2
B.整个过程中有H O参加反应,而且包含了硫氧键的断裂与形成
2
C.1molSO -在第Ⅱ、Ⅲ两个阶段共失去电子数目为N
3 A
D.硫酸盐转化过程中发生的总反应方程式为:SO +2NO +H O=HSO +NO +HNO
2 2 2
11.(2024·山东枣庄·二模)实验室中利用洁净的铜片和浓硫酸按图示流程实验,经检测所得固体中含有
和白色物质W,下列说法错误的是A.该实验能体现浓硫酸的吸水性和强氧化性
B.当Cu完全反应时共转移电子0.050mol
C.溶解步骤中生成固体Y的质量为0.192g
D.将W溶液蒸发结晶并灼烧可再次得到固体W
12.(2024·江苏南通·二模)第四周期过渡元素形成的化合物具有重要作用。黄铜( )用
溶液浸泡后生成单质硫,所得 溶液可用于制取纳米 , 能与酸发生反应。
可用于低温下催化氧化HCHO:
。 具有强氧化性,可与盐酸反应生成氯气。由 、 、 和 反应制备的
配合物 可应用于 的鉴定。
下列化学反应表示正确的是
A. 与稀硫酸反应:
B. 溶液和 反应:
C. 与足量盐酸反应:
D.制备 的反应:
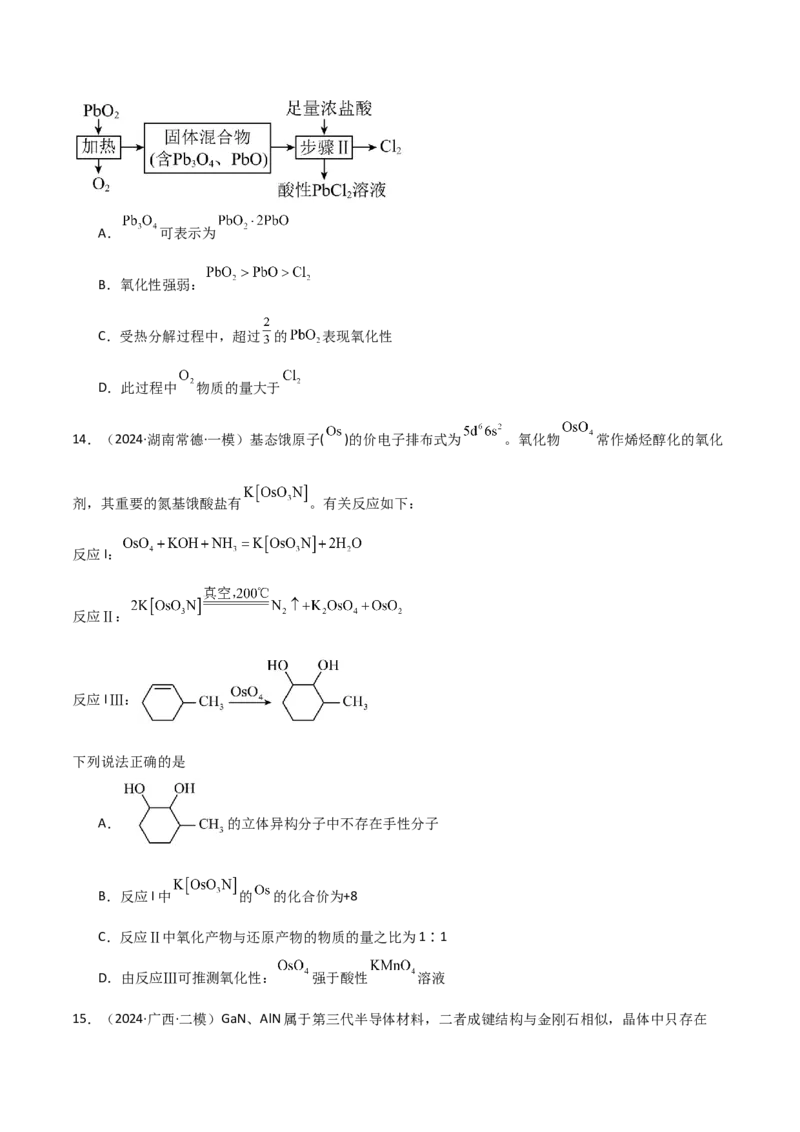
13.(2024·贵州黔西·一模)实验室利用固体 进行如图实验,已知 中Pb为 、 价。下列说
法不正确的是A. 可表示为
B.氧化性强弱:
C.受热分解过程中,超过 的 表现氧化性
D.此过程中 物质的量大于
14.(2024·湖南常德·一模)基态饿原子( )的价电子排布式为 。氧化物 常作烯烃醇化的氧化
剂,其重要的氮基饿酸盐有 。有关反应如下:
反应I:
反应Ⅱ:
反应IⅢ:
下列说法正确的是
A. 的立体异构分子中不存在手性分子
B.反应I中 的 的化合价为+8
C.反应Ⅱ中氧化产物与还原产物的物质的量之比为1∶1
D.由反应Ⅲ可推测氧化性: 强于酸性 溶液
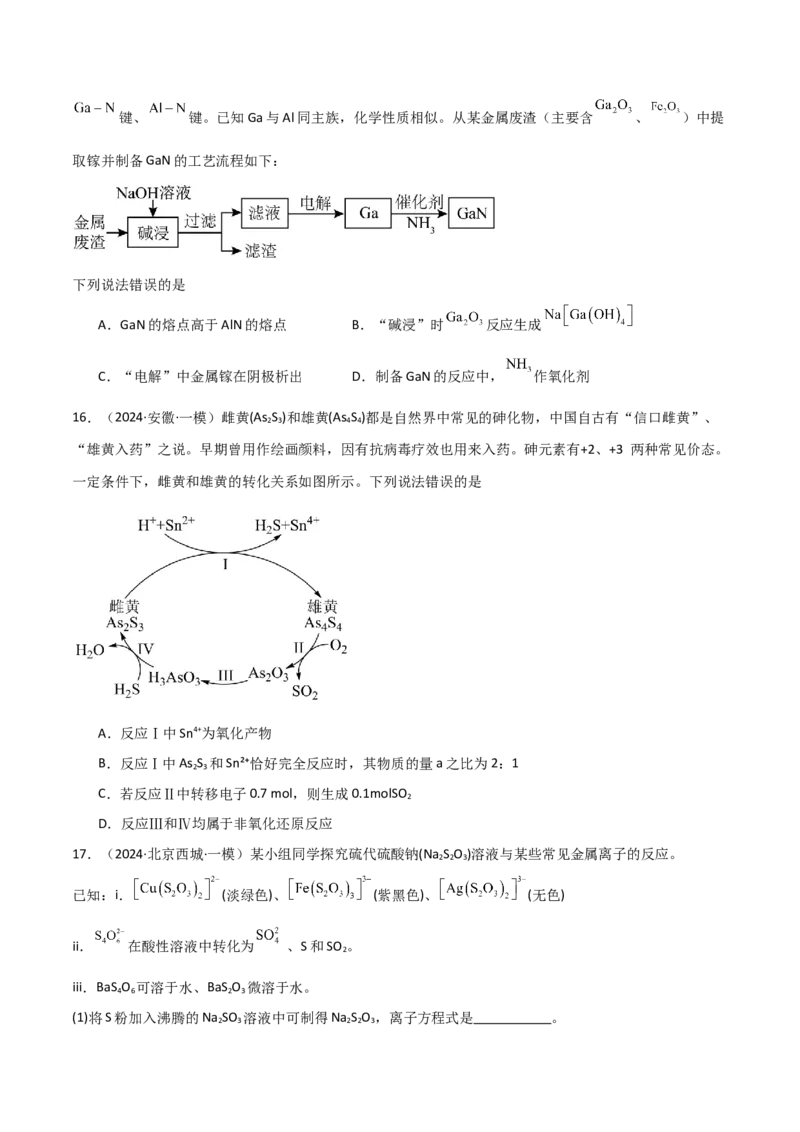
15.(2024·广西·二模)GaN、AlN属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在键、 键。已知Ga与Al同主族,化学性质相似。从某金属废渣(主要含 、 )中提
取镓并制备GaN的工艺流程如下:
下列说法错误的是
A.GaN的熔点高于AlN的熔点 B.“碱浸”时 反应生成
C.“电解”中金属镓在阴极析出 D.制备GaN的反应中, 作氧化剂
16.(2024·安徽·一模)雌黄(As S )和雄黄(As S )都是自然界中常见的砷化物,中国自古有“信口雌黄”、
2 3 4 4
“雄黄入药”之说。早期曾用作绘画颜料,因有抗病毒疗效也用来入药。砷元素有+2、+3 两种常见价态。
一定条件下,雌黄和雄黄的转化关系如图所示。下列说法错误的是
A.反应Ⅰ中Sn4+为氧化产物
B.反应Ⅰ中As S 和Sn²⁺恰好完全反应时,其物质的量a之比为2:1
2 3
C.若反应Ⅱ中转移电子0.7 mol,则生成0.1molSO
2
D.反应Ⅲ和Ⅳ均属于非氧化还原反应
17.(2024·北京西城·一模)某小组同学探究硫代硫酸钠(Na S O )溶液与某些常见金属离子的反应。
2 2 3
已知:i. (淡绿色)、 (紫黑色)、 (无色)
ii. 在酸性溶液中转化为 、S和SO 。
2
iii.BaS O 可溶于水、BaS O 微溶于水。
4 6 2 3
(1)将S粉加入沸腾的Na SO 溶液中可制得Na S O ,离子方程式是 。
2 3 2 2 3(2)研究 Na S O 与某些常见金属离子的反应,进行如下实验。
2 2 3
序
X溶液 现象
号
I CuCl 溶液 溶液变为淡绿色,水浴加热至50℃以上,逐渐析出黑色沉淀
2
Ⅱ FeCl 溶液 溶液变为紫黑色,片刻后溶液变为无色
3
AgNO 溶 逐滴加入AgNO 溶液,生成白色沉淀,振荡后沉淀溶解,得无
Ⅲ 3 3
液 色溶液
①取I中的浊液,离心分离,经检验,沉淀是Cu S和S的混合物,清液中存在 。
2
i.补全I中生成黑色沉淀的总反应的离子方程式:
□___________ □___________ □___________ □___________+
ii.查阅资料可知,常温时,生成黑色沉淀反应的平衡常数很大,但仍需水浴加热至50℃以上才出现沉淀,
原因是 。
②Ⅱ中, 被Fe3+氧化的主要产物是 ,还有很少量的 。取Ⅱ中的无色溶液进行如下实验证实
了此结论。
用H O代替Ⅱ中的FeCl 溶液,重复上述实验, CS 溶解后几乎无固体剩余。
2 3 2
i.仅由溶液1中加入足量的盐酸后得到沉淀2,不能说明Ⅱ中生成了 ,理由是 。
ii.补全实验方案证实上述结论:将沉淀1洗净, 。
③向Ⅲ的无色溶液中继续加入0.5mL 0.1mol·L-1AgNO 溶液,产生白色沉淀Ag S O 。静置,得到黑色沉淀
3 2 2 3
Ag S,同时生成强酸。生成Ag S的化学方程式是 。
2 2
(3)软硬酸碱原理认为,Ⅲ中, Ag+为软酸, 为软碱, S2-是比 更软的碱,可解释 与Ag+反
应的最终产物为Ag S。由此推测,Ⅰ中, Cu+和Cu2+, 是更软的酸。
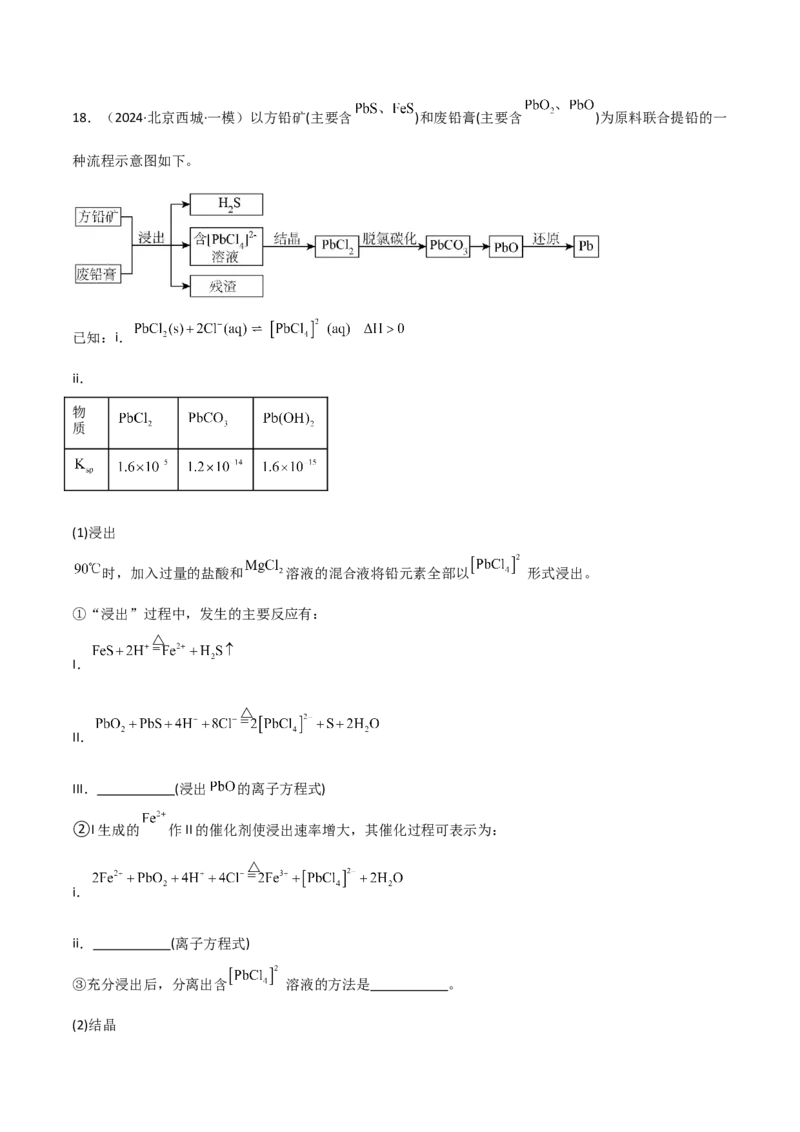
218.(2024·北京西城·一模)以方铅矿(主要含 )和废铅膏(主要含 )为原料联合提铅的一
种流程示意图如下。
已知:i.
ii.
物
质
(1)浸出
时,加入过量的盐酸和 溶液的混合液将铅元素全部以 形式浸出。
①“浸出”过程中,发生的主要反应有:
I.
II.
III. (浸出 的离子方程式)
②I生成的 作II的催化剂使浸出速率增大,其催化过程可表示为:
i.
ii. (离子方程式)
③充分浸出后,分离出含 溶液的方法是 。
(2)结晶向含 的溶液中加入适量的冷水结晶获得 ,结合浓度商(Q)与平衡常数(K)的影响因素及大小关
系,解释加入冷水的作用: 。
(3)脱氯碳化
室温时,向 溶液中加入少量浓氨水调至 ,然后加入 固体进行脱氯碳化。
①随着脱氯碳化反应进行,溶液的 (填“增大”“减小”或“不变”)。
②脱氯碳化过程中,检测到 。 浊液转化为 的最低 。
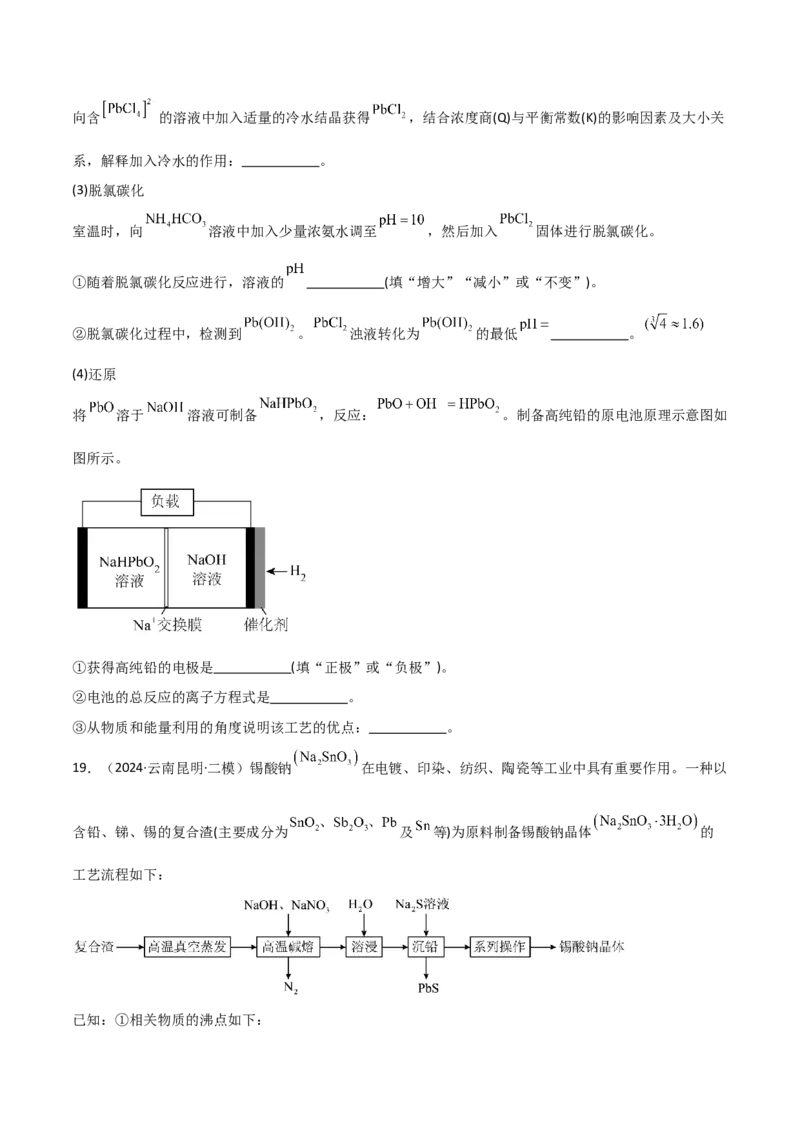
(4)还原
将 溶于 溶液可制备 ,反应: 。制备高纯铅的原电池原理示意图如
图所示。
①获得高纯铅的电极是 (填“正极”或“负极”)。
②电池的总反应的离子方程式是 。
③从物质和能量利用的角度说明该工艺的优点: 。
19.(2024·云南昆明·二模)锡酸钠 在电镀、印染、纺织、陶瓷等工业中具有重要作用。一种以
含铅、锑、锡的复合渣(主要成分为 及 等)为原料制备锡酸钠晶体 的
工艺流程如下:
已知:①相关物质的沸点如下:物质
沸点 1800 2260 1550 1740
②锡酸钠晶体易溶于水,难溶于乙醇。
回答下列问题:
(1) 元素在周期表中的位置为 。
(2)“高温真空蒸发”控制温度在 左右,目的是 。
(3)“高温碱熔”时,单质 与 和 反应生成 的化学方程式为 。
(4)已知“溶浸”后溶液中的阴离子主要为 和少量 ,“沉铅”时发生反应的离子方程式为
。
(5)获得锡酸钠晶体的“系列操作”是蒸发浓缩、冷却结晶、过滤、 (填试剂名称)洗涤、
(填“低温”或“高温”)干燥。
(6)利用焦炭在 高温下还原 可制得单质 。 存在白锡、灰锡和脆锡三种同素异形体,其
中灰锡的晶体结构与金刚石相似。若晶胞参数为 ,则最近的两个锡原子间的距离为 。
20.(2024·河南濮阳·二模)钯(Pd)是航天、航空等高科技领域不可缺少的关键材料。一种从铂钯精矿
[含有Pt、Pd、Au、Cu、Bi]中分离提取钯的工艺流程如图所示:
(1)“滤液1”中含有 和 , 中Cu的化合价为 ;Bi与As在周期表中位于同一主族,基态As原子的简化电子排布式为 。
(2)“氯化溶解”时氯气的作用是 。
(3)“分金”时, 的氧化性 (填“大于”或“小于”) ,理由是 。
(4)“沉铂”时发生反应的化学方程式为 。
(5)“沉钯”时反应的化学方程式为 。“滤液3”可以进入到 中循环利用。
(6) (水合肼)将 还原为金属钯时,还原剂与氧化剂的物质的量之比为 。
参考答案
1.D【详解】A. 溶液暴露在空气中: ,A正确;
B.铅酸蓄电池放电的负极反应: ,B正确;
C.葡萄糖与新制氢氧化铜反应:
,C正确;
D.煅烧黄铁矿制SO : ,D错误;
2
故选D。
2.C【详解】A.反应中Fe3+的化合价升高到+6价,被氧化,故Fe3+是还原剂,A正确;
B.反应中H和O的化合价均未改变,故H O既不是还原产物也不是氧化产物,B正确;
2
C.反应中Fe3+的化合价升高到+6价,则生成 ,转移3mol电子,C错误;
D.反应中 是氧化产物,Cl-是还原产物,故氧化产物与还原产物的物质的量之比为 ,D正确;
故答案为:C。
3.B【分析】 该反应中N元素化合价由+5价降为0价,S元素化合价由0价降为-2价,C元素化合价由0价升为+4价,故S和 为氧化剂,C为还原剂,CO 氧化产物,
2
、N 为还原产物。
2
A.该反应中CO 氧化产物, 、N 为还原产物,氧化产物与还原产物的物质的量之比为3∶2,故A错
2 2
误;
B.每生成 ,生成1molK S,硫得到2mol电子,被S氧化的C的物质的量为 ,故B正确;
2
C.火药中的Li CO 、NaNO 不稳定,受热易分解,参与化学反应,故C错误;
2 3 3
D.燃放烟花产生大量有毒烟尘颗粒物污染环境,故D错误;
故答案为:B。
4.A【详解】A.银氨溶液中存在[Ag(NH ) ] +,银氨溶液滴加盐酸,生成氯化银沉淀,离子方程式为:
3 2
[Ag(NH ) ] ++OH-+3H++Cl-=AgCl↓+2 +2H O,故A错误;
3 2 2
B.FeSO 溶液中加入H O 产生氢氧化铁沉淀,其反应的离子方程式为:2Fe2+
4 2 2
+H O +4H O═2Fe(OH) ↓+4H+,故B正确;
2 2 2 3
C.将二氧化硫通入氢硫酸中产生黄色沉淀,化学方程式为:2H S+SO =3S↓+2H O,故C正确;
2 2 2
D.乙醇被酸性重铬酸钾氧化为乙酸、铬离子和水,离子方程式为:
,故D正确;
故选:A。
5.B【详解】A.侯氏制碱法中制备碳酸氢钠的反应为二氧化碳与氨气和氯化钠溶液反应生成碳酸氢钠沉
淀和氯化铵,反应的离子方程式为Na++NH +CO +H O=NaHCO ↓+NH ,故A错误;
3 2 2 3
B.酸性条件下催化电解二氧化碳制乙醇时,通入二氧化碳的电极为电解池的阴极,酸性条件下二氧化碳
在阴极得到电子发生还原反应生成乙醇和水,电极反应式为2CO +12e−+12H+=CH CH OH+3H O,故B正确;
2 3 2 2
C.苯酚钠溶液与少量二氧化碳反应生成苯酚和碳酸氢钠,反应的离子方程式为 + CO +H O
2 2
+ HCO ,故C错误;D.碳酸铵溶液与氢氧化钙溶液反应生成碳酸钙沉淀、一水合氨,反应的离子方程式为CO +2NH +Ca2+
+2OH—=CaCO ↓+2NH ·H O,故D错误;
3 3 2
故选B。
6.B【详解】A.草酸是弱酸,不能拆写,用高锰酸钾溶液滴定草酸:
,A错误;
B.电解饱和食盐水: ,B正确;
C.向 溶液中加入足量稀硝酸: ,C错误;
D.将足量 通入 溶液中: ,D错误;
故选B。
7.C【详解】A.原离子方程式电荷不守恒,电解饱和的AlCl 溶液正确的离子方程式为2Al3++6Cl-+6H O
3 2
2Al(OH) ↓+3H ↑ +3Cl ↑,故A错误;
3 2 2
B.漂粉精的制备是将氯气通入石灰乳,由于不是溶液中的反应,所以不能拆,正确的离子方程式为:
Ca(OH) +2Cl =CaCl +Ca(ClO) +2H O,B错误;
2 2 2 2 2
C.乙醛发生银镜反应,生成乙酸铵、氨气、水和银,离子方程式为CH CHO+2[Ag(NH ) ]++2OH−
3 3 2
CH COO−+ +2Ag↓+3NH +H O,C正确;
3 3 2
D.氨水过量,氢氧化铜溶解,正确的离子方程式为Cu2++4NH H O=[Cu(NH ) ]2++4H O,D错误;
3 2 3 4 2
本题选C。 ⋅
8.C【详解】A.标准状况下, 为液体,无法计算其物质的量,A错误;
B.方程式 转移6个电子,则当反应中转移电子数为 时,可产
生0.67mol ,B错误;C.单质溴和水反应方程式为Br +H O HBr+HBrO,是可逆反应,则将反应生成的1mol 溶于水,所得溶
2 2
⇌
液中含溴的微粒总数小于 ,C正确;
D.根据方程式 可知,当有5mol水参与反应,则有1 mol 被氧
化,D错误;
故选C。
9.B【分析】废料碱浸后生成Na GeO 、NaAO ,加入过氧化氢溶液氧化除砷,加入盐酸蒸馏得到GeCl ,
2 3 S 2 4
加入纯水GeCl 水解,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,过滤得到 ,烘干得到
4
GeO ,据此分析解题。
2
A. Ge在周期表中位于第四周期第IVA族,故A错误;
B. “氧化”时,+3价砷转化为+5价砷,离子反应为AO +H O +2OH-=AO +2H O,故B正确;
S 2 2 S 2
C. “操作1”是蒸馏,“操作2”为蒸发浓缩、冷却结晶、过滤、洗涤、干燥,所用仪器主要为蒸发皿、铁
架台(带铁圈)、酒精灯、玻璃棒、漏斗、烧杯,故C错误;
D.GeCl 极易发生水解 ,若改成1mol/L的盐酸,可能造成GeCl 水解,产率降低,故D错误;
4 4
故选B。
10.B【分析】由图可知,硫酸盐转化过程中发生的反应为二氧化氮与亚硫酸根离子和水反应生成亚硝酸、
亚硝酸根离子和硫酸氢根离子,反应的离子方程式为SO +2NO +H O=HSO +NO +HNO ,反应中氮元素的
2 2 2
化合价降低被还原,二氧化氮是反应的氧化剂,硫元素化合价升高被氧化,亚硫酸根离子是反应的还原剂。
A.SO 和NO 的中心原子的价层电子对数为 =4、 =3,杂化轨道类型分别
是:sp3、sp2,A正确;
B.由图可知,整个过程中有H O参加反应,但是没有硫氧键的断裂,B错误;
2
C.由图可知SO 在第Ⅱ、Ⅲ两个阶段被氧化生成HSO ,则反应中消耗1mol SO ,共失去电子数目为
1mol×(6—5)×N mol-1=N 个,故C正确;
A A
D.由分析可知,硫酸盐转化过程中发生的总反应方程式为:SO +2NO +H O=HSO +NO +HNO ,D正
2 2 2确;
故选B。
11.B【分析】由图知,铜与足量浓硫酸反应生成Cu S和白色物质W,无气体生成,生成Cu S时铜元素从
2 2
0价升高到+1价、硫元素从+6价降低到-2价,则按得失电子数守恒、必定存在其他产物(所含元素化合价升
高)、按元素质量守恒只能为CuSO ,则白色物质W为CuSO ,配平得到该反应方程式为:
4 4
,Cu S和白色物质CuSO 加稀硫酸和稀硝酸时溶解,存在反应:
2 4
,Y为S单质,则NO为还原产物、Y为氧化产物;n(Cu)=
=0.03mol,Cu与浓硫酸发生反应生成CuSO 、Cu S,设Cu S的物质的量为x,则CuSO 的物质的量
4 2 2 4
为(0.03-2x),依据得失电子守恒的原则可得:2x+2(0.03-2x)=8x,从而求出x=0.006mol,0.03-2x=0.018mol,
即Cu S为0.006mol,CuSO 为0.018mol,据此回答。
2 4
A.由 可知,硫元素从+6价降低到-2价时表现强氧化性,所得固
体中含有白色物质W为硫酸铜,表现出吸水性,故A正确;
B.微热5min待Cu反应结束后,按Cu计算,转移电子的物质的量为0.006mol×2+0.018mol×2=0.048mol,
故B错误;
C.由分析知,5n(Cu) n(Cu S) n(S),n(S)= =0.006mol,m(S)=32g/mol 0.006mol=0.192g,故C正确;
2
D.W为CuSO ,将硫酸铜溶液蒸发结晶并灼烧可再次得到固体CuSO ,故D正确;
4 4
答案选B。
12.B【详解】A. 与稀硫酸发生歧化反应,离子方程式为: ,故A错
误;
B. 溶液和 反应,生成Fe2+和单质S,离子方程式为: ,
故B正确;
C. 具有强氧化性,可与盐酸反应生成氯气,故 与足量盐酸反应生成Cl 和Co2+,化学方程
2式为: ,故C错误;
D.制备 时的离子方程式,醋酸要保留化学式,离子方程式为:
,故D错误。
答案选B。
13.B【详解】A. 中Pb为 、 价, 可表示为 ,A说法正确;
B.“加热”过程中PbO 被还原为 和 ,因此氧化性:PbO >PbO,步骤II中部分HCl被 氧化
2 2
为Cl ,根据化合价变化可知该反应中氧化剂为+4价Pb,即氧化性PbO >Cl ,无法比较PbO与Cl 的氧化性,
2 2 2 2
B说法错误;
C.受热分解过程中,若PbO 完全分解只生成Pb O 和O , 的 表现氧化性,由于PbO 完全分解为
2 3 4 2 2
Pb O 、PbO混合物,所以超过 的 表现氧化性,C说法正确;
3 4
D.若PbO 完全分解只生成Pb O 和O ,根据得失电子守恒,生成1mol Pb O 的同时生成1mol O ,1mol
2 3 4 2 3 4 2
Pb O 与浓盐酸反应生成1molCl ,由于PbO 完全分解为Pb O 、PbO混合物,所以生成O 的物质的量大于
3 4 2 2 3 4 2
Cl ,D说法正确;
2
答案选B。
14.B【详解】A.手性分子在用是否有手性碳原子来判断,手性碳原子是指与四个各不相同原子或基团相
连的碳原子,观察结构可知,存在3个手性碳原子,因此立体异构分子中存在手性分子,故A错误;
B.基态饿原子(Os)的价电子排布式为 ,氧化物OsO ,O为-2价,则Os为+8价,观察反应I未变价,
4
由此可知反应I中 的Os化合价为+8,故B正确;
C.反应Ⅱ中, 中Os化合价为+8价,降低到K OsO 中Os化合价为+6价,而产物OsO 中Os化
2 4 2
合价为+4价,也是还原产物,因此K OsO 为还原产物,则N 为氧化产物,氧化产物与还原产物的物质的
2 4 2
量之比为2∶1,故C错误;
D.反应Ⅲ中双键并未断裂,而酸性 溶液可将碳碳双键氧化断键生成羧基,由可推测氧化性:弱于酸性 溶液,故D错误;
故答案选B。
15.A【分析】金属废渣中的 与氢氧化钠溶液反应生成可溶性物质四羟基合镓酸钠,过滤分离出氧
化铁和含镓元素溶液,含镓元素溶液电解得到镓,再催化和氨气反应生成氮化镓。
A.GaN和AlN都是共价晶体,原子半径越小,电负性越强共价键越稳定,熔点越高,N相同,镓原子半径
大于铝原子半径,GaN的熔点低于AlN的熔点,故A错误;
B.“碱浸”时发生反应 ,故B正确;
C. 中镓为+3价,生成单质化合价降低,得电子,故电解时金属镓应该在阴极析出,故C正
确;
D.制备GaN的反应中,Ga由0价变为+3价,为还原剂,故 为氧化剂,故D正确;
故选:A。
16.B【详解】A.反应I中Sn元素化合价升高,Sn4+为氧化产物,A正确;
B.反应I方程式2As S +2Sn2++4H+=As S +2Sn4++2H S↑,As S 与Sn2+恰好完全反应的物质的量之比为1:1,B
2 3 4 4 2 2 3
错误;
C.反应Ⅱ中As S +7O =2As O +4SO ,转移28mol电子,生成4mol SO ,所以转移0.7mol电子,生成0.1mol
4 4 2 2 3 2 2
SO ,C正确;
2
D.反应Ⅲ和Ⅳ中各元素化合价都没有变化,均属于非氧化还原反应,D正确;
本题选B。
17.(1)
(2) 2Cu2++2 +2H O Cu S↓+S↓+2 +4H+ 室温下,该反应速率小,加热增大了反
2 2
应速率 无色溶液中含有 , 微溶于水,溶液1中含有的 与盐酸反应生成的 也存在
于沉淀2中 加入足量的盐酸,充分反应后过滤,将不溶物用 充分溶解,得固体2,固体2的质量比固体1的小
(3)
【详解】(1)S与 发生归中反应得到 ,化学方程式为 ;答案为
。
(2)①i根据元素守恒,可知产物中Cu S的系数是1, 中S的化合价为+2价,Cu S中Cu和S的化
2 2
合价分别为+1和-2,Cu从+2价降低到+1,S的化合价从+2价降低到-2;生成1molCu S,共得到了
2
6mol电子。其他产物中还有S和 , 转化成S,化合价从+2价降低到0;转化为 ,化合价
从+2价降低到+6;在氧化还原反应中,得失电子守恒,可知S和 的系数分别是1和2。再结合电荷守
恒,可得Ⅰ中生成黑色沉淀的总反应的离子方程式为2Cu2++2 +2H O Cu S↓+S↓+2 +4H
2 2
+。
ii生成黑色沉淀反应的平衡常数很大,说明反应进行得很完全,但是仍需要加热至50℃才会出现沉淀,可
知在常温下,该反应的反应速率很慢,升高温度加快了反应速率。
② 被Fe3+氧化的主要产物是 ,还有少量的 ,加入过量的BaCl 溶液,沉淀1为BaS O 和
2 2 3
BaSO 沉淀。溶液1中含有 ,加入足量的盐酸, 在酸性溶液中转化为 、S和SO ,沉淀2中
4 2
含有BaSO 和S。加入CS 溶解S单质,剩余的固体1为BaSO 。
4 2 4
i根据已知, 被Fe3+氧化成 ,方程式:2 +2Fe3+= +2Fe2+,实验Ⅱ中加入的Fe3+和
的比例为1:2,可知 是过量的,因此无色溶液中含有 ,虽然加入了过量的BaCl ,但是
2BaS O 微溶于水,溶液1中仍会有少量的 ,加入盐酸后, 与H+反应,方程式: +2H+
2 3
=S↓+SO ↑+H O,也会生成S单质存在于沉淀2中,因此S单质不一定来自于 。
2 2
ii证实结论: 被Fe3+氧化的主要产物是 ,还有很少量的 。可知沉淀1中出了BaS O 外,还
2 3
有少量的BaSO 。BaSO 固体不溶于盐酸,可用于证明沉淀1中含有BaSO ,并且BaSO 的量应比固体1中的
4 4 4 4
少。实验操作为加入足量的盐酸,充分反应后过滤,将不溶物用CS 充分溶解,得固体2,固体2的质量比
2
固体1的小。
③Ag S O 发生歧化反应,得到Ag S,另一种物质为强酸,为H SO ,则方程式为Ag S O +H O=Ag S+
2 2 3 2 2 4 2 2 3 2 2
H SO 。
2 4
答案为2Cu2++2 +2H O Cu S↓+S↓+2 +4H+ 室温下,该反应速率小,加热增大了反应速
2 2
率 无色溶液中含有 , 微溶于水,溶液1中含有的 与盐酸反应生成的S也存在于沉淀2
中 Ag S O +H O=Ag S+H SO 。
2 2 3 2 2 2 4
(3)Ag+为软酸, 为软碱,S2-是比 更软的碱,可解释 与Ag+反应的最终产物为Ag S;可
2
知软酸容易与更软的碱的结合。Ⅰ中, 与Cu2+反应的最终产物为Cu S,可知Cu+是比Cu2+更软的酸。
2
答案是Cu+。
18.(1) 趁热过
滤
(2) 的 ,加入冷水,温度降低,K减小,溶液被稀释,Q增大,
,平衡逆向移动,析出 晶体
(3) 减小 7.5
(4) 正极 可循环使用,制备高纯铅的过程中获得电能【分析】方铅矿(主要含 )和废铅膏(主要含 )混合浸出,加入过量的盐酸和 溶液
的混合液将铅元素全部以 形式浸出,得到H S、含 溶液和含S的残渣,滤液结晶得到
2
PbCl 、PbCl 脱氧碳化得到PbCO ,PbCO 受热分解得到PbO,还原PbO得到Pb,以此解答。
2 2 3 3
(1)①浸出 的过程中,PbO转化为 ,根据电荷守恒配平离子方程式为:
;
②I生成的 作II的催化剂使浸出速率增大,其催化过程可表示为:i.
,第ii步反应中有Fe2+生成,说明PbS和Fe3+发生氧化
还原反应达到Fe2+和 ,根据得失电子守恒和电荷守恒配平离子方程式为:
;
③充分浸出后得到的溶液中含有残渣,分离出含 溶液的方法是:趁热过滤。
(2) 的 ,加入冷水,温度降低,K减小,溶液被稀释,Q增大,
,平衡逆向移动,析出 晶体。
(3)①室温时,向 溶液中加入少量浓氨水调至 ,然后加入 固体进行脱氯碳化,离
子方程式为: ,c(H+)增大,溶液的 减小;
② 浊液中存在 ,c(Pb2+)c2(Cl-)=K ( )= ,2c(Pb2+)≈c(Cl-),则
sp
4c3(Pb2+)= K ( )= ,c(Pb2+)= mol/L=1.6 mol/L,c(OH-)=
sp,c(H+)= mol/L,pH=7.5。
(4)①由图可知, 在正极得到电子生成Pb;
②由图可知, 在正极得到电子生成Pb,电极方程式为: +e-+H O=Pb++3OH-,H 在负极失去电
2 2
子生成H O,电极方程式为:H -2e-+2OH-=2H O,则电池的总反应的离子方程式是
2 2 2
;
③从物质和能量利用的角度说明该工艺的优点: 可循环使用,制备高纯铅的过程中获得电能。
19.(1)第五周期、第IVA族
(2)将 气化分离
(3)
(4)
(5) 乙醇 低温
(6)
【分析】将复合渣送入高温真空蒸发装置中,可以就爱那个复合渣中的某些物质汽化除去,随后将剩余固
体与NaOH、NaNO 共熔,可以将含Sn元素的物质转化为Na SnO ,后续利用溶浸、Na S沉铅等方法进一
3 2 3 2
步纯化锡酸钠溶液,最后将含有锡酸钠的溶液通过蒸发浓缩、冷却结晶、过滤、醇洗等方法进行结晶,得
到锡酸钠晶体。
(1)Sn元素在周期表中的位置为第五周期ⅣA族
(2)Sb O 的沸点为1550℃,为了分离除去Sb O ,“高温真空蒸发”应控制温度在1600℃左右;
2 3 2 3
(3)“高温碱熔”时,单质Sn参与的反应为:5Sn+6NaOH+4NaNO =5Na SnO +2N ↑+3H O;
3 2 3 2 2
(4)沉铅”时发生反应的离子方程式为:S2-+PbO +2H O=PbS↓+4OH-;
2
(5)锡酸钠易溶于水,难溶于乙醇,为了防止锡酸钠损失,过滤后用乙醇进行洗涤,并低温干燥,防止
锡酸钠脱水;(6)灰锡的晶体结构与金刚石相似,最近的两个锡原子间的距离为体对角线的四分之一,即 。
20.(1)
(2)作氧化剂(合理即可)
(3) 大于 只还原了 (合理即可)
(4)
(5) 沉铂、沉钯(合理即可)
(6)1:2
【分析】铂钯精矿[含有Pt、Pd、Au、Cu、Bi]用浓盐酸酸浸,“滤液1”中含有 和 ,滤饼中
含有Pt、Pd、Au,氯化溶解后加入亚硫酸钠溶液分金,金不溶解过滤除去,滤液中加入氯化铵沉铂,过滤
后加入氯化铵和次氯酸钠溶液沉钯, (水合肼)将 还原为金属钯,以此解答。
(1) 中Cl为-1价,H为+1价,Cu显 价;基态As原子的简化电子排布式为 。
(2)“氯化溶解”时氯气的作用是作氧化剂。
(3)由于“分金”时 只还原了 ,未还原 ,故 的氧化性大于 。
(4)“沉铂”时发生复分解反应,化学方程式为 。
(5)“沉钯”时次氯酸钠被还原为 , 被氧化为 ,配平后化学方程式为
。盐酸参与反应的化学方程式为
,“滤液3”为 溶液,可以进入“沉铂”、“沉钯”
步骤中循环利用。
(6) (还原剂)中N为 价,被氧化为 时失去 , (氧化剂)中Pd为价,被还原为金属Pd时得到 ,根据电子守恒可知,还原剂与氧化剂的物质的量之比为1:2。