文档内容
广东省新高考普通高中学科综合素养评价高三年级期末考
化学参考答案
一、选择题
1 2 3 4 5 6 7 8 9 10 11 12 13
D B C A B D C D C A B C D
二、非选择题
14.(11分)
(1)4s24p2(1分) Zn>Cu>Ge(1分)
(2)Ⅱ <Ⅳ(1分) p(1分)
(3)AC(2分)
(4)Ⅲ(2分) Ⅰ(1分)
(5)x= (2分)
21
858×10
15.(11分 2 ×) A×
(1)FeTiO +2H SO =FeSO +TiOSO +2H O(2分) 还原Fe3+(1分)
3 2 4 4 4 2
(2)TiO2++2NH ·H O=TiO(OH) ↓+2 (2分)
3 2 2
+
取最后的洗涤液于试管中,滴入BaCl N溶H液4 不产生白色沉淀(检测不到 ,2分)
2
2−
(3)1.5%(1分) 1-1.5(1分) SO4
(4)Ca2++2e-=Ca(2分)
16.(12分)
Ⅰ.(1)溶液有漂白性(1分)(合理答案均可)
(2)Ca2++2ClO-+CO +H O=2HClO+CaCO ↓(2分)
2 2 3
(3)①木条复燃(1分) ②成立(1分) ③CuSO (1分)④6(1分) H O(1分)
4 2
Ⅱ.(1)71.5(2分)
(2)①10.0mL(1分) ②0.20mol/L(1分)
17.(11分)
(1)2CO (g)+2H O(l)=CH COOH(l)+2O (g) ΔH=E E (kJ/mol)(3分)
2 2 3 2 2 1
(2)① 122.5(1分) Ⅱ(1分)
−
② a (1分)
−
温度低于 260℃时,主要以放热反应Ⅰ为主,此时 CH OCH 选择性较高,吸热反应Ⅱ的影
3 3
响较小,所以曲线b在260℃以前随温度升高而下降(2分)
③高压(1分)
(3)108/p3(2分)
0
— 1 —18.(11分)
(1)羧基(1分)
(2)⑦(1分) ⑥(1分)
COOH COOH O O + H O
(3) O 2 (2分)
CHO
(4)6(2分) (1分)
COOH
O
O O
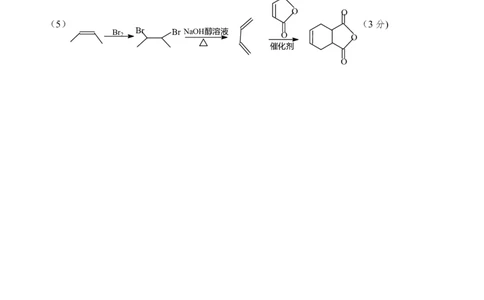
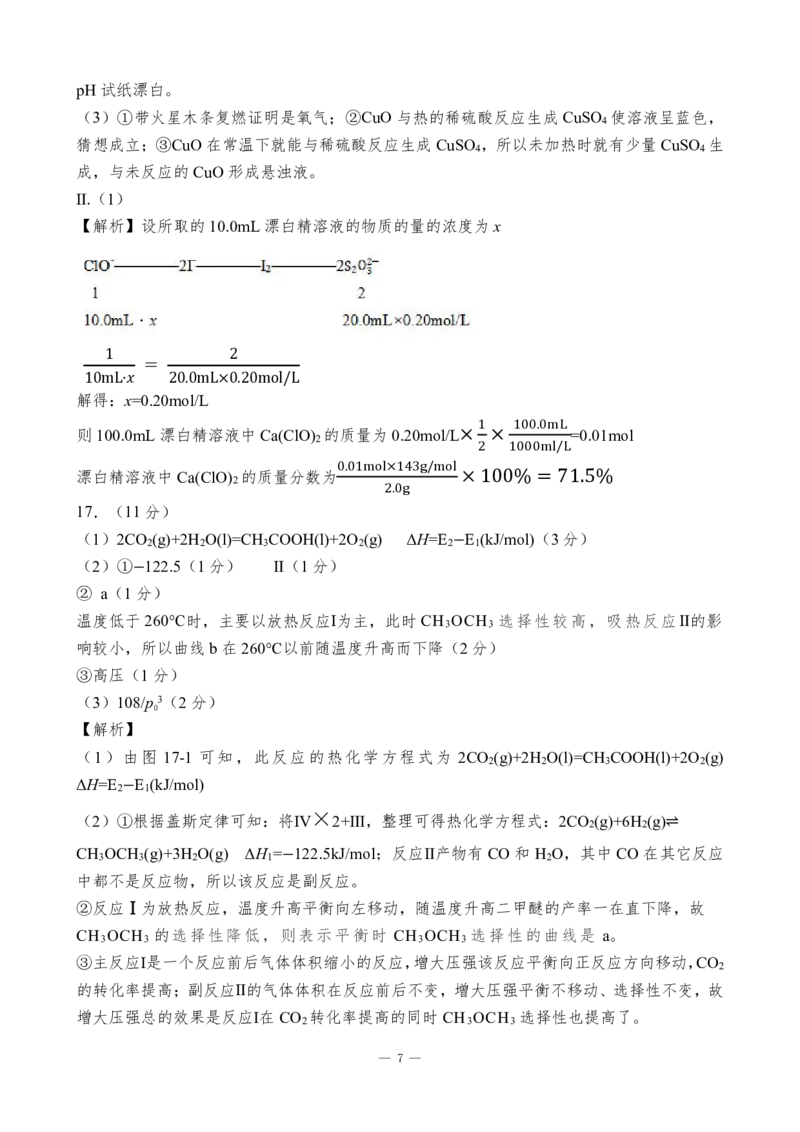
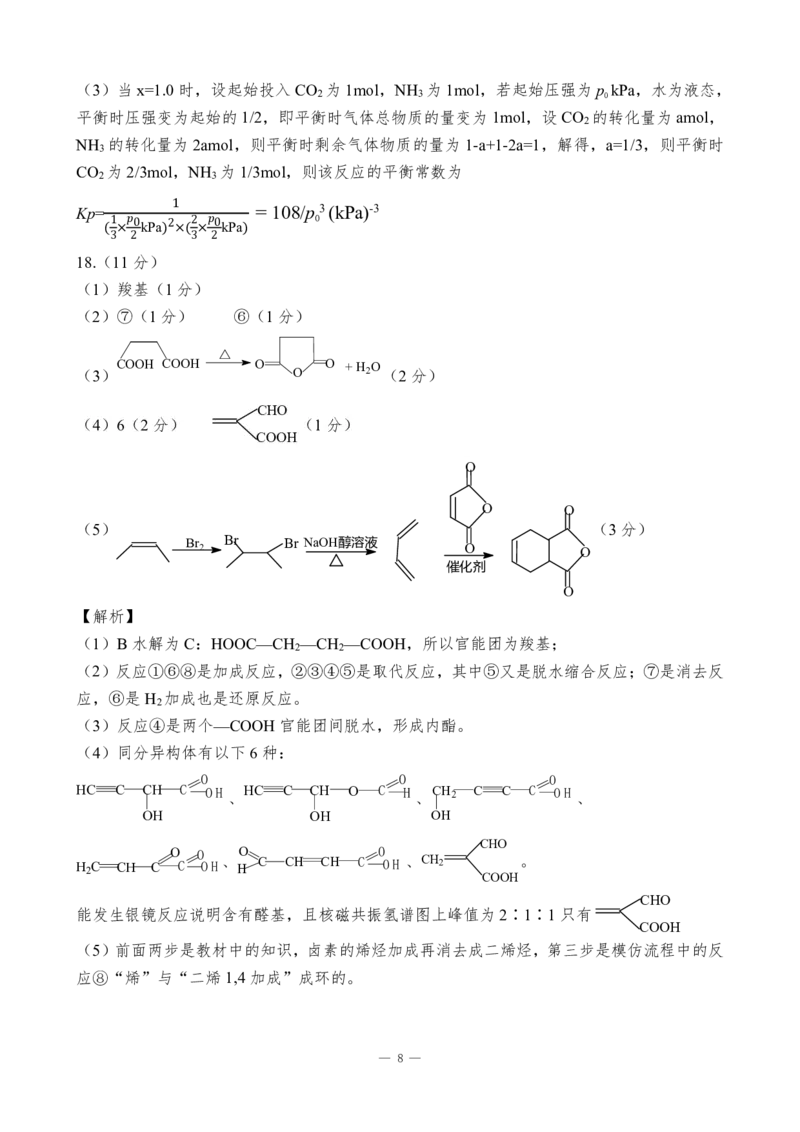
(5) (3分)
Br Br Br NaOH醇溶液
2 O O
催化剂
O
— 2 —答案详解
1.【答案】D
【解析】
A、B、C 的主要成分都是纤维素,D是金属铜,故选D。
2.【答案】B
【解析】
ACD 说法正确;B 选项中酒精没有强氧化性,故错误;D 选项中“洁厕精”含 HCl、“84 消毒
液”含HClO,混合后会发生氧化还原反应产生氯气。
3.【答案】C
【解析】
A 选项:空间站许多部件使用的是铝合金或铝基复合材料利用了铝质量轻、表面能形成氧化
膜的特性,正确。
B 选项:N O 与偏二甲肼[(CH ) N-NH ]燃烧生成H O 和N ,产物无污染,正确。
2 4 3 2 2 2 2
C 选项:氮化铝是原子晶体,陈述Ⅱ错误,且与陈述Ⅰ无因果关系。
D 选项:柠檬酸与碳酸氢钠反应产生二氧化碳,说明柠檬酸的酸性强于碳酸,正确。
4.【答案】A
【解析】
A 选项:说法正确;
B 选项:向MgCl 溶液中通入CO ,不能生成 MgCO 沉淀;
2 2 3
C 选项:SO 和Cl 同时通入水生成的亚硫酸和次氯酸会发生氧化还原反应而失去各自的漂白
2 2
性,错误;
D 选项:硝酸根在酸性条件下相当于溶液中有稀硝酸,与铜发生氧化还原反应,错误。
5.【答案】B
【解析】
由图可知ACD都正确,状态①先断的是CH 中的C—H键,所以B 错误。
4
6.【答案】D
【解析】
A 选项:苯酚的电离常数大于碳酸的二级电离常数,往C H O-溶液中通入CO 只能生成 ,
6 5 2
−
错误; HCO3
B 选项:铜与稀硝酸反应生成的是 NO,错误;
C 选项:电荷不守恒,或电子得失不相等,错误;
D 选项正确。
7.【答案】C
【解析】
A 选项:第二步错误,氨水是弱碱,不能溶解Al(OH) 形成 O ;
3
−
— 3 — Al 2B 选项:盐酸不能与SiO 反应,错误;
2
C 选项:转化可以完成,正确;
D 选项:铁在点燃条件下与氧气生成的是Fe O ;FeCl 与NaOH 生成Fe(OH) 沉淀,错误。
3 4 3 3
8.【答案】D
【解析】
A 选项:铁离子会水解,故铁离子数目小于0.2N ,错误;
A
B 选项:亚铁离子还原性强于溴离子,氯气通入时先氧化Fe2+,0.1molCl 先氧化0.1molFe2+,
2
再氧化0.1molBr—生成0.05molBr ,错误;
2
C 选项:溶液 pH=1 是指溶液中 c(H+)=0.1mol/L,包括了水电离的 H+,同时溶液体积未知,
说法错误;
D 选项:符合阿伏加德罗定律,正确。
9.【答案】C
【解析】
A 选项:后验的水蒸气可能是混合气体通过了含水的溶液带出的水蒸气,错误;
B 选项:验水后先通澄清石灰水,SO 溶于水形成的亚硫酸的酸性强于碳酸,生成沉淀可能
2
是CaSO ,若SO 过量还可能没有沉淀,验不了CO ,错误;
3 2 2
C 选项正确;
D 选项:食盐水不能吸收SO ,错误。
2
10.【答案】A
【解析】
X 只有一个质子,是 H;R 有三层电子在第三周期,负一价只能是 Cl;原子序数满足关系
Y+W=E+Z,根据题10图化合价Y四价、W一价、E二价、Z三价,只能是6(C)+9(F)=8(O)+7(N);
所以Y 是碳、W是氟、E是氧、Z是氮。
A 选项:还原性Cl->F-,正确;
B 选项:稳定性CH O2->F-,错误;
D 选项:HNO 是强酸,错误。
3
11.【答案】B
【解析】
由题 11 图可以看出,a 极 CO →HCOO-碳的化合价降低,得电子,a 极是阴(负)极;b 极
2
CH (CH ) NH →CH (CH ) CN,氮的化合价升高,失电子,b 极是阳(正)极,所以 A选项
3 2 7 2 3 2 6
错;B选项Ni P电极是阳极,阳极失电子,正确;C选项In/In O 电极是阴极,得电子发生
2 2 3-x
的是还原反应,C 叙述错误;D选项电荷不守恒,错误。
12.【答案】C
【解析】
A 选项:原溶液可能本来就存在Fe3+,错误;
— 4 —B 选项:如果溶液显酸性,向溶液中加入硝酸根,组成稀硝酸,可能把原溶液的 氧化成
了 ,所以错误; 2−
SO3
C 选项2−:Fe3+溶液加入维C后黄色变浅绿色,说明Fe3+被还原为Fe2+,维C 有还原性,正确;
SO4
D 选项:碘离子被氧化为碘单质,海带中含的是I-,而不是I ,错误。
2
13.【答案】D
【解析】
由曲线可知二元酸H R是弱酸。纵坐标数值相同时,曲线a 的pH小于曲线b,所以曲线a
2
是一级电离的lg ,曲线b是二级电离lg ,A正确;
− 2−
(HR ) (R )
−
b 曲线(10,2.8 )(H2意R)思是二级电离 pH=10, c((HHR+))=10-10,lg =2.8, =102.8,则:
2− 2−
(R ) (R )
− −
K = = ,所以B 正确; (HR ) (HR )
a2
2− +
(R ). (H ) 2.8 −10 −7.2
C 是电 荷 (HR 守− ) 恒,=正10确;×10 10
D 的排序应该是c(Na+)>c(R2—)>c(OH—)>c(HR—)>c(H+),所以D错误。
14.(11分)
(1)4s24p2(1分) Zn>Cu>Ge(1分)
(2)Ⅱ <Ⅳ(1分) p(1分)
(3)AC(2分)
(4)Ⅲ(2分) Ⅰ(1分)
(5)x= (2分)
21
858×10
【解析】 2
× A×
(1)特征电子排布:Ge(4s24p2)、Zn(3d104s2)、Cu(3d104s1),Zn轨道全满,第一电离
能最大;Ge 的 4p2分两个轨道排单电子,Cu 的 4s1也是单电子排一个轨道,但 4p 能量高于
4s 轨道,把电子轰击出来4p所需能量小于4s 轨道,所以第一电离能:Zn>Cu>Ge。
(2)Ⅱ、Ⅳ两种物质如果R 基相同,Ⅱ的分子量(分子间力)小于Ⅳ,所以沸点Ⅱ< Ⅳ;Ge
是第四周期、ⅣA 元素,最后填的电子在4p,所以位于元素周期表的p区。
(3)Ge—O—Ge 中O有两对孤对电子,采取sp3杂化,A正确;I中Ge 与O的有Ge—O键
和 Ge=O 键,键能显然不相等,B 错误;Ⅱ中 Ge 与 Ge 键为同种元素之间的共价键,是非极
性共价键,C 正确;在Ⅲ中Me-C=O两个键一个单键、一个双键,虽为sp2杂化,但键角不是
标准的 120°,D 选项错误;物质Ⅰ中有—COOH,其中的—O—C=O 不能在在 Ni 催化下发生
加氢,E选项错误。
(4)I中存在 ,其中的CH 是sp3杂化,H不可能都与C 原子在同一平面;Ⅱ、Ⅳ的
2
R 基中可能存在CH 、CH ,H也不可能都与C原子在同一平面;只有Ⅲ是sp2杂化、平面型
2 3
分子。含有—OH 的物质水溶性好,因为可以与水分子形成氢键,故 Ⅰ的水溶性最好。
— 5 —(5)确定化学式用均摊法。Ba 原子:(8×1/8)+1=2,Ge 原子:[(4×1/2)+(4×1/4)+1]×2=8,为
Ba Ge ,即2BaGe 。M (BaGe )=(137+73×2)=429
2 8 4 A 4
所以: = ,变形得 x=
21
2×429 858×10
15.(11分) −7 2 −7 2
(a×10 ) ∙( ×10 ) A a × A×
(1)FeTiO +2H SO =FeSO +TiOSO +2H O(2分) 还原Fe3+(1分)
3 2 4 4 4 2
(2)TiO2++2NH ·H O=TiO(OH) ↓+2 (2分)
3 2 2
+
取最后的洗涤液于试管中,滴入BaCl N溶H液4 不产生白色沉淀(检测不到 ,2分)
2
2−
(3)1.5%(1分) 1-1.5(1分) SO4
(4)Ca2++2e-=Ca(2分)
【解析】
钛精矿[主要成分是钛酸亚铁(FeTiO ),含少量 SiO 等杂质]经硫酸酸溶,SiO 等杂质变成
3 2 2
了滤渣1,Fe2+变成了FeSO ,可能有部分在过滤时被空气氧化为 Fe3+,所以滤液用铁粉还原,
4
滤渣2中是过量的铁粉;酸溶时钛变成了TiOSO 。加入氨水是将TiO2+变为TiO(OH) 沉淀;
4 2
加入HNO 是将TiO(OH) 沉淀溶解为TiO(NO ) 。加入氨水和SDBS 是为了形成较小颗粒的
3 2 3 2
TiO(OH) 胶体;干燥后煅烧脱水获得纳米级别的TiO 。
2 2
(1)FeTiO 与H SO 反应,生成FeSO 、TiOSO 和H O是照方程质量守恒配的;铁粉还原
3 2 4 4 4 2
可能有部分在过滤时被空气氧化为Fe3+。
(2)题干说了“整个过程中钛的化合价没有变化”,即钛的化合价都是+4 价,所以 TiO2+
与NH ·H O 反应生成 TiO(OH) ↓和 ;铁粉的加入,除了还原Fe3+以外,还与过量的H SO
3 2 2 2 4
+
反应,到了加入氨水的环节,根据电N荷H4守恒: 与TiO2+物质的量相等,所以检查洗涤液的
2−
SO4
的存在,相当于检查了TiO2+是否还存在。
2−
S(O34)晶粒平均大小为 15nm—20nm左右时,根据题15-2 图SDBS质量分数为1.5%;根据题15-2
图pH 范围在1-1.5之间。
(4)依据题干中“用石墨作阳极、钛网作阴极、熔融的CaF -CaO作电解质,利用图示装置
2
获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛”,所以电极反应中Ca2+得电子。
16.(12分)
Ⅰ.(1)溶液有漂白性(1分)(合理答案均可)
(2)Ca2++2ClO-+CO +H O=2HClO+CaCO ↓(2分)
2 2 3
(3)①木条复燃(1分) ②成立(1分) ③CuSO (1分)④6(1分) H O(1分)
4 2
Ⅱ.(1)71.5(2分)
(2)①10.0mL(1分) ②0.20mol/L(1分)
【解析】
Ⅰ.(2)漂白精溶于水,ClO-与水中少量 H CO 反应生成 CaCO 和 HClO,HClO 直接把黄色
2 3 3
— 6 —pH 试纸漂白。
(3)①带火星木条复燃证明是氧气;②CuO 与热的稀硫酸反应生成 CuSO 使溶液呈蓝色,
4
猜想成立;③CuO在常温下就能与稀硫酸反应生成CuSO ,所以未加热时就有少量CuSO 生
4 4
成,与未反应的CuO形成悬浊液。
Ⅱ.(1)
【解析】设所取的10.0mL 漂白精溶液的物质的量的浓度为x
=
1 2
解得:x=0.20mol/L
10mL∙ 20.0mL×0.20mol/L
则100.0mL 漂白精溶液中Ca(ClO) 的质量为0.20mol/L =0.01mol
2
1 100.0mL
漂白精溶液中Ca(ClO) 的质量分数为 × 2 × 1000ml/L
2
0.01mol×143g/mol
17.(11分)
2.0g × 100% = 71.5%
(1)2CO (g)+2H O(l)=CH COOH(l)+2O (g) ΔH=E E (kJ/mol)(3分)
2 2 3 2 2 1
(2)① 122.5(1分) Ⅱ(1分)
−
② a(1分)
−
温度低于260℃时,主要以放热反应Ⅰ为主,此时CH OCH 选择性较高,吸热反应Ⅱ的影
3 3
响较小,所以曲线b在260℃以前随温度升高而下降(2分)
③高压(1分)
(3)108/p3(2分)
0
【解析】
(1)由图 17-1 可知,此反应的热化学方程式为 2CO (g)+2H O(l)=CH COOH(l)+2O (g)
2 2 3 2
ΔH=E E (kJ/mol)
2 1
×
(2)①−根据盖斯定律可知:将Ⅳ 2+Ⅲ,整理可得热化学方程式:2CO (g)+6H (g)
2 2
CH 3 OCH 3 (g)+3H 2 O(g) ΔH 1 = 122.5kJ/mol;反应Ⅱ产物有 CO 和 H 2 O,其中 CO 在其 ⇌ 它反应
中都不是反应物,所以该反应是副反应。
−
②反应Ⅰ为放热反应,温度升高平衡向左移动,随温度升高二甲醚的产率一在直下降,故
CH OCH 的选择性降低,则表示平衡时 CH OCH 选择性的曲线是 a。
3 3 3 3
③主反应Ⅰ是一个反应前后气体体积缩小的反应,增大压强该反应平衡向正反应方向移动,CO
2
的转化率提高;副反应Ⅱ的气体体积在反应前后不变,增大压强平衡不移动、选择性不变,故
增大压强总的效果是反应Ⅰ在CO 转化率提高的同时CH OCH 选择性也提高了。
2 3 3
— 7 —(3)当x=1.0 时,设起始投入CO 为 1mol,NH 为1mol,若起始压强为p kPa,水为液态,
2 3 0
平衡时压强变为起始的1/2,即平衡时气体总物质的量变为1mol,设CO 的转化量为amol,
2
NH 的转化量为 2amol,则平衡时剩余气体物质的量为 1-a+1-2a=1,解得,a=1/3,则平衡时
3
CO 为2/3mol,NH 为1/3mol,则该反应的平衡常数为
2 3
Kp= = 108/p 3(kPa)-3
0
kPa kPa
1
1 0 2 2 0
18.((
31
× 12分)) ×(
3
×
2
)
(1)羧基(1分)
(2)⑦(1分) ⑥(1分)
COOH COOH O O + H O
(3) O 2 (2分)
CHO
(4)6(2分) (1分)
COOH
O
O O
(5) (3分)
Br Br Br NaOH醇溶液
2 O O
催化剂
O
【解析】
(1)B 水解为C:HOOC—CH —CH —COOH,所以官能团为羧基;
2 2
(2)反应①⑥⑧是加成反应,②③④⑤是取代反应,其中⑤又是脱水缩合反应;⑦是消去反
应,⑥是H 加成也是还原反应。
2
(3)反应④是两个—COOH 官能团间脱水,形成内酯。
(4)同分异构体有以下6种:
O O O
HC C CH C OH HC C CH O C H CH C C C OH
、 、 2 、
OH OH OH
CHO
O O O O
H 2 C CH C C OH 、 H C CH CH C OH 、CH 2 。
COOH
CHO
能发生银镜反应说明含有醛基,且核磁共振氢谱图上峰值为2∶1∶1只有
COOH
(5)前面两步是教材中的知识,卤素的烯烃加成再消去成二烯烃,第三步是模仿流程中的反
应⑧“烯”与“二烯1,4加成”成环的。
— 8 —