文档内容
素养说明:最新考试大纲明确要求考生:“熟记并正确书写常见元素的名称、符
号、离子符号;掌握原子结构示意图、电子式、分子式、结构式和结构简式等表示
方法”。所以对“一图五式”的强化,符合学科素养和考试说明的要求,是学生规
范答题的重要一环。
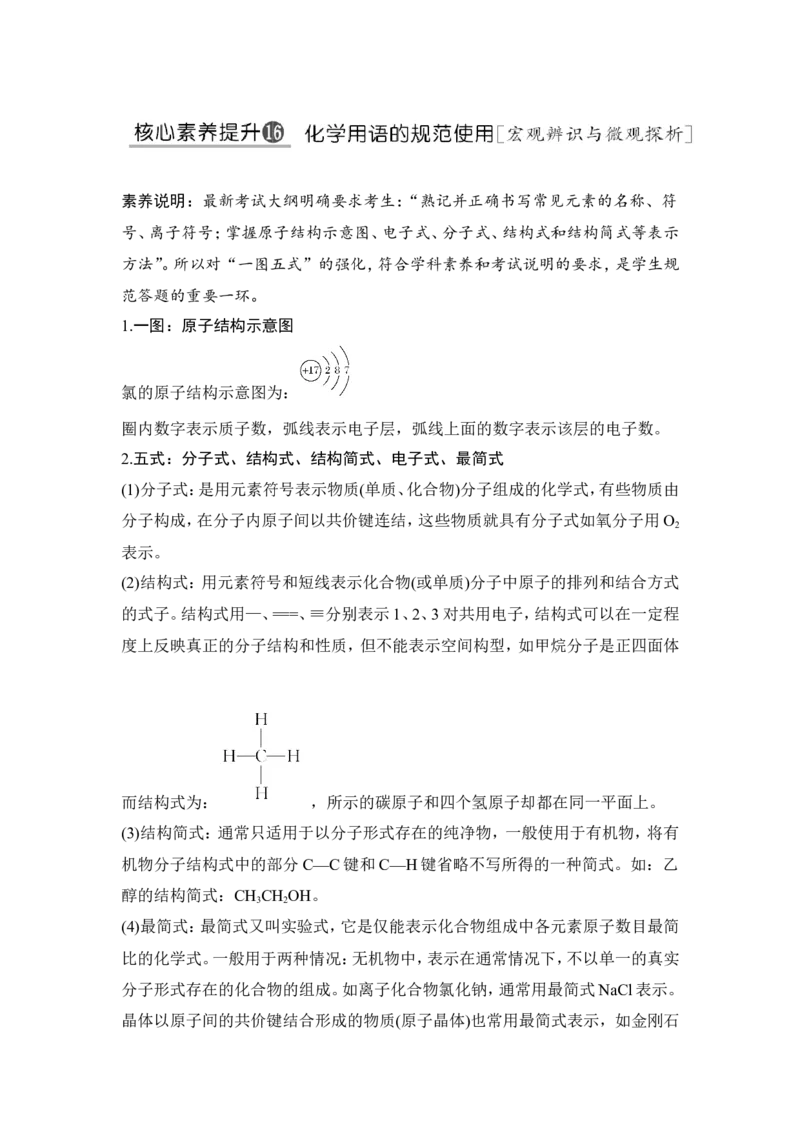
1.一图:原子结构示意图
氯的原子结构示意图为:
圈内数字表示质子数,弧线表示电子层,弧线上面的数字表示该层的电子数。
2.五式:分子式、结构式、结构简式、电子式、最简式
(1)分子式:是用元素符号表示物质(单质、化合物)分子组成的化学式,有些物质由
分子构成,在分子内原子间以共价键连结,这些物质就具有分子式如氧分子用O
2
表示。
(2)结构式:用元素符号和短线表示化合物(或单质)分子中原子的排列和结合方式
的式子。结构式用—、===、≡分别表示1、2、3对共用电子,结构式可以在一定程
度上反映真正的分子结构和性质,但不能表示空间构型,如甲烷分子是正四面体
而结构式为: ,所示的碳原子和四个氢原子却都在同一平面上。
(3)结构简式:通常只适用于以分子形式存在的纯净物,一般使用于有机物,将有
机物分子结构式中的部分C—C键和C—H键省略不写所得的一种简式。如:乙
醇的结构简式:CH CH OH。
3 2
(4)最简式:最简式又叫实验式,它是仅能表示化合物组成中各元素原子数目最简
比的化学式。一般用于两种情况:无机物中,表示在通常情况下,不以单一的真实
分子形式存在的化合物的组成。如离子化合物氯化钠,通常用最简式NaCl表示。
晶体以原子间的共价键结合形成的物质(原子晶体)也常用最简式表示,如金刚石用C表示。有机物中,由于碳之间可以成键,种类很多,而因为最简式仅表示组成
物质分子中原子的最简整数比,所以不同的化合物可以有相同的最简式。例如苯
和乙炔的最简式均为CH;单烯烃(通式C H )的最简式都为CH 。
n 2n 2
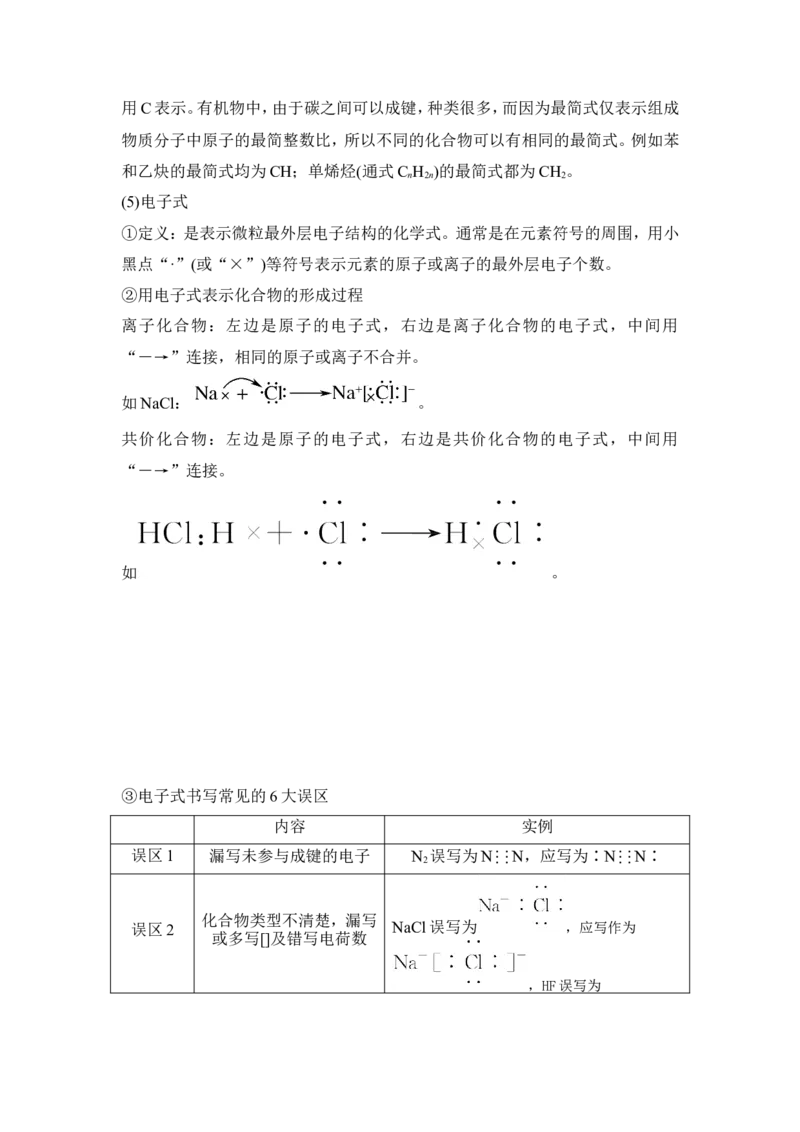
(5)电子式
①定义:是表示微粒最外层电子结构的化学式。通常是在元素符号的周围,用小
黑点“·”(或“×”)等符号表示元素的原子或离子的最外层电子个数。
②用电子式表示化合物的形成过程
离子化合物:左边是原子的电子式,右边是离子化合物的电子式,中间用
“―→”连接,相同的原子或离子不合并。
如NaCl: 。
共价化合物:左边是原子的电子式,右边是共价化合物的电子式,中间用
“―→”连接。
如 。
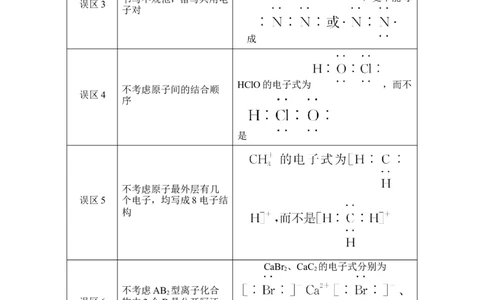
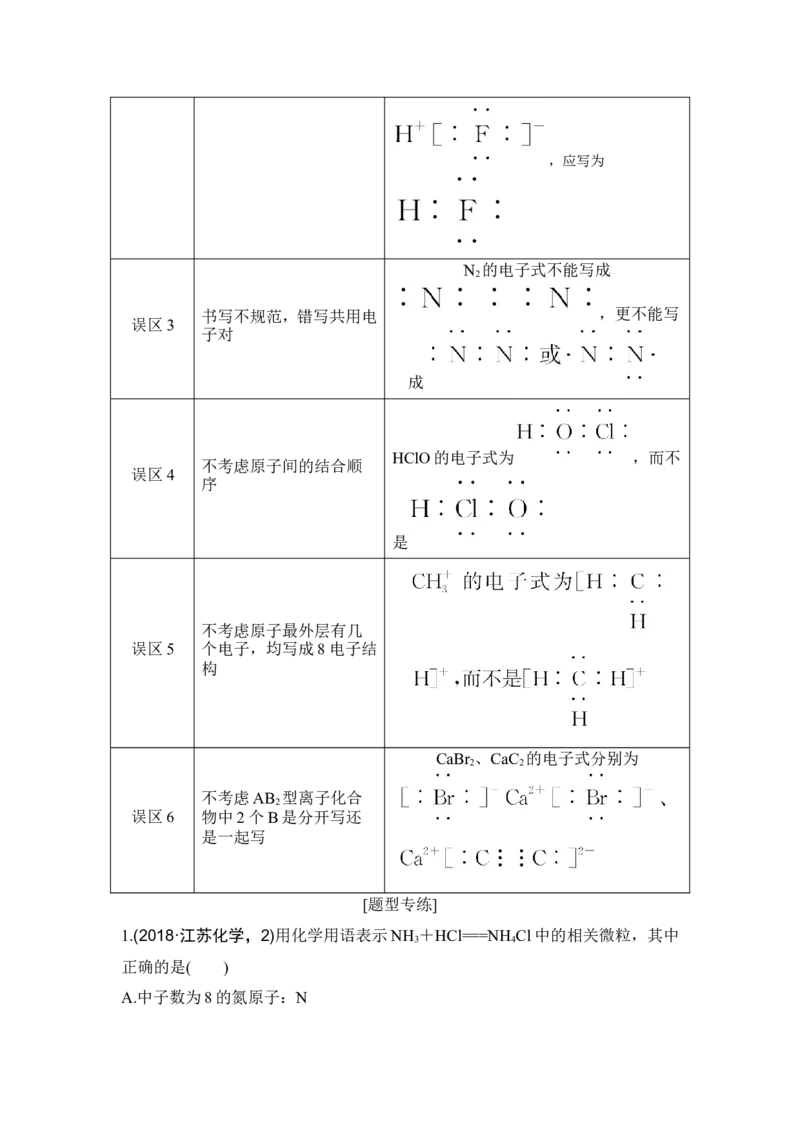
③电子式书写常见的6大误区
内容 实例
误区1 漏写未参与成键的电子 N 误写为N⋮⋮N,应写为∶N⋮⋮N∶
2
化合物类型不清楚,漏写
误区2 NaCl误写为 ,应写作为
或多写[]及错写电荷数
,HF误写为,应写为
N 的电子式不能写成
2
书写不规范,错写共用电 ,更不能写
误区3
子对
成
HClO的电子式为 ,而不
不考虑原子间的结合顺
误区4
序
是
不考虑原子最外层有几
误区5 个电子,均写成8电子结
构
CaBr 、CaC 的电子式分别为
2 2
不考虑AB 型离子化合
2
误区6 物中2个B是分开写还
是一起写
[题型专练]
1.(2018·江苏化学,2)用化学用语表示NH +HCl===NH Cl中的相关微粒,其中
3 4
正确的是( )
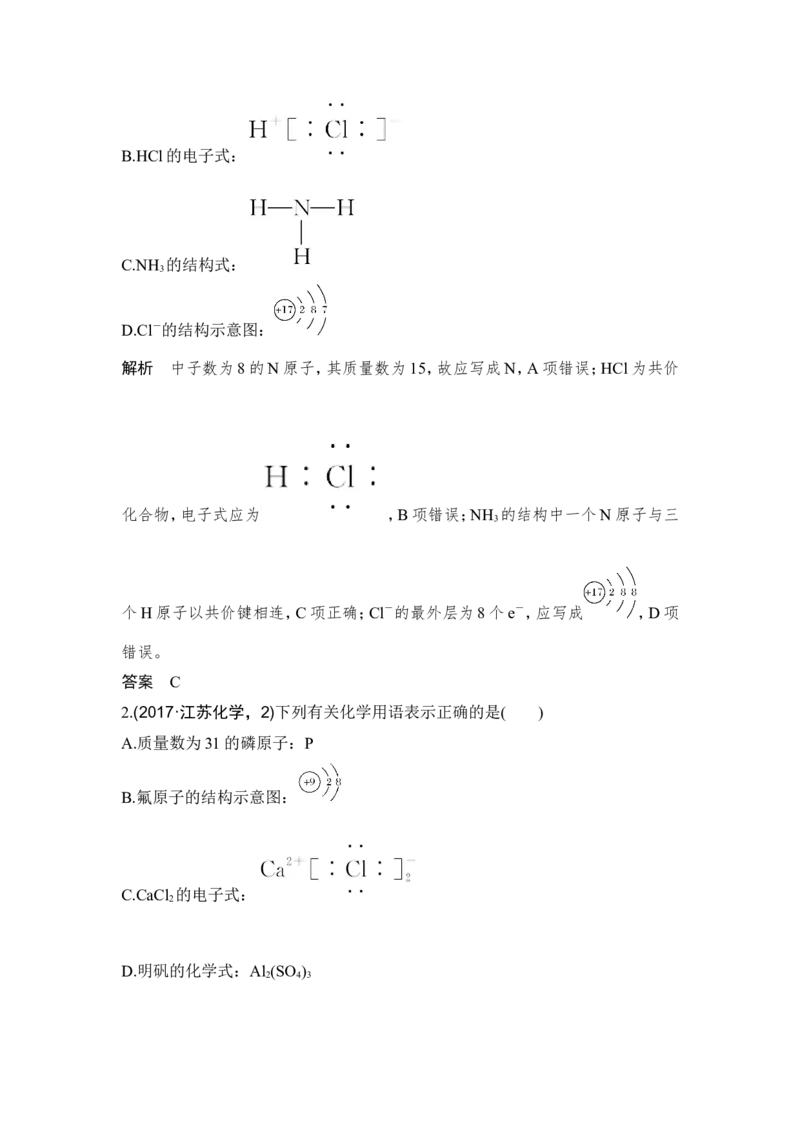
A.中子数为8的氮原子:NB.HCl的电子式:
C.NH 的结构式:
3
D.Cl-的结构示意图:
解析 中子数为8的N原子,其质量数为15,故应写成N,A项错误;HCl为共价
化合物,电子式应为 ,B项错误;NH 的结构中一个N原子与三
3
个H原子以共价键相连,C项正确;Cl-的最外层为8个e-,应写成 ,D项
错误。
答案 C
2.(2017·江苏化学,2)下列有关化学用语表示正确的是( )
A.质量数为31的磷原子:P
B.氟原子的结构示意图:
C.CaCl 的电子式:
2
D.明矾的化学式:Al (SO )
2 4 3解析 B项,氟原子结构示意图为 ,错误;C项,CaCl 的电子式为
2
,错误;D项,明矾化学式
为KAl(SO ) ·12H O,错误。
4 2 2
答案 A
3.写出符合下列要求的电子式:
(1)化合物乙的球棍模型为“ ”,写出乙的电子式:________。
(2)漂白粉是由丙、丁形成的混合物,丙的水溶液显碱性,丙的水溶液中存在酸戊,
戊的电子式为________,丁的水溶液呈中性,丁的电子式为________。
(3)电石(CaC )遇水生成乙炔(C H ),电石的电子式为________;萤石(CaF )可以制
2 2 2 2
备能刻蚀玻璃的酸,写出该酸的电子式:________。
(4)以硼酸为原料可制得硼氢化钠(NaBH ),它是有机合成中的重要还原剂,其电
4
子式为_______________________________________________________________
_____________________________________________________________________
。
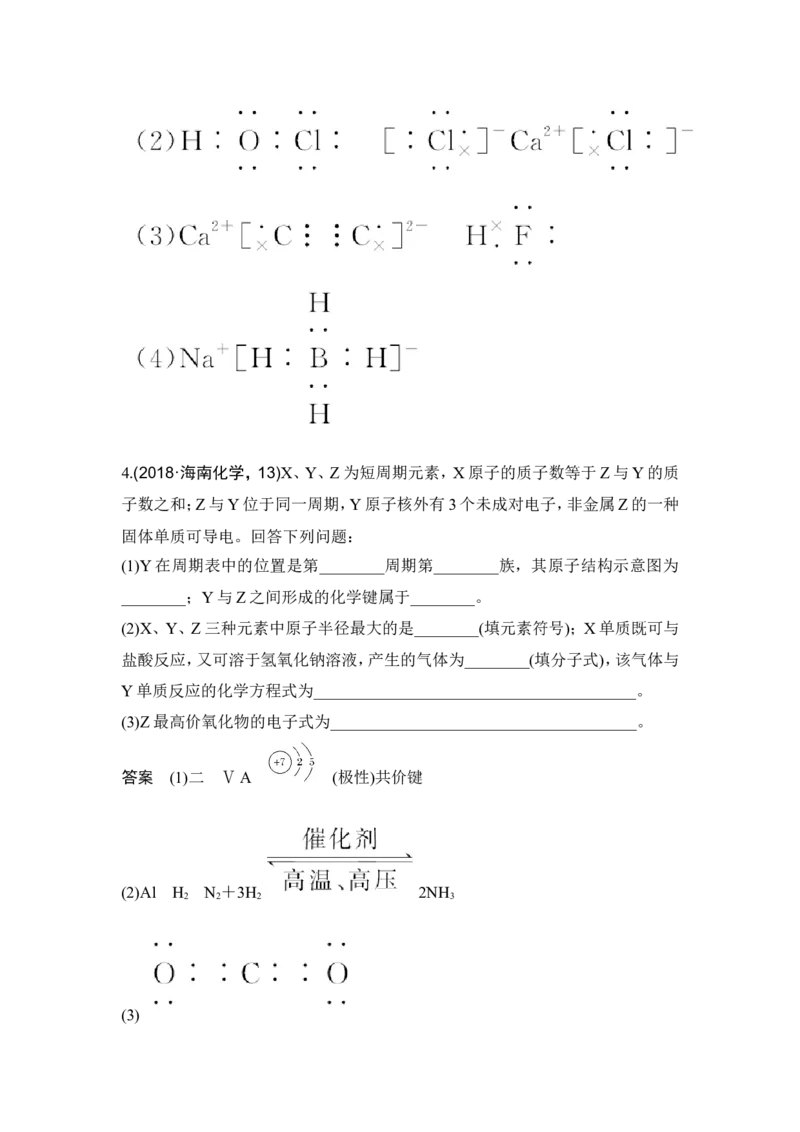
答案 (1)∶N⋮⋮C∶C⋮⋮N∶4.(2018·海南化学,13)X、Y、Z为短周期元素,X原子的质子数等于Z与Y的质
子数之和;Z与Y位于同一周期,Y原子核外有3个未成对电子,非金属Z的一种
固体单质可导电。回答下列问题:
(1)Y在周期表中的位置是第________周期第________族,其原子结构示意图为
________;Y与Z之间形成的化学键属于________。
(2)X、Y、Z三种元素中原子半径最大的是________(填元素符号);X单质既可与
盐酸反应,又可溶于氢氧化钠溶液,产生的气体为________(填分子式),该气体与
Y单质反应的化学方程式为________________________________________。
(3)Z最高价氧化物的电子式为______________________________________。
答案 (1)二 ⅤA (极性)共价键
(2)Al H N +3H 2NH
2 2 2 3
(3)