文档内容
模板 02 工艺流程中陌生方程式的书写
第一步:确定反应物和生 根据题干信息或流程图的入口和出口判断出反应物和生成物。显性
成物 的:直接从题给信息中确定;隐性的:根据反应原理分析确定。
第二步:初步配平 写出已确定的物质的关系式,根据守恒法(电子守恒、质量守恒)进
行配平。
第三步:补充缺失微粒, 依据题给信息(如溶液的酸碱性等)补齐缺失的物质,并配平。若反
并配平 应是在水溶液中惊醒,一般是补齐H+、OH-或HO。
2
第四步:检查验证 检查物质拆分是否正确,电荷、质量是否守恒。
技法01 化工流程中常考试剂的作用
1.氧化剂和还原剂类别 物质 作用
HO 、HNO 、空气、次氯酸盐、
2 2 3
氧化某些还原性物质,便于后续分离,如氧化
氧化剂 KMnO 、
4
Fe2+、Co2+等
MnO 等
2
还原某些氧化性物质,便于后续分离,如还原
还原剂 SO 、NaSO 、I-、金属单质等
2 2 3
Fe3+等
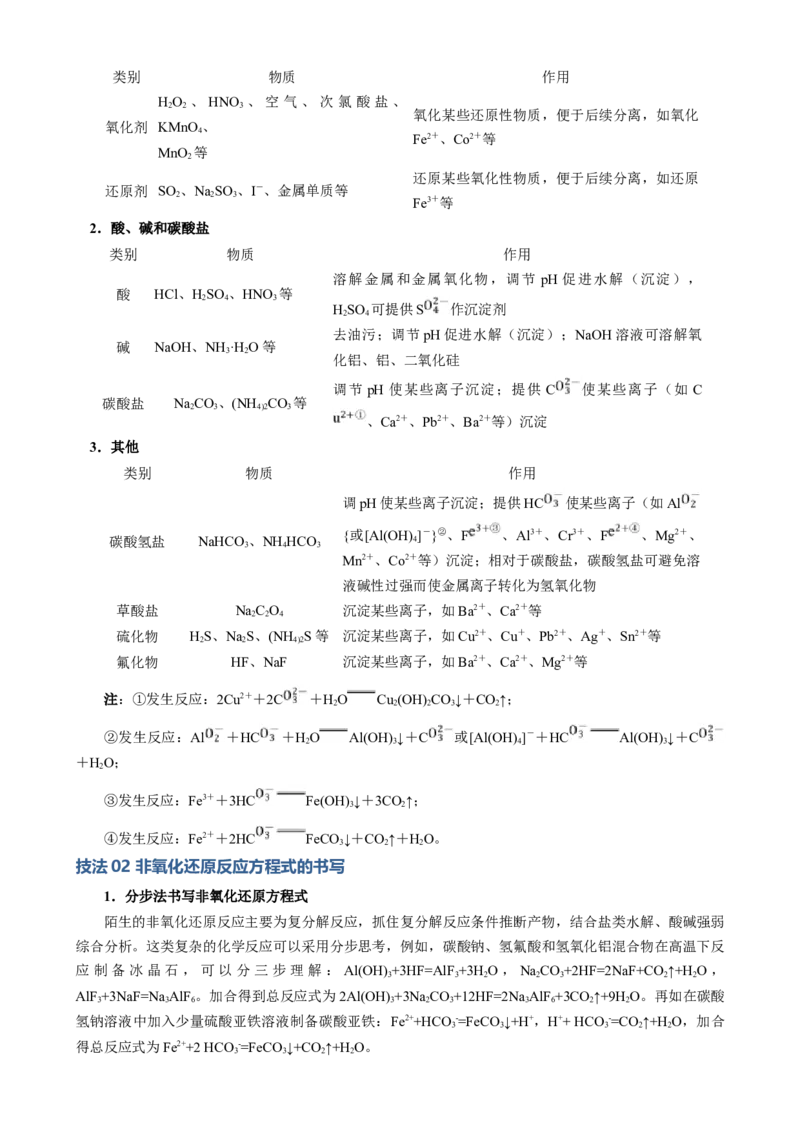
2.酸、碱和碳酸盐
类别 物质 作用
溶解金属和金属氧化物,调节 pH 促进水解(沉淀),
酸 HCl、HSO 、HNO 等
2 4 3
HSO 可提供S 作沉淀剂
2 4
去油污;调节pH促进水解(沉淀);NaOH溶液可溶解氧
碱 NaOH、NH ·H O等
3 2
化铝、铝、二氧化硅
调节 pH 使某些离子沉淀;提供 C 使某些离子(如 C
碳酸盐 NaCO、(NH CO 等
2 3 4)2 3
、Ca2+、Pb2+、Ba2+等)沉淀
3.其他
类别 物质 作用
调pH使某些离子沉淀;提供HC 使某些离子(如Al
{或[Al(OH) ]-}②、F 、Al3+、Cr3+、F 、Mg2+、
碳酸氢盐 NaHCO 、NH HCO 4
3 4 3
Mn2+、Co2+等)沉淀;相对于碳酸盐,碳酸氢盐可避免溶
液碱性过强而使金属离子转化为氢氧化物
草酸盐 NaC O 沉淀某些离子,如Ba2+、Ca2+等
2 2 4
硫化物 HS、NaS、(NH S等 沉淀某些离子,如Cu2+、Cu+、Pb2+、Ag+、Sn2+等
2 2 4)2
氟化物 HF、NaF 沉淀某些离子,如Ba2+、Ca2+、Mg2+等
注:①发生反应:2Cu2++2C +HO Cu (OH) CO↓+CO↑;
2 2 2 3 2
②发生反应:Al +HC +HO Al(OH) ↓+C 或[Al(OH) ]-+HC Al(OH) ↓+C
2 3 4 3
+HO;
2
③发生反应:Fe3++3HC Fe(OH) ↓+3CO↑;
3 2
④发生反应:Fe2++2HC FeCO↓+CO↑+HO。
3 2 2
技法02 非氧化还原反应方程式的书写
1.分步法书写非氧化还原方程式
陌生的非氧化还原反应主要为复分解反应,抓住复分解反应条件推断产物,结合盐类水解、酸碱强弱
综合分析。这类复杂的化学反应可以采用分步思考,例如,碳酸钠、氢氟酸和氢氧化铝混合物在高温下反
应制备冰晶石,可以分三步理解: Al(OH) +3HF=AlF +3H O,NaCO+2HF=2NaF+CO ↑+H O,
3 3 2 2 3 2 2
AlF+3NaF=Na AlF。加合得到总反应式为2Al(OH) +3Na CO+12HF=2Na AlF+3CO ↑+9H O。再如在碳酸
3 3 6 3 2 3 3 6 2 2
氢钠溶液中加入少量硫酸亚铁溶液制备碳酸亚铁:Fe2++HCO-=FeCO ↓+H+,H++ HCO -=CO ↑+H O,加合
3 3 3 2 2
得总反应式为Fe2++2 HCO -=FeCO ↓+CO ↑+H O。
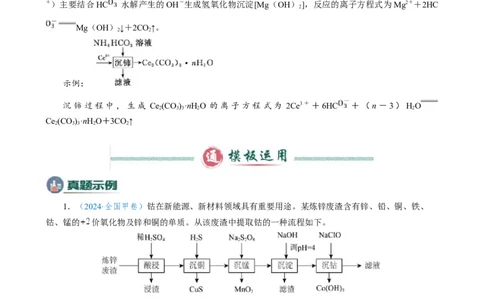
3 3 2 22.工业流程中用HC 沉淀金属阳离子的离子方程式的书写方法
HC 在水溶液中既存在电离平衡又存在水解平衡
HC 的电离平衡:HC H++C
HC 的水解平衡:HC +HO HCO+OH-
2 2 3
(1)若金属阳离子(以Ca2+为例)的K (CaCO )<K [Ca(OH) ],则溶液中的金属阳离子(Ca2
sp 3 sp 2
+)主要结合 HC 电离产生的 C 生成碳酸盐沉淀(CaCO ),反应的离子方程式为 Ca2++2HC
3
CaCO ↓+HO+CO↑。
3 2 2
(2)若金属阳离子(以Mg2+为例)的K (MgCO )>K [Mg(OH) ],则溶液中的金属阳离子(Mg2
sp 3 sp 2
+)主要结合HC 水解产生的OH-生成氢氧化物沉淀[Mg(OH) ],反应的离子方程式为Mg2++2HC
2
Mg(OH)↓+2CO↑。
2 2
示例:
沉铈过程中,生成 Ce (CO)·nHO 的离子方程式为 2Ce3++6HC +(n-3)HO
2 3 3 2 2
Ce (CO)·nHO+3CO↑
2 3 3 2 2
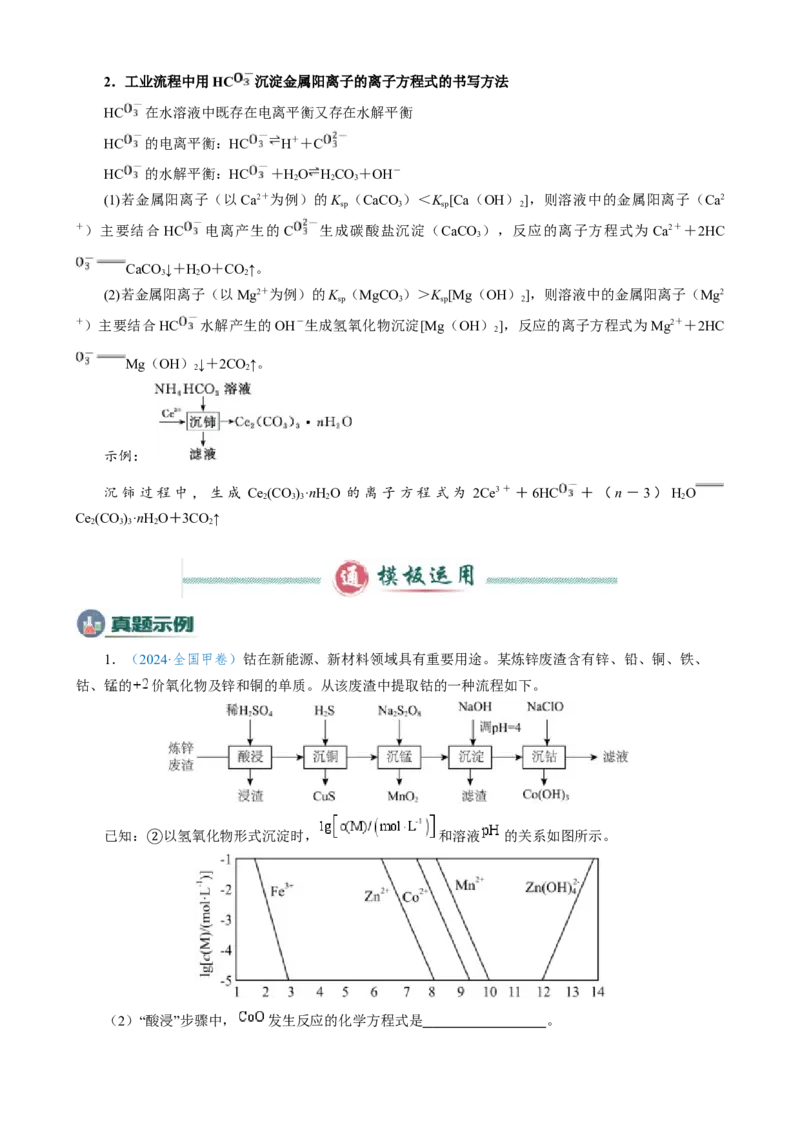
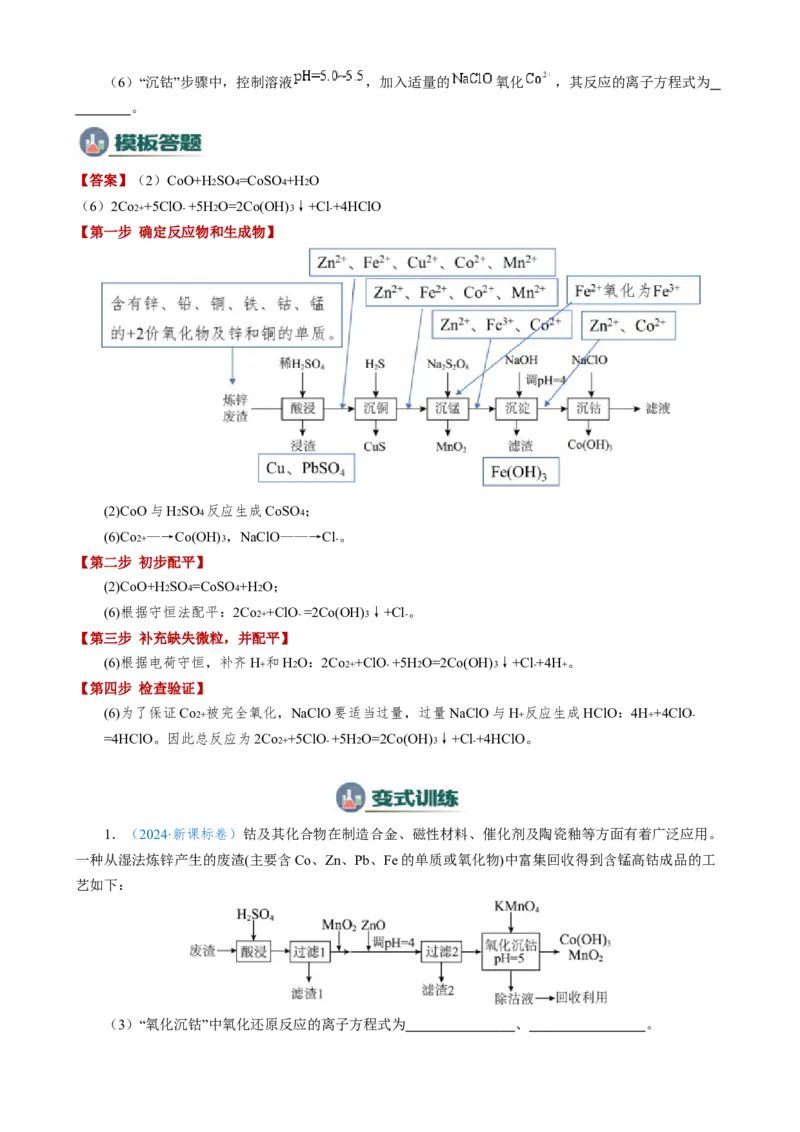
1.(2024·全国甲卷)钴在新能源、新材料领域具有重要用途。某炼锌废渣含有锌、铅、铜、铁、
钴、锰的 价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。
已知: 以氢氧化物形式沉淀时, 和溶液 的关系如图所示。
②
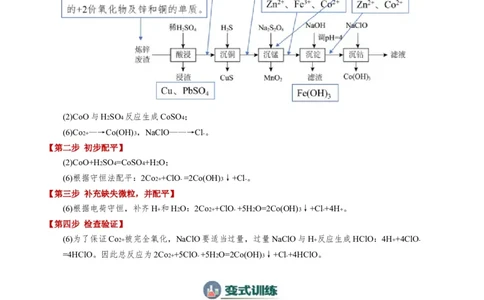
(2)“酸浸”步骤中, 发生反应的化学方程式是 。(6)“沉钴”步骤中,控制溶液 ,加入适量的 氧化 ,其反应的离子方程式为
。
【答案】(2)CoO+H2SO4=CoSO4+H2O
(6)2Co2++5ClO- +5H2O=2Co(OH)3 ↓+Cl-+4HClO
【第一步 确定反应物和生成物】
(2)CoO与H2SO4 反应生成CoSO4 ;
(6)Co2+ —→Co(OH)3 ,NaClO——→Cl- 。
【第二步 初步配平】
(2)CoO+H2SO4=CoSO4+H2O;
(6)根据守恒法配平:2Co2++ClO- =2Co(OH)3 ↓+Cl- 。
【第三步 补充缺失微粒,并配平】
(6)根据电荷守恒,补齐H+ 和H2O:2Co2++ClO- +5H2O=2Co(OH)3 ↓+Cl-+4H+ 。
【第四步 检查验证】
(6)为了保证Co2+ 被完全氧化,NaClO要适当过量,过量NaClO与H+ 反应生成HClO:4H++4ClO-
=4HClO。因此总反应为2Co2++5ClO- +5H2O=2Co(OH)3 ↓+Cl-+4HClO。
1.(2024·新课标卷)钴及其化合物在制造合金、磁性材料、催化剂及陶瓷釉等方面有着广泛应用。
一种从湿法炼锌产生的废渣(主要含Co、Zn、Pb、Fe的单质或氧化物)中富集回收得到含锰高钴成品的工
艺如下:
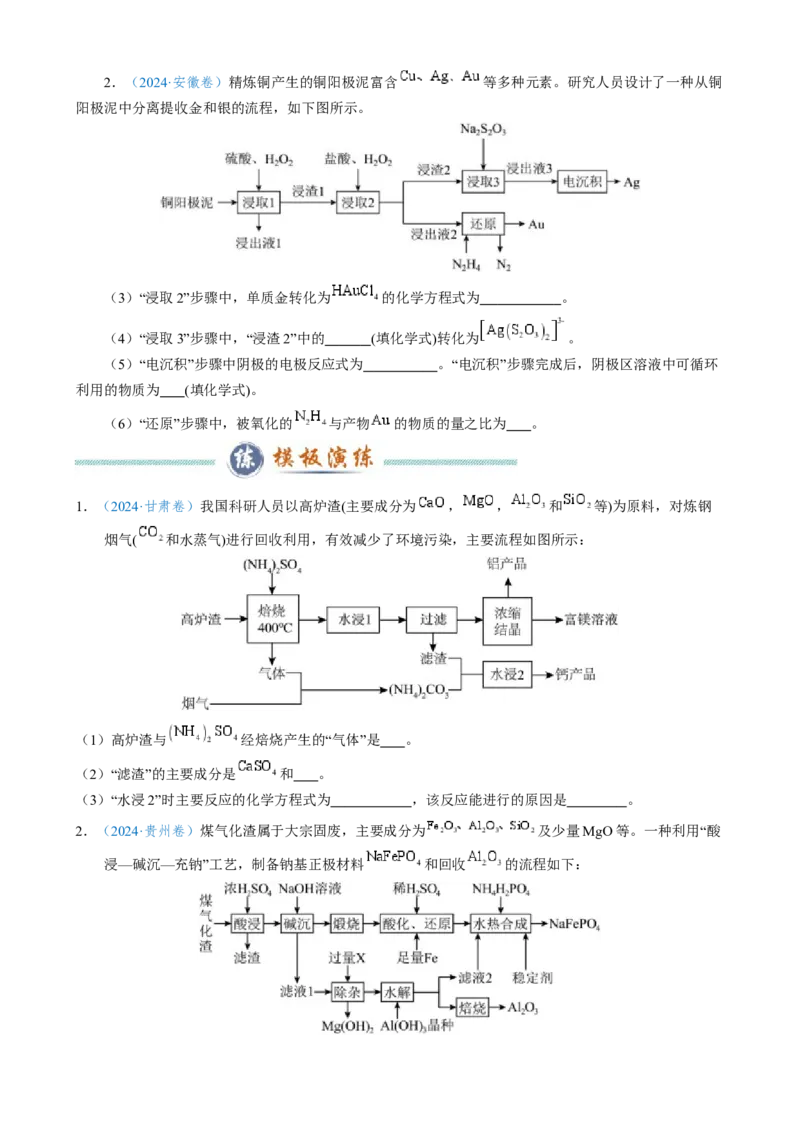
(3)“氧化沉钴”中氧化还原反应的离子方程式为 、 。2.(2024·安徽卷)精炼铜产生的铜阳极泥富含 等多种元素。研究人员设计了一种从铜
阳极泥中分离提收金和银的流程,如下图所示。
(3)“浸取2”步骤中,单质金转化为 的化学方程式为 。
(4)“浸取3”步骤中,“浸渣2”中的 (填化学式)转化为 。
(5)“电沉积”步骤中阴极的电极反应式为 。“电沉积”步骤完成后,阴极区溶液中可循环
利用的物质为 (填化学式)。
(6)“还原”步骤中,被氧化的 与产物 的物质的量之比为 。
1.(2024·甘肃卷)我国科研人员以高炉渣(主要成分为 , , 和 等)为原料,对炼钢
烟气( 和水蒸气)进行回收利用,有效减少了环境污染,主要流程如图所示:
(1)高炉渣与 经焙烧产生的“气体”是 。
(2)“滤渣”的主要成分是 和 。
(3)“水浸2”时主要反应的化学方程式为 ,该反应能进行的原因是 。
2.(2024·贵州卷)煤气化渣属于大宗固废,主要成分为 及少量MgO等。一种利用“酸
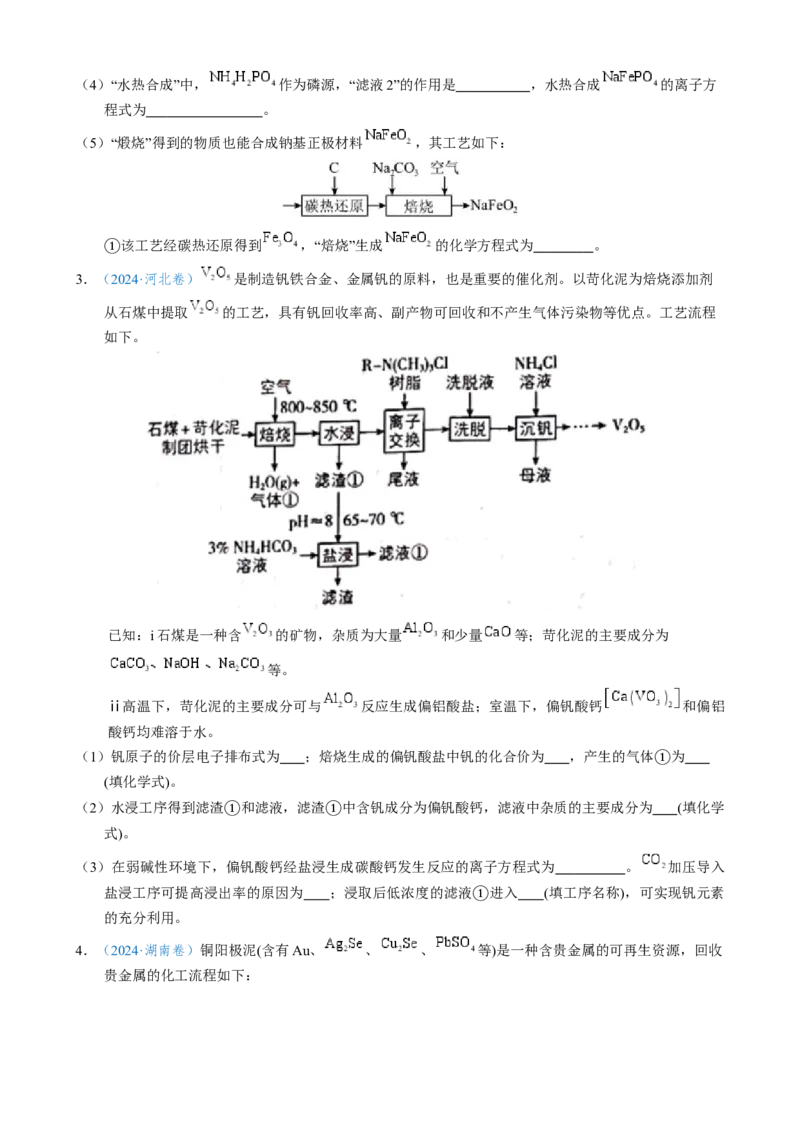
浸—碱沉—充钠”工艺,制备钠基正极材料 和回收 的流程如下:(4)“水热合成”中, 作为磷源,“滤液2”的作用是 ,水热合成 的离子方
程式为 。
(5)“煅烧”得到的物质也能合成钠基正极材料 ,其工艺如下:
该工艺经碳热还原得到 ,“焙烧”生成 的化学方程式为 。
3.(①2024·河北卷) 是制造钒铁合金、金属钒的原料,也是重要的催化剂。以苛化泥为焙烧添加剂
从石煤中提取 的工艺,具有钒回收率高、副产物可回收和不产生气体污染物等优点。工艺流程
如下。
已知:i石煤是一种含 的矿物,杂质为大量 和少量 等;苛化泥的主要成分为
等。
ⅱ高温下,苛化泥的主要成分可与 反应生成偏铝酸盐;室温下,偏钒酸钙 和偏铝
酸钙均难溶于水。
(1)钒原子的价层电子排布式为 ;焙烧生成的偏钒酸盐中钒的化合价为 ,产生的气体 为
(填化学式)。
①
(2)水浸工序得到滤渣 和滤液,滤渣 中含钒成分为偏钒酸钙,滤液中杂质的主要成分为 (填化学
式)。
① ①
(3)在弱碱性环境下,偏钒酸钙经盐浸生成碳酸钙发生反应的离子方程式为 。 加压导入
盐浸工序可提高浸出率的原因为 ;浸取后低浓度的滤液 进入 (填工序名称),可实现钒元素
的充分利用。
①
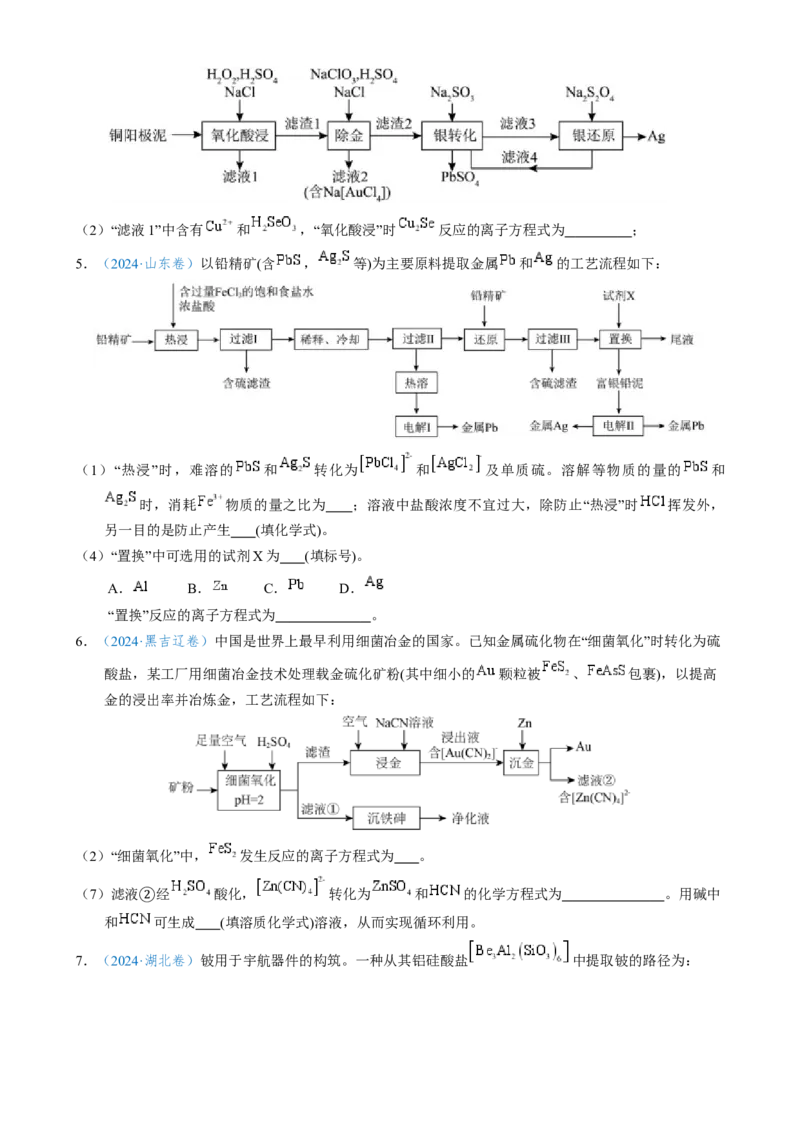
4.(2024·湖南卷)铜阳极泥(含有Au、 、 、 等)是一种含贵金属的可再生资源,回收
贵金属的化工流程如下:(2)“滤液1”中含有 和 ,“氧化酸浸”时 反应的离子方程式为 ;
5.(2024·山东卷)以铅精矿(含 , 等)为主要原料提取金属 和 的工艺流程如下:
(1)“热浸”时,难溶的 和 转化为 和 及单质硫。溶解等物质的量的 和
时,消耗 物质的量之比为 ;溶液中盐酸浓度不宜过大,除防止“热浸”时 挥发外,
另一目的是防止产生 (填化学式)。
(4)“置换”中可选用的试剂X为 (填标号)。
A. B. C. D.
“置换”反应的离子方程式为 。
6.(2024·黑吉辽卷)中国是世界上最早利用细菌冶金的国家。已知金属硫化物在“细菌氧化”时转化为硫
酸盐,某工厂用细菌冶金技术处理载金硫化矿粉(其中细小的 颗粒被 、 包裹),以提高
金的浸出率并冶炼金,工艺流程如下:
(2)“细菌氧化”中, 发生反应的离子方程式为 。
(7)滤液 经 酸化, 转化为 和 的化学方程式为 。用碱中
和
②
可生成 (填溶质化学式)溶液,从而实现循环利用。
7.(2024·湖北卷)铍用于宇航器件的构筑。一种从其铝硅酸盐 中提取铍的路径为:(4)写出反萃取生成 的化学方程式 。“滤液2”可以进入 步骤再利用。
8.以黄铁矿(主要成分是FeS,含少量SiO)和软锰矿(主要成分是MnO ,含少量Fe O、Al O)为原
2 2 2 2 3 2 3
料制备MnSO ·H O的工艺流程如下。回答下列问题:
4 2
(1)“酸浸”过程得到的滤液中含有Mn2+、Fe3+,则该过程中主要反应的离子方程式是
(2)“沉锰”时,Mn2+参与反应的离子方程式是 。
9.钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以
及SiO、Fe O。采用以下工艺流程可由黏土钒矿制备NH VO 。
2 3 4 4 3
“酸浸氧化”中,VO+和VO2+被氧化成V ,同时还有 被氧化,其反应的离子方程式为
。
写出VO+转化为V 反应的离子方程式: 。
10.镍、钴及其化合物在工业上有广泛的应用。以含镍废料(主要成分为NiO,含少量FeO、Fe O 、
2 3
CoO、BaO和SiO)为原料制备NiO 和碳酸钴(CoCO)的工艺流程如图。
2 x y 3(1)“滤渣Ⅰ”的主要成分是 。
(2)“氧化”时反应的离子方程式是 ,为证明添加NaClO 已足量,可用 (写化
3
学式)溶液进行检验。
(3)“调pH”过程中生成黄钠铁钒沉淀,该反应的离子方程式为 。
11.碲( Te)被誉为“国防与尖端技术的维生素”。工业上常以铜阳极泥(主要成分是Cu Te,含Ag、Au
52 2
等杂质)为原料提取碲并回收金属,其工艺流程如图:
已知:TeO 微溶于水,易与较浓的强酸、强碱反应。
2
(1)已知Te为第ⅥA族元素,TeO 被浓NaOH溶液溶解,所生成盐的化学式为 。
2
(2)“酸浸1”过程中,控制溶液的酸度使Cu Te转化为TeO ,反应的化学方程式为 ;“还
2 2
原”过程中,发生反应的离子方程式为 。
12.碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回答下列问题:
以NaIO 为原料制备I 的方法是:先向NaIO 溶液中加入计量的NaHSO ,生成碘化物;再向混合溶
3 2 3 3
液 中 加 入 NaIO 溶 液 , 反 应 得 到 I 。 上 述 制 备 I 的 总 反 应 的 离 子 方 程 式 为
3 2 2
___________________________。
13.以焙烧黄铁矿FeS2(杂质为石英等)产生的红渣为原料制备铵铁蓝Fe(NH4)Fe(CN)6 颜料。工艺流程如
下:
(1)还原工序中,不生成S单质的反应的化学方程式为_______。
(2)沉铁工序产生的白色沉淀Fe(NH4)2Fe(CN)6 中 的化合价为_______,氧化工序发生反应的离子方程式
为____________________________。
14.磁选后的炼铁高钛炉渣,主要成分有TiO 、SiO 、Al O 、MgO、CaO以及少量的Fe O 。为节约和充
2 2 2 3 2 3
分利用资源,通过如下工艺流程回收钛、铝、镁等。该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表
金属离子 Fe3+ Al3+ Mg2+ Ca2+
开始沉淀的pH 2.2 3.5 9.5 12.4
沉淀完全(c=1.0×10-5 mol·L-1)的pH 3.2 4.7 11.1 13.8
回答下列问题:
“焙烧”中,TiO 、SiO 几乎不发生反应,Al O 、 MgO、CaO、 Fe O 转化为相应的硫酸盐。写出
2 2 2 3 2 3
Al O 转化为NH Al(SO ) 的化学方程式:__________________________________。
2 3 4 4 2
15.绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相氧化法制备高价
铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了
Cr—Fe—Al—Mg的深度利用和Na+内循环。工艺流程如图:
(1)工序③中发生反应的离子方程式为_________________________。
(2)物质Ⅴ可代替高温连续氧化工序中的 NaOH,此时发生的主要反应的化学方程式为
__________________,可代替NaOH的化学试剂还有____________(填化学式)。
16.Ce (CO) 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以CePO 形式存在,还含
2 3 3 4
有SiO、Al O、Fe O、CaF 等物质。以独居石为原料制备Ce (CO)·nHO的工艺流程如下:
2 2 3 2 3 2 2 3 3 2(1)“沉铈”过程中,生成Ce (CO)·nHO的离子方程式为_______________________。
2 3 3 2
(2)滤渣Ⅱ的主要成分为 FePO ,在高温条件下,LiCO 、葡萄糖(C H O)和 FePO 可制备电极材料
4 2 3 6 12 6 4
LiFePO ,同时生成CO和HO,该反应的化学方程式为________________________。
4 2
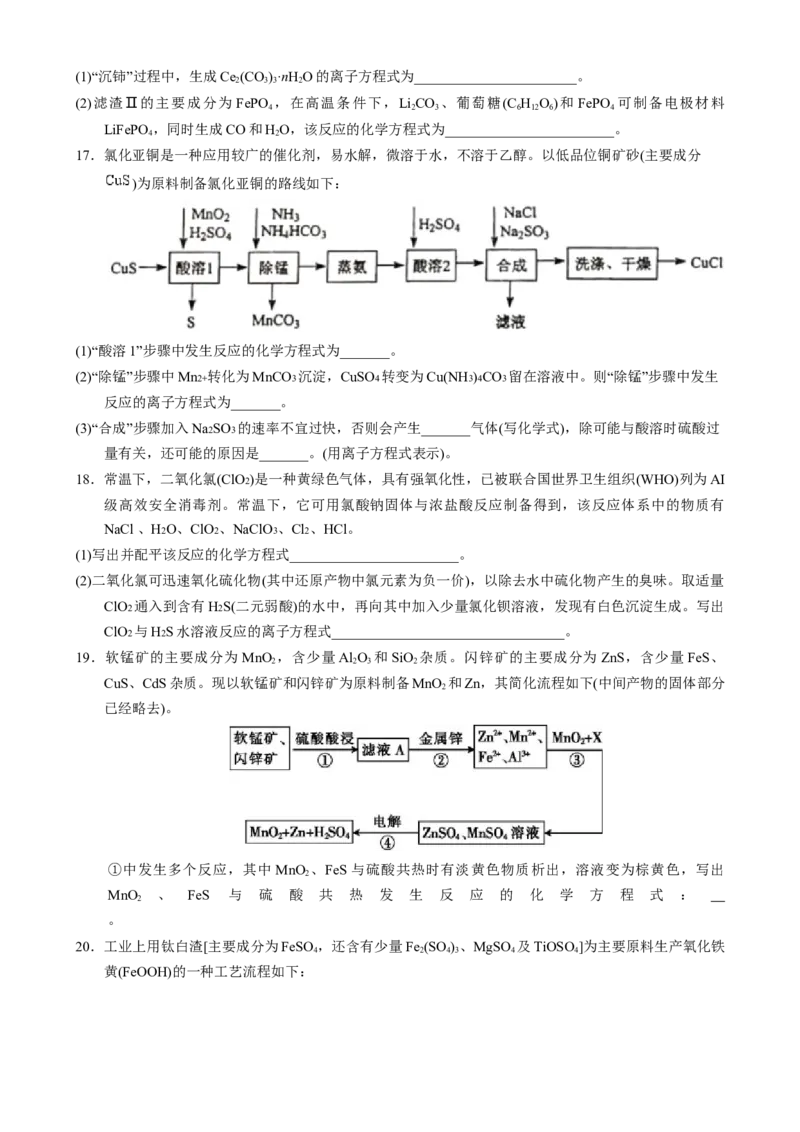
17.氯化亚铜是一种应用较广的催化剂,易水解,微溶于水,不溶于乙醇。以低品位铜矿砂(主要成分
)为原料制备氯化亚铜的路线如下:
(1)“酸溶1”步骤中发生反应的化学方程式为_______。
(2)“除锰”步骤中Mn2+ 转化为MnCO3 沉淀,CuSO4 转变为Cu(NH3)4CO3 留在溶液中。则“除锰”步骤中发生
反应的离子方程式为_______。
(3)“合成”步骤加入Na2SO3 的速率不宜过快,否则会产生_______气体(写化学式),除可能与酸溶时硫酸过
量有关,还可能的原因是_______。(用离子方程式表示)。
18.常温下,二氧化氯(ClO2)是一种黄绿色气体,具有强氧化性,已被联合国世界卫生组织(WHO)列为AI
级高效安全消毒剂。常温下,它可用氯酸钠固体与浓盐酸反应制备得到,该反应体系中的物质有
NaCl 、H2O、ClO2 、NaClO3 、Cl2 、HCl。
(1)写出并配平该反应的化学方程式________________________。
(2)二氧化氯可迅速氧化硫化物(其中还原产物中氯元素为负一价),以除去水中硫化物产生的臭味。取适量
ClO2 通入到含有H2S(二元弱酸)的水中,再向其中加入少量氯化钡溶液,发现有白色沉淀生成。写出
ClO2 与H2S水溶液反应的离子方程式_________________________________。
19.软锰矿的主要成分为 MnO ,含少量Al O 和SiO 杂质。闪锌矿的主要成分为 ZnS,含少量FeS、
2 2 3 2
CuS、CdS杂质。现以软锰矿和闪锌矿为原料制备MnO 和Zn,其简化流程如下(中间产物的固体部分
2
已经略去)。
①中发生多个反应,其中MnO 、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出
2
MnO 、 FeS 与 硫 酸 共 热 发 生 反 应 的 化 学 方 程 式 :
2
。
20.工业上用钛白渣[主要成分为FeSO ,还含有少量Fe (SO ) 、MgSO 及TiOSO]为主要原料生产氧化铁
4 2 4 3 4 4
黄(FeOOH)的一种工艺流程如下:(1)“溶解”时,TiOSO4 发生水解生成难溶于水的H2TiO3 ,反应的化学方程式为_____________。
(2)“氧化”时,Fe2+ 生成FeOOH的离子方程式是___________________________。