文档内容
模板 02 工艺流程中陌生方程式的书写
第一步:确定反应物和生 根据题干信息或流程图的入口和出口判断出反应物和生成物。显性
成物 的:直接从题给信息中确定;隐性的:根据反应原理分析确定。
第二步:初步配平 写出已确定的物质的关系式,根据守恒法(电子守恒、质量守恒)进
行配平。
第三步:补充缺失微粒, 依据题给信息(如溶液的酸碱性等)补齐缺失的物质,并配平。若反
并配平 应是在水溶液中惊醒,一般是补齐H+、OH-或HO。
2
第四步:检查验证 检查物质拆分是否正确,电荷、质量是否守恒。
技法01 化工流程中常考试剂的作用
1.氧化剂和还原剂类别 物质 作用
HO 、HNO 、空气、次氯酸盐、
2 2 3
氧化某些还原性物质,便于后续分离,如氧化
氧化剂 KMnO 、
4
Fe2+、Co2+等
MnO 等
2
还原某些氧化性物质,便于后续分离,如还原
还原剂 SO 、NaSO 、I-、金属单质等
2 2 3
Fe3+等
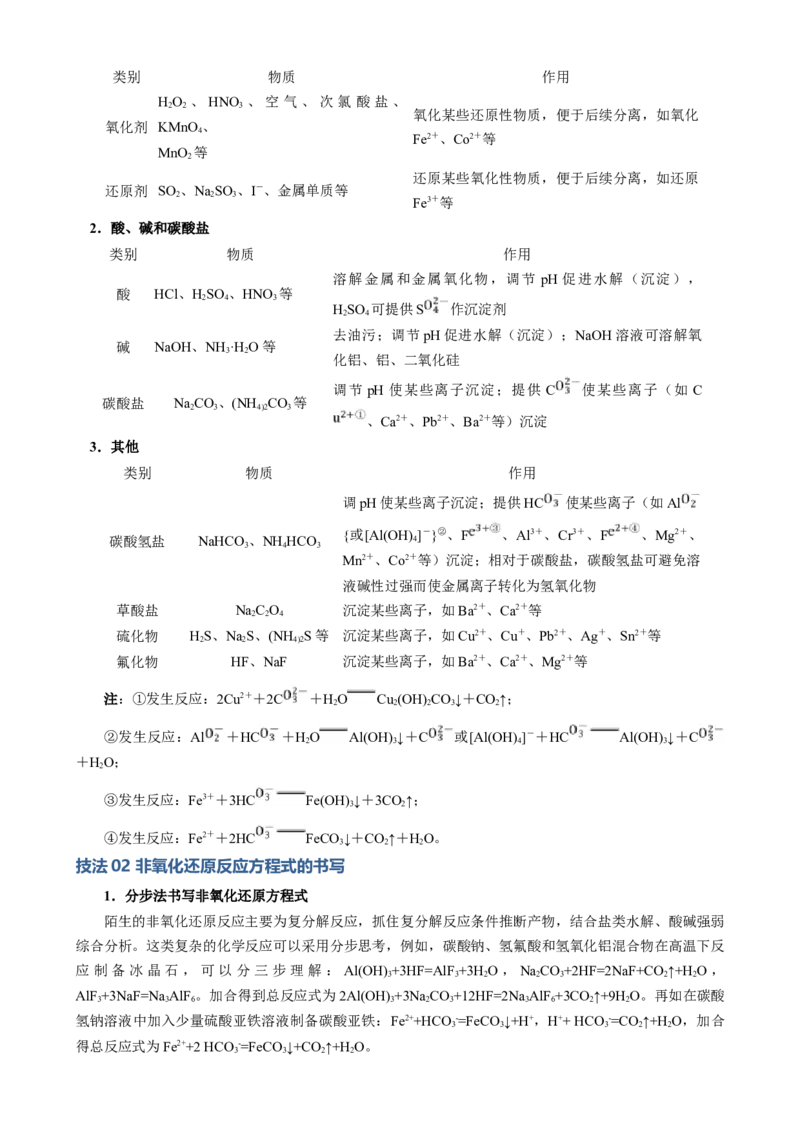
2.酸、碱和碳酸盐
类别 物质 作用
溶解金属和金属氧化物,调节 pH 促进水解(沉淀),
酸 HCl、HSO 、HNO 等
2 4 3
HSO 可提供S 作沉淀剂
2 4
去油污;调节pH促进水解(沉淀);NaOH溶液可溶解氧
碱 NaOH、NH ·H O等
3 2
化铝、铝、二氧化硅
调节 pH 使某些离子沉淀;提供 C 使某些离子(如 C
碳酸盐 NaCO、(NH CO 等
2 3 4)2 3
、Ca2+、Pb2+、Ba2+等)沉淀
3.其他
类别 物质 作用
调pH使某些离子沉淀;提供HC 使某些离子(如Al
{或[Al(OH) ]-}②、F 、Al3+、Cr3+、F 、Mg2+、
碳酸氢盐 NaHCO 、NH HCO 4
3 4 3
Mn2+、Co2+等)沉淀;相对于碳酸盐,碳酸氢盐可避免溶
液碱性过强而使金属离子转化为氢氧化物
草酸盐 NaC O 沉淀某些离子,如Ba2+、Ca2+等
2 2 4
硫化物 HS、NaS、(NH S等 沉淀某些离子,如Cu2+、Cu+、Pb2+、Ag+、Sn2+等
2 2 4)2
氟化物 HF、NaF 沉淀某些离子,如Ba2+、Ca2+、Mg2+等
注:①发生反应:2Cu2++2C +HO Cu (OH) CO↓+CO↑;
2 2 2 3 2
②发生反应:Al +HC +HO Al(OH) ↓+C 或[Al(OH) ]-+HC Al(OH) ↓+C
2 3 4 3
+HO;
2
③发生反应:Fe3++3HC Fe(OH) ↓+3CO↑;
3 2
④发生反应:Fe2++2HC FeCO↓+CO↑+HO。
3 2 2
技法02 非氧化还原反应方程式的书写
1.分步法书写非氧化还原方程式
陌生的非氧化还原反应主要为复分解反应,抓住复分解反应条件推断产物,结合盐类水解、酸碱强弱
综合分析。这类复杂的化学反应可以采用分步思考,例如,碳酸钠、氢氟酸和氢氧化铝混合物在高温下反
应制备冰晶石,可以分三步理解: Al(OH) +3HF=AlF +3H O,NaCO+2HF=2NaF+CO ↑+H O,
3 3 2 2 3 2 2
AlF+3NaF=Na AlF。加合得到总反应式为2Al(OH) +3Na CO+12HF=2Na AlF+3CO ↑+9H O。再如在碳酸
3 3 6 3 2 3 3 6 2 2
氢钠溶液中加入少量硫酸亚铁溶液制备碳酸亚铁:Fe2++HCO-=FeCO ↓+H+,H++ HCO -=CO ↑+H O,加合
3 3 3 2 2
得总反应式为Fe2++2 HCO -=FeCO ↓+CO ↑+H O。
3 3 2 22.工业流程中用HC 沉淀金属阳离子的离子方程式的书写方法
HC 在水溶液中既存在电离平衡又存在水解平衡
HC 的电离平衡:HC H++C
HC 的水解平衡:HC +HO HCO+OH-
2 2 3
(1)若金属阳离子(以Ca2+为例)的K (CaCO )<K [Ca(OH) ],则溶液中的金属阳离子(Ca2
sp 3 sp 2
+)主要结合 HC 电离产生的 C 生成碳酸盐沉淀(CaCO ),反应的离子方程式为 Ca2++2HC
3
CaCO ↓+HO+CO↑。
3 2 2
(2)若金属阳离子(以Mg2+为例)的K (MgCO )>K [Mg(OH) ],则溶液中的金属阳离子(Mg2
sp 3 sp 2
+)主要结合HC 水解产生的OH-生成氢氧化物沉淀[Mg(OH) ],反应的离子方程式为Mg2++2HC
2
Mg(OH)↓+2CO↑。
2 2
示例:
沉铈过程中,生成 Ce (CO)·nHO 的离子方程式为 2Ce3++6HC +(n-3)HO
2 3 3 2 2
Ce (CO)·nHO+3CO↑
2 3 3 2 2
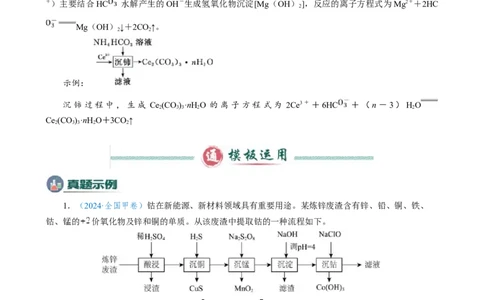
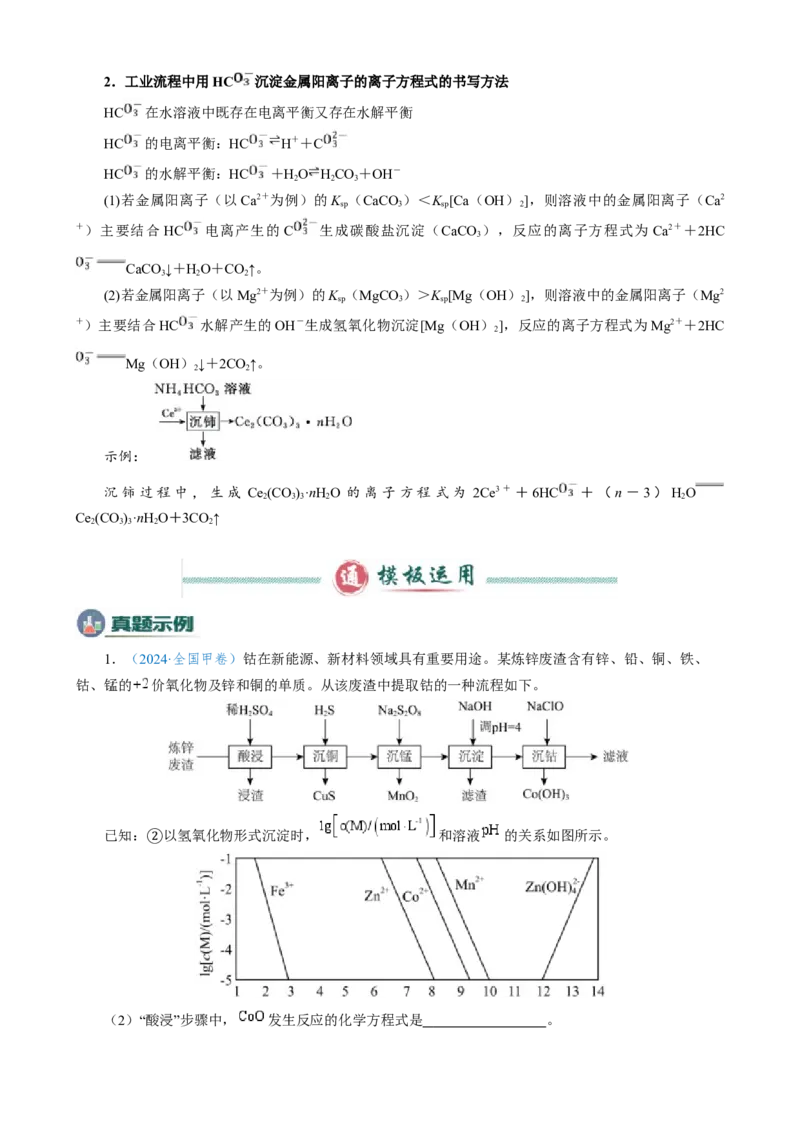
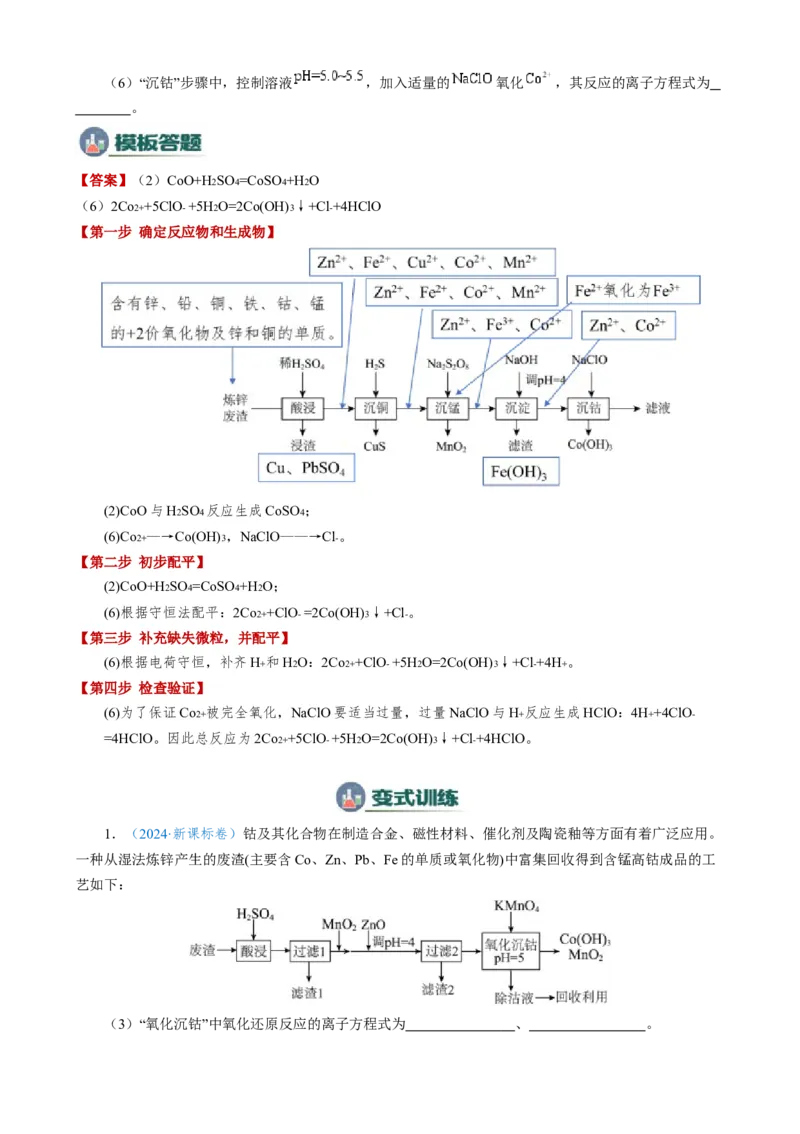
1.(2024·全国甲卷)钴在新能源、新材料领域具有重要用途。某炼锌废渣含有锌、铅、铜、铁、
钴、锰的 价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。
已知: 以氢氧化物形式沉淀时, 和溶液 的关系如图所示。
②
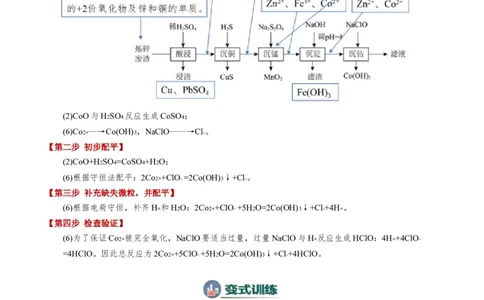
(2)“酸浸”步骤中, 发生反应的化学方程式是 。(6)“沉钴”步骤中,控制溶液 ,加入适量的 氧化 ,其反应的离子方程式为
。
【答案】(2)CoO+H2SO4=CoSO4+H2O
(6)2Co2++5ClO- +5H2O=2Co(OH)3 ↓+Cl-+4HClO
【第一步 确定反应物和生成物】
(2)CoO与H2SO4 反应生成CoSO4 ;
(6)Co2+ —→Co(OH)3 ,NaClO——→Cl- 。
【第二步 初步配平】
(2)CoO+H2SO4=CoSO4+H2O;
(6)根据守恒法配平:2Co2++ClO- =2Co(OH)3 ↓+Cl- 。
【第三步 补充缺失微粒,并配平】
(6)根据电荷守恒,补齐H+ 和H2O:2Co2++ClO- +5H2O=2Co(OH)3 ↓+Cl-+4H+ 。
【第四步 检查验证】
(6)为了保证Co2+ 被完全氧化,NaClO要适当过量,过量NaClO与H+ 反应生成HClO:4H++4ClO-
=4HClO。因此总反应为2Co2++5ClO- +5H2O=2Co(OH)3 ↓+Cl-+4HClO。
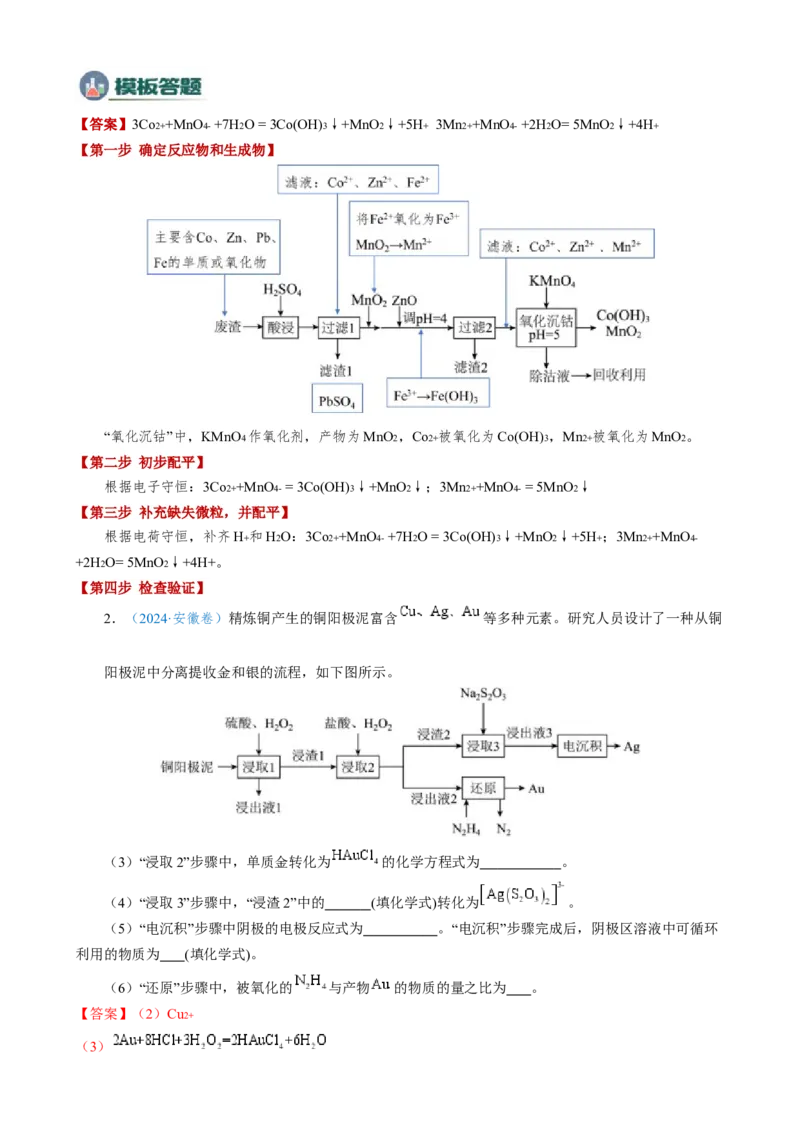
1.(2024·新课标卷)钴及其化合物在制造合金、磁性材料、催化剂及陶瓷釉等方面有着广泛应用。
一种从湿法炼锌产生的废渣(主要含Co、Zn、Pb、Fe的单质或氧化物)中富集回收得到含锰高钴成品的工
艺如下:
(3)“氧化沉钴”中氧化还原反应的离子方程式为 、 。【答案】3Co2++MnO4- +7H2O = 3Co(OH)3 ↓+MnO2 ↓+5H+ 3Mn2++MnO4- +2H2O= 5MnO2 ↓+4H+
【第一步 确定反应物和生成物】
“氧化沉钴”中,KMnO4 作氧化剂,产物为MnO2 ,Co2+ 被氧化为Co(OH)3 ,Mn2+ 被氧化为MnO2 。
【第二步 初步配平】
根据电子守恒:3Co2++MnO4- = 3Co(OH)3 ↓+MnO2 ↓;3Mn2++MnO4- = 5MnO2 ↓
【第三步 补充缺失微粒,并配平】
根据电荷守恒,补齐H+ 和H2O:3Co2++MnO4- +7H2O = 3Co(OH)3 ↓+MnO2 ↓+5H+ ;3Mn2++MnO4-
+2H2O= 5MnO2 ↓+4H+。
【第四步 检查验证】
2.(2024·安徽卷)精炼铜产生的铜阳极泥富含 等多种元素。研究人员设计了一种从铜
阳极泥中分离提收金和银的流程,如下图所示。
(3)“浸取2”步骤中,单质金转化为 的化学方程式为 。
(4)“浸取3”步骤中,“浸渣2”中的 (填化学式)转化为 。
(5)“电沉积”步骤中阴极的电极反应式为 。“电沉积”步骤完成后,阴极区溶液中可循环
利用的物质为 (填化学式)。
(6)“还原”步骤中,被氧化的 与产物 的物质的量之比为 。
【答案】(2)Cu2+
(3)(4)AgCl
(5)
(6)3:4
【解析】(2)由分析可知,铜阳极泥加入硫酸、H2O2 浸取,Cu被转化为Cu2+ 进入浸取液1中,故浸取
液1中含有的金属离子主要是Cu2+ ;
(3)浸取2步骤中,Au与盐酸、H2O2 反应氧化还原反应,生成HAuCl4 和H2O,根据得失电子守恒及质
量守恒,可得反应得化学方程式为: ;
(4)根据分析可知,浸渣2中含有AgCl,与 反应转化为 ;
(5)电沉积步骤中,阴极发生还原反应, 得电子被还原为Ag,电极反应式为:
;阴极反应生成 ,同时阴极区溶液中含有Na+ ,故电沉积步骤完成
后,阴极区溶液中可循环利用得物质为 ;
(6)还原步骤中, HAuCl4 被还原为Au,Au化合价由+3价变为0价,一个HAuCl4 转移3个电子,N2H4
被氧化为N2 ,N的化合价由-2价变为0价,一个N2H4 转移4个电子,根据得失电子守恒,被氧化的N2H4
与产物Au的物质的量之比为3:4。
1.(2024·甘肃卷)我国科研人员以高炉渣(主要成分为 , , 和 等)为原料,对炼钢
烟气( 和水蒸气)进行回收利用,有效减少了环境污染,主要流程如图所示:
(1)高炉渣与 经焙烧产生的“气体”是 。
(2)“滤渣”的主要成分是 和 。
(3)“水浸2”时主要反应的化学方程式为 ,该反应能进行的原因是 。
【答案】【答案】(1)NH3
(2)SiO2
(3)CaSO4+(NH4)2CO3=CaCO3+(NH4)2SO4 Ksp(CaSO4)>Ksp(CaCO3),微溶的硫酸钙转化为更难溶的碳酸
钙
【分析】高炉渣(主要成分为CaO,MgO,Al2O3 和SiO2 等)加入(NH4)2SO4 在400 下焙烧,生成硫酸钙、
硫酸镁、硫酸铝,同时产生气体,该气体与烟气(CO2 和水蒸气)反应,生成(NH4) ℃2CO3 ,所以该气体为
NH3 ;焙烧产物经过水浸1,然后过滤,滤渣为CaSO4 以及未反应的SiO2 ,滤液溶质主要为硫酸镁、硫酸铝及硫酸铵;滤液浓缩结晶,析出 ,剩余富镁溶液;滤渣加入 溶液,滤
渣中的 会转化为更难溶的碳酸钙。
【解析】(1)由分析可知,高炉渣与(NH4)2SO4 经焙烧产生的“气体”是NH3 ;
(2)由分析可知,“滤渣”的主要成分是 和未反应的SiO2 ;
(3)“水浸2”时主要反应为硫酸钙与碳酸铵生成更难溶的碳酸钙,反应方程式为CaSO4+
(NH4)2CO3=CaCO3+(NH4)2SO4 ,该反应之所以能发生,是由于 ,
,Ksp(CaSO4)>Ksp(CaCO3),微溶的硫酸钙转化为更难溶的碳酸钙;
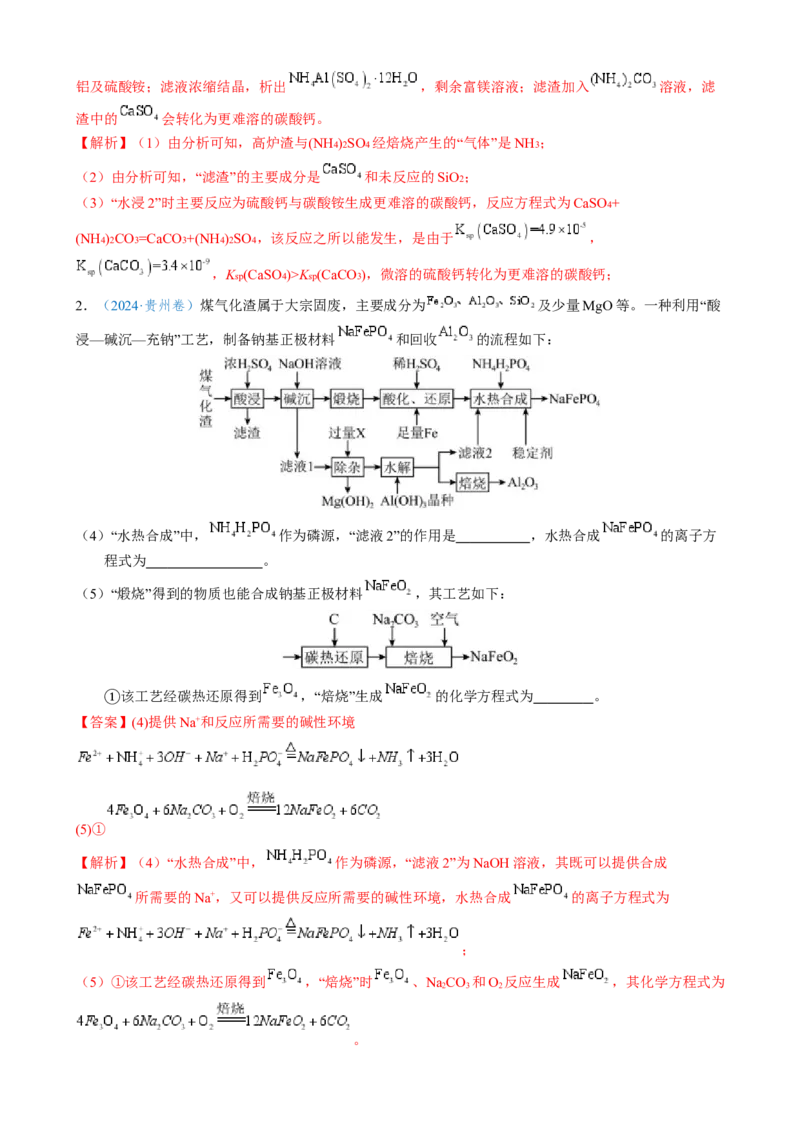
2.(2024·贵州卷)煤气化渣属于大宗固废,主要成分为 及少量MgO等。一种利用“酸
浸—碱沉—充钠”工艺,制备钠基正极材料 和回收 的流程如下:
(4)“水热合成”中, 作为磷源,“滤液2”的作用是 ,水热合成 的离子方
程式为 。
(5)“煅烧”得到的物质也能合成钠基正极材料 ,其工艺如下:
该工艺经碳热还原得到 ,“焙烧”生成 的化学方程式为 。
【答案】(4)提供Na+和反应所需要的碱性环境
①
(5)①
【解析】(4)“水热合成”中, 作为磷源,“滤液2”为NaOH溶液,其既可以提供合成
所需要的Na+,又可以提供反应所需要的碱性环境,水热合成 的离子方程式为
;
(5)①该工艺经碳热还原得到 ,“焙烧”时 、NaCO 和O 反应生成 ,其化学方程式为
2 3 2
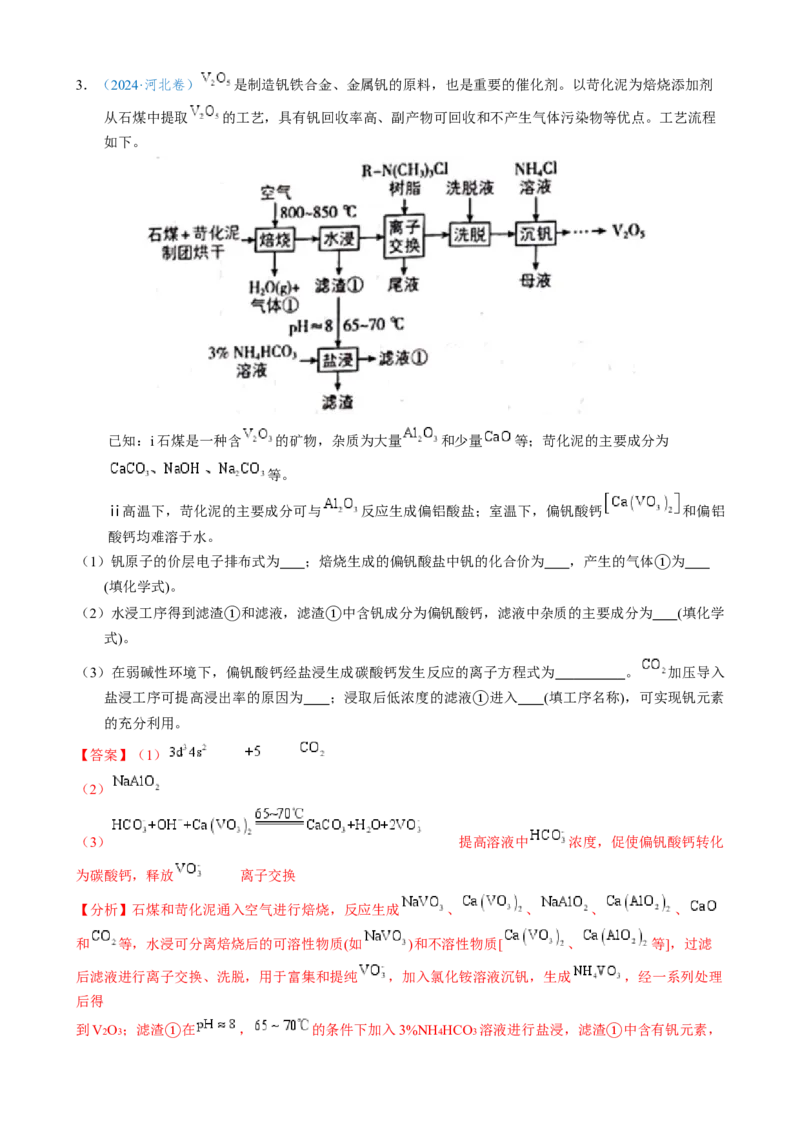
。3.(2024·河北卷) 是制造钒铁合金、金属钒的原料,也是重要的催化剂。以苛化泥为焙烧添加剂
从石煤中提取 的工艺,具有钒回收率高、副产物可回收和不产生气体污染物等优点。工艺流程
如下。
已知:i石煤是一种含 的矿物,杂质为大量 和少量 等;苛化泥的主要成分为
等。
ⅱ高温下,苛化泥的主要成分可与 反应生成偏铝酸盐;室温下,偏钒酸钙 和偏铝
酸钙均难溶于水。
(1)钒原子的价层电子排布式为 ;焙烧生成的偏钒酸盐中钒的化合价为 ,产生的气体 为
(填化学式)。
①
(2)水浸工序得到滤渣 和滤液,滤渣 中含钒成分为偏钒酸钙,滤液中杂质的主要成分为 (填化学
式)。
① ①
(3)在弱碱性环境下,偏钒酸钙经盐浸生成碳酸钙发生反应的离子方程式为 。 加压导入
盐浸工序可提高浸出率的原因为 ;浸取后低浓度的滤液 进入 (填工序名称),可实现钒元素
的充分利用。
①
【答案】(1)
(2)
(3) 提高溶液中 浓度,促使偏钒酸钙转化
为碳酸钙,释放 离子交换
【分析】石煤和苛化泥通入空气进行焙烧,反应生成 、 、 、 、
和 等,水浸可分离焙烧后的可溶性物质(如 )和不溶性物质[ 、 等],过滤
后滤液进行离子交换、洗脱,用于富集和提纯 ,加入氯化铵溶液沉钒,生成 ,经一系列处理
后得
到V2O3 ;滤渣 在 , 的条件下加入3%NH4HCO3 溶液进行盐浸,滤渣 中含有钒元素,
① ①通过盐浸,使滤渣 中的钒元素进入滤液 中,再将滤液 回流到离子交换工序,进行 的富集。
【解析】(1)钒是①23号元素,其价层电子①排布式为 ①;焙烧过程中,氧气被还原, 被氧化生
成 ,偏钒酸盐中钒的化合价为 价; 在 以上开始分解,生成的气体 为 。
(2)由已知信息可知,高温下,苛化泥的主要成分与 反应生成偏铝酸钠和偏铝酸①钙,偏铝酸钠溶
于水,偏铝酸钙难溶于水,所以滤液中杂质的主要成分是 。
(3)在弱碱性环境下, 与 和 反应生成 、 和 ,离子方程式为:
; CO2 加压导入盐浸工序可提高浸出率,因为C可提
高溶液中 浓度,促使偏钒酸钙转化为碳酸钙,释放 ;滤液 中含有 、 等,且浓度较
低,若要利用其中的钒元素,需要通过离子交换进行分离、富集,故滤液 应进入离子交换工序。
①
4.(2024·湖南卷)铜阳极泥(含有Au、 、 、 等)是一种①含贵金属的可再生资源,回收
贵金属的化工流程如下:
(2)“滤液1”中含有 和 ,“氧化酸浸”时 反应的离子方程式为 ;
【答案】(2)
【解析】(2)滤液1中含有Cu2+ 和H2SeO3 ,氧化酸浸时Cu2Se与H2O2 、H2SO4 发生氧化还原反应,生成
、 和 ,反应的离子方程式为: 。
5.(2024·山东卷)以铅精矿(含 , 等)为主要原料提取金属 和 的工艺流程如下:
(1)“热浸”时,难溶的 和 转化为 和 及单质硫。溶解等物质的量的 和
时,消耗 物质的量之比为 ;溶液中盐酸浓度不宜过大,除防止“热浸”时 挥发外,
另一目的是防止产生 (填化学式)。
(4)“置换”中可选用的试剂X为 (填标号)。A. B. C. D.
“置换”反应的离子方程式为 。
【答案】(1)1:1 H2S
(4)C
【解析】(1)“热浸”时, 将 和 中-2价的硫氧化为单质硫, 被还原为Fe2+,在这个过程
中Pb和Ag的化合价保持不变,所以等物质的量的 和 时,S2-物质的量相等,所以消耗 的物
质的量相等,比值为1:1;溶液中盐酸浓度过大,这里主要考虑氢离子浓度会过大,会生成HS 气体。
2
(4)“置换”中加入试剂X可以可以得到富银铅泥,为了防止引入其他杂质,则试剂X应为Pb,发生的反
应为: 。
6.(2024·黑吉辽卷)中国是世界上最早利用细菌冶金的国家。已知金属硫化物在“细菌氧化”时转化为硫
酸盐,某工厂用细菌冶金技术处理载金硫化矿粉(其中细小的 颗粒被 、 包裹),以提高
金的浸出率并冶炼金,工艺流程如下:
(2)“细菌氧化”中, 发生反应的离子方程式为 。
(7)滤液 经 酸化, 转化为 和 的化学方程式为 。用碱中
和
②
可生成 (填溶质化学式)溶液,从而实现循环利用。
【答案】(2)
(7) NaCN
【解析】(2)“细菌氧化”的过程中,FeS2 在酸性环境下被O2 氧化为Fe3+ 和 ,离子方程式为:
;
(7)滤液 含有 ,经过H2SO4 的酸化, 转化为ZnSO4 和HCN,反应得化学方
②
程式为: ;用碱中和HCN得到的产物,可实现循环
利用,即用NaOH中和HCN生成NaCN,NaCN可用于“浸金”步骤,从而循环利用。
7.(2024·湖北卷)铍用于宇航器件的构筑。一种从其铝硅酸盐 中提取铍的路径为:(4)写出反萃取生成 的化学方程式 。“滤液2”可以进入 步骤再利用。
【答案】(4) 反萃取
【解析】(4)反萃取生成 的化学方程式为
,滤液2的主要成分为NaOH,可进入反萃取步骤再利用。
8.以黄铁矿(主要成分是FeS,含少量SiO)和软锰矿(主要成分是MnO ,含少量Fe O、Al O)为原
2 2 2 2 3 2 3
料制备MnSO ·H O的工艺流程如下。回答下列问题:
4 2
(1)“酸浸”过程得到的滤液中含有Mn2+、Fe3+,则该过程中主要反应的离子方程式是
(2)“沉锰”时,Mn2+参与反应的离子方程式是 。
【答案】(1)3MnO +2FeS+12H+ 3Mn2++2Fe3++4S↓+6HO
2 2 2
(2)Mn2++HC +NH ·H O MnCO ↓+N +HO
3 2 3 2
【解析】(1)“酸浸”过程得到的滤液中含有Mn2+、Fe3+,它们是由MnO 和FeS 反应转化而来的,故该
2 2
过程中主要反应的离子方程式是3MnO +2FeS+12H+ 3Mn2++2Fe3++4S↓+6HO。
2 2 2
(2)“沉锰”时,Mn2+参与反应的离子方程式是Mn2++HC +NH ·HO MnCO ↓+N +HO。
3 2 3 2
9.钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以
及SiO、Fe O。采用以下工艺流程可由黏土钒矿制备NH VO 。
2 3 4 4 3
“酸浸氧化”中,VO+和VO2+被氧化成V ,同时还有 被氧化,其反应的离子方程式为。
写出VO+转化为V 反应的离子方程式: 。
【答案】Fe2+ MnO +2Fe2++4H+ Mn2++2Fe3++2HO VO++MnO +2H+ V +Mn2++HO
2 2 2 2
【解析】“酸浸氧化”中,钒矿粉中的Fe O 与硫酸反应生成FeSO 、Fe (SO ) 和水,MnO 具有氧化性,
3 4 4 2 4 3 2
Fe2+具有还原性,则VO+和VO2+被氧化成V 的同时还有Fe2+被氧化成Fe3+,离子方程式为MnO +
2
2Fe2++4H+ Mn2++2Fe3++2HO。
2
VO+转化为V 时,钒元素的化合价由+3价升至+5价,1 mol VO+失去2 mol电子,MnO 被还原为
2
Mn2+,Mn元素的化合价由+4价降至+2价,1 mol MnO 得到2 mol电子,根据得失电子守恒、质量守恒
2
和电荷守恒,再根据书写陌生氧化还原反应方程式的流程,可得VO+转化为V 反应的离子方程式为
VO++MnO +2H+ V +Mn2++HO。
2 2
10.镍、钴及其化合物在工业上有广泛的应用。以含镍废料(主要成分为NiO,含少量FeO、Fe O 、
2 3
CoO、BaO和SiO)为原料制备NiO 和碳酸钴(CoCO)的工艺流程如图。
2 x y 3
(1)“滤渣Ⅰ”的主要成分是 。
(2)“氧化”时反应的离子方程式是 ,为证明添加NaClO 已足量,可用 (写化
3
学式)溶液进行检验。
(3)“调pH”过程中生成黄钠铁钒沉淀,该反应的离子方程式为 。
【答案】(1)SiO、BaSO
2 4
(2)6Fe2++6H++Cl 6Fe3++Cl-+3HO K[Fe(CN)]
2 3 6
(3)3Fe3++Na++2S +3HO+3C NaFe (SO )(OH)↓+3CO↑
2 3 4 2 6 2
【解析】(1)含镍废料的主要成分为NiO,含少量FeO、Fe O 、CoO、BaO和SiO ,加入硫酸“酸浸”,
2 3 2
SiO 不与稀硫酸反应,所以会出现在“滤渣Ⅰ”中,BaO与稀硫酸反应最终变成BaSO 沉淀,所以也会出现
2 4
在“滤渣Ⅰ”中。(2)“氧化”步骤的目的是将二价铁转变成三价铁,便于在后续步骤中通过沉淀法除去,
所以离子方程式为6Fe2++6H++Cl 6Fe3++Cl-+3HO;为证明添加NaClO 已足量,可检验溶液
2 3
中是否含有Fe2+,可用K[Fe(CN) ]溶液进行检验。(3)根据黄钠铁钒渣的化学式以及调节pH时所加
3 6
入的物质,结合原子守恒、电荷守恒,可知“调pH”过程中生成黄钠铁钒沉淀的离子方程式为3Fe3++Na+
+2S +3HO+3C NaFe (SO )(OH)↓+3CO↑。
2 3 4 2 6 2
11.碲( Te)被誉为“国防与尖端技术的维生素”。工业上常以铜阳极泥(主要成分是Cu Te,含Ag、Au
52 2
等杂质)为原料提取碲并回收金属,其工艺流程如图:已知:TeO 微溶于水,易与较浓的强酸、强碱反应。
2
(1)已知Te为第ⅥA族元素,TeO 被浓NaOH溶液溶解,所生成盐的化学式为 。
2
(2)“酸浸1”过程中,控制溶液的酸度使Cu Te转化为TeO ,反应的化学方程式为 ;“还
2 2
原”过程中,发生反应的离子方程式为 。
【答案】(1)NaTeO
2 3
(2)Cu Te+2O+2HSO 2CuSO +TeO +2HO Te4++2SO +4HO 2S +Te↓+8H+
2 2 2 4 4 2 2 2 2
【解析】(1)Te与S同主族,SO 与氢氧化钠反应生成NaSO ,所以TeO 与浓NaOH溶液反应生成盐的
2 2 3 2
化学式为NaTeO 。(2)“酸浸1”过程中,控制溶液的酸度使Cu Te与氧气、硫酸反应生成硫酸铜和
2 3 2
TeO ,
2
反应的化学方程式是Cu Te+2O +2HSO 2CuSO +TeO +2HO;“还原”过程中,四氯化碲与二氧化
2 2 2 4 4 2 2
硫反应生成单质碲和硫酸,反应的离子方程式是Te4++2SO +4HO 2S +Te↓+8H+。
2 2
12.碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回答下列问题:
以NaIO 为原料制备I 的方法是:先向NaIO 溶液中加入计量的NaHSO ,生成碘化物;再向混合溶
3 2 3 3
液 中 加 入 NaIO 溶 液 , 反 应 得 到 I 。 上 述 制 备 I 的 总 反 应 的 离 子 方 程 式 为
3 2 2
___________________________。
【答案】2IO +5HSO ===I +5SO +3H++HO
2 2
【解析】先向NaIO 溶液中加入计量的NaHSO ,生成碘化物即含I-的物质;再向混合溶液(含I-)中加入
3 3
NaIO 溶液,反应得到I ,上述制备I 的两个反应中I-为中间产物,总反应为IO 与HSO 发生氧化还原
3 2 2
反应,生成SO 和I ,根据得失电子守恒、电荷守恒及原子守恒配平离子方程式即可得:2IO +5HSO
2
===I +5SO +3H++HO。
2 2
13.以焙烧黄铁矿FeS2(杂质为石英等)产生的红渣为原料制备铵铁蓝Fe(NH4)Fe(CN)6 颜料。工艺流程如
下:
(1)还原工序中,不生成S单质的反应的化学方程式为_______。
(2)沉铁工序产生的白色沉淀Fe(NH4)2Fe(CN)6 中 的化合价为_______,氧化工序发生反应的离子方程式
为____________________________。
【答案】(1)7Fe2(SO4)3+FeS2+8H2O=15FeSO4+8H2SO4(2) +2 Fe(NH4)2Fe(CN)6+ClO-+2H+=Fe(NH4)Fe(CN)6+H2O+Cl-+NH4+
【解析】(1)还原工序中,不产生S单质沉淀,则硫元素被氧化为SO42- ,反应原理为:14Fe3+
+FeS2+8H2O=15Fe2++2 SO42-+16H+ ,故化学方程式为:7Fe2(SO4)3+FeS2+8H2O=15FeSO4+8H2SO4 ;(2)沉铁
工序中产生的白色沉淀Fe(NH4)2Fe(CN)6 中Fe的化合价为+2价和[Fe(CN)6]4- 中的+3价,由分析可知,氧化
工序所发生的离子方程式为:6Fe(NH4)2Fe(CN)6+ ClO3- +6H+=6Fe(NH4)Fe(CN)6+3H2O+Cl-+6 NH4+ 。
14.磁选后的炼铁高钛炉渣,主要成分有TiO 、SiO 、Al O 、MgO、CaO以及少量的Fe O 。为节约和充
2 2 2 3 2 3
分利用资源,通过如下工艺流程回收钛、铝、镁等。
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表
金属离子 Fe3+ Al3+ Mg2+ Ca2+
开始沉淀的pH 2.2 3.5 9.5 12.4
沉淀完全(c=1.0×10-5 mol·L-1)的pH 3.2 4.7 11.1 13.8
回答下列问题:
“焙烧”中,TiO 、SiO 几乎不发生反应,Al O 、 MgO、CaO、 Fe O 转化为相应的硫酸盐。写出
2 2 2 3 2 3
Al O 转化为NH Al(SO ) 的化学方程式:__________________________________。
2 3 4 4 2
【答案】Al O+4(NH )SO 2NH Al(SO )+6NH ↑+3HO↑
2 3 4 2 4 4 4 2 3 2
【解析】氧化铝转化为硫酸铝铵发生的反应为氧化铝、硫酸铵在高温条件下反应生成硫酸铝铵、氨气和
水,反应的化学方程式为Al O+4(NH )SO 2NH Al(SO )+6NH ↑+3HO↑。
2 3 4 2 4 4 4 2 3 2
15.绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相氧化法制备高价
铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了
Cr—Fe—Al—Mg的深度利用和Na+内循环。工艺流程如图:
(1)工序③中发生反应的离子方程式为_________________________。(2)物质Ⅴ可代替高温连续氧化工序中的 NaOH,此时发生的主要反应的化学方程式为
__________________,可代替NaOH的化学试剂还有____________(填化学式)。
【答案】(1)2Na++2CrO +2CO+HO===Cr O +2NaHCO ↓
2 2 2 3
(2)4Fe(CrO )+7O+16NaHCO 8NaCrO+2Fe O+16CO+8HO NaCO
2 2 2 3 2 4 2 3 2 2 2 3
【解析】(1)工序③中发生的反应为铬酸钠溶液与过量的二氧化碳反应生成重铬酸钠和碳酸氢钠沉淀,反
应的离子方程式为2Na++2CrO +2CO+HO===Cr O +2NaHCO ↓。
2 2 2 3
(2)碳酸氢钠代替高温连续氧化工序中的氢氧化钠发生的主要反应为高温下Fe(CrO ) 与氧气和碳酸氢钠反
2 2
应生成铬酸钠、氧化铁、二氧化碳和水,反应的化学方程式为 4Fe(CrO ) +7O +16NaHCO
2 2 2 3
8NaCrO+2Fe O+16CO+8HO;若将碳酸氢钠换为碳酸钠也能发生类似的反应。
2 4 2 3 2 2
16.Ce (CO) 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以CePO 形式存在,还含
2 3 3 4
有SiO、Al O、Fe O、CaF 等物质。以独居石为原料制备Ce (CO)·nHO的工艺流程如下:
2 2 3 2 3 2 2 3 3 2
(1)“沉铈”过程中,生成Ce (CO)·nHO的离子方程式为_______________________。
2 3 3 2
(2)滤渣Ⅱ的主要成分为 FePO ,在高温条件下,LiCO 、葡萄糖(C H O)和 FePO 可制备电极材料
4 2 3 6 12 6 4
LiFePO ,同时生成CO和HO,该反应的化学方程式为________________________。
4 2
【答案】(1)6HCO +2Ce3++(n-3)H O===Ce (CO)·nHO+3CO↑
2 2 3 3 2 2
(2)6FePO +3LiCO+C H O 9CO↑+6HO↑+6LiFePO
4 2 3 6 12 6 2 4
【解析】(1)用碳酸氢铵“沉铈”,则结合原子守恒、电荷守恒可知,生成Ce (CO)·nHO的离子方程式为
2 3 3 2
6HCO +2Ce3++(n-3)H O===Ce (CO)·nHO+3CO↑。
2 2 3 3 2 2
(2)由在高温条件下,LiCO 、葡萄糖(C H O)和FePO 可制备电极材料LiFePO ,同时生成CO和HO可
2 3 6 12 6 4 4 2
知,该反应中Fe价态降低,C价态部分降低、部分升高,结合得失电子守恒、原子守恒可知该反应的化
学方程式为6FePO +3LiCO+C H O 9CO↑+6HO↑+6LiFePO 。
4 2 3 6 12 6 2 4
17.氯化亚铜是一种应用较广的催化剂,易水解,微溶于水,不溶于乙醇。以低品位铜矿砂(主要成分
)为原料制备氯化亚铜的路线如下:(1)“酸溶1”步骤中发生反应的化学方程式为_______。
(2)“除锰”步骤中Mn2+ 转化为MnCO3 沉淀,CuSO4 转变为Cu(NH3)4CO3 留在溶液中。则“除锰”步骤中发生
反应的离子方程式为_______。
(3)“合成”步骤加入Na2SO3 的速率不宜过快,否则会产生_______气体(写化学式),除可能与酸溶时硫酸过
量有关,还可能的原因是_______。(用离子方程式表示)。
【答案】(1)CuS+MnO2+2H2SO4=CuSO4+MnSO4+S+2H2O
(2)Mn2++2HCO3-=MnCO3↓+CO2↑+H2O
(3)SO2 2Cu2++2Cl-+ SO32-+H2O=2CuCl↓+ SO42-+2H+
【解析】(1)酸溶1步骤中加入硫酸、MnO2 得到S,除锰步骤Mn2+ 转化成MnCO3 沉淀,可知二氧化锰将
CuS中-2价的S氧化为硫单质,则加入硫酸生成硫酸铜、硫酸锰以及S,反应的化学方程式为
CuS+MnO2+2H2SO4=CuSO4+MnSO4+S+2H2O。(2)“除锰”步骤中Mn2+ 转化为MnCO3 沉淀,则“除锰”步骤中
发生反应的离子方程式为Mn2++2HCO3-=MnCO3↓+CO2↑+H2O。(3)若加入Na2SO3 的速率过快,则Na2SO3
会与酸反应产生SO2 气体,硫酸铜和氯化钠和亚硫酸钠和水反应生成氯化亚铜沉淀和硫酸钠和硫酸,若加
入较快会生成更多的酸,离子方程式为:Cu2++2Cl-+ SO32-+H2O=2CuCl↓+ SO42-+2H+ 。
18.常温下,二氧化氯(ClO2)是一种黄绿色气体,具有强氧化性,已被联合国世界卫生组织(WHO)列为AI
级高效安全消毒剂。常温下,它可用氯酸钠固体与浓盐酸反应制备得到,该反应体系中的物质有
NaCl 、H2O、ClO2 、NaClO3 、Cl2 、HCl。
(1)写出并配平该反应的化学方程式________________________。
(2)二氧化氯可迅速氧化硫化物(其中还原产物中氯元素为负一价),以除去水中硫化物产生的臭味。取适量
ClO2 通入到含有H2S(二元弱酸)的水中,再向其中加入少量氯化钡溶液,发现有白色沉淀生成。写出
ClO2 与H2S水溶液反应的离子方程式_________________________________。
【答案】(1)2NaClO3 + 4HCl(浓)= 2ClO2↑ + Cl2↑ + 2H2O + 2NaCl
(2)5H2S + 8ClO2 + 4H2O = 5SO42- + 8Cl- + 18H+
【解析】(1)氯酸钠具有强氧化性,浓盐酸具有还原性,氯酸钠固体与浓盐酸发生氧化还原反应生成二氧
化氯、氯气、氯化钠和水,反应的化学方程式为2NaClO3 + 4HCl(浓)= 2ClO2↑ + Cl2↑ + 2H2O + 2NaCl;(2)
由题意可知,ClO2 与H2S水溶液发生氧化还原反应生成盐酸和硫酸,根据得失电子守恒、原子守恒和电
荷守恒配平,反应的离子方程式为H2S + 8ClO2 + 4H2O = 5SO42-+ 8Cl-+ 18H+ 。
19.软锰矿的主要成分为 MnO ,含少量Al O 和SiO 杂质。闪锌矿的主要成分为 ZnS,含少量FeS、
2 2 3 2
CuS、CdS杂质。现以软锰矿和闪锌矿为原料制备MnO 和Zn,其简化流程如下(中间产物的固体部分
2
已经略去)。
①中发生多个反应,其中MnO 、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出
2
MnO 、
2
FeS与硫酸共热发生反应的化学方程式: 。【答案】3MnO +2FeS+6H SO Fe (SO )+3MnSO +2S+6H O
2 2 4 2 4 3 4 2
【解析】①中MnO 、FeS与硫酸共热时有淡黄色的S单质析出,溶液变为棕黄色,说明有Fe3+生成。
2
20.工业上用钛白渣[主要成分为FeSO ,还含有少量Fe (SO ) 、MgSO 及TiOSO]为主要原料生产氧化铁
4 2 4 3 4 4
黄(FeOOH)的一种工艺流程如下:
(1)“溶解”时,TiOSO4 发生水解生成难溶于水的H2TiO3 ,反应的化学方程式为_____________。
(2)“氧化”时,Fe2+ 生成FeOOH的离子方程式是___________________________。
【答案】(1)TiOSO4 +2H2O=H2TiO3↓+H2SO4
(2)4Fe2+ +O2 +8OH-=4FeOOH↓+2H2O
【解析】(1)TiOSO4 水解生成难溶于水的H2TiO3 和硫酸,反应方程式为:TiOSO4 +2H2O=H2TiO3↓+
H2SO4 ;(2)碱性条件下Fe2+ 与空气中的氧气结合生成FeOOH,离子方程式为:4Fe2+ +O2 +8OH-
=4FeOOH↓+2H2O。