文档内容
热点突破 元素"位一构一性”关系的分析
目录
01考情透视·目标导航............................................................................................................................
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
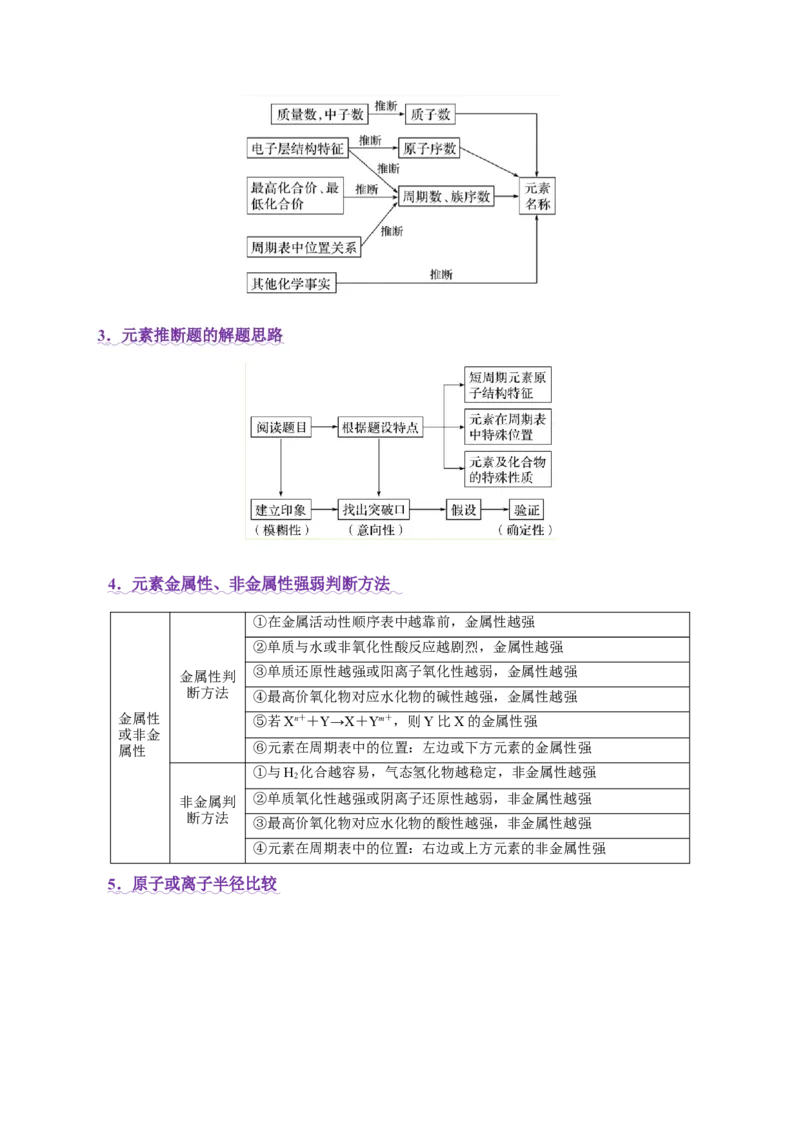
1.元素推断题解题的一般步骤.............................................................................................................................
2.元素推断题的思维模型.....................................................................................................................................
3.元素推断题的解题思路.....................................................................................................................................
4.元素金属性、非金属性强弱判断方法......................................................
5.原子或离子半径比较....................................................................
【命题预测】...........................................................................................................................................................
考向1文字陈述型元素推断题...............................................................................................................................
考向2片段周期表元素推断...................................................................................................................................
考向3物质结构式元素推断...................................................................................................................................
考向4根据化合物转化关系推断...........................................................................................................................
考点要求 考题统计 考情分析
2024·全国甲卷,5,6分;2024·浙江 1月 元素推断题主要考查元素周
期表中“位、构、性”的关
卷,12,3分;2024·浙江6月卷,10,3分;
系及学生利用物质结构和性
2024·河北卷,7,3分;2024·全国新课标卷, 质进行综合推断的能力,是
高考命题中的常客。解题
文字陈述
5,6分;2024·辽吉黑卷,11,3分;2024·江西
时,首先确定其为何种元
型元素推
素,然后以此为突破口,推
断 卷,5,3分;2023•全国乙卷,10,6分;2023•
知其他未知元素。预计2025
浙江省 1 月,10,3 分;2023•湖北卷,6,3 年高考仍会以考查递变规律
和性质为主,题目一般通过
分;2023•湖南卷,6,3分;2023•全国甲卷,
图表、文字等手段推断元素
11,6分;2023•浙江省6月,11,3分;2023•广 种类,尤其是通过未知物的东卷,14,3 分;2022•重庆卷,10,3 分;
2022•福建卷,4,3分;2022•全国甲卷,12,6
分;2022•全国乙卷,11,6分;2022•海南卷,
结构式,在确定元素的基础
10,2分;2022•辽宁卷,5,3分;2022•浙江省
上,能将元素周期表、原子
结构、元素单质及其化合物
1月,11,3分;2022•浙江省6月,11,3分;
的性质等内容结合起来进行
2024·湖北卷,9,3分;2024·福建卷,3,4分; 综合运用。
物质结构 2024·广西卷,1,3分;2024· 重庆卷,12,3
式型元素 分;2024· 贵州卷,9,3 分;2024·广东卷,
推断 12,3分;2024·甘肃卷,5,3分;2023•辽宁
卷,9,3分;2022•湖南卷,3,3分;
的
1.(2024·全国甲卷,5,3分)W、X、Y、Z为原子序数依次增大 短周期元素。W和X原子序数之和
等于 的核外电子数,化合物W+[ZY]-可用作化学电源的电解质。下列叙述正确的是( )
6
A.X和Z属于同一主族 B.非属性:C.气态氢化物的稳定性: D.原子半径:
【答案】A
【解析】W、X、Y、Z为原子序数依次增大的短周期元素,且能形成离子化合物W+[ZY]-,则W为Li
6
或Na;又由于W和X原子序数之和等于Y-的核外电子数,若W为Na,X原子序数大于Na,则W和X原
子序数之和大于18,不符合题意,因此W只能为Li元素;由于Y可形成Y-,故Y为第Ⅶ主族元素,且原
子序数Z大于Y,故Y不可能为Cl元素,因此Y为F元素,X的原子序数为10-3=7,X为N元素;根据
W、Y、Z形成离子化合物W+[ZY]-,可知Z为P元素;综上所述,W为Li元素,X为N元素,Y为F元
6
素,Z为P元素。A项, X为N元素,Z为P元素,X和Z属于同一主族,A正确;B项,X为N元素,
Y为F元素,Z为P元素,非金属性:F>N>P,B错误;C项,Y为F元素,Z为P元素,非金属性越强,
其简单气态氢化物的稳定性越强,即气态氢化物的稳定性:HF>PH ,C错误;D项,W为Li元素,X为
3
N元素,Y为F元素,同周期主族元素原子半径随着原子序数的增大而减小,故原子半径:Li>N>F,D
错误;故选A。
2.(2024·浙江1月卷,12,3分)X、Y、Z、M和Q五种主族元素,原子序数依次增大,X原子半径最
小,短周期中M电负性最小,Z与Y、Q相邻,基态Z原子的s能级与p能级的电子数相等,下列说法不
正确的是( )
A.沸点:XZ>XQ
2 2
B.M与Q可形成化合物MQ、MQ
2 2 2
C.化学键中离子键成分的百分数: MZ>MQ
2 2
D.YZ-与QZ2-离子空间结构均为三角锥形
3 3
【答案】D
【解析】X半径最小为H,短周期电负性最小则M为Na,Z原子的s能级与p能级的电子数相等,则
Z为O,Z与Y、Q相邻,Y为N,Q为S。A项,HO中含有氢键,则沸点高于HS,A正确;B项,Na
2 2
与O形成NaO、NaO,则O与S同族化学性质性质相似,B正确;C项,NaO的电子式为
2 2 2 2
,NaS的电子式为 ,离子键百分比 = (电负性差值 / 总电负性差值),
2
O的电负性大于S,则NaO离子键成分的百分数大于NaS,C正确;D项,NO -为sp2杂化,孤电子对为
2 2 3
0,为平面三角形,SO 2-为sp3杂化,孤电子对为0,正四面体,D错误;故选D。
3
3.(2024·浙江6月卷,10,3分)X、Y、Z、M四种主族元素,原子序数依次增大,分别位于三个不同
短周期,Y与M同主族,Y与Z核电荷数相差2,Z的原子最外层电子数是内层电子数的3倍。下列说法不正确的是( )
A.键角:YX +>YX - B.分子的极性:YX>XZ
3 3 2 2 2 2
C.共价晶体熔点:Y>M D.热稳定性:YX >MX
4 4
【答案】B
【解析】X、Y、Z、M四种主族元素,原子序数依次增大,分别位于三个不同短周期,Y与M同主族,
Y与Z核电荷数相差2,Z的原子最外层电子数是内层电子数的3倍,则Z为O元素,Y为C元素,X为H
元素,M为Si元素。A项,YX +为CH+,其中C原子的杂化类型为sp2,CH+的空间构型为平面正三角形,
3 3 3
键角为120°;YX -为CH-,其中C原子的杂化类型为sp3,CH-的空间构型为三角锥形,由于C原子还有1
3 3 3
个孤电子对,故键角小于109°28´,因此,键角的大小关系为YX +>YX -,A正确;B项,YX 为C H,
3 3 2 2 2 2
其为直线形分子,分子结构对称,分子中正负电荷的重心是重合的,故其为百极性分子;HO 分子结构不
2 2
对称,分子中正负电荷的重心是不重合的,故其为极性分子,因此,两者极性的大小关系为YX<XZ,
2 2 2 2
B不正确;C项,金则石和晶体硅均为共价晶体,但是由于C的原子半径小于Si,因此,C—C键的键能大
于Si—Si键的,故共价晶体熔点较高的是金刚石,C正确;D项,元素的非金属性越强,其气态氢化物的
热稳定性越强;C的非金属性强于Si,因此,甲烷的稳定热稳定性较高,D正确; 故选B。
4.(2024·河北卷,7,3分)侯氏制碱法工艺流程中的主反应为QR+YW +XZ +WZ=QWXZ +YW R,其
3 2 2 3 4
中W、X、Y、Z、Q、R分别代表相关化学元素。下列说法正确的是( )
A.原子半径:W<X<Y B.第一电离能:X<Y<Z
C.单质沸点:Z<R<Q D.电负性:W<Q<R
【答案】C
【解析】侯氏制碱法主反应的化学方程式为NaCl+NH +CO +H O= NaHCO ↓ + NH Cl,则可推出W、
3 2 2 3 4
X、Y、Z、Q、R分别为H元素、C元素、N元素、O元素、Na元素、Cl元素。A项,一般原子的电子层
数越多半径越大,电子层数相同时,核电荷数越大,半径越小,则原子半径:H<N<C,故A错误;B项,
同周期从左到右元素第一电离能呈增大趋势,Ⅱ A族、ⅤA族原子的第一电离能大于同周期相邻元素,则
第一电离能:C<O<N,故B错误;C项,O、Cl 为分子晶体,相对分子质量越大,沸点越高,二者在常
2 2
温下均为气体,Na在常温下为固体,则沸点:O <Cl <Na,故C正确;D项,同周期元素,从左往右电
2 2
负性逐渐增大,同族元素,从上到下电负性逐渐减小,电负性:Na<H<Cl,故D错误;故选C。
5.(2024·全国新课标卷,5,3分)我国科学家最近研究的一种无机盐Y[Z(WX)] 纳米药物具有高效的
3 6 2
细胞内亚铁离子捕获和抗氧化能力。W、X、Y、Z的原子序数依次增加,且W、X、Y属于不同族的短周
期元素。W的外层电子数是其内层电子数的2倍,X和Y的第一电离能都比左右相邻元素的高。Z的M层
未成对电子数为4。下列叙述错误的是( )
A.W、X、Y、Z四种元素的单质中Z的熔点最高
的
B.在X 简单氢化物中X原子轨道杂化类型为sp3C.Y的氢氧化物难溶于NaCl溶液,可以溶于NH Cl溶液
4
D.Y[Z(WX)] 中WX-提供电子对与Z3+形成配位键
3 6 2
【答案】A
【解析】W、X 、Y、Z的原子序数依次增加,且W、X、Y属于不同族的短周期元素。W的外层电
子数是其内层电子数的2倍,则W为C元素;每个周期的ⅡA和ⅤA的元素的第一电离能都比左右相邻
元素的高,由于配合物Y[Z(WX)] 中Y在外界,Y可形成简单阳离子,则Y属于金属元素,故X和Y分
3 6 2
别为 N和Mg;Z的M层未成对电子数为 4,则其 3d轨道上有 4个不成对电子,其价电子排布式为
3d64s2,Z为Fe元素,Y[Z(WX)] 为Mg[Fe(CN) ] 。A项,W、X、 Y、Z四种元素的单质中,N元素的
3 6 2 3 6 2
单质形成分子晶体,Mg和Fe均形成金属晶体,C元素既可以形成金刚石又可以形成石墨,石墨的熔点最
高,A不正确;B项,在X的简单氢化物是CH ,其中C原子轨道杂化类型为sp3,B正确;C项,Y的氢
4
氧化物是 Mg(OH) ,其属于中强碱,其难溶于水,难溶于 NaCl溶液,但是,由于 NH Cl电离产生的
2 4
NH +可以破坏 Mg(OH) 的沉淀溶解平衡,因此 Mg(OH) 可以溶于 NH Cl 溶液,C 正确;D 项,
4 2 2 4
Mg[Fe(CN) ] 中CN-提供电子对与Fe3+形成配位键,D正确;故选A。
3 6 2
6.(2024·辽吉黑卷,11,3分)如下反应相关元素中,W、X、Y、Z为原子序数依次增大的短周期元素,
基态X原子的核外电子有5种空间运动状态,基态Y、Z原子有两个未成对电子,Q是ds区元素,焰色试
验呈绿色。下列说法错误的是( )
QZY 溶液 QZX YW 溶液
4 4 4 12
A.单质沸点:Z>Y>W B.简单氢化物键角:X>Y
C.反应过程中有蓝色沉淀产生 D.QZX YW 是配合物,配位原子是Y
4 4 12
【答案】D
【解析】Q是ds区元素,焰色试验呈绿色,则Q为Cu元素;空间运动状态数是指电子占据的轨道数,
基态X原子的核外电子有5种空间运动状态,则X为第2周期元素,满足此条件的主族元素有
N(1s22s22p3)、O(1s22s22p4)、F(1s22s22p5);X、Y、Z为原子序数依次增大,基态Y、Z原子有两个未成对电
子,若Y、Z为第2周期元素,则满足条件的可能为C(1s22s22p2)或O(1s22s22p4),C原子序数小于N,所以
Y不可能为C,若Y、Z为第3周期元素,则满足条件的可能为Si(1s22s22p63s23p2)或S(1s22s22p63s23p4),Y、
Z可与Cu形成CuZY ,而O、Si、S中只有O和S形成的SO 2-才能形成CuZY ,所以Y、Z分别为O、S
4 4 4
元素,则X只能为N;W能与X形成WX,则W为IA族或VIIA族元素,但W原子序数小于N,所以W
3
为H元素,综上所述,W、X、Y、Z、Q分别为H、N、O、S、Cu。A项,W、Y、Z分别为H、O、S,S
单质常温下呈固态,其沸点高于氧气和氢气,O 和H 均为分子晶体,O 的相对分子质量大于H,O 的范
2 2 2 2 2
德华力大于 H,所以沸点O>H,即沸点S>O>H,故A正确;B项,Y、X的 简单氢化物分别为
2 2 2 2 2HO和NH ,HO的中心原子O原子的价层电子对数为2+ ×(6-2×1)=4、孤电子对数为2,空间构型为V
2 3 2
形,键角约105º,NH 的中心原子N原子的价层电子对数为3+ ×(5-3×1)=4、孤电子对数为1,空间构型
3
为三角锥形,键角约107º18´,所以键角:X>Y,故B正确;C项,硫酸铜溶液中滴加氨水,氨水不足时
生成蓝色沉淀氢氧化铜,氨水过量时氢氧化铜溶解,生成Cu(NH )SO ,即反应过程中有蓝色沉淀产生,
3 4 4
故C正确;D项,QZX YW 为Cu(NH )SO ,其中铜离子提供空轨道、NH 的N原子提供孤电子对,两
4 4 12 3 4 4 3
者形成配位键,配位原子为N,故D错误;故选D。
7.(2024·江西卷,5,3分)某新材料阳离子为W X YZM+。W、X、Y、Z和M是原子序数依次增大
36 18 2 6
的前20号主族元素,前四周期中M原子半径最大,X、Y、Z同周期。XW 分子含有大π键( ),XZ 分
6 6 2
子呈直线形。下列说法正确的是( )
A.WYZ 是强酸 B.MZW是强碱 C.MZ 是共价化合物 D.XW 是离子化合物
2 2 2 2 2
【答案】B
【解析】W、X、Y、Z和M是原子序数依次增大的前20号主族元素,前四周期中M原子半径最大,
M为K元素,X、Y、Z同周期,XW 分子含有大π键( ),说明XW 是苯,X为C元素,W为H元素,
6 6 6 6
XZ 分子呈直线形,为CO ,Z为O元素,Y为N元素。A项,W为H元素、Y为N元素、Z为O元素,
2 2
HNO 是弱酸,不是强酸,A错误;B项,M为K元素、Z为O元素,W为H元素,KOH是强碱,B正确;
2
C项,M为K元素、Z为O元素,KO 中存在K+和O2-,属于离子化合物,C错误;D项,X为C元素、
2 2 2
W为H元素,C H 为乙炔的分子式,乙炔中没有离子键,属于共价化合物,D错误;故选B。
2 2
8.(2024·湖北卷,9,3分)主族元素W、X、Y、Z原子序数依次增大,X、Y的价电子数相等,Z的
价电子所在能层有16个轨道,4种元素形成的化合物如图。下列说法正确的是( )
A.电负性:W>Y B.酸性:WYX >WYX
2 3 2 4
C.基态原子的未成对电子数:W>X D.氧化物溶于水所得溶液的pH :Z>Y
【答案】D
【解析】主族元素W、X、Y、Z原子序数依次增大,X、Y的价电子数相等,Z的价电子所在能层有
16个轨道,则Z个有4个能层。根据这4种元素形成的化合物的结构可以推断,W、X、Y、Z分别为H、O、S、K。A项,W和Y可以形成HS,其中S显-2价,因此,电负性S>H,A不正确;B项,HSO 是中
2 2 3
强酸,而HSO 是强酸,因此,在相同条件下,后者的酸性较强,B不正确;C项,H只有1个电子,O的
2 4
2p轨道上有4个电子,O有2个未成对电子,因此,基态原子的未成对电子数 O>H,C不正确;D项,K
的氧化物溶于水且与水反应生成强碱KOH,S的氧化物溶于水且与水反应生成HSO 或HSO ,因此,氧
2 3 2 4
化物溶于水所得溶液的pH的大小关系为 K>S,D正确;故选D。
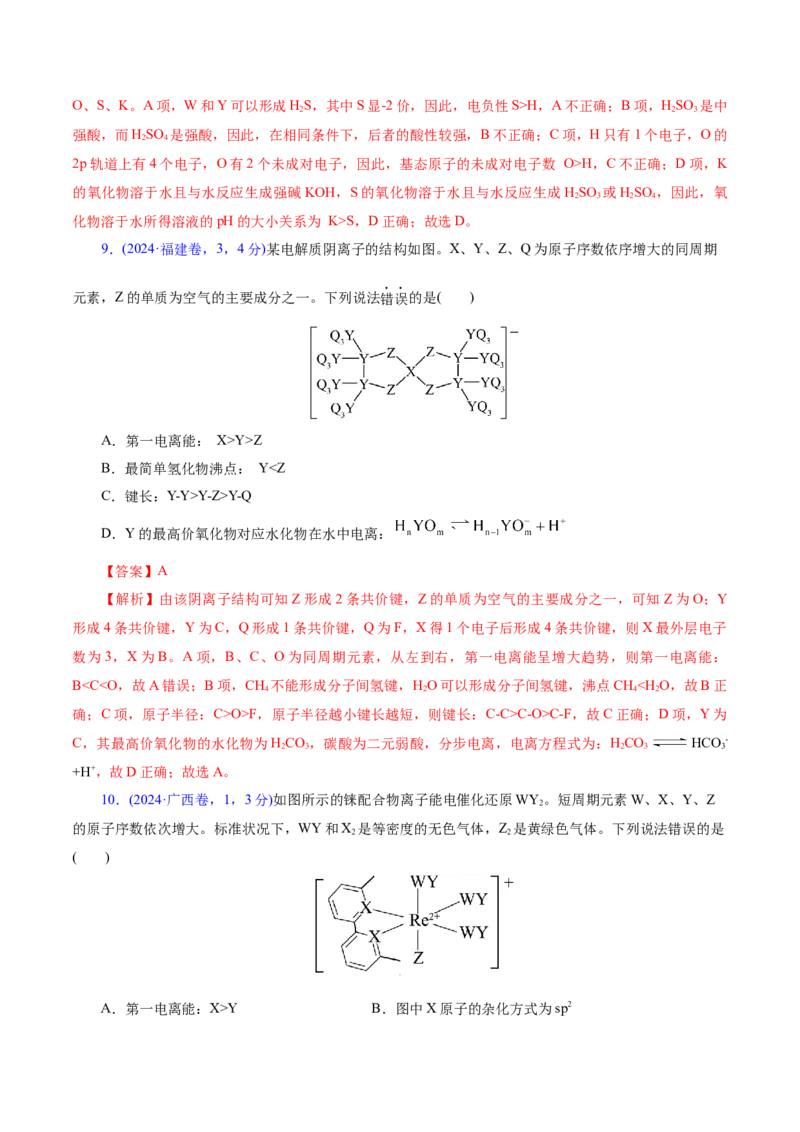
9.(2024·福建卷,3,4分)某电解质阴离子的结构如图。X、Y、Z、Q为原子序数依序增大的同周期
元素,Z的单质为空气的主要成分之一。下列说法错误的是( )
A.第一电离能: X>Y>Z
B.最简单氢化物沸点: YY-Z>Y-Q
D.Y的最高价氧化物对应水化物在水中电离:
【答案】A
【解析】由该阴离子结构可知Z形成2条共价键,Z的单质为空气的主要成分之一,可知Z为O;Y
形成4条共价键,Y为C,Q形成1条共价键,Q为F,X得1个电子后形成4条共价键,则X最外层电子
数为3,X为B。A项,B、C、O为同周期元素,从左到右,第一电离能呈增大趋势,则第一电离能:
BO>F,原子半径越小键长越短,则键长:C-C>C-O>C-F,故C正确;D项,Y为
C,其最高价氧化物的水化物为HCO ,碳酸为二元弱酸,分步电离,电离方程式为:HCO HCO -
2 3 2 3 3
+H+,故D正确;故选A。
10.(2024·广西卷,1,3分)如图所示的铼配合物离子能电催化还原WY。短周期元素W、X、Y、Z
2
的原子序数依次增大。标准状况下,WY和X 是等密度的无色气体,Z 是黄绿色气体。下列说法错误的是
2 2
( )
A.第一电离能:X>Y B.图中X原子的杂化方式为sp2C. 元素以原子的形态与Re2+配位 D.Y的电负性大于 中的化学键是极性键
【答案】C
【解析】短周期元素W、X、Y、Z的原子序数依次增大。Z 是黄绿色气体,Z为氯;X形成3个共用
2
电子对,X与Re2+之间为配位键,推测X为氮,标准状况下,WY和X 是等密度的无色气体,则WY为一
2
氧化碳、X 为氮气,故W为碳、X为氮、Y为氧、Z为氯。A项,同一周期随着原子序数变大,第一电离
2
能变大,N的2p轨道为半充满稳定状态,第一电离能大于同周期相邻元素,故第一电离能大小:N>O,A
正确;B项,图中X原子处于环中,且存在平面大π键,则其杂化方式为sp2,B正确;C项,由图可知,
整个离子带1个单位正电荷,而其中Re2+带2个单位正电荷,则氯元素以Cl-的形态与Re2+配位,C错误;
D项,同周期从左到右,金属性减弱,非金属性变强,元素的电负性变强;O的电负性大于C,则CO中
的化学键是极性键,D正确;故选C。
11.(2024· 重庆卷,12,3分)R、X、Y和Z为短周期元素,XY ZR 的分子结构如下所示。R中电子
3 3
只有一种自旋取向,X、Y和Z处于同一周期,X的核外电子数等于Y的最高能级电子数,且等于Z的最
外层电子数。下列说法正确的是( )
A.原子半径:Z<X B.非金属性: Y<Z
C.单质的沸点:X<Y D.最高正化合价:X<R
【答案】A
【解析】R、X、Y和Z为短周期元素,R中电子只有一种自旋取向,R为H元素;X、Y和Z处于同
一周期,X的核外电子数等于Y的最高能级电子数,且等于Z的最外层电子数,XY ZR 的分子中X、Z均
3 3
形成4个共价键,则X为B元素、Z为N元素;Y只形成1个共价键,结合位置可知Y为F元素。A项,
X为B元素、Z为N元素,同周期主族元素从左向右原子半径减小,则原子半径:Z<X,故A正确;B项,
Y为F元素、Z为N元素,同周期主族元素从左向右非金属性增强,则非金属性:Y>Z,故B错误;C项,
X为B元素、Y为F元素,X的单质为共价晶体,Y的单质为分子晶体,单质的沸点:X>Y,故C错误;
D项,R为H元素、X为B元素,最高正化合价:X(+3)>R(+1),故D错误;故选A。
12.(2024· 贵州卷,9,3分)某化合物由原子序数依次增大的短周期主族元素W、X、Y、Z、Q组成
(结构如图)。X的最外层电子数等于内层电子数,Y是有机物分子骨架元素,Q和W能形成两种室温下常
见的液态化合物。下列说法错误的是( )A.第一电离能: B.该化合物中Q和W之间可形成氢键
C.X与Al元素有相似的性质 D.W、Z、Q三种元素可形成离子化合物
【答案】A
【解析】X的最外层电子数等于内层电子数,则X的核外电子排布式为1s22s2,X为Be元素,W只能
形成一条共价键,结合W的位置可知W为H元素,Y是有机物分子骨架元素,则Y为C元素,Q和W能
形成两种室温下常见的液态化合物,则Q为O元素,则Z为N元素。A项,同一周期,从左到右,元素的
第一电离能呈增大的趋势,N原子中2p能级上电子为半满结构,较为稳定,第一电离能大于同周期与之相
邻的元素,则第一电离能:CB>A>D
D.工业上常用电解C和E的化合物来制备E单质
【答案】D
【解析】A是宇宙中含量最高的元素,故A为H,B元素的一种核素可对文物进行年代测定,故B为
C,C元素最高价氧化物对应水化物是常见的最强酸,故C为Cl,D元素的焰色试验呈砖红色,故D为
Ca,基态E+的轨道全部充满,故E为Cu。A项,H、C两种元素可以形成成千上万种烃类化合物,故A正
确;B项,C为Cl,氯气单质可用于自来水消毒,故B正确;C项,电负性大小:Cl>C>H>Cu,故C正确;
D项,工业上制备Cu,常用火法炼铜或者湿法炼铜,故D错误;故选D。
2.(2025·浙江省名校协作体三开学测试)W、R、Q、X、Y、Z是原子序数依次递增的前两周期主族元
素,基态R原子无未成对电子,基态Q原子有2个未成对电子。W、R、X、Z四种元素可以组成离子化合
物:(XW )RZ ,其阴、阳离子均为正四面体结构。下列说法正确的是( )
4 2 4
A.(XW )RZ 阴阳离子中均含有配位键 B.XW 分子空间结构为平面形
4 2 4 2 4
C.QWZ 一定是非极性分子 D.氢化物热稳定性: Y>X
2 2 2
【答案】A
【解析】由题干信息可知,W、R、Q、X、Y、Z是原子序数依次递增的前两周期主族元素,基态R
原子无未成对电子,则R为1s22s2即Be,基态Q原子有2个未成对电子,即为1s22s22p2或者1s22s22p4,故
Q为C或者O,结合原子序数递增可知,Q为C,则W为H,W、R、X、Z四种元素可以组成离子化合物:
(XW )RZ ,其阴、阳离子均为正四面体结构,故X为N、Y为O,Z为F。A项,(XW )RZ 阴、阳离子分
4 2 4 4 2 4
别为NH +、BeF 2-中每个均含有配位键,A正确;B项,X为N、W为H,故XW 即NH 分子空间结构不
4 4 2 4 2 4
为平面形,每个N原子的价层电子对数均为4,每个N原子与周围的原子形成三角锥形结构,B错误;C
项,Q为C、W为H、Z为F,QWZ 为CHF=CHF或者CF=CH ,均一定是极性分子,C错误;D项,Y
2 2 2 2 2
为O,X为N,非金属性O大于N,故氢化物热稳定性HO>NH ,但HO 的热稳定性弱于NH ,D错误;
2 3 2 2 3
故选A。
3.[原创题]X、Y、Z、G、Q五种短周期主族元素,原子序数依次增大。元素X、Y、Q的单质在常
温下呈气态,元素Y的最高正价和最低负价之和为2,元素Z在同周期的主族元素中原子半径最大,元素
G是地壳中含最多的金属元素。下列说法不正确的是
A.X与Z形成的二元化合物与水反应属于非氧化还原反应
B.元素X、Y可以形成YX 、YX 等化合物
3 2 4
C.元素Z、G的最高价氧化物对应的水化物能相互反应
D.G、Q两种元素形成的化合物的水溶液呈酸性
【答案】A
【解析】元素Y的最高正价与最低负价之和为2,推测该元素最高价为+5,最低价为-3价,则Y可能为N或P,又其单质常温下呈气态,故Y为N,Z在同周期中原子半径最大,又Z原子序数比Y大,故
Z只能为第三周期的Na,G元素为地壳中含量最多的金属元素,故G为Al,Al后面的同周期主族元素对
应单质常温下呈气态的只有Cl对应的Cl,故Q为Cl,N元素之前的主族元素中对应单质常温为气态的只
2
有H对应的H,故X为H。A项,H元素与Na形成的二元化合物即NaH与水反应生成氢氧化钠和氢气,
2
属于氧化还原反应,A错误;B项,X为H,Y为N,可形成NH 、NH 等化合物,B正确;C项,Z、G
3 2 4
最高价氧化物对应水化物分别为NaOH、Al(OH) ,Al(OH) 有两性,可以与NaOH反应生成NaAlO ,C正
3 3 2
确;D项,G、Q形成化合物AlCl ,由于Al3+水解,故AlCl 溶液显酸性,D正确;故选A。
3 3
4.[真题改编](2022·浙江省6月选考,16改编)X、Y、Z、M、Q五种短周期主族元素,原子序数依次
增大。X的核外电子数等于其周期数,YX 分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。
3
M与X同主族,Q是同周期中非金属性最强的元素。下列说法正确的是( )
A.X与Z形成的10电子微粒有2种
B.Z与Q形成的一种化合物可用于饮用水的消毒
C.MZ与MQ的晶体类型不同
2
D.由X、Y、Z三种元素组成的化合物的水溶液均显酸性
【答案】B
【解析】X的核外电子数等于其周期数,X为H,YX 分子呈三角锥形,Y为N,Z的核外电子数等于
3
X、Y核外电子数之和,则Z为O,M与X同主族,则M为Na,Q是同周期中非金属性最强的元素,则Q
为Cl,综合分析,X为H,Y为N,Z为O,M为Na,Q为Cl。A项,X为H,Z为O,则其形成的10电
子微粒有HO、OH-、HO+,A错误;B项,Z为O,Q为Cl,可形成ClO ,有氧化性,可用于自来水消毒,
2 3 2
B正确;C项,Z为O,M为Na,Q为Cl,则MZ为NaO,为离子晶体,MQ为NaCl,为离子晶体,晶
2 2
体类型相同,C错误;D项,X为H,Y为N,Z为O,这三种元素可以形成NH ·H O,其溶液显碱性,D
错误;故选B。 ₃ ₂
5.[真题改编] (2024·甘肃卷,5,3分)X、Y、Z、W、Q为短周期元素,原子序数依次增大,最外层
电子数之和为18。Y原子核外有两个单电子,Z和Q同族,Z的原子序数是Q的一半,W元素的焰色试验
呈黄色。下列说法错误的是( )
A.X、Y组成的化合物有可燃性 B.X、Q组成的化合物有还原性
C.Z、W组成的化合物能与水反应 D.W、Q组成的化合物溶于水呈酸性
【答案】D
【解析】X、Y、Z、W、Q为短周期元素,W元素的焰色试验呈黄色,W为Na元素;Z和Q同族,Z
的原子序数是Q的一半,则Z为O、Q为S;Y原子核外有两个单电子、且原子序数小于Z,Y为C元素;
X、Y、Z、W、Q的最外层电子数之和为18,则X的最外层电子数为18-4-6-1-6=1,X可能为H或Li。A
项,若X为H,H与C组成的化合物为烃,烃能够燃烧,若X为Li,Li与C组成的化合物也具有可燃性,
A项正确;B项,X、Q组成的化合物中Q(即S)元素呈-2价,为S元素的最低价,具有还原性,B项正确;C项,Z、W组成的化合物为NaO、NaO,NaO与水反应生成NaOH,NaO 与水反应生成NaOH和O,
2 2 2 2 2 2 2
C项正确;D项,W、Q组成的化合物NaS属于强碱弱酸盐,其溶于水所得溶液呈碱性,D项错误;故选
2
D。
考向 2 片段周期表元素推断
6.四种短周期元素X、Y、Z和W在元素周期表中的位置如图,其中X原子的最外层电子数是次外层
电子数的3倍。下列说法正确的是( )
X
Y Z W
A.X位于第2周期第ⅣA族 B.Y的非金属性比Z的强
C.Z的原子半径比X的大 D.W的含氧酸一定是强酸
【答案】C
【解析】X原子的最外层电子数是次外层电子数的3倍,X位于第二周期,因此X是O,则Y是Si,
Z是P,W是Cl。A项,X是O,位于第2周期第ⅥA族,A错误;B项,同周期自左向右非金属性逐渐增
强,Y的非金属性比Z的弱,B错误;C项,核外电子层数越多,原子半径越大,则Z的原子半径比X的
大,C正确;D项,应该是W的最高价含氧酸高氯酸一定是强酸,D错误;故选C。
7.X、Y、Z、Q和R五种短周期元素在周期表中的位置如图所示,其中 X原子的次外层电子数是最
外层电子数的一半。下列说法不正确的是( )
X Y Z
Q R
A.Y的原子半径比Z的小
B.Y元素位于第二周期VA族
C.R元素的气态氢化物比Q元素的稳定
D.与X元素同主族的下一周期元素的单质可作为半导体材料
【答案】A
【解析】X、Y、Z、Q和R五种短周期元素,结合周期表中的位置可知XYZ为第二周期元素,QR为
第三周期元素;X原子的次外层电子数是最外层电子数的一半,可知X为C,则Y为N,Z为O,Q为S,
R为Cl。A项,同周期元素原子半径从左到右逐渐减小,则Y的原子半径比Z的大,故A错误;B项,Y
为N,位于第二周期VA族,故B正确;C项,元素的非金属性越强,气态氢化物越稳定,非金属性:
Cl>S,因此稳定性:HCl>H S,故C正确;D项,与X元素同主族的下一周期元素为硅,硅单质是常用的
2半导体材料,故D正确;故选A。
8.[真题改编](2022•广东选择性考试,7)甲~戊均为短周期元素,在元素周期表中的相对位置如图所
示。戊的最高价氧化物对应的水化物为强酸。下列说法不正确的是( )
A.原子半径:丁>戊>乙
B.非金属性:戊>丁>丙
C.甲的氢化物遇氯化氢一定有白烟产生
D.丙的最高价氧化物对应的水化物一定能与强碱反应
【答案】C
【解析】
A项,根据层多径大,同电子层结构核多径小原则,则原子半径:丁>戊>乙,故 A正确;B项,根
据同周期从左到右非金属性逐渐增强,则非金属性:戊>丁>丙,故B正确;C项,甲的氢化物可能为氨
气,可能为甲烷、乙烷等,若是氨气,则遇氯化氢一定有白烟产生;若是甲烷、乙烷等,则遇氯化氢不反
应,没有白烟生成,故C错误;D项,丙的最高价氧化物对应的水化物可能是硅酸、也可能是磷酸,都一
定能与强碱反应,故D正确。故选C。
9.如表为元素周期表的一部分,其中 、 、 、 为短周期元素, 元素的原子质子数为 元素
的原子的 倍,下列说法不正确的是( )
A.R、W、Z元素的原子半径依次递增,而 、 、 的氢化物的空间结构都呈 形, 的氢化物
的沸点高于 的氢化物
B.Y、Z、W的最高价氧化物的水化物的酸性依次递增
C.I:Z>W,是因为 的3p轨道电子填充处于半充满状态
1
D.YR 晶体熔化、液态WR 气化克服的作用力不同
2 3
【答案】A
【解析】R、Y、Z、W为短周期元素,W元素的原子质子数为R元素的原子的2倍,则R为O元素、W为硫元素;由元素在元素周期表中的相对位置可知,Y为Si元素、Z为P元素。A项,磷化氢分子中磷
原子的价层电子对数为4、孤对电子对数为1,分子的空间结构为三角锥形,故A错误;B项,同周期元素,
从左到右元素的非金属性依次增强,最高价氧化物的水化物的酸性依次增强,则硅、磷、硫三种元素的非
金属性依次增强,最高价氧化物的水化物的酸性依次递增,故B正确;C项,同周期元素,从左到右第一
电离能呈增大趋势,磷原子的3p轨道为稳定的半充满结构,元素的第一电离能大于相邻元素,则磷元素的
第一电离能大于硫元素,故C正确;D项,二氧化硅为共价晶体,熔化时破坏的是共价键,而液态三氧化
硫是分子晶体,气化时克服的是分子间作用力,则二氧化硅晶体熔化和液态三氧化硫气化克服的作用力不
同,故D正确;故选A。
10. X、Y、Z、W为短周期元素,它们在周期表的位置如图所示,Y原子的最外层电子数是次外层
电子数的3倍。下列说法中正确的是( )
X Y
Z W
A.X的单质中 键和 键个数之比为1∶1 B.Y和Z只能组成一种化合物
C.Z的氧化物的晶体属于分子晶体 D.最高价氧化物对应水化物的酸性:Z>W
【答案】C
【解析】由于Y原子的最外层电子数是次外层电子数的 3倍,即Y为O。X、Z、W分别为N、S、
Cl。A项,X的单质为N ,分子中含有三键应该为1个σ 键和 2个π 键,个数之比为1∶2,A项错误;B
2
项,S与O能形成SO 和SO ,B项错误;C项,Z的氧化物为SO 和SO ,熔点较低,属于分子晶体,C
2 3 2 3
项正确;D项,同周期从左往右非金属性增强,最高价氧化为的水化物酸性增强:ZX B.反应过程中有蓝色沉淀生成
C.元素电负性:X>Y>Z D.单质沸点:Z>Y>W
【答案】C
【解析】R是ds区元素,R的单质呈紫红色,则R为Cu;空间运动状态数是指电子占据的轨道数,
基态X原子的核外电子有5种空间运动状态,则X为第2周期元素,满足此条件的主族元素有
N(1s22s22p3)、O(1s22s22p4)、F(1s22s22p5);基态Y、Z原子有两个未成对电子,若Y、Z为第2周期元素,则
满足条件的可能为C(1s22s22p2)或O(1s22s22p4),C原子序数小于N,所以Y不可能为C;若Y、Z为第3周
期元素,则满足条件的可能为Si(1s22s22p63s23p2)或S(1s22s22p63s23p4),Y、Z可与Cu形成CuZY ,而O、
4
Si、S中只有O和S形成的SO 2-才能形成CuZY ,所以Y、Z分别为O、S元素,则X只能为N;W能与X
4 4
形成XW,则W为IA族或VIIA族元素,但W原子序数小于N,所以W为H元素,综上所述,W、X、
3
Y、Z、Q分别为H、N、O、S、Cu。A项,Y、X的 简单氢化物分别为HO和NH ,非金属性:O>N,
2 3
则简单氢化物的稳定性:Y>X,故A正确;B项,硫酸铜溶液中滴加氨水,氨水不足时生成蓝色沉淀氢氧化铜,氨水过量时氢氧化铜溶解,生成Cu(NH )SO ,即反应过程中有蓝色沉淀产生,故B正确;C项,
3 4 4
非金属性越强,其电负性越大,非金属性O>N>S,则电负性:Y>X>Z,故C错误;D项,W、Y、Z分
别为H、O、S,S单质常温下呈固态,其沸点高于氧气和氢气,O 和H 均为分子晶体,O 的相对分子质
2 2 2
量大于H,O 的范德华力大于 H,所以沸点O>H,即沸点S>O>H,即Z>Y>W,故D正确;故选
2 2 2 2 2 2 2
C。
13.(2025·浙江省强基联盟高三10月联考)一种麻醉剂的分子结构式如图所示,其中X的原子核只有1
个质子;元素Y、Z、W的原子序数依次增大,且均位于X的下一周期;元素E的原子比W原子多8个电
子,下列说法不正确的是( )
A.键角:YX +>YX -
3 3
B.物质的碱性:NE>NX
3 3
C.分子的极性:YX <XX
2 2 2
D.X、Y、Z、W四种原子的电负性的大小顺序是W>Z>Y>W
【答案】B
【解析】由图可知,X、Y、Z、W、E形成的共价键数目分别为1、4、2、1、1,X的原子核只有1个
质子;元素Y、Z、W的原子序数依次增大,且均位于X的下一周期;元素E的原子比W原子多8个电子,
则X是H元素、Y为C元素、Z为O元素、W为F元素、E为Cl元素。A项,CH+中碳原子的价层电子对
3
数为3、孤对电子对数为0,离子的空间构型为平面三角形,CH-中碳原子的价层电子对数为4、孤对电子
3
对数为1,离子的空间构型为三角锥形,所以CH+的键角大于CH-,故A正确;B项,氯元素的电负性大
3 3
于氢元素,三氯化氮分子中氯原子是吸电子基,会使氮原子周围的电子云密度下降,给出孤电子对的能力
弱,所以氨分子的碱性强于三氯化氮,故B错误;C项,乙炔分子的空间结构为直线形,是结构对称的非
极性分子,水分子的空间结构是V形,是结构不对称的极性分子,所以乙炔分子的极性小于水分子,故C
正确;D项,元素的非金属性越强,电负性越大,四种元素的非金属性强弱顺序为F>O>C>H,则电负
性的大小顺序为F>O>C>H,故D正确;故选B。
14.(2025·浙江省天域全国名校协作体高三联考)W、X、Y、Z是原子序数依次增大的短周期元素,原
子序数总和为25,由这四种元素形成的化合物M的结构如图所示。下列叙述不正确的是( )A.M中电负性最大的元素是Y
B.M中不存在配位键
C.M具有强氧化性,可用于消毒杀菌
D.X元素的最高价含氧酸可以形成分子间氢键
【答案】B
【解析】Z是短周期元素,且能够形成Z+,其原子序数比W、X、Y大,因此Z为Na,根据M的结构
示意图,8个Y原子均形成了2个共价键,原子序数比Na小,形成2个共价键的为O,因此Y为O;4个
W原子均形成1个共价键,且原子序数比O小,因此W为H;四种元素的原子序数总和为25,则X的原
子序数为5,为B;综上W、X、Y、Z分别为H、B、O、Na。A项,在上述元素中,O的非金属性最强,
电负性最大,即Y的电负性最大,故A正确;B项,根据M的结构,B原子连有4个键,其中含有一个配
位键,故B错误;C项,该化合物中含有O-O键,具有强氧化性,能够杀菌消毒,故C正确;D项,X是
B元素,因而X的最高价含有酸为HBO,结构简式为 ,含有羟基,可以形成分子间氢键,
3 3
故D正确;故选B。
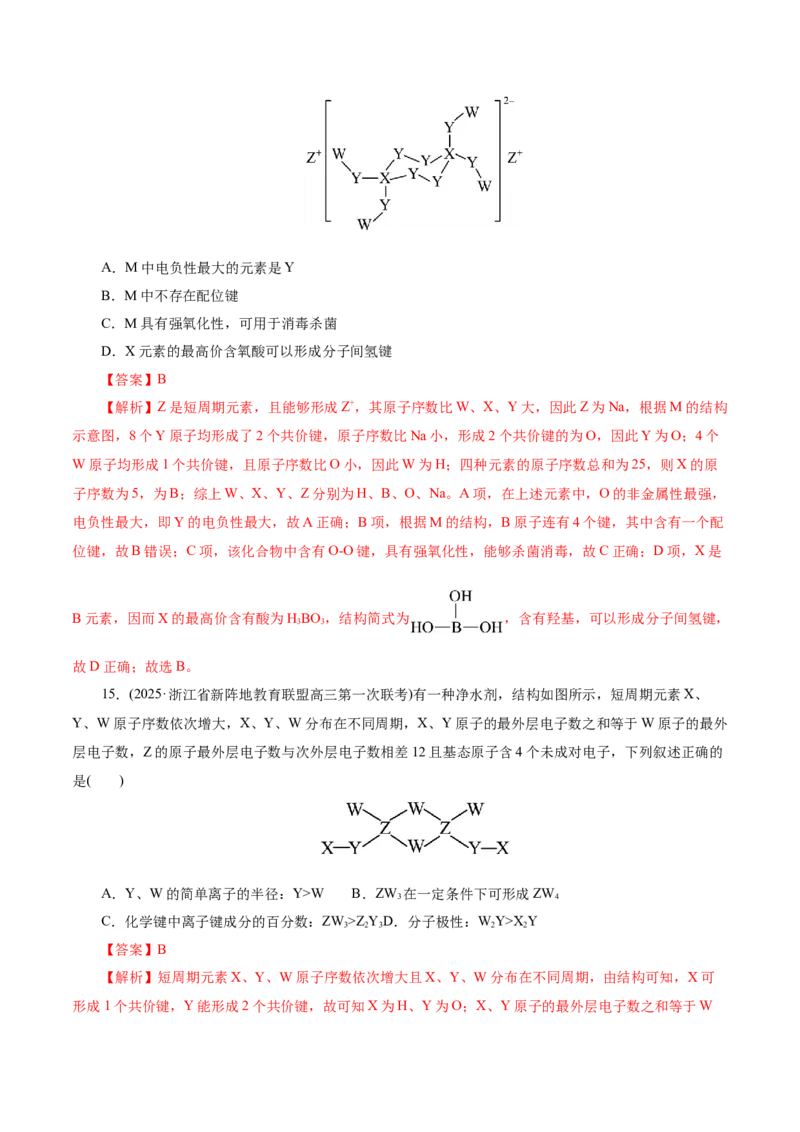
15.(2025·浙江省新阵地教育联盟高三第一次联考)有一种净水剂,结构如图所示,短周期元素X、
Y、W原子序数依次增大,X、Y、W分布在不同周期,X、Y原子的最外层电子数之和等于W原子的最外
层电子数,Z的原子最外层电子数与次外层电子数相差12且基态原子含4个未成对电子,下列叙述正确的
是( )
A.Y、W的简单离子的半径:Y>W B.ZW 在一定条件下可形成ZW
3 4
C.化学键中离子键成分的百分数:ZW>ZY D.分子极性:WY>XY
3 2 3 2 2
【答案】B
【解析】短周期元素X、Y、W原子序数依次增大且X、Y、W分布在不同周期,由结构可知,X可
形成1个共价键,Y能形成2个共价键,故可知X为H、Y为O;X、Y原子的最外层电子数之和等于W原子的最外层电子数,则W最外层上有7个电子,又W形成1个共价键,即W为Cl;Z的原子最外层电
子数与次外层电子数相差12且基态原子含4个未成对电子,则Z为Fe。A项,Y、W的简单离子分别为氧
离子和氯离子,氯离子核外有三个电子层而氧离子核外只有两个电子层,所以半径:W > Y,A错误;B
项,三氯化铁在一定条件下可与氯离子以配位键结合,B正确;C项,因氧的电负性大于氯,所以化学键
中离子键成分的百分数ZY> ZW ,C错误;D项,因氧的电负性大于氯,所以分子极性XY > W Y,D错
2 3 3 2 2
误; 故选B。
16.如图所示的化合物是一种重要的化工原料,X、Y、Z、W、E是原子序数依次增大的短周期主族
元素,其中Z、E同族,基态Y原子的核外有3个未成对电子。下列说法正确的是( )
A.原子半径:W>Y>Z>E B.WZ 中只含有离子键
2 2
C.Z、W、E组成化合物的水溶液一定显中性 D.电负性:Z>Y>X
【答案】D
【解析】X、Y、Z、W、E是原子序数依次增大的短周期主族元素,基态 Y原子的核外有3个未成对
电子,结合图示的化合物结构可知,Y为N;E核外有6个电子,Z、E同族,则Z核外也有6个电子,所
以Z为O,E为S;从图示可知,X为H,W为Na。A项,一般地,电子层数越多,原子半径越大,电子
层数相同时,质子数越多,原子半径越小,所以原子半径:Na>S>N>O,故A错误;B项,NaO 中既有离
2 2
子键,又有共价键,故B错误;C项,Z、W、E组成NaSO ,其水溶液显中性,若组成NaSO ,则其水
2 4 2 3
溶液呈碱性,故C错误;D项,元素的非金属性越强,电负性越强,同周期从左到右,元素电负性增强,
H和N形成的化合物中,N为负价,所以H的电负性比氮小,故电负性:O>N>H,故D正确;故选D。
17.某化合物结构如图所示。其中 为原子序数依次增大的短周期非金属元素,X是有机
分子的骨架元素,W基态原子的M层为全充满、N层只有一个电子。下列说法正确的是( )
A.原子半径:X>Y>Z B.第一电离能:X>Y>M>W
C.该配合物中X均满足8电子稳定结构 D.该配合物中X的杂化类型有sp2、sp3【答案】D
【解析】X是有机分子的骨架元素,说明X为C元素;W基态原子的M层为全充满、N层只有一个
电子,即W的价电子排布式为3d104s1,即W为Cu元素;M、X、Y、Z为原子序数依次增大的短周期非金
属元素,根据结构式可知,M为H元素,Y为N元素,Z为P元素。A项,电子层数越多,半径越大,电
子层数相同,核电荷数越小,半径越大,则原子半径由大到小的顺序为:Z>X>Y,A错误;B项,N原
子属于半充满状态,第一电离能较高,H原子比C原子半径小得多,核外电子受到原子核的引力大,电离
需要更多的能量,故H>C,而Cu的电子层数最大,较容易失去一个电子,,其第一电离能最小,故第一
电离能由大到小的顺序为:Y>M>X>W,B错误;C项,该配合物中与W形成配位键的X,不满足8电
子稳定结构,C错误;D项,该配合物中X的价层电子对有4和3,故其杂化类型有sp2、sp3,D正确;故
选D。
18.M、X、Y、Z、Q为相邻两个短周期的主族元素,且原子序数依次增大。这五种元素可形成化合
物甲,其结构式如图所示,1mol甲含58mol电子。下列说法正确的是( )
A.Q是五种元素中原子半径最大的 B.水中溶解性:MQ<YZ
2
C.XQ 中所有原子均达到8e-稳定结构 D.甲中X、Y、Z均为sp3杂化
3
【答案】D
【解析】M、X、Y、Z、Q为相邻两个短周期的主族元素,且原子序数依次增大。M的原子序数最小,
且在化合物甲中形成一个共价键,则M为H;X、Y、Z、Q为第二周期元素。根据它们在化合物甲中形成
化学键的个数可知,X为B(形成了一个配位键),Y为C,Z为O(和B形成一个配位键),Q为F,符合
1mol甲含58mol电子。A项,F位于第二周期第ⅦA族,是第二周期元素原子半径最小的(除了稀有气体),
故A错误;B项,HF能和水形成氢键,而CO 不能和水形成氢键,所以HF在水中的溶解度大于CO 在水
2 2
中的溶解度,故B错误;C项,BF 中B原子没有达到8电子稳定结构,B最外层只有6个电子,故C错误;
3
D项,C和B的价层电子对数都是4,且没有孤电子对,均为sp3杂化;O形成了三个σ键,还有一孤电子
对,价层电子对数也是4,也是sp3杂化,故D正确;故选D。
考向 4 根据化合物转化关系推断
19.(2024·浙江省绍兴鲁迅中学高三选考模拟)短周期主族元素W、X、Y、Z的原子序数依次增大,Y
和Z同主族,且Z的原子序数是Y的2倍。n、q、s是上述元素的单质。m、p、r是由这些元素组成的二元
化合物,其中m的水溶液显碱性。上述物质的转化关系如图所示。下列说法正确的是( )A.Z的常见氧化物均为酸性氧化物
B.W和X形成的化合物一定是共价化合物
C.原子半径:Z>Y>X
D.四种元素组成的化合物一定能促进水的电离
【答案】A
【解析】据题意可知,Y、Z分别为O和S,m为NH ,则W、X分别为H和N。Z的常见氧化物
3
SO 、SO 均为酸性氧化物,A正确;W和X形成的化合物NH H为离子化合物,B错误;原子半径:S
2 3 4
>N>O,C错误;四种元素组成的化合物NH HSO 抑制水的电离,D错误。
4 4
20.(2024·内蒙古赤峰三模)X、Y、Z、W、Q为短周期主族元素,原子序数依次增大且原子序数总和
为49。它们的化合物在常温下有如图所示的转化关系:
已知:乙、戊分子都含有 10个电子。甲为三元化合物,其他化合物均为二元化合物。下列说法错误
的是( )
A.原子半径:
B.简单氢化物的沸点:
C.化合物WQ 中含有非极性键和离子键
2 2
D.最高价氧化物对应水化物的酸性:
【答案】C
【解析】由题中转化关系可以看出,丁能使品红溶液褪色,加热后又恢复红色,所以丁是二氧化硫,
乙、戊分子都含有 10个电子且丙和戊能产生白烟,所以戊是氨气,则五种元素中含H、N、O、S,又五
种元素原子序数总和等于49,则另一种元素的原子序数为49-16-8-7-1=17,为Cl,结合原子序数大小X、
Y、Z、W、Q依次为H、N、O、S、Cl;乙为含10电子的液态物质,乙为HO;则甲中应含S、Cl,丙为
2HCl。A项,原子半径: S>Cl>O,A正确;B项,由于水中分子间氢键数目大于氨气中分子间氢键数目,
硫化氢中无氢键,所以简单氢化物的沸点:HO>NH >H S,B正确;C项,化合物SCl 中不含离子键,C
2 3 2 2 2
错误;D项,非金属性Cl>S,所以最高价氧化物对应水化物的酸性HClO>H SO ,D正确; 故选C。
4 2 4
21.(2024·陕西铜川高三模拟预测)X、Y、Z、W为原子序数依次增大的四种短周期主族元素,其中Z
为金属元素,X、W为同一主族元素。X、Z、W的最高价氧化物分别为甲、乙、丙,x、y、z、w分别为
X、Y、Z、W的单质,单质w为常见半导体材料,丁是剧毒化合物,其转化关系如图所示。下列说法正确
的是( )
A.原子半径:Z>W>X>Y B.甲分子中含有非极性共价键
C.熔融条件下乙不可以导电 D.最简单氢化物热稳定性:W>X
【答案】A
【解析】X、Y、Z、W 为原子序数依次增大的四种短周期元素,其中Z为金属元素,X、Z、W形成
的最高价氧化物分别为甲、乙、丙。x、y、z、w分别为X、Y、Z、W的单质,丁是剧毒化合物。氧化物
甲能与金属单质Z反应生成氧化物乙与单质X,可知甲为CO,Z为Mg,乙为MgO,X为C,故y为O,
2 2
故X为C元素、Y为O元素、Z为Mg元素;X、W为同一主族元素,则W为Si元素;丙为SiO,W为
2
Si、丁为CO。由题干可知,元素X、Y、Z、W分别为C,O、Mg、Si。A项,同周期元素从左至右原子
半径逐渐减小,故原子半径:Z>W>X>Y,A项正确;B项,CO 分子中不含有非极性共价键,B项错误;
2
C项,MgO为离子化合物,熔融条件下可以导电,C项错误;D项,非金属元素的非金属性越强,其最简
单氢化物越稳定,故最简单氢化物热稳定性:X>W,D项错误;故选A。
22.已知X、Y、Z是三种原子序数依次增大的短周期元素。甲、乙、丙分别是三种元素形成的单质,
A、B、C、D分别是由三种元素中的两种形成的化合物,且A与C中均含有10个电子。它们之间的转化
关系如图所示。下列说法正确的是( )
A.原子半径:Z>Y>X
B.X与Z形成的化合物为共价晶体
C.Y有多种同素异形体,且均具有高熔点、高沸点、硬度大的性质
D.Y的最简单氢化物的空间结构为正四面体形【答案】D
【解析】A与C中均含有10个电子,A燃烧可生成C,由转化关系可知,A应为CH ,丙为O ,B为
4 2
CO ,C为HO,B、C都可与乙在高温下反应,乙应为C,则D为CO,甲为H ,X为H元素,Y为C元
2 2 2
素,Z为O元素。同周期主族元素从左到右原子半径逐渐减小,同主族元素,原子核外电子层数越多,原
子半径越大,所以原子半径Y>Z>X,A项错误;X为H元素,Z为O元素,二者形成的化合物,如HO、
2
HO 均为分子晶体,B项错误;Y为C元素,C元素有多种同素异形体,其中金刚石具有高熔点、高沸点、
2 2
硬度大的性质,而石墨则质地软,C项错误;Y的最简单氢化物为CH ,其空间结构为正四面体形,D项
4
正确。
23.短周期主族元素W、X、Y、Z的原子序数依次增大,Y和Z位于同一主族。m、n、p均为由这些
元素组成的二元化合物,甲、乙、丙为其中三种元素对应的单质,丙为淡黄色固体,易溶于 XZ ,n是一
2
种二元弱酸。上述物质的转化关系如图所示(反应条件省略)。下列说法正确的是( )
A.原子半径:W>Y>X B.W与X组成的化合物中只含有极性键
C.简单氢化物的沸点:YX>W
【答案】D
【解析】短周期主族元素W、X、Y、Z的原子序数依次增大,Y和Z位于同一主族。m、n、p均为由
这些元素组成的二元化合物,甲、乙、丙为其中三种元素对应的单质,丙为淡黄色固体,易溶于XZ ,丙
2
是硫单质,所以X是C,Z是S。n是一种二元弱酸,根据转化关系可判断n是HS,则甲是氢气,乙是氧
2
气。p是SO ,m是水,因此W是H,Y是O。同周期元素自左向右原子半径逐渐减小,同主族元素从上
2
到下原子半径逐渐增大,则原子半径:WZ,C项错误。
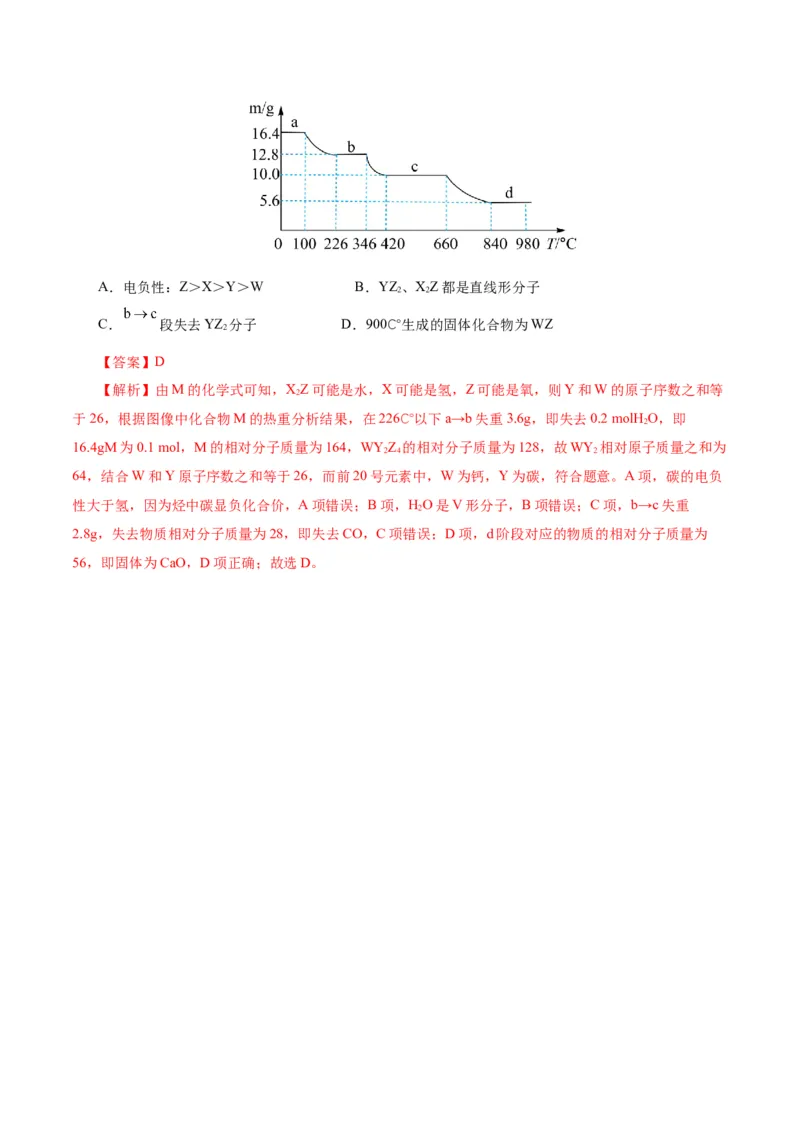
24.前20号不同主族元素 的原子序数依次增大,它们的原子序数之和等于35,分析试
剂M(WY Z·X Z)常用于稀土金属分离的载体、陶瓷上釉等。加热16.4g固体 ,剩余固体质量(m)与温度
2 4 2
(T)的关系如图所示。下列叙述正确的是( )A.电负性:Z>X>Y>W B.YZ、XZ都是直线形分子
2 2
C. 段失去YZ 分子 D.900℃生成的固体化合物为WZ
2
【答案】D
【解析】由M的化学式可知,XZ可能是水,X可能是氢,Z可能是氧,则Y和W的原子序数之和等
2
于26,根据图像中化合物M的热重分析结果,在226℃以下a→b失重3.6g,即失去0.2molHO,即
2
16.4gM为0.1mol,M的相对分子质量为164,WYZ 的相对分子质量为128,故WY 相对原子质量之和为
2 4 2
64,结合W和Y原子序数之和等于26,而前20号元素中,W为钙,Y为碳,符合题意。A项,碳的电负
性大于氢,因为烃中碳显负化合价,A项错误;B项,HO是V形分子,B项错误;C项,b→c失重
2
2.8g,失去物质相对分子质量为28,即失去CO,C项错误;D项,d阶段对应的物质的相对分子质量为
56,即固体为CaO,D项正确;故选D。