文档内容
知识清单 05 钠及其重要化合物
知识点01单质钠的结构和性质 知识点02 钠的氧化物的结构和性质
知识点03 碳酸钠的性质和应用 知识点04 碳酸氢钠的性质和应用
知识点05 碱金属元素 知识点06 焰色试验知识点 01 单质钠的结构和性质
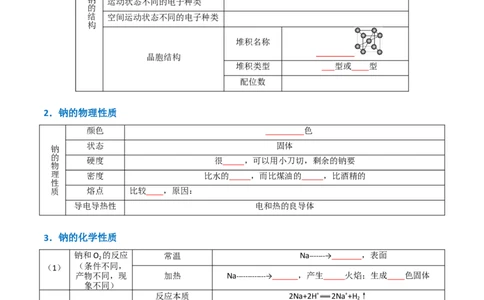
1.金属钠的结构
构成微粒 和
作用力
电子排布式
能量不同的电子种类
钠 运动状态不同的电子种类
的
结 空间运动状态不同的电子种类
构
堆积名称
晶胞结构
堆积类型 型或 型
配位数
2.钠的物理性质
颜色 色
状态 固体
钠
的
硬度 很 ,可以用小刀切,剩余的钠要
物
理 密度 比水的 ,而比煤油的 ,比酒精的
性
质 熔点 比较 ,原因:
导电导热性 电和热的良导体
3.钠的化学性质
钠和O 的反应 常温 Na-------→ ,表面
2
(1) (条件不同,
产物不同,现 加热 Na-------------→ ,产生 火焰;生成 色固体
象不同)
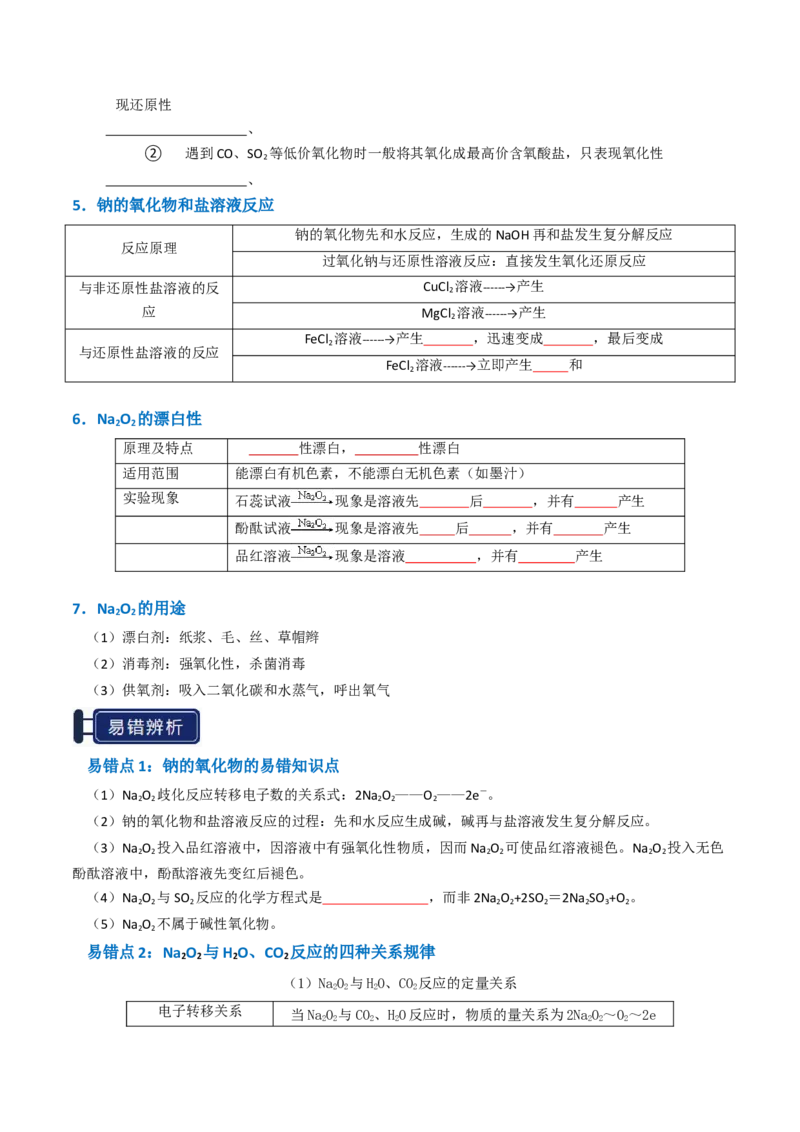
反应本质 2Na+2H+ 2Na++H ↑
2
水
钠与活性氢的
(2) 现象
反应
盐酸
乙醇现象 钠 , 反应冒出
乙酸
苯酚
反应速率快慢 > > > >
反应原理 发生 反应
钠 钠和熔融盐反应 熔融
与
(3) 盐 TiCl 4、 KCl
反
反应原理 Na
应
CuSO 溶液反应
4
主要现象 有 产生,产生 沉淀
4.钠的存在、制备、保存和用途
存在形态 只以 形式存在
制备
2NaCl(熔融) 2Na+Cl ↑
2
变质 钠在空气中长期放置最终变成
保存 一般保存在 或 中
灭火 钠着火时一般用 扑灭
制钠的化合物: 制Na O 等
2 2
冶金还原剂 从熔融的卤化物中置换出钛、锆、铌、钽等难熔金属
用途
制 灯 黄光,射程远、透雾能力强
原子反应堆导热剂 ,室温下是液体,吸热能力强
钠的易错知识点
(1)钠与盐溶液反应,不能置换出盐中的 ,如:钠与CuSO 溶液反应不能置换出铜;钠与熔
4
融的盐反应才可能置换出盐中的金属。
(2)Na与足量O 反应无论生成Na O还是Na O ,只要参与反应的Na的 相等,则转移 数一定
2 2 2 2
相等。
(3)Na分别与H O和乙醇发生反应均能生成 ,但反应的剧烈程度不同,前者反应 ,后者反
2
应 。
(4)Na与酸溶液反应:直接与 反应,而不是先和水反应。
(5)一定量的钠与足量的某溶液反应,产生氢气的量相同,与该溶液中溶质的多少无关。
(6)钠与水、酸反应的实质都是与H+的反应。
1.研究金属钠的性质,实验如下(钠的大小相同):
实验装置 液体 现象蒸馏水 Ⅰ.钠浮在水面,剧烈反应,有少量白雾
盐酸 Ⅱ.钠浮在液面,反应比I剧烈,有白雾产生
Ⅲ.钠浮在液面,反应比I缓慢,产生大量白雾,底部
浓盐酸
有白色固体
无水乙醇 Ⅳ.钠沉入底部,反应比I缓慢得多,未见有固体生成
下列说法正确的是
A.I中反应的离子方程式为
B.随着 增大,钠与盐酸反应的剧烈程度增大
C.对比实验I、Ⅳ可知羟基极性:
D.推测Ⅲ中溶液中的 以及生成的 固体对反应剧烈程度有影响
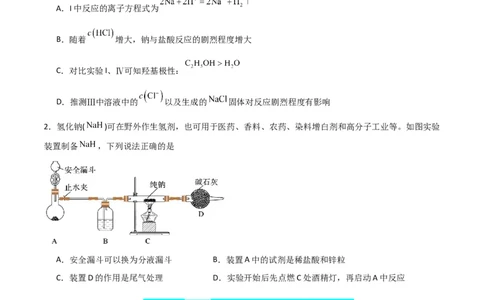
2.氢化钠( )可在野外作生氢剂,也可用于医药、香料、农药、染料增白剂和高分子工业等。如图实验
装置制备 ,下列说法正确的是
A.安全漏斗可以换为分液漏斗 B.装置A中的试剂是稀盐酸和锌粒
C.装置D的作用是尾气处理 D.实验开始后先点燃C处酒精灯,再启动A中反应
知识点 02 钠的氧化物的结构和性质
1.氧化钠和过氧化钠的比较
物质 氧化钠(NaO) 过氧化钠(NaO)
2 2 2
色态 固体 色固体
化物
类别 氧化物
(非碱性氧化物)氧的价态 -2
电子式
阴阳离子
个数比
化学键 离子键
生成条件 常温 加热或点燃
相互转化
热稳定性 不稳定 稳定
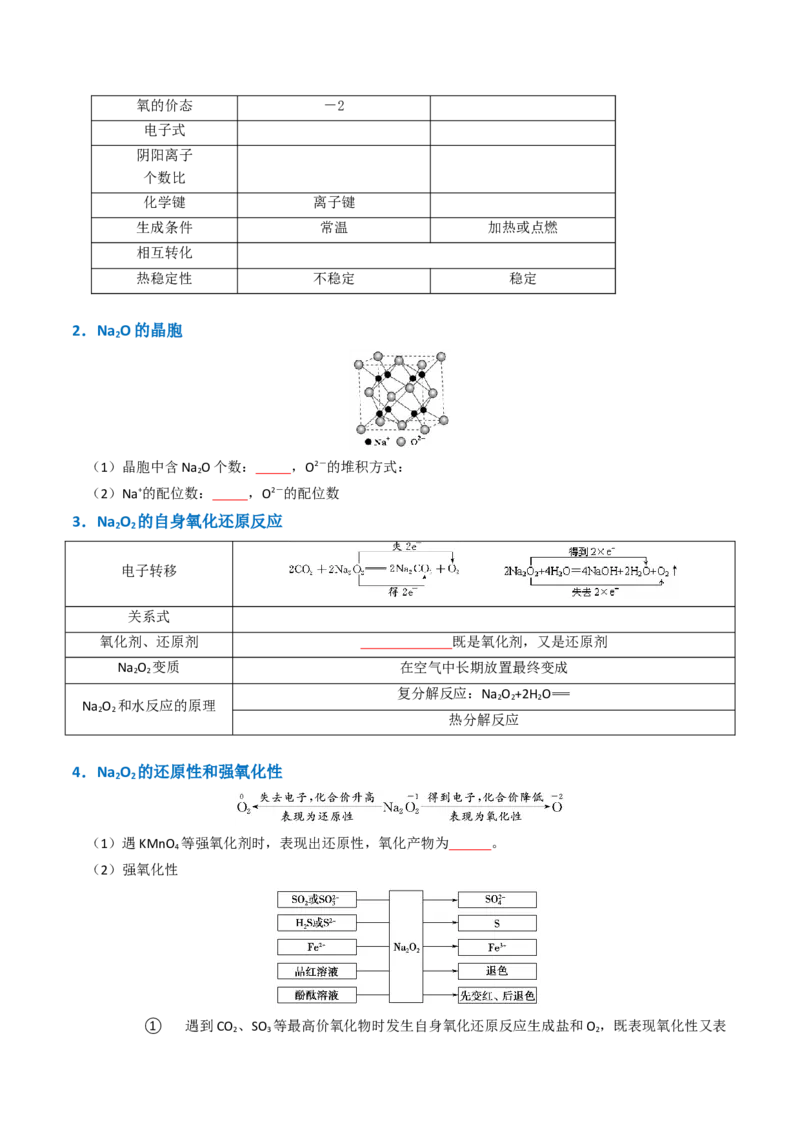
2.Na O的晶胞
2
(1)晶胞中含Na O个数: ,O2-的堆积方式:
2
(2)Na+的配位数: ,O2-的配位数
3.Na O 的自身氧化还原反应
2 2
电子转移
关系式
氧化剂、还原剂 既是氧化剂,又是还原剂
Na O 变质 在空气中长期放置最终变成
2 2
复分解反应:Na O +2H O
2 2 2
Na O 和水反应的原理
2 2
热分解反应
4.Na O 的还原性和强氧化性
2 2
(1)遇KMnO 等强氧化剂时,表现出还原性,氧化产物为 。
4
(2)强氧化性
① 遇到CO 、SO 等最高价氧化物时发生自身氧化还原反应生成盐和O ,既表现氧化性又表
2 3 2现还原性
、
② 遇到CO、SO 等低价氧化物时一般将其氧化成最高价含氧酸盐,只表现氧化性
2
、
5.钠的氧化物和盐溶液反应
钠的氧化物先和水反应,生成的NaOH再和盐发生复分解反应
反应原理
过氧化钠与还原性溶液反应:直接发生氧化还原反应
与非还原性盐溶液的反 CuCl 溶液------→产生
2
应 MgCl 溶液------→产生
2
FeCl 溶液------→产生 ,迅速变成 ,最后变成
2
与还原性盐溶液的反应
FeCl 溶液------→立即产生 和
2
6.Na O 的漂白性
2 2
原理及特点 性漂白, 性漂白
适用范围 能漂白有机色素,不能漂白无机色素(如墨汁)
实验现象 石蕊试液 现象是溶液先 后 ,并有 产生
酚酞试液 现象是溶液先 后 ,并有 产生
品红溶液 现象是溶液 ,并有 产生
7.Na O 的用途
2 2
(1)漂白剂:纸浆、毛、丝、草帽辫
(2)消毒剂:强氧化性,杀菌消毒
(3)供氧剂:吸入二氧化碳和水蒸气,呼出氧气
易错点1:钠的氧化物的易错知识点
(1)Na O 歧化反应转移电子数的关系式:2Na O ——O ——2e-。
2 2 2 2 2
(2)钠的氧化物和盐溶液反应的过程:先和水反应生成碱,碱再与盐溶液发生复分解反应。
(3)Na O 投入品红溶液中,因溶液中有强氧化性物质,因而Na O 可使品红溶液褪色。Na O 投入无色
2 2 2 2 2 2
酚酞溶液中,酚酞溶液先变红后褪色。
(4)Na O 与SO 反应的化学方程式是 ,而非2Na O +2SO =2Na SO +O 。
2 2 2 2 2 2 2 3 2
(5)Na O 不属于碱性氧化物。
2 2
易错点2:Na O 与H O、CO 反应的四种关系规律
2 2 2 2
(1)NaO 与HO、CO 反应的定量关系
2 2 2 2
电子转移关系 当NaO 与CO、HO反应时,物质的量关系为2NaO~O~2e
2 2 2 2 2 2 2-,
若CO、水蒸气(或两混合气体)通过足量NaO,气体体积的减
气体体积变化关系 2 2 2
少量是原来气体体积的,等于生成氧气的量,
由于CO 能够与NaOH反应,所以一定量的NaO 与一定量的HO
2 2 2 2
先后顺序关系 (g)和CO 的混合物反应,可视为NaO 先与CO 反应,剩余的
2 2 2 2
NaO 再与HO(g)反应。
2 2 2
CO、水蒸气分别与足量NaO 反应时,固体相当于吸收了CO 中
2 2 2 2
固体质量变化关系 的“CO”、水蒸气中的“H”,所以固体增加的质量Δm(CO)
2 2
=28 g·mol-1×n(CO),Δm(HO)=2 g·mol-1×n(HO)
2 2 2
(2)特殊应用:凡分子组成符合(CO) ·(H ) 的物质,m g该物质在O 中完全燃烧,将其产物[CO
m 2 n 2 2
和H O(g)]通入足量Na O 后,固体增重必为m g。或者是由C、H、O三种元素组成的物质,只要C、
2 2 2
O原子个数比为1∶1,即可满足上述关系。
无机化合物 H 、CO及H 和CO的混合气体
2 2
CH OH(甲醇)、HCHO(甲醛)、CH COOH(乙
3 3
有机化合物 酸)、
HCOOCH (甲酸甲酯)、C H O (葡萄糖)等
3 6 12 6
3.在潜水艇和消防员的呼吸面具中, 作为氧气的来源。下列说法不正确的是
A. 和 反应可生成
B. 可使酚酞溶液先变红色后褪色
C.工业上用未经过处理的空气和钠直接反应来制备
D.可用焰色试验来检验 中的阳离子
4.研究小组探究Na O 与水反应。取1.56gNa O 粉末加入到40mL水中,充分反应得溶液A(液体体积无明
2 2 2 2
显变化),进行以下实验。
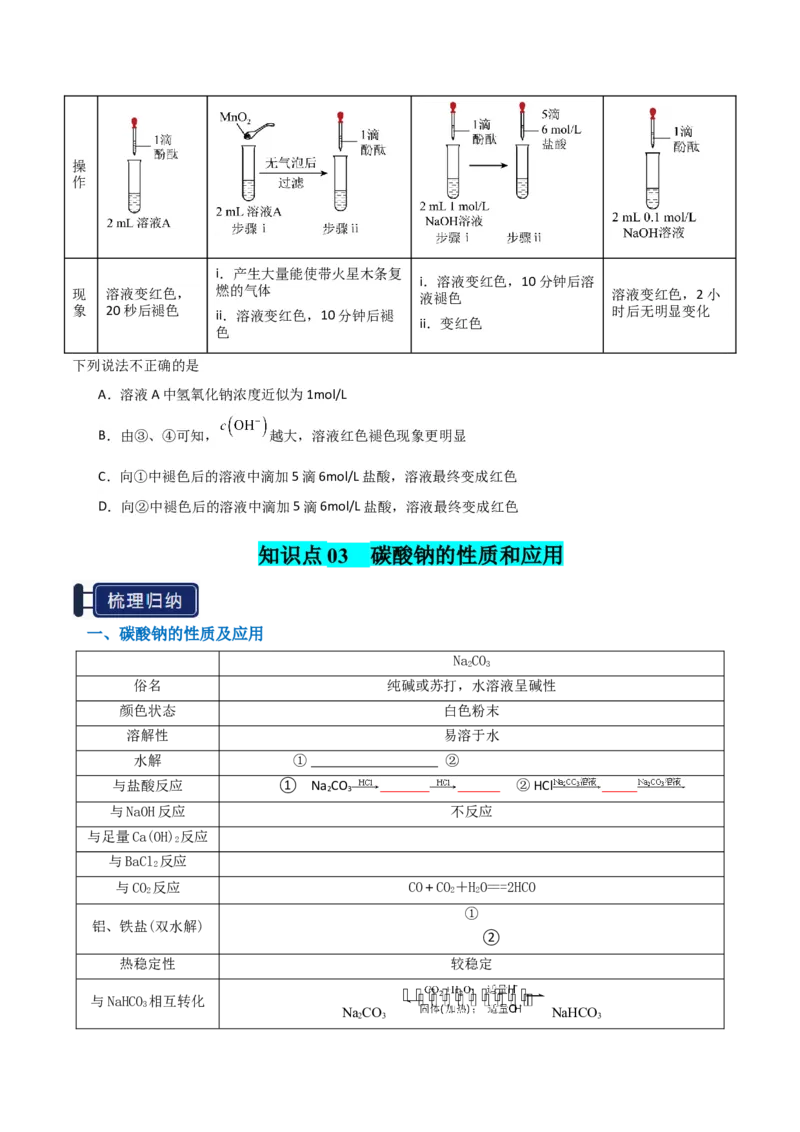
编
① ② ③ ④
号操
作
i.产生大量能使带火星木条复
i.溶液变红色,10分钟后溶
现 溶液变红色, 燃的气体 液褪色 溶液变红色,2小
象 20秒后褪色 ii.溶液变红色,10分钟后褪 时后无明显变化
ii.变红色
色
下列说法不正确的是
A.溶液A中氢氧化钠浓度近似为1mol/L
B.由③、④可知, 越大,溶液红色褪色现象更明显
C.向①中褪色后的溶液中滴加5滴6mol/L盐酸,溶液最终变成红色
D.向②中褪色后的溶液中滴加5滴6mol/L盐酸,溶液最终变成红色
知识点 03 碳酸钠的性质和应用
一、碳酸钠的性质及应用
NaCO
2 3
俗名 纯碱或苏打,水溶液呈碱性
颜色状态 白色粉末
溶解性 易溶于水
水解 ① ②
与盐酸反应 ① Na CO ②HCl
2 3
与NaOH反应 不反应
与足量Ca(OH) 反应
2
与BaCl 反应
2
与CO 反应 CO+CO+HO===2HCO
2 2 2
①
铝、铁盐(双水解)
②
热稳定性 较稳定
与NaHCO 相互转化
3
NaCO NaHCO
2 3 3制玻璃① ②
制肥皂:油脂的碱性水解,其主要成分是高级脂肪酸钠
NaCO 的用途
2 3
去污剂:热的碱液去除餐具上的油污
造纸、纺织
钠的碳酸盐的易错知识点
(1)除去CO 中的HCl气体,应选用饱和 溶液;
2
(2)向饱和Na CO 溶液中通入过量CO ,有 晶体析出。
2 3 2
(3)鉴别Na CO 和NaHCO 溶液不能用Ca(OH) 或Ba(OH) ,二者均会产生 沉淀
2 3 3 2 2
(4)Na CO 溶液与盐酸反应的过程为:Na CO NaHCO CO ,可以用互滴法鉴别两种无色溶液。
2 3 2 3 3 2
5.常温下,分别向相同浓度的NaHCO 、Na CO 溶液中逐滴加入盐酸,滴加过程中溶液的pH变化如下图
3 2 3
所示。下列说法正确的是
A.曲线①表示盐酸滴入NaHCO 溶液的过程
3
B.d、e点水的电离程度:d>e
C.a点的K 大于d点的K
W W
D.b、c、e点均满足:
6.过碳酸钠( )是一种白色固体,具有碳酸钠和过氧化氢的性质,可用于杀菌消毒等。实
验室中用如下方法合成过碳酸钠晶体。下列说法错误的是
A.采用冰水浴控制三颈烧瓶中反应的温度
B.操作①使用的玻璃仪器是漏斗、烧杯和玻璃棒
C.过碳酸钠晶体内 与 以氢键结合
D.操作③可用加热法干燥
知识点 04 碳酸氢钠的性质和应用
碳酸氢钠的性质及应用
NaHCO
3
俗名 小苏打,水溶液呈 性
颜色状态 白色细小的晶体
易溶于水(溶解度比NaCO )原因是NaHCO 中含有
2 3 3
溶解性
饱和NaCO 溶液------→现象是有
2 3
水解 HCO+HO HCO+OH-
2 2 3
与盐酸反应
与NaOH反应 HCO+OH-===CO+HO
2
与足量Ca(OH) 反应
2
少量Ca(OH) 2NaHCO+Ca(OH) CaCO↓+NaCO+2HO
2 3 2 3 2 3 2
与BaCl 反应 不反应
2
与CO 反应 不反应
2
①
与铝、铁盐(双水解)
②
与Na[Al(OH)]或NaAlO
4 2
酸碱中和反应热稳定性 2NaHCO=====NaCO+CO↑+HO
3 2 3 2 2
与碳酸钠相互转化
NaCO NaHCO
2 3 3
流程:饱和NaCl NaHCO NaCO
3 2 3
原理:利用NaHCO 的溶解度小,析出晶体
3
侯氏制碱法 ② 制NaHCO :
3
③ 制Na CO :
2 3
④ 循环利用的物质:
发酵粉:①中和食品发酵产生的有机酸;②加热分解产生大量CO
2
治胃酸:中和胃中过多的盐酸
NaHCO 的用途
3
干粉灭火剂①:
泡沫灭火器②:Al3++3HCO- Al(OH)↓+3CO↑
3 3 2
易混易错点:碳酸钠、碳酸氢钠的除杂和鉴别
1.Na CO 、NaHCO 的除杂
2 3 3
序号 混合物(括号内为杂质) 除杂方法
① Na CO (s)(NaHCO )
2 3 3
NaHCO (aq)
② 3
(Na CO )
2 3
Na CO (aq)
③ 2 3
(NaHCO )
3
2.Na CO 、NaHCO 的鉴别
2 3 3
(1)固体的鉴别
①加热法:产生使澄清石灰水变浑浊的气体的是 固体。
②气体法:滴入稀盐酸,产生气泡速率快的是 固体。
(2)溶液的鉴别
①沉淀法:加入 溶液或 溶液,产生沉淀的是Na CO 溶液。
2 3
②测pH法:用pH试纸测相同浓度的稀溶液,pH大的是 溶液。
3.Na CO 和NaHCO 的检验
2 3 3
(1)步骤
①向溶液中加入足量的 溶液或 溶液,过滤
③ 分别向沉淀和滤液中加入足量的
③将产生的气体依次通过 溶液和
(2)现象及结论:品红溶液不褪色,澄清石灰水变浑浊①沉淀上产生该现象:原溶液中含有
② 滤液中产生该现象:原溶液中含有
③ 同时产生该现象:原溶液中含有Na CO 和NaHCO
2 3 3
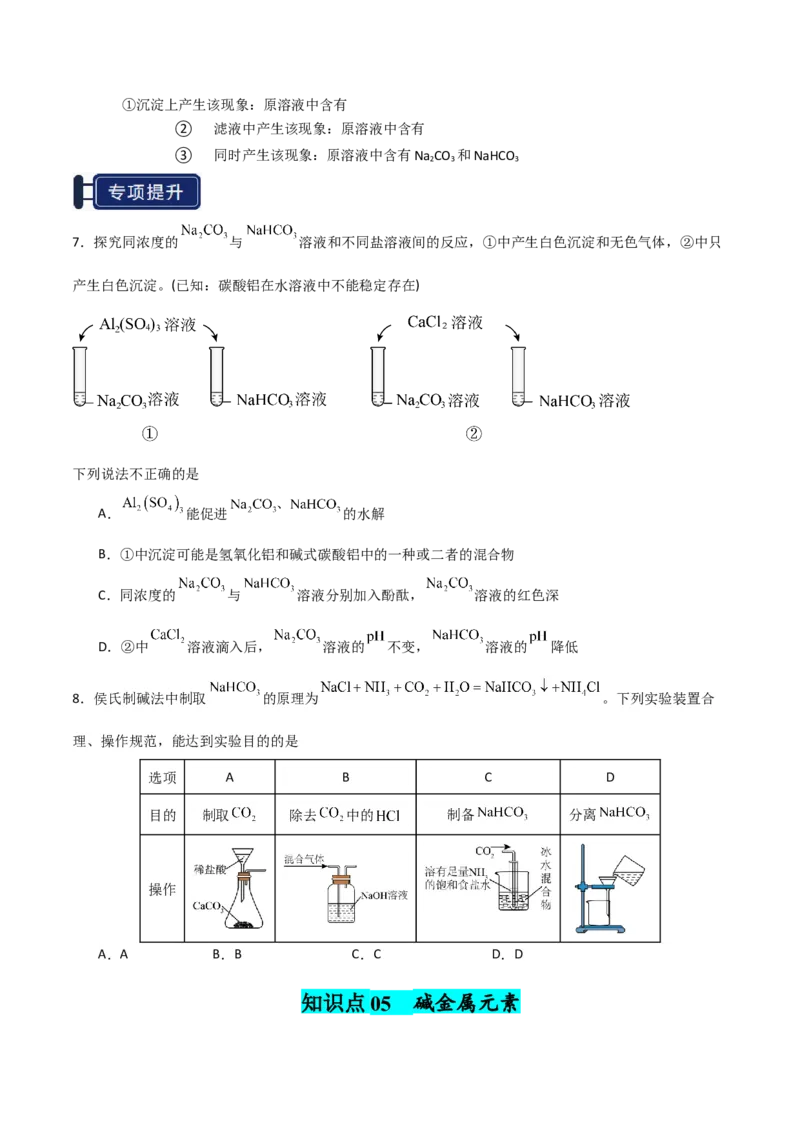
7.探究同浓度的 与 溶液和不同盐溶液间的反应,①中产生白色沉淀和无色气体,②中只
产生白色沉淀。(已知:碳酸铝在水溶液中不能稳定存在)
下列说法不正确的是
A. 能促进 的水解
B.①中沉淀可能是氢氧化铝和碱式碳酸铝中的一种或二者的混合物
C.同浓度的 与 溶液分别加入酚酞, 溶液的红色深
D.②中 溶液滴入后, 溶液的 不变, 溶液的 降低
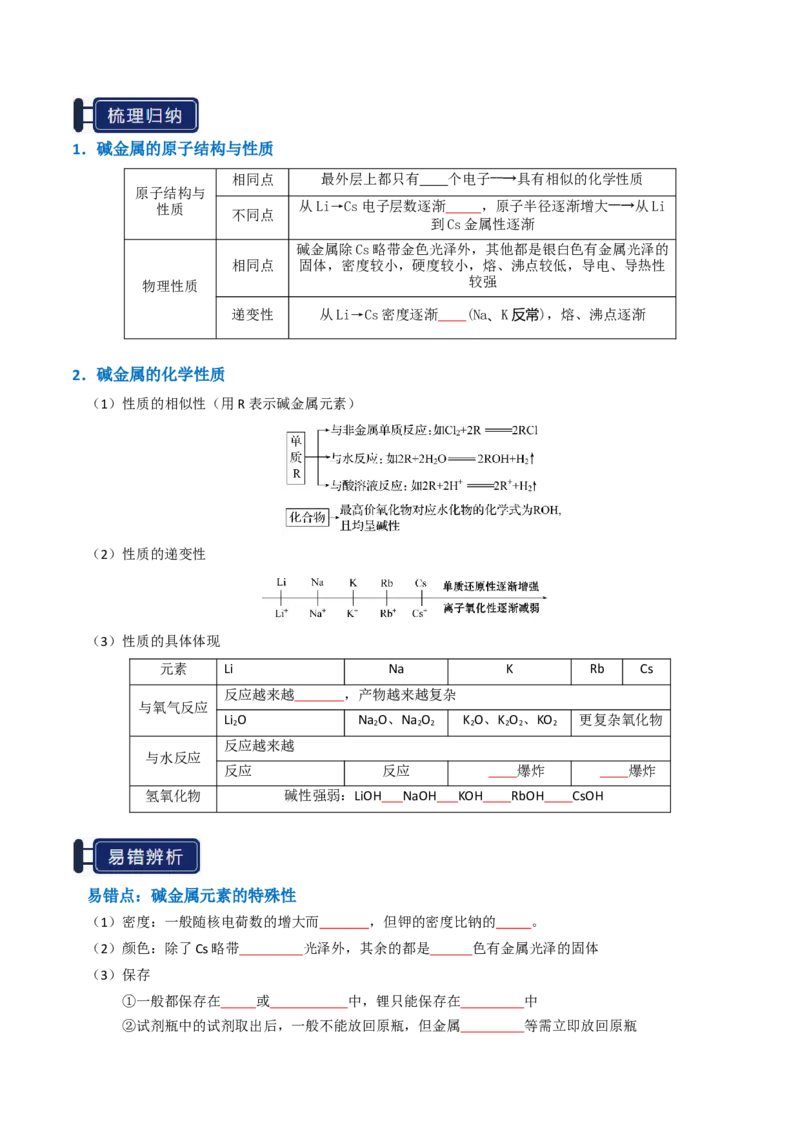
8.侯氏制碱法中制取 的原理为 。下列实验装置合
理、操作规范,能达到实验目的的是
选项 A B C D
目的 制取 除去 中的 制备 分离
操作
A.A B.B C.C D.D
知识点 05 碱金属元素1.碱金属的原子结构与性质
相同点 最外层上都只有 个电子――→具有相似的化学性质
原子结构与
性质 从Li→Cs电子层数逐渐 ,原子半径逐渐增大――→从Li
不同点
到Cs金属性逐渐
碱金属除Cs略带金色光泽外,其他都是银白色有金属光泽的
相同点 固体,密度较小,硬度较小,熔、沸点较低,导电、导热性
较强
物理性质
递变性 从Li→Cs密度逐渐 (Na、K反常),熔、沸点逐渐
2.碱金属的化学性质
(1)性质的相似性(用R表示碱金属元素)
(2)性质的递变性
(3)性质的具体体现
元素 Li Na K Rb Cs
反应越来越 ,产物越来越复杂
与氧气反应
Li O Na O、Na O K O、K O 、KO 更复杂氧化物
2 2 2 2 2 2 2 2
反应越来越
与水反应
反应 反应 爆炸 爆炸
氢氧化物 碱性强弱:LiOH NaOH KOH RbOH CsOH
易错点:碱金属元素的特殊性
(1)密度:一般随核电荷数的增大而 ,但钾的密度比钠的 。
(2)颜色:除了Cs略带 光泽外,其余的都是 色有金属光泽的固体
(3)保存
①一般都保存在 或 中,锂只能保存在 中
②试剂瓶中的试剂取出后,一般不能放回原瓶,但金属 等需立即放回原瓶(4)盐的溶解性
①一般情况下,碱金属所形成的盐均 水,并且在一定温度下,酸式盐比正盐的溶解度
②NaHCO 的溶解度比Na CO 的
3 2 3
(5)碱金属氢化物(如NaH):碱金属可与H 发生反应生成RH(R代表碱金属),属于离子化合物,H元素
2
显-1价,碱金属氢化物是强还原剂。如NaH+HO===NaOH+H↑,NaH是还原剂,HO是氧化剂,氧化产物
2 2 2
为 H,还原产物也为 H。
2 2
(6)锂与O 反应与钠不同,只生成 ,而不生成Li O 。
2 2 2
(7)碱金属氧化物的结构
氧化物 氧化钠 过氧化钠 超氧化钾 臭氧化钾
化学式 Na O Na O KO KO
2 2 2 2 3
1 1
氧的价态 -2价 -1价
-2价 -3价
所含离子 2Na++1 2Na++1 K++1 K++1
化学键 离子键 离子键和 和共价键 离子键和共价键
9.下列关于Li、Na、K、Rb、Cs的叙述均正确的一组是
①金属性最强的是铯
②形成的离子中氧化性最强的是锂离子
③在自然界中均以化合态形式存在
④Li的密度最小
⑤铯与水反应十分剧烈,甚至会发生爆炸
⑥它们的氧化物都只有 和 两种形式
⑦粒子半径:
A.①②③④ B.④⑤⑥⑦ C.②⑥ D.①②③④⑤⑦
10.第87号元素钫,它位于碱金属族,根据元素周期表结构及元素性质变化趋势,下列关于碱金属某些元
素原子结构和性质的判断,错误的是
①锂与水反应比钠剧烈 ②金属单质都可以密封保存在煤油中 ③钾的氧化物暴露在空气中易吸收二氧化
碳 ④锂的阳离子的最外层电子数和钠的相同 ⑤钫单质是强还原剂 ⑥钫在化合物中显+1价 ⑦钫单质
的密度应该大于 ⑧钫单质有较高的熔点A.①②④⑧ B.①②③⑦ C.③④⑤⑧ D.①③④⑥
知识点 06 焰色试验
1.实验图示
2.操作顺序
3.图解操作
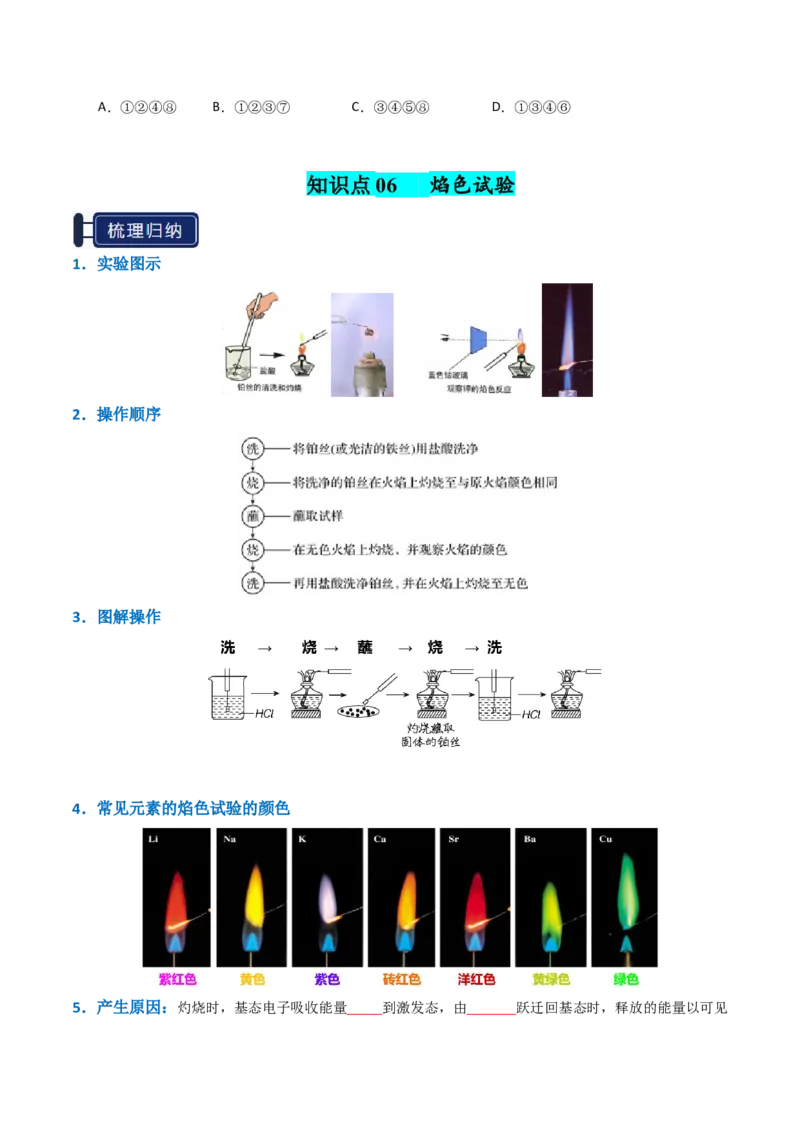
4.常见元素的焰色试验的颜色
5.产生原因:灼烧时,基态电子吸收能量 到激发态,由 跃迁回基态时,释放的能量以可见光形式呈现
易错点:焰色试验“易错点”
(1)焰色试验体现的是元素的性质,无论元素是游离态还是化合态,同一元素均具有相同的 。
(2)焰色试验发生的是 变化。
(3)在观察钾元素的焰色时,应透过蓝色的钴玻璃片观察,蓝色钴玻璃可以将 过滤掉,避免钠元
素的干扰。
①若肉眼看不到紫色火焰,则样品中 含钾元素
②若肉眼看到紫色火焰,则样品中 含钠元素
(4)洗涤做焰色反应的铂丝,可选用稀盐酸,不能用稀硫酸。选用稀盐酸,生成的 在高温时可
挥发,不能选择稀硫酸,硫酸不挥发。
11.下列有关焰色试验操作的描述正确的是
A.取一根洁净的细铁丝,放在酒精灯上灼烧至无色,再蘸取少量NaCl溶液,进行焰色试验
B.在观测焰色试验时均要透过蓝色钴玻璃片,以便隔绝钠元素的黄光的干扰
C.铂丝在做完氯化钠溶液的焰色试验后,用稀硫酸洗净,再蘸取少量的K SO 溶液,重复以上实验
2 4
D.用洁净的铂丝蘸取某溶液,放在火焰上灼烧,观察到黄色火焰,则证明该溶液中一定有Na+,没有
K+
12.下列说法中正确的是
A.焰色试验是化学变化
B.用稀硫酸清洗做焰色试验的铂丝(镍丝或铁丝)
C.焰色试验均应透过蓝色钴玻璃观察
D.利用焰色试验不能区分NaCl与Na CO 固体
2 3