文档内容
专题 01 物质及其变化
第 02 练 离子反应
1.下列物质中,属于电解质的是( )
A.Zn B.NaOH C.稀HNO D.KSO 溶液
3 2 4
2.下列属于强电解质的是( )
A.Al B.CHOH C.NH ·H O D.BaSO
3 3 2 4
3.下列属于非电解质的是( )
A.SO B.KClO C.Ca(OH) D.Cl
3 3 2 2
4.下列属于电解质的是( )
A.氯化钠 B.蔗糖 C.氯气 D.铁
5.下列物质中属于电解质而且能导电的是( )
A.Cu(OH) 浊液 B.熔融的MgO C.煤油 D.SO
2 2
6.下列物质的水溶液能导电,且属于强电解质的是( )
A.CHCOOH B.Cl C.NH HCO D.SO
3 2 4 3 3
7.下列反应可以用离子方程式表示,又属于氧化还原反应的是( )
A.Zn与CuSO 溶液反应 B.HS气体的燃烧
4 2
C.NH Cl与Ca(OH) 加热制NH D.CO 与NaOH溶液反应
4 2 3 2
8.下列物质在水溶液中的电离方程式书写正确的是( )
A.NaHCO ===Na++HCO B.Al O===2Al3++3O2-
3 2 3
C.MgCl ===Mg2++Cl D.NaHSO===Na++HSO
2 4
9.KSO 的电离方程式书写正确的是( )
2 4
A.KSO =K++SO2- B.KSO =2K++ SO 2-
2 4 4 2 4 4
C.KSO =K++2SO2- D.KSO =K2++ SO 2-
2 4 4 2 4 4
【答案】B
【解析】硫酸钾是强电解质完全电离出K+和SO 2- ,电离方程式为KSO =2K++ SO 2-;故选B。
4 2 4 4
10.下列方程式书写正确的是( )
A.醋酸的电离方程式:CHCOOH=CH COO-+H+
3 3
B.钠与水反应的离子方程式:Na+2HO=Na++2OH-+H ↑
2 2C.用过量氨水吸收二氧化硫气体:NH •H O+SO =NHHSO
3 2 2 4 3
D.乙烯使溴的四氯化碳溶液褪色:CH=CH +Br →CHBrCHBr
2 2 2 2 2
11.下列方程式不正确的是( )
A.镁在二氧化碳中燃烧的化学方程式:2Mg+CO 2MgO+C
2
B.一水合氨在水中的电离方程式:NH ·H O= +OH-
3 2
C.氯化铁水解的离子方程式:Fe3++3HO Fe(OH) +3H+
2 3
D.乙醇在铜催化下被氧化的化学方程式:2CHCHOH+O 2CHCHO+2HO
3 2 2 3 2
12.下列离子方程式正确的是( )
A.向硫酸溶液中加入Cu:Cu+2H+=Cu2++H ↑
2
B.氢氧化钡溶液与稀硫酸反应:Ba2++SO2-+ H++OH-=BaSO ↓+H O
4 4 2
C.钠与水反应:Na+2HO=Na++OH-+ H ↑
2 2
D. 与稀硝酸反应:3Cu +2NO -+8H+=3Cu2++NO↑+4HO
3 2
13.下列离子方程式书写正确的是( )
A.铜与浓硫酸在加热条件下反应:Cu+4H++SO2- Cu2++ SO ↑+2H O
4 2 2
B.水玻璃中通入过量二氧化碳气体:SiO2-+CO +H O=HSiO↓+CO 2-
3 2 2 2 3 3
C.(NH )SO 溶液与Ba(OH) 溶液反应:Ba2++SO2-=BaSO ↓
4 2 4 2 4 4
D.过量铁粉与稀硝酸反应:3Fe +2NO -+8H+=3Fe 2++NO↑+4HO
3 2
14.室温下,下列各组离子在指定溶液中能大量共存的是( )
A.FeCl 溶液中:K+、H+、NO -、SO 2-
2 3 4
B.无色透明溶液中:K+、Mg2+、Cl-、NO -
3
C.强酸性溶液中:K+、Na+、HCO -、Cl-
3
D.FeCl 溶液中:Na+、SO 2-、SCN-、NO -
3 4 3
15.下列各组离子在溶液中能大量共存的是( )
A.Na+、NH +、Cl-、OH- B.Na+、Fe2+、H+、NO -
4 3
C.Na+、NH +、SO 2-、Cl- D.K+、Ba2+、SO 2-、Cl-
4 4 4
1.下列离子方程式正确的是( )
A.大理石与醋酸反应:CO2-+2CHCOOH=2CHCOO-+HO+CO↑
3 3 3 2 2B.高锰酸钾与浓盐酸制氯气的反应:MnO -+4Cl-+8H+=Mn2++2Cl↑+4HO
4 2 2
C.漂白粉溶液吸收少量二氧化硫气体:SO +HO+ClO-=SO 2-+Cl-+2H+
2 2 4
D.氢氧化钠溶液与过量的碳酸氢钙溶液反应:OH-+Ca2++HCO -=CaCO ↓+2HO
3 3 2
2.下列检验方法或指定反应的离子(或化学)方程式正确的是( )
A.向NaAlO 溶液中滴入Ca(HCO ) 溶液:AlO-+HCO-+H O=Al(OH) ↓+CO 2-
2 3 2 2 3 2 3 3
B.用溴水检验丙烯醛CH=CHCHO中的碳碳双键:CH=CHCHO+Br→CHBr—CHBr—CHO
2 2 2 2
C.NaS溶液吸收少量SO [已知K (H SO )>K (H S)]:S2-+SO+H O=SO 2-+HS↑
2 2 a2 2 3 a1 2 2 2 3 2
D.往二元弱酸亚磷酸(H PO )溶液中滴加过量的烧碱溶液:HPO +2OH-=HPO 2-+2H O
3 3 3 3 3 2
3.下列反应的离子方程式书写正确的是( )
A.硫酸铜溶液中加过量的氨水:Cu2++2NH ·H O=Cu(OH) ↓+2NH +
3 2 2 4
B.用食醋检验牙膏中碳酸钙的存在:CaCO +2H+=Ca2++CO↑+HO
3 2 2
C.将去膜的铝片投入到NaOH溶液中:2Al+2OH—+6H O=2[Al(OH) ]— +3H ↑
2 4 2
D.用碘化钾淀粉溶液检验亚硝酸钠中NO -的存在:NO -+2I-+2H+=NO↑+I +HO
2 2 2 2
4.不能正确表示下列变化的离子方程式的是( )
A.MnO 与浓盐酸加热:MnO +4H++2Cl- Mn2++Cl↑+2HO
2 2 2 2
B.FeCl 溶液在空气中变质:12Fe2++3O+6HO=8Fe3++4Fe(OH) ↓
2 2 2 3
C.NaClO溶液中通入少量CO:2ClO-+CO+HO=2HClO+CO2-
2 2 2 3
D.R-NH 电离:R-NH +HO R-NH ++OH-
2 2 2 3
5.下列离子方程式不正确的是( )
A.Ba(OH) 溶液中滴加NaHSO 至完全沉淀:Ba2++OH-+H++SO2-=BaSO ↓+H O
2 4 4 4 2
B.漂白粉的生产原理:2OH-+Cl=Cl-+ClO-+H O
2 2
C.二氧化硫通入溴水中,溴水褪色:SO +Br +2HO=4H++2Br-+SO 2-
2 2 2 4
D.AlCl 溶液加入过量的氨水:Al3++3NH·H O=Al(OH) ↓+3NH+
3 3 2 3 4
6.工业废水中存在大量的Na+、Cl-、Cu2+、SO 2-,欲除去其中的Cu2+、SO 2-,设计工艺流程如图所示:
4 4
下列有关说法错误的是( )
A.NaOH的作用是除去Cu2+
B.试剂a为NaCO,试剂b为BaCl
2 3 2
C.操作x为过滤,试剂c为稀盐酸
D.检验SO 2-是否除尽可取适量待测溶液,先加入盐酸,再加入BaCl 溶液
4 27.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.在0.01 mol/L Ba(OH) 溶液中:Al3+、NH、NO、HCO
2
B.0.1 mol/L的FeCl 溶液中:H+、Al3+、SO、ClO-
2
C.滴加KSCN溶液显红色的溶液中:NH、K+、Cl-、I-
D.由水电离产生的c(H+)=1×10-13 mol/L的溶液中:Na+、Ba2+、NO、Cl-
8.下列各组粒子在指定溶液中一定能大量共存的是( )
A.中性透明溶液中:K+、SO、NO、Fe3+
B.在酸性KMnO 溶液中:SO、Mg2+、NO、CHCHOH
4 3 2
C.常温下由水电离出的c(H+)·c(OH-)=10-20 mol2·L-2的溶液中:Na+、NH、Cl-、SiO
D.离子的物质的量浓度相同的溶液中:CHCOO-、SO、NH、Cu2+
3
9.25 ℃时,下列各组离子在指定溶液中一定能大量共存的是( )
A.pH=1的溶液中:Na+、K+、MnO、CO
B.c(H+)=1×10-13 mol·L-1的溶液中:Mg2+、Cu2+、SO、NO
C.0.1 mol·L-1 NH HCO 溶液中:K+、Na+、NO、Cl-
4 3
D.0.1 mol·L-1 FeCl 溶液中:Fe2+、NH、SCN-、SO
3
10.(2022•广东选择性考试)实验室进行粗盐提纯时,需除去Ca2+、Mg2+和SO 2-,所用试剂包括BaCl
4 2
以及( )
A.NaCO、NaOH、HCl B.NaCO、HCl、KOH
2 3 2 3
C.KCO、HNO、NaOH D.NaCO、NaOH、HNO
2 3 3 2 3 3
11.甲、乙、丙、丁四位同学分别进行实验,测定四份不同澄清溶液的成分,记录如下:
甲 MgCl 、NaSO 、 KOH 乙 KCO、Ba(OH) 、 NaCl
2 2 4 2 3 2
丙 KSO 、CuCl 、 NaCl 丁 HCl、KCl、 NaCO
2 4 2 2 3
其中记录合理的是( )
A.甲 B.乙 C.丙 D.丁
12.(NH )SO 是一种常见的化肥,某工厂用石膏、NH 、HO和 制备(NH )SO 的工艺流程如肉,
4 2 4 3 2 4 2 4
下列说法不正确的是( )A.通入NH 和CO 的顺序不可以互换
3 2
B.步骤②中反应的化学方程式为:CaSO+2NH+CO +H O=(NH )SO +CaCO ↓
4 3 2 2 4 2 4 4
C.操作1为分液
D.操作2为将滤液蒸发浓缩、降温结晶、过滤、洗涤、干燥,可得(NH )SO
4 2 4
13.某溶液中可能含有K+、Fe3+、 NH +、CO2-、SO 2-和Cl-。取该溶液100mL,加入过量NaOH溶液
4 3 4
加热,得到0.02mol气体,同时产生红褐色的沉淀;沉淀过滤、洗涤、灼烧,得到1.6g固体;向滤液中加
足量BaCl 溶液,得到4.66g不溶于盐酸的沉淀。由此可知原溶液中( )
2
A.至少存在5种离子
B.Cl- 一定存在,且c(Cl- ) ≥0.4mol/L
C.NH +、SO 2-一定存在,Cl-可能不存在
4 4
D.CO2-、 K+一定不存在,Cl-可能存在
3
14.某钠盐溶液中可能含有SO 2-、SO 2-、NO -、CO2-、Cl-、I-等阴离子。现取2份此溶液样品,编号
4 3 3 3
①②,分别进行如下实验:
向①中加入足量BaCl 溶液,产生白色沉淀,加稀硝酸后沉淀消失且有气体生成。
2
向②中加入过量的硝酸酸化的AgNO 溶液,有沉淀生成且放出无色气体,该气体遇空气变红棕色。
3
根据上述实验现象,下列说法正确的是( )
A.原溶液中CO2-与SO 2-至少存在一种.
3 3
B.原溶液中一定存在Na+、CO2-、I-
3
C.原溶液中一定存在CO2-,可能存在SO 2-、Cl-
3 3
D.原溶液中一定不存在SO 2-、I-,无法判断是否存在SO 2-
4 3
1.(2022•全国甲卷)能正确表示下列反应的离子方程式为( )
A.硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
B.明矾溶液与过量氨水湿合:Al3++4NH+2H O=AlO-+4NH+
3 2 2 4
C.硅酸钠溶液中通入二氧化碳:SiO2-+CO +H O=HSiO -+HCO-
3 2 2 3 3D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO2-
2 4 4 4
=BaSO ↓+2H O
4 2
2.(2022•全国乙卷)某白色粉末样品,可能含有NaSO 、NaSO 、NaSO 和NaCO。取少量样品进
2 4 2 3 2 2 3 2 3
行如下实验:
①溶于水,得到无色透明溶液
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
③取②的上层清液,向其中滴加BaCl 溶液有沉淀生成。
2
该样品中确定存在的是( )
A.NaSO 、NaSO B.NaSO 、NaSO
2 4 2 2 3 2 3 2 2 3
C.NaSO 、NaCO D.NaSO 、NaCO
2 4 2 3 2 3 2 3
3.(2022•湖南选择性考试)下列离子方程式正确的是( )
A.Cl 通入冷的 NaOH溶液:Cl+2OH-=Cl-+ClO-+H O
2 2 2
B.用醋酸和淀粉 溶液检验加碘盐中的IO -:IO -+5I-+6H+=3I +3H O
3 3 2 2
C.FeSO 溶液中加入HO 产生沉淀:2Fe2++ H O+4H O=2Fe(OH) ↓+4H+
4 2 2 2 2 2 3
D.NaHCO 溶液与少量的Ba(OH) 溶液混合:HCO -+Ba2++OH-=BaCO ↓+H O
3 2 3 3 2
4.(2022•广东选择性考试)下列关于 的化合物之间转化反应的离子方程式书写正确的是( )
A.碱转化为酸式盐:OH-+2H++CO 2-=HCO-+H O
3 3 2
B.碱转化为两种盐:Cl+2OH-=Cl-+ClO-+H O
2 2
C.过氧化物转化为碱:2O2-+2H O=4OH-+O ↑
2 2 2
D.盐转化为另一种盐:NaSiO+2H+=H SiO↓+2Na+
2 3 2 3
5.(2022·浙江省1月选考)下列实验对应的离子方程式不正确的是( )
A.将碳酸氢钙溶液与过量的澄清石灰水混合:HCO -+Ca2++OH-=CaCO ↓+H O
3 3 2
B.将少量NO 通入NaOH溶液:2NO +2OH-= NO -+NO-+H O
2 2 3 2 2
C.将少量SO 通入NaClO溶液:SO +H O+2ClO-= SO 2-+2HClO
2 2 2 3
D.向氨水中滴入少量硝酸银溶液:Ag++2NH·H O= Ag(NH)++2H O
3 2 3 2 2
6.(2022·浙江省6月选考)下列反应的离子方程式不正确的是( )
A.盐酸中滴加NaSiO 溶液:SiO2-+2H+= H SiO↓
2 3 3 2 3
B.NaCO 溶液中通入过量SO :CO2-+ SO +H O=2HSO -+ CO
2 3 2 3 2 2 3 2
C.乙醇与KCr O 酸性溶液反应:3CHCHOH+2Cr O2-+16H+→3CHCOOH+4Cr3++11H O
2 2 7 3 2 2 7 3 2
D.溴与冷的NaOH溶液反应:Br +OH-= Br-+ BrO-+H+
2
7.(2021•全国乙卷)下列过程中的化学反应,相应的离子方程式正确的是( )A.用碳酸钠溶液处理水垢中的硫酸钙:CO2-+CaSO =CaCO +SO2-
3 4 3 4
B.过量铁粉加入稀硝酸中:Fe+4H++NO-=Fe3++NO↑+2HO
3 2
C.硫酸铝溶液中滴加少量氢氧化钾溶液:Al3++4OH-=AlO +2H O
2 2
D.氯化铜溶液中通入硫化氢:Cu2++S2-=CuS↓
8.(2021•浙江1月选考)下列反应的方程式不正确的是( )
A.石灰石与醋酸反应:CO2-+2CH COOH=2CH COO- +CO ↑+H O
3 3 3 2 2
B.铜片上电镀银的总反应(银作阳极,硝酸银溶液作电镀液):Ag(阳极) Ag(阴极)
C.铜与稀硝酸反应:3Cu+2NO-+8H+=3Cu2+ +2NO↑+4HO
3 2
D.明矾溶液中加入少量氢氧化钡溶液:2Al3+ +3SO2-+ 3Ba2++6OH-=2Al(OH) ↓+ 3BaSO↓
4 3 4
9.(2021•浙江6月选考)不能正确表示下列变化的离子方程式是( )
A.碳酸镁与稀盐酸反应:CO2-+2H+= H O+CO↑
3 2 2
B.亚硫酸氢钠的水解:HSO -+H O HSO +OH-
3 2 2 3
C.锌溶于氢氧化钠溶液:Zn+2OH-+2H O=[Zn(OH) ]-+H ↑
2 4 2
D.亚硝酸钠与氯化铵溶液受热反应:NO -+NH+ N↑+2H O
2 4 2 2
10.(2021•北京卷)下列方程式书写错误的是( )
A.CHCOONa溶液呈碱性:CHCOO-+H O CHCOOH+OH-
3 3 2 3
B.高锰酸钾与草酸反应:2 MnO-+5C O2-+1⇌6H+=2Mn2++10CO ↑+8H O
4 2 4 2 2
C.铝与NaOH溶液反应:2Al+2NaOH+2H O=2NaAlO +3H ↑
2 2 2
D.将SO 通入HS溶液,得到黄色浊液:SO +2H S=3S↓+2H O
2 2 2 2 2
11.(2021•天津卷)常温下,下列各组离子在给定溶液中能大量共存的是( )
A.pH=1的溶液:Fe2+、Mg2+、SO 2-、NO -
4 3
B.pH=12的溶液:K+、Na+、NO -、CO2-
3 3
C.pH=7的溶液:Na+、Cu2+、S2-、Cl-
D.pH=7的溶液:Al3+、K+、Cl-、HCO -
3
12.(2021•湖北选择性考试)对于下列实验,不能正确描述其反应的离子方程式是( )
A.向氢氧化钡溶液中加入盐酸:H+OH=HO
2
B.向硝酸银溶液中滴加少量碘化钾溶液:Ag+I=AgI↓
C.向烧碱溶液中加入一小段铝片:2Al+2OH+6HO=2[Al(OH) ]+3H↑
2 4 2
D.向次氯酸钙溶液中通入少量二氧化碳气体:ClO+CO+HO=HClO+HCO
2 2 3
13.下列A~D四组反应中,其中I和II可用同一个离子方程式表示的是( )I II
A 把金属铁放入稀硫酸中 把金属铁放入稀硝酸中
B 将3 mol Cl 通入含1 mol FeBr 的溶液 将1 mol Cl 通入含3 mol FeBr 的溶液
2 2 2 2
C NaHSO 溶液与Ba(OH) 溶液反应恰好呈中性 NaHSO 溶液与Ba(OH) 溶液反应使SO 2-恰好沉淀
4 2 4 2 4
D Ca(OH) 溶液中加入足量的NaHCO 溶液 Ca(HCO ) 溶液中加入足量的NaOH溶液
2 3 3 2
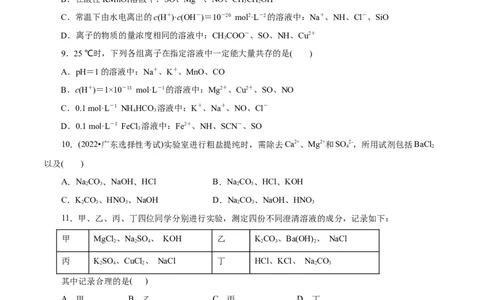
14.下列实验方案与实验结论均正确的是( )
选项 实验方案 实验结论
稀盐酸可以将Fe2+氧
A 向Fe(NO ) 溶液中滴加稀盐酸,再加入几滴KSCN溶液,溶液变为红色
3 2 化为Fe3+
取未知溶液于试管中,加入足量稀盐酸,无明显现象,再加入BaCl 溶
B 2 溶液中一定含有SO 2-
液,溶液中有白色沉淀生成 4
取未知溶液于试管中,加入BaCl 溶液,有白色沉淀生成,再加入足量
C 2 溶液中一定含有SO 2-
稀盐酸,沉淀不溶解 4
取未知溶液于试管中,滴入几滴0.1mol·L-1的NaOH溶液,将湿润的红
D 溶液中不含NH +
色石蕊试纸放在试管口处,试纸不变色 4
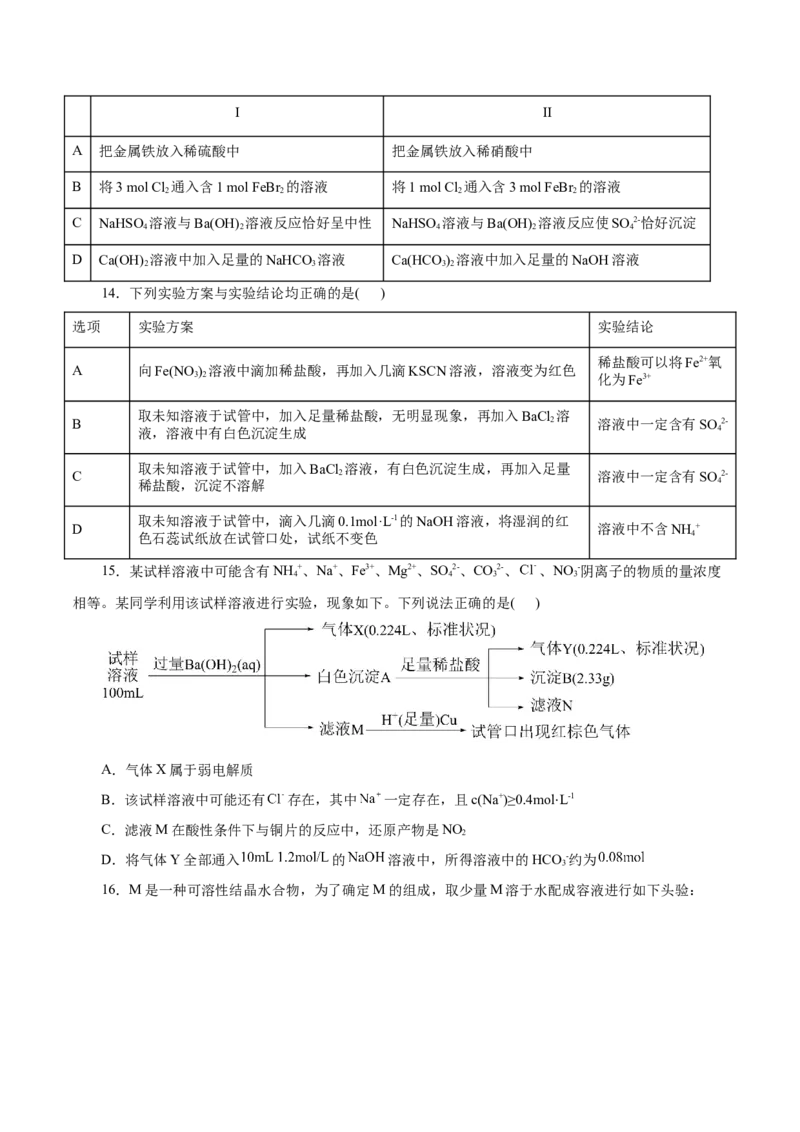
15.某试样溶液中可能含有NH +、Na+、Fe3+、Mg2+、SO 2-、CO2-、 、NO -阴离子的物质的量浓度
4 4 3 3
相等。某同学利用该试样溶液进行实验,现象如下。下列说法正确的是( )
A.气体X属于弱电解质
B.该试样溶液中可能还有 存在,其中 一定存在,且c(Na+)≥0.4molL-1
C.滤液M在酸性条件下与铜片的反应中,还原产物是NO ⋅
2
D.将气体Y全部通入 的 溶液中,所得溶液中的HCO -约为
3
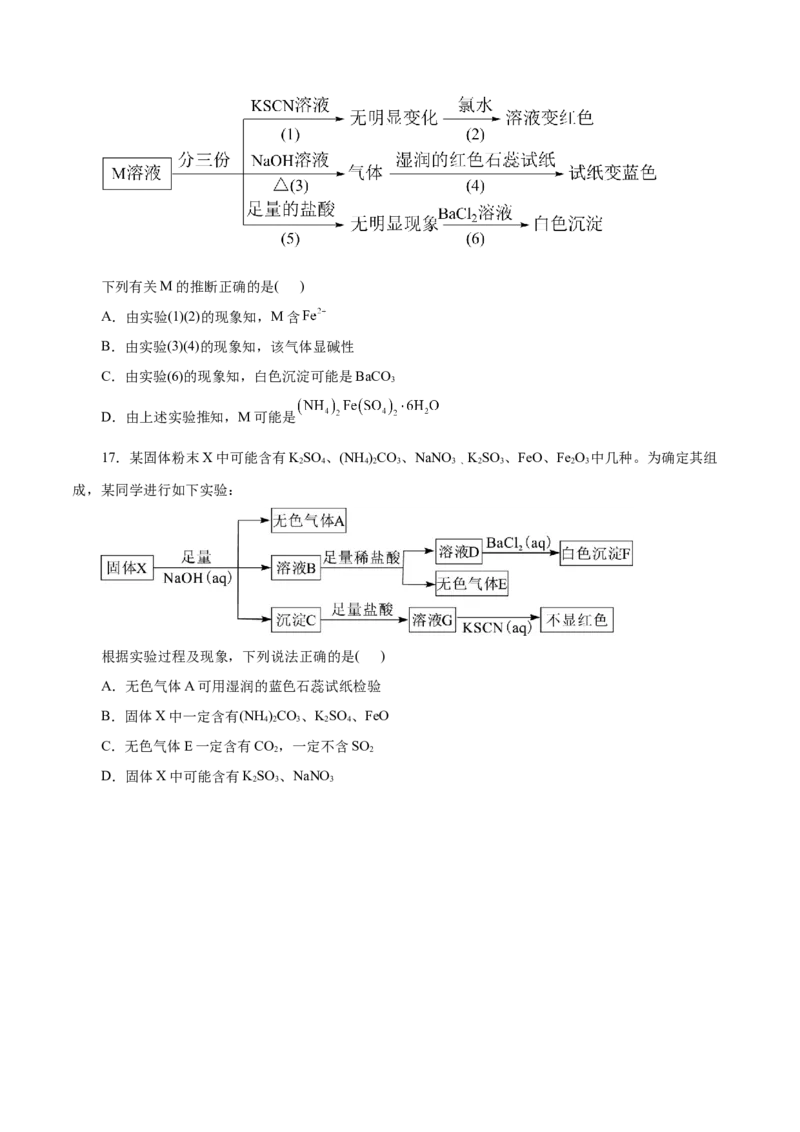
16.M是一种可溶性结晶水合物,为了确定M的组成,取少量M溶于水配成容液进行如下头验:下列有关M的推断正确的是( )
A.由实验(1)(2)的现象知,M含
B.由实验(3)(4)的现象知,该气体显碱性
C.由实验(6)的现象知,白色沉淀可能是BaCO
3
D.由上述实验推知,M可能是
17.某固体粉末X中可能含有KSO 、(NH )CO、NaNO KSO 、FeO、Fe O 中几种。为确定其组
2 4 4 2 3 3 、 2 3 2 3
成,某同学进行如下实验:
根据实验过程及现象,下列说法正确的是( )
A.无色气体A可用湿润的蓝色石蕊试纸检验
B.固体X中一定含有(NH )CO、KSO 、FeO
4 2 3 2 4
C.无色气体E一定含有CO,一定不含SO
2 2
D.固体X中可能含有KSO 、NaNO
2 3 3