文档内容
第 13 讲 原子结构 化学键
【学科核心素养】
1.宏观辨识与微观探析:能从离子或原子结构示意图等不同层次认识原子的结构以及核外电子的排布
规律,能从宏观和微观相结合的视角分析原子结构与元素性质的关系。能从不同层次认识分子的构型,并
对共价键进行分类,能从宏观和微观相结合的视角分析与解决实际问题。
2.证据推理与模型认知:能运用原子结构模型解释化学现象,揭示现象的本质与规律。能运用构造原
理
和能量最低原理揭示元素原子核外电子排布规律。认识共价键的本质及类型,能多角度、动态地分析分子
的空间结构及性质,并运用相关理论解决实际问题。
3.科学态度与社会责任:具有可持续发展意识和绿色化学观念,能对与原子结构有关的社会热点问题
做出正确的价值判断。
【核心素养发展目标】
1.掌握元素、核素、同位素、相对原子质量、相对分子质量、原子构成、原子核外电子排布的含义。
2.掌握原子序数、核电荷数、质子数、中子数、核外电子数以及它们之间的相互关系。
3.掌握1~18号元素的原子结构示意图的表示方法。
4.了解化学键的定义。
5.了解离子键、共价键的形成。
6.掌握电子式的表示方法。
本部分内容是高考的常考点,高考中常以选择题型出题。考查原子(离子)的结构及微粒间的数量关系,
也常考查对元素、核素、同位素概念的理解以及结合元素周期表的推断等。
【知识点解读】
知识点一 原子结构、同位素
1.原子结构
(1)原子的构成粒子
(2)构成原子或离子的微粒间的数量关系
①原子中:质子数(Z)=核电荷数=核外电子数。
②质量数(A)=质子数(Z)+中子数(N)。
③阳离子的核外电子数=质子数-阳离子所带电荷数。如Mg2+的核外电子数是10。
④阴离子的核外电子数=质子数+阴离子所带电荷数。如Cl-的核外电子数是18。
(3)一个信息丰富的符号【特别提醒】
①原子中不一定都含有中子,如H中没有中子。
②电子排布完全相同的原子不一定是同一种原子,如互为同位素的各原子。
③易失去1个电子形成+1价阳离子的不一定是金属原子,如氢原子失去1个电子形成H+。
④形成稳定结构的离子最外层不一定是8个电子,如Li+为2个电子稳定结构。
2.核素、同位素
(1)概念辨析
(2)同位素的特征
①相同存在形态的同位素,化学性质几乎完全相同,物理性质不同。
②天然存在的同一元素各核素所占的原子百分数(丰度)一般不变。
(3)同位素的“六同三不同”
(4)常见的重要核素及其应用
核素 U C H(D) H(T) O
用途 核燃料 用于考古断代 制氢弹 示踪原子
(5)元素、核素、同位素的联系与区别
①现行元素周期表已发现的元素有118种,由于同位素的存在,故核素的种数远大于118种。
②不同核素可能具有相同的质子数,如H、H;也可能具有相同的中子数,如C、O;也可能具有相同
的质量数,如C、N。
③同位素之间的转化,既不是物理变化也不是化学变化,是核反应。
④同位素之间可形成不同的同位素单质。如氢的三种同位素形成的单质有六种:H、D、T、HD、
2 2 2
HT、DT,他们的物理性质(如密度)有所不同,但化学性质几乎完全相同。
⑤同位素之间可形成不同的同位素化合物。如水分子有HO(普通水)、DO(重水)、TO(超重水)等。他
2 2 2们的相对分子质量不同,物理性质(如密度)有所不同,但化学性质几乎完全相同。
知识点二 核外电子排布
1.核外电子排布
(1)核外电子排布规律
核外电子总是先排布在能量最低的电子层里,然后再按照由里向外的顺序依次排布在能量逐渐升高的
电子层里。
①每层最多容纳的电子数为2n2个。
②最外层不超过8个(K层为最外层时不超过2个)。
③次外层不超过18个,倒数第三层不超过32个。
【特别提醒】核外电子排布的几条规律是相互联系的,不能孤立地理解,必须同时满足各项要求,如
M层不是最外层时,最多能容纳18个电子,当M层为最外层时,最多容纳8个电子。
(2)最外层电子数与元素性质的关系
①稀有气体元素原子最外层已排满8个电子(He排满2个),既不易得到电子又不易失去电子,通常表
现为0价。
②金属元素原子最外层电子数一般小于4,常易失去最外层电子,形成8电子或2电子(如Li+)稳定结
构的阳离子,在化合物中显正化合价。
③非金属元素原子最外层电子数一般大于或等于4,易得到电子或形成共用电子对,达到最外层8电
子稳定结构,在化合物中既显正价又显负价(F无正价)。
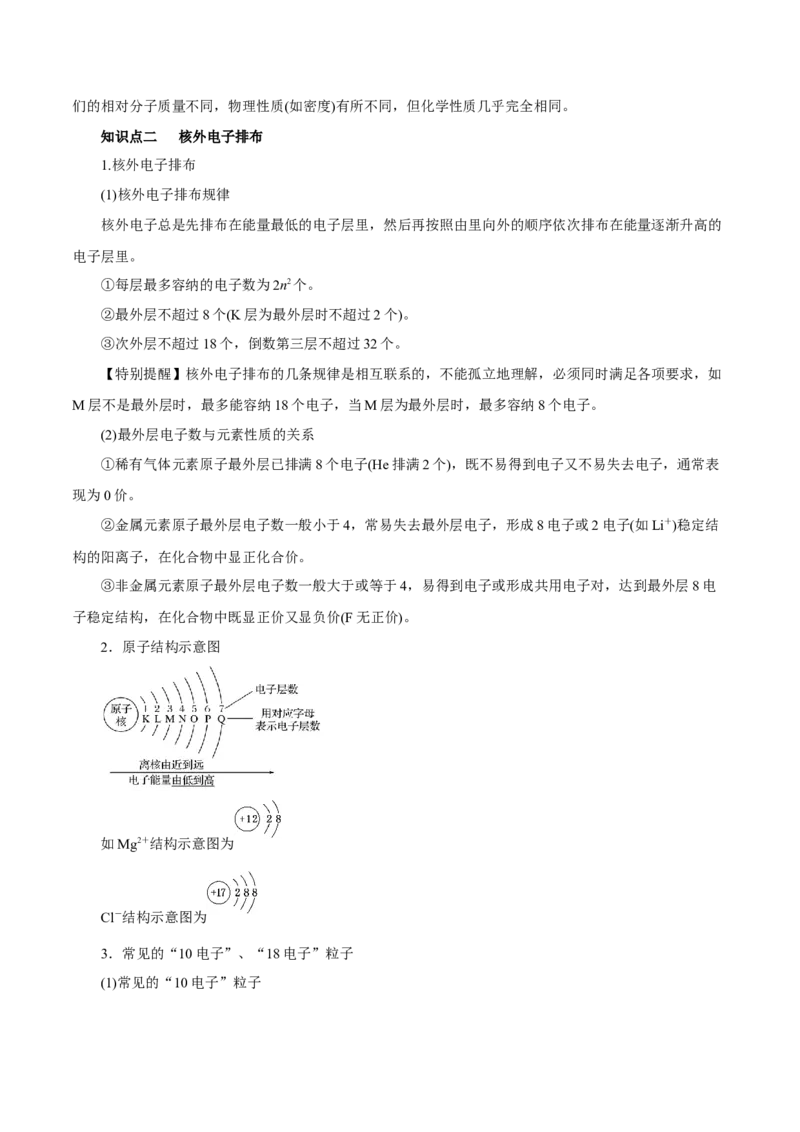
2.原子结构示意图
如Mg2+结构示意图为
Cl-结构示意图为
3.常见的“10电子”、“18电子”粒子
(1)常见的“10电子”粒子(2)常见的“18电子”粒子
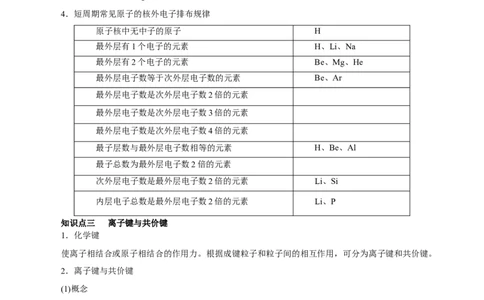
4.短周期常见原子的核外电子排布规律
原子核中无中子的原子 H
最外层有1个电子的元素 H、Li、Na
最外层有2个电子的元素 Be、Mg、He
最外层电子数等于次外层电子数的元素 Be、Ar
最外层电子数是次外层电子数2倍的元素
最外层电子数是次外层电子数3倍的元素
最外层电子数是次外层电子数4倍的元素
最子层数与最外层电子数相等的元素 H、Be、Al
最子总数为最外层电子数2倍的元素
次外层电子数是最外层电子数2倍的元素 Li、Si
内层电子总数是最外层电子数2倍的元素 Li、P
知识点三 离子键与共价键
1.化学键
使离子相结合或原子相结合的作用力。根据成键粒子和粒子间的相互作用,可分为离子键和共价键。
2.离子键与共价键
(1)概念
①离子键:带相反电荷离子之间的相互作用。
②共价键:原子间通过共用电子对所形成的相互作用。
(2)对比
共价键
项目 离子键
非极性键 极性键
带相反电荷离子之间
概念 原子间通过共用电子对所形成的相互作用
的相互作用
成键粒子 阴、阳离子 原子
成键实质 阴、阳离子间的静电 共用电子对不偏 共用电子对偏向作用 向任何一方 一方原子
非金属性强的元素与
同种元素原子之 不同种元素原子
形成条件 金属性强的元素经得失电
间成键 之间成键
子,形成离子键
非金属单质如 共价化合物如
离子化合物如NaCl、
H、Cl、N 等;某些 HCl、CO、CH 或离
形成的物质 KCl、MgCl 、CaCl 、 2 2 2 2 4
2 2 共价化合物如HO 或 子化合物如NaOH、
ZnSO、NaOH等 2 2
4 离子化合物如NaO NH Cl
2 2 4
3.化学键类型的判断
(1)从物质构成角度判断
(2)从物质类别角度判断
物质类别 含化学键情况
非金属单质,如Cl、N、I、P、金刚石等
2 2 2 4
非金属元素构成的化合物,如HSO 、CO、NH 、HCl、 只有共价键
2 4 2 3
CCl 、CS 等
4 2
活泼非金属元素与活泼金属元素形成的化合物,如NaCl、
只有离子键
CaCl 、KO等
2 2
含有原子团的离子化合物,如NaSO 、Ba(OH) 、NH Cl、 既有离子键又有共
2 4 2 4
NaO 等 价键
2 2
稀有气体,如Ne、Ar等 没有化学键
【特别提醒】
①由活泼金属与活泼非金属形成的化学键不一定都是离子键,如AlCl 中Al—Cl键为共价键。
3
②非金属元素的两个原子之间一定形成共价键,但多个原子间也可能形成离子键,如NH Cl等。
4
③影响离子键强弱的因素是离子半径和所带电荷数:离子半径越小,离子所带电荷数越多,离子键越
强,熔、沸点越高。
4.电子式
(1)电子式的书写
概念:在元素符号周围,用“·”或“×”来表示原子的最外层电子(价电子)的式子
粒子的种类 电子式的表示方法 注意事项 举例
价电子少于4时以
原子 元素符号周围标有价电子 单电子分布,多于4时
多出部分以电子对分布
阳 单核 离子符号 右上方标明电荷 Na+离 元素符号紧邻铺开,
多核 用“[ ]”,并标明电荷
子 周围标清电子分布
元素符号周围合理分 用“[ ]”,右上方标明
单核
阴 布价电子及所得电子 电荷
离
相同原子不得加和,用
子 元素符号紧邻铺开,合理
多核 “[ ]”,右上方标明电
分布价电子及所得电子
荷
单 离子化合 用阳离子电子式和阴 同性不相邻,离子
质 物 离子电子式组成 合理分布
及
化 单质及共 各原子紧邻铺开,标 原子不加和,无“[
合 价化合物 明价电子及成键电子情况 ]”,不标明电荷
物
(2)电子式书写的常见错误
内容 实例
错误1 漏写未参与成键的电子
化合物类型不清楚,漏写或多写[ ]
错误2
及错写电荷数
错误3 书写不规范,错写共用电子对
错误4 不考虑原子间的结合顺序
不考虑原子最外层有几个电子,均
错误5
写成8电子结构
不考虑AB 型离子化合物中2个B
错误6 2
是分开写还是一起写
(3)用电子式表示化合物的形成过程
①离子化合物:左边是原子的电子式,右边是离子化合物的电子式,中间用“―→”连接,相同的原子或离子不合并。
如NaCl: 。
②共价化合物:左边是原子的电子式,右边是共价化合物的电子式,中间用“―→”连接。
如HCl: 。
知识点四 化学键与物质类别的关系、分子间作用力
1.离子化合物与共价化合物
(1)离子化合物与共价化合物的比较
项目 离子化合物 共价化合物
定义 含有离子键的化合物 只含有共价键的化合物
构成微粒 阴、阳离子 分子或原子
一定含有离子键,
化学键类型 只含有共价键
可能含有共价键
与物质类 ①强碱、②绝大多数盐、③ ①酸、②弱碱、③气态氢化物、
别的关系 活泼金属氧化物 ④非金属氧化物、⑤极少数盐
(2)离子化合物和共价化合物的判断方法
【特别提醒】
熔融状态下能导电的化合物一定是离子化合物,水溶液中能导电的化合物不一定是离子化合物,如
HCl。
2.化学键与物质类别的关系
(1)只含有极性共价键的物质一般是不同种非金属元素形成的共价化合物,如SiO、HCl、CH 等。
2 4(2)只含有非极性共价键的物质是同种非金属元素形成的单质,如Cl、P、金刚石等。
2 4
(3)既有极性键又有非极性键的共价化合物一般由多个原子组成,如HO、C H 等。
2 2 2 4
(4)只含离子键的物质主要是由活泼非金属元素与活泼金属元素形成的化合物,如NaS、CaCl 、NaCl
2 2
等。
(5)既有离子键又有极性共价键的物质,如NaOH、KSO 等;既有离子键又有非极性共价键的物质,
2 4
如NaO 等。
2 2
(6)仅由非金属元素形成的离子化合物,如NH Cl、NH NO 等。
4 4 3
(7)金属元素和非金属元素间可能存在共价键,如AlCl 等。
3
3.化学键对物质性质的影响
(1)对物理性质的影响
金刚石、晶体硅、石英、金刚砂等物质硬度大、熔点高,就是因为其中的共价键很强,破坏时需消耗
很多的能量。NaCl等部分离子化合物中也有很强的离子键,故其熔点也较高。
(2)对化学性质的影响
N 分子中有很强的共价键,故在通常状况下,N 的性质很稳定,HS、HI等分子中的共价键较弱,故
2 2 2
它们受热时易分解。
4.分子间作用力和氢键
(1)分子间作用力
定义 把分子聚集在一起的作用力,又称范德华力
①分子间作用力比化学键得多,它主要影响物质的熔点、沸点等物理性
质,而化学键主要影响物质的化学性质;
特点 ②分子间作用力存在于由共价键形成的多数共价化合物和绝大多数气态、
液态、固态非金属单质分子之间。但像二氧化硅、金刚石等由共价键形成的物
质,微粒之间不存在分子间作用力
一般来说,对于组成和结构相似的物质,相对分子质量越大,分子间作用
变化规律
力越大,物质的熔、沸点也越高。例如,熔、沸点:IBr ClF
2 2 2 2
(2)氢键
定义 分子间存在的一种比分子间作用力稍强的相互作用
形成条件 除H外,形成氢键的原子通常是O、F、N
氢键存在广泛,如蛋白质分子、醇、羧酸分子、HO、NH 、HF等分子之
存在 2 3
间。分子间氢键会使物质的熔点和沸点升高
①存在氢键的物质,其熔、沸点明显高于同族同类物质。如HO的熔、沸
2
点高于HS
2
性质
②氨极易液化,是因为NH 分子间存在氢键;NH 极易溶于水,也是因为
3 3
影响
NH 分子与HO分子间易形成氢键
3 2
③水结冰时体积膨胀、密度减小,是因为结冰时形成了氢键
【典例剖析】高频考点一 同位素与同素异形体
例1.(2021·广东卷)“天问一号”着陆火星,“嫦娥五号”采回月壤。腾飞中国离不开化学,长征系
列运载火箭使用的燃料有液氢和煤油等化学品。下列有关说法正确的是
A.煤油是可再生能源
B.H 燃烧过程中热能转化为化学能
2
C.火星陨石中的 质量数为20
D.月壤中的 与地球上的 互为同位素
【举一反三】(2020·浙江卷)下列说法正确的是( )
A. 和 是两种不同的元素 B. 单晶硅和石英互为同素异形体
C. 和 互为同系物 D. H与Na在元素周期表中处于同一主族
【易错警示】
①元素的种类由原子核内的质子数决定,因此划分元素种类的唯一标准是质子数(即核电荷数)。
②元素概念中的原子是泛指,即各种状况下的原子或离子(包括游离态和化合态),所以H、D、T、H
+、H-都属于氢元素。
③元素是个宏观概念,元素只讲种类,不讲个数,元素组成物质。
【变式探究】我国稀土资源丰富。下列有关稀土元素Sm与
Sm的说法正确的是( )
A.Sm与Sm互为同位素
B.Sm与Sm的质量数相同
C.Sm与Sm是同一种核素
D.Sm与Sm的核外电子数和中子数均为62
高频考点二 “10电子”“18电子”微粒的应用
例2.(2021·湖南卷)W、X、Y、Z为原子序数依次增大的短周期主族元素,Y的原子序数等于W与
X的原子序数之和,Z的最外层电子数为K层的一半,W与X可形成原子个数比为2:1的 分子。下
列说法正确的是
A.简单离子半径:
B.W与Y能形成含有非极性键的化合物
C.X和Y的最简单氢化物的沸点:D.由W、X、Y三种元素所组成化合物的水溶液均显酸性
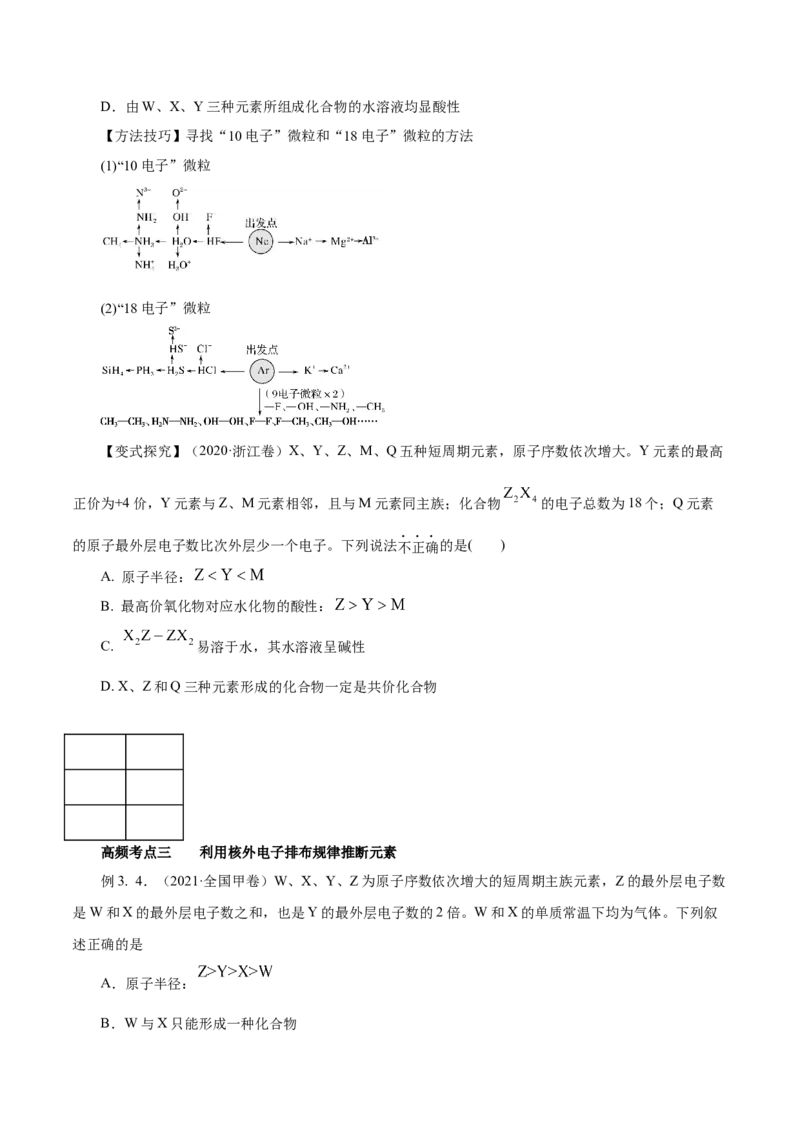
【方法技巧】寻找“10电子”微粒和“18电子”微粒的方法
(1)“10电子”微粒
(2)“18电子”微粒
【变式探究】(2020·浙江卷)X、Y、Z、M、Q五种短周期元素,原子序数依次增大。Y元素的最高
正价为+4价,Y元素与Z、M元素相邻,且与M元素同主族;化合物 的电子总数为18个;Q元素
的原子最外层电子数比次外层少一个电子。下列说法不正确的是( )
A. 原子半径:
B. 最高价氧化物对应水化物的酸性:
C. 易溶于水,其水溶液呈碱性
D. X、Z和Q三种元素形成的化合物一定是共价化合物
高频考点三 利用核外电子排布规律推断元素
例3. 4.(2021·全国甲卷)W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子数
是W和X的最外层电子数之和,也是Y的最外层电子数的2倍。W和X的单质常温下均为气体。下列叙
述正确的是
A.原子半径:
B.W与X只能形成一种化合物C.Y的氧化物为碱性氧化物,不与强碱反应
D.W、X和Z可形成既含有离子键又含有共价键的化合物
【举一反三】(2020·新课标Ⅲ)W、X、Y、Z为原子序数依次增大的短周期元素,四种元素的核外
电子总数满足X+Y=W+Z;化合物XW 与WZ相遇会产生白烟。下列叙述正确的是( )
3
A. 非金属性:W> X>Y> Z B. 原子半径:Z>Y>X>W
C. 元素X的含氧酸均为强酸 D. Y的氧化物水化物为强碱
【变式探究】(2020·浙江7月选考,16)X、Y、Z、M、Q五种短周期元素,原子序数依次增大。Y元
素的最高正价为+4价,Y元素与Z、M元素相邻,且与M元素同主族;化合物ZX 的电子总数为18个;
2 4
Q元素的原子最外层电子数比次外层少一个电子。下列说法不正确的是( )
A.原子半径:Z<Y<M
B.最高价氧化物对应水化物的酸性:Z>Y>M
C.XZ—ZX 易溶于水,其水溶液呈碱性
2 2
D.X、Z和Q三种元素形成的化合物一定是共价化合物
高频考点四 8电子结构与电子式的判断及其应用
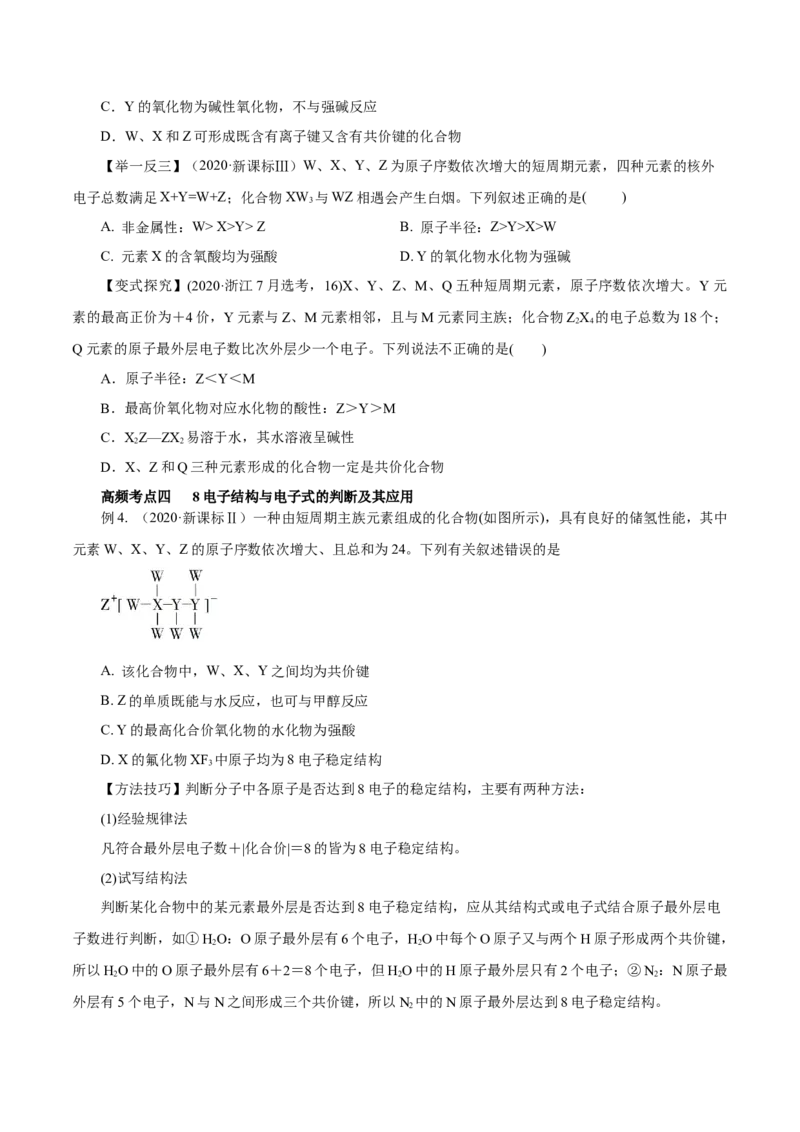
例4. (2020·新课标Ⅱ)一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中
元素W、X、Y、Z的原子序数依次增大、且总和为24。下列有关叙述错误的是
A. 该化合物中,W、X、Y之间均为共价键
B. Z的单质既能与水反应,也可与甲醇反应
C. Y的最高化合价氧化物的水化物为强酸
D. X的氟化物XF 中原子均为8电子稳定结构
3
【方法技巧】判断分子中各原子是否达到8电子的稳定结构,主要有两种方法:
(1)经验规律法
凡符合最外层电子数+|化合价|=8的皆为8电子稳定结构。
(2)试写结构法
判断某化合物中的某元素最外层是否达到8电子稳定结构,应从其结构式或电子式结合原子最外层电
子数进行判断,如①HO:O原子最外层有6个电子,HO中每个O原子又与两个H原子形成两个共价键,
2 2
所以HO中的O原子最外层有6+2=8个电子,但HO中的H原子最外层只有2个电子;②N:N原子最
2 2 2
外层有5个电子,N与N之间形成三个共价键,所以N 中的N原子最外层达到8电子稳定结构。
2【变式探究】(2019·海南,13)自门捷列夫发现元素周期律以来,人类对自然的认识程度逐步加深,元
素周期表中的成员数目不断增加。回答下列问题:
(1)2016年IUPAC确认了四种新元素,其中一种为 Mc,中文名为“镆”。元素Mc可由反应:Am+
Ca===Mc+3n得到。该元素的质子数为________,287Mc与288Mc互为__________________。
(2)Mc位于元素周期表中第ⅤA族,同族元素N的一种氢化物为HN—NH ,写出该化合物分子的电
2 2
子式:______________________,该分子内存在的共价键类型有________________。
(3)该族中的另一元素P能呈现多种化合价,其中+3价氧化物的分子式为_______________,+5价简
单含氧酸的分子式为__________________________。
高频考点五 化学键类型的判断
例5.1.(2021·浙江卷)下列含有共价键的盐是
A.CaCl B.HSO C.Ba(OH) D.NaCO
2 2 4 2 2 3
【举一反三】 (2018·全国卷II)W、X、Y和Z为原子序数依次增大的四种短周期元素。W与X可生成
一种红棕色有刺激性气味的气体;Y的周期数是族序数的3倍;Z原子最外层的电子数与W的电子总数相
同。下列叙述正确的是( )
A.X与其他三种元素均可形成两种或两种以上的二元化合物
B.Y与其他三种元素分别形成的化合物中只含有离子键
C.四种元素的简单离子具有相同的电子层结构
D.W的氧化物对应的水化物均为强酸
【变式探究】下列说法中正确的是( )
A.离子键就是使阴、阳离子结合成化合物的静电引力
B.NH NO 晶体中含共价键,是共价化合物
4 3
C.HO、NH 分子中只含有极性共价键
2 2 2 4
D.某化合物熔融状态能导电,可以证明该化合物内一定存在离子键
高频考点六 化学键与化合物类别的关系
例6.(2021·河北卷)用中子轰击 X原子产生α粒子(即氮核 He)的核反应为: X+ n→ Y+ He。
已知元素Y在化合物中呈+1价。下列说法正确的是
A.HXO 可用于中和溅在皮肤上的NaOH溶液
3 3
B.Y单质在空气中燃烧的产物是YO
2 2
C.X和氢元素形成离子化合物
D.6Y和7Y互为同素异形体
HBOHBO
3 3 3 3
【举一反三】(2018·全国卷Ⅰ)主族元素W、X、Y、Z的原子序数依次增加,且均不大于20。W、X、Z最外层电子数之和为10;W与Y同族;W与Z形成的化合物可与浓硫酸反应,其生成物可腐蚀玻璃。下
列说法正确的是( )
A.常温常压下X的单质为气态
B.Z的氢化物为离子化合物
C.Y和Z形成的化合物的水溶液呈碱性
D.W与Y具有相同的最高化合价
【变式探究】下列说法错误的是( )
A.含有共价键的化合物一定是共价化合物
B.在共价化合物中一定含有共价键
C.含有离子键的化合物一定是离子化合物
D.双原子单质分子中含有的共价键一定是非极性共价键