文档内容
考点 06 原子结构
(核心考点精讲)
一、3年真题考点分布
考点内容 考题统计
2022重庆卷5题,3分;2021河北卷5题,3分;
原子结构
2021辽宁卷2题,3分;2021天津卷5题,4分
2023天津卷7题,4分;2022山东卷3,2分;2022
浙江1月7题,2分;2022浙江6月7题,2分;2021
核素、同位素
河北卷5题,3分;2021北京卷2题,4分;2021天
津卷3题,4分
2022浙江1月5题,2分;2022浙江6月5题,2
分;2022重庆卷2题,3分;2022江苏卷2题,3
电子式
分;2022辽宁卷2题,3分;2021浙江1月5题,2
分
二、命题规律及备考策略
【命题规律】
从近三年高考试题来看,本考点考查在各微粒数量间的关系,微粒的结构示意图,电子式的表示方法,
认识化学键的本质是原子间的静电作用,能多角度、动态的分析化学键。试题的难度不大,一般属于了解
层次。
【备考策略】
高考中该类型题主要是通过重大科技成果(化学科学的新发展、新发明等)尤其是放射性元素、放射性
同位素、农业、医疗、考古等方面的应用为题材,来考查粒子的个微粒的相互关系,备考过程中多关注重
大科技成果。
【命题预测】
预测2024年原子结构高考考查力度不是很大,注意有关概念辨析,复习备考时注重原子结构示意图、
电子式的书写及粒子“量”的关系,注意加强核素、同位素的概念辨析和化学键类型与存在的判断。
考法 1 原子结构
1.原子构成
(1)构成原子的微粒及作用
原子(X)
资料收集整理【淘宝店铺:向阳百分百】(2)微粒之间的关系
①原子中:质子数(Z)=核电荷数=核外电子数;
②质量数(A)=质子数(Z)+中子数(N);
③阳离子的核外电子数=质子数-阳离子所带的电荷数;
④阴离子的核外电子数=质子数+阴离子所带的电荷数。
(3)微粒符号周围数字的含义
(4)两种相对原子质量
①原子(即核素)的相对原子质量:一个原子(即核素)的质量与12C质量的的比值。一种元素有几种同位
素,就有几种不同核素的相对原子质量。
②元素的相对原子质量:是按该元素各种天然同位素原子所占的原子百分比算出的平均值。如:
A(Cl)=A(35Cl)×a%+A(37Cl)×b%。
r r r
2.元素、核素、同位素
(1)元素、核素、同位素的概念及相互关系
(2)同位素的特征
①同一元素的各种核素的中子数不同,质子数相同,化学性质几乎完全相同,物理性质差异较大;
②同一元素的各种稳定核素在自然界中所占的原子百分数(丰度)不变。
(3)氢元素的三种核素
H:名称为氕,不含中子;
H:用字母D表示,名称为氘或重氢;
H:用字母T表示,名称为氚或超重氢。
(4)几种重要核素的用途
核素 U C H H O
用途 核燃料 用于考古断代 制氢弹 示踪原子
3.核外电子排布
(1)核外电子排布规律
资料收集整理【淘宝店铺:向阳百分百】(2)原子结构示意图
(3)核外电子排布与元素性质的关系
①金属元素原子的最外层电子数一般小于4,较易失去电子,形成阳离子,表现出还原性,在化合物
中显正化合价。
②非金属元素原子的最外层电子数一般大于或等于4,较易得到电子,活泼非金属原子易形成阴离子,
在化合物中主要显负化合价。
③稀有气体元素的原子最外层为8电子(氦为2电子)稳定结构,不易失去或得到电子,通常表现为0价。
(1)原子不一定都有中子,如H。
(2)质子数相同的微粒不一定属于同一种元素,如F与OH-。
(3)核外电子数相同的微粒,其质子数不一定相同,如Al3+与Na+、F-等,NH与OH-等。
(4)不同的核素可能具有相同的质子数,如H与H;也可能具有相同的中子数,如C与O;也可能具有
相同的质量数,如C与N;也可能质子数、中子数、质量数均不相同,如H与C。
(5)同位素的物理性质不同,但化学性质几乎相同。
(6)不同核素之间的转化属于核反应,不属于化学反应。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)任何原子或离子的组成中都含有质子( )
(2)元素原子的多样性是由构成原子的质子和中子数目引起的( )
(3)元素的化学性质主要取决于元素原子的最外层电子数( )
(4)U和U是同位素,核反应属于化学变化( )
(5)2H+核外电子数为2( )
(6)两种粒子,若核外电子排布完全相同,则其化学性质一定相同( )
(7)一种元素可以有多种核素,也可能只有一种核素,有多少种核素就有多少种原子( )
(8)核聚变如 H+H―→He+n,因为有新微粒生成,所以该变化是化学变化(×)
资料收集整理【淘宝店铺:向阳百分百】(9)Cl与Cl得电子能力几乎相同( )
(10)一种核素只有一种质量数( )
(11)最外层电子数为8的粒子一定是稀有气体元素原子( )
(12)核外电子排布相同的微粒化学性质也相同( )
(13)40K和40Ca原子中的质子数和中子数都相等( )
(14)某元素的原子最外层只有一个电子,则它一定是金属元素( )
(15)同位素的不同核素的物理、化学性质完全相同( )
(16)当原子形成简单离子后,其最外层上的电子数可超过8个( )
(17)原子最外层上的电子数少于4个时,电子数越多,还原性越强( )
(18)原子核外电子中,最外层上的电子能量最高( )
(19)当最外层上的电子数变为4个时即达稳定结构( )
(20)若两种不同的核素具有相同的中子数,则二者一定不属于同种元素( )
答案:(1)√ (2)√ (3)√ (4)× (5)× (6)× (7)√ (8)× (9)√ (10)√ (11)× (12)× (13)× (14)×
(15)× (16)× (17)× (18)√ (19)× (20)√
例1 天然铊有两种稳定同位素 Tl和 Tl。下列有关铊的同位素说法中,不正确的是( )
A. Tl和 Tl质子数相同 B. Tl和 Tl互为同素异形体
C. Tl和 Tl中子数之差为2 D. Tl原子核内中子数与核外电子数之差为43
【答案】B
【解析】A项,同位素是质子数相同,中子数不同的同种元素的不同原子,两种核素均为铊元素的核
素,质子数相同,均为81,故A正确;B项,同种元素构成的不同种单质互称为同素异形体,此为两种原
子,不是单质,故B错误;C项,中子数=质量数-质子数, Tl的中子数为203-81=122, Tl的中子数
为205-81=124,两者之差为2,故C正确;D项,原子的核外电子数=质子数, Tl的电子数为81,中子
数为205-81=124,两者之差为124-81=43,故D正确。故选B。
例2 (2023·天津市和平区高三联考) 是目前发现的最后一种元素,也是最重的一种元素,元素符
号为Og,是人工合成的放射性稀有气体元素,它的发现标志着元素周期表第七周期被全部填满。用钙离子
撞击锎(Cf)靶,可以产生Og,其反应可表示为: ,下列说法错误的是( ) ( )
资料收集整理【淘宝店铺:向阳百分百】A. 原子核内有176个中子,质子数为118
B. 与 的化学性质几乎相同
C.Og是一种性质稳定的非金属元素
D.锎为过渡元素
【答案】C
【解析】 ,即 。A项, 为 ,则其原子核内有
294-118=176个中子,质子数为118,A正确;B项, 与 互为同位素,电子数相同,基态原子电子
排布方式相同,化学性质几乎相同,B正确;C项,Og具有放射性,不稳定,C不正确;D项, 锎核电荷
数为98,位于第七周期ⅢB,是一种锕系元素,属于过渡元素,D正确;故选C。
对点1 钋-210属于极毒性放射性元素,以相同重量来比较,钋-210的毒性是氰化物的2.5亿倍,
只需一颗尘埃大小就足以取人性命,而且没有解毒剂。下列有关210 P 说法正确的是( )
84 O
218 218
A. 84 与 互为同素异形体 B. 84 与 互为同位素
218
C. 84 的质子数为84,中子数为126 D.Po元素的相对原子质量为210
【答案】C
218 218
【解析】A项, 84 与 是同种元素的不同核素,应互为同位素,故A错误;B项, 84 与
218
为两种不同元素的核素,不能称为同位素,故B错误;C项, 84 的质子数为84,中子数为210-
84=126,故C正确;D项,钋-210的近似相对原子质量为210,钋元素的相对原子质量不是210,故D错
误;故选C。
对点2 地表水和地下水都来源于大气降水,但重水和轻水中同位素含量是不同的,有时差别还相当
大,氢包括两种稳定核素:H和D,氧常见的核素16O、17O和18O,下列有关说法正确的是( )
A.H 和D 互为同分异构体,其化学性质完全相同
2 2
B.HO、HO、HO互为同位素,都能与金属钠发生反应
C.18O 和18O 互为同素异形体,其密度之比为2∶3
2 3
D.电解一定量的DO时,阴、阳两极所得气体的质量之比约为2∶9
【答案】D
【解析】同分异构体一般指分子式相同,结构不同的有机物,H 和D 为组成和结构都相同的无机物,
2 2
资料收集整理【淘宝店铺:向阳百分百】A错误;16O、17O、18O互为同位素,HO、HO、HO既不互为同位素,也不是同素异形体,B错误;18O 和
2
18O 互为同素异形体,但只有在同温同压下,它们的密度之比才为2∶3,C错误;电解一定量的DO时,阴
3
阳两极会收集到物质的量之比为2∶1的D 和18O,其质量之比约为2∶9,D正确。
2 2
考法 2 电子式
1.概念
在元素符号周围用“·”或“×”来表示原子的最外层电子的式子。
2.书写方法
(1)原子的电子式:将原子的所有最外层电子数在元素符号的周围标出.例如:
氢原子( )、钠原子( )、镁原子( )、铝原子( )、碳原子( )、氮原子( )、硫原
子( )、氩原子( )。
(2)离子的电子式:
①阴离子:在书写阴离子的电子式时,须在阴离子符号的周围标出其最外层的 8个电子(H-为2个电
子),外加方括号,再在括号外的右上角注明阴离子所带的电荷数.例如S2-的电子式为[ ]2- ,OH-
的电子式为 。
②阳离子;对于简单阳离子,其电子式即为阳离子符号,如钠离子Na+、镁离子Mg2+等.对于带正电
荷的原子团,书写方法与阴离子类似,区别在于在方括号右上角标上阳离子所带的正电荷数.如 NH +电
4
子式为 。
(3)离子化合物的电子式:在书写离子化合物的电子式时,每个离子都要分开写.如CaCl 的电子式应
2
为 。
(4)用电子式表示化合物的形成过程:先在左边写出构成该化合物的元素原子的电子式,标上“→”,
再在右边写出化合物的电子式.例如:
.. + .. -
离子化合物NaCl的形成过程: Na×+ . . C . l: Na[×.C . l . :]
.. ..
H× +.C
.
l
.
: H ×.C.l. :
共价化合物HCl的形成过程:
资料收集整理【淘宝店铺:向阳百分百】1.8电子结构的判断方法
(1)经验规律法
①凡符合最外层电子数+|化合价|=8的皆为8电子结构。
②原子序数≤5的原子不能形成8电子稳定结构。
(2)试写结构法
判断某化合物中的某原子最外层是否达到8电子稳定结构,应从其结构式或电子式结合原子最外层电
子数进行判断,如①COCl 可根据结构式 判断各原子均为8电子稳定结构。②N ,写出其电子式
2 2
,判断两氮原子均满足8电子稳定结构。
2.电子式书写常见的四大误区
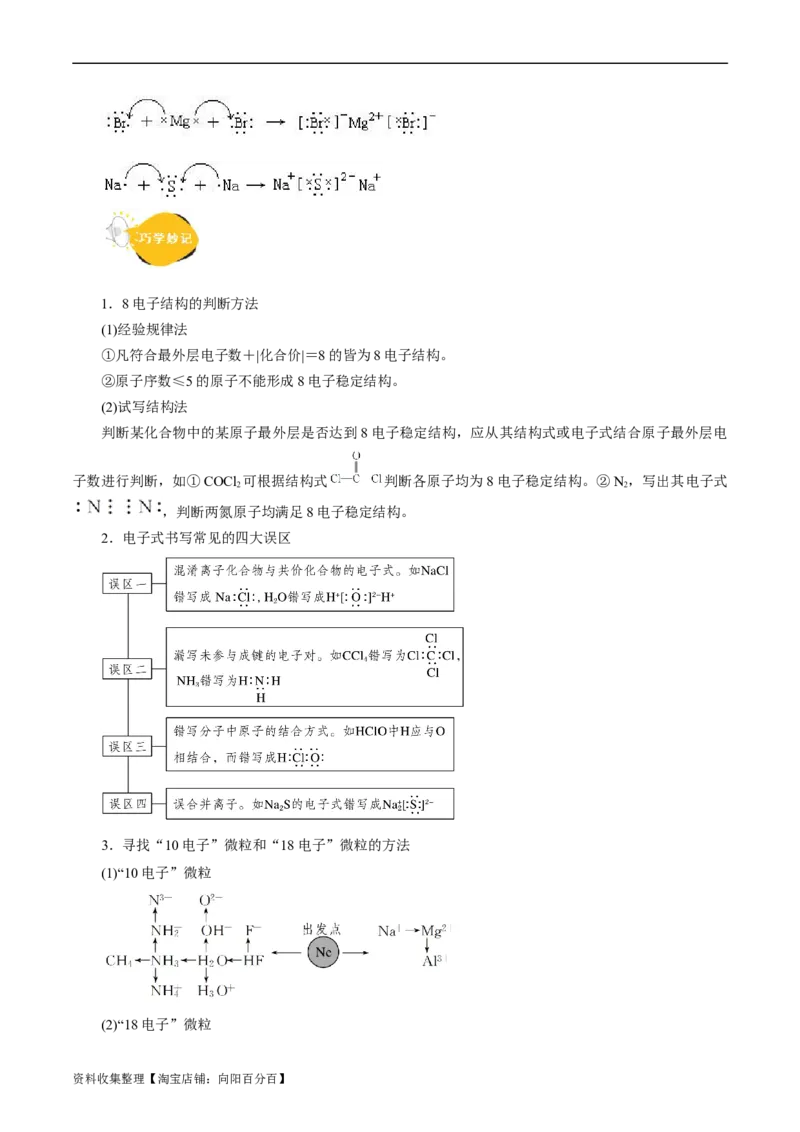
3.寻找“10电子”微粒和“18电子”微粒的方法
(1)“10电子”微粒
(2)“18电子”微粒
资料收集整理【淘宝店铺:向阳百分百】