文档内容
[复习目标] 1.掌握常见无机物性质的转化关系。2.掌握无机物性质的转化在环境保护、化
工流程、微型实验中的应用。
(一)钠及其化合物
钠是“极其活泼”金属的代表,学习钠的性质可类比知道第ⅠA族、第ⅡA族活泼金属的
一般性质,复习时应从以下几个方面掌握:
1.树立物质转化思想
(1)理清知识主线
Na→NaO→NaO→NaOH→NaCO→NaHCO
2 2 2 2 3 3
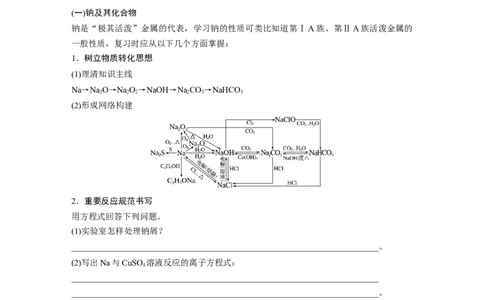
(2)形成网络构建
2.重要反应规范书写
用方程式回答下列问题。
(1)实验室怎样处理钠屑?
________________________________________________________________________。
(2)写出Na与CuSO 溶液反应的离子方程式:
4
________________________________________________________________________
________________________________________________________________________。
(3)怎样将NaCO 溶液转化为NaOH溶液(用化学方程式表示)?
2 3
________________________________________________________________________。
(4)向NaOH、NaCO、NaHCO 溶液中逐滴滴入少量盐酸,写出发生反应的离子方程式:
2 3 3
________________________________________________________________________;
________________________________________________________________________;
________________________________________________________________________。
(5)怎样除去CO 中的SO 气体(用离子方程式表示)?
2 2________________________________________________________________________。
(6)怎样除去NaCO 溶液中的NaHCO (用离子方程式表示)?
2 3 3
________________________________________________________________________。
(7)怎样除去NaHCO 溶液中的NaCO(用离子方程式表示)?
3 2 3
________________________________________________________________________。
(8)用化学方程式表示呼吸面具中产生O 的原理:_____________________________;
2
________________________________________________________________________。
(二)铝及其化合物
铝是“氢前”且其氧化物、氢氧化物均具有两性的金属代表,它是典型的轻金属。学习铝的
性质可类比知道铍、锌等元素的一般性质,复习时应从以下几个方面掌握:
1.树立物质转化思想
(1)理清知识主线
Al→Al O←Al(OH) →
2 3 3
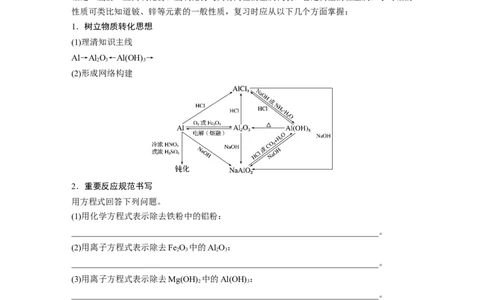
(2)形成网络构建
2.重要反应规范书写
用方程式回答下列问题。
(1)用化学方程式表示除去铁粉中的铝粉:
________________________________________________________________________。
(2)用离子方程式表示除去Fe O 中的Al O:
2 3 2 3
________________________________________________________________________。
(3)用离子方程式表示除去Mg(OH) 中的Al(OH) :
2 3
________________________________________________________________________。
(4)现有AlCl 溶液、氨水、NaOH溶液,制备Al(OH) 的最佳方案是(用化学方程式表示):
3 3
________________________________________________________________________。
(5)现有NaAlO 溶液、CO、盐酸,制备Al(OH) 的最佳方案是(用离子方程式表示):
2 2 3
________________________________________________________________________
________________________________________________________________________。
(6)用离子方程式表示泡沫灭火器的灭火原理:________________________________。
(7)用离子方程式分别表示:
①Al3+、AlO;②AlO、HCO不能大量共存的原理:①______________________________________________________________________;
②______________________________________________________________________。
(8)铵明矾[NH Al(SO )·12H O]是常见的食品添加剂,用于焙烤食品,向铵明矾溶液中逐滴
4 4 2 2
滴入NaOH溶液,试写出反应的离子方程式:
________________________________________________________________________;
________________________________________________________________________;
________________________________________________________________________。
(三)铁及其重要化合物
铁是“氢前”且是“变价”金属的代表,它是典型的黑色金属,也是工农业生产中用途最广
的金属。复习时应从以下几个方面掌握:
1.树立物质转化思想
(1)理清知识主线
Fe→→→
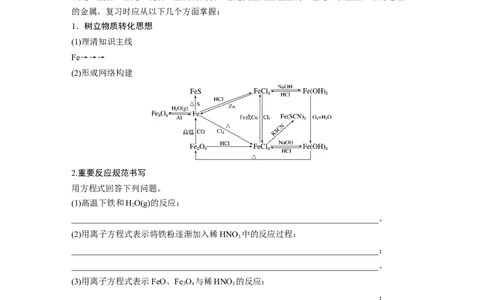
(2)形成网络构建
2.重要反应规范书写
用方程式回答下列问题。
(1)高温下铁和HO(g)的反应:
2
________________________________________________________________________。
(2)用离子方程式表示将铁粉逐渐加入稀HNO 中的反应过程:
3
________________________________________________________________________;
________________________________________________________________________。
(3)用离子方程式表示FeO、Fe O 与稀HNO 的反应:
3 4 3
________________________________________________________________________;
________________________________________________________________________。
(4)用离子方程式表示下列反应。
①Fe(OH) 与稀HNO 反应:
2 3
________________________________________________________________________;
②Fe(OH) 与氢碘酸反应:
3
________________________________________________________________________。
(5)用方程式表示铁发生吸氧腐蚀生成铁锈的过程:
负极:________________________________________________________________________,正极:________________________________________________________________________,
______________________________________________________________________________,
______________________________________________________________________________,
Fe(OH) 脱去一部分水生成Fe O·xHO。
3 2 3 2
(6)怎样除去Fe (SO ) 中的FeSO (用适当的文字和离子方程式说明)?
2 4 3 4
________________________________________________________________________
________________________________________________________________________
(7)怎样检验Fe O 中的FeO(用适当的文字和离子方程式说明)?
2 3
________________________________________________________________________
________________________________________________________________________
(四)铜及其重要化合物
铜是“氢后”且是“变价”金属的代表,它是典型的有色金属,也是典型的重金属。复习时
应从以下几个方面掌握:
1.树立物质转化思想
(1)理清知识主线
Cu→←Cu(OH) →
2
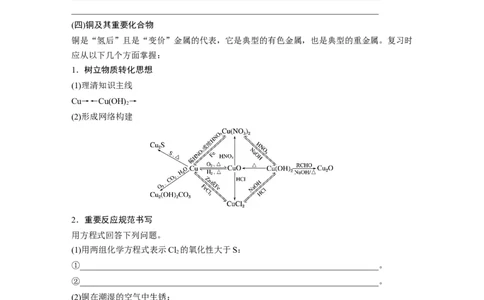
(2)形成网络构建
2.重要反应规范书写
用方程式回答下列问题。
(1)用两组化学方程式表示Cl 的氧化性大于S:
2
①______________________________________________________________________。
②______________________________________________________________________。
(2)铜在潮湿的空气中生锈:
________________________________________________________________________。
(3)将Cu和浓HSO 混合加热:
2 4
________________________________________________________________________。
(4)Cu和稀HNO 反应的离子方程式:
3
________________________________________________________________________。
(5)常用FeCl 溶液腐蚀铜板(用离子方程式表示):
3
________________________________________________________________________。
(6)用惰性电极电解CuSO 溶液(用化学方程式表示):
4________________________________________________________________________。
(五)碳、硅及其重要化合物
硅元素的非金属性不强,但其具有“亲氧”特性,使硅元素在自然界中没有游离态,只有化
合态,其主要以二氧化硅和硅酸盐的形式存在。对于碳、硅两元素,复习时应从以下几个方
面掌握:
1.树立物质转化思想
(1)理清知识主线
CH←――C―→CO―→CO
4 2
SiH←――Si―→SiO(H SiO)
4 2 2 3
(2)形成网络构建
2.重要反应规范书写
用方程式回答下列问题。
(1)Mg在CO 中燃烧:______________________________________________________。
2
(2)“水滴石穿”的反应原理(用离子方程式表示):_______________________________。
(3)“钟乳石”的形成过程(用化学方程式表示):_________________________________,
___________________________________________________________________________。
(4)向饱和NaCO 溶液中通入过量CO 的离子方程式:______________________________。
2 3 2
(5) 氢 氟 酸 不 能 用 玻 璃 瓶 盛 放 , 其 原 因 是 ( 用 化 学 方 程 式 表 示 ) :
___________________________。
(6)盛放 NaOH 溶液的试剂瓶不能用玻璃塞,其原因是(用离子方程式表示):
___________________________________________________________________________。
(7)侯氏制碱法的原理(用化学方程式表示):______________________________________。
(六)卤素及其重要化合物(以氯为例)
氯是典型的活泼非金属元素,在自然界中以化合态存在,复习时应从以下几个方面掌握:
1.树立物质转化思想
(1)理清知识主线
HCl―→Cl―→HClO―→HClO―→HClO―→HClO
2 2 3 4
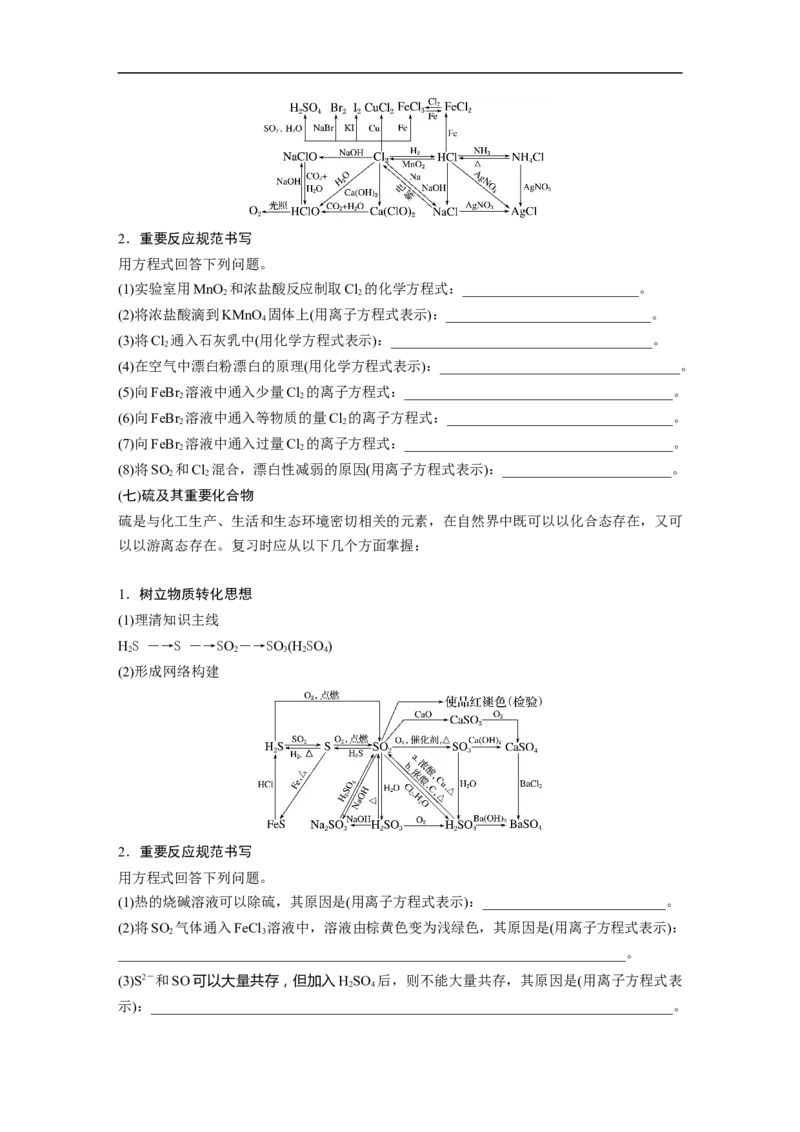
(2)形成网络构建2.重要反应规范书写
用方程式回答下列问题。
(1)实验室用MnO 和浓盐酸反应制取Cl 的化学方程式:_________________________。
2 2
(2)将浓盐酸滴到KMnO 固体上(用离子方程式表示):_____________________________。
4
(3)将Cl 通入石灰乳中(用化学方程式表示):_____________________________________。
2
(4)在空气中漂白粉漂白的原理(用化学方程式表示):__________________________________。
(5)向FeBr 溶液中通入少量Cl 的离子方程式:______________________________________。
2 2
(6)向FeBr 溶液中通入等物质的量Cl 的离子方程式:________________________________。
2 2
(7)向FeBr 溶液中通入过量Cl 的离子方程式:______________________________________。
2 2
(8)将SO 和Cl 混合,漂白性减弱的原因(用离子方程式表示):________________________。
2 2
(七)硫及其重要化合物
硫是与化工生产、生活和生态环境密切相关的元素,在自然界中既可以以化合态存在,又可
以以游离态存在。复习时应从以下几个方面掌握:
1.树立物质转化思想
(1)理清知识主线
HS ―→S ―→SO―→SO(H SO)
2 2 3 2 4
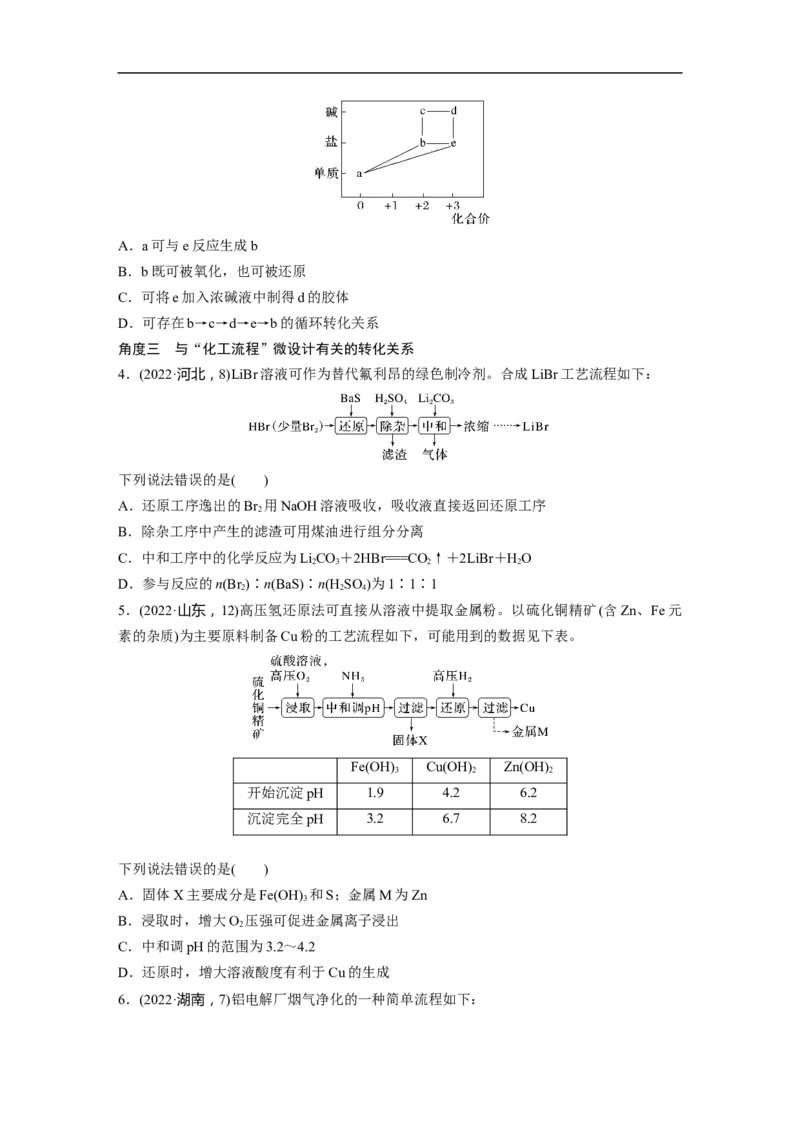
(2)形成网络构建
2.重要反应规范书写
用方程式回答下列问题。
(1)热的烧碱溶液可以除硫,其原因是(用离子方程式表示):__________________________。
(2)将SO 气体通入FeCl 溶液中,溶液由棕黄色变为浅绿色,其原因是(用离子方程式表示):
2 3
________________________________________________________________________。
(3)S2-和SO可以大量共存,但加入HSO 后,则不能大量共存,其原因是(用离子方程式表
2 4
示):__________________________________________________________________________。(4)将SO 通入BaCl 溶液中无明显现象,若加入KNO 则有白色沉淀生成,其原因是(用离子
2 2 3
方程式表示):___________________________________________________________________。
(5)书写下列反应的化学方程式。
①将HS气体通入CuSO 溶液中:
2 4
________________________________________________________________________。
②将SO 通入HS溶液中:
2 2
________________________________________________________________________。
③Cu和浓HSO 混合加热:
2 4
________________________________________________________________________。
④C和浓HSO 混合加热:
2 4
________________________________________________________________________。
⑤实验室利用NaSO 和浓HSO 制SO :
2 3 2 4 2
________________________________________________________________________。
(八)氮及其重要化合物
氮是与化工生产、生活和生态环境密切相关的另一重要元素,在自然界中既可以以游离态存
在,又可以以化合态存在。复习时应从以下几个方面掌握:
1.树立物质转化思想
(1)理清知识主线
NH―→N2 ―→NO―→NO―→NO―→HNO
3 2 2 3
(2)形成网络构建
2.重要反应规范书写
用方程式回答下列问题。
(1)书写离子方程式。
①将NH 通入AlCl 溶液中:
3 3
________________________________________________________________________。
②将NO 通入NaOH溶液中:
2
________________________________________________________________________。
③将炽热的炭放入浓HNO 中:
3
________________________________________________________________________。
(2)书写化学方程式。
①实验室用Ca(OH) 和NH Cl制氨气:
2 4
________________________________________________________________________。②将NH 通入灼热的CuO中,固体由黑色变红色:___________________________。
3
③用NH 可以检验Cl 管道是否漏气,若漏气则有白烟生成:___________________。
3 2
④制硝基苯:_____________________________________________________________。
角度一 与“环境”有关的转化关系
1.(2020·全国卷Ⅱ,9)二氧化碳的过量排放可对海洋生物的生存环境造成很大影响,其原理
如下图所示。下列叙述错误的是( )
A.海水酸化能引起HCO浓度增大、CO浓度减小
B.海水酸化能促进CaCO 的溶解,导致珊瑚礁减少
3
C.CO 能引起海水酸化,其原理为HCOH++CO
2
D.使用太阳能、氢能等新能源可改善珊瑚的生存环境
2.(2018·全国卷Ⅱ,8)研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如
下图所示)。下列叙述错误的是( )
A.雾和霾的分散剂相同
B.雾霾中含有硝酸铵和硫酸铵
C.NH 是形成无机颗粒物的催化剂
3
D.雾霾的形成与过度施用氮肥有关
角度二 与“价—类二维图”有关的物质转化
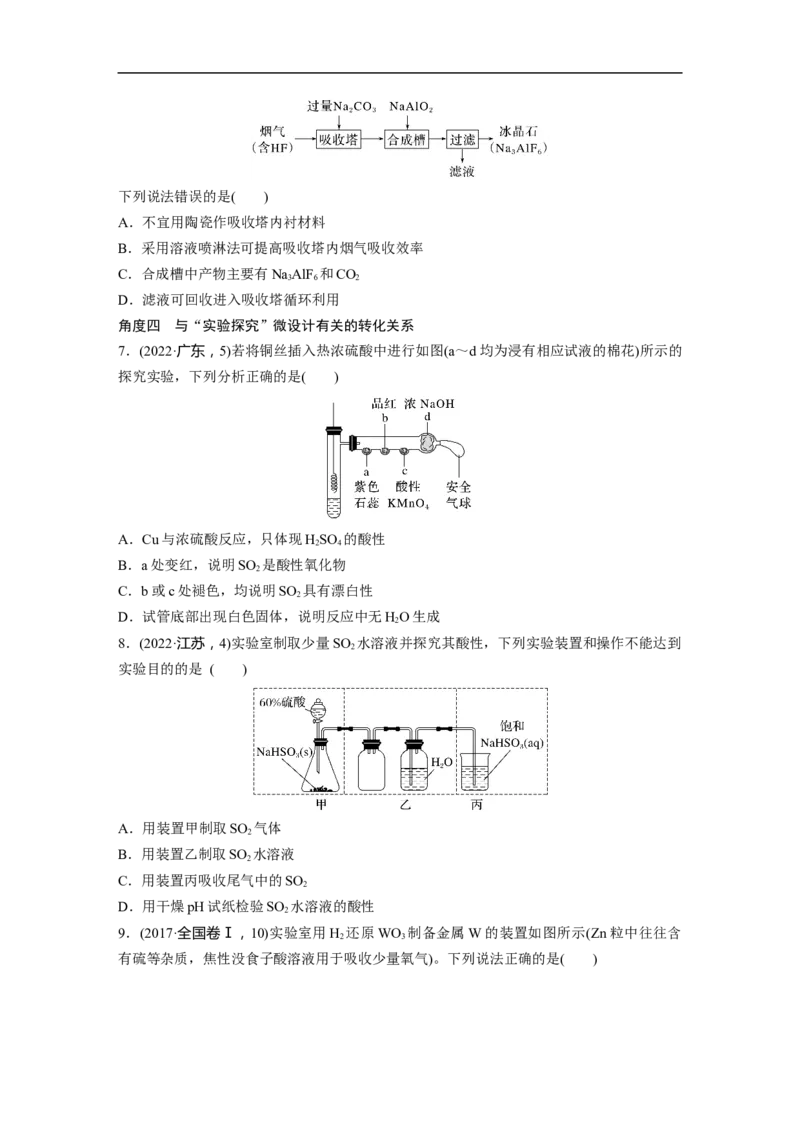
3.(2021·广东,10)部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是(
)A.a可与e反应生成b
B.b既可被氧化,也可被还原
C.可将e加入浓碱液中制得d的胶体
D.可存在b→c→d→e→b的循环转化关系
角度三 与“化工流程”微设计有关的转化关系
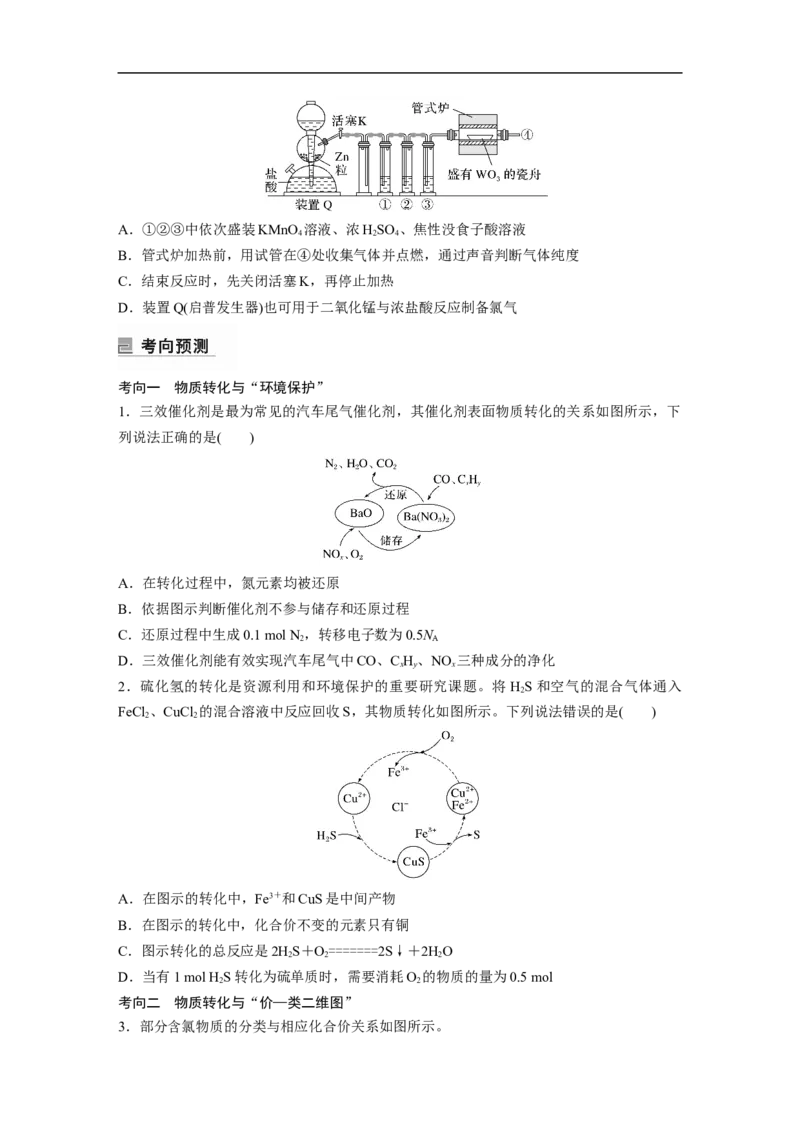
4.(2022·河北,8)LiBr溶液可作为替代氟利昂的绿色制冷剂。合成LiBr工艺流程如下:
下列说法错误的是( )
A.还原工序逸出的Br 用NaOH溶液吸收,吸收液直接返回还原工序
2
B.除杂工序中产生的滤渣可用煤油进行组分分离
C.中和工序中的化学反应为LiCO+2HBr===CO↑+2LiBr+HO
2 3 2 2
D.参与反应的n(Br)∶n(BaS)∶n(H SO )为1∶1∶1
2 2 4
5.(2022·山东,12)高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含Zn、Fe元
素的杂质)为主要原料制备Cu粉的工艺流程如下,可能用到的数据见下表。
Fe(OH) Cu(OH) Zn(OH)
3 2 2
开始沉淀pH 1.9 4.2 6.2
沉淀完全pH 3.2 6.7 8.2
下列说法错误的是( )
A.固体X主要成分是Fe(OH) 和S;金属M为Zn
3
B.浸取时,增大O 压强可促进金属离子浸出
2
C.中和调pH的范围为3.2~4.2
D.还原时,增大溶液酸度有利于Cu的生成
6.(2022·湖南,7)铝电解厂烟气净化的一种简单流程如下:下列说法错误的是( )
A.不宜用陶瓷作吸收塔内衬材料
B.采用溶液喷淋法可提高吸收塔内烟气吸收效率
C.合成槽中产物主要有NaAlF 和CO
3 6 2
D.滤液可回收进入吸收塔循环利用
角度四 与“实验探究”微设计有关的转化关系
7.(2022·广东,5)若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的
探究实验,下列分析正确的是( )
A.Cu与浓硫酸反应,只体现HSO 的酸性
2 4
B.a处变红,说明SO 是酸性氧化物
2
C.b或c处褪色,均说明SO 具有漂白性
2
D.试管底部出现白色固体,说明反应中无HO生成
2
8.(2022·江苏,4)实验室制取少量SO 水溶液并探究其酸性,下列实验装置和操作不能达到
2
实验目的的是 ( )
A.用装置甲制取SO 气体
2
B.用装置乙制取SO 水溶液
2
C.用装置丙吸收尾气中的SO
2
D.用干燥pH试纸检验SO 水溶液的酸性
2
9.(2017·全国卷Ⅰ,10)实验室用H 还原WO 制备金属W的装置如图所示(Zn粒中往往含
2 3
有硫等杂质,焦性没食子酸溶液用于吸收少量氧气)。下列说法正确的是( )A.①②③中依次盛装KMnO 溶液、浓HSO 、焦性没食子酸溶液
4 2 4
B.管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体纯度
C.结束反应时,先关闭活塞K,再停止加热
D.装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气
考向一 物质转化与“环境保护”
1.三效催化剂是最为常见的汽车尾气催化剂,其催化剂表面物质转化的关系如图所示,下
列说法正确的是( )
A.在转化过程中,氮元素均被还原
B.依据图示判断催化剂不参与储存和还原过程
C.还原过程中生成0.1 mol N,转移电子数为0.5N
2 A
D.三效催化剂能有效实现汽车尾气中CO、CH、NO 三种成分的净化
x y x
2.硫化氢的转化是资源利用和环境保护的重要研究课题。将 HS和空气的混合气体通入
2
FeCl 、CuCl 的混合溶液中反应回收S,其物质转化如图所示。下列说法错误的是( )
2 2
A.在图示的转化中,Fe3+和CuS是中间产物
B.在图示的转化中,化合价不变的元素只有铜
C.图示转化的总反应是2HS+O=======2S↓+2HO
2 2 2
D.当有1 mol H S转化为硫单质时,需要消耗O 的物质的量为0.5 mol
2 2
考向二 物质转化与“价—类二维图”
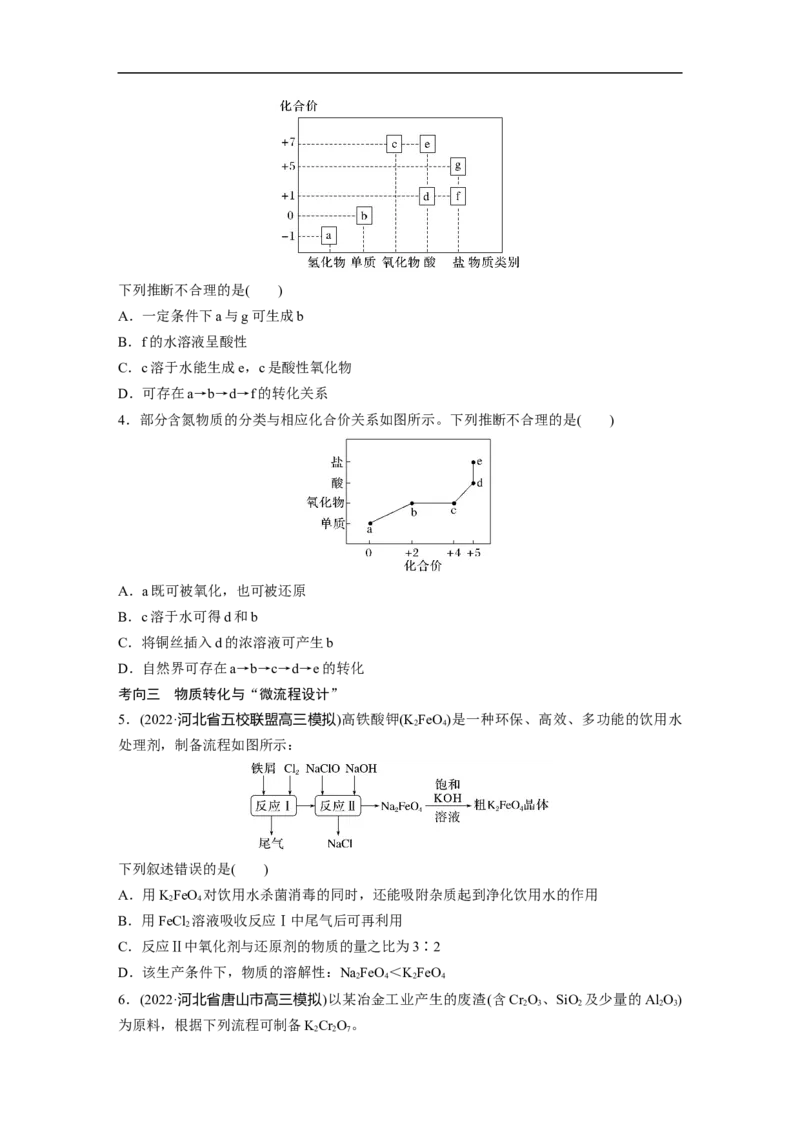
3.部分含氯物质的分类与相应化合价关系如图所示。下列推断不合理的是( )
A.一定条件下a与g可生成b
B.f的水溶液呈酸性
C.c溶于水能生成e,c是酸性氧化物
D.可存在a→b→d→f的转化关系
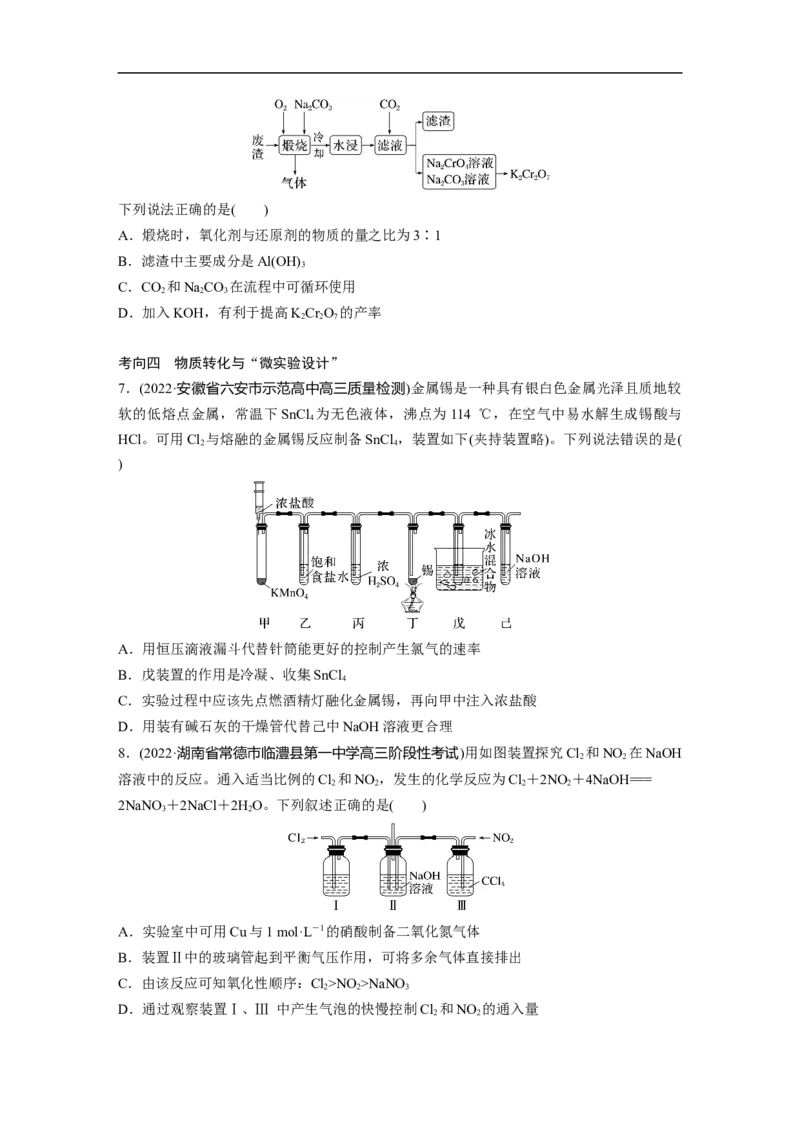
4.部分含氮物质的分类与相应化合价关系如图所示。下列推断不合理的是( )
A.a既可被氧化,也可被还原
B.c溶于水可得d和b
C.将铜丝插入d的浓溶液可产生b
D.自然界可存在a→b→c→d→e的转化
考向三 物质转化与“微流程设计”
5.(2022·河北省五校联盟高三模拟)高铁酸钾(K FeO)是一种环保、高效、多功能的饮用水
2 4
处理剂,制备流程如图所示:
下列叙述错误的是( )
A.用KFeO 对饮用水杀菌消毒的同时,还能吸附杂质起到净化饮用水的作用
2 4
B.用FeCl 溶液吸收反应Ⅰ中尾气后可再利用
2
C.反应Ⅱ中氧化剂与还原剂的物质的量之比为3∶2
D.该生产条件下,物质的溶解性:NaFeO<KFeO
2 4 2 4
6.(2022·河北省唐山市高三模拟)以某冶金工业产生的废渣(含Cr O 、SiO 及少量的Al O)
2 3 2 2 3
为原料,根据下列流程可制备KCr O。
2 2 7下列说法正确的是( )
A.煅烧时,氧化剂与还原剂的物质的量之比为3∶1
B.滤渣中主要成分是Al(OH)
3
C.CO 和NaCO 在流程中可循环使用
2 2 3
D.加入KOH,有利于提高KCr O 的产率
2 2 7
考向四 物质转化与“微实验设计”
7.(2022·安徽省六安市示范高中高三质量检测)金属锡是一种具有银白色金属光泽且质地较
软的低熔点金属,常温下SnCl 为无色液体,沸点为114 ℃,在空气中易水解生成锡酸与
4
HCl。可用Cl 与熔融的金属锡反应制备SnCl ,装置如下(夹持装置略)。下列说法错误的是(
2 4
)
A.用恒压滴液漏斗代替针筒能更好的控制产生氯气的速率
B.戊装置的作用是冷凝、收集SnCl
4
C.实验过程中应该先点燃酒精灯融化金属锡,再向甲中注入浓盐酸
D.用装有碱石灰的干燥管代替己中NaOH溶液更合理
8.(2022·湖南省常德市临澧县第一中学高三阶段性考试)用如图装置探究Cl 和NO 在NaOH
2 2
溶液中的反应。通入适当比例的Cl 和NO ,发生的化学反应为Cl+2NO +4NaOH===
2 2 2 2
2NaNO +2NaCl+2HO。下列叙述正确的是( )
3 2
A.实验室中可用Cu与1 mol·L-1的硝酸制备二氧化氮气体
B.装置Ⅱ中的玻璃管起到平衡气压作用,可将多余气体直接排出
C.由该反应可知氧化性顺序:Cl>NO>NaNO
2 2 3
D.通过观察装置Ⅰ、Ⅲ 中产生气泡的快慢控制Cl 和NO 的通入量
2 2