文档内容
[复习目标] 1.掌握原子及物质结构的特点,掌握常见元素及物质的性质。2.掌握元素周期
表中“位—构—性”关系及其应用。
考点一 根据原子结构推断
1.常考短周期主族元素原子的核外电子排布特点
(1)最外层电子数为1的原子有H、Li、Na。
(2)最外层电子数为2的原子有He、Be、Mg。
(3)最外层电子数与次外层电子数相等的原子是Be。
(4)最外层电子数是次外层电子数2倍的原子是C。
(5)最外层电子数是次外层电子数3倍的原子是O。
(6)次外层电子数是最外层电子数2倍的原子有Li、Si。
(7)内层电子总数是最外层电子数2倍的原子有Li、P。
(8)电子层数(周期序数)与最外层电子数(族序数)相等的原子有H、Be、Al。
(9)电子层数为最外层电子数2倍的原子是Li。
(10)最外层电子数是电子层数2倍的原子是C、S。
(11)最外层电子数是电子层数3倍的原子是O。
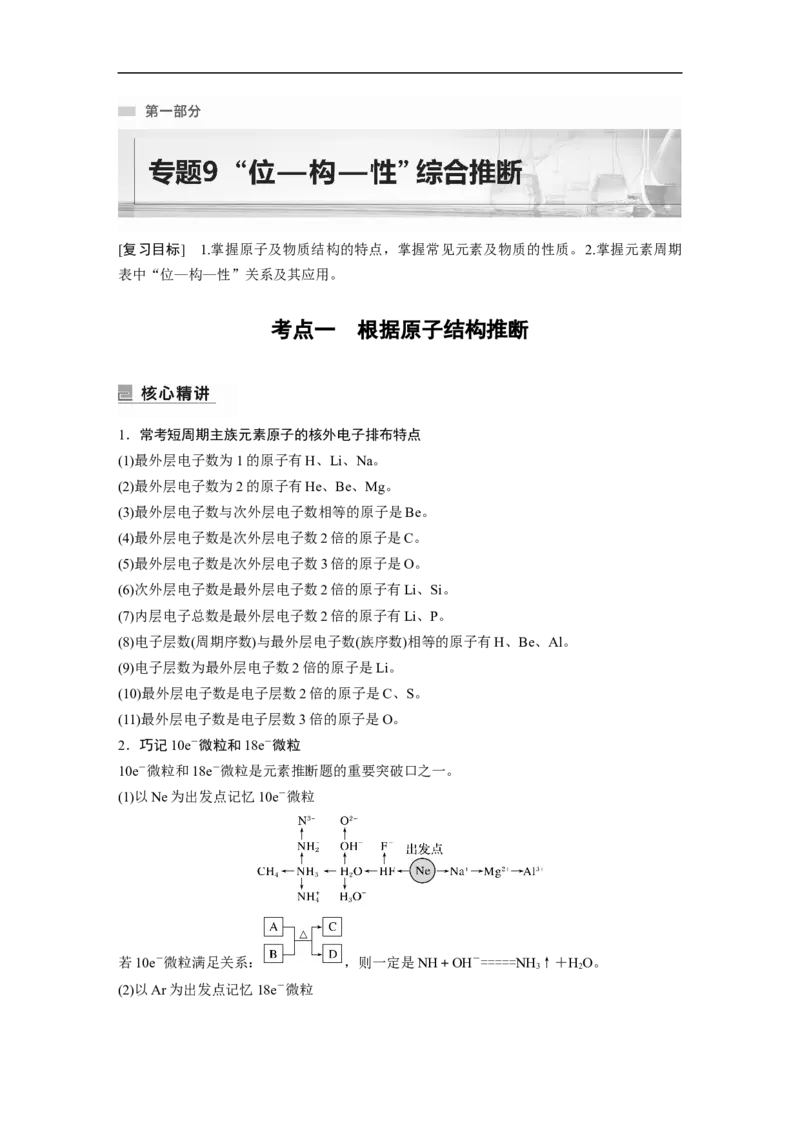
2.巧记10e-微粒和18e-微粒
10e-微粒和18e-微粒是元素推断题的重要突破口之一。
(1)以Ne为出发点记忆10e-微粒
若10e-微粒满足关系: ,则一定是NH+OH-=====NH ↑+HO。
3 2
(2)以Ar为出发点记忆18e-微粒1.(2021·全国甲卷,11)W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层
电子数是W和X的最外层电子数之和,也是Y的最外层电子数的2倍。W和X的单质常温
下均为气体。下列叙述正确的是( )
A.原子半径:Z>Y>X>W
B.W与X只能形成一种化合物
C.Y的氧化物为碱性氧化物,不与强碱反应
D.W、X和Z可形成既含有离子键又含有共价键的化合物
2.(2021·全国乙卷,11)我国嫦娥五号探测器带回1.731 kg的月球土壤,经分析发现其构成
与地球土壤类似,土壤中含有的短周期元素W、X、Y、Z,原子序数依次增大,最外层电
子数之和为15。X、Y、Z为同周期相邻元素,且均不与W同族。下列结论正确的是( )
A.原子半径大小顺序为W>X>Y> Z
B.化合物XW中的化学键为离子键
C.Y单质的导电性能弱于Z单质的
D.Z的氧化物的水化物的酸性强于碳酸
3.(2022·全国甲卷,12)Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外层电
子数之和为19。Q与X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是Q原子
内层电子数的2倍。下列说法正确的是( )
A.非金属性:X>Q
B.单质的熔点:X>Y
C.简单氢化物的沸点:Z>Q
D.最高价含氧酸的酸性:Z>Y
1.(2022·四川省德阳市高三下学期第二次检测)X、Y、Z、W、M是原子序数依次增大的短
周期主族元素,X的原子半径是短周期中最小的,Y的最外层电子数是其内层电子数的3倍,
Y、M同主族,Z、W、M同周期,W的族序数等于周期序数。下列叙述错误的是( )
A.简单离子的半径:Y>Z>W
B.简单氢化物的沸点:Y>M
C.X、Y、Z可形成含共价键的离子化合物D.Z、W的单质都能通过电解对应熔融氯化物制得
2.(2022·成都市第七中学高三下学期测试)W、X、Y、Z、Q为原子半径依次增大的短周期主
族元素,X的原子序数等于W与Y的原子序数之和,Z的原子半径是第三周期中最小的,
W与X形成的物质可用来杀菌消毒且该物质的分子中含 18e-,Q原子最外层电子数为X原
子最外层电子数的一半。下列说法不正确的是( )
A.X元素与Q元素组成的化合物可做耐火材料
B.由W、X、Y三种元素所组成化合物的水溶液可能显酸性也可能显碱性
C.简单氢化物的沸点:X>Y>Z
D.由Z和Q形成的化合物中存在离子键
考点二 根据物质结构推断
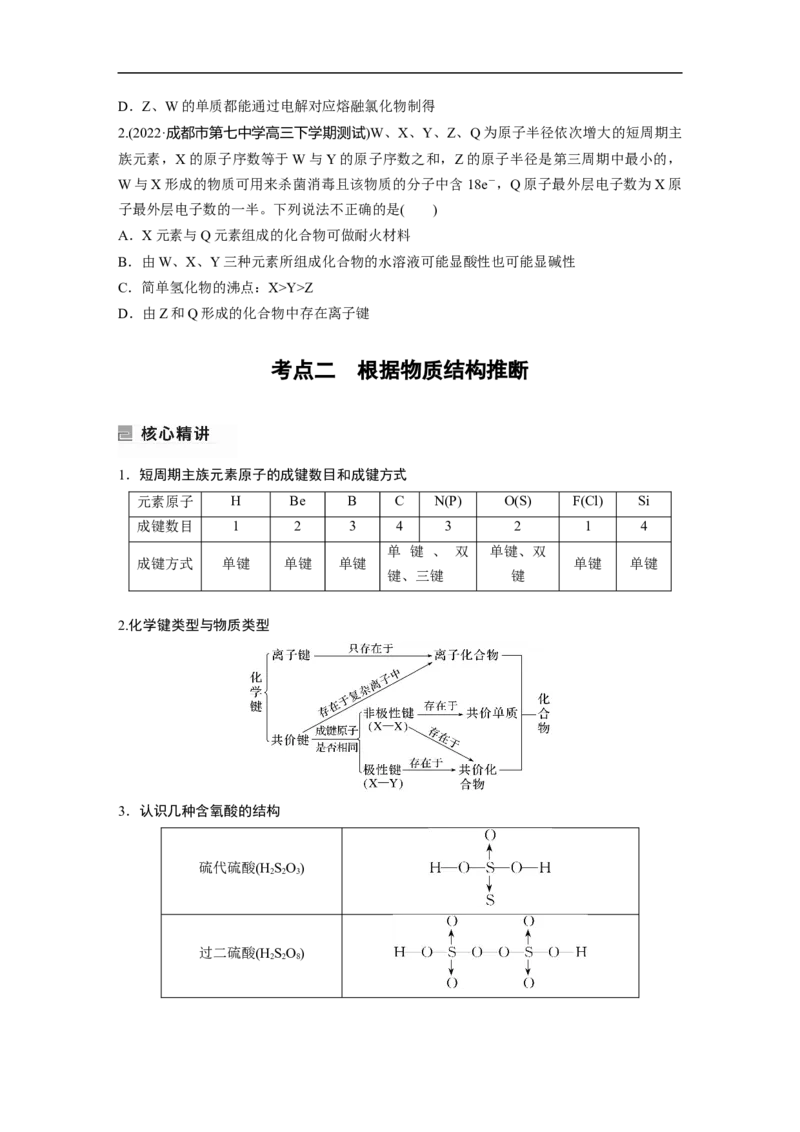
1.短周期主族元素原子的成键数目和成键方式
元素原子 H Be B C N(P) O(S) F(Cl) Si
成键数目 1 2 3 4 3 2 1 4
单 键 、 双 单键、双
成键方式 单键 单键 单键 单键 单键
键、三键 键
2.化学键类型与物质类型
3.认识几种含氧酸的结构
硫代硫酸(H SO)
2 2 3
过二硫酸(H SO)
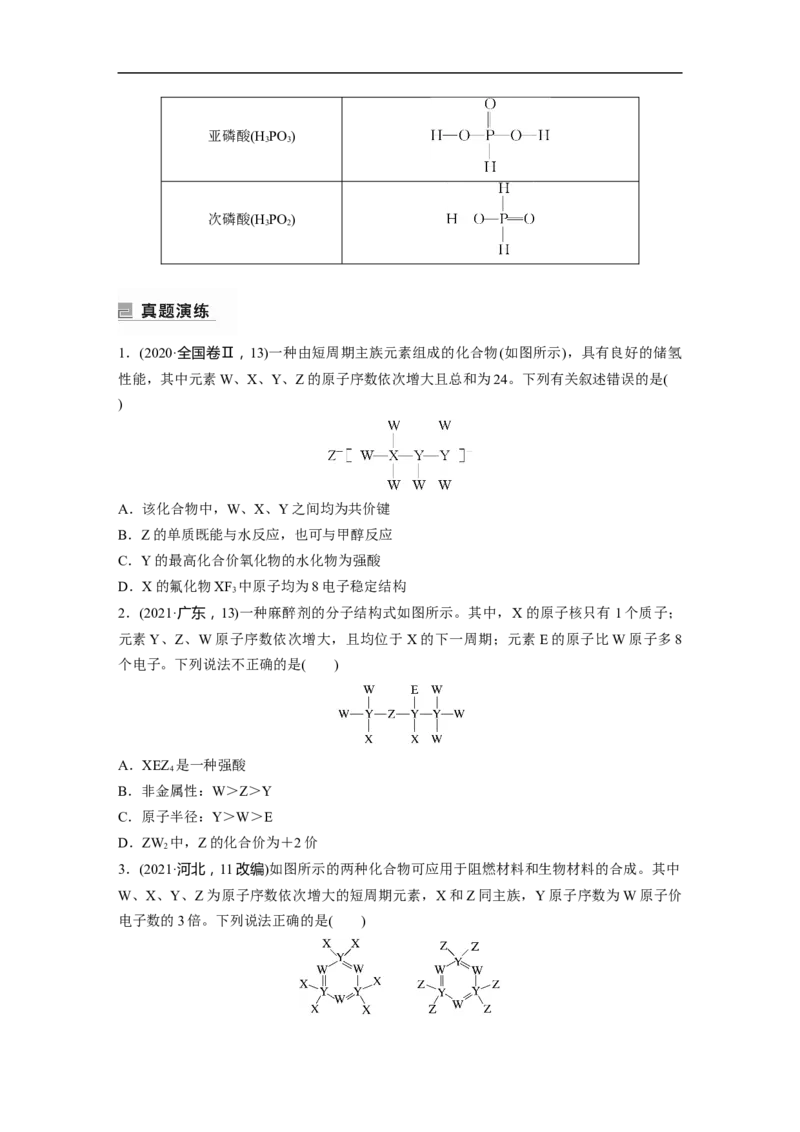
2 2 8亚磷酸(H PO )
3 3
次磷酸(H PO )
3 2
1.(2020·全国卷Ⅱ,13)一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢
性能,其中元素W、X、Y、Z的原子序数依次增大且总和为24。下列有关叙述错误的是(
)
A.该化合物中,W、X、Y之间均为共价键
B.Z的单质既能与水反应,也可与甲醇反应
C.Y的最高化合价氧化物的水化物为强酸
D.X的氟化物XF 中原子均为8电子稳定结构
3
2.(2021·广东,13)一种麻醉剂的分子结构式如图所示。其中,X的原子核只有1个质子;
元素Y、Z、W原子序数依次增大,且均位于X的下一周期;元素E的原子比W原子多8
个电子。下列说法不正确的是( )
A.XEZ 是一种强酸
4
B.非金属性:W>Z>Y
C.原子半径:Y>W>E
D.ZW 中,Z的化合价为+2价
2
3.(2021·河北,11改编)如图所示的两种化合物可应用于阻燃材料和生物材料的合成。其中
W、X、Y、Z为原子序数依次增大的短周期元素,X和Z同主族,Y原子序数为W原子价
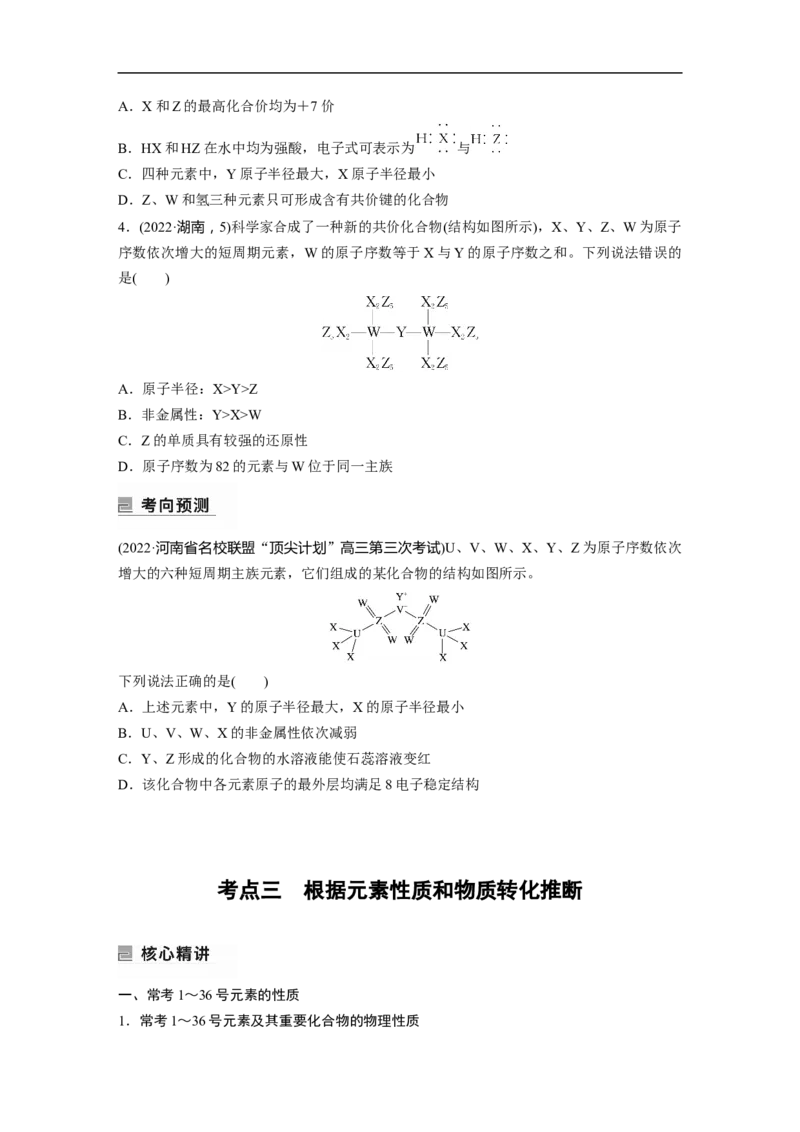
电子数的3倍。下列说法正确的是( )A.X和Z的最高化合价均为+7价
B.HX和HZ在水中均为强酸,电子式可表示为 与
C.四种元素中,Y原子半径最大,X原子半径最小
D.Z、W和氢三种元素只可形成含有共价键的化合物
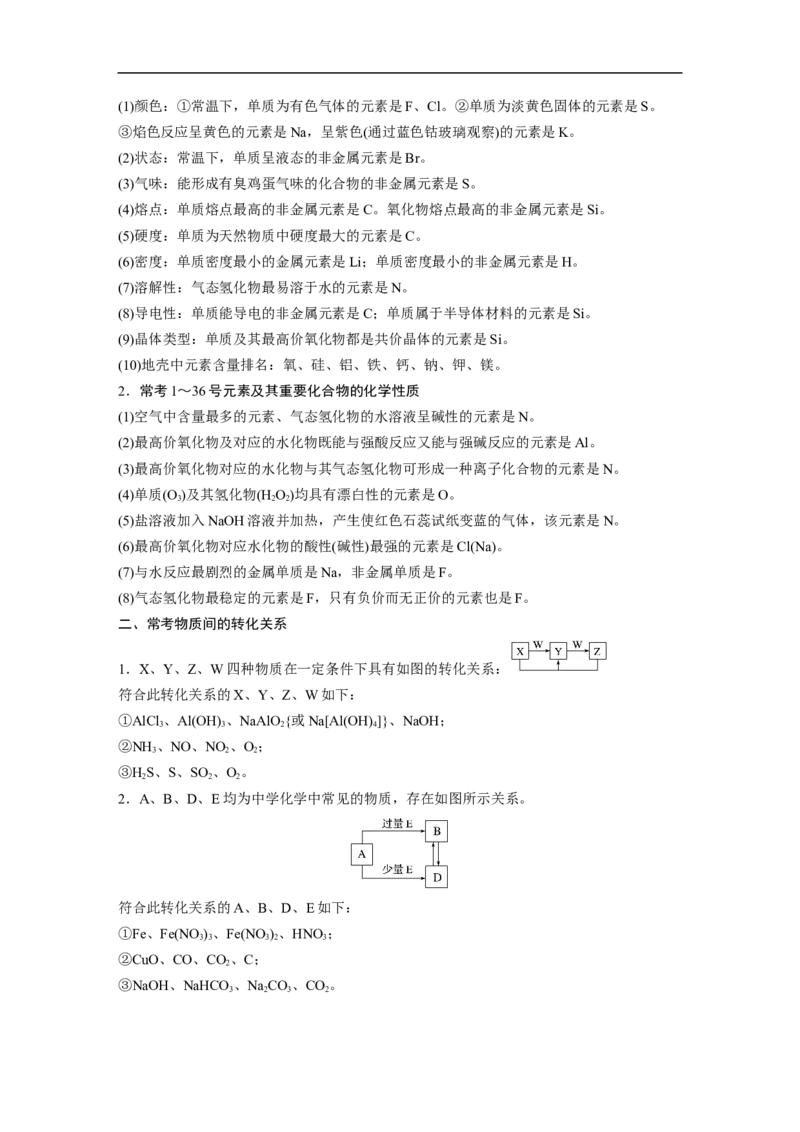
4.(2022·湖南,5)科学家合成了一种新的共价化合物(结构如图所示),X、Y、Z、W为原子
序数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和。下列说法错误的
是( )
A.原子半径:X>Y>Z
B.非金属性:Y>X>W
C.Z的单质具有较强的还原性
D.原子序数为82的元素与W位于同一主族
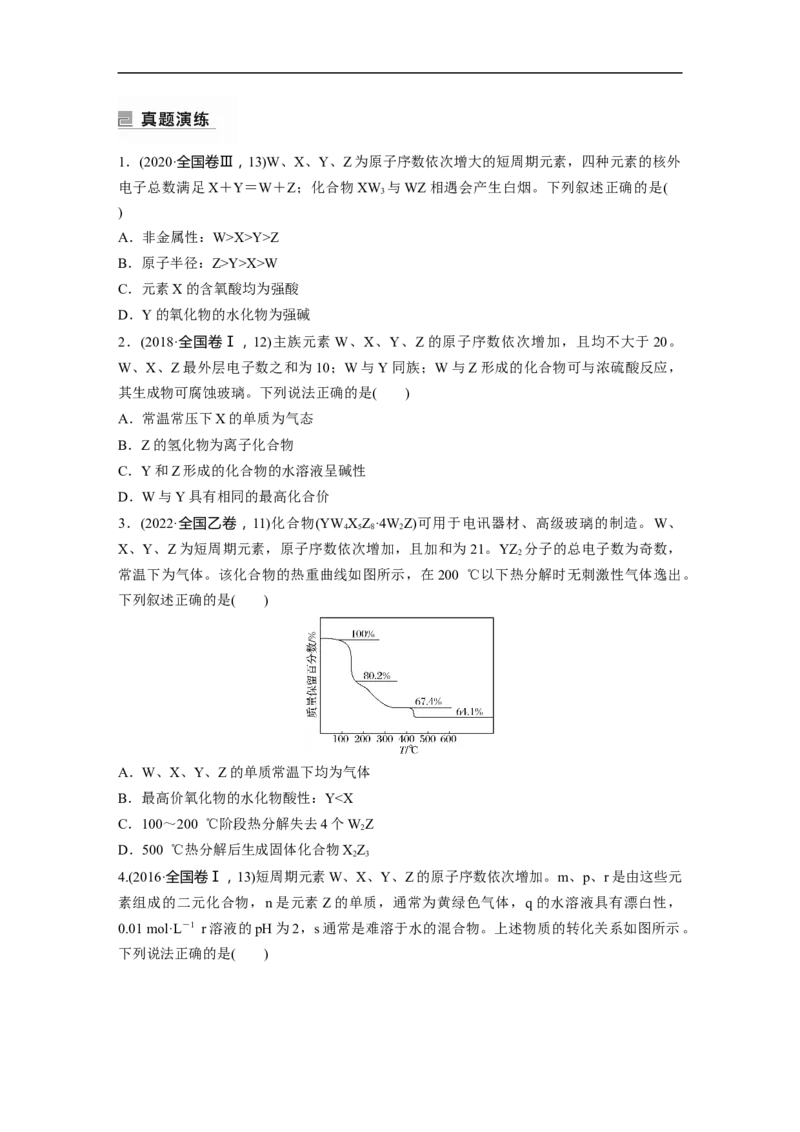
(2022·河南省名校联盟“顶尖计划”高三第三次考试)U、V、W、X、Y、Z为原子序数依次
增大的六种短周期主族元素,它们组成的某化合物的结构如图所示。
下列说法正确的是( )
A.上述元素中,Y的原子半径最大,X的原子半径最小
B.U、V、W、X的非金属性依次减弱
C.Y、Z形成的化合物的水溶液能使石蕊溶液变红
D.该化合物中各元素原子的最外层均满足8电子稳定结构
考点三 根据元素性质和物质转化推断
一、常考1~36号元素的性质
1.常考1~36号元素及其重要化合物的物理性质(1)颜色:①常温下,单质为有色气体的元素是F、Cl。②单质为淡黄色固体的元素是S。
③焰色反应呈黄色的元素是Na,呈紫色(通过蓝色钴玻璃观察)的元素是K。
(2)状态:常温下,单质呈液态的非金属元素是Br。
(3)气味:能形成有臭鸡蛋气味的化合物的非金属元素是S。
(4)熔点:单质熔点最高的非金属元素是C。氧化物熔点最高的非金属元素是Si。
(5)硬度:单质为天然物质中硬度最大的元素是C。
(6)密度:单质密度最小的金属元素是Li;单质密度最小的非金属元素是H。
(7)溶解性:气态氢化物最易溶于水的元素是N。
(8)导电性:单质能导电的非金属元素是C;单质属于半导体材料的元素是Si。
(9)晶体类型:单质及其最高价氧化物都是共价晶体的元素是Si。
(10)地壳中元素含量排名:氧、硅、铝、铁、钙、钠、钾、镁。
2.常考1~36号元素及其重要化合物的化学性质
(1)空气中含量最多的元素、气态氢化物的水溶液呈碱性的元素是N。
(2)最高价氧化物及对应的水化物既能与强酸反应又能与强碱反应的元素是Al。
(3)最高价氧化物对应的水化物与其气态氢化物可形成一种离子化合物的元素是N。
(4)单质(O )及其氢化物(H O)均具有漂白性的元素是O。
3 2 2
(5)盐溶液加入NaOH溶液并加热,产生使红色石蕊试纸变蓝的气体,该元素是N。
(6)最高价氧化物对应水化物的酸性(碱性)最强的元素是Cl(Na)。
(7)与水反应最剧烈的金属单质是Na,非金属单质是F。
(8)气态氢化物最稳定的元素是F,只有负价而无正价的元素也是F。
二、常考物质间的转化关系
1.X、Y、Z、W四种物质在一定条件下具有如图的转化关系:
符合此转化关系的X、Y、Z、W如下:
①AlCl 、Al(OH) 、NaAlO {或Na[Al(OH)]}、NaOH;
3 3 2 4
②NH 、NO、NO 、O;
3 2 2
③HS、S、SO 、O。
2 2 2
2.A、B、D、E均为中学化学中常见的物质,存在如图所示关系。
符合此转化关系的A、B、D、E如下:
①Fe、Fe(NO )、Fe(NO )、HNO;
3 3 3 2 3
②CuO、CO、CO、C;
2
③NaOH、NaHCO 、NaCO、CO。
3 2 3 21.(2020·全国卷Ⅲ,13)W、X、Y、Z为原子序数依次增大的短周期元素,四种元素的核外
电子总数满足X+Y=W+Z;化合物XW 与WZ相遇会产生白烟。下列叙述正确的是(
3
)
A.非金属性:W>X>Y>Z
B.原子半径:Z>Y>X>W
C.元素X的含氧酸均为强酸
D.Y的氧化物的水化物为强碱
2.(2018·全国卷Ⅰ,12)主族元素W、X、Y、Z的原子序数依次增加,且均不大于20。
W、X、Z最外层电子数之和为10;W与Y同族;W与Z形成的化合物可与浓硫酸反应,
其生成物可腐蚀玻璃。下列说法正确的是( )
A.常温常压下X的单质为气态
B.Z的氢化物为离子化合物
C.Y和Z形成的化合物的水溶液呈碱性
D.W与Y具有相同的最高化合价
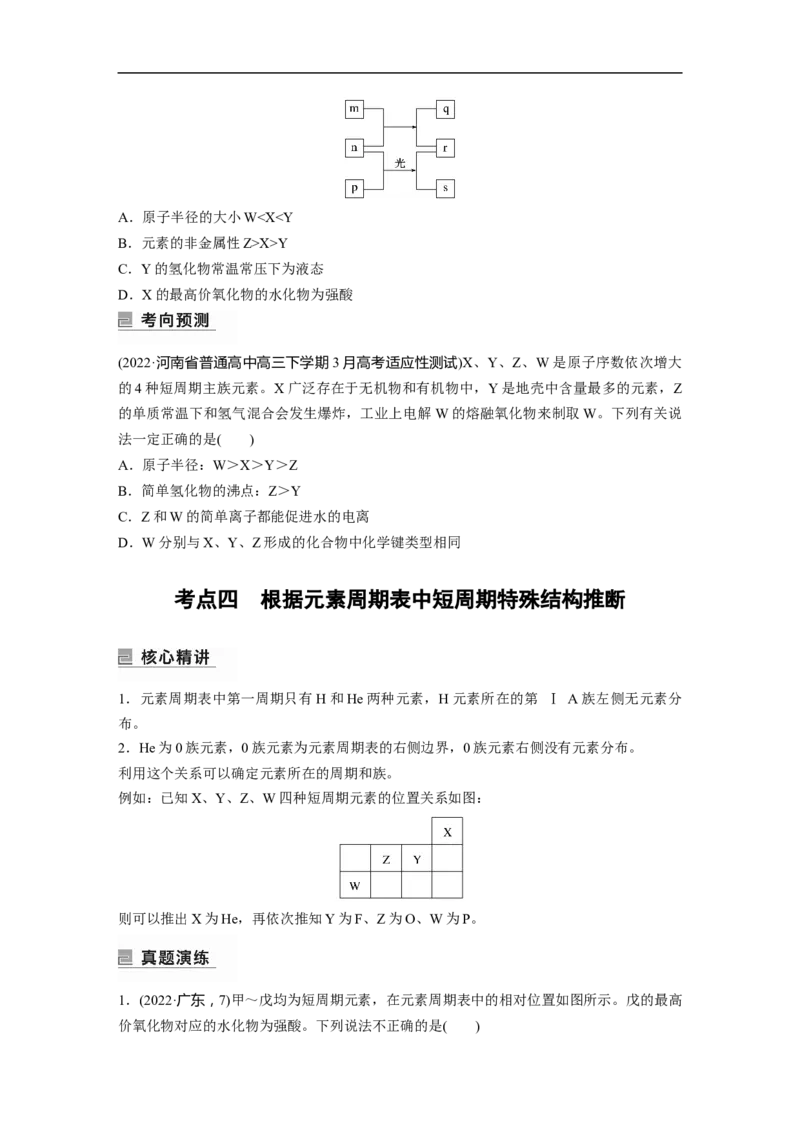
3.(2022·全国乙卷,11)化合物(YW XZ·4W Z)可用于电讯器材、高级玻璃的制造。W、
4 5 8 2
X、Y、Z为短周期元素,原子序数依次增加,且加和为21。YZ 分子的总电子数为奇数,
2
常温下为气体。该化合物的热重曲线如图所示,在200 ℃以下热分解时无刺激性气体逸出。
下列叙述正确的是( )
A.W、X、Y、Z的单质常温下均为气体
B.最高价氧化物的水化物酸性:YX>Y
C.Y的氢化物常温常压下为液态
D.X的最高价氧化物的水化物为强酸
(2022·河南省普通高中高三下学期3月高考适应性测试)X、Y、Z、W是原子序数依次增大
的4种短周期主族元素。X广泛存在于无机物和有机物中,Y是地壳中含量最多的元素,Z
的单质常温下和氢气混合会发生爆炸,工业上电解 W的熔融氧化物来制取W。下列有关说
法一定正确的是( )
A.原子半径:W>X>Y>Z
B.简单氢化物的沸点:Z>Y
C.Z和W的简单离子都能促进水的电离
D.W分别与X、Y、Z形成的化合物中化学键类型相同
考点四 根据元素周期表中短周期特殊结构推断
1.元素周期表中第一周期只有H和He两种元素,H元素所在的第 Ⅰ A族左侧无元素分
布。
2.He为0族元素,0族元素为元素周期表的右侧边界,0族元素右侧没有元素分布。
利用这个关系可以确定元素所在的周期和族。
例如:已知X、Y、Z、W四种短周期元素的位置关系如图:
则可以推出X为He,再依次推知Y为F、Z为O、W为P。
1.(2022·广东,7)甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高
价氧化物对应的水化物为强酸。下列说法不正确的是( )A.原子半径:丁>戊>乙
B.非金属性:戊>丁>丙
C.甲的氢化物遇氯化氢一定有白烟产生
D.丙的最高价氧化物对应的水化物一定能与强碱反应
2.(2021·浙江6月选考,15改编)已知短周期元素X、Y、Z、M、Q和R在元素周期表中的
相对位置如图所示,其中Y的最高化合价为+3。下列说法不正确的是( )
A.还原性:ZQQ
(2022·山西省高三下学期高考考前适应性测试)W、X、Y、Z是原子序数依次增大的短周期
主族元素,W、Y在元素周期表中的相对位置如图所示,W元素最外层与次外层的电子数
之差为3,W的核电荷数与Z元素的最外层电子数之和等于X的原子序数。下列推断正确的
是( )
A.简单离子半径:Y<Z
B.氢化物的稳定性:X<Y<Z
C.氧化物对应水化物的酸性:W<X<Z
D.化合物WZ、YZ 中既含离子键又含共价键
3 2 2