文档内容
第 26 讲 难溶电解质的溶解平衡
第一部分:高考真题感悟
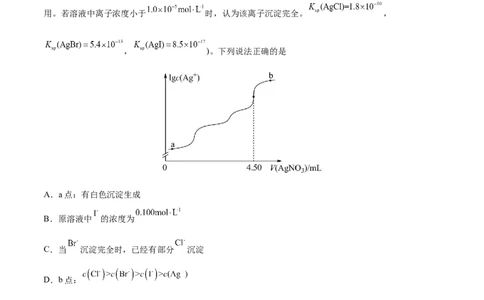
1.(2022·湖南·高考真题)室温时,用 的标准 溶液滴定 浓度相等的 、
和 混合溶液,通过电位滴定法获得 与 的关系曲线如图所示(忽略沉淀对离子的吸附作
用。若溶液中离子浓度小于 时,认为该离子沉淀完全。 ,
, )。下列说法正确的是
A.a点:有白色沉淀生成
B.原溶液中 的浓度为
C.当 沉淀完全时,已经有部分 沉淀
D.b点:
【答案】C
【解析】向含浓度相等的 Cl-、 Br-和 I-混合溶液中滴加硝酸银溶液,根据三种沉淀的溶度积常数,三种离
子沉淀的先后顺序为I-、Br-、Cl-,根据滴定图示,当滴入4.50mL硝酸银溶液时,Cl-恰好沉淀完全,此时
共消耗硝酸银的物质的量为4.50mL×10-3L/mL×0.1000mol/L=4.5×10-4mol,所以Cl-、 Br-和 I-均为1.5×10-
4mol。A.I-先沉淀,AgI是黄色的,所以a点有黄色沉淀AgI生成,故A错误;B.原溶液中I-的物质的量为1.5×10-4mol,则I-的浓度为 =0.0100molL-1,故B错误;C.当Br-沉淀完全时(Br-浓度为
⋅
1.0×10-5mol/L),溶液中的c(Ag+)= =5.4×10-8mol/L,若Cl-已经开始沉淀,则此时溶液
中的c(Cl-)= =3.3×10-3mol/L,原溶液中的c(Cl-)= c(I-)=0.0100molL-1,则已经有部分
⋅
Cl-沉淀,故C正确;D.b点加入了过量的硝酸银溶液,溶液中的I-、Br-、Cl-全部转化为沉淀,则Ag+浓度
最大,根据溶度积可知,b点各离子浓度为: ,故D错误;故选C。
2.(2021·江苏·高考真题)室温下,用0.5mol·L-1NaCO 溶液浸泡CaSO 粉末,一段时间后过滤,向滤渣
2 3 4
中加稀醋酸,产生气泡。已知K (CaSO)=5×10-5,K (CaCO)=3×10-9。下列说法正确的是
sp 4 sp 3
A.0.5mol·L-1NaCO 溶液中存在:c(OH-)=c(H+)+c(HCO )+c(H CO)
2 3 2 3
B.反应CaSO+CO CaCO +SO 正向进行,需满足 > ×104
4 3
C.过滤后所得清液中一定存在:c(Ca2+)= 且c(Ca2+)≤
D.滤渣中加入醋酸发生反应的离子方程式:CaCO +2H+=Ca2++CO ↑+H O
3 2 2
【答案】C
【解析】A.0.5mol·L-1NaCO 溶液中存在质子守恒:c(OH-)=c(H+)+c(HCO )+2c(H CO),A错误;B.该
2 3 2 3
反应的平衡常数K= = = = = ×104,当浓度商 <K时,反应正
向进行,B错误;C.上层清液为碳酸钙的保护溶液,所以清液中满足c(Ca2+)= ,由于硫酸钙沉淀转化为碳酸钙沉淀,所以清液为硫酸钙的不饱和溶液,则c(Ca2+)≤ ,C正确;D.醋酸为
弱酸,不能拆成离子形式,D错误;综上所述答案为C。
3.(2022·山东·高考真题)高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含Zn、Fe元素的杂
质)为主要原料制备Cu粉的工艺流程如下,可能用到的数据见下表。
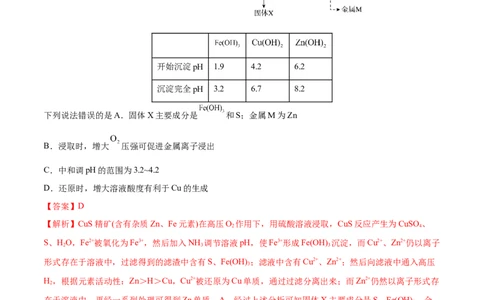
开始沉淀pH 1.9 4.2 6.2
沉淀完全pH 3.2 6.7 8.2
下列说法错误的是A.固体X主要成分是 和S;金属M为Zn
B.浸取时,增大 压强可促进金属离子浸出
C.中和调pH的范围为3.2~4.2
D.还原时,增大溶液酸度有利于Cu的生成
【答案】D
【解析】CuS精矿(含有杂质Zn、Fe元素)在高压O 作用下,用硫酸溶液浸取,CuS反应产生为CuSO 、
2 4
S、HO,Fe2+被氧化为Fe3+,然后加入NH 调节溶液pH,使Fe3+形成Fe(OH) 沉淀,而Cu2+、Zn2+仍以离子
2 3 3
形式存在于溶液中,过滤得到的滤渣中含有S、Fe(OH) ;滤液中含有Cu2+、Zn2+;然后向滤液中通入高压
3
H,根据元素活动性:Zn>H>Cu,Cu2+被还原为Cu单质,通过过滤分离出来;而Zn2+仍然以离子形式存
2
在于溶液中,再经一系列处理可得到Zn单质。A.经过上述分析可知固体X主要成分是S、Fe(OH) ,金
3
属M为Zn,A正确;B.CuS难溶于硫酸,在溶液中存在沉淀溶解平衡CuS(s) Cu2+(aq)+S2-(aq),增大O
2
的浓度,可以反应消耗S2-,使之转化为S,从而使沉淀溶解平衡正向移动,从而可促进金属离子的浸取,
B正确;C.根据流程图可知:用NH 调节溶液pH时,要使Fe3+转化为沉淀,而Cu2+、Zn2+仍以离子形式
3
存在于溶液中,结合离子沉淀的pH范围,可知中和时应该调节溶液pH范围为3.2~4.2,C正确;D.在
用H 还原Cu2+变为Cu单质时,H 失去电子被氧化为H+,与溶液中OH-结合形成HO,若还原时增大溶液
2 2 2
的酸度,c(H+)增大,不利于H 失去电子还原Cu单质,因此不利于Cu的生成,D错误;故合理选项是D。
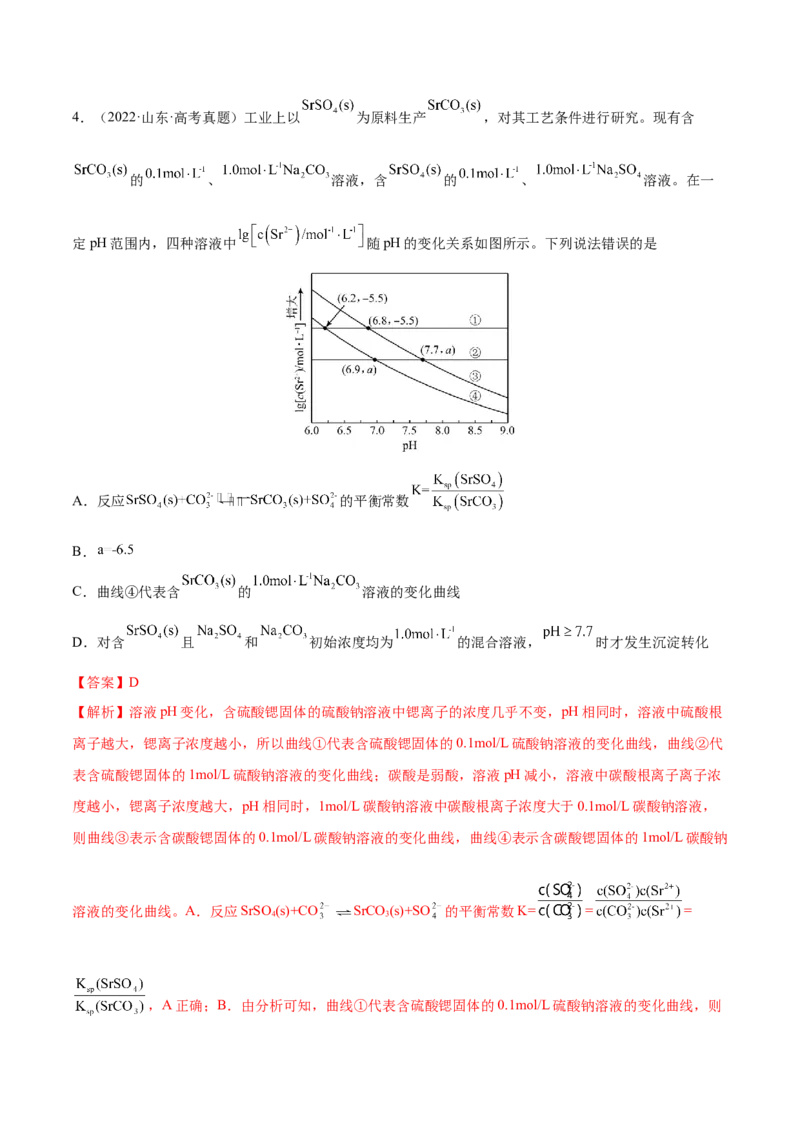
24.(2022·山东·高考真题)工业上以 为原料生产 ,对其工艺条件进行研究。现有含
的 、 溶液,含 的 、 溶液。在一
定pH范围内,四种溶液中 随pH的变化关系如图所示。下列说法错误的是
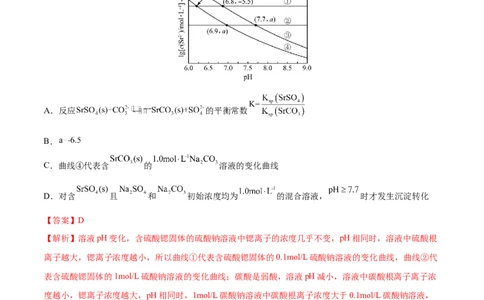
A.反应 的平衡常数
B.
C.曲线④代表含 的 溶液的变化曲线
D.对含 且 和 初始浓度均为 的混合溶液, 时才发生沉淀转化
【答案】D
【解析】溶液pH变化,含硫酸锶固体的硫酸钠溶液中锶离子的浓度几乎不变,pH相同时,溶液中硫酸根
离子越大,锶离子浓度越小,所以曲线①代表含硫酸锶固体的0.1mol/L硫酸钠溶液的变化曲线,曲线②代
表含硫酸锶固体的1mol/L硫酸钠溶液的变化曲线;碳酸是弱酸,溶液pH减小,溶液中碳酸根离子离子浓
度越小,锶离子浓度越大,pH相同时,1mol/L碳酸钠溶液中碳酸根离子浓度大于0.1mol/L碳酸钠溶液,
则曲线③表示含碳酸锶固体的0.1mol/L碳酸钠溶液的变化曲线,曲线④表示含碳酸锶固体的1mol/L碳酸钠
溶液的变化曲线。A.反应SrSO (s)+CO SrCO (s)+SO 的平衡常数K= = =
4 3
,A正确;B.由分析可知,曲线①代表含硫酸锶固体的0.1mol/L硫酸钠溶液的变化曲线,则硫酸锶的溶度积K (SrSO )=10—5.5×0.1=10—6.5,温度不变,溶度积不变,则溶液pH为7.7时,锶离子的浓度
sp 4
为 =10—6.5,则a为-6.5,B正确;C.由分析可知,曲线④表示含碳酸锶固体的1mol/L碳酸钠溶液
的变化曲线,C正确;D.对含SrSO (s)且NaSO 和NaCO 初始浓度均为1.0mol·L-1的混合溶液中锶离子
4 2 4 2 3
的浓度为10-6, 5,根据图示, 锶离子的降低,所以 发生沉淀转化,D错误;故选D。
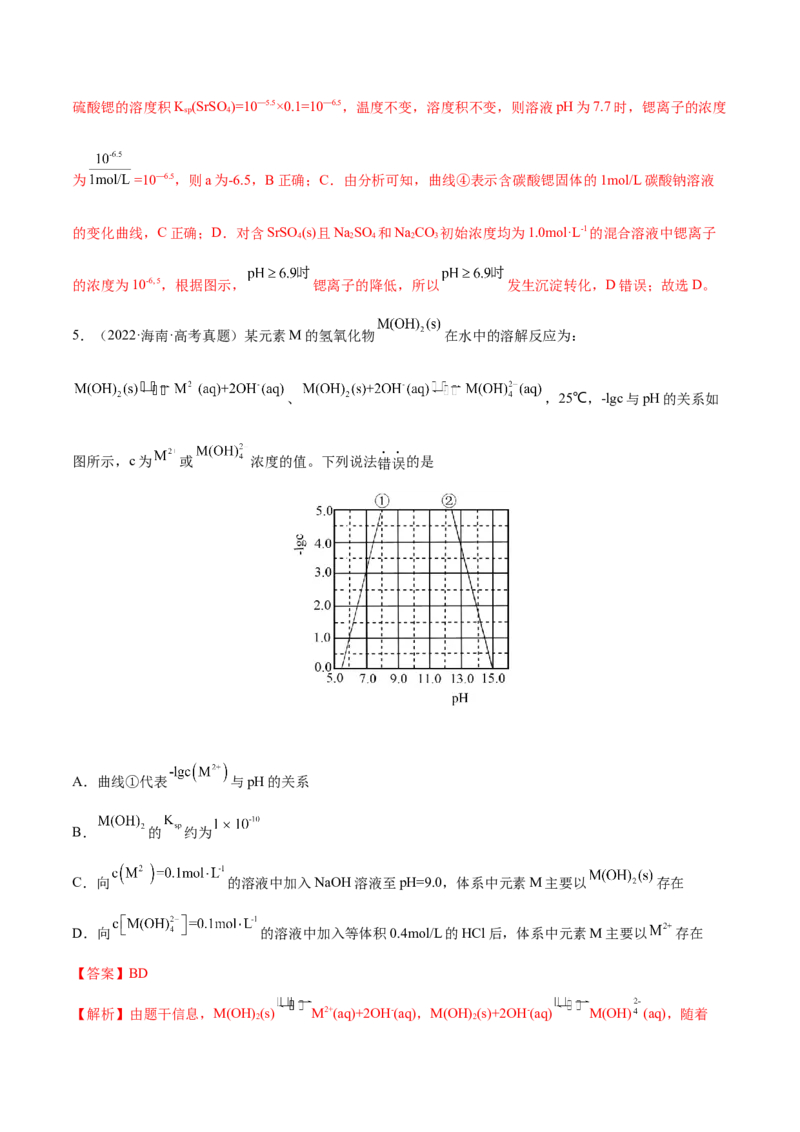
5.(2022·海南·高考真题)某元素M的氢氧化物 在水中的溶解反应为:
、 ,25℃,-lgc与pH的关系如
图所示,c为 或 浓度的值。下列说法错误的是
A.曲线①代表 与pH的关系
B. 的 约为
C.向 的溶液中加入NaOH溶液至pH=9.0,体系中元素M主要以 存在
D.向 的溶液中加入等体积0.4mol/L的HCl后,体系中元素M主要以 存在
【答案】BD
【解析】由题干信息,M(OH) (s) M2+(aq)+2OH-(aq),M(OH) (s)+2OH-(aq) M(OH) (aq),随着
2 2pH增大,c(OH-)增大,则c(M2+)减小,c[M(OH) ]增大,即-lg c(M2+)增大,-lg c[M(OH) ]减小,因此曲线
①代表-lg c(M2+)与pH的关系,曲线②代表-lg c[M(OH) ]与pH的关系,据此分析解答。
A.由分析可知,曲线①代表-lg c(M2+)与pH的关系,A正确;B.由图象,pH=7.0时,-lg c(M2+)=3.0,则
M(OH) 的K =c(M2+)·c2(OH-)=1×10-17,B错误;C.向c(M2+)=0.1mol/L的溶液中加入NaOH溶液至
2 sp
pH=9.0,根据图像,pH=9.0时,c(M2+)、c[M(OH) ]均极小,则体系中元素M主要以M(OH) (s)存在,C
2
正确;D.c[M(OH) ]=0.1mol/L的溶液中,由于溶解平衡是少量的,因此加入等体积的0.4mol/L的HCl后,
体系中元素M仍主要以M(OH) 存在,D错误;答案选BD。
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·江苏·模拟预测)化工生产中含Cu2+的废水常用MnS作沉淀剂除去,反应原理为MnS(s)+Cu2+
(aq) CuS(s)+Mn2+(aq)。已知:K (MnS)=2.6×10-13,K (CuS)=1.3×10-36。下列说法正确的是
sp sp
A.基态Mn2+的电子排布式为[Ar]3d6
B.当溶液中c(Cu2+)=c(Mn2+)时,反应达到平衡
C.MnS(s)+Cu2+(aq) CuS(s)+Mn2+(aq),该反应的平衡常数K=2.0×1023
D.反应后上层清液中一定存在:c(S2-)>
【答案】C
【解析】A.Mn原子电子排布式为[Ar]3d54s2,Mn失去最外层两个电子形成Mn2+,故基态Mn2+电子排布
式为[Ar]3d5,A错误;B.该反应平衡常数表达式:K= =,故平衡时c(Mn2+)=2×1023c(Cu2+),B错误;C.由B选项分析知,C正确;D.生成CuS
后的溶液是ZnS、CuS的饱和溶液,故上层清液存在c(S2-)= = ,D错误;故答案选C。
2.(2022·北京市十一学校三模)实验室探究 溶液与碱反应的规律。实验数据和现象如下表所示(溶
液体积均取用 )。
组
药品1 药品2 实验现象
别
Ⅰ 溶液 溶液 生成白色沉淀
Ⅱ 氨水 溶液 无现象
Ⅲ 氨水 溶液 生成白色沉淀
Ⅳ 氨水 溶液 现象Ⅳ
Ⅴ 氨水 溶液 无现象
下列说法正确的是A.Ⅲ中反应的离子方程式为:
B.Ⅲ中 是Ⅱ中 的10倍,因此Ⅱ中无现象而Ⅲ中有沉淀
C.现象Ⅳ无法通过预测确定
D.上述实验说明: 溶液与氨水反应时,改变相同浓度时,氨水的影响大于氯化镁
【答案】D
【解析】A.Ⅲ中发生的反应为氯化镁溶液与氨水反应生成氯化铵和氢氧化镁沉淀,反应的离子方程式为
,故A错误;B.氨水是弱碱,在溶液中存在电离平衡,浓度越小,
电离程度越大,所以1mol/L氨水中氢氧根离子浓度比0.1mol/L氨水中氢氧根离子浓度的10倍要小,故B
错误;C.Ⅲ中生成白色沉淀说明0.1mol/L氨水与0.1mol/L氯化镁溶液反应能生成氢氧化镁沉淀,溶液中
c(Mg2+)c2(OH—)>K [Mg(OH) ],1mol/L氯化镁溶液中镁离子浓度大于0.1mol/L氯化镁溶液中镁离子浓度,
sp 2
所以溶液中c(Mg2+)c2(OH—)>K [Mg(OH) ],会有氢氧化镁白色沉淀生成,故C错误;D.由0.1mol/L氨水
sp 2与0.1mol/L氯化镁溶液和1mol/L氯化镁溶液都不能反应生成白色沉淀,而1mol/L氨水与0.1mol/L氯化镁
溶液和1mol/L氯化镁溶液都能反应生成白色沉淀可知,氯化镁溶液与氨水反应时,改变相同浓度时,氨水
的影响大于氯化镁,故D正确;故选D。
3.(2022·重庆一中模拟预测)室温下,在 悬浊液中存在如下平衡:
,已知
下列说法错误的是
A.平衡时,
B.平衡时,
C.该温度下,
D.加入少量 固体, 减小, 增大
【答案】D
【解析】A.由 ,平衡时,
,A正确;B.由 ,平衡时,
,解得 ,则
,B正确;C.将两个平衡式相加可得
,该温度下, ,C正确;D.
加入少量 固体,Ca2+与 结合生成CaCO 沉淀,促进沉淀溶解平衡正向移动, 增大,
3由于仍是饱和溶液,温度不变则 不变,D错误;故选:D。
4.(2022·安徽·合肥市第八中学模拟预测)MA 是一种微溶盐,M(OH) 是二元强碱,HA是一元弱酸。
2 2
25℃时,实验测得随着c(H+)变化,MA 饱和溶液中pM与δ(A-)的关系如图所示,其中a点对应的pH=5.0,
2
[已知pM=-lgc(M2+),δ(A-)= ]。则下列说法错误的是
A.HA的电离常数Ka为1.0×10-5
B.a点对应溶液中有c(M2+)=c(HA)
C.Ksp(MA )的数量级为10-9
2
D.b点对应溶液中c(OH-)=9×10-5
【答案】D
【解析】A.a点时δ(A-)=0.5,可知 ,此时pH=5.0,HA的电离常数Ka=
,故A正确;B.a点,根据物料守恒可知:2c(M2+)= ,又此时
,则c(M2+)=c(HA),故B正确;C.a点时c(M2+)= mol/L,c(M2+)=c(HA)= , =
mol/L,则Ksp(MA )= = ,故C正确;D.b点时δ(A-)=0.1,则 ,由
2
以上已知:Ka= ,则 = =9×10-5,c(OH-)= ,故D错误;故选:D。
5.(2022·江苏·扬州中学三模)室温下,可用NaS、FeS等处理含Hg2+的废水。已知:
2
, , , 。当离子浓度小
于 时,认为该离子沉淀完全。下列说法正确的是
A.向 溶液中存在:
B. 的平衡常数为
C.向 溶液中通入过量 气体,可使 沉淀完全
D.向含有 的废水中加入 ,如果 完全转化为 ,则上层清液中一定存在
【答案】D
【解析】A.根据质子守恒可知, 溶液中存在: ,A错
误;B. 的平衡常数为Kh= = = = ≠
,B错误;C.向1L0.1mol/LFeCl 溶液中通入过量HS气体,则该反应为:Fe2++H S
2 2 2
FeS+2H+,该反应的K= = = =0.6<<105,即不可使
Fe2+沉淀完全,C错误;D.向含有 的废水中加入 ,如果 完全转化为 ,则上层清液中一定
存在 ,D正确;故答案为:D。
6.(2022·内蒙古·满洲里市教研培训中心三模)表中是有关物质的溶解度(20℃),下列说法正确的是物质 CaCl Ca(OH) CaCO
2 2 3
溶解度(g/100g) 74.5 0.165 0.0013
A.除去粗盐中含有的CaCl 杂质,最佳除杂试剂为NaOH溶液
2
B.0.1mol的Ca(OH) 和0.1molCaCO 混合加入1L水中,所得溶液中:c(OH-)>c(Ca2+)>c(CO )
2 3
C.将CaCl 、Ca(OH) 、CaCO 三种物质和水混合,加热、灼烧,最终的固体产物相同
2 2 3
D.用足量的NaOH溶液与Ca(HCO ),发生的离子方程式式为:4OH-+Ca2++2HCO =Ca(OH) ↓+2CO
3 2 2
+2H O
2
【答案】B
【解析】A.根据表中数据可知,除去粗盐中含有的氯化钙杂质,最佳除杂试剂为碳酸钠,故A不符合题
意;B.氢氧化钙微溶于水,碳酸钙难溶于水,因此离子浓度大小顺序是c(OH-)>c(Ca2+)>c(CO ),故B
符合题意;C.氯化钙加热、灼烧得到物质氯化钙,氢氧化钙、碳酸钙灼烧最后得到物质是CaO,故C不
符合题意;D.碳酸钙比氢氧化钙更难溶,足量氢氧化钠与碳酸氢钙反应的离子方程式为2OH-+2HCO
+Ca2+=CaCO ↓+CO +2H O,故D不符合题意;答案为B。
3 2
7.(2022·黑龙江·哈九中模拟预测)2022年1月中旬南太平洋岛国汤加的洪阿哈阿帕伊岛多次发生火山喷
发并引发大范围海啸,大量的火山灰和火山气体对气候造成极大的影响。硫在自然界的循环过程如图所示。
下图是火山喷发产生的化学物质,在自然界的转化历程和工业应用。下列说法错误的是
A.火山喷发形成硫酸型酸雨,反应总反应为2SO +O +H O=2HSO
2 2 2 2 4
B.火山喷发会影响气温下降的可能原因是大量气体进入平流层形成硫酸气溶胶阻挡太阳辐射
C.自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO 溶液,向地下深层渗透遇到难溶的
4PbS,慢慢转变为铜蓝(CuS),离子方程式为Cu2++ +Pb2++S2—=PbSO↓+CuS↓
4
D.工业制备硫酸可用硫铁矿经FeS→SO →SO →HSO 多步反应制备
2 2 3 2 4
【答案】C
【解析】A.由图可知,火山喷发会生成二氧化硫,二氧化硫与空气中的氧气和雨水反应生成硫酸,使雨
水呈酸性形成硫酸型酸雨,反应的总反应方程式为2SO +O +H O=2HSO ,故A正确;B.火山喷发产生
2 2 2 2 4
的大量气体进入平流层后,会形成硫酸气溶胶阻挡太阳辐射从而导致气温下降,故B正确;C.由题意可
知,硫化铅转化为硫化铜的反应为硫化铅与硫酸铜溶液反应生成硫酸铅和硫化铜,反应的离子方程式为
PbS+Cu2++ =CuS+PbSO ,故C错误;D.工业上可以用煅烧硫铁矿的方法制备硫酸,硫铁矿经
4
FeS→SO →SO →HSO 多步反应制得硫酸,故D正确;故选C。
2 2 3 2 4
8.(2022·湖北·房县第一中学三模)国家速滑馆又称为“冰丝带”,所用的碲化镉(CdTe)发电玻璃被誉为
“挂在墙上的油田”。一种以镉废渣(含CdO及少量ZnO、 、MnO、FeO杂质)为原料制备镉的工艺
流程如图所示:
已知:部分金属阳离子以氢氧化物形式沉淀时溶液的pH如下表所示:
金属阳离子
开始沉淀时的pH 2.7 6.3 3.4
完全沉淀时的pH 3.2 8.3 5.0
下列说法错误的是A.调节 的目的是除去Fe和Al等杂质元素
B.“滤渣2”的主要成分为 、
C.“置换”后滤液溶质中含有
D.“纯化”过程中发生的反应为
【答案】A【解析】根据流程图可知,镉废渣中加入硫酸溶液后生成多种硫酸盐,加入石灰乳调节 ,生成沉淀
和 向滤液中加入 溶液,将 氧化为 沉淀、将 氧化为 ;向滤
液中加入锌置换出Cd,得到海绵镉,用氢氧化钠溶液溶解海绵镉中过量的锌,得到Cd和 。
A.调节 ,生成的沉淀为 和 ,没除去Fe元素,选项A错误;B.滤液中加入
溶液,将 氧化为 沉淀,将 氧化为 ,则“滤渣2”主要成分为 、 ,选
项B正确;C.滤液中加入锌置换出Cd,“置换”后滤液溶质中含有 ,选项C正确;D.“纯化”
过程中发生反应的化学方程式为 ,选项D正确;答案选A。
9.(2022·河北张家口·三模)某温度下,CuS和 的溶解曲线如图所示,其中 ,
, 为 或 ,下列说法错误的是
A.曲线Ⅰ是CuS的溶解曲线 B.
C.M点的坐标为(23,13) D.此温度下的饱和溶液:
【答案】D
【解析】A.CuS的阴阳离子个数比为1:1,Ag S的阴阳离子个数比为1:2,曲线Ⅰ在横轴与纵轴上的截距
2
相同,因此曲线Ⅰ是CuS的溶解曲线,则曲线Ⅱ是 的溶解曲线,A正确;B.由曲线Ⅱ与纵轴交点的
坐标可知, ,则当 时,,因此 ,B正确;C.由曲线I与纵轴交点的坐标可知,
,设M点的坐标为 ,则有 , ,解得
, ,因此M点的坐标为 ,C正确;D. , ,此温
度下CuS的饱和溶液中 ,Ag S的饱和溶液中
2
,则此温度下的饱和溶液: ,D错误;答案
选D。
10.(2022·江苏连云港·模拟预测)已知:25℃,K (H C O)=5.0×10-2,K (H C O)=5.0×10-5,
a1 2 2 4 a2 2 2 4
K(NH ·H O)=1.8×10-5。常温下,通过下列实验探究NH HC O 溶液的性质,有关说法正确的是
b 3 2 4 2 4
实验 实验操作及现象
1 用pH试纸测0.1 mol·L-1 NH HC O 溶液的pH<7
4 2 4
2 向10 mL 0.1 mol·L-1 NH HC O 溶液中滴加10 mL 0.1 mol·L-1Ba(OH) 溶液,产生白色沉淀,过滤
4 2 4 2
向实验2所得白色沉淀中加入10 mL饱和NaCO 溶液,浸泡一段时间,无明显现象,过滤,向滤
3 2 3
渣中滴加盐酸,有气体生成
A.实验1溶液中存在:c(HC O )>c(NH )>c(C O )>c(HC O)
2 2 2 2 4
B.实验2反应的离子方程式为:HC O +Ba2++OH-═ BaC O↓+HO
2 2 4 2
C.实验3中发生:BaC O+CO BaCO +C O , 不变时说明沉淀转化达平衡
2 4 3 2
D.由实验3可得:K (BaC O)>K (BaCO)
sp 2 4 sp 3
【答案】C
【解析】A.已知K(NH ·H O)=1.8×10-5,根据NH + H O NH ·H O+H+,NH 的水解常数为: =
b 3 2 2 3 2
⇌≈5.6×10-10,已知 K (H C O)=5.0×10-2,根据HC O +H2O HC O+OH- ,HC O 的水解常数为:
a1 2 2 4 2 2 2 4 2
⇌
= =2×10-13,再根据K (H C O)=5.0×10-5,可知草酸氢根的电离大于铵根离子的水解大于草酸氢
a2 2 2 4
根的水解,可得:c(NH )>c(HC O )>c(HC O)>c(C O ),A错误;B.根据n=cv,可知
2 2 2 4 2
n(NH HC O)=n(Ba(OH) )=10×10-3L×0.1 mol·L-1=10-3mol,根据电荷守恒和原子守恒,可得反应的离子方程
4 2 4 2
式为:NH +HC O +Ba2++2OH--═ BaC O↓+H O+NH ·H O,B错误;C.根据实验3,可知草酸钡沉淀中加
2 2 4 2 3 2
入饱和碳酸钠溶液转化为碳酸钡和草酸根离子,反应的离子方程式为:BaC O+CO BaCO +C O ,根
2 4 3 2
⇌
据该反应,可得,K= , 不变时说明沉淀转化达平衡,C正确;D.Qc > Ksp时生成碳酸
钡沉淀,由现象不能比较Ksp大小,D错误;故选C。
11.(2022·河北保定·二模)已知:AgA、 都是难溶盐。室温下,向体积均为10mL、浓度均为
的NaA溶液、 溶液中分别滴加 的 溶液,溶液中pX与 溶液体积的
关系如图所示[已知: 或 ]。下列推断错误的是
A.室温下,
B.对应溶液中 :C.室温下,在等量的水中,AgA溶解的物质的量更少
D.若 变为 ,则c点向e点移动
【答案】D
【解析】由图可知,室温下,加入10mL硝酸银溶液时,NaA溶液完全反应得到AgA饱和溶液,溶液中A
—离子和Ag+离子浓度都为10—bmol/L,AgA的溶度积为10—2b,加入20mL硝酸银溶液时,NaB溶液完全反
2
应得到Ag B饱和溶液,溶液中B2—离子浓度为10—amol/L、Ag+离子都为2×10—2mol/L,Ag B的溶度积为
2 2
4×10-3a。A.由分析可知,室温下,Ag B的溶度积K (Ag B)=4×10-3a,故A正确;B.由图可知,e点时
2 sp 2
NaA溶液过量,f点时NaA溶液恰好反应,由温度不变,溶度积不变可知,e点银离子浓度小于f点,故B
正确;C.由分析可知,AgA饱和溶液中银离子浓度小于Ag B饱和溶液,所以AgA的溶解度小于Ag B,
2 2
故C正确;D.若硝酸银溶液浓度变为0.05mol/L,则加入20mL硝酸银溶液时,NaA溶液完全反应得到
AgA饱和溶液,由温度不变,溶度积不变可知,溶液中Ag+离子浓度还是10—bmol/L,则c点会向d点移动,
故D错误;故选D。
12.(2022·辽宁·二模)锅炉水垢中含有的 可先用 处理,使其转化为易溶于酸的 除去。
室温下,用 溶液浸泡 粉末,一段时间后过滤,向滤液和滤渣中分别加醋酸,均产生
气泡。已知 、 的 分别为 、 。下列说法正确的是
A. 溶液中存在:
B.使 正向进行,需满足
C.过滤后所得清液中存在: 且
D.向滤液中加入少量醋酸时,反应的离子方程式:
【答案】C
【解析】A. 溶液中存在质子守恒为: ,A项错误;B.反应的平衡常数
,当 时,即浓度商>K,平
衡逆向移动,B项错误;C.向滤液和滤渣中分别加醋酸,均产生气泡,说明上层清夜为碳酸钙的饱和溶
液,则清夜中 ,由于 沉淀转化为了更难溶的 沉淀,所以上层清夜为硫
酸钙的不饱和溶液,则 ,C项正确;D.滤液中加入少量醋酸时生成 ,离子方
程式为: ,D项错误;故答案选C。
二、主观题(共3小题,共40分)
13.(2020·湖北荆州·模拟预测)(12分)已知K、K、K 、K、K 分别表示弱酸的电离平衡常数、弱
a b w h sp
碱的电离平衡常数,水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。通过查阅资料获得
温度为25℃时以下数据:K =1.0×10-14,K(CHCOOH)=1.8×10-5,K(HSCN)=0.13,K(HF)=4.0×10-
w a 3 a a
4,K [Mg(OH) ]=1.8×10-11
sp 2
(1)有关上述常数的说法正确的是__________。
a.它们都能反映一定条件下对应变化进行的程度
b.所有弱电解质的电离常数和难溶电解质的K 都随温度的升高而增大
sp
c.常温下,CHCOOH在水中的K 大于在饱和CHCOONa溶液中的K
3 a 3 a
d.一定温度下,在CHCOONa溶液中,K =K·K
3 w a h
(2)已知CHCOONH 溶液为中性,又知CHCOOH溶液加到NaCO 溶液中有气体放出,现有25℃时等浓
3 4 3 2 3
度的四种溶液:A.NH Cl,B.NH SCN,C.CHCOONH,D.NH HCO 。回答下列问题:
4 4 3 4 4 3
①试推断NH HCO 溶液的pH__________7(填“>”、“<”或“=”);
4 3
②将四种溶液按NH +浓度由大到小的顺序排列是:__________(填序号)。
4
③NH SCN溶液中所有离子浓度由大到小的顺序为_________。
4
(3)为探究Mg(OH) 在酸中的溶解性,利用以上数据可以计算出反应:Mg(OH) (s)+2CHCOOH(aq) Mg2
2 2 3
+(aq)+2CHCOO-(aq)+2HO(l)在25℃时的平衡常数K=________,并据此推断Mg(OH) _________(填
3 2 2“能”或“不能”)溶解于醋酸。(已知1.83≈5.8)
【答案】(每空2分)(1)ad
(2)①> ②A>B>C>D ③c(SCN-)> c(NH +)> c(H+)> c(OH-)
4
(3) 能
【解析】(1)a. 平衡常数等于生成物浓度幂之积与反应物浓度幂之积的比,所以它们都能反映一定条件
下对应变化进行的程度,a正确;
b. 难溶电解质Ca(OH) 的K 随温度的升高而减小,b错误;
2 sp
c. 电离平衡常数只与温度有关,温度相同电离平衡常数相同,c错误;
d. 一定温度下,在CHCOONa溶液中, ,所以K =K K,
3 W a h
⋅
d正确;故答案为:ad;
(2)①已知CHCOONH 溶液为中性,说明CHCOO-和NH +水解程度相同,又知CHCOOH溶液加到
3 4 3 4 3
NaCO 溶液中有气体放出,说明酸性:CHCOOH>H CO,越弱越水解,可知HCO -水解程度大于NH +水
2 3 3 2 3 3 4
解程度,所以NH HCO 溶液显碱性,pH>7;故答案为:>;
4 3
②根据电离平衡常数可知,酸性:HSCN> CH COOH>H CO,越弱越水解,所以四种溶液按NH +浓度由
3 2 3 4
大到小的顺序:A>B>C>D;故答案为:A>B>C>D;
③酸性:HSCN> CH COOH ,CHCOO-和NH +水解程度相同,所以NH +水解程度大于SCN-水解程度,
3 3 4 4
NH SCN溶液显酸性,其所有离子浓度由大到小的顺序为:c(SCN-)> c(NH +)> c(H+)> c(OH-);故答案为:
4 4
c(SCN-)> c(NH +)> c(H+)> c(OH-);
4
(3)在25℃时,平衡常数K= ,据此推断Mg(OH) 能溶解于醋酸,故答案为: ;能。
2
14.(2021·山西太原·模拟预测)(12分)山西老陈醋是中国四大名醋之首,食醋的主要成分为醋酸。已
知:25℃时CHCOOH的电离常数K=1.8×10-5。请回答:
3 a
(1)25℃时,pH=2的醋酸溶液中,c(H+)______;将其加水稀释, 的值将______(填“增大”
“减小”或“无法判断”)。
(2)醋酸钠溶液呈碱性的原因是______(用离子方程式表示),溶液中各离子浓度由大到小的顺序为______。
(3)已知25℃时,HS的K =1.3×10-7、K =7.1×10-15、,则25℃时等浓度的CHCOONa、NaS两种溶液的碱
2 a1 a2 3 2
性较强的是______。
(4)日常生活中可用醋酸除水垢,但工业锅炉的水垢中常含有硫酸钙,需先用NaCO 溶液处理,最后再用
2 3NH Cl溶液除去。已知:25℃时,K (CaCO)=2.8×10-9、K (CaSO)=9.1×10-6、,结合化学平衡原理解释加
4 sp 3 sp 4
入NaCO 溶液的原因:______(用溶解平衡表达式和必要的文字叙述加以说明)。
2 3
【答案】(每空2分)(1)10-2mol/L 增大
(2)CH COO-+H O CHCOOH+OH- c(Na+)>c(CHCOO-)>c(OH-)>c(H+)
3 2 3 3
(3)Na S
2
(4)硫酸钙饱和溶液中存在沉淀溶解平衡CaSO Ca2++SO ,加入NaCO 溶液后,CO 与Ca2+结合,转
4 2 3
化为K 更小的CaCO 沉淀,使CaSO 的沉淀溶解平衡向溶解方向移动
sp 3 4
【解析】(1)pH=2则溶液中c(H+)=10-2mol/L; ,加水稀释K 不变,酸性减弱c(H+)减
a
小,所以 增大;
(2)醋酸钠溶液中因存在醋酸根的水解CHCOO-+H O CHCOOH+OH-,所以显碱性;水解是微弱的,所
3 2 3
以溶液中c(Na+)>c(CHCOO-)>c(OH-)>c(H+);
3
(3)根据题目所给信息可知K (H S)<K (CHCOOH),所以S2-的水解程度大于CHCOO-,则浓度相等时
a2 2 a 3 3
NaS的碱性更强;
2
(4)硫酸钙饱和溶液中存在沉淀溶解平衡CaSO Ca2++SO ,加入NaCO 溶液后,CO 与Ca2+结合,转
4 2 3
化为K 更小的CaCO 沉淀,使CaSO 的沉淀溶解平衡向溶解方向移动,最终全部转化为可以和酸反应的
sp 3 4
碳酸钙。
15.(2022·广东·珠海市第二中学模拟预测)(16分)AgNO 为中学常用化学试剂,某学习小组研究其性
3
质。
(1)测量 0.1 mol/LAgNO 溶液pH值为4,用离子方程式解释其原因___________。
3
(2)AgSCN为白色沉淀,设计实验证明K (AgSCN)>K (AgI),完善以下实验步骤:
sp sp
取0.1 mL1 mol/L AgNO 溶液于洁净的试管中,加入___________,振荡,再加入___________,振荡,观
3
察到白色沉淀变成黄色,则证明上述结论。
探究一:证明AgNO 具有氧化性
3
(3)同学乙认为:氧化Fe2+的,可能是Ag+,也可能是 。若向b试管中滴加少量“检测试剂”,无明显
现象,则证明氧化剂为Ag+。写出这种“检测试剂”的配方:___________。探究二:AgNO 溶液与过量铁粉的反应
3
向酸化的0.1 mol/L AgNO 溶液[pH≈2]中加入过量铁粉,搅拌后静置,随着反应进行,在不同时间取上层清
3
液,滴加KSCN溶液,溶液变红,同时有白色沉淀生成,且溶液颜色深浅、沉淀量多少与取样时间有关,
对比实验记录如下:
序号 取样时间/min 现象
① 3 产生大量白色沉淀;溶液呈红色
② 30 产生白色沉淀,较3 min时量少;溶液红色较3 min时加深
③ 120 产生白色沉淀,较30 min时量少;溶液红色较30 min时变浅
(4)用离子方程式解释实验中①出现红色的原因: ,___________,___________。
(5)解释实验②的现象:___________。
(6)用离子方程式解释实验③中红色变浅的原因:___________。
【答案】(每空2分)(1)Ag++H O AgOH+H+
2
(2)过量KSCN溶液(或加KSCN溶液至不再有白色沉淀产生) 几滴KI溶液
(3)配制0.1 mol/L AgNO 溶液中,滴入适量硝酸,调pH为4或向0.1 mol/L NaNO 溶液中,滴加0.1 mol/L
3 3
硝酸,调pH为4
(4)Fe2++Ag+=Fe3++Ag Fe3++3SCN- Fe(SCN)
3
(5)此时主要发生反应为 ,c(Ag+)比3 min时减小,产生的AgSCN的白色沉淀减少;
c(Fe3+)较3 min时增大,生成Fe(SCN) 增多,溶液红色加深
3
(6)Fe+2Fe3+=3Fe2+
【解析】(1)AgNO 是强酸弱碱盐,在溶液中Ag+会发生水解反应,消耗水电离产生的OH-产生AgOH和
3
H+,水解反应的离子方程式为:Ag++H O AgOH+H+,水解反应的发生使水的电离平衡正向移动,最终
2
达到平衡时溶液中c(H+)>c(OH-),因此溶液显酸性,pH=4;
(2)向0.1 mL1 mol/L的AgNO 溶液中加入过量KSCN溶液(或加KSCN溶液至不再有白色沉淀产生),会发
3
生沉淀反应:Ag++SCN-=AgSCN↓,产生AgSCN白色沉淀,AgSCN在溶液中存在沉淀溶解平衡:
AgSCN(s) Ag+(aq)+SCN-(aq),再向溶液中加入几滴KI溶液,I-与AgSCN溶解电离产生的Ag+反应产生
AgI黄色沉淀,从而证明在溶液中存在沉淀转化,说明溶度积常数:K (AgSCN)>K (AgI);
sp sp
(3)同学乙认为:氧化Fe2+的,可能是Ag+,也可能是 。若向b试管中滴加少量“检测试剂”,无明显现象,则证明氧化剂为Ag+。则该溶液应该含有 ,同时溶液pH=4,进行实验对比,故这种“检测试
剂”的配方为:向0.1 mol/L NaNO 溶液中,滴加0.1 mol/L硝酸,调pH为4;
3
(4)①白色沉淀可能为Ag+与SCN-反应生成的AgSCN,Ag++SCN-=AgSCN↓,溶液变为红色的原因可能是由
于:Fe+2Ag+=Fe2++2Ag,Fe2++Ag+=Fe3++Ag,Fe3++3SCN- Fe(SCN) ;
3
(5)②实验②中产生白色沉淀,较3 min时量少;溶液红色较3 min时加深,可能是由于此时主要发生反应
为Fe2++Ag+=Fe3++Ag,导致c(Ag+)比3 min时减小,产生的AgSCN的白色沉淀减少;c(Fe3+)较3 min时增大,
生成Fe(SCN) 增多,c[Fe(SCN) ]增大,溶液红色加深;
3 3
(6)③在120 min时溶液红色较30 min时变浅,可能是由于溶液中生成的Fe3+与加入的过量的Fe发生反应:
Fe+2Fe3+=3Fe2+,导致c(Fe3+)较30 min时减小,生成Fe(SCN) 的量减少,c[Fe(SCN) ]减小,因而溶液红色
3 3
变浅。