文档内容
第 29 讲 分子结构与性质
1.布洛芬对胃、肠道有刺激性,可以对其进行分子修饰减缓。下列说法错误的是
A.甲中仅有1个手性碳原子 B.甲中共平面的碳原子数最少为10
C.乙能与氢氧化钠溶液发生反应 D.乙中氮原子为 杂化
【答案】B
【解析】A.手性碳原子是指与四个各不相同原子或基团相连的碳原子,甲中有 1个手性碳原子,位置
为: ,选项A正确;
B.甲中苯环上6个碳原子及与苯环直接相连的2个碳原子一定共平面,则共平面的碳原子数最少有8个,
选项B错误;
C.乙中含酯基,能与氢氧化钠溶液反应,选项C正确;
D.含N原子的六元环与苯环一样均含大π键,N原子的杂化方式为sp2杂化,选项D正确;
故选B。
2.下列说法正确的是
A.基态 Cr 原子有 6 个未成对电子
B.元素 Ga 的核外电子排布式为 ,位于元素周期表中 p 区
C.NH 中 N—H 间的键角比 CH 中 C—H 间的键角大
3 4
D.XY 分子为 V 形,则 X 原子一定为 sp2 杂化
2
【答案】A
【解析】A.铬为24号元素,基态Cr原子价电子排布为3d54s1,基态 Cr 原子有 6 个未成对电子,A正
确;
B.元素Ga为31号元素,位于元素周期表中p区,其核外电子排布式为[Ar]3d104s24p1,B错误;C.NH 是三角锥形含有1对孤电子对,CH 是正四面体形无孤电子对,因此NH 中N-H间的键角比CH 中
3 4 3 4
C-H间的键角小,C错误;
D.XY 分子中原子个数比为1:2,XY 分子为 V 形,则X原子不一定为sp2杂化,也可能含有2对孤电子
2 2
对为sp3杂化,D错误;
故选A。
3.百服宁口服液为解热镇痛药,其主要化学成分的结构简式如图所示,下列有关该有机化合物的叙述正
确的是
A.分子式为
B.碳原子杂化轨道类型只有 杂化
C.1 mol该有机物最多与2 mol NaOH反应
D.能发生氧化、还原、水解、消去反应
【答案】C
【解析】A.根据该物质结构简式可知,分子式为: ,故A错误;
B.该有机物含甲基碳原子,杂化类型为sp3杂化,故B错误;
C.该有机物中含酚羟基和酰胺基,酰胺基水解后可形成羧基,所以 1 mol该有机物最多与2 mol NaOH反
应,故C正确;
D.该有机物含酚羟基,可被氧化;含酰胺基,可发生水解反应;苯环和氢气发生反应,能发生还原反
应,不能发生消去反应,故D错误;
答案选C。
4.下列分子属于极性分子的是
A.OF B.CS C.SiCl D.O
2 2 4 2
【答案】A
【解析】A.OF 分子中氧原子的价层电子对数为4、孤对电子对数为2,分子的空间构型为V形,则OF 分
2 2
子是结构不对称的极性分子,故A正确;
B.二硫化碳分子中碳原子的价层电子对数为2、孤对电子对数为0,分子的空间构型为直线形,则二硫化碳是结构对称的非极性分子,故B错误;
C. 四氯化硅分子中硅原子的价层电子对数为4、孤对电子对数为0,分子的空间构型为正四面体形,则四
氯化硅是结构对称的非极性分子,故C错误;
D.氧气分子是同种元素形成的双原子分子,正负电荷中心重合,属于非极性分子,故D错误;
故选A。
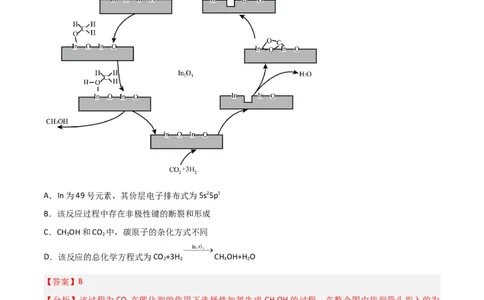
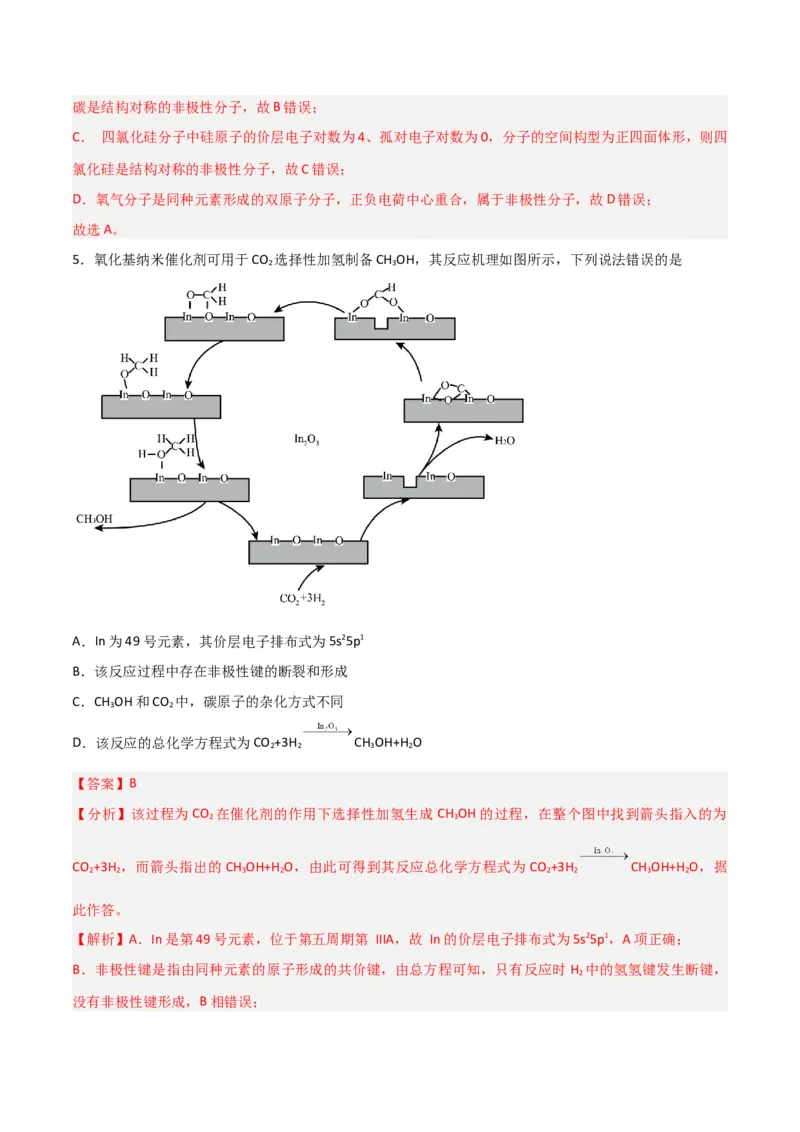
5.氧化基纳米催化剂可用于CO 选择性加氢制备CH OH,其反应机理如图所示,下列说法错误的是
2 3
A.In为49号元素,其价层电子排布式为5s25p1
B.该反应过程中存在非极性键的断裂和形成
C.CH OH和CO 中,碳原子的杂化方式不同
3 2
D.该反应的总化学方程式为CO +3H CH OH+H O
2 2 3 2
【答案】B
【分析】该过程为CO 在催化剂的作用下选择性加氢生成 CH OH的过程,在整个图中找到箭头指入的为
2 3
CO +3H ,而箭头指出的CH OH+H O,由此可得到其反应总化学方程式为 CO +3H CH OH+H O,据
2 2 3 2 2 2 3 2
此作答。
【解析】A.In是第49号元素,位于第五周期第 IIIA,故 In的价层电子排布式为5s25p1,A项正确;
B.非极性键是指由同种元素的原子形成的共价键,由总方程可知,只有反应时H 中的氢氢键发生断键,
2
没有非极性键形成,B相错误;C.CH OH中碳原子所连四个键均为单键,因而是 sp3杂化类型,CO 中碳原子已达到8电子饱和,无孤电
3 2
子对,价层电子对数为2,因此为sp杂化类型,两者碳原子的杂化方式不同,故C正确;
D.由上述可知,在整个图中找到箭头指入的为CO +3H ,而箭头指出的CH OH+H O,由此可得到其反应总
2 2 3 2
化学方程式为CO +3H CH OH+H O,故D正确;
2 2 3 2
故选B。
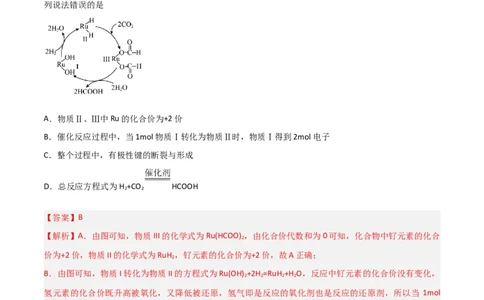
6.为了实现“碳中和”目标,某研究小组通过钌化合物可催化CO 转化为甲酸,其反应机理如图所示。下
2
列说法错误的是
A.物质Ⅱ、Ⅲ中Ru的化合价为+2价
B.催化反应过程中,当1mol物质Ⅰ转化为物质Ⅱ时,物质Ⅰ得到2mol电子
C.整个过程中,有极性键的断裂与形成
D.总反应方程式为H +CO HCOOH
2 2
【答案】B
【解析】A.由图可知,物质III的化学式为Ru(HCOO) ,由化合价代数和为0可知,化合物中钌元素的化合
2
价为+2价,物质II的化学式为RuH ,钌元素的化合价为+2价,故A正确;
2
B.由图可知,物质I转化为物质II的方程式为Ru(OH) +2H =RuH +H O,反应中钌元素的化合价没有变化,
2 2 2 2
氢元素的化合价既升高被氧化,又降低被还原,氢气即是反应的氧化剂也是反应的还原剂,所以当 1mol
物质I转化为物质II时,氢气得到2mol电子,物质I并没有电子得失,B错误;
C.由图可知,整个过程中,二氧化碳参与反应时有极性键的断裂,生成甲酸时有极性键的形成,故 C正
确;
D.由图可知,二氧化碳转化为甲酸的反应为催化剂作用下二氧化碳与氢气反应生成甲酸,反应的化学方
程式为H +CO HCOOH,故D正确;
2 2故答案选B。
7.三硫化四磷( )是黄绿色针状晶体,易燃、有毒,分子结构如图所示。下列有关 的说法中正确的
是
A. 中仅P原子最外层均满足8电子稳定结构
B.键角:
C. 中P原子为 杂化,S原子为 杂化
D. 分子中含有6mol极性共价键
【答案】D
【解析】A.P最外层5个电子,形成了3个共价键,S最外层6个电子,形成了2个键,因此都满足8电
子稳定结构,不仅仅是P原子,故A错误;
B. 均采用sp3杂化,PCl 的中心原子有一对孤电子,而 无孤电子对,因为孤电子对对成键
3
电子对有排斥力,所以导致Cl-P-Cl键角更小,即键角比较: ,故B错误;
C.S原子价层电子对数是4,则S原子是sp3杂化,故C错误;
D.根据结构简式可知1mol 分子中含有6mol极性共价键,3mol非极性共价键,故D正确;
答案选D。
8.化合物A的结构如图所示,其广泛应用于新材料的生产及电化学研究。其中X、Y、Z、E、Q、W为原子
序数依次增大的短周期主族元素,Z与Q、E与W分别位于同一主族。下列有关说法错误的是A. Y X 是含有极性键的非极性分子 B.氢化物的沸点:YW>Q
【答案】B
【分析】X、Y、Z、E、Q、W为原子序数依次增大的短周期主族元素,根据原子的成共价键的数量和所带
电荷数可判断X为H,Y为C,Z为N。根据原子序数大小,且Z与Q、E与W分别位于同一主族,可知Q为
P,E为F,W为Cl。
【解析】A.由分析可知,Y为C,X为H,Y X 为乙炔,为含有极性键的非极性分子,A正确;
2 2
B.由分析可知,Y为C,Z为N,由于C的氢化物有很多,有固态、液态和气态,而 N的氢化物为NH3和
N2H4等,故无法比较它们氢化物的沸点,B错误;
C.原子序数为83的元素为铋,其位于第六周期第ⅤA族,与N位于同一主族,C正确;
D.由分析可知,E为F、W为Cl、Q为P,根据同一周期元素的第一电离从左往右增大趋势但ⅡA与ⅢA、
ⅤA与ⅥA反常,同一主族从上往下依次减小,故三种元素的第一电离能大小顺序为:F>Cl>P即
E>W>Q,D正确;
故答案为:B。
9.一种新型锂离子电池的电解质的阴离子结构如图,其由同一短周期的X、Y、Z、W四种元素组成,且W
的原子序数为Y、Z最外层电子数之和。下列说法一定正确的是
A.氢化物的沸点:W>X B.元素Y与H组成的微粒中含有两个共价键
C. 分子构型为直线形 D.最高价氧化物对应水化物的酸性:X>Z
【答案】D
【分析】W能形成1个共价键,结合X、Y、Z、W四种元素同周期,W的原子序数为Y、Z最外层电子数之和,可知W最外层7电子,为F元素;Y能形成2个共价键,则为O元素;则Z最外层3电子,为B元素;
X能成4个共价键,为C元素;
【解析】A.W氢化物为HF,分子间存在氢键,但其沸点不一定高于碳氢化合物,故A错误;
B.O元素和H元素可形成H O或者H O ,后者分子中含3个共价键,故B错误;
2 2 2
C. 分子为OF 分子,中心原子O原子价层电子对数: ,分子构型为V形,故C错
2
误;
D.最高价氧化物对应水化物的酸性与非金属性有关,非金属性:C>B,所以最高价氧化物对应水化物的
酸性:X>Z,故D正确;
答案选D。
10.某种化学品的结构如下图所示,已知W、X、Y、Z、M均为短周期主族元素,其中W、X、Y在同一周
期,Z、M同处另一周期,M的简单阳离子半径是同周期中最小的,则下列说法中正确的是
A.元素电负性大小的顺序:X>W>Y>Z
B.W的某种单质的分子,是极性分子且分子中含有极性键
C.同一周期中,元素第一电离能处在Z和M之间的有2种
D.该分子中Y原子的杂化方式为sp2
【答案】B
【分析】W、X、Y、Z、M均为短周期主族元素,其中W、X、Y在同一周期,Z、M同处另一周期,M的简
单阳离子半径是同周期中最小的,可知M为Al元素,化合物中Z形成6个共价键,Z为S元素;X形成1个
共价键、Y形成4个共价键、W形成2个共价键,则X为F元素、Y为C元素、W为O元素,以此来解答。
【解析】由上述分析可知,W为O元素、X为F元素、Y为C元素、Z为S元素、M为Al元素,
A.同周期,从左到右,元素的电负性逐渐增大,同主族从上到下,元素的电负性逐渐变小,则电负性
F>O>S>C,故A错误;
B.O 的空间结构为V形,分子中正电荷中心和负电荷中心不重合,O 是极性分子,分子中含有极性键,
3 3
故B正确;
C.同一周期中,随着核电荷数的增加,元素的第一电离呈现增大趋势,Ⅱ A族、ⅤA族反常,则元素第一电离能处在Al和S之间的有Si共1种,故C错误;
D.Y为C原子,价层电子对数是4,杂化方式为sp3,故D错误;
故选:B。
11.我国科学家提出的聚集诱导发光机制已成为研究热点之一,一种具有聚集诱导发光性能的物质,其分
子结构如图所示。下列说法正确的是
A.分子中C原子有sp2、sp3两种杂化方式,N原子均为sp3杂化
B.分子中含有手性碳原子
C.该物质可发生取代反应、加成反应、消去反应
D.该物质既有酸性又有碱性
【答案】D
【解析】A.该分子中左边的N原子有一个孤对电子和两个σ键,为sp2杂化,右边的N原子有一个孤对电
子和三个σ键,为sp3杂化,故A错误;
B.手性碳原子是指连有四个不同原子团的碳原子,该有机物中没有手性碳原子,故B错误;
C.该分子存在苯环、碳氮双键,可以发生加成反应,有卤素原子、羧基,能发生取代反应,不能发生消
去反应,故C错误;
D.该物质中存在羧基,具有酸性,该物质中还含有 ,具有碱性,故D正确;
故选D。
12.尿素可以减少柴油机尾气氮氧化物的排放,发生反应: ,
设 为阿伏伽德罗常数,下列有关说法正确的是
A. 均为非极性分子 B.标况下, 含有电子数
C. 中含有 键数目为 D.反应过程中生成 时转移电子数为
【答案】C
【解析】A.N 、CO 均为直线形分子,分子中正负电荷中心重合,故均为非极性分子,H O为V形结构,
2 2 2分子正负电荷中心不重合,属于极性分子,A错误;
B.已知1分子NO 中含有(7+2×8)=23个电子,故标况下, 即 =1molNO 中含有电子数
2 2
为 ,B错误;
C.已知CO(NH ) 中含有一个C=O双键,其余原子间均为单键,即1分子CO(NH ) 中含有1个 键,故
2 2 2 2
中含有 键数目为 ,C正确;
D.反应中 转移电子数为:16mol电子,则反应过程中生成
即 =1mol时转移电子数为 ,D错误;
故答案为:C。
13.利用 、 和 反应制联氨( ),反应方程式为
,下列关于该反应的说法不正确的是
A. 与 的晶体类型不同
B.此反应过程中既有极性键、非极性键的断裂,也有极性键、非极性键的形成
C. 与 分子间易形成氢键,结构可表示为
D. 分子中 为吸电子基,导致N原子与 的配位能力减弱,等物质的量浓度的 和 的
水溶液, 水溶液碱性较弱
【答案】B
【解析】A.NH Cl为离子晶体,而NH Cl由分子构成,属于分子晶体,A正确;
4 2
B.该反应中有N-Cl等极性键的断裂,也有极性键(N-H)、非极性键(N-N)的形成,但是没有非极性键的断裂,B错误;
C.NH 与H O分子间容易形成分子间氢键,结构可表示为 ,C正确;
3 2
D.N H 分子中-NH 为吸电子基,则N原子的孤电子对被吸引,导致N原子与H+的配位能力减弱,N H 结
2 4 2 2 4
合氢离子的能力弱于NH ,因此等物质的量浓度的N H 和NH 的水溶液,N H 水溶液碱性较弱,D正确;
3 2 4 3 2 4
故答案选B。
14.雄黄(As S , )与雌黄(As S , )在古代均曾入药,二者可发生如图转化:N 表示
4 4 2 3 A
阿伏加德罗常数的值,下列说法正确的是
A.1mol雄黄分子中含有σ键的数目为10N
A
B.反应Ⅰ氧化剂与还原剂物质的量之比为1∶7
C . 0.1mol/L 的 NaH AsO 溶 液 中 离 子 浓 度 存 在 如 下 关 系 :
2 3
D.雌黄分子中As原子的杂化方式为sp3,S原子的杂化方式为sp2
【答案】A
【解析】A.单键均为σ键,由图知,一个雄黄分子中含有10个σ键,所以1mol雄黄中含有的σ键为
10N ,A正确;
A
B.根据图示的反应历程知,反应I的方程为: ,氧化剂与还原剂物质的量之比为
7∶1,B错误;
C . 0.1mol/L 的 NaH AsO 溶 液 中 离 子 浓 度 存 在 关 系 :
2 3
,C错误;
D.由图知。雄黄分子中S上由2个σ键,由于S的最外层有6个电子,故应该还有两个孤电子对,因此,
S原子的杂化方式为sp3,D错误;故选A。
15.X 射线研究表明 CuCl 是共价化合物,为平面链状结构,以(CuCl )n形式存在,如图所示。CuCl 易溶于
2 2 2
水、乙醇、丙酮和氨水等,其水溶液常呈绿色,原因是[Cu(H O) ]2+(蓝色)+4Cl- [CuCl ]2−(绿色)+4H O。下
2 4 4 2
列说法不正确的是
A.由图结构可知 CuCl 为非极性分子
2
B.CuSO 溶液中加入 NaCl 固体,可使溶液颜色变绿
4
C.CuCl 中加入过量氨水可生成含[Cu(NH ) ]2+深蓝色溶液,说明 NH 配位能力大于 Cl-
2 3 4 3
D.1mol[Cu(NH ) ]2+中存在 4N 个σ键
3 4 A
【答案】D
【解析】A.CuCl 是共价化合物,为平面链状结构,根据图中结构,可知 CuCl 为非极性分子,故A正
2 2
确;
B.CuSO 溶液中加入 NaCl 固体,题干中平衡正向移动,可使溶液颜色变绿色,故B正确;
4
C.CuCl 中加入过量氨水可生成含[Cu(NH ) ]2+深蓝色溶液,说明[CuCl ]2−变为[Cu(NH ) ]2+,则NH 配位能力大
2 3 4 4 3 4 3
于 Cl-,故C正确;
D.1个NH 有3个σ键,配位键为σ键,则1mol[Cu(NH ) ]2+中存在 16N 个σ键,故D错误;
3 3 4 A
综上所述,答案为D。
16.硫酸铵俗称肥田粉,是一种重要的铵态氮肥,下列说法不正确的是
A.NH 和 SO 的中心原子杂化方式相同 B.第一电离能:N>S
C.饱和硫酸铵溶液会使蛋白质发生变性 D.硫酸铵不能与草木灰混合施用
【答案】C
【解析】A.铵根离子和硫酸根离子的中心原子都是sp3杂化,A正确;
B.第一电离能N>P,而P又大于S,故N>S,B正确;
C.饱和硫酸铵溶液使蛋白质发生盐析而不是变性,C错误;
D. 草木灰的成分是碳酸钾,呈碱性,不能与铵态氮肥使用,否则会降低肥效,D正确;
故选C。
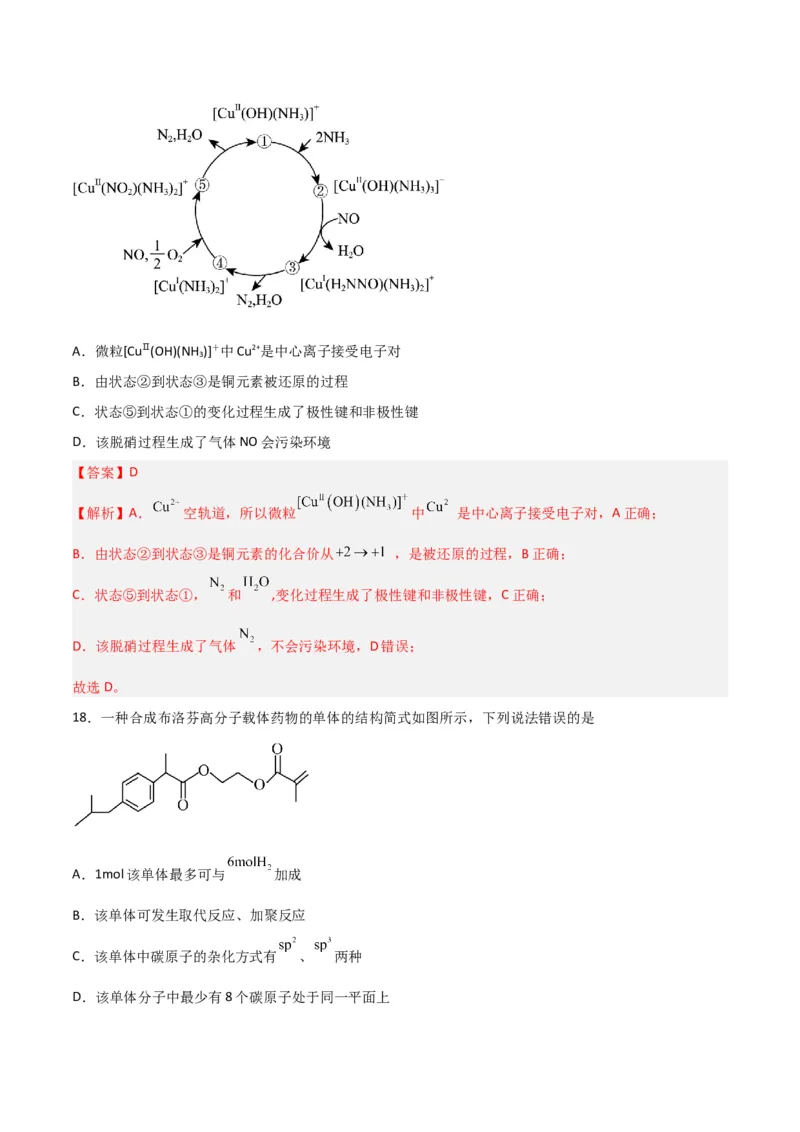
17.某种含二价铜微粒[CuⅡ(OH)(NH )]+的催化剂可用于汽车尾气脱硝,催化机理如图,下列说法错误的是
3A.微粒[CuⅡ(OH)(NH )]+中Cu2+是中心离子接受电子对
3
B.由状态②到状态③是铜元素被还原的过程
C.状态⑤到状态①的变化过程生成了极性键和非极性键
D.该脱硝过程生成了气体NO会污染环境
【答案】D
【解析】A. 空轨道,所以微粒 中 是中心离子接受电子对,A正确;
B.由状态②到状态③是铜元素的化合价从 ,是被还原的过程,B正确;
C.状态⑤到状态①, 和 ,变化过程生成了极性键和非极性键,C正确;
D.该脱硝过程生成了气体 ,不会污染环境,D错误;
故选D。
18.一种合成布洛芬高分子载体药物的单体的结构简式如图所示,下列说法错误的是
A.1mol该单体最多可与 加成
B.该单体可发生取代反应、加聚反应
C.该单体中碳原子的杂化方式有 、 两种
D.该单体分子中最少有8个碳原子处于同一平面上【答案】A
【解析】A.1mol苯环可与 加成,1mol碳碳双键可与 加成,酯基与 不能发生加成反应,
故1mol该单体最多可与 加成,A项错误;
B.分子中含有的酯基可以发生水解反应,即取代反应,含有的碳碳双键可以发生加聚反应,B项正确;
C.连接四个单键的碳原子为 杂化,碳氧双键、碳碳双键、苯环上的碳原子为 杂化,C项正确;
D.苯环上的6个碳原子和取代苯环上氢原子的2个碳原子一定处于同一平面,D项正确;
答案选A。
19. 催化除去 的机理如图所示,下列说法不正确的是
A.反应①~④均是氧化还原反应 B.反应②中碳氧双键未断裂
C. 中碳原子采取 杂化 D.上述机理总反应为
【答案】A
【解析】A.反应④为 ,该反应没有元素的化合价发生变化,不是氧化还原反
应,故A错误;
B.由图可知,反应②为 ,该过程中碳氧双键没有断裂,故B正确;
C. 中碳原子价层电子对数为3,采取 杂化,故C正确;
D.由图可知,该反应的机理是在 作催化剂的条件下,O 和HCHO反应生成CO 和H O,则总反应为
2 2 2HCHO+O CO +H O,故D正确;
2 2 2
答案选A。
20.W、X、Y、Z是原子序数依次增大的短周期主族元素,且原子序数总和为25,由这四种元素形成的某
化合物结构如图所示。下列叙述错误的是
A.简单离子半径:
B.该化合物中X、Y的杂化方式相同
C.X的最高价氧化物对应的水化物为弱酸
D.该化合物的阴离子中各原子最外层均达到8电子稳定结构
【答案】D
【分析】根据W、X、Y、Z是原子序数依次增大的短周期主族元素,且原子序数总和为25,结合该四种元
素化合物结构,其中Z元素简单阳离子为Z+,推断Z为Na元素,W为单键,则为氢元素,Y形成2个单
键,推断为O元素,则Y为B元素,故分析可得W、X、Y、Z分别为H、B、O、Na元素。
【解析】A.Y的简单离子为O2-,Z的简单离子为Na+,O2- 、Na+都有2个电子层,当电子层数相同,原子
序数越小半径越大,故离子半径O2-> Na+,故简单离子半径: ,故A项正确;
B.Y为氧原子,价电子数为6,与氢原子、硼原子形成两个单键,故杂化轨道数 ,故为
sp3杂化;X为硼原子,价电子数为3,与周围4个氧原子形成4个单键,且整个原子团带两个单位负电
荷,故两个硼原子均得到 1个电子,故杂化轨道数 ,故为sp3杂化,两者杂化方式相
同,故B项正确;
C.B的最高价氧化物对应的水化物为H BO ,H BO 为一元弱酸,故C项正确;
3 3 3 3
D.该化合物的阴离子中氢原子最外层是2个电子,未达到8电子稳定结构,故D项错误。
故答案选D。