文档内容
第 29 讲 分子结构与性质
1.布洛芬对胃、肠道有刺激性,可以对其进行分子修饰减缓。下列说法错误的是
A.甲中仅有1个手性碳原子 B.甲中共平面的碳原子数最少为10
C.乙能与氢氧化钠溶液发生反应 D.乙中氮原子为 杂化
2.下列说法正确的是
A.基态 Cr 原子有 6 个未成对电子
B.元素 Ga 的核外电子排布式为 ,位于元素周期表中 p 区
C.NH 中 N—H 间的键角比 CH 中 C—H 间的键角大
3 4
D.XY 分子为 V 形,则 X 原子一定为 sp2 杂化
2
3.百服宁口服液为解热镇痛药,其主要化学成分的结构简式如图所示,下列有关该有机化合物的叙述正
确的是
A.分子式为
B.碳原子杂化轨道类型只有 杂化
C.1 mol该有机物最多与2 mol NaOH反应
D.能发生氧化、还原、水解、消去反应
4.下列分子属于极性分子的是
A.OF B.CS C.SiCl D.O
2 2 4 2
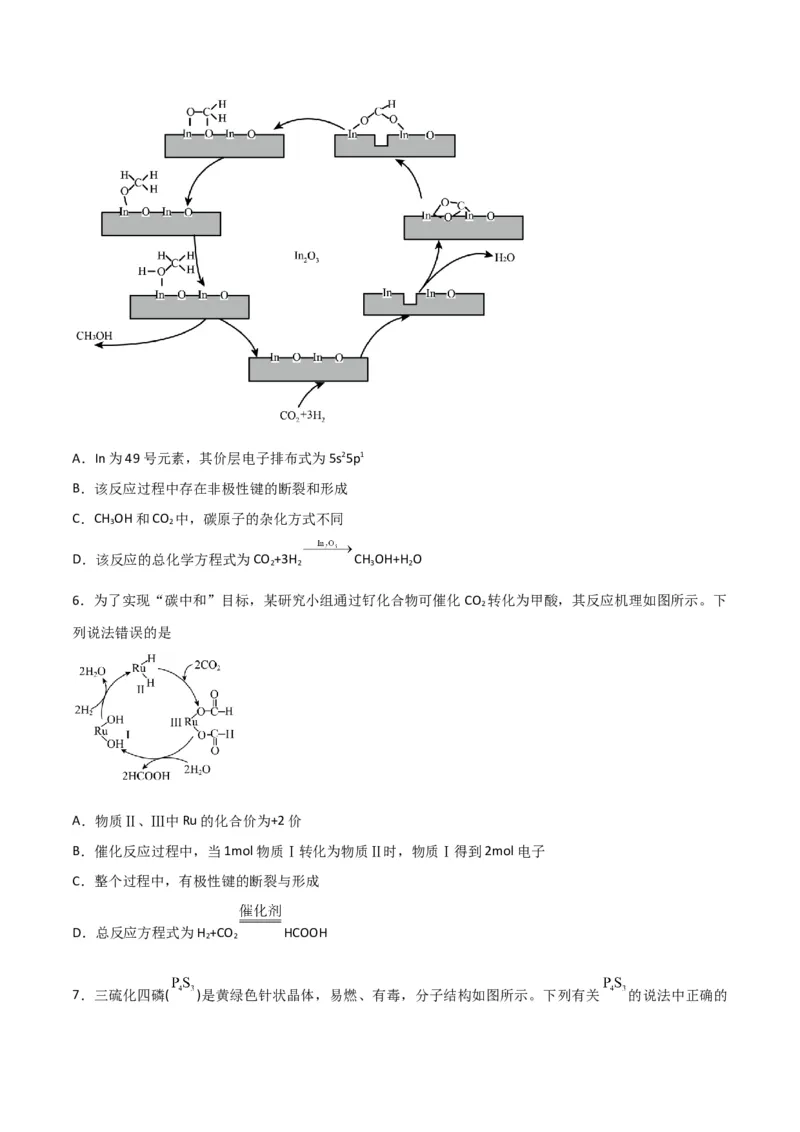
5.氧化基纳米催化剂可用于CO 选择性加氢制备CH OH,其反应机理如图所示,下列说法错误的是
2 3A.In为49号元素,其价层电子排布式为5s25p1
B.该反应过程中存在非极性键的断裂和形成
C.CH OH和CO 中,碳原子的杂化方式不同
3 2
D.该反应的总化学方程式为CO +3H CH OH+H O
2 2 3 2
6.为了实现“碳中和”目标,某研究小组通过钌化合物可催化CO 转化为甲酸,其反应机理如图所示。下
2
列说法错误的是
A.物质Ⅱ、Ⅲ中Ru的化合价为+2价
B.催化反应过程中,当1mol物质Ⅰ转化为物质Ⅱ时,物质Ⅰ得到2mol电子
C.整个过程中,有极性键的断裂与形成
D.总反应方程式为H +CO HCOOH
2 2
7.三硫化四磷( )是黄绿色针状晶体,易燃、有毒,分子结构如图所示。下列有关 的说法中正确的是
A. 中仅P原子最外层均满足8电子稳定结构
B.键角:
C. 中P原子为 杂化,S原子为 杂化
D. 分子中含有6mol极性共价键
8.化合物A的结构如图所示,其广泛应用于新材料的生产及电化学研究。其中X、Y、Z、E、Q、W为原子
序数依次增大的短周期主族元素,Z与Q、E与W分别位于同一主族。下列有关说法错误的是
A. Y X 是含有极性键的非极性分子 B.氢化物的沸点:YW>Q
9.一种新型锂离子电池的电解质的阴离子结构如图,其由同一短周期的X、Y、Z、W四种元素组成,且W
的原子序数为Y、Z最外层电子数之和。下列说法一定正确的是
A.氢化物的沸点:W>X B.元素Y与H组成的微粒中含有两个共价键
C. 分子构型为直线形 D.最高价氧化物对应水化物的酸性:X>Z
10.某种化学品的结构如下图所示,已知W、X、Y、Z、M均为短周期主族元素,其中W、X、Y在同一周期,Z、M同处另一周期,M的简单阳离子半径是同周期中最小的,则下列说法中正确的是
A.元素电负性大小的顺序:X>W>Y>Z
B.W的某种单质的分子,是极性分子且分子中含有极性键
C.同一周期中,元素第一电离能处在Z和M之间的有2种
D.该分子中Y原子的杂化方式为sp2
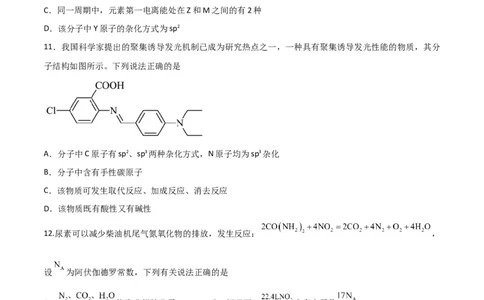
11.我国科学家提出的聚集诱导发光机制已成为研究热点之一,一种具有聚集诱导发光性能的物质,其分
子结构如图所示。下列说法正确的是
A.分子中C原子有sp2、sp3两种杂化方式,N原子均为sp3杂化
B.分子中含有手性碳原子
C.该物质可发生取代反应、加成反应、消去反应
D.该物质既有酸性又有碱性
12.尿素可以减少柴油机尾气氮氧化物的排放,发生反应: ,
设 为阿伏伽德罗常数,下列有关说法正确的是
A. 均为非极性分子 B.标况下, 含有电子数
C. 中含有 键数目为 D.反应过程中生成 时转移电子数为
13.利用 、 和 反应制联氨( ),反应方程式为
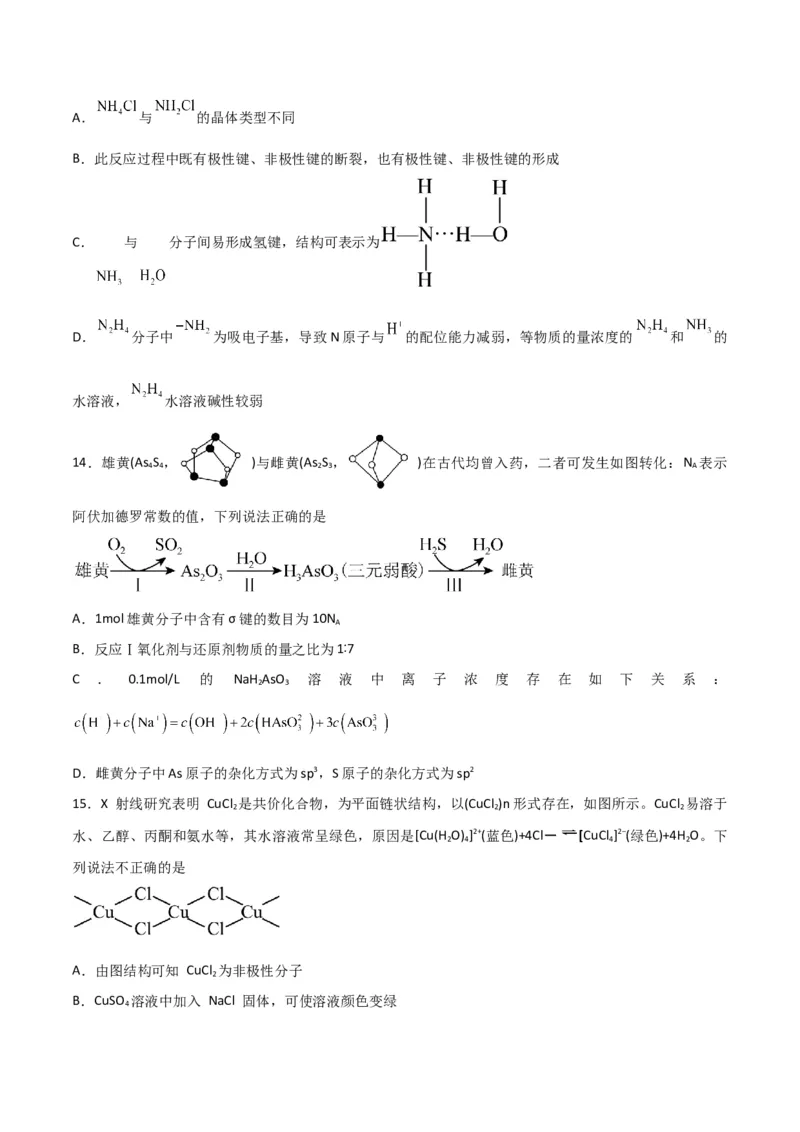
,下列关于该反应的说法不正确的是A. 与 的晶体类型不同
B.此反应过程中既有极性键、非极性键的断裂,也有极性键、非极性键的形成
C. 与 分子间易形成氢键,结构可表示为
D. 分子中 为吸电子基,导致N原子与 的配位能力减弱,等物质的量浓度的 和 的
水溶液, 水溶液碱性较弱
14.雄黄(As S , )与雌黄(As S , )在古代均曾入药,二者可发生如图转化:N 表示
4 4 2 3 A
阿伏加德罗常数的值,下列说法正确的是
A.1mol雄黄分子中含有σ键的数目为10N
A
B.反应Ⅰ氧化剂与还原剂物质的量之比为1∶7
C . 0.1mol/L 的 NaH AsO 溶 液 中 离 子 浓 度 存 在 如 下 关 系 :
2 3
D.雌黄分子中As原子的杂化方式为sp3,S原子的杂化方式为sp2
15.X 射线研究表明 CuCl 是共价化合物,为平面链状结构,以(CuCl )n形式存在,如图所示。CuCl 易溶于
2 2 2
水、乙醇、丙酮和氨水等,其水溶液常呈绿色,原因是[Cu(H O) ]2+(蓝色)+4Cl- [CuCl ]2−(绿色)+4H O。下
2 4 4 2
列说法不正确的是
A.由图结构可知 CuCl 为非极性分子
2
B.CuSO 溶液中加入 NaCl 固体,可使溶液颜色变绿
4C.CuCl 中加入过量氨水可生成含[Cu(NH ) ]2+深蓝色溶液,说明 NH 配位能力大于 Cl-
2 3 4 3
D.1mol[Cu(NH ) ]2+中存在 4N 个σ键
3 4 A
16.硫酸铵俗称肥田粉,是一种重要的铵态氮肥,下列说法不正确的是
A.NH 和 SO 的中心原子杂化方式相同 B.第一电离能:N>S
C.饱和硫酸铵溶液会使蛋白质发生变性 D.硫酸铵不能与草木灰混合施用
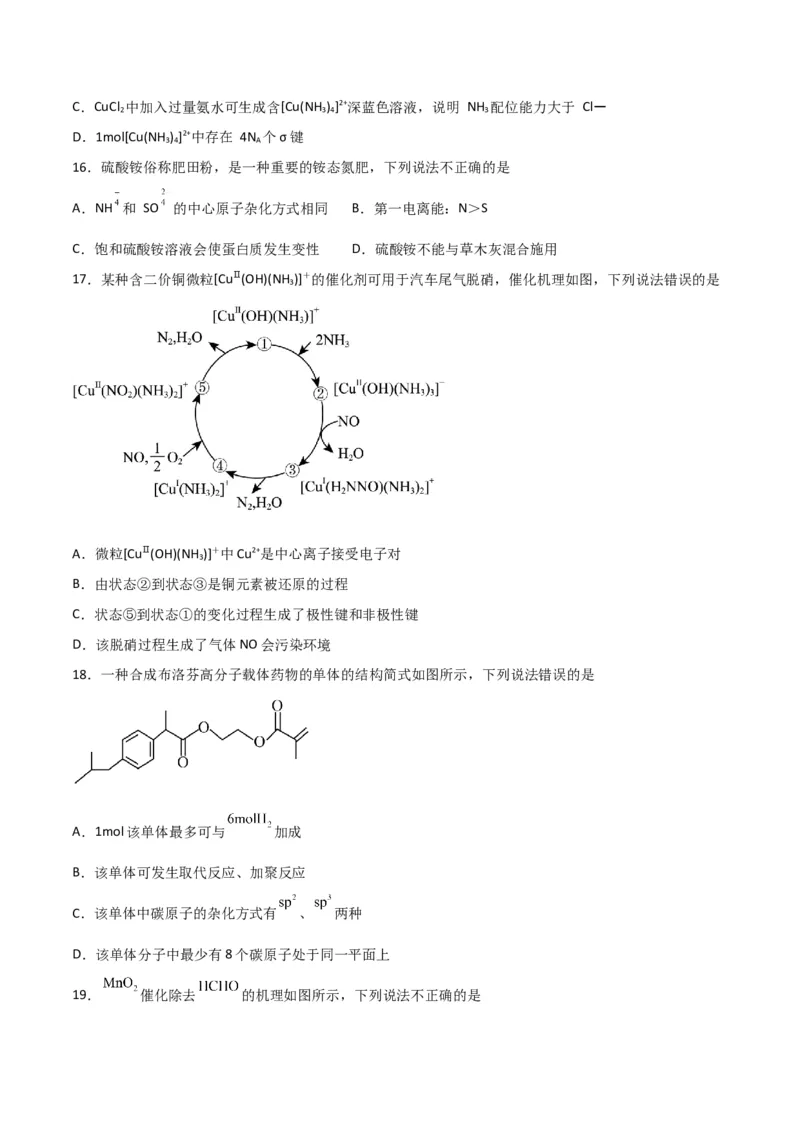
17.某种含二价铜微粒[CuⅡ(OH)(NH )]+的催化剂可用于汽车尾气脱硝,催化机理如图,下列说法错误的是
3
A.微粒[CuⅡ(OH)(NH )]+中Cu2+是中心离子接受电子对
3
B.由状态②到状态③是铜元素被还原的过程
C.状态⑤到状态①的变化过程生成了极性键和非极性键
D.该脱硝过程生成了气体NO会污染环境
18.一种合成布洛芬高分子载体药物的单体的结构简式如图所示,下列说法错误的是
A.1mol该单体最多可与 加成
B.该单体可发生取代反应、加聚反应
C.该单体中碳原子的杂化方式有 、 两种
D.该单体分子中最少有8个碳原子处于同一平面上
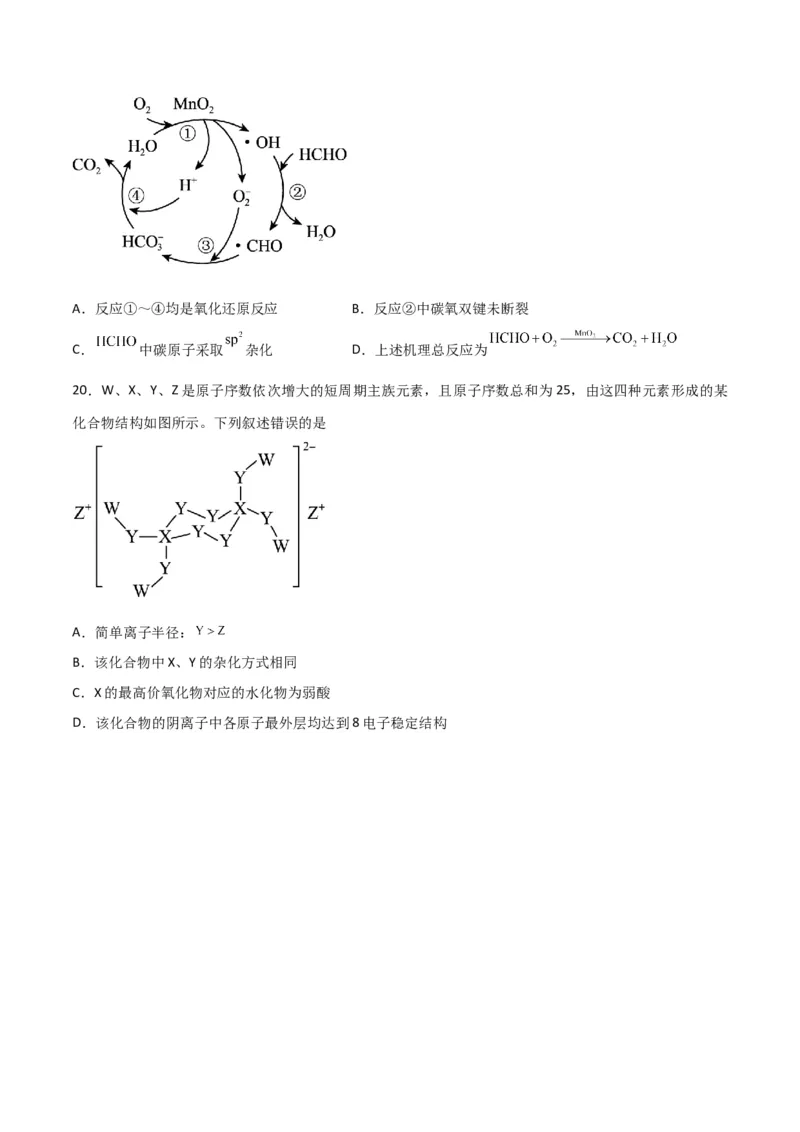
19. 催化除去 的机理如图所示,下列说法不正确的是A.反应①~④均是氧化还原反应 B.反应②中碳氧双键未断裂
C. 中碳原子采取 杂化 D.上述机理总反应为
20.W、X、Y、Z是原子序数依次增大的短周期主族元素,且原子序数总和为25,由这四种元素形成的某
化合物结构如图所示。下列叙述错误的是
A.简单离子半径:
B.该化合物中X、Y的杂化方式相同
C.X的最高价氧化物对应的水化物为弱酸
D.该化合物的阴离子中各原子最外层均达到8电子稳定结构