文档内容
第 30 讲 盐类水解
(模拟精练+真题演练)
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12×5分)
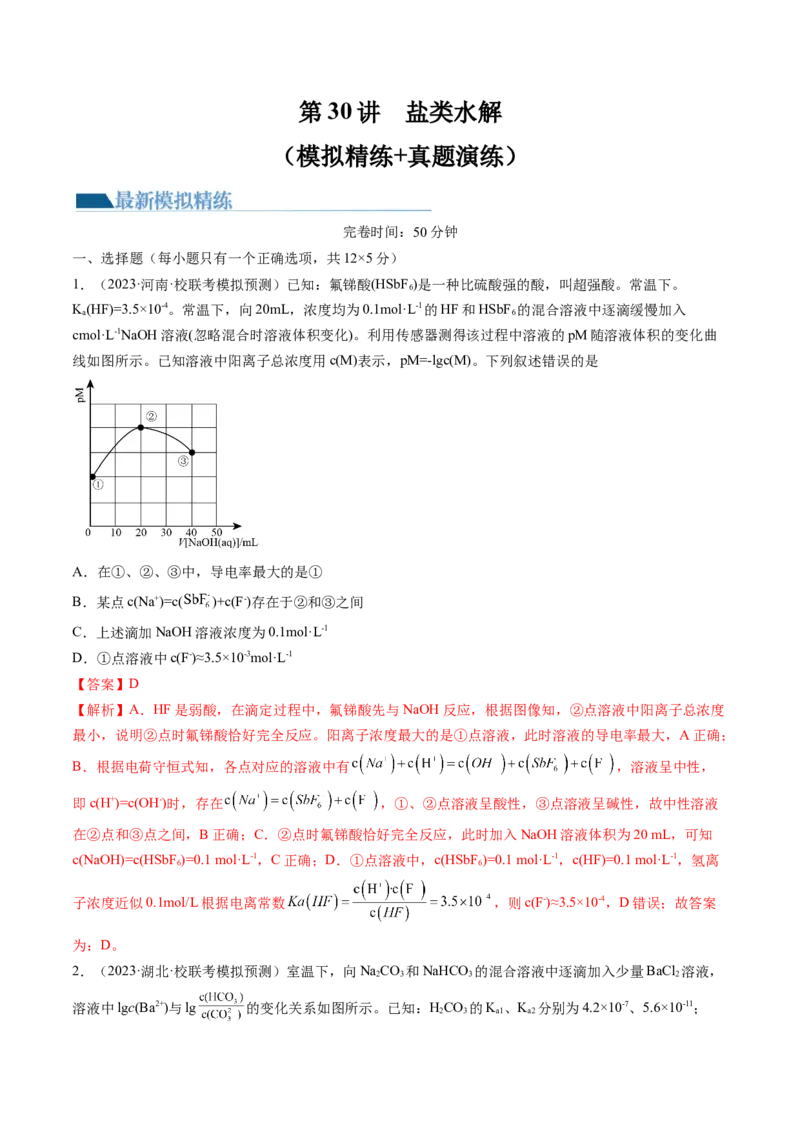
1.(2023·河南·校联考模拟预测)已知:氟锑酸(HSbF )是一种比硫酸强的酸,叫超强酸。常温下。
6
K(HF)=3.5×10-4。常温下,向20mL,浓度均为0.1mol·L-1的HF和HSbF 的混合溶液中逐滴缓慢加入
a 6
cmol·L-1NaOH溶液(忽略混合时溶液体积变化)。利用传感器测得该过程中溶液的pM随溶液体积的变化曲
线如图所示。已知溶液中阳离子总浓度用c(M)表示,pM=-lgc(M)。下列叙述错误的是
A.在①、②、③中,导电率最大的是①
B.某点c(Na+)=c( )+c(F-)存在于②和③之间
C.上述滴加NaOH溶液浓度为0.1mol·L-1
D.①点溶液中c(F-)≈3.5×10-3mol·L-1
【答案】D
【解析】A.HF是弱酸,在滴定过程中,氟锑酸先与NaOH反应,根据图像知,②点溶液中阳离子总浓度
最小,说明②点时氟锑酸恰好完全反应。阳离子浓度最大的是①点溶液,此时溶液的导电率最大,A正确;
B.根据电荷守恒式知,各点对应的溶液中有 ,溶液呈中性,
即c(H+)=c(OH-)时,存在 ,①、②点溶液呈酸性,③点溶液呈碱性,故中性溶液
在②点和③点之间,B正确;C.②点时氟锑酸恰好完全反应,此时加入NaOH溶液体积为20 mL,可知
c(NaOH)=c(HSbF )=0.1 mol·L-1,C正确;D.①点溶液中,c(HSbF )=0.1 mol·L-1,c(HF)=0.1 mol·L-1,氢离
6 6
子浓度近似0.1mol/L根据电离常数 ,则c(F-)≈3.5×10-4,D错误;故答案
为:D。
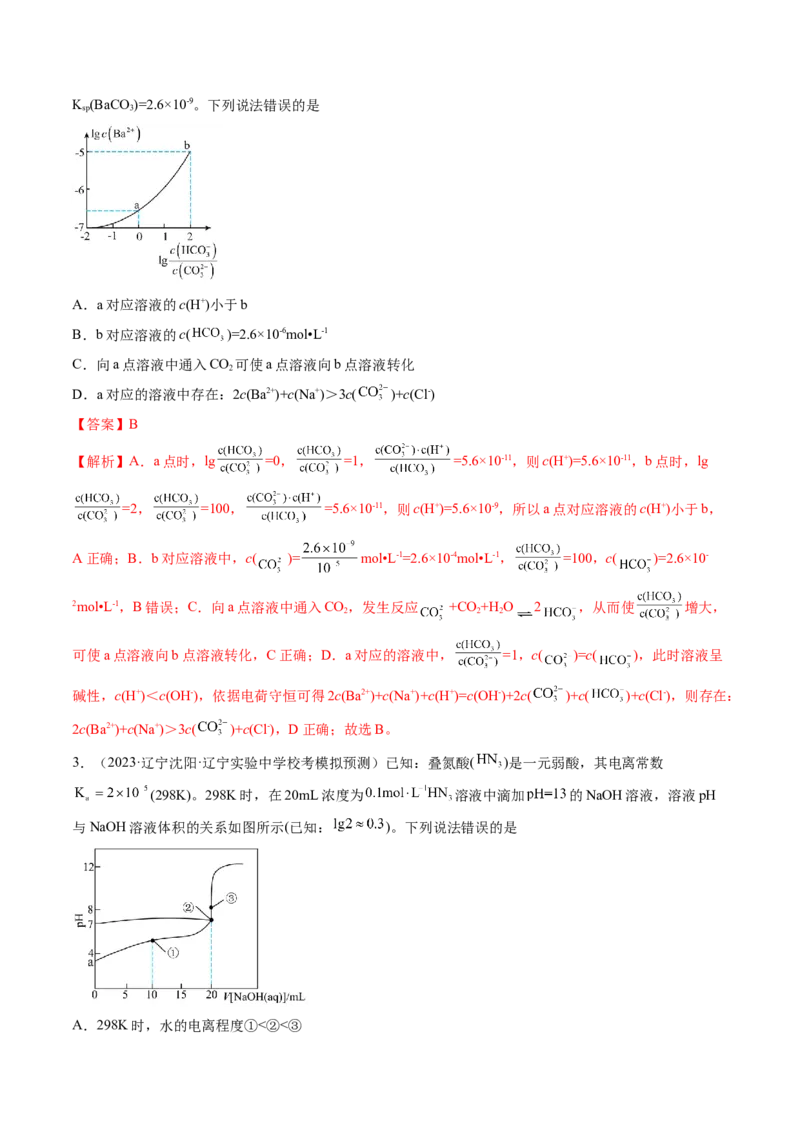
2.(2023·湖北·校联考模拟预测)室温下,向NaCO 和NaHCO 的混合溶液中逐滴加入少量BaCl 溶液,
2 3 3 2
溶液中lgc(Ba2+)与lg 的变化关系如图所示。已知:HCO 的K 、K 分别为4.2×10-7、5.6×10-11;
2 3 a1 a2K (BaCO)=2.6×10-9。下列说法错误的是
sp 3
A.a对应溶液的c(H+)小于b
B.b对应溶液的c( )=2.6×10-6mol•L-1
C.向a点溶液中通入CO 可使a点溶液向b点溶液转化
2
D.a对应的溶液中存在:2c(Ba2+)+c(Na+)>3c( )+c(Cl-)
【答案】B
【解析】A.a点时,lg =0, =1, =5.6×10-11,则c(H+)=5.6×10-11,b点时,lg
=2, =100, =5.6×10-11,则c(H+)=5.6×10-9,所以a点对应溶液的c(H+)小于b,
A正确;B.b对应溶液中,c( )= mol•L-1=2.6×10-4mol•L-1, =100,c( )=2.6×10-
2mol•L-1,B错误;C.向a点溶液中通入CO,发生反应 +CO +H O 2 ,从而使 增大,
2 2 2
可使a点溶液向b点溶液转化,C正确;D.a对应的溶液中, =1,c( )=c( ),此时溶液呈
碱性,c(H+)<c(OH-),依据电荷守恒可得2c(Ba2+)+c(Na+)+c(H+)=c(OH-)+2c( )+c( )+c(Cl-),则存在:
2c(Ba2+)+c(Na+)>3c( )+c(Cl-),D正确;故选B。
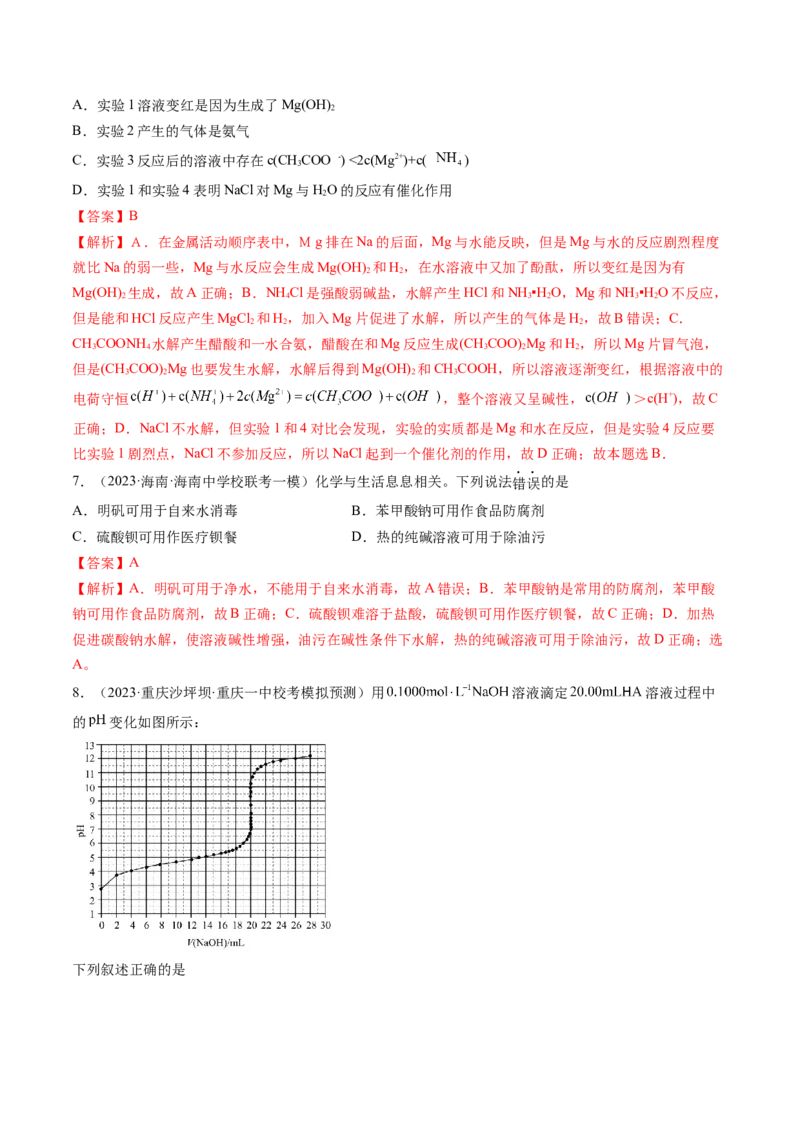
3.(2023·辽宁沈阳·辽宁实验中学校考模拟预测)已知:叠氮酸( )是一元弱酸,其电离常数
(298K)。298K时,在20mL浓度为 溶液中滴加 的NaOH溶液,溶液pH
与NaOH溶液体积的关系如图所示(已知: )。下列说法错误的是
A.298K时,水的电离程度①<②<③B.a点pH约为2.7
C.①点溶液中:
D.②点溶液中:
【答案】B
【解析】A.298K时,在20mL浓度为0.1molL-1HN 溶液中滴加pH=13的NaOH溶液,①加入
3
10mLNaOH溶液,为等浓度的HN 和NaN ,酸抑制水的电离,②为加入15mlNaOH溶液,为HN 和
3 3 ⋅ 3
NaN ,NaN 为主,溶液pH=7,③为加入20mLNaOH溶液,恰好完全中和,为NaN 溶液,NaN 水解促进
3 3 3 3
水的电离,298K时,水的电离程度①<②<③,故A正确;B.叠氮酸(HN )是一元弱酸,
3
c(HN )=0.1mol/L,c(H+)≈c(HN )其电离常数K= =2×10-5,c(H+)≈ mol/L≈ ×10-
3 3 a
3mol/L,pH=-lgc(H+)=-lg ×10-3=3- lg2≈2.85,故B错误;C.①点溶液中存在电荷守恒:c(H+)
+c(Na+)=c(OH-)+c( ),物料守恒为:2c(Na+)=c( )+c(HN),整理得到:c( )+2c(OH-)=c(HN)+2c(H+),
3 3
故C正确;D.②点溶液pH=7,溶液显中性,液中存在电荷守恒:c(H+)+c(Na+)=c(OH-)+c( ),得到
c(Na+)=c( )>c(H+)=c(OH-),故D正确;故选:B。
4.(2023·吉林通化·梅河口市第五中学校考模拟预测)常温下,0.1mol·L-1HR 溶液中HR、HR-、R2-三者
2 2
所占物质的量分数(分布系数δ )随pH变化的关系如图1所示,向0.1mol·L-1NaR溶液中滴加稀盐酸,所得
2
混合溶液的pH与P[P=lg 或lgc ]变化关系如图2所示。下列说法正确的是
A.图1中M点即为图2中N点,反应HR+R2- 2HR-的平衡常数K=100
2
B.水的电离程度c=d>b> a
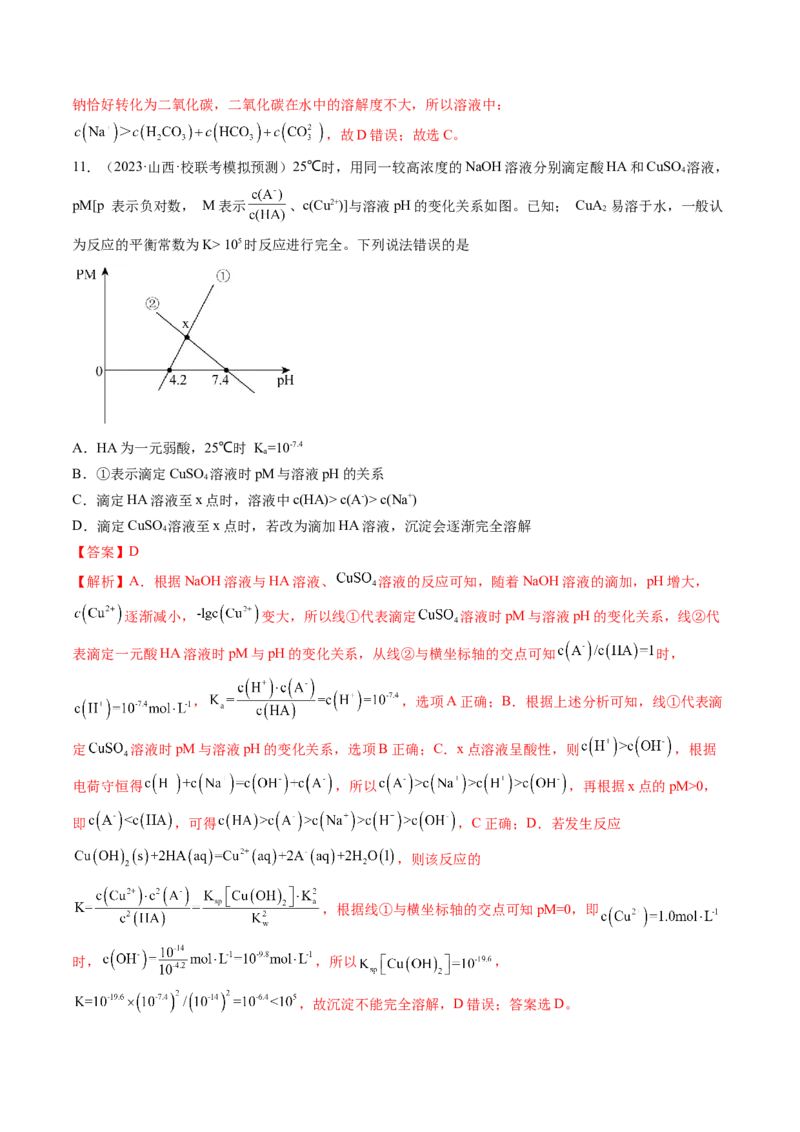
C.d点时,3c (HR-) -c (OH- ) 105时反应进行完全。下列说法错误的是
A.HA为一元弱酸,25℃时 K=10-7.4
a
B.①表示滴定CuSO 溶液时pM与溶液pH的关系
4
C.滴定HA溶液至x点时,溶液中c(HA)> c(A-)> c(Na+)
D.滴定CuSO 溶液至x点时,若改为滴加HA溶液,沉淀会逐渐完全溶解
4
【答案】D
【解析】A.根据NaOH溶液与HA溶液、 溶液的反应可知,随着NaOH溶液的滴加,pH增大,
逐渐减小, 变大,所以线①代表滴定 溶液时pM与溶液pH的变化关系,线②代
表滴定一元酸HA溶液时pM与pH的变化关系,从线②与横坐标轴的交点可知 时,
, ,选项A正确;B.根据上述分析可知,线①代表滴
定 溶液时pM与溶液pH的变化关系,选项B正确;C.x点溶液呈酸性,则 ,根据
电荷守恒得 ,所以 ,再根据x点的pM>0,
即 ,可得 ,C正确;D.若发生反应
,则该反应的
,根据线①与横坐标轴的交点可知pM=0,即
时, ,所以 ,
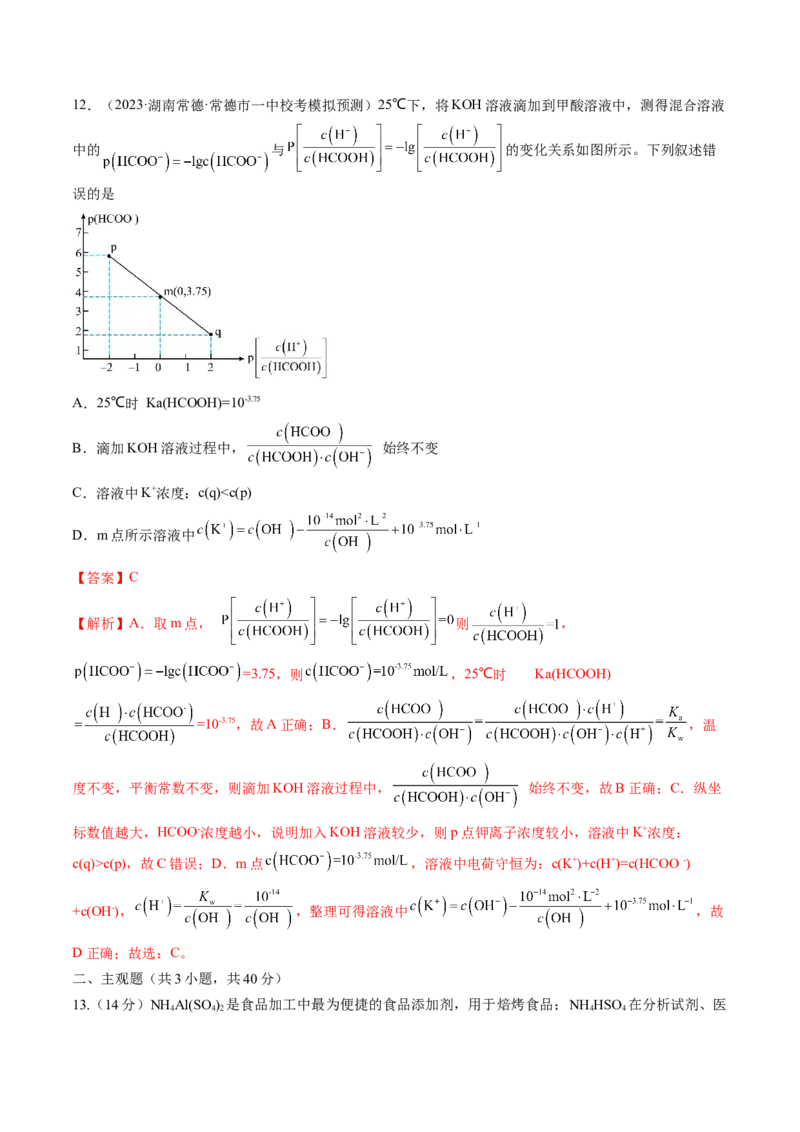
,故沉淀不能完全溶解,D错误;答案选D。12.(2023·湖南常德·常德市一中校考模拟预测)25℃下,将KOH溶液滴加到甲酸溶液中,测得混合溶液
中的 与 的变化关系如图所示。下列叙述错
误的是
A.25℃时 Ka(HCOOH)=10-3.75
B.滴加KOH溶液过程中, 始终不变
C.溶液中K+浓度:c(q)c(p),故C错误;D.m点 ,溶液中电荷守恒为:c(K+)+c(H+)=c(HCOO -)
+c(OH-), ,整理可得溶液中 ,故
D正确;故选:C。
二、主观题(共3小题,共40分)
13.(14分)NH Al(SO ) 是食品加工中最为便捷的食品添加剂,用于焙烤食品;NH HSO 在分析试剂、医
4 4 2 4 4药、电子工业中用途广泛。
请回答下列问题:
(1)NH Al(SO ) 可作净水剂,其原理是__________________(用必要的化学用语和相关文字说明)。
4 4 2
(2)相同条件下,0.1 mol·L-1 NH Al(SO ) 溶液中c(NH)________(填“等于”“大于”或“小于”)0.1 mol·L
4 4 2
-1 NH HSO 溶液中c(NH)。
4 4
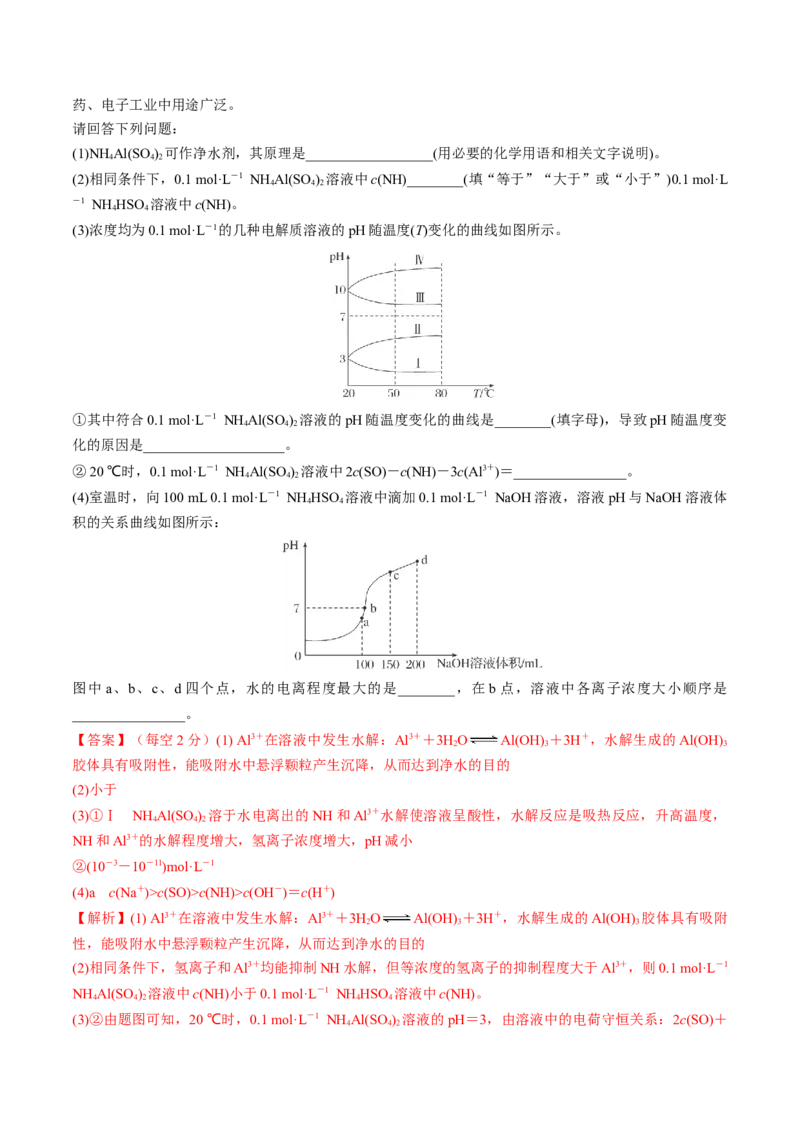
(3)浓度均为0.1 mol·L-1的几种电解质溶液的pH随温度(T)变化的曲线如图所示。
①其中符合0.1 mol·L-1 NH Al(SO ) 溶液的pH随温度变化的曲线是________(填字母),导致pH随温度变
4 4 2
化的原因是____________________。
②20 ℃时,0.1 mol·L-1 NH Al(SO ) 溶液中2c(SO)-c(NH)-3c(Al3+)=________________。
4 4 2
(4)室温时,向100 mL 0.1 mol·L-1 NH HSO 溶液中滴加0.1 mol·L-1 NaOH溶液,溶液pH与NaOH溶液体
4 4
积的关系曲线如图所示:
图中a、b、c、d四个点,水的电离程度最大的是________,在b点,溶液中各离子浓度大小顺序是
________________。
【答案】(每空2分)(1) Al3+在溶液中发生水解:Al3++3HO Al(OH) +3H+,水解生成的Al(OH)
2 3 3
胶体具有吸附性,能吸附水中悬浮颗粒产生沉降,从而达到净水的目的
(2)小于
(3)①Ⅰ NH Al(SO ) 溶于水电离出的NH和Al3+水解使溶液呈酸性,水解反应是吸热反应,升高温度,
4 4 2
NH和Al3+的水解程度增大,氢离子浓度增大,pH减小
②(10-3-10-11)mol·L-1
(4)a c(Na+)>c(SO)>c(NH)>c(OH-)=c(H+)
【解析】(1) Al3+在溶液中发生水解:Al3++3HO Al(OH) +3H+,水解生成的Al(OH) 胶体具有吸附
2 3 3
性,能吸附水中悬浮颗粒产生沉降,从而达到净水的目的
(2)相同条件下,氢离子和Al3+均能抑制NH水解,但等浓度的氢离子的抑制程度大于Al3+,则0.1 mol·L-1
NH Al(SO ) 溶液中c(NH)小于0.1 mol·L-1 NH HSO 溶液中c(NH)。
4 4 2 4 4
(3)②由题图可知,20 ℃时,0.1 mol·L-1 NH Al(SO ) 溶液的pH=3,由溶液中的电荷守恒关系:2c(SO)+
4 4 2c(OH-)=c(NH)+c(H+)+3c(Al3+)可得20 ℃时,2c(SO)-c(NH)-3c(Al3+)=c(H+)-c(OH-)=(10-3-10-
11)mol·L-1。
(4)向 100 mL 0.1 mol·L-1 NH HSO 溶液中滴加 0.1 mol·L-1 NaOH 溶液,发生的反应为 H++OH-
4 4
===H O、OH-+NHNH ·H O,a点时氢氧化钠溶液恰好中和溶液中氢离子,得到等浓度的硫酸铵和硫
2 3 2
酸钠的混合溶液,溶液中的 NH 水解促进水的电离;a 点之后,NH 与 OH-反应生成抑制水电离的
NH ·H O,NH浓度越小,对水的电离程度促进越小,所以溶液中水的电离程度最大的是 a点。由题图可知
3 2
b点时,溶液pH=7,该点为硫酸钠、硫酸铵和NH ·H O的混合溶液,则溶液中各离子浓度大小顺序是
3 2
c(Na+)>c(SO)>c(NH)>c(OH-)=c(H+)。
14.(12分)(2023·江西宜春·江西省宜丰中学校考模拟预测)已知25℃时电离常数:
酸 HCO CHCOOH HCN
2 3 3
K K =4.5×10-7K =5.6×10-11 1.75×10-5 6.2×10-10
a a1 a2
(1)H CO、CHCOOH、HCN三种酸中酸性最弱的是 。常温下,pH均为10的NaCO、
2 3 3 2 3
CHCOONa、NaCN、NaHCO 四种溶液中,物质的量浓度最大的是 。
3 3
(2)常温下,向20mL0.01mol·L-1CHCOOH溶液中逐滴加入0.01mol·L-1KOH溶液,其pH变化曲线如图所示
3
(忽略温度变化)。请回答下列有关问题:
①若想观察滴定终点,滴定过程中宜选用 作指示剂(填“酚酞”、“石蕊”或“甲基橙”)。
②b点时,溶液中离子浓度由大到小的顺序是 。
(3)常温下,向NaCN溶液中通入少量CO 发生反应的化学方程式为: 。
2
(4)在一定条件下,NaCO 溶液中存在CO +H O HCO +OH-平衡,下列说法不正确的是_______。
2 3 2
A.稀释溶液, 增大 B.通入CO,溶液pH减小
2
C.升高温度,水解平衡常数增大 D.加入NaO固体, 减小
2
【答案】(每空2分)(1)HCN CH COONa
3
(2)酚酞 c(CHCOO-)>c(K+)>c(H+)>c(OH-)
3
(3)NaCN+CO +H O=NaHCO +HCN
2 2 3
(4)A
【解析】(1)电离平衡常数越大,说明电离程度越强,根据表中数据可知,酸性强弱顺序是
CHCOOH>H CO>HCN,因此三种酸中酸性最弱的是HCN;酸的酸性越强,对应酸根离子水解程度越弱,
3 2 3
pH为10的四种盐溶液中,物质的量浓度最大的是CHCOONa;
3(2)①中和滴定实验中,不用石蕊作指示剂,CHCOOH与KOH恰好完全反应生成CHCOOK,
3 3
CHCOOK为强碱弱酸盐,溶液显碱性,选择指示剂原则之一是指示剂的变色范围与溶液的酸碱性一致,
3
因此用KOH滴定CHCOOH溶液,指示剂为酚酞;②根据图像可知,b点时,混合溶液显酸性;b点加入
3
KOH溶液10mL,此时溶液中溶质为CHCOOK、CHCOOH,且两者物质的量相等,b点溶液显酸性,说
3 3
明醋酸的电离程度大于醋酸根离子的水解程度,因此离子浓度大小顺序是
c(CHCOO-)>c(K+)>c(H+)>c(OH-);
3
(3)根据表中数据,电离平衡常数大小顺序是CHCOOH>H CO>HCN>HCO ,因此NaCN溶液中通入少
3 2 3
量CO,发生NaCN+CO+H O=HCN+NaHCO;
2 2 2
(4)A. ,加水稀释,促使平衡
向右进行,n(CO )减小,n(Na+)、K 不变,因此该比值应减小,故A错误;B.通入CO,CO 与OH-反
h 2 2
应生成HCO ,c(OH-)降低,pH降低,故B正确;C.盐类水解为吸热反应,升高温度,促进水解,水解
常数增大,故C正确;D.加入NaO,氧化钠与水反应生成NaOH,c(OH-)增大,平衡左移,c(HCO )减
2
小,c(CO )增大,该比值减小,故D正确;答案选A。
15.(14分)(2023春·北京通州·高三统考开学考试)某实验小组对 与 的反应进行探究。
【实验前的预测】
(1)甲同学认为配制 溶液时,应先将 固体溶于浓盐酸,再稀释至指定浓度。请结合化学用语说明
甲同学配制 溶液时加浓盐酸的目的: 。
(2)乙同学分析 溶液中的微粒组成认为:
①溶液含 、 、 微粒,且
②溶液显碱性,且
你认为乙同学观点正确的是 (填序号)。
丙同学根据物质的价态预测 与 两物质可能会发生氧化还原反应,丙同学建议根据原电池原理
设计实验并进行操作。
【实验设计与操作】
(3)两溶液不接触的实验
按丙同学思路,设计以下实验进行相关探究。
装置 实验现象 相关探究①写出负极的电极反应式为 。
闭合开关后灵敏电流计指针发
②探究正极产物的实验方案为 。(操作
生偏转
与现象)
(4)两溶液接触的反应
在 溶液中滴加 溶液,边滴加边振荡并观察现象。
实验
实验现象
编号
溶液由橘黄色变为红褐色并有沉淀生成,振荡后沉淀消
I 1.0 1.0 失。继续滴加 ,溶液颜色加深,放置一小时后溶
液变为绿色
溶液由橘黄色变为红褐色,没有沉淀生成,继续滴加
II 1.0 0.1
,溶液颜色加深,放置一小时后溶液变为黄色
溶液由橘黄色变为红褐色,没有沉淀生成,继续滴加
III 0.1 1.0 ,溶液颜色加深,放置一小时后溶液基本没有变
化依然为红褐色
溶液由橘黄色变为红色,没有沉淀生成,继续滴加
IV 0.1 0.1 ,溶液颜色也加深,放置一小时后溶液颜色变为
浅绿色,接近无色
甲同学认为实验III红褐色的“溶液”可能是氢氧化铁胶体,他用 实验证实了推测。
【实验结论与反思】
(5)通过对实验现象分析,小组同学得出如下结论:
① 溶液与 溶液同时发生氧化还原反应和相互促进的水解反应。
②当 时水解反应占主导地位。
你同意他们的哪些观点 (填序号,若均不同意则填无)。此外,若兼顾化学反应速率和化学反应限度
两个角度,你还能得出什么结论: 。
【答案】(除标注外,每空2分)(1) ,加盐酸,增大氢离子浓度,抑制水
解
(2)①②
(3) 取少量正极产物的溶液于试管中,向试管中滴加几滴铁氰化钾溶液,生成蓝色沉淀,则说明有亚铁离子生成
(4)丁达尔效应(1分)
(5)①(1分) 化学反应速率较慢,氧化还原反应和水解反应都是有限度的
【分析】配置氯化铁溶液时先加浓盐酸,再稀释至所需体积。亚硫酸钠溶液中微粒含有含 、 、
、Na+、OH-、H+、HO等微粒,利用原电池原理分析亚硫酸钠和氯化铁溶液反应,氯化铁作正极,
2
亚硫酸钠作负极,用不同浓度的亚硫酸钠和氯化铁溶液混合进行探究性实验,根据实验现象进行分析得到
两者既发生氧化还原反应又发生双水解反应,且反应速率较慢,两者反应都有一定的限度。
【解析】(1)由于铁离子发生水解,加盐酸,增大氢离子浓度,水解平衡逆向移动,抑制水解,因此甲
同学配制 溶液时加浓盐酸的目的: ,加盐酸,增大氢离子浓度,抑制
水解;故答案为: ,加盐酸,增大氢离子浓度,抑制水解。
(2)乙同学分析 溶液中的微粒组成认为:①溶液含 、 、 、Na+、OH-、H+、
HO微粒,根据物料守恒得到 ,故①正确;②由于亚硫酸根水
2
解生成亚硫酸氢根和氢氧根,因此溶液显碱性,根据质子守恒得到 ,
故②正确;综上所述,答案为:①②。
(3)①根据分析亚硫酸根化合价升高,铁离子化合价降低,因此亚硫酸钠作负极,其电极反应式为
;故答案为: 。
②正极是铁离子得到电子变为亚铁离子,主要通过验证溶液中是否有亚铁离子,因此探究正极产物的实验
方案为取少量正极产物的溶液于试管中,向试管中滴加几滴铁氰化钾溶液,生成蓝色沉淀,则说明有亚铁
离子生成;故答案为:取少量正极产物的溶液于试管中,向试管中滴加几滴铁氰化钾溶液,生成蓝色沉淀,
则说明有亚铁离子生成。
(4)甲同学认为实验III红褐色的“溶液”可能是氢氧化铁胶体,胶体具有丁达尔效应,因此他用丁达尔
效应实验证实了推测;故答案为:丁达尔效应。
(5)根据实验I有红褐色沉淀生成,说明发生了相互促进的双水解反应,根据IV溶液颜色最终变为无色,
说明发生了氧化还原反应,根据实验III的现象说明当 时水解反应占主导地位,几乎
没有发生氧化还原反应,因此同意他们的观点①。根据实验都继续滴加 ,增大亚硫酸根的浓度,
一小时后变化的现象才清晰,说明化学反应速率较慢,氧化还原反应和水解反应都是有限度的;故答案为:
①;化学反应速率较慢,氧化还原反应和水解反应都是有限度的。
1.(2023·北京·统考高考真题)下列过程与水解反应无关的是
A.热的纯碱溶液去除油脂
B.重油在高温、高压和催化剂作用下转化为小分子烃
C.蛋白质在酶的作用下转化为氨基酸D.向沸水中滴入饱和 溶液制备 胶体
【答案】B
【解析】A.热的纯碱溶液因碳酸根离子水解显碱性,油脂在碱性条件下能水解生成易溶于水的高级脂肪
酸盐和甘油,故可用热的纯碱溶液去除油脂,A不符合题意;B.重油在高温、高压和催化剂作用下发生
裂化或裂解反应生成小分子烃,与水解反应无关,B符合题意;C.蛋白质在酶的作用下可以发生水解反
应生成氨基酸,C不符合题意;D. Fe3+能发生水解反应生成 Fe(OH) ,加热能增大Fe3+ 的水解程度,D
3
不符合题意;故选B。
2.(2021·天津·统考高考真题)常温下,下列有关电解质溶液的叙述正确的是
A.在 溶液中
B.在 溶液中
C.在 溶液中
D.氨水和NH Cl溶液混合,形成pH=9的溶液中
4
【答案】A
【解析】A.由于磷酸为多元酸,第一步电离大于第二步电离大于第三步电离,所以在 溶
液中,离子浓度大小为: ,故A正确;B.在 溶
液中,根据电荷守恒得到 ,故B错误;C.在 溶液
中,根据物料守恒得到 ,故C错误;D.氨水和NH Cl溶液混合,
4
形成pH=9的溶液,则 ,根据电荷守恒 ,则 ,故
D错误;故选A。
3.(2021·北京·高考真题)下列实验中,均产生白色沉淀。
下列分析不正确的是
A.NaCO 与NaHCO 溶液中所含微粒种类相同
2 3 3
B.CaCl 能促进NaCO、NaHCO 水解
2 2 3 3
C.Al (SO ) 能促进NaCO、NaHCO 水解
2 4 3 2 3 3
D.4个实验中,溶液滴入后,试管中溶液pH均降低
【答案】B
【解析】A.NaCO 溶液、NaHCO 溶液均存在Na+、 、 、HCO、H+、OH-、HO,故含有的微
2 3 3 2 3 2
粒种类相同,A正确;B. H++ ,加入Ca2+后,Ca2+和 反应生成沉淀,促进 的
电离,B错误;C.Al3+与 、 都能发生互相促进的水解反应,C正确;D.由题干信息可知形成沉淀时会消耗碳酸根和碳酸氢根,则它们浓度减小,水解产生的氢氧根的浓度会减小,pH减小,D正确;
故选B。
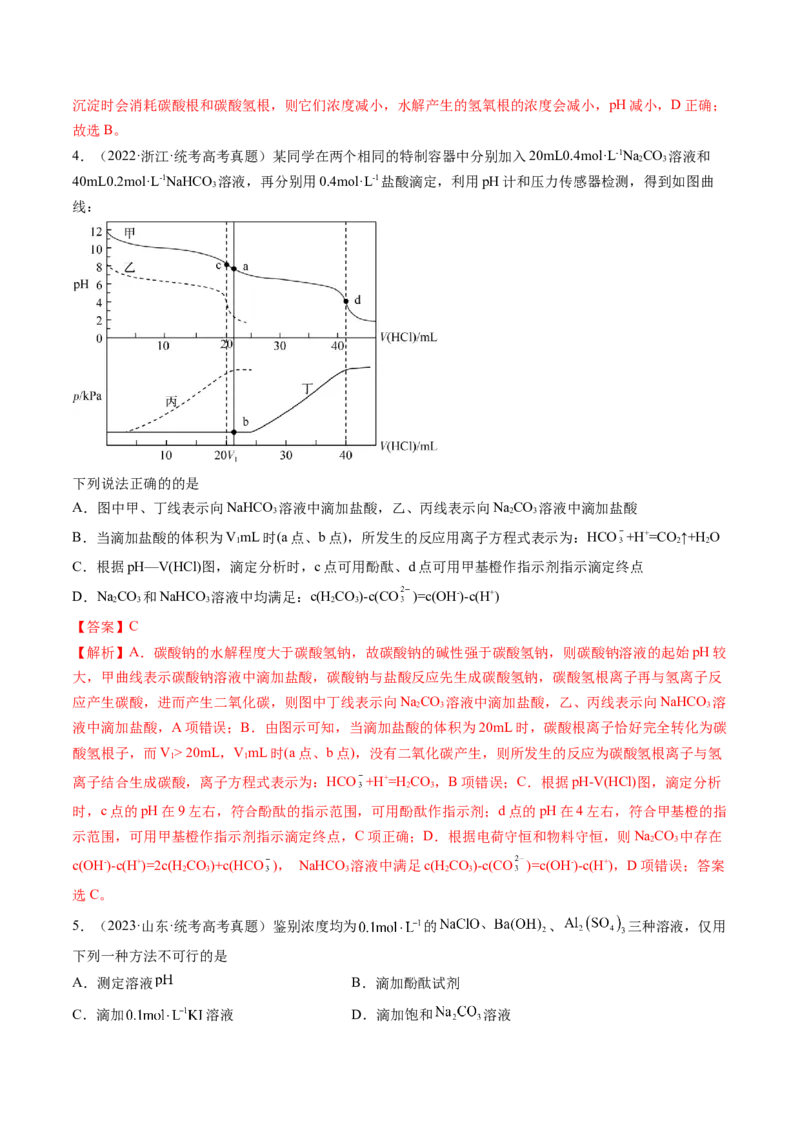
4.(2022·浙江·统考高考真题)某同学在两个相同的特制容器中分别加入20mL0.4mol·L-1NaCO 溶液和
2 3
40mL0.2mol·L-1NaHCO 溶液,再分别用0.4mol·L-1盐酸滴定,利用pH计和压力传感器检测,得到如图曲
3
线:
下列说法正确的的是
A.图中甲、丁线表示向NaHCO 溶液中滴加盐酸,乙、丙线表示向NaCO 溶液中滴加盐酸
3 2 3
B.当滴加盐酸的体积为VmL时(a点、b点),所发生的反应用离子方程式表示为:HCO +H+=CO ↑+H O
1 2 2
C.根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D.NaCO 和NaHCO 溶液中均满足:c(HCO)-c(CO )=c(OH-)-c(H+)
2 3 3 2 3
【答案】C
【解析】A.碳酸钠的水解程度大于碳酸氢钠,故碳酸钠的碱性强于碳酸氢钠,则碳酸钠溶液的起始pH较
大,甲曲线表示碳酸钠溶液中滴加盐酸,碳酸钠与盐酸反应先生成碳酸氢钠,碳酸氢根离子再与氢离子反
应产生碳酸,进而产生二氧化碳,则图中丁线表示向NaCO 溶液中滴加盐酸,乙、丙线表示向NaHCO 溶
2 3 3
液中滴加盐酸,A项错误;B.由图示可知,当滴加盐酸的体积为20mL时,碳酸根离子恰好完全转化为碳
酸氢根子,而V> 20mL,VmL时(a点、b点),没有二氧化碳产生,则所发生的反应为碳酸氢根离子与氢
1 1
离子结合生成碳酸,离子方程式表示为:HCO +H+=H CO,B项错误;C.根据pH-V(HCl)图,滴定分析
2 3
时,c点的pH在9左右,符合酚酞的指示范围,可用酚酞作指示剂;d点的pH在4左右,符合甲基橙的指
示范围,可用甲基橙作指示剂指示滴定终点,C项正确;D.根据电荷守恒和物料守恒,则NaCO 中存在
2 3
c(OH-)-c(H+)=2c(H CO)+c(HCO ), NaHCO 溶液中满足c(HCO)-c(CO )=c(OH-)-c(H+),D项错误;答案
2 3 3 2 3
选C。
5.(2023·山东·统考高考真题)鉴别浓度均为 的 、 三种溶液,仅用
下列一种方法不可行的是
A.测定溶液 B.滴加酚酞试剂
C.滴加 溶液 D.滴加饱和 溶液【答案】C
【解析】A. 溶液显弱碱性, 溶液显强碱性, 溶液显酸性,则测定溶液 是可
以鉴别出来的,故A不符合题意;B. 溶液显弱碱性,滴入酚酞先变红后褪色, 溶液显强
碱性,滴入酚酞溶液,显红色, 溶液显酸性,滴入酚酞不变色,则滴加酚酞试剂是可以鉴别出
来的,故B不符合题意;C. 溶液滴入碘化钾溶液,发生氧化还原反应生成碘,液面会由无色变成
黄色,振荡后会变成无色,而 溶液, 溶液滴入碘化钾溶液后,因不与两者反应而没有
现象,则仅用滴加 溶液无法鉴别,则C符合题意;D.饱和 溶液和 溶液不反应,
和 溶液反应生成碳酸钡沉淀,和 溶液发生双水解反应生成沉淀和气体,则滴入饱和
溶液是可以鉴别出来的,故D不符合题意;答案C。
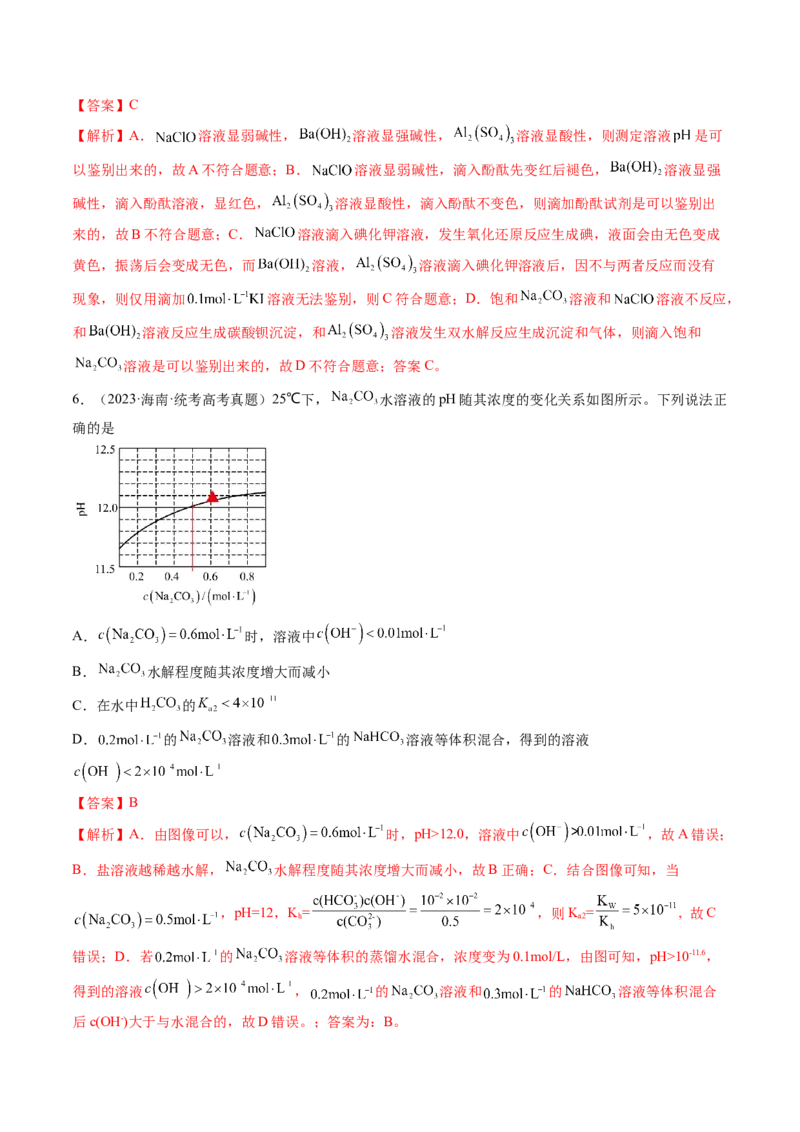
6.(2023·海南·统考高考真题)25℃下, 水溶液的pH随其浓度的变化关系如图所示。下列说法正
确的是
A. 时,溶液中
B. 水解程度随其浓度增大而减小
C.在水中 的
D. 的 溶液和 的 溶液等体积混合,得到的溶液
【答案】B
【解析】A.由图像可以, 时,pH>12.0,溶液中 ,故A错误;
B.盐溶液越稀越水解, 水解程度随其浓度增大而减小,故B正确;C.结合图像可知,当
,pH=12,K= ,则K = , 故C
h a2
错误;D.若 的 溶液等体积的蒸馏水混合,浓度变为0.1mol/L,由图可知,pH>10-11.6,
得到的溶液 , 的 溶液和 的 溶液等体积混合
后c(OH-)大于与水混合的,故D错误。;答案为:B。