文档内容
专题 11 水溶液中的离子反应与平衡
第 31 练 水的电离和溶液的 pH
1.(2022·浙江省1月选考)水溶液呈酸性的盐是( )
A.NH Cl B.BaCl C.HSO D.Ca(OH)
4 2 2 4 2
2.下列溶液一定显中性的是( )
A.溶液中c(OH-)>c(H+) B.c(H+)=
C.溶液中c(H+)=10-7 mol·L-1 D.pH<7的溶液
3.下列溶液一定显酸性的是( )
A.溶液中c(OH-)>c(H+) B.滴加紫色石蕊试液后变红色的溶液
C.溶液中c(H+)=10-6 mol·L-1 D.pH<7的溶液
4.常温下,0.10mol·L−1盐酸溶液中c(Cl-)是水电离出的c(H+)的( )
A.13倍 B.10-13倍 C.1012倍 D.12倍
5.某温度下,测得0.01mol/LNaOH溶液pH=10,则下列说法正确的是( )
A.该溶液温度为25℃ B.与等体积的pH=4的盐酸刚好中和
C.该温度下蒸馏水pH=6 D.该溶液中c(H+)=10-12mol/L
6.在25 ℃的条件下,将体积都为10 mL、pH都等于3的醋酸和盐酸,加水稀释到a mL和b mL,
测得稀释后溶液的pH均为5,则稀释时加入水的体积为( )
A.a=b=1000 mL B.a=b>1000 mL
C.ab
7.下列有关溶液的酸碱性与pH的说法错误的是( )
A.溶液pH越小,酸性越强,反之,碱性越强
B.pH<7的溶液,可能呈酸性
C.当溶液中的c(H+)或c(OH-)较小时,用pH表示其酸碱性更为方便
D.把pH试纸直接插入待测溶液中,测其pH
8.下列关于溶液酸碱性的说法正确的是( )
A.pH=7的溶液呈中性
B.中性溶液中一定有c(H+)=1.0×10-7mol·L-1
C.c(H+)= mol·L-1的溶液呈中性
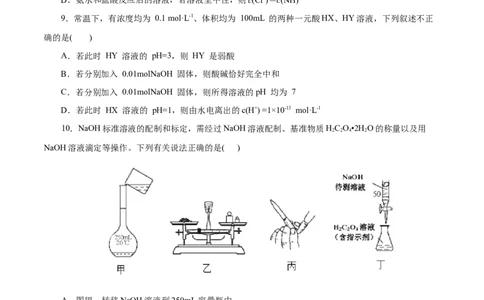
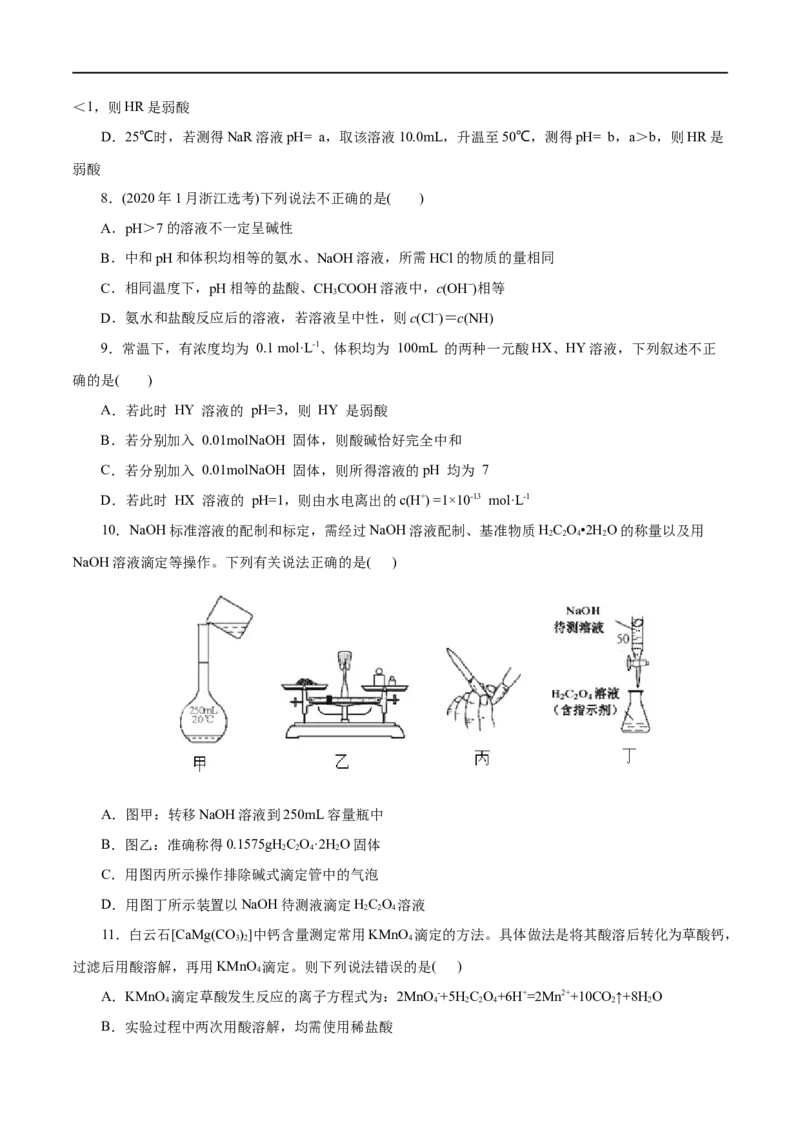
D.在100 ℃时,纯水的pH<7,因此呈酸性9.用pH试纸测定溶液的pH,下列叙述正确的是( )
A.测得某浓度的NaClO溶液的pH为10
B.常温下测得NH Cl溶液pH约为4.1
4
C.用湿润的pH试纸测pH相同的盐酸和醋酸溶液的pH,误差较大的是盐酸
D.在试管内放入少量溶液并煮沸,把pH试纸放在管口观察其颜色并与标准比色卡比较
10.常温下,0.10mol·L−1盐酸溶液中c(Cl-)是水电离出的c(H+)的( )
A.13倍 B.10-13倍 C.1012倍 D.12倍
11.常温下,10LpH=2的硫酸溶液,该溶液的浓度是( )
A.1×10-1mol/L B.1×10-2mol/L C.2×10-2mol/L D.0.5×10-2mol/L
12. 25℃时,pH=12的NaOH溶液中,由水电离出的H+离子浓度是( )
A.1×10-7mol/L B.1×10-12mol/L C.1×10-2mol/L D.1×10-14mol/L
13.某温度下,测得0.01mol/LNaOH溶液pH=10,则下列说法正确的是( )
A.该溶液温度为25℃ B.与等体积的pH=4的盐酸刚好中和
C.该温度下蒸馏水pH=6 D.该溶液中c(H+)=10-12mol/L
14.用pH试纸测定溶液的pH,下列叙述正确的是( )
A.测得某浓度的NaClO溶液的pH为10
B.常温下测得NH Cl溶液pH约为4.1
4
C.用湿润的pH试纸测pH相同的盐酸和醋酸溶液的pH,误差较大的是盐酸
D.在试管内放入少量溶液并煮沸,把pH试纸放在管口观察其颜色并与标准比色卡比较
15.某温度下,水的离子积常数K =10-12。该温度下,将pH=4的硫酸与pH=9的氢氧化钠溶液混合并
w
保持恒温,当混合溶液的pH=7时,硫酸与氢氧化钠溶液的体积比约为( )
A.9:1 B.1:10 C.10:1 D.99:21
1.下列事实不能证明亚硝酸(HNO)是弱酸的是( )
2
A.0.01mol·L-1的HNO 溶液的pH=3
2
B.HNO 溶液的导电能力比盐酸弱
2
C.25℃时NaNO 溶液的pH大于7
2
D.25℃时将pH=2的HNO 溶液稀释至原体积的100倍,溶液的pH=3.7
2
2.对室温下100ml pH=3的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是( )A.加水稀释至溶液体积为1000ml,醋酸溶液的pH变为4
B.温度都升高 后,两溶液的pH不再相等
C.加水稀释至溶液体积为200ml后,两种溶液中c(OH-)都减小
D.加足量的锌充分反应后,两溶液中产生的氢气体积可用如图表示
3.常温下,水存在HO H+ + OH-的平衡,下列说法错误的是( )
2
A.将水加热,K 增大,pH减小
w
B.向水中滴入少量稀盐酸,平衡逆向移动,K 减小
w
C.向水中加入少量固体NH Cl,c(H+) > 10-7mol/L,K 不变
4 w
D.向水中加入少量固体CHCOONa,平衡正向移动,c(H+)降低
3
4.在相同温度下,0.01 mol·L-1 NaOH溶液和0.01 mol·L-1的盐酸相比,下列说法正确的是( )
A.两溶液中由水电离的c(H+)都是1.0×10-12 mol·L-1
B.NaOH溶液和盐酸由水电离出c(OH-)分别为1.0×10-2 mol·L-1、1.0×10-12 mol·L-1
C.两溶液中由水电离出的c(H+)相等
D.两者都促进了水的电离
5.pH相同的醋酸溶液和盐酸,分别用蒸馏水稀释到原体积的 m和n倍,稀释后两溶液pH仍相同,
则m和n的关系是( )
A.m=n B.m>n C.mV(乙)
C.物质的量浓度:c(甲)>10c(乙)
D.甲中的c(OH-)为乙中的c(OH-)的10倍
3.水的电离平衡曲线如图所示,下列说法正确的是( )
A.图中五点K 间的关系:B>C>A>D=E
W
B.若从A点到D点,可采用在水中加入少量NaOH的方法
C.若从A点到C点,可采用温度不变时在水中加入适量HSO 的方法
2 4
D.若处在B点时,将pH=2的硫酸与pH=12的KOH等体积混合后,溶液显碱性
4.部分弱酸的电离平衡常数如下表:弱酸 HCOOH HCN HCO
2 3
K =4.3×10-7 K =
i1 i2
电离平衡常数(25 ℃) K=1.77×10-4 K=4.9×10-10
i i
5.6×10-11
下列选项错误的是( )
A.2CN-+HO+CO===2HCN+CO
2 2
B.2HCOOH+CO===2HCOO-+HO+CO↑
2 2
C.由数据可知酸性:HCOOH>H CO>HCN>HCO
2 3
D.25 ℃时,在等浓度的CHCOOH溶液和HCN溶液中,水的电离程度后者大
3
5.(2020•浙江1月选考)室温下,向20.00 mL 0.1000mol·L−1盐酸中滴加0.1000mol·L−1 NaOH溶液,溶
液的pH随NaOH溶液体积的变化如图。已知lg5=0.7。下列说法不正确的是( )
A.NaOH与盐酸恰好完全反应时,pH=7
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D.V(NaOH)=30.00 mL时,pH=12.3
6.(2021•浙江1月选考)实验测得10 mL 0.50 mol·L-1NH Cl溶液、10 mL 0.50mol·L-1CHCOONa溶液的
4 3
pH分别随温度与稀释加水量的变化如图所示。已知25 ℃时CHCOOH和NH ·H O的电离常数均为1.8×10-
3 3 2
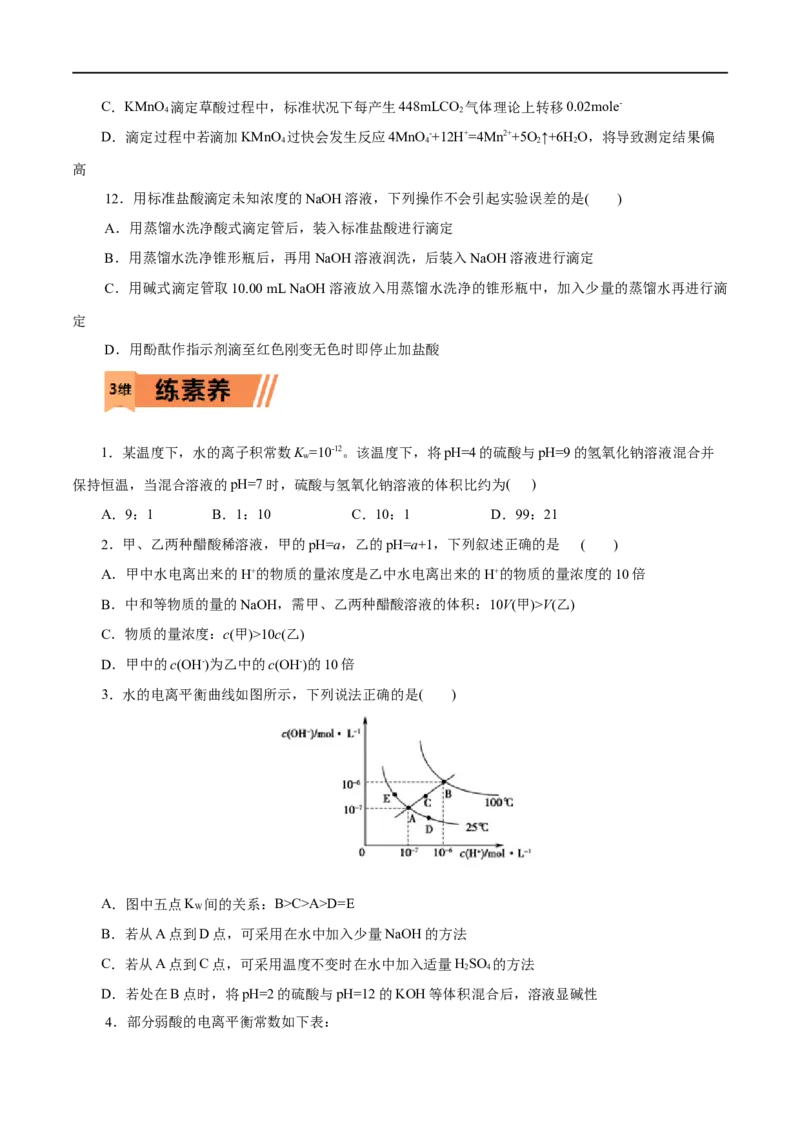
5.下列说法不正确的是( )A.图中实线表示pH随加水量的变化,虚线表示pH随温度的变化'
B.将NH Cl溶液加水稀释至浓度 mol·L-1,溶液pH变化值小于lgx
4
C.随温度升高,K 增大,CHCOONa溶液中c(OH- )减小,c(H+)增大,pH减小
w 3
D.25 ℃时稀释相同倍数的NH Cl溶液与CHCOONa溶液中:c(Na+ )-c(CHCOO- )=c(Cl-)-c(NH +)
4 3 3 4
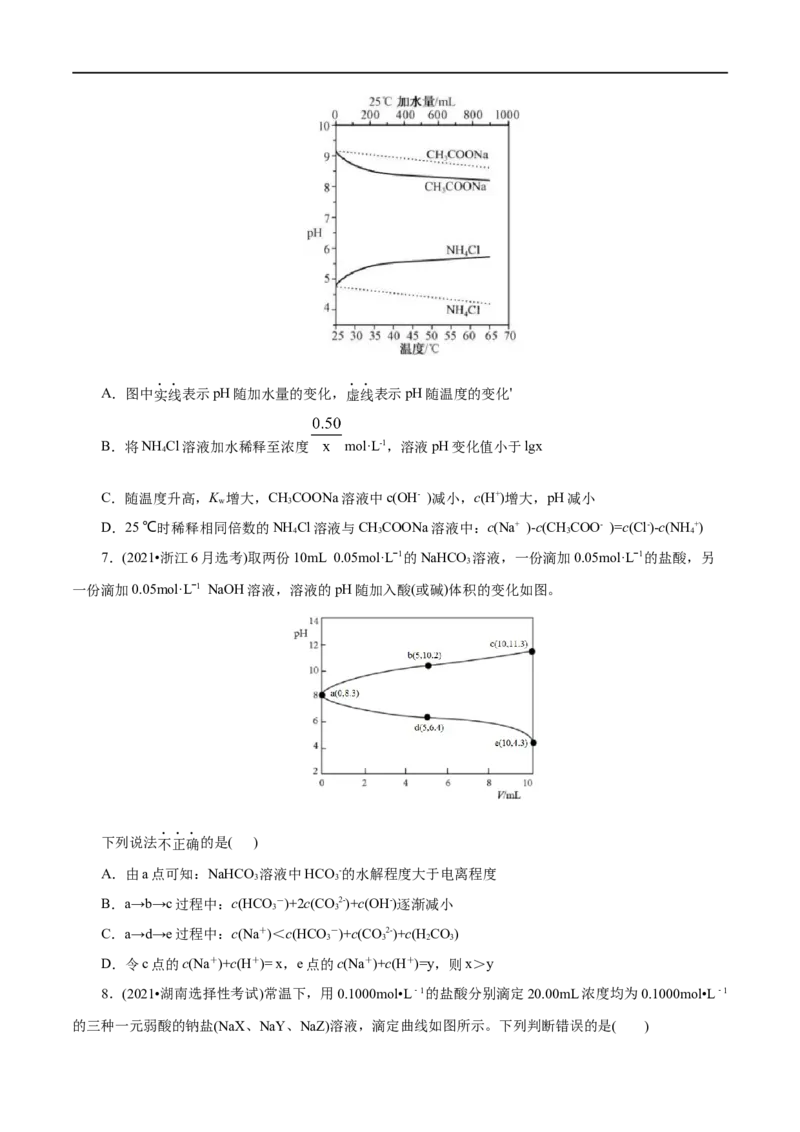
7.(2021•浙江6月选考)取两份10mL 0.05mol·Lˉ1的NaHCO 溶液,一份滴加0.05mol·Lˉ1的盐酸,另
3
一份滴加0.05mol·Lˉ1 NaOH溶液,溶液的pH随加入酸(或碱)体积的变化如图。
下列说法不正确的是( )
A.由a点可知:NaHCO 溶液中HCO -的水解程度大于电离程度
3 3
B.a→b→c过程中:c(HCO -)+2c(CO2-)+c(OH-)逐渐减小
3 3
C.a→d→e过程中:c(Na+)<c(HCO -)+c(CO2-)+c(H CO)
3 3 2 3
D.令c点的c(Na+)+c(H+)= x,e点的c(Na+)+c(H+)=y,则x>y
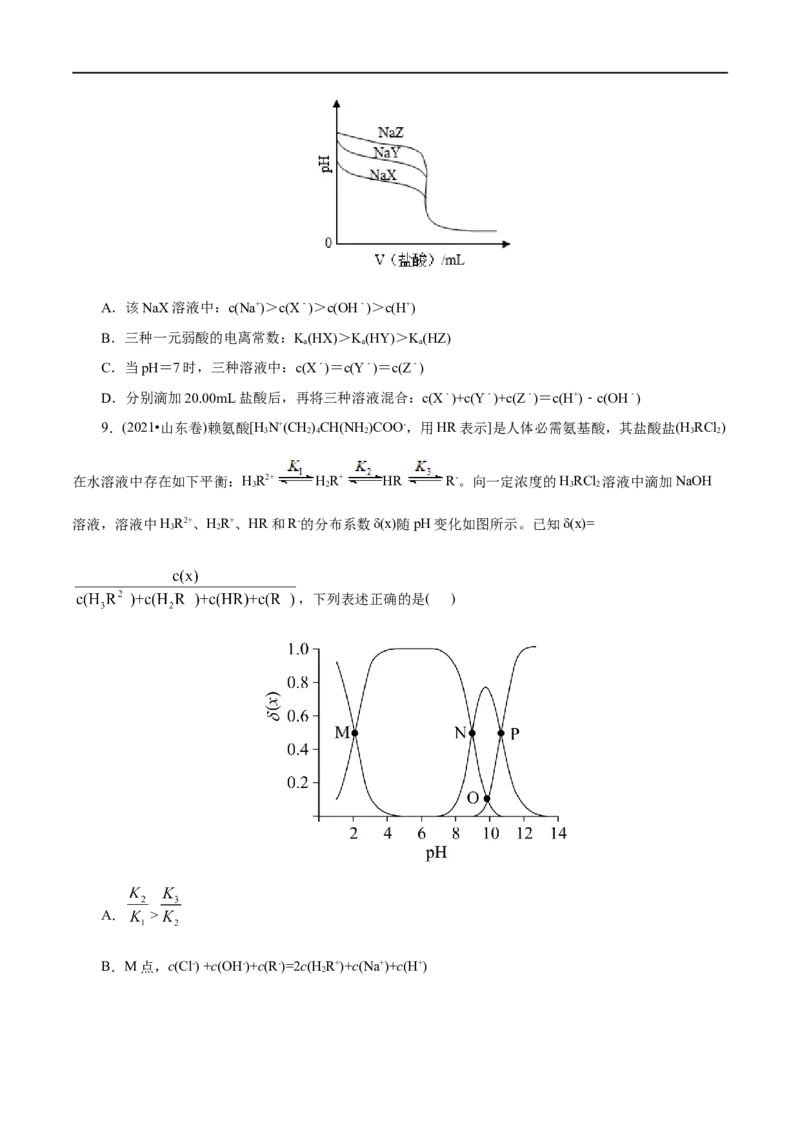
8.(2021•湖南选择性考试)常温下,用0.1000mol•L﹣1的盐酸分别滴定20.00mL浓度均为0.1000mol•L﹣1
的三种一元弱酸的钠盐(NaX、NaY、NaZ)溶液,滴定曲线如图所示。下列判断错误的是( )A.该NaX溶液中:c(Na+)>c(X﹣)>c(OH﹣)>c(H+)
B.三种一元弱酸的电离常数:K(HX)>K(HY)>K(HZ)
a a a
C.当pH=7时,三种溶液中:c(X﹣)=c(Y﹣)=c(Z﹣)
D.分别滴加20.00mL盐酸后,再将三种溶液混合:c(X﹣)+c(Y﹣)+c(Z﹣)=c(H+)﹣c(OH﹣)
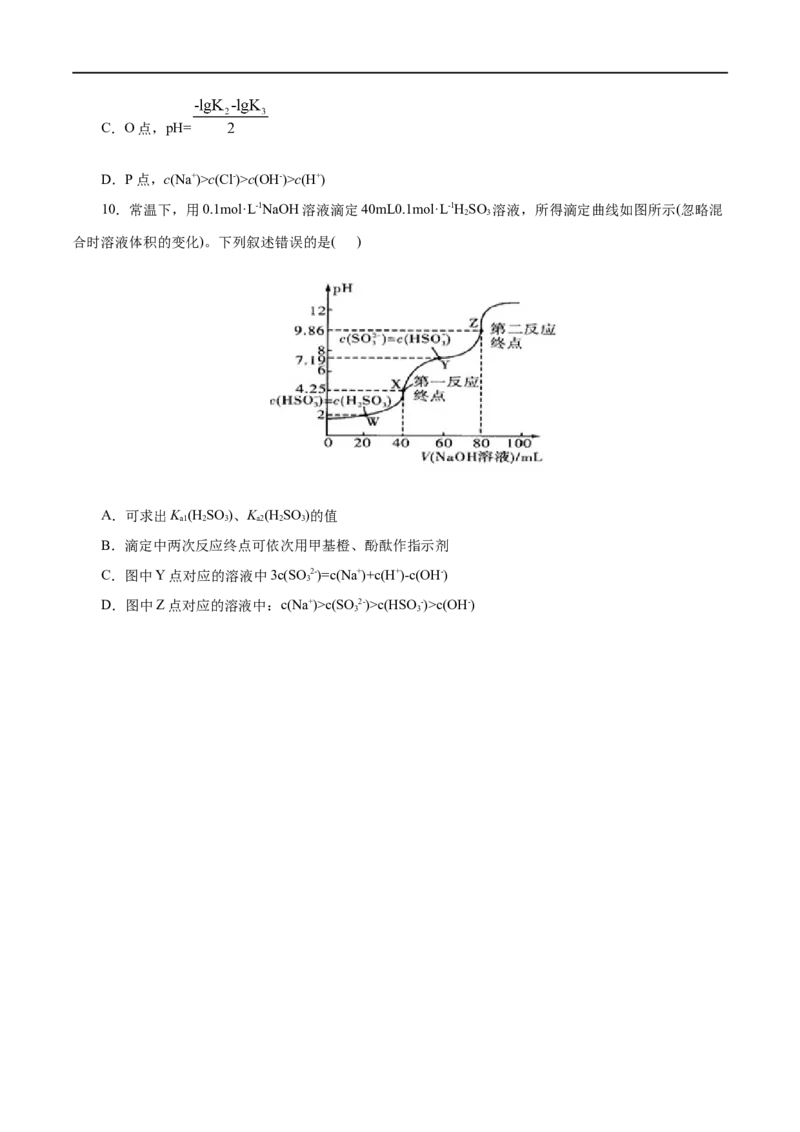
9.(2021•山东卷)赖氨酸[H N+(CH)CH(NH)COO-,用HR表示]是人体必需氨基酸,其盐酸盐(H RCl )
3 2 4 2 3 2
在水溶液中存在如下平衡:HR2+ HR+ HR R-。向一定浓度的HRCl 溶液中滴加NaOH
3 2 3 2
溶液,溶液中HR2+、HR+、HR和R-的分布系数δ(x)随pH变化如图所示。已知δ(x)=
3 2
,下列表述正确的是( )
A. >
B.M点,c(Cl-) +c(OH-)+c(R-)=2c(H R+)+c(Na+)+c(H+)
2C.O点,pH=
D.P点,c(Na+)>c(Cl-)>c(OH-)>c(H+)
10.常温下,用0.1mol·L-1NaOH溶液滴定40mL0.1mol·L-1HSO 溶液,所得滴定曲线如图所示(忽略混
2 3
合时溶液体积的变化)。下列叙述错误的是( )
A.可求出K (H SO )、K (H SO )的值
a1 2 3 a2 2 3
B.滴定中两次反应终点可依次用甲基橙、酚酞作指示剂
C.图中Y点对应的溶液中3c(SO 2-)=c(Na+)+c(H+)-c(OH-)
3
D.图中Z点对应的溶液中:c(Na+)>c(SO2-)>c(HSO -)>c(OH-)
3 3