文档内容
第 38 讲 晶体结构与性质
第一部分:高考真题感悟
1.(2022·湖北·高考真题)某立方卤化物可用于制作光电材料,其晶胞结构如图所示。下列说法错误的是
A. 的配位数为6 B.与 距离最近的是
C.该物质的化学式为 D.若 换为 ,则晶胞棱长将改变
【答案】B
【解析】A. 配位数为与其距离最近且等距离的F-的个数,如图所示, 位于体心,F-位于面心,
所以 配位数为6,A正确;B. 与 的最近距离为棱长的 , 与 的最近距离为棱长的 ,
所以与 距离最近的是 ,B错误;C. 位于顶点,所以 个数= =1,F-位于面心,F-个数=
=3, 位于体心,所以 个数=1,综上,该物质的化学式为 ,C正确;D. 与 半径不同,
替换后晶胞棱长将改变,D正确;故选B。
2.(2021·天津·高考真题)下列各组物质的晶体类型相同的是
A.SiO 和SO B.I 和NaCl C.Cu和Ag D.SiC和MgO
2 3 2
【答案】C
【解析】A.SiO 为原子晶体,SO 为分子晶体,晶体类型不同,故A错误;B.I 为分子晶体,NaCl为离
2 3 2
子晶体,晶体类型不同,故B错误;C.Cu和Ag都为金属晶体,晶体类型相同,故C正确;D.SiC为原
子晶体,MgO为离子晶体,晶体类型不同,故D错误;故选C。
3.(2022·江苏·高考真题)我国古代就掌握了青铜(铜-锡合金)的冶炼、加工技术,制造出许多精美的青铜器;Pb、 是铅蓄电池的电极材料,不同铅化合物一般具有不同颜色,历史上曾广泛用作颜料,下列
物质性质与用途具有对应关系的是
A.石墨能导电,可用作润滑剂
B.单晶硅熔点高,可用作半导体材料
C.青铜比纯铜熔点低、硬度大,古代用青铜铸剑
D.含铅化合物颜色丰富,可用作电极材料
【答案】C
【解析】A.石墨是过渡型晶体,质软,可用作润滑剂,故A错误;B.单晶硅可用作半导体材料与空穴
可传递电子有关,与熔点高无关,故B错误;C.青铜是铜合金,比纯铜熔点低、硬度大,易于锻造,古
代用青铜铸剑,故C正确;D.含铅化合物可在正极得到电子发生还原反应,所以可用作电极材料,与含
铅化合物颜色丰富无关,故D错误;故选C。
4.(2022·山东·高考真题) 、 属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存
在 键、 键。下列说法错误的是
A. 的熔点高于 B.晶体中所有化学键均为极性键
C.晶体中所有原子均采取 杂化 D.晶体中所有原子的配位数均相同
【答案】A
【解析】Al和Ga均为第ⅢA元素,N属于第ⅤA元素,AlN、GaN的成键结构与金刚石相似,则其为共
价晶体,且其与金刚石互为等电子体,等电子体之间的结构和性质相似。AlN、GaN晶体中,N原子与其
相邻的原子形成3个普通共价键和1个配位键。A.因为AlN、GaN为结构相似的共价晶体,由于Al原子
的半径小于Ga,N—Al的键长小于N—Ga的,则N—Al的键能较大,键能越大则其对应的共价晶体的熔
点越高,故GaN的熔点低于AlN,A说错误;B.不同种元素的原子之间形成的共价键为极性键,故两种
晶体中所有化学键均为极性键,B说法正确;C.金刚石中每个C原子形成4个共价键(即C原子的价层
电子对数为4),C原子无孤电子对,故C原子均采取sp3杂化;由于AlN、GaN与金刚石互为等电子体,
则其晶体中所有原子均采取sp3杂化,C说法正确;D.金刚石中每个C原子与其周围4个C原子形成共价
键,即C原子的配位数是4,由于AlN、GaN与金刚石互为等电子体,则其晶体中所有原子的配位数也均
为4,D说法正确。
综上所述,本题选A。
5.(2022·山东·高考真题) 是一种钠离子电池正极材料,充放电过程中正极材料立方晶胞(示意图)
的组成变化如图所示,晶胞内未标出因放电产生的0价Cu原子。下列说法正确的是A.每个 晶胞中 个数为x
B.每个 晶胞完全转化为 晶胞,转移电子数为8
C.每个 晶胞中0价Cu原子个数为
D.当 转化为 时,每转移 电子,产生 原子
【答案】BD
【解析】A.由晶胞结构可知,位于顶点和面心的硒离子个数为8× +6× =4,位于体内的铜离子和亚铜
离子的个数之和为8,设晶胞中的铜离子和亚铜离子的个数分别为a和b,则a+b=8-4x,由化合价代数和为
0可得2a+b=4×2,解得a=4x,故A错误;B.由题意可知,NaSe转化为Cu Se的电极反应式为NaSe-2e-
2 2-x 2
+(2-x)Cu=Cu Se+2Na+,由晶胞结构可知,位于顶点和面心的硒离子个数为8× +6× =4,则每个晶胞中
2-x
含有4个NaSe,转移电子数为8,故B正确;C.由题意可知,Cu Se转化为NaCuSe的电极反应式为
2 2-x
Cu Se+ e-+Na+=NaCuSe+(1-x)Cu,由晶胞结构可知,位于顶点和面心的硒离子个数为8× +6× =4,则每
2-x
个晶胞中含有4个NaCuSe,晶胞中0价铜而个数为(4-4x),故C错误;D.由题意可知,NaCu Se转化为
y 2-x
NaCuSe的电极反应式为NaCu Se+(1-y) e-+(1-y) Na+=NaCuSe+(1-x)Cu,所以每转移(1-y)电子,产生(1-
y 2-x
x)mol铜,故D正确;故选BD。
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
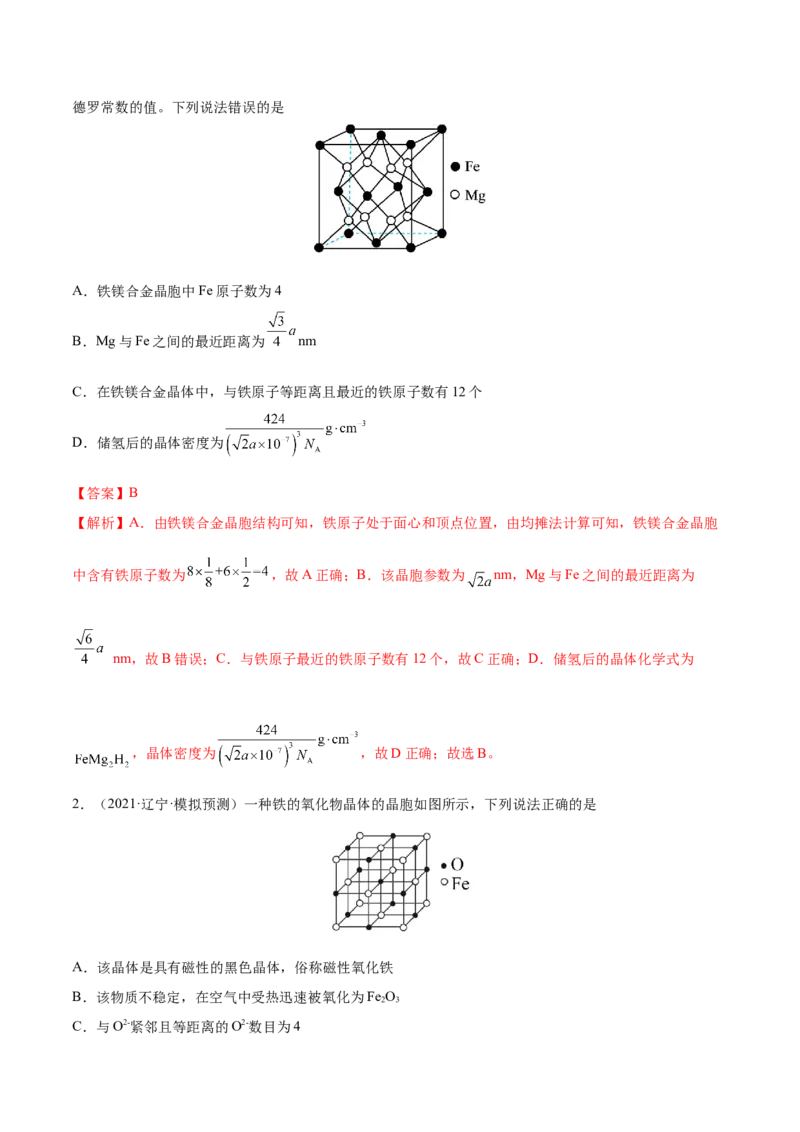
1.(2021·湖北·模拟预测)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,晶胞结构如图所示。
储氢时, 分子在晶胞的体心和棱的中心位置,且最近的两个氢分子之间的距离为a nm, 表示阿伏加德罗常数的值。下列说法错误的是
A.铁镁合金晶胞中Fe原子数为4
B.Mg与Fe之间的最近距离为 nm
C.在铁镁合金晶体中,与铁原子等距离且最近的铁原子数有12个
D.储氢后的晶体密度为
【答案】B
【解析】A.由铁镁合金晶胞结构可知,铁原子处于面心和顶点位置,由均摊法计算可知,铁镁合金晶胞
中含有铁原子数为 ,故A正确;B.该晶胞参数为 nm,Mg与Fe之间的最近距离为
nm,故B错误;C.与铁原子最近的铁原子数有12个,故C正确;D.储氢后的晶体化学式为
,晶体密度为 ,故D正确;故选B。
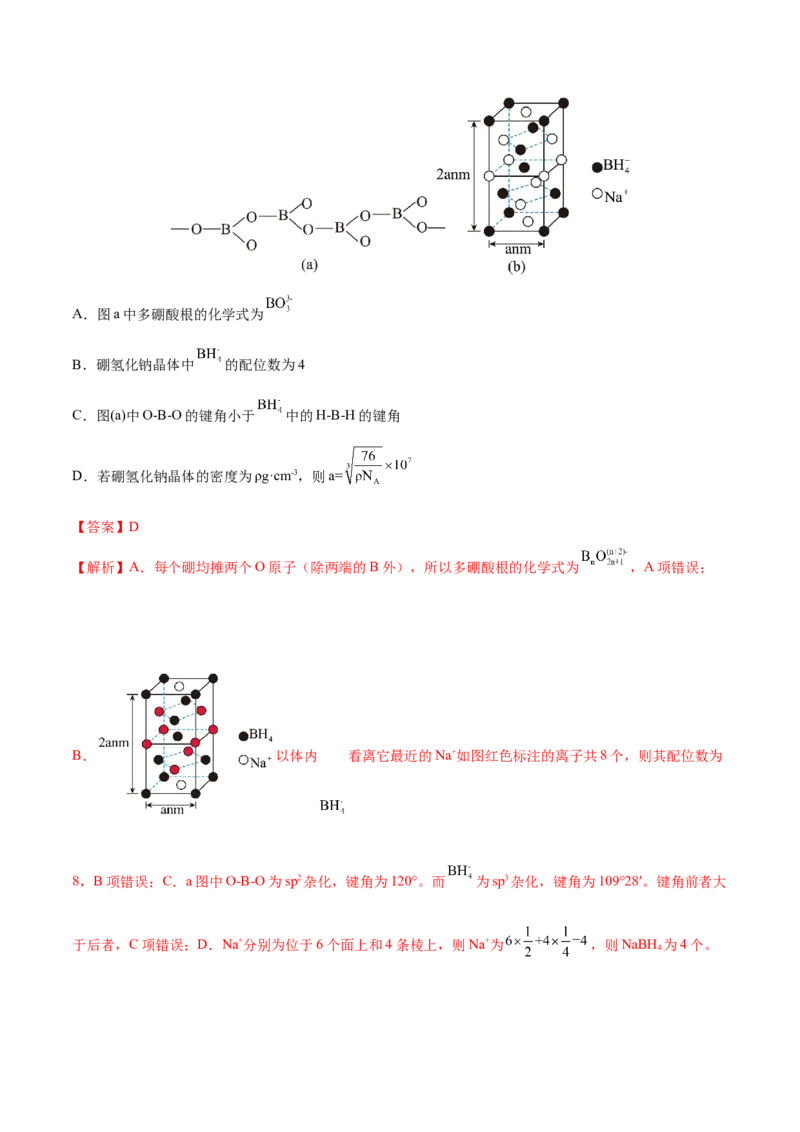
2.(2021·辽宁·模拟预测)一种铁的氧化物晶体的晶胞如图所示,下列说法正确的是
A.该晶体是具有磁性的黑色晶体,俗称磁性氧化铁
B.该物质不稳定,在空气中受热迅速被氧化为Fe O
2 3
C.与O2-紧邻且等距离的O2-数目为4D.一个该晶胞中所含离子总数为8
【答案】D
【解析】A.O原子位于棱心和内部,所以一个晶胞中O的个数为 +1=4,Fe原子位于面心和顶点,
个数为 =4,化学式为FeO,磁性氧化铁为Fe O,A错误;B.FeO不稳定,在空气中受热迅速
3 4
被氧化为Fe O,B错误;C.以体心O2-看,与棱心O2-的距离最近,则与O2-紧邻且等距离的O2-数目为
3 4
12,C错误;D.FeO为离子化合物,阳离子数、阴离子数之和为离子总数,结合选项A可知一个该晶胞
中所含离子总数为8,D正确;综上所述答案为D。
3.(2021·山东泰安·模拟预测)硫化锌有两种常见的晶体,分别是六方硫化锌(晶胞结构如图甲所示)和立
方硫化锌(晶胞结构如图乙所示)。下列说法错误的是
A.可用X-射线衍射实验鉴别硫化锌是否属于晶体
B.每个六方硫化锌晶胞中含2个S原子
C.立方硫化锌中锌的配位数为4
D.氧化锌的熔点低于六方硫化锌和立方硫化锌
【答案】D
【解析】A.晶体与非晶体最本质的区别是组成物质的粒子在微观空间是否有序排列,x射线衍射可以看到
微观结构,所以可用X-射线衍射实验鉴别硫化锌是否属于晶体,A正确;B.每个六方硫化锌晶胞中有4
个S原子位于棱上,1个S原子位于内部,含4× +1=2个S原子,B正确;C.据图可知Zn原子位于4个
S原子形成的正四面体空隙中,所以立方硫化锌中锌的配位数为4,C正确;D.O2-的半径小于S2-,所以
O2-与Zn2+形成的离子键更强,晶格能更大,熔点更高,D错误;综上所述答案为D。
4.(2022·上海闵行·一模)2021年5月15日中国火星探测器“祝融号”在一种比空气还轻的气凝胶材料
保护下成功着陆火星。有种气凝胶材料主要成分为SiO,有关其描述错误的是
2
A.由原子构成 B.含极性键 C.熔点高 D.极性分子
【答案】D
【解析】SiO 是Si原子和O原子形成的正四面体网状结构,每个Si原子以sp3杂化和4个O原子形成Si—
2O极性共价键,属于熔点很高的共价晶体,不是极性分子,故答案为:D
5.(2022·上海·模拟预测)某晶体中只含有非极性键和极性键,关于该晶体的说法错误的是
A.可能是离子晶体也可能是分子晶体 B.可能是电解质也可能是非电解质
C.可能是有机物也可能是无机物 D.可能是极性分子也可能是非极性分子
【答案】A
【解析】A.极性键和非极性键均属于共价键,由题意知该晶体中不含离子键,故不可能是离子晶体,A
错误;B.由题意知,下列物质符合题意,CHCOOH(属于电解质)、CH=CH (属于非电解质)、C H
3 2 2 6 6
(属于非电解质)等,B正确;C.过氧化氢,乙烯,苯等只含非极性键和极性键,HO 是无机物,
2 2
C H、C H 是有机物,C正确;D.HO 是极性分子,C H、C H 是非极性分子,D正确;故答案选A。
2 4 6 6 2 2 2 4 6 6
6.(2022·辽宁沈阳·三模)某种离子型铁的氧化物晶胞如图所示,它由A、B方块组成。已知该晶体的密
度为 ,阿伏加德罗常数的值为 ,下列说法中错误的是
A.该铁的氧化物化学式为 B.距离Fe3+最近的 有6个
C.晶体中的 只能构成正四面体空隙 D.晶胞的边长为
【答案】C
【解析】由A方块可知,位于顶点和体心的亚铁离子个数为4× +1= 、位于体内的氧离子个数为4,B
方块则位于顶点的亚铁离子个数为4× = ,位于体内的铁离子和氧离子都为4,则由4个A方块和4个B
方块组成的晶胞中亚铁离子、铁离子和氧离子的个数比为( + )×4:4×4:(4+4)×4=1:2:4,所以晶胞的
化学式为 。A.由分析可知,铁的氧化物化学式为 ,故A正确;B.由B方块可知,小立方体
中位于顶点的铁离子与位于顶点的氧离子个数的距离最近,所以距离铁离子最近的氧离子有6个,故B正确;C.由B方块可知,晶体中的氧离子构成正四面体空隙,由B方块可知,晶体中的氧离子构成正八面
体空隙,故C错误;D.由分析可知,晶胞中含有8个 ,设晶胞的边长为anm,由晶胞的质量公式可
得: =10—21a3d,解得a= ,故D正确;故选C。
7.(2022·辽宁·渤海大学附属高级中学模拟预测)元素X的某价态离子Xn+中所有电子正好充满K、L、M
三个电子层,它与N3-形成晶体的晶胞结构如图所示。下列说法正确的是
A.X元素的原子序数是19
B.该晶体中阳离子与阴离子个数比为3 : 2
C.Xn+中n=1
D.晶体中每个Xn+周围有4个等距离且最近的N3-
【答案】C
【解析】A.从“元素X的某价态离子Xn+中所有电子正好充满K、L、M三个电子层”可以看出,Xn+共有
28个电子,A错误;B.图中Xn+位于每条棱的中点,一个晶胞拥有的Xn+个数为12× =3,N3-位于顶点,
一个晶胞拥有N3-的个数为8× =1,B错误;C.由于该物质的化学式为XN,故X显+1,C正确;D.由
3
图可知,晶体中每个Xn+周围有2个等距且最近的N3-,D错误;故选C。
8.(2022·广东·梅州市梅江区梅州中学模拟预测)如图为几种晶体或晶胞的结构示意图。下列说法错误的是
A.18g冰晶体中含有2mol氢键
B.在金刚石晶体中,碳原子与碳碳键个数的比为1∶2
C.碘单质是分子晶体,碘单质在 中比水中溶解度更大
D.金刚石、MgO、碘单质三种晶体的熔点顺序为:MgO>金刚石>碘单质
【答案】D
【解析】A.由图可知,1个水分子能形成4个氢键,每个氢键为2个水分子所共有,每个水分子含有4×
=2个氢键,所以18g冰晶体中含有氢键的物质的量为 ×2=2mol,故B正确;B.由晶胞结构可
知,在金刚石晶体中,每个碳原子与4个碳原子形成共价键,每个共价键为2个碳原子所共有,每个碳原
子形成的共价键为4× =2个,则碳原子与碳碳键个数的比为1:2,故B正确;C.碘单质是非极性分子
形成的分子晶体,在非极性有机溶剂中的溶解度大于在极性分子水中的溶解度,故C正确;D.金刚石是
原子晶体,熔点高于离子晶体氧化镁,故D错误;故选D。
9.(2022·湖北·襄阳五中模拟预测) (式量为M)是生物医药、太阳能电池等领域的理想荧光材料,
其晶胞结构如图所示,阿伏加德罗常数为 。已知:原子中运动的电子有两种相反的自旋状态,一种自
旋状态用 表示,与之相反的 表示,称为电子的自旋磁量子数。下列说法错误的是A. 的价层电子排布式为
B.基态S原子电子自旋磁量子数的代数和为1
C.若A点的分数坐标为 ,则B点的分数坐标为
D. 晶体的密度为
【答案】B
【解析】A. 位于第五周期ⅢA、核外电子排布式为 ,A正确;B. 基态S原子电子排布式为
,同一个轨道中电子自旋方向相反、电子自旋磁量子数的代数和为0, 中有2个p电子
位于同一个轨道、另2个电子分占两个p轨道且自旋方向相同,则电子自旋磁量子数的代数和为1或-1,B
不正确;C. 由晶胞示意图可知,若A点的分数坐标为 ,则B点的分数坐标为 ,C正确;
D.晶胞中Cu有8个位于顶点、4个面心、1个晶胞内,个数为8× +4× +1=4,In有4位于棱上、6个在
面心,个数为4× +6× =4,8个S位于晶胞内,则 晶体的密度为 ,D正确;答案选B。
10.(2022·北京·和平街第一中学三模)通过下列实验可从 的 溶液中回收 。
下列说法正确的是
A.通过过滤可将水溶液与 分离
B.回收的粗碘可通过升华进行纯化
C. 溶液与 反应的离子方程式:
D.向加酸后的上层清液中滴加 溶液生成 沉淀,1个 晶胞(见图)中含14个
【答案】B
【解析】I 的CCl 溶液加浓NaOH溶液,生成碘离子和碘酸根离子,分液后向水层溶液中加入稀硫酸,碘
2 4
离子和碘酸根离子又生成碘单质,过滤可以得到粗碘。A.CCl 和水溶液都能透过滤纸,不能用过滤的方
4
法将水溶液与 CCl 分离,故A错误;B.碘易升华,可以通过升华将粗碘纯化,故B正确;C.NaOH溶
4
液与I 反应的离子方程式为:3I+6OH-=5I-+ +3H O,故C错误;D.晶胞是晶体构成的基本结构单元,
2 2 2
I-位于晶胞的顶点和面心,顶点上的I-被8个晶胞共有,每个晶胞含有八分之一的I-,面心上的I-被2个晶
胞共有,每个晶胞含有二分之一的I-,所以1个AgI晶胞中含4个I-,故D错误;故选B。
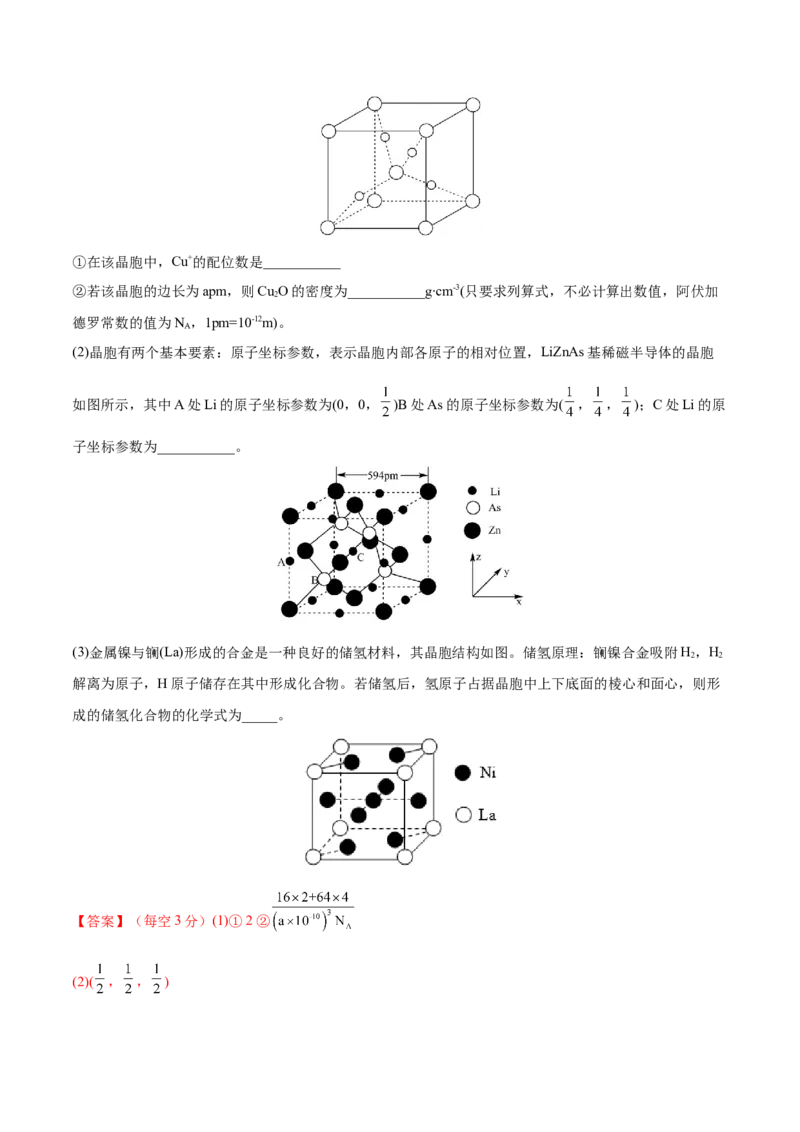
11.(2022·辽宁丹东·二模)硼及其化合物在材料制造、有机合成等方面应用广泛。图(a)为一种无限长单
链状结构的多硼酸根,图(b)硼氢化钠晶胞结构。N 代表阿伏伽德罗常数的值,下列说法正确的是
AA.图a中多硼酸根的化学式为
B.硼氢化钠晶体中 的配位数为4
C.图(a)中O-B-O的键角小于 中的H-B-H的键角
D.若硼氢化钠晶体的密度为ρg·cm-3,则a=
【答案】D
【解析】A.每个硼均摊两个O原子(除两端的B外),所以多硼酸根的化学式为 ,A项错误;
B. 以体内 看离它最近的Na+如图红色标注的离子共8个,则其配位数为
8,B项错误;C.a图中O-B-O为sp2杂化,键角为120°。而 为sp3杂化,键角为109°28′。键角前者大
于后者,C项错误;D.Na+分别为位于6个面上和4条棱上,则Na+为 ,则NaBH 为4个。
4由密度计算公式为 ,且 ,
, ,则D正确;答案选D。
12.(2022·湖北·模拟预测)铁有δ、γ、α三种同素异形体,如图所示,三种晶体在不同温度下能发生转
化。下列说法不正确的是
δ-Fe γ-Fe α-Fe
A.δ-Fe晶体中与每个铁原子等距离且最近的铁原子有8个
B.α-Fe晶体中与每个铁原子等距离且最近的铁原子有6个
C.δ-Fe晶胞中Fe原子数与α-Fe晶胞中Fe原子数之比为2:1
D.将铁加热到1500℃分别急速冷却和缓慢冷却,得到的晶体相同
【答案】D
【解析】A.由题图知,δ-Fe晶体中与每个铁原子等距离且最近的铁原子有8个,A正确;B.α-Fe晶体中
与每个铁原子等距离且最近的铁原子有6个,B正确;C.根据均摊法原则可知δ-Fe晶体中铁原子个数是
1+ =2,α-Fe晶胞中Fe原子数是 =1,则δ-Fe晶胞中Fe原子数与α-Fe晶胞中Fe原子数之比为2:
1,C正确;D.将铁加热后急速冷却和缓慢冷却,得到的晶体不同,D错误;答案为D。
二、主观题(共3小题,共40分)
13.(2022·山东泰安·三模)(12分)六方晶胞是一种常见晶胞,镁、锌和钛的常见晶胞属于六方晶胞。
(1)已知以上三种金属的盐的熔沸点(℃)如下表:
氯化物
物理性
质
熔点 712 290 -24.1沸点 1412 732 136.4
已知: 熔融状态下能够导电。请解释三种氯化物熔沸点差异的原因_______。 的熔沸点明显偏
低的另一个原因是该分子空间构型是_______,分子高度对称,没有极性,分子间作用力很弱。
(2)某晶体属于六方晶系,其晶胞参数 , 。晶胞沿着不同方向投影如下,其中深色
小球代表A原子,浅色大球代表B原子(化学环境完全等同)。已知A2原子坐标为 ,
B1原子沿c方向原子坐标参数 。
①该物质的化学式为_______。
②晶胞中原子A1—A2在ab面投影的距离为_______(保留四位有效数字)。
③B1原子坐标参数为_______。
【答案】(除标注外,每空2分)(1) 与 是离子晶体, 的晶格能大于 ; 属于
分子晶体,熔沸点比离子晶体低得多 正四面体
(2)① ②0.1407nm(3分) ③ (3分)
【解析】(1) 与 是离子晶体, 的晶格能大于 ;TiCl 常温下呈液态,可知其属于分
4
子晶体,熔沸点比离子晶体低得多。根据价层电子对互斥理论,TiCl 具有4对成键电子对,中心原子Ti发
4
生sp杂化,形成正四面体结构的分子。
(2)①A原子处于晶胞顶点,c棱中心和内部,计算1+1+6=8,而B原子完全处于晶胞内部(从a方向投影
图可看出),计量数为4,故化学式为AB。化学式在保证化学意义的前提下取最简整数比;
2
②从图易得晶胞顶点A原子的坐标参数为(0,0,0),棱上A原子的坐标参数为(0,0,0.5)。由A1
原子的坐标参数(1,0,0)和A2原子的坐标参数(0.8300,0.1700,0.2500),利用勾股定理和余弦定理
易得d=∣0.8300-1∣×0.4780nm=0.081260nm
a
d=∣0.1700-0∣×0.47800nm=0.081260nm
b
d=∣0.2500-0∣×0.7800nm=0.19500nm
c
d= nm=0.2405nm,晶胞
中原子A1—A2在ab面投影的距离为 ;
③两种对称性值得我们注意:晶胞的反演中心和z=0.2500=1/4处的镜面。由此易得B 原子的坐标参数为:
1
(1/3,2/3,0.0630)。
14.(2021·广东·模拟预测)(16分)硼(B)及其化合物在化学中有重要的地位。请回答下列问题:
(1)硼酸(H BO)是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
3 3
①硼酸中B原子的杂化轨道类型为_______。
②硼酸晶体中存在的作用力有范德华力和_______。
③加热时,硼酸的溶解度增大,主要原因是_______。
④硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的OH-而呈酸性。写出硼酸的电离方程式:_______。
(2)硼氢化钠(NaBH )是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表
4
示其反应原理:_______。[BH]-的空间构型是_______。
4
(3)B NH 可用来制造具有耐油、耐高温性能的特殊材料。写出它的一种等电子体物质的分子式:_______。
3 3 6
(4)硼化镁晶体在39 K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,如图是该晶体微观
结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为_______。
(5)金刚石的晶胞如图。立方氮化硼的结构与金刚石相似,已知晶胞边长为361.5 pm,则立方氮化硼的密度
是_______ g· cm-3。(只要求列算式,不必计算出数值,阿伏加德罗常数用N 表示)。
A【答案】(除标注外,每空2分)(1)①sp2(1分)
②氢键、共价键
③加热破坏了硼酸分子之间的氢键
④HBO+HO [B(OH) ]-+H+
3 3 2 4
(2)NaBH
4
+4H
2
O⇌=Na[B(OH)
4
]+4H
2
↑(或NaBH
4
+2H
2
O=NaBO
2
+4H
2
↑) 正四面体(1分)
(3)C H
6 6
(4)MgB
2
(5)
【解析】(1)①硼酸中,B的轨道杂化类型为sp2;
②硼酸晶体中,存在范德华力,还存在氢键和共价键;
③加热会破坏硼酸分子间的氢键,使得硼酸在热水中的溶解度更大;
④根据题意可得硼酸的电离方程式为: ;
(2) 根据题中信息可得,硼氢化钠和热水反应的化学方程式为:NaBH +4H O=Na[B(OH) ]+4H ↑(或
4 2 4 2
NaBH +2H O=NaBO+4H ↑);[BH]-的空间构型为正四面体;
4 2 2 2 4
(3)一个B NH 含有30个价电子和12个原子,一个C H 分子也含有30个价电子和12个原子,则B NH
3 3 6 6 6 3 3 6
的一种等电子体为C H;
6 6
(4)每个Mg周围有6个B,每个B周围有3个Mg,所以硼化镁的化学式为MgB ;
2
(5)晶胞中有4个B原子和4个N原子,则有a3·ρ·N =4M(BN),ρ= = 。
A
15.(2022·河南南阳·高三期末)(12分)回答下列问题:
(1)甲醛与新制Cu(OH) 加热可得砖红色沉淀Cu O,已知Cu O晶胞的结构如图所示:
2 2 2①在该晶胞中,Cu+的配位数是___________
②若该晶胞的边长为apm,则Cu O的密度为___________g∙cm-3(只要求列算式,不必计算出数值,阿伏加
2
德罗常数的值为N ,1pm=10-12m)。
A
(2)晶胞有两个基本要素:原子坐标参数,表示晶胞内部各原子的相对位置,LiZnAs基稀磁半导体的晶胞
如图所示,其中A处Li的原子坐标参数为(0,0, )B处As的原子坐标参数为( , , );C处Li的原
子坐标参数为___________。
(3)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构如图。储氢原理:镧镍合金吸附H,H
2 2
解离为原子,H原子储存在其中形成化合物。若储氢后,氢原子占据晶胞中上下底面的棱心和面心,则形
成的储氢化合物的化学式为_____。
【答案】(每空3分)(1)①2 ②
(2)( , , )(3)
【解析】(1)①大白球位于顶点和体心,个数为 =2,小白球位于晶胞内部,有4个,根据氧化亚铜
的化学式,小白球为Cu+,大白球为O2-,根据晶胞图,Cu+的配位数为2;故答案为2;
②晶胞的质量为 g,晶胞的体积为(a×10-10)3cm3,则晶胞的密度为 g/cm3,故
答案为 ;
(2)根据晶胞图以及所给原子坐标可知,C位于晶胞体心,则Li的原子坐标参数为( , , );故答案为(
, , );
(3)Ni位于晶胞面和体心,个数为 =5,La位于顶点,个数为 =1,H原子位于上下底面的棱心
和面心,个数为 =3,化学式为LaNiH;故答案为LaNiH;
5 3 5 3