文档内容
考点 02 物质的量 气体摩尔体积
(核心考点精讲)
一、3年真题考点分布
考点内容 考题统计
2023辽宁卷5题,3分;2023全国甲卷10题,6分;2023浙江6月7题,3
分;2022福建卷5题,4分;2022重庆卷5题,32分;2022全国甲卷11题,6
分;2022浙江6月12题,2分;2022浙江1月12题,2分;2022海南卷7
阿伏加德罗常
题,3分;2022辽宁卷3题,3分;2021全国甲卷8题,6分;2021浙江6月
数
18题,2分;2021湖南卷5题,3分;2021河北卷7题,3分;2021广东卷11
题,4分;2021天津卷7题,4分;2021浙江1月18题,2分;2021湖北卷6
题,3分;2021海南卷7题,3分
阿伏加德罗定
2021年山东卷6题,3分
律
二、命题规律及备考策略
【命题规律】
分析近几年高考试题,有关化学计量主要体现在单独考查 N 及化学计算中。选择题常与电离平衡、
A
氧化还原反应、化学反应中的能量变化等考点结合进行考查;填空题保持实验题、反应原理题等融合,涉
及物质的量及阿伏加德罗定律的灵活运用。
【备考策略】
1.了解物质的量及其单位、摩尔质量、气体摩尔体积、物质的量浓度、阿伏伽德罗常数的含义;
2.能根据微粒(原子、分子、离子等)物质的量、数目、气体体积(标准状况下)之间的相互关系进行有
关计算;
3.正确判断有关阿伏加德罗常数正误的“三大步骤”
第一步:查看物质的状态及所处状况——正确运用气体摩尔体积的前提;
第二步:分析题干所给物理量与物质的量的关系——正确进行换算的前提;
第三步:准确把握物质的微观结构和物质变化过程中微粒数目的变化——正确判断微粒数目的前提。
【命题预测】
预计2024年依旧关注N 考查的常见角度,如物质结构、氧化还原反应、盐类水解、有机物结构等;
A
填空题中往往渗透于化学平衡计算、物质的组成或含量的计算,充分利用化学计算技法,如守恒法、关系
式法等。
资料收集整理【淘宝店铺:向阳百分百】考法 1 物质的量
1.物质的量(n)
表示含有一定数目粒子的集合体的物理量,单位为摩尔(mol)。
2.物质的量的规范表示方法:
(1)用mol为单位只能用于物质的微观粒子,如分子、原子、离子或它们的特定组合。不能用于宏观物
质。
(2)用mol为单位必须指明物质微粒(或微粒组合)的符号。
3.阿伏加德罗常数(N )
A
0.012 kg 12C中所含的碳原子数为阿伏加德罗常数,其数值约为 6.02×1023,单位为mol-1。公式:N
A
=。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)摩尔是物质的量的单位( )
(2)1 mol NaCl和1 mol HCl含有相同的粒子数目( )
(3)1 mol任何物质都含有6.02×1023个分子( )
(4)1 mol水中含有2 mol氢和1 mol氧( )
(5)阿伏加德罗常数(N )就是6.02×1023( )
A
(6)0.012 kg 12C中约含有6.02×1023个碳原子( )
答案:(1)√ (2)√ (3)× (4)× (5)× (6)√
资料收集整理【淘宝店铺:向阳百分百】例1 “物质的量”是国际单位制中的一个基本物理量,下列有关说法正确的是( )
A.质量相等的CO和CO,物质的量之比为2∶3
2
B.2 mol氧气的摩尔质量为62 g·mol-1
C.1 mol任何物质都含有6.02×1023个分子
D.2 g H 含有1 mol氢分子
2
【答案】D
【解析】设质量均为m,则n(CO)∶n(CO)=∶=11∶7,A错误;摩尔质量的单位是g·mol-1,数值上等
2
于物质的相对分子(原子)质量,B错误;1 mol任何物质都约含有6.02×1023个微粒,不一定是分子,也有可
能是离子或原子,C错误;2 g H 的物质的量是1 mol,含有1 mol氢分子,D正确。
2
例2 下列关于物质的量的叙述,错误的是( )
A.1molNe中含有10×6.02×1023个电子
B.0.012 kg 12C含有约6.02×1023个C
C.1molH O中含有2mol氢原子和1mol氧原子
2
D.1mol任何物质都含有 个分子
【答案】D
【解析】A项,1个氖原子核外有10个电子,则1 mol Ne中含有10×6.02×1023个电子, A正确;B项,
0.012 kg 12C的物质的量为1mol,则含有约6.02×1023个C原子,B正确;C项,一个水分子中含两个氢原
子和一个氧原子,因此1molH O中含有2molH和1molO,C正确;D项,因为有些物质是由分子构成的
2
(例如水、硫酸等),有些物质是由离子构成的[例如NaCl、Ca(OH) 等],还有些物质是由原子直接构成的
2
(例如金刚石等),所以不是1mol 任何物质都含有6.02×1023个分子,D错误;故选D。
对点1 下列关于物质的量及粒子数的叙述,正确的是( )
A.1 mol任何物质都含有6.02×1023个分子
B.0.012 kg12 C中含有约6.02×1023个12C
C.1 mol CO 中含有1 mol碳和2 mol氧
2
D.1 mol H含有6.02×1024个质子
【答案】B
【解析】1 mol任何粒子都约含有6.02×1023个粒子,不一定为分子,A项错误;0.012 kg 12C中含有约
6.02×1023个12C,B项正确;1 mol CO 中含有 1 mol 碳原子和 2 mol 氧原子,C项错误;1 mol H 含有
2
6.02×1023个质子,D项错误。
对点2 下列结论中,正确的是( )
资料收集整理【淘宝店铺:向阳百分百】A.摩尔是七个基本物理量之一 B.每摩尔物质都含有N 个指定粒子
A
C.1 mol H就是指1 mol氢 D.18 g HO中含有6.02×1023个原子
2
【答案】B
【解析】A项,物质的量是七个基本物理量之一,摩尔是其单位,故A错误;B项,使用摩尔时必须
指明物质微粒的名称或符号或化学式的特定组合,每摩尔物质都含有N 个指定组成粒子,故B正确;C项,
A
1 mol H表示1摩尔氢原子,但如果说“1摩尔氢”就违反了使用准则,因为“氢”是元素名称,不是微粒
名称,也不是微粒的符号或化学式,不符合上述要求,故C错误;D项,18 g HO就是1 mol H O,一个水
2 2
分子中含有2个H原子和1个O原子,故18 g HO中应含有3 mol原子,即3×6.02×1023个原子,故D错误;
2
故选B。
考法 2 摩尔质量
1.定义:单位物质的量的物质所具有的质量,其符号为M,单位为g·mol-1。
2.数值:以g·mol-1为单位时,任何粒子的摩尔质量在数值上等于该微粒的相对分子(或原子)质量。
3.摩尔质量与物质的量、物质的质量之间的关系:n=。
4.求气体摩尔质量M的常用方法
(1)根据物质的质量(m)和物质的量(n):M=m/n。
(2)根据一定质量(m)的物质中微粒数目(N)和阿伏加德罗常数(N ):M=N ·m/N。
A A
(3)根据标准状况下气体的密度ρ:M=ρ×22.4(g·mol-1)。
(4)根据气体的相对密度(D=ρ/ρ):M/M=D。
1 2 1 2
(5)对于混合气体,求其平均摩尔质量,上述计算式仍然成立;还可以用下式计算:M=M×a%+
1
M×b%+M×c%……,a%、b%、c%……指混合物中各成分的物质的量分数(或体积分数)。
2 3
摩尔质量与相对原子(分子)质量是两个不同的概念,当摩尔质量以g·mol-1为单位时,二者在数值上
相等。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)硫酸的摩尔质量为98 g( )
(2)2 mol H O是1 mol H O摩尔质量的2倍( )
2 2
(3)NaOH的摩尔质量为40 g( )
(4)1 mol O 的质量与它的相对分子质量相等( )
2
(5)1 mol OH-的质量为17 g·mol-1( )
资料收集整理【淘宝店铺:向阳百分百】(6)氖气的摩尔质量(单位g·mol-1)在数值上等于它的相对原子质量( )
(7)2 mol H O的摩尔质量是1 mol H O的摩尔质量的2倍( )
2 2
(8)相同质量的CO与N 所含分子数、原子数均相同( )
2
(9)17 g —OH与17 g OH-所含电子数均为10N ( )
A
(10)31 g白磷中所含共价键数目为N ( )
A
(11)30 g SiO 中含有硅氧键个数为N ( )
2 A
(12)32 g甲醇中所含共价键数目为5N ( )
A
答案:(1) × (2)× (3)× (4)× (5)× (6)√ (7)× (8) √ (9)× (10)× (11)× (12)√
例1 下列叙述中正确的是( )
A.镁的原子质量就是镁的相对原子质量
16
g
B.一个氧原子的实际质量约等于
6.02×1023
C.水的相对分子质量等于18g
D.二氧化硫的摩尔质量是64g
【答案】B
【解析】相对原子质量是比值,不是原子的实际质量,故A不正确;1mol氧原子的实际质量是16g,
16
g
故一个氧原子的质量为
6.02×1023
,所以B正确;相对分子质量的单位是1,不是g,所以C错误;摩尔
质量的单位为g·mol-1,所以D也是错的。
例2 科学家屠呦呦因发现青蒿素和双氢青蒿素治疗疟疾的新疗法而获得诺贝尔生理学或医学奖。双
氢青蒿素的化学式为C H O,相对分子质量为284。下列关于双氢青蒿素的说法正确的是( )
15 24 5
A.N 个双氢青蒿素的质量为284 g·mol-1
A
B.均为N 的C、H、O三种原子的质量比6∶1∶8
A
C.14.2 g双氢青蒿素中含有的原子总数为2.2N
A
D.含有N 个碳原子的双氢青蒿素的物质的量为1 mol
A
【答案】C
【解析】质量的单位是 g,不是g·mol-1,A错误;当摩尔质量的单位是 g·mol-1时,均为N 个C、
A
H、O三种原子的物质的量为1 mol,分别乘以各自的摩尔质量12 g·mol-1、1 g·mol-1、16 g·mol-1,得到
质量比12∶1∶16,B错误;14.2 g双氢青蒿素的物质的量是14.2 g÷284 g·mol-1=0.05 mol,由于在一个分子
中含有的原子个数是44个,所以0.05 mol双氢青蒿素中含有的原子的总数为2.2N ,C正确;一个双氢青
A
蒿素的分子中含有15个碳,含有N 个碳原子的双氢青蒿素的物质的量为1 mol÷15≈0.067 mol,D错误。
A
资料收集整理【淘宝店铺:向阳百分百】对点1 我国神舟系列火箭使用的一种燃料是偏二甲肼(C HN),反应的化学方程式为C HN+2N O
2 8 2 2 8 2 2 4
3N+2X+4H O,下列有关叙述正确的是( )。
2 2
A.偏二甲肼的摩尔质量为60 g
B.标准状况下,生成X和HO的体积之比为1∶2
2
C.X的化学式为CO
2
D.常温下,6 g C HN 完全反应产生6.72 L N
2 8 2 2
【答案】C
【解析】偏二甲肼的相对分子质量为60,则其摩尔质量为60 g·mol-1,A项错误;标准状况下,二氧
化碳是气态,水不是气态,二者无法比较体积,B项错误;由质量守恒定律可得,X的化学式是CO ,C
2
项正确;常温下,气体摩尔体积不是22.4 L·mol-1,D项错误。
对点2 光纤通讯是一种现代化的通讯手段,光纤通讯容量大,一对光纤上可同时传送3万门电话的
信号。制造光导纤维的主要原料是SiO 下列关于SiO 的说法正确的是( )
2, 2
A.SiO 摩尔质量是60 B.1 mol SiO 中含有1 mol O
2 2 2
C.1.5mol SiO 中含有1.806×1024个氧原子 D.1 mol SiO 质量是60 g mol-1
2 2
【答案】C
【解析】A项,摩尔质量有单位,单位为g/mol,所以SiO 摩尔质量是60g/mol,故A错误;B项,1
2
mol SiO 含有2molO原子,不存在氧气分子,故B错误;C项,1.5mol SiO 中含有3mol氧原子,其个数为
2 2
3mol×6.02×1023mol-1=1.806×1024,故C正确;D项,质量的单位是g,1 mol SiO 质量是1 mol×60gmol-1=60g
2
,故D错误;故选C。
考法 3 气体摩尔体积
1.影响物质体积的因素
2.气体的摩尔体积
(1)定义:单位物质的量的气体所占的体积。用符号V 表示,常用的单位为L·mol-1。
m
(2)数值:在标准状况下(273 K和101 kPa时),气体摩尔体积才是22.4 L·mol-1,在非标准状况下,1
mol气体的体积可能是22.4 L,也可能不是22.4 L,因此,在使用气体摩尔体积时,一定要看清气体所处的
状况。
(3)公式:V =。
m
资料收集整理【淘宝店铺:向阳百分百】3.阿伏加德罗定律及其推论
(1)阿伏加德罗定律:在相同的温度和压强下,相同体积的任何气体,含有相同数目的粒子(或气体的
物质的量相同)。
(2)阿伏加德罗定律的推论
相同条件 推论公式 语言叙述
T 、 p 相
= 同温、同压下,气体的体积与其物质的量成正比
同
T、V 相
= 温度、体积相同的气体,其压强与其物质的量成正比
同
T 、 p 相 同温、同压下,气体的密度与其摩尔质量(或相对分子质
=
同 量)成正比
1.气体摩尔体积使用的对象是气体;标准状况是0 ℃、1.01×105 Pa,不是常温、常压。
2.在标准状况下,气体摩尔体积约为22.4 L·mol-1,非标准状况下,气体摩尔体积一般不是22.4
L·mol-1。
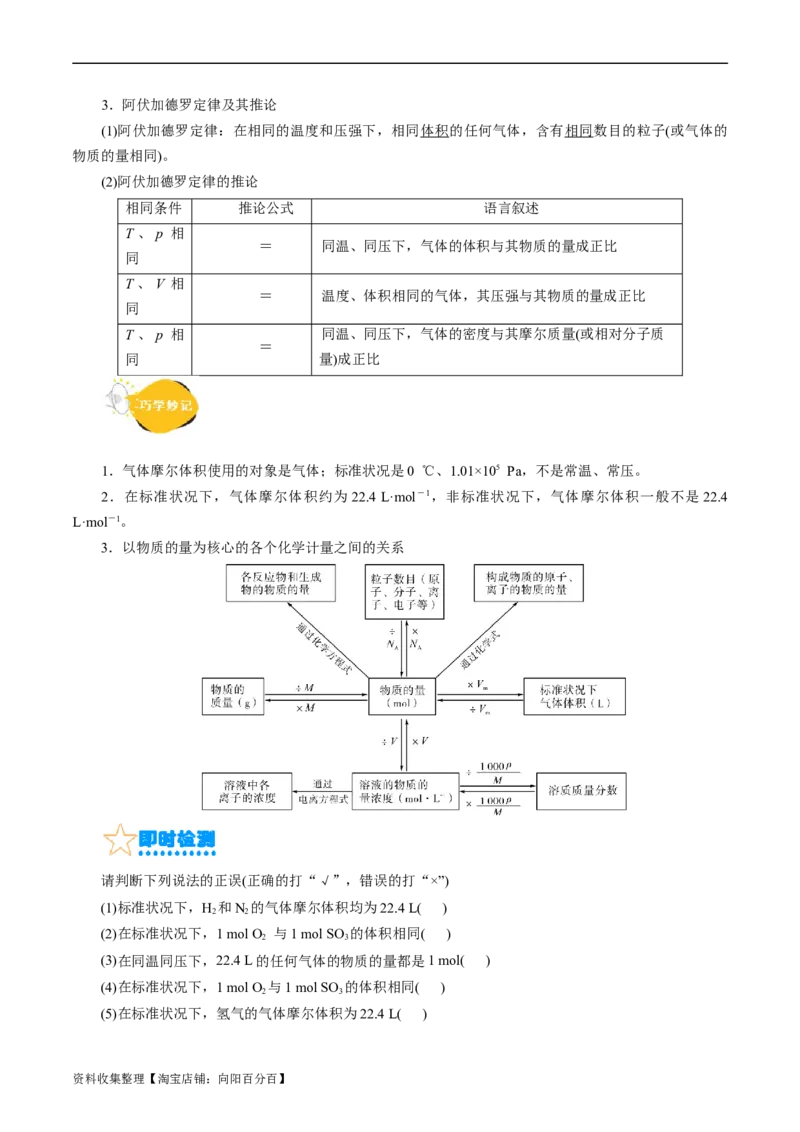
3.以物质的量为核心的各个化学计量之间的关系
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)标准状况下,H 和N 的气体摩尔体积均为22.4 L( )
2 2
(2)在标准状况下,1 mol O 与1 mol SO 的体积相同( )
2 3
(3)在同温同压下,22.4 L的任何气体的物质的量都是1 mol( )
(4)在标准状况下,1 mol O 与1 mol SO 的体积相同( )
2 3
(5)在标准状况下,氢气的气体摩尔体积为22.4 L( )
资料收集整理【淘宝店铺:向阳百分百】