文档内容
考点 11 镁、铝及其重要化合物
1.3年真题考点分布
考点分布
年份 卷区 铝及其化合物的性
镁及其化合物的性质 海水提镁 综合应用
质
北京 √
2022 湖南 √
浙江 √ √
湖北 √ √ 湖北
湖南 √
2021
福建 √
浙江 √ √
浙江 √ √
2020
江苏 √
2.命题规律及备考策略
【命题规律】近3年新高考卷对于该专题主要考查:
1.镁及其化合物的性质及应用
2.海水提镁
3.铝及其化合物的性质及应用
4.铝土矿炼铝
【备考策略】熟练掌握镁、铝及其化合物之间的转化关系,熟悉各物质的特特殊性质及其应用;明确元素化合
物和化学反应原理、物质结构和性质之间的联系。
【命题预测】镁、铝及其化合物的性质多与日常生活、生产中的应用有关,高考题型有选择题、实验题、化学
工艺流程题等。选择题重点考查化学方程式、离子方程式、离子共存、物质鉴别、物质制取等,非选择题中常
借助工艺流程的形式,以除杂或提纯等相关问题为主线综合考查金属元素化合物的性质。
考法 1 镁及其化合物的性质
1.镁的物理性质
(1)镁:镁是________色有金属光泽的固体,密度较________,硬度较________,有延展性,是电和热的良
导体。
(2)镁合金:密度较________,硬度和强度都较________。
2.镁及其化合物的化学性质
物质 主要性质 反应方程式
与O 反应 ________________________________
2
镁 与N 反应 ________________________________
2
与CO 反应 ________________________________
2
资料收集整理【淘宝店铺:向阳百分百】与非氧化性强酸反应 ________________________________
与沸水反应 ________________________________
氧化镁 碱性氧化物 ________________________________
中强碱 ________________________________
氢氧化镁 难溶于水 ________________________________
溶解度小于碳酸镁 ________________________________
【典例1】(2022·张家口高三上学期期中)下列有关镁及其化合物的离子方程式书写正确的是( )。
A.MgCO 与盐酸反应:CO2-+2H+ CO↑+2H O
3 3 2 2
B.Mg(OH) 与HSO 反应:Mg2++2OH-+2H++SO2- MgSO ↓+2H O
2 2 4 4 4 2
C.碳酸氢镁与足量的氢氧化钠溶液反应:Mg2++2HCO-+2OH- MgCO ↓+CO 2-+2H O
3 3 3 2
D.工业上以海水为原料制取Mg(OH):Ca(OH)+Mg2+ Mg(OH)↓+Ca2+
2 2 2
【思维拓展】镁的化合物间的重要转化关系
1.MgN 的结构和性质
3 2
(1)MgN 的电子式:
3 2
(2)水解反应:MgN+6HO 3Mg(OH)↓+2NH ↑
3 2 2 2 3
(3)与酸反应
①少量盐酸:MgN+6HCl 3MgCl +2NH ↑
3 2 2 3
②过量盐酸:MgN+8HCl 3MgCl +2NH Cl
3 2 2 4
2.镁的化合物间的重要转化关系
(1)某些镁盐加热蒸干、灼烧的产物
①MgCl Mg ( OH ) MgO
2 2
②Mg(NO ) Mg ( OH ) MgO
3 2 2
③MgSO Mg SO
4 4
④Mg(HCO ) MgCO Mg ( OH ) MgO
3 2 3 2
(2)惰性电极电解某些镁的化合物
①MgCl 溶液:MgCl +2H O Mg ( OH ) ↓ +C l ↑ +H ↑
2 2 2 2 2 2
②熔融MgCl :MgCl Mg+Cl↑(工业上炼镁原理)
2 2 2
③熔融MgO: 2 MgO 2Mg+O ↑(耗能多,不适于炼镁)
2
3.碳酸镁转化成氢氧化镁
(1)转化的实质:沉淀的转化
①MgCO +HO Mg ( OH ) +CO ↑
3 2 2 2
②MgCO +2OH- Mg ( OH ) +CO 2-
3 2 3
(2)转化的原因:MgCO 的溶解度比Mg(OH) 的大
3 2
(3)转化的应用:Mg(HCO ) 溶液与NaOH溶液的反应
3 2
①少量NaOH: Mg ( HCO ) + 2 NaOH Mg ( OH ) ↓+2 Na H CO
3 2 2 3
②少量NaOH: Mg ( HCO ) + 4 NaOH Mg ( OH ) ↓+2Na CO + 2 H O
3 2 2 2 3 2
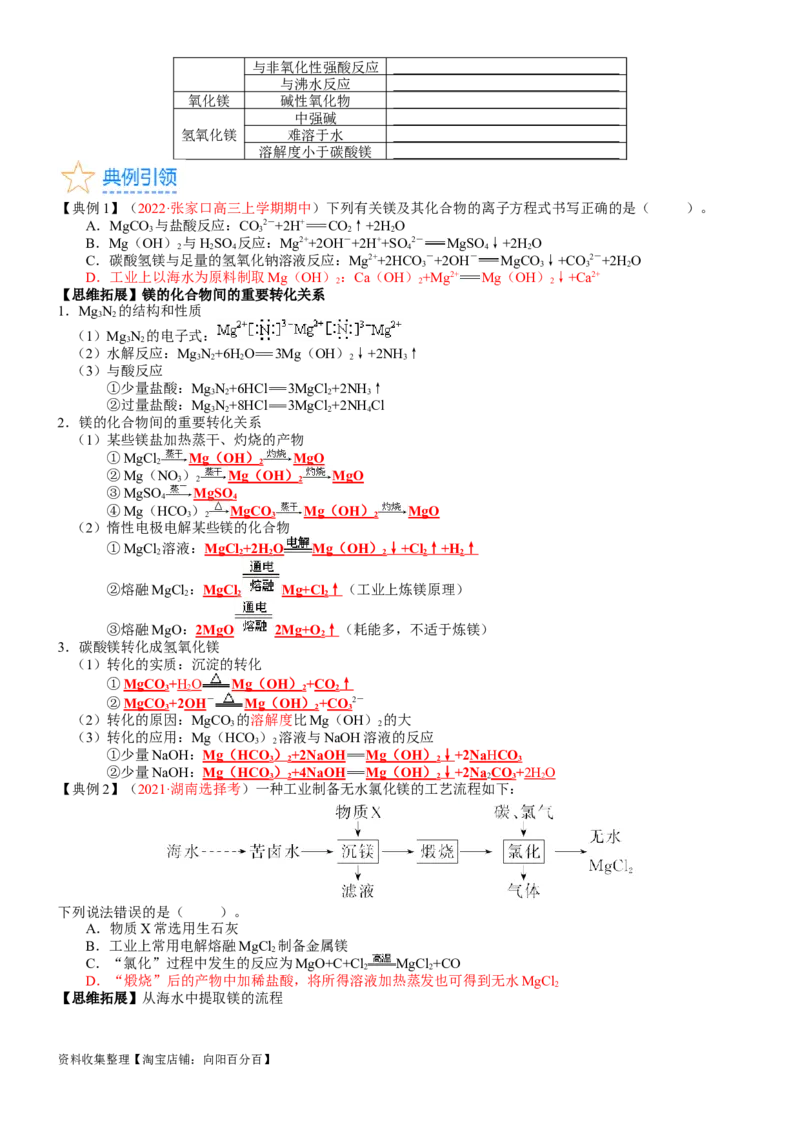
【典例2】(2021·湖南选择考)一种工业制备无水氯化镁的工艺流程如下:
下列说法错误的是( )。
A.物质X常选用生石灰
B.工业上常用电解熔融MgCl 制备金属镁
2
C.“氯化”过程中发生的反应为MgO+C+Cl MgCl +CO
2 2
D.“煅烧”后的产物中加稀盐酸,将所得溶液加热蒸发也可得到无水MgCl
2
【思维拓展】从海水中提取镁的流程
资料收集整理【淘宝店铺:向阳百分百】2.主要化学反应
(1)制取石灰乳:CaCO CaO+CO ↑、CaO+H O=Ca(OH)
3 2 2 2
(2)沉淀Mg2+:Mg2++Ca(OH)=Mg(OH)+Ca2+
2 2
(3)提取MgCl :Mg(OH)+2HCl=MgCl +2H O
2 2 2 2
(4)制氯化镁晶体:MgCl +6H O MgCl ·6H O
2 2 2 2
(5)氯化镁晶体脱水:MgCl ·6H O MgCl +6H O
2 2 2 2
(6)制金属镁:MgCl (熔融) Mg+Cl ↑
2 2
3.重要操作
(1)从MgCl 溶液中获取晶体的操作
2
①基本操作:加热浓缩、冷却结晶、过滤洗涤、干燥称量
②基本仪器:酒精灯、烧杯、玻璃棒、漏斗、干燥器、天平
(2)氯化镁晶体脱水HCl的作用
①带走部分水蒸气,减少MgCl 的水解
2
② 抑制 MgC l 的水解,得到无水 MgC l
2 2
(3)制金属镁加入少量CaCl 的作用: 降低 MgC l 的 熔点 , 节能
2 2
3.原料
(1)直接原料:海水、贝壳和盐酸
(2)间接原料:氢气
(3)循环利用:氯气
4.海水提镁过程中应该注意的问题
(1)制取Mg(OH) 沉淀时,所用的试剂是廉价的熟石灰,而不是NaOH。
2
(2)海水提镁,可以用提取食盐剩下的苦卤,因为Mg2+得到了富集,浓度大。
(3)由MgCl ·6HO晶体脱水制无水MgCl 时,MgCl ·6HO晶体在HCl气氛中加热脱水,防止MgCl 和
2 2 2 2 2 2
HO反应生成Mg(OH) 沉淀。
2 2
(4)因为海水提镁用的是石灰乳,不是澄清石灰水,所以反应MgCl +Ca(OH)=CaCl +Mg(OH)↓的
2 2 2 2
离子方程式应该写成Mg2++Ca(OH)=Ca2++Mg(OH)↓的形式。
2 2
(5)制备单质镁时所用的方法是电解熔融的氯化镁,而不是电解氯化镁溶液,也不是电解熔融的氧化镁。
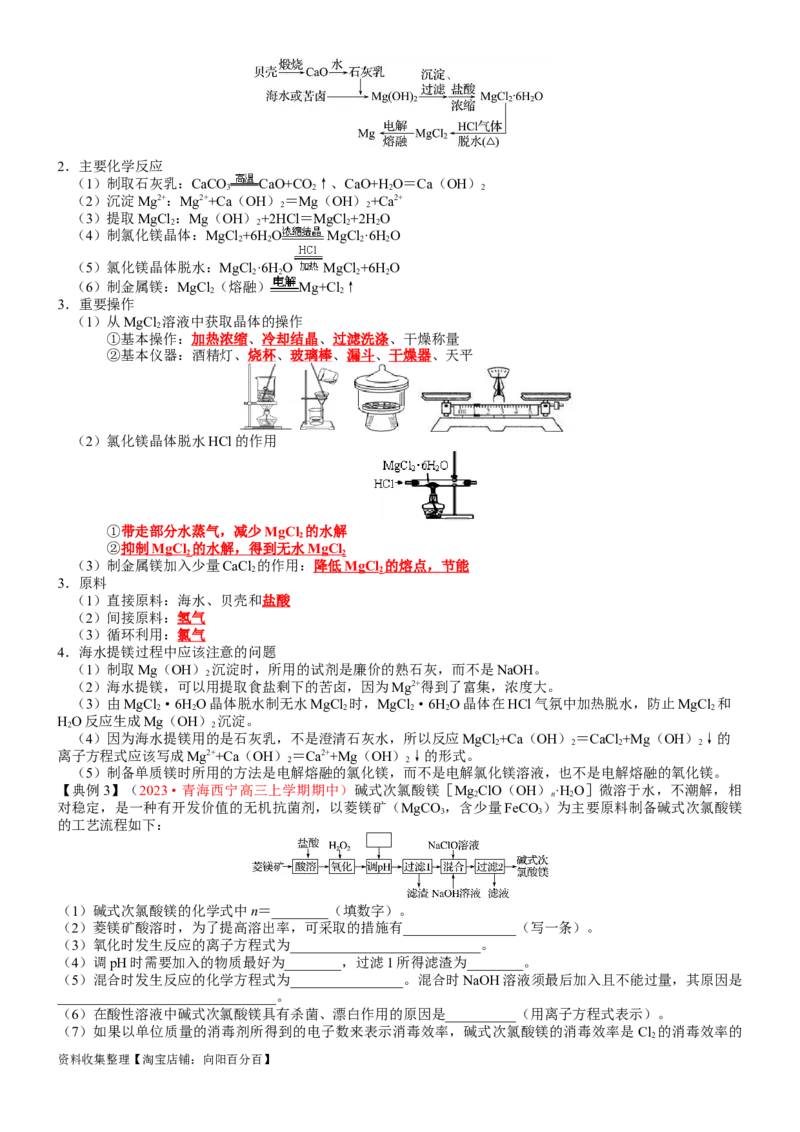
【典例3】(2023·青海西宁高三上学期期中)碱式次氯酸镁[MgClO(OH) ·H O]微溶于水,不潮解,相
2 n 2
对稳定,是一种有开发价值的无机抗菌剂,以菱镁矿(MgCO ,含少量FeCO )为主要原料制备碱式次氯酸镁
3 3
的工艺流程如下:
(1)碱式次氯酸镁的化学式中n=________(填数字)。
(2)菱镁矿酸溶时,为了提高溶出率,可采取的措施有________________(写一条)。
(3)氧化时发生反应的离子方程式为___________________________。
(4)调pH时需要加入的物质最好为________,过滤1所得滤渣为________。
(5)混合时发生反应的化学方程式为________________。混合时NaOH溶液须最后加入且不能过量,其原因是
_______________________________。
(6)在酸性溶液中碱式次氯酸镁具有杀菌、漂白作用的原因是__________(用离子方程式表示)。
(7)如果以单位质量的消毒剂所得到的电子数来表示消毒效率,碱式次氯酸镁的消毒效率是 Cl 的消毒效率的
2
资料收集整理【淘宝店铺:向阳百分百】________。
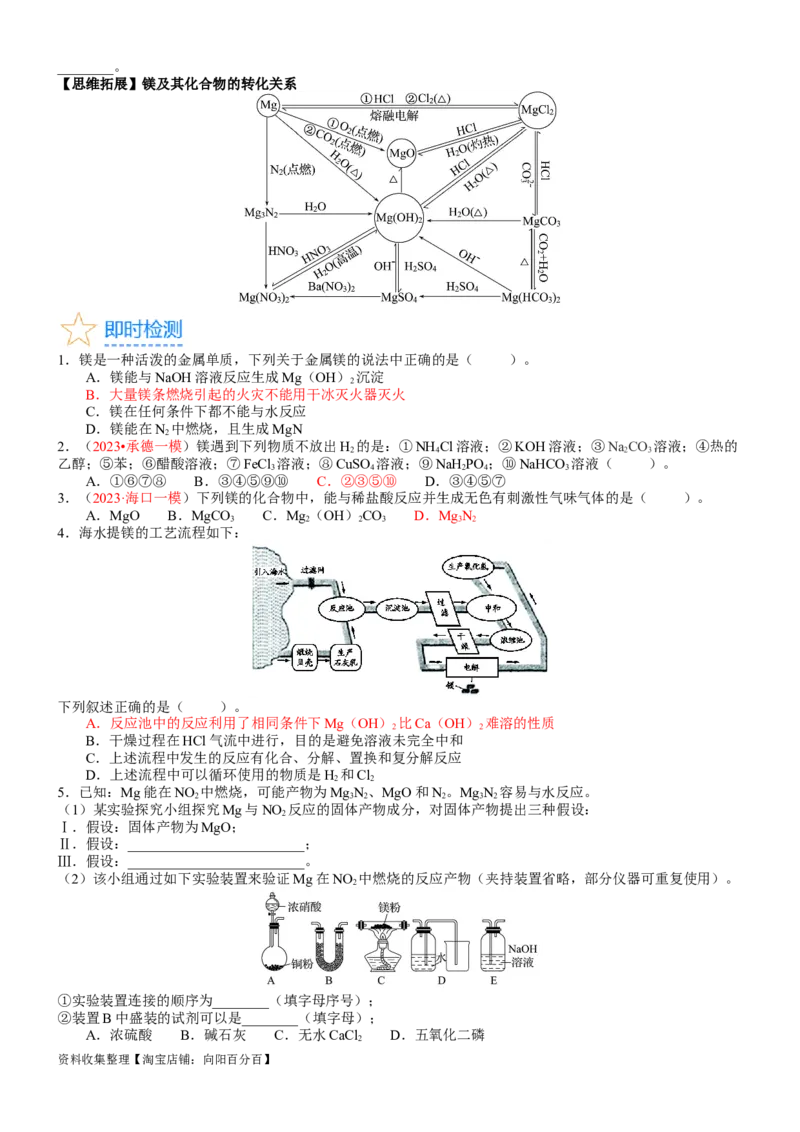
【思维拓展】镁及其化合物的转化关系
1.镁是一种活泼的金属单质,下列关于金属镁的说法中正确的是( )。
A.镁能与NaOH溶液反应生成Mg(OH) 沉淀
2
B.大量镁条燃烧引起的火灾不能用干冰灭火器灭火
C.镁在任何条件下都不能与水反应
D.镁能在N 中燃烧,且生成MgN
2
2.(2023•承德一模)镁遇到下列物质不放出H 的是:①NH Cl溶液;②KOH溶液;③NaCO 溶液;④热的
2 4 2 3
乙醇;⑤苯;⑥醋酸溶液;⑦FeCl 溶液;⑧CuSO 溶液;⑨NaH PO ;⑩NaHCO 溶液( )。
3 4 2 4 3
A.①⑥⑦⑧ B.③④⑤⑨⑩ C.②③⑤⑩ D.③④⑤⑦
3.(2023·海口一模)下列镁的化合物中,能与稀盐酸反应并生成无色有刺激性气味气体的是( )。
A.MgO B.MgCO C.Mg(OH)CO D.MgN
3 2 2 3 3 2
4.海水提镁的工艺流程如下:
下列叙述正确的是( )。
A.反应池中的反应利用了相同条件下Mg(OH) 比Ca(OH) 难溶的性质
2 2
B.干燥过程在HCl气流中进行,目的是避免溶液未完全中和
C.上述流程中发生的反应有化合、分解、置换和复分解反应
D.上述流程中可以循环使用的物质是H 和Cl
2 2
5.已知:Mg能在NO 中燃烧,可能产物为MgN、MgO和N。MgN 容易与水反应。
2 3 2 2 3 2
(1)某实验探究小组探究Mg与NO 反应的固体产物成分,对固体产物提出三种假设:
2
Ⅰ.假设:固体产物为MgO;
Ⅱ.假设:_________________________;
Ⅲ.假设:_________________________。
(2)该小组通过如下实验装置来验证Mg在NO 中燃烧的反应产物(夹持装置省略,部分仪器可重复使用)。
2
①实验装置连接的顺序为________(填字母序号);
②装置B中盛装的试剂可以是________(填字母);
A.浓硫酸 B.碱石灰 C.无水CaCl D.五氧化二磷
2
资料收集整理【淘宝店铺:向阳百分百】③确定产物中有N 生成的实验现象为___________________________。
2
(3)设计实验证明:产物中存在MgN:___________________________。
3 2
(4)已知装置C中初始加入Mg粉质量为13.2g,在足量的NO 中充分燃烧,实验结束后,硬质玻璃管冷却至
2
室温、称量,测得硬质玻璃管中剩余固体的质量为21.0g,产生N 的体积为1120mL(标准状况)。写出玻璃管
2
中发生反应的化学方程式:___________________________。
考法 2 铝 的性质
1.铝的结构、存在
(1)原子结构示意图:__________。
(2)在周期表中的位置:第_____周期第_____族
(3)存在形态:铝是地壳中含量_____的金属元素,全部以_____形式存在。
2.物理性质
颜色 状态 密度 质地 延展性、导电性、传热性
_____色、有金属光泽 固体 较小 柔软 良好
3.化学性质
写出图中有关反应的化学方程式或离子方程式:
①常温下铝具有_____性(表面形成致密的氧化膜),点燃条件下剧烈燃烧,放出耀眼的白光
②_________________________
③铝常温下遇到浓硫酸和浓硝酸发生_____;遇稀盐酸放氢气:____________________
④___________________________________或 2Al+2NaOH+2H O 2NaAlO +3H ↑
2 2 2
⑤_________________________
3.制备和用途
(1)铝的冶炼:____________________。
(2)铝的用途:纯铝用作导线,铝合金用于制造汽车、飞机、生活用品等。
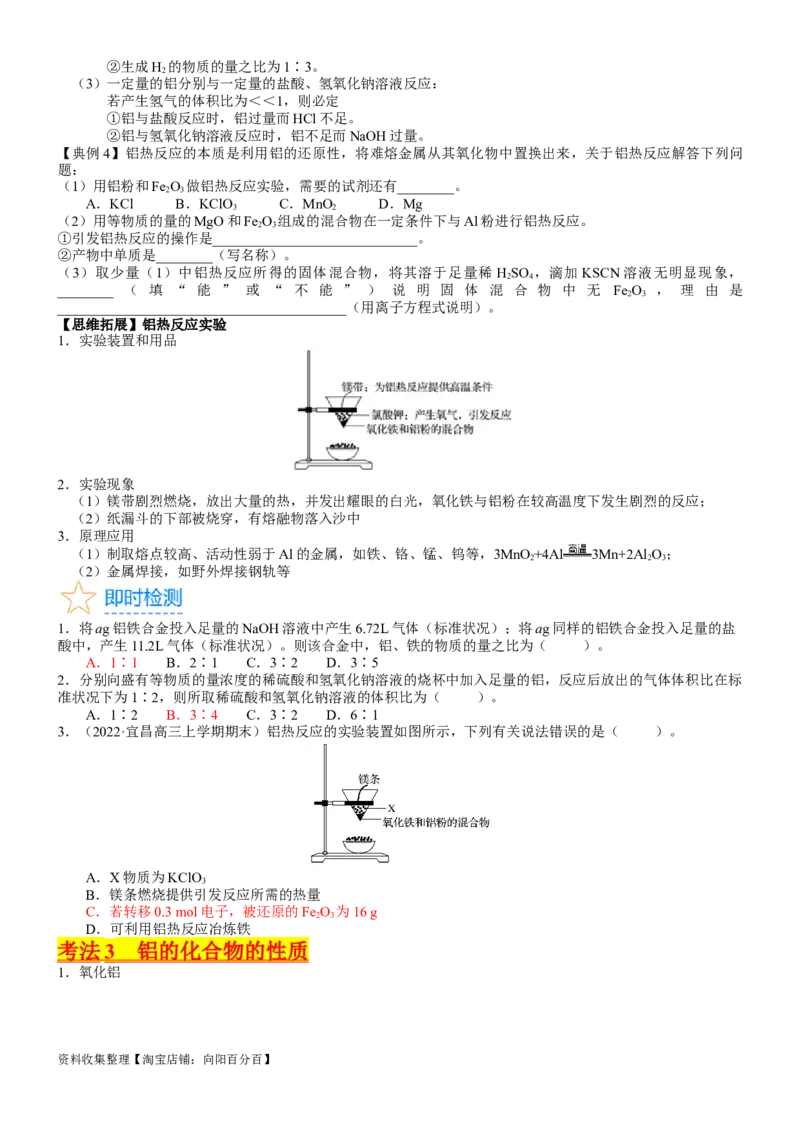
【典例3】(2023·阜阳模拟)根据如图的转化关系判断,下列说法正确的是(反应条件已略去)( )。
A.生成等质量H 时,①和②反应消耗n(HCl)=n(NaOH)
2
B.反应③中氧化剂与还原剂的物质的量之比为2∶3
C.反应③和④消耗等量的Al时,生成的n(Cu)∶n(Fe)=3∶2
D.等浓度等体积的稀HCl和NaOH溶液与足量Al反应,①②生成H 的分子数之比为3∶1
2
【思维拓展】铝与酸或碱反应生成H 的量的关系
2
1.依据的化学方程式
2Al+6HCl=2AlCl +3H ↑
3 2
2Al+2NaOH+6H O=2Na[Al(OH)]+3H ↑或2Na+4HO+2Al=2NaAlO +4H ↑
2 4 2 2 2 2
2.反应规律
(1)等质量的铝与足量的盐酸、氢氧化钠溶液分别反应:
①产生H 的物质的量相等。
2
②消耗H+、OH-的物质的量之比为n(H+)∶n(OH-)=3∶1。
(2)足量的铝分别与等物质的量的HCl和NaOH反应:
①消耗Al的物质的量之比为1∶3。
资料收集整理【淘宝店铺:向阳百分百】②生成H 的物质的量之比为1∶3。
2
(3)一定量的铝分别与一定量的盐酸、氢氧化钠溶液反应:
若产生氢气的体积比为<<1,则必定
①铝与盐酸反应时,铝过量而HCl不足。
②铝与氢氧化钠溶液反应时,铝不足而NaOH过量。
【典例4】铝热反应的本质是利用铝的还原性,将难熔金属从其氧化物中置换出来,关于铝热反应解答下列问
题:
(1)用铝粉和Fe O 做铝热反应实验,需要的试剂还有________。
2 3
A.KCl B.KClO C.MnO D.Mg
3 2
(2)用等物质的量的MgO和Fe O 组成的混合物在一定条件下与Al粉进行铝热反应。
2 3
①引发铝热反应的操作是_____________________________。
②产物中单质是________(写名称)。
(3)取少量(1)中铝热反应所得的固体混合物,将其溶于足量稀 HSO ,滴加KSCN溶液无明显现象,
2 4
________ ( 填 “ 能 ” 或 “ 不 能 ” ) 说 明 固 体 混 合 物 中 无 Fe O , 理 由 是
2 3
_________________________________________(用离子方程式说明)。
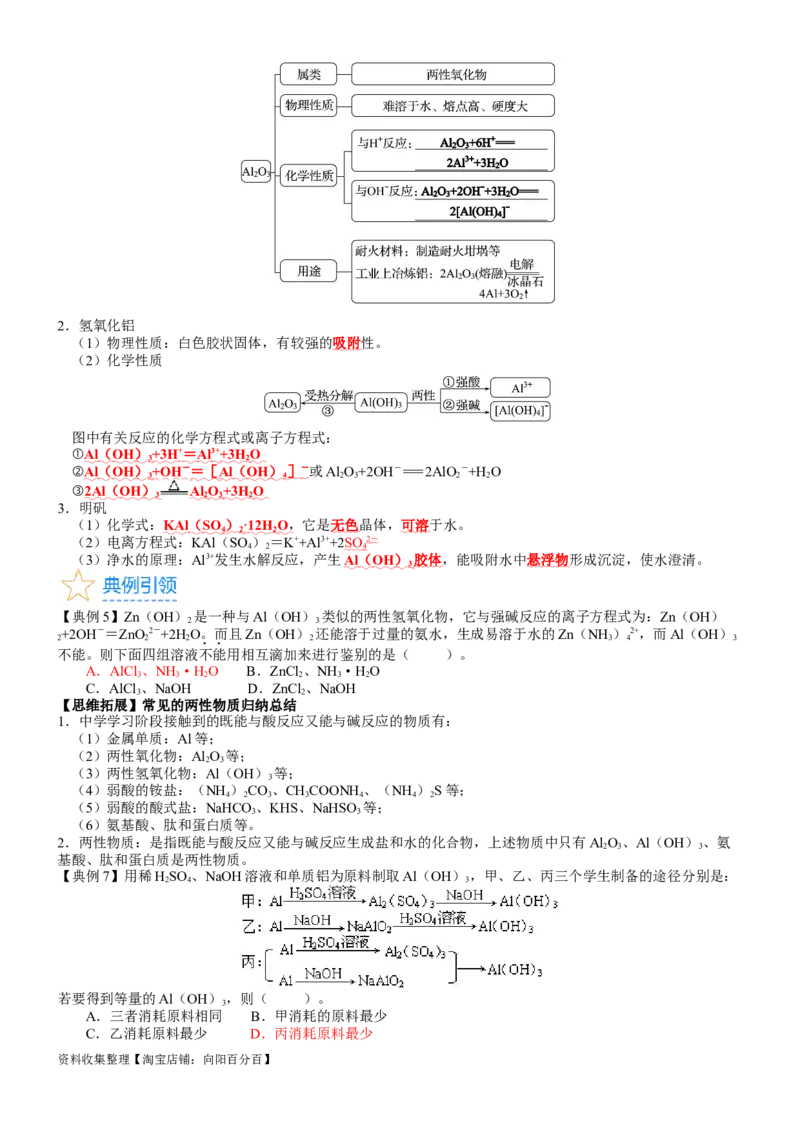
【思维拓展】铝热反应实验
1.实验装置和用品
2.实验现象
(1)镁带剧烈燃烧,放出大量的热,并发出耀眼的白光,氧化铁与铝粉在较高温度下发生剧烈的反应;
(2)纸漏斗的下部被烧穿,有熔融物落入沙中
3.原理应用
(1)制取熔点较高、活动性弱于Al的金属,如铁、铬、锰、钨等,3MnO +4Al 3Mn+2Al O;
2 2 3
(2)金属焊接,如野外焊接钢轨等
1.将ag铝铁合金投入足量的NaOH溶液中产生6.72L气体(标准状况);将ag同样的铝铁合金投入足量的盐
酸中,产生11.2L气体(标准状况)。则该合金中,铝、铁的物质的量之比为( )。
A.1∶1 B.2∶1 C.3∶2 D.3∶5
2.分别向盛有等物质的量浓度的稀硫酸和氢氧化钠溶液的烧杯中加入足量的铝,反应后放出的气体体积比在标
准状况下为1∶2,则所取稀硫酸和氢氧化钠溶液的体积比为( )。
A.1∶2 B.3∶4 C.3∶2 D.6∶1
3.(2022·宜昌高三上学期期末)铝热反应的实验装置如图所示,下列有关说法错误的是( )。
A.X物质为KClO
3
B.镁条燃烧提供引发反应所需的热量
C.若转移0.3 mol电子,被还原的Fe O 为16 g
2 3
D.可利用铝热反应冶炼铁
考法 3 铝的化合物的性质
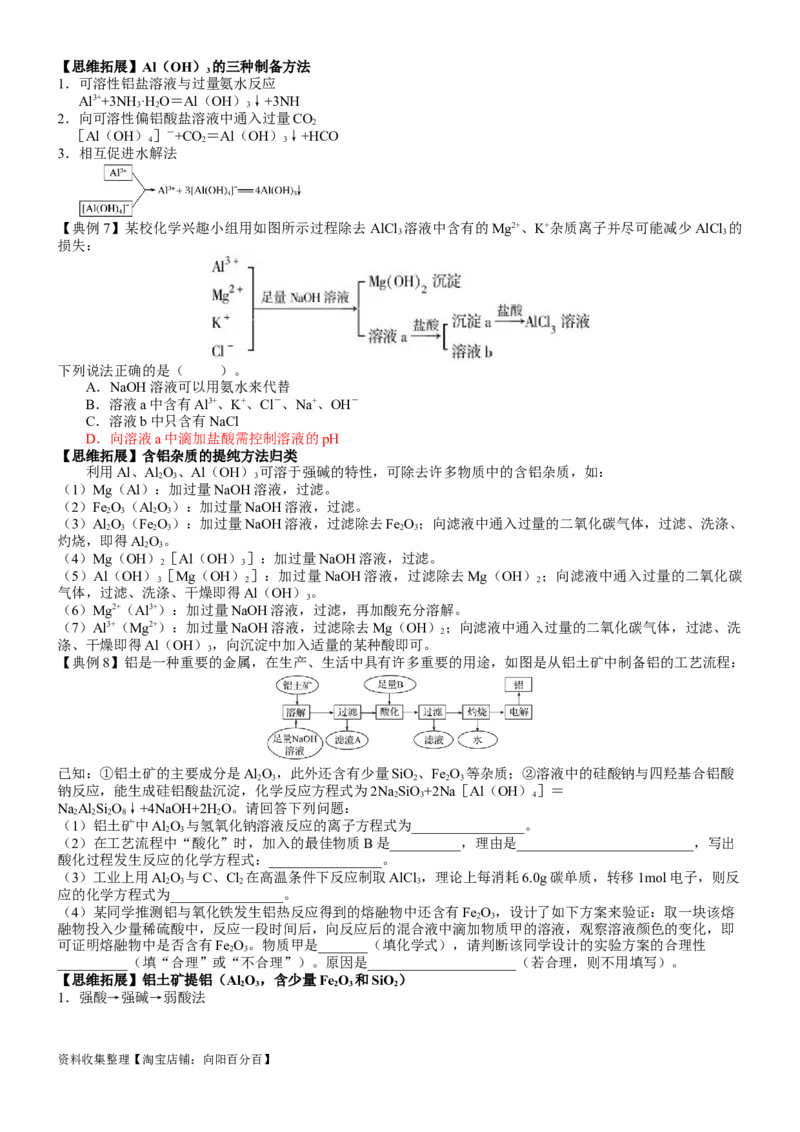
1.氧化铝
资料收集整理【淘宝店铺:向阳百分百】2.氢氧化铝
(1)物理性质:白色胶状固体,有较强的吸附性。
(2)化学性质
图中有关反应的化学方程式或离子方程式:
① Al ( OH ) +3H + = Al 3+ +3H O
3 2
② Al ( OH ) +OH - =[ Al ( OH ) ] - 或Al O+2OH- 2AlO-+H O
3 4 2 3 2 2
③ 2Al ( OH ) Al O+3H O
3 2 3 2
3.明矾
(1)化学式: KAl ( SO ) · 12H O,它是无色晶体,可溶于水。
4 2 2
(2)电离方程式:KAl(SO )=K++Al3++2SO 2-
4 2 4
(3)净水的原理:Al3+发生水解反应,产生 Al ( OH ) 胶体,能吸附水中悬浮物形成沉淀,使水澄清。
3
【典例5】Zn(OH) 是一种与Al(OH) 类似的两性氢氧化物,它与强碱反应的离子方程式为:Zn(OH)
2 3
+2OH-=ZnO2-+2H O。而且Zn(OH) 还能溶于过量的氨水,生成易溶于水的Zn(NH )2+,而Al(OH)
2 2 2 2 3 4 3
不能。则下面四组溶液不能用相互滴加来进行鉴别的是( )。
A.AlCl 、NH ·HO B.ZnCl、NH ·HO
3 3 2 2 3 2
C.AlCl 、NaOH D.ZnCl、NaOH
3 2
【思维拓展】常见的两性物质归纳总结
1.中学学习阶段接触到的既能与酸反应又能与碱反应的物质有:
(1)金属单质:Al等;
(2)两性氧化物:Al O 等;
2 3
(3)两性氢氧化物:Al(OH) 等;
3
(4)弱酸的铵盐:(NH )CO、CHCOONH、(NH )S等;
4 2 3 3 4 4 2
(5)弱酸的酸式盐:NaHCO 、KHS、NaHSO 等;
3 3
(6)氨基酸、肽和蛋白质等。
2.两性物质:是指既能与酸反应又能与碱反应生成盐和水的化合物,上述物质中只有Al O、Al(OH)、氨
2 3 3
基酸、肽和蛋白质是两性物质。
【典例7】用稀HSO 、NaOH溶液和单质铝为原料制取Al(OH),甲、乙、丙三个学生制备的途径分别是:
2 4 3
若要得到等量的Al(OH),则( )。
3
A.三者消耗原料相同 B.甲消耗的原料最少
C.乙消耗原料最少 D.丙消耗原料最少
资料收集整理【淘宝店铺:向阳百分百】【思维拓展】Al(OH) 的三种制备方法
3
1.可溶性铝盐溶液与过量氨水反应
Al3++3NH·HO=Al(OH)↓+3NH
3 2 3
2.向可溶性偏铝酸盐溶液中通入过量CO
2
[Al(OH)]-+CO =Al(OH)↓+HCO
4 2 3
3.相互促进水解法
【典例7】某校化学兴趣小组用如图所示过程除去AlCl 溶液中含有的Mg2+、K+杂质离子并尽可能减少AlCl 的
3 3
损失:
下列说法正确的是( )。
A.NaOH溶液可以用氨水来代替
B.溶液a中含有Al3+、K+、Cl-、Na+、OH-
C.溶液b中只含有NaCl
D.向溶液a中滴加盐酸需控制溶液的pH
【思维拓展】含铝杂质的提纯方法归类
利用Al、Al O、Al(OH) 可溶于强碱的特性,可除去许多物质中的含铝杂质,如:
2 3 3
(1)Mg(Al):加过量NaOH溶液,过滤。
(2)Fe O(Al O):加过量NaOH溶液,过滤。
2 3 2 3
(3)Al O(Fe O):加过量NaOH溶液,过滤除去Fe O;向滤液中通入过量的二氧化碳气体,过滤、洗涤、
2 3 2 3 2 3
灼烧,即得Al O。
2 3
(4)Mg(OH)[Al(OH)]:加过量NaOH溶液,过滤。
2 3
(5)Al(OH) [Mg(OH) ]:加过量NaOH溶液,过滤除去Mg(OH) ;向滤液中通入过量的二氧化碳
3 2 2
气体,过滤、洗涤、干燥即得Al(OH)。
3
(6)Mg2+(Al3+):加过量NaOH溶液,过滤,再加酸充分溶解。
(7)Al3+(Mg2+):加过量NaOH溶液,过滤除去Mg(OH);向滤液中通入过量的二氧化碳气体,过滤、洗
2
涤、干燥即得Al(OH),向沉淀中加入适量的某种酸即可。
3
【典例8】铝是一种重要的金属,在生产、生活中具有许多重要的用途,如图是从铝土矿中制备铝的工艺流程:
已知:①铝土矿的主要成分是Al O,此外还含有少量SiO、Fe O 等杂质;②溶液中的硅酸钠与四羟基合铝酸
2 3 2 2 3
钠反应,能生成硅铝酸盐沉淀,化学反应方程式为2NaSiO+2Na[Al(OH)]=
2 3 4
NaAl Si O↓+4NaOH+2HO。请回答下列问题:
2 2 2 8 2
(1)铝土矿中Al O 与氢氧化钠溶液反应的离子方程式为________________。
2 3
(2)在工艺流程中“酸化”时,加入的最佳物质B是__________,理由是_________________________,写出
酸化过程发生反应的化学方程式:________________。
(3)工业上用Al O 与C、Cl 在高温条件下反应制取AlCl ,理论上每消耗6.0g碳单质,转移1mol电子,则反
2 3 2 3
应的化学方程式为________________。
(4)某同学推测铝与氧化铁发生铝热反应得到的熔融物中还含有Fe O,设计了如下方案来验证:取一块该熔
2 3
融物投入少量稀硫酸中,反应一段时间后,向反应后的混合液中滴加物质甲的溶液,观察溶液颜色的变化,即
可证明熔融物中是否含有Fe O。物质甲是_______(填化学式),请判断该同学设计的实验方案的合理性
2 3
__________(填“合理”或“不合理”)。原因是_____________________(若合理,则不用填写)。
【思维拓展】铝土矿提铝(Al O,含少量FeO 和SiO )
2 3 2 3 2
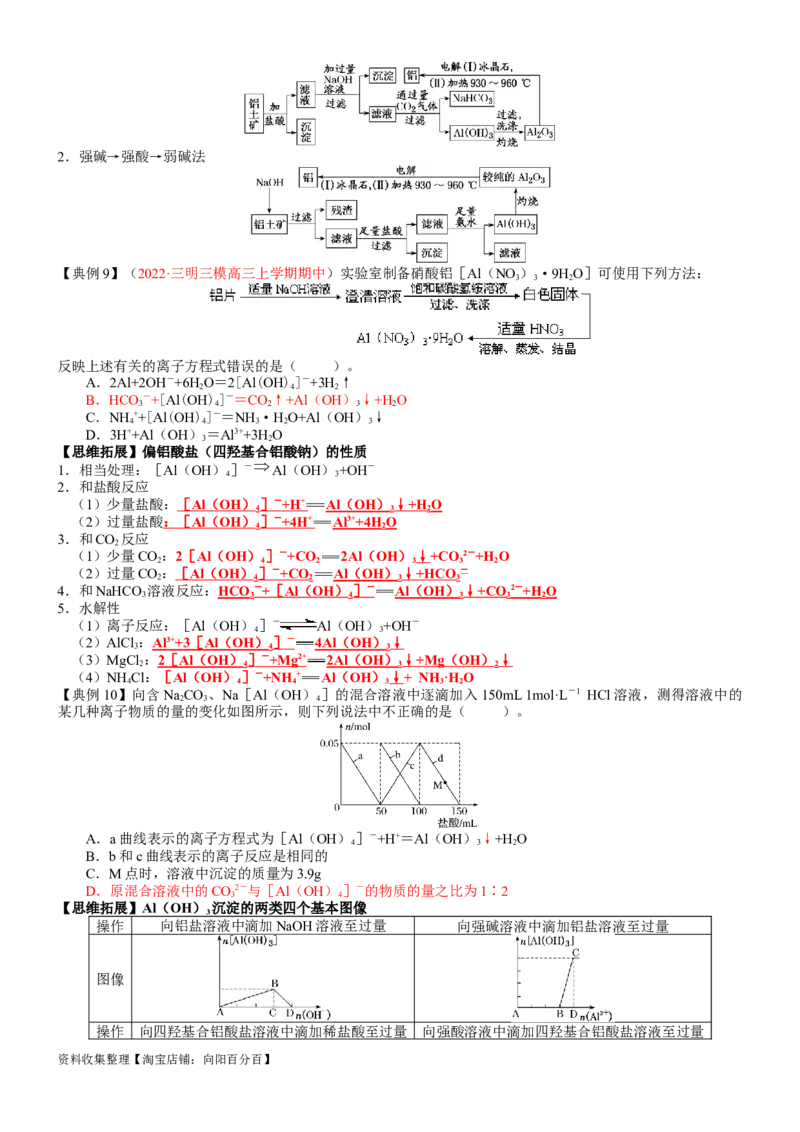
1.强酸→强碱→弱酸法
资料收集整理【淘宝店铺:向阳百分百】2.强碱→强酸→弱碱法
【典例9】(2022·三明三模高三上学期期中)实验室制备硝酸铝[Al(NO )·9HO]可使用下列方法:
3 3 2
反映上述有关的离子方程式错误的是( )。
A.2Al+2OH-+6HO=2[Al(OH)]-+3H ↑
2 4 2
B.HCO -+[Al(OH)]-=CO↑+Al(OH)↓+H O
3 4 2 3 2
C.NH ++[Al(OH)]-=NH ·HO+Al(OH)↓
4 4 3 2 3
D.3H++Al(OH)=Al3++3H O
3 2
【思维拓展】偏铝酸盐(四羟基合铝酸钠)的性质
1.相当处理:[Al(OH)]- Al(OH)+OH-
4 3
2.和盐酸反应
(1)少量盐酸: [ A l ( OH ) ] - +H + Al ( OH ) ↓ +H O
4 3 2
(2)过量盐酸 : [ A l ( OH ) ] - +4H + Al 3+ +4H O
4 2
3.和CO 反应
2
(1)少量CO:2[Al(OH)]-+CO 2Al(OH)↓+CO2-+H O
2 4 2 3 3 2
(2)过量CO: [ A l ( OH ) ] - +CO Al ( OH ) ↓ +HCO -
2 4 2 3 3
4.和NaHCO 溶液反应:HCO - + [ A l ( OH ) ] - Al ( OH ) ↓ +CO 2 - +H O
3 3 4 3 3 2
5.水解性
(1)离子反应:[Al(OH)]- Al(OH)+OH-
4 3
(2)AlCl : Al 3+ + 3 [ Al ( OH ) ] - 4 Al ( OH ) ↓
3 4 3
(3)MgCl : 2 [ Al ( OH ) ] - + M g 2 + 2 Al ( OH ) ↓ + M g ( OH ) ↓
2 4 3 2
(4)NH Cl:[Al(OH)]-+NH+ Al(OH)↓+ NH ·HO
4 4 4 3 3 2
【典例10】向含NaCO 、Na[Al(OH) ]的混合溶液中逐滴加入150mL 1mol·L-1 HCl溶液,测得溶液中的
2 3 4
某几种离子物质的量的变化如图所示,则下列说法中不正确的是( )。
A.a曲线表示的离子方程式为[Al(OH)]-+H+=Al(OH)↓+H O
4 3 2
B.b和c曲线表示的离子反应是相同的
C.M点时,溶液中沉淀的质量为3.9g
D.原混合溶液中的CO2-与[Al(OH)]-的物质的量之比为1∶2
3 4
【思维拓展】Al(OH) 沉淀的两类四个基本图像
3
操作 向铝盐溶液中滴加NaOH溶液至过量 向强碱溶液中滴加铝盐溶液至过量
图像
操作 向四羟基合铝酸盐溶液中滴加稀盐酸至过量 向强酸溶液中滴加四羟基合铝酸盐溶液至过量
资料收集整理【淘宝店铺:向阳百分百】图像
【特别提醒】①沉淀Al3+所需n(OH-)与Al(OH) 溶解所需n(OH-)的比为3∶1;
3
②沉淀[Al(OH)]-所需n(H+)与Al(OH) 溶解所需n(H+)的比为1∶3。
4 3
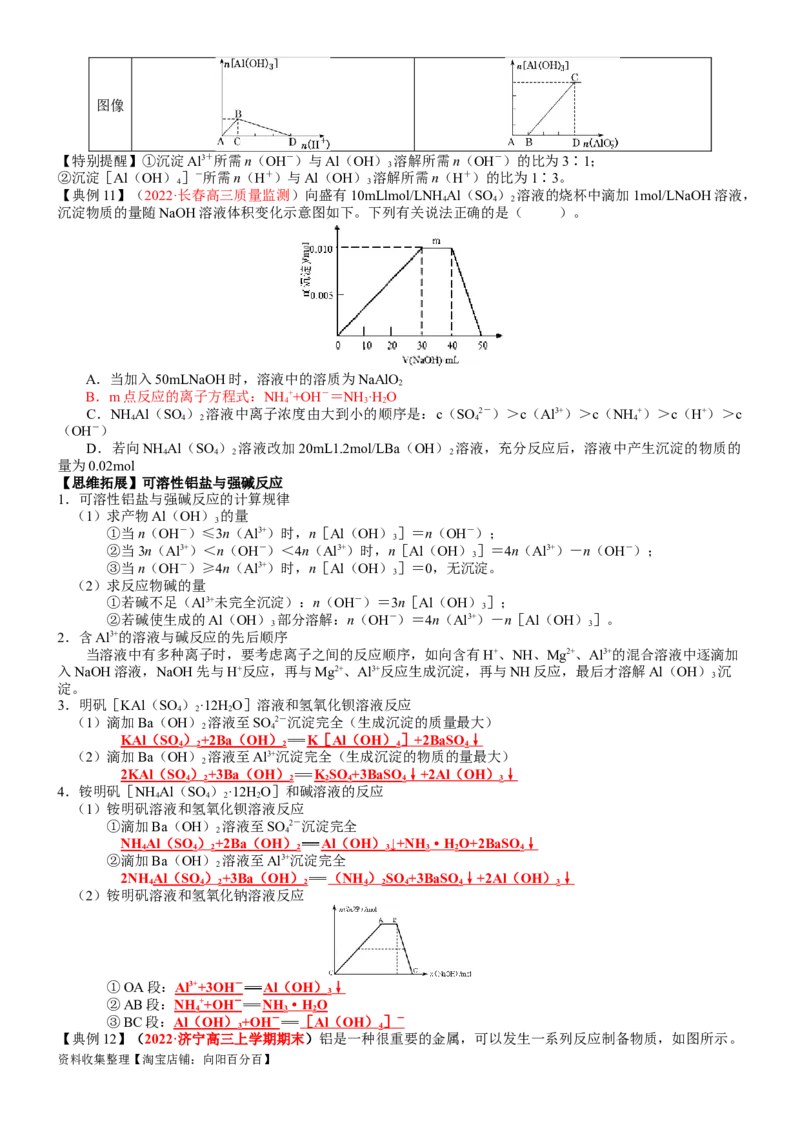
【典例11】(2022·长春高三质量监测)向盛有10mLlmol/LNH Al(SO ) 溶液的烧杯中滴加1mol/LNaOH溶液,
4 4 2
沉淀物质的量随NaOH溶液体积变化示意图如下。下列有关说法正确的是( )。
A.当加入50mLNaOH时,溶液中的溶质为NaAlO
2
B.m点反应的离子方程式:NH ++OH-=NH ·HO
4 3 2
C.NH Al(SO ) 溶液中离子浓度由大到小的顺序是:c(SO 2-)>c(Al3+)>c(NH +)>c(H+)>c
4 4 2 4 4
(OH-)
D.若向NH Al(SO ) 溶液改加20mL1.2mol/LBa(OH) 溶液,充分反应后,溶液中产生沉淀的物质的
4 4 2 2
量为0.02mol
【思维拓展】可溶性铝盐与强碱反应
1.可溶性铝盐与强碱反应的计算规律
(1)求产物Al(OH) 的量
3
①当n(OH-)≤3n(Al3+)时,n[Al(OH)]=n(OH-);
3
②当3n(Al3+)<n(OH-)<4n(Al3+)时,n[Al(OH)]=4n(Al3+)-n(OH-);
3
③当n(OH-)≥4n(Al3+)时,n[Al(OH)]=0,无沉淀。
3
(2)求反应物碱的量
①若碱不足(Al3+未完全沉淀):n(OH-)=3n[Al(OH)];
3
②若碱使生成的Al(OH) 部分溶解:n(OH-)=4n(Al3+)-n[Al(OH)]。
3 3
2.含Al3+的溶液与碱反应的先后顺序
当溶液中有多种离子时,要考虑离子之间的反应顺序,如向含有H+、NH、Mg2+、Al3+的混合溶液中逐滴加
入NaOH溶液,NaOH先与H+反应,再与Mg2+、Al3+反应生成沉淀,再与NH反应,最后才溶解Al(OH) 沉
3
淀。
3.明矾[KAl(SO )·12HO]溶液和氢氧化钡溶液反应
4 2 2
(1)滴加Ba(OH) 溶液至SO 2-沉淀完全(生成沉淀的质量最大)
2 4
KAl ( SO ) +2Ba ( OH ) K [ Al ( OH ) ] +2BaSO ↓
4 2 2 4 4
(2)滴加Ba(OH) 溶液至Al3+沉淀完全(生成沉淀的物质的量最大)
2
2KAl ( SO ) +3Ba ( OH ) KSO +3BaSO ↓ +2A l ( OH ) ↓
4 2 2 2 4 4 3
4.铵明矾[NH Al(SO )·12HO]和碱溶液的反应
4 4 2 2
(1)铵明矾溶液和氢氧化钡溶液反应
①滴加Ba(OH) 溶液至SO 2-沉淀完全
2 4
NH Al ( SO ) +2Ba ( OH ) Al ( OH ) ↓ + NH · H O +2BaSO ↓
4 4 2 2 3 3 2 4
②滴加Ba(OH) 溶液至Al3+沉淀完全
2
2NH Al ( SO ) +3Ba ( OH ) ( NH )SO +3BaSO ↓ +2A l ( OH ) ↓
4 4 2 2 4 2 4 4 3
(2)铵明矾溶液和氢氧化钠溶液反应
①OA段: Al 3+ +3OH - Al ( OH ) ↓
3
②AB段:NH + +OH - NH · H O
4 3 2
③BC段: Al ( OH ) +OH - [ A l ( OH ) ] -
3 4
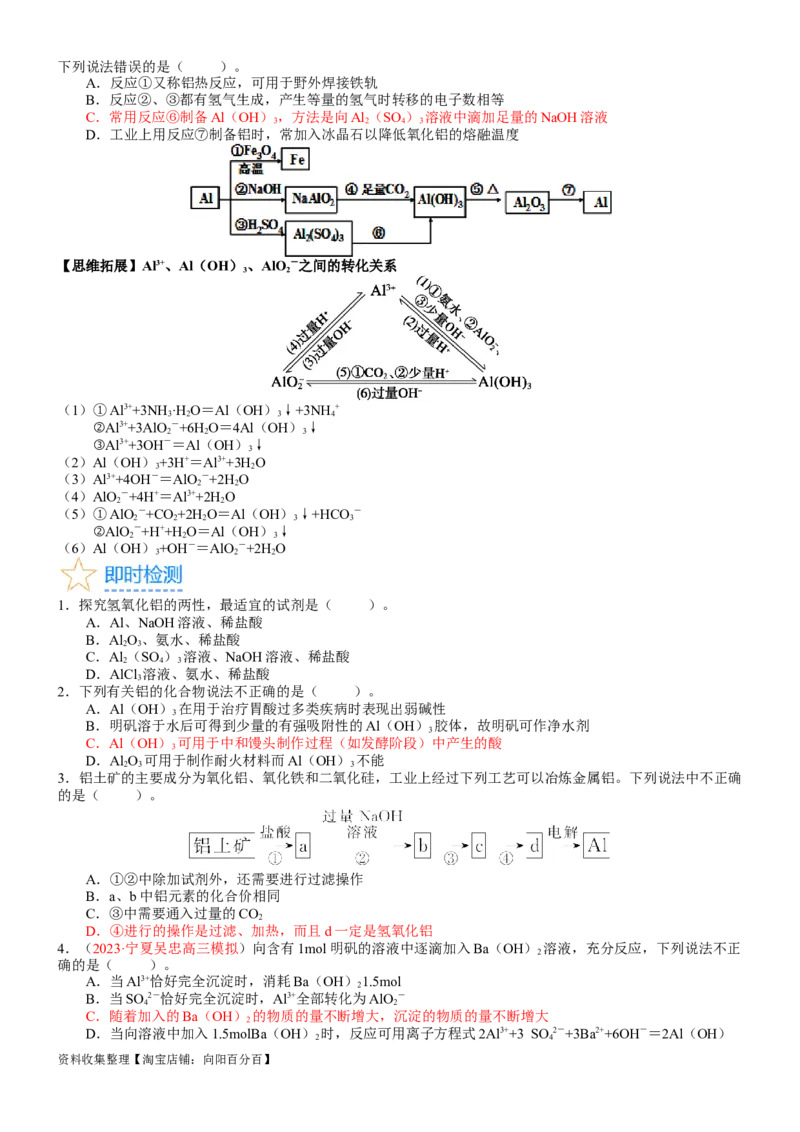
【典例12】(2022·济宁高三上学期期末)铝是一种很重要的金属,可以发生一系列反应制备物质,如图所示。
资料收集整理【淘宝店铺:向阳百分百】下列说法错误的是( )。
A.反应①又称铝热反应,可用于野外焊接铁轨
B.反应②、③都有氢气生成,产生等量的氢气时转移的电子数相等
C.常用反应⑥制备Al(OH),方法是向Al (SO ) 溶液中滴加足量的NaOH溶液
3 2 4 3
D.工业上用反应⑦制备铝时,常加入冰晶石以降低氧化铝的熔融温度
【思维拓展】Al3+、Al(OH)、AlO -之间的转化关系
3 2
(1)①Al3++3NH·HO=Al(OH)↓+3NH+
3 2 3 4
②Al3++3AlO -+6H O=4Al(OH)↓
2 2 3
③Al3++3OH-=Al(OH)↓
3
(2)Al(OH)+3H+=Al3++3H O
3 2
(3)Al3++4OH-=AlO-+2H O
2 2
(4)AlO-+4H+=Al3++2H O
2 2
(5)①AlO-+CO +2H O=Al(OH)↓+HCO-
2 2 2 3 3
②AlO -+H++H O=Al(OH)↓
2 2 3
(6)Al(OH)+OH-=AlO-+2H O
3 2 2
1.探究氢氧化铝的两性,最适宜的试剂是( )。
A.Al、NaOH溶液、稀盐酸
B.Al O、氨水、稀盐酸
2 3
C.Al (SO ) 溶液、NaOH溶液、稀盐酸
2 4 3
D.AlCl 溶液、氨水、稀盐酸
3
2.下列有关铝的化合物说法不正确的是( )。
A.Al(OH) 在用于治疗胃酸过多类疾病时表现出弱碱性
3
B.明矾溶于水后可得到少量的有强吸附性的Al(OH) 胶体,故明矾可作净水剂
3
C.Al(OH) 可用于中和馒头制作过程(如发酵阶段)中产生的酸
3
D.Al O 可用于制作耐火材料而Al(OH) 不能
2 3 3
3.铝土矿的主要成分为氧化铝、氧化铁和二氧化硅,工业上经过下列工艺可以冶炼金属铝。下列说法中不正确
的是( )。
A.①②中除加试剂外,还需要进行过滤操作
B.a、b中铝元素的化合价相同
C.③中需要通入过量的CO
2
D.④进行的操作是过滤、加热,而且d一定是氢氧化铝
4.(2023·宁夏吴忠高三模拟)向含有1mol明矾的溶液中逐滴加入Ba(OH) 溶液,充分反应,下列说法不正
2
确的是( )。
A.当Al3+恰好完全沉淀时,消耗Ba(OH)1.5mol
2
B.当SO 2-恰好完全沉淀时,Al3+全部转化为AlO-
4 2
C.随着加入的Ba(OH) 的物质的量不断增大,沉淀的物质的量不断增大
2
D.当向溶液中加入1.5molBa(OH) 时,反应可用离子方程式2Al3++3 SO 2-+3Ba2++6OH-=2Al(OH)
2 4
资料收集整理【淘宝店铺:向阳百分百】↓+3BaSO ↓表示
3 4
【基础过关】
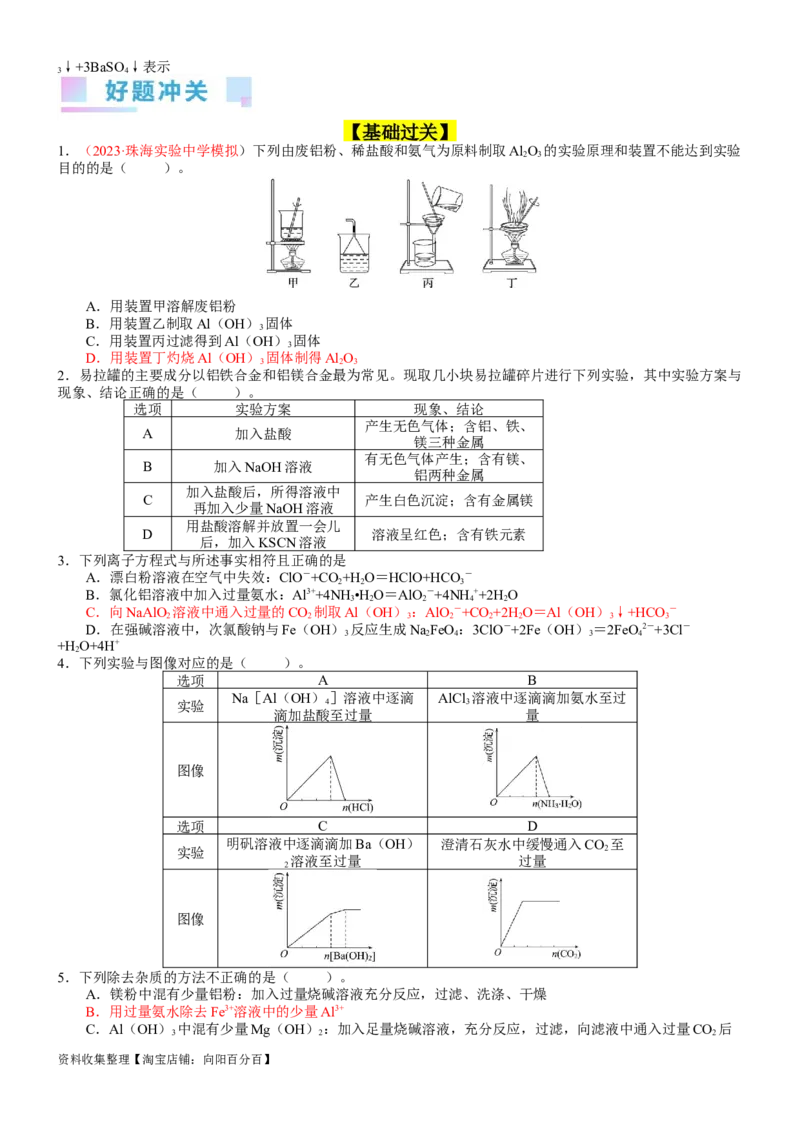
1.(2023·珠海实验中学模拟)下列由废铝粉、稀盐酸和氨气为原料制取Al O 的实验原理和装置不能达到实验
2 3
目的的是( )。
A.用装置甲溶解废铝粉
B.用装置乙制取Al(OH) 固体
3
C.用装置丙过滤得到Al(OH) 固体
3
D.用装置丁灼烧Al(OH) 固体制得Al O
3 2 3
2.易拉罐的主要成分以铝铁合金和铝镁合金最为常见。现取几小块易拉罐碎片进行下列实验,其中实验方案与
现象、结论正确的是( )。
选项 实验方案 现象、结论
产生无色气体;含铝、铁、
A 加入盐酸
镁三种金属
有无色气体产生;含有镁、
B 加入NaOH溶液
铝两种金属
加入盐酸后,所得溶液中
C 产生白色沉淀;含有金属镁
再加入少量NaOH溶液
用盐酸溶解并放置一会儿
D 溶液呈红色;含有铁元素
后,加入KSCN溶液
3.下列离子方程式与所述事实相符且正确的是
A.漂白粉溶液在空气中失效:ClO-+CO +H O=HClO+HCO -
2 2 3
B.氯化铝溶液中加入过量氨水:Al3++4NH•H O=AlO-+4NH++2H O
3 2 2 4 2
C.向NaAlO 溶液中通入过量的CO 制取Al(OH):AlO-+CO +2H O=Al(OH)↓+HCO-
2 2 3 2 2 2 3 3
D.在强碱溶液中,次氯酸钠与Fe(OH) 反应生成NaFeO:3ClO-+2Fe(OH)=2FeO2-+3Cl-
3 2 4 3 4
+H O+4H+
2
4.下列实验与图像对应的是( )。
选项 A B
Na[Al(OH)]溶液中逐滴 AlCl 溶液中逐滴滴加氨水至过
实验 4 3
滴加盐酸至过量 量
图像
选项 C D
明矾溶液中逐滴滴加Ba(OH) 澄清石灰水中缓慢通入CO 至
实验 2
溶液至过量 过量
2
图像
5.下列除去杂质的方法不正确的是( )。
A.镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥
B.用过量氨水除去Fe3+溶液中的少量Al3+
C.Al(OH) 中混有少量Mg(OH):加入足量烧碱溶液,充分反应,过滤,向滤液中通入过量CO 后
3 2 2
资料收集整理【淘宝店铺:向阳百分百】