文档内容
考点 11 铝、镁及其重要化合物
目录
1.高考真题考点分布
2.命题规律及备考策略
考法01 铝及其化合物
考法02 镁及其化合物
1.高考真题考点分布
考点内容 考点分布
铝、镁及其化 2024·浙江卷,3分;2024·广东卷,3分;2023天津卷第题,3分;2023浙江1月卷第
合物的性质与 12题,2分;2023浙江6月卷第4题,2分;2023湖南卷第7题,3分;2022全国甲
应用 卷第9题,6分;2022海南卷第6题,2分;2022河北卷第4题,3分;2022湖北卷
第1题,3分;2022浙江1月卷第8题,2分;2022浙江6月卷第8题,2分;
铝、镁及其化
2023辽宁卷第16题,3分;2022全国卷第26题,1分;
合物的工艺流
2022湖南卷第6题,3分;2021湖南卷第6题,3分
程
2.命题规律及备考策略
【命题规律】
高频考点从近几年全国高考试题来看,镁、铝、氧化镁、氧化铝及氢氧化镁、氢氧化铝的性质与用途仍是
高考命题的热点。
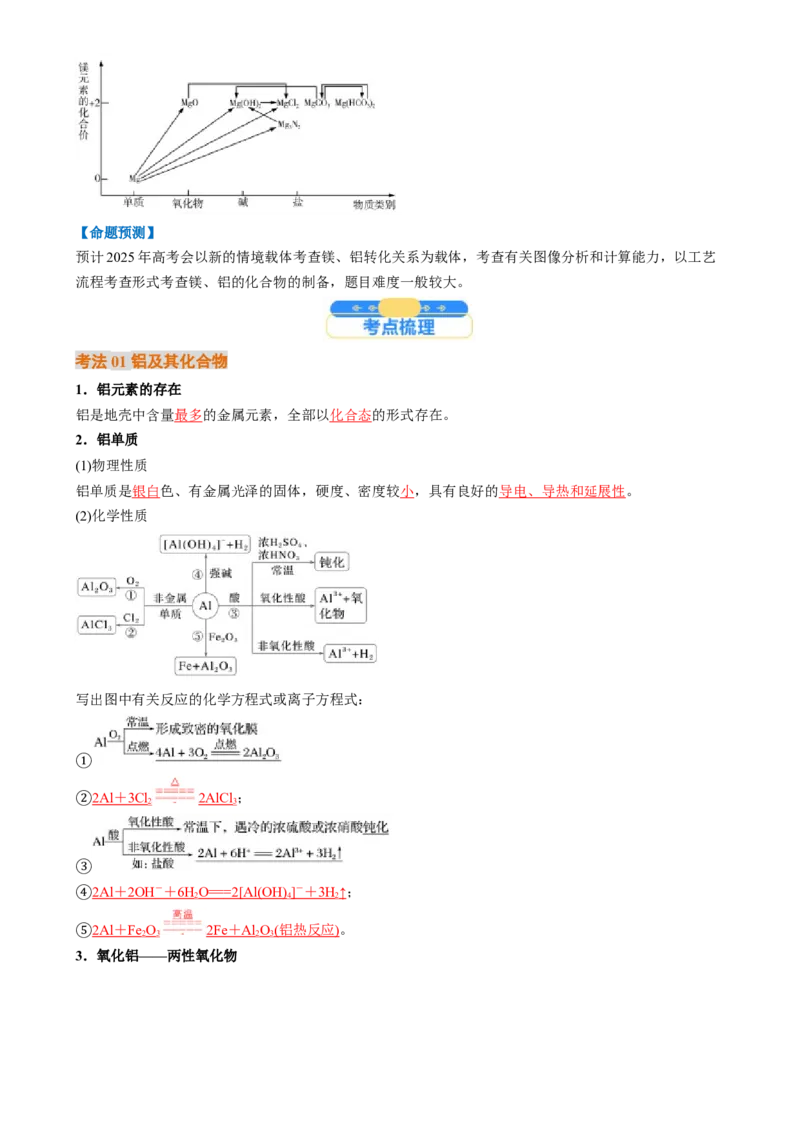
【备考策略】铝元素的价类二维图及转化关系
镁元素的价类二维图及转化关系【命题预测】
预计2025年高考会以新的情境载体考查镁、铝转化关系为载体,考查有关图像分析和计算能力,以工艺
流程考查形式考查镁、铝的化合物的制备,题目难度一般较大。
考法01 铝及其化合物
1.铝元素的存在
铝是地壳中含量最多的金属元素,全部以化合态的形式存在。
2.铝单质
(1)物理性质
铝单质是银白色、有金属光泽的固体,硬度、密度较小,具有良好的导电、导热和延展性。
(2)化学性质
写出图中有关反应的化学方程式或离子方程式:
①
2Al + 3Cl 2AlCl ;
2 3
②
2Al + 2OH - + 6H O == =2[Al(OH) ] - + 3H ↑;
③ 2 4 2
④
2Al + Fe O 2Fe + Al O ( 铝热反应 ) 。
2 3 2 3
3.氧化铝——两性氧化物
⑤4.氢氧化铝
(1)物理性质:白色胶状不溶于水的固体,有较强的吸附性。
(2)化学性质
写出图中有关反应的化学方程式或离子方程式:
2Al(OH) Al O + 3H O。
3 2 3 2
Al(OH) + 3H + == =A l 3 + + 3H O。
① 3 2
Al(OH) + OH - == =[Al(OH ) ] - 。
② 3 4
(3)Al(OH) 的制备
③ 3
写出下列反应的离子方程式:
Al3+与氨水反应: Al 3 + + 3NH ·H O == =Al(OH) ↓ + 3NH 。
3 2 3
①向含[Al(OH) ]-的溶液中通入过量的CO:[Al(OH) ] - + CO == =Al(OH) ↓ + HCO 。
4 2 4 2 3
Al3+与[Al(OH) ]-发生相互促进的水解反应: Al 3 + + 3[Al(OH) ] - == =4Al(OH) ↓。
② 4 4 3
5.明矾
③
(1)明矾的化学式为KAl(SO )·12H O,属于复盐。
4 2 2
(2)明矾净水的原理:明矾溶于水时发生电离,电离方程式为 KAl(SO ) == =K + + Al 3 + + 2SO ,其中Al3+
4 2
发
生水解反应,产生Al(OH) 胶体,其吸附能力很强,可以吸附水中的悬浮杂质并形成沉淀,使水变澄清。
3
6.有关氢氧化铝的图像分析与计算
(1)可溶性铝盐溶液与NaOH溶液反应的图像
滴加顺序 向AlCl 中滴加NaOH 向NaOH中滴加AlCl
3 3
立即产生白色沉淀→渐多→最多→ 无沉淀(有但即溶)→沉淀→渐多→最多→不消
现象
渐少→消失 失
图像
离子方 OA段 Al3++3OH-===Al(OH) 3 ↓ Al3++4OH-===AlO +2H 2 O程式 AB段 Al(OH) +OH-===AlO +2HO Al3++3AlO +6HO===4Al(OH) ↓
3 2 2 3
(2)偏铝酸盐溶液与盐酸反应的图像
滴加顺序 向AlO 中滴加H+ 向H+中滴加AlO
立即产生白色沉淀→渐多→最多→渐少→ 无沉淀(有但即溶)→沉淀→渐多→最多→
现象
消失 不消失
图像
OA段 AlO +H++HO===Al(OH) ↓ AlO +4H+===Al3++2HO
离子方 2 3 2
程式
AB段 Al(OH) 3 +3H+===Al3++3H 2 O Al3++3AlO +6H 2 O===4Al(OH) 3 ↓
(3)向AlCl 溶液中逐滴加入氨水或NaAlO 溶液至过量,图像如图甲所示。
3 2
(4)向NaAlO 溶液中逐滴加入AlCl 溶液或通入CO 至过量,图像如图乙所示。
2 3 2
(5)向MgCl 、AlCl 和盐酸的混合溶液(即将Mg、Al溶于过量盐酸所得的溶液)中逐滴滴入NaOH溶液至过
2 3
量,图像如图丙所示。
(6)向MgCl 、AlCl 混合溶液中先加入NaOH溶液,后加入盐酸(NaOH与盐酸的物质的量浓度相等),沉淀
2 3
图像如图丁所示。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
1.MgO与Al粉的混合物也可称为铝热剂( )
2.实验室可用氧化铝坩埚熔化NaOH、NaCO 固体等( )
2 3
3.铝和酸反应时,氧化剂是酸,铝和碱反应时,氧化剂是碱( )
4.明矾可作净水剂,起到杀菌消毒的作用( )
5.氧化铝熔点高,常用于制造耐高温材料( )
6.工业上通过电解六水合氯化镁制取金属镁( )
7.铝热反应非常剧烈,操作时要戴上石棉手套和护目镜( )
【答案】1.× 2.× 3.× 4.× 5.√ 6.× 7.√考向01 考查铝及其化合物的性质
【例1】(2024·河北衡水·期中)下列变化不可能通过一步实验直接完成的是
A. B.
C. D.
【答案】B
【解析】A.氢氧化铝受热反应生成氧化铝和水,A不符合题意;
B.氧化铝不溶于水不和水反应,不能一步生成氢氧化铝,B符合题意;
C.Al与NaOH发生反应生成氢气和 ,C不符合题意;
D.铝盐与弱碱(氨水)反应生成氢氧化铝,D不符合题意;
故选B。
【思维建模】铝与酸或碱反应生成H 的量的关系
2
2Al+6HCl===2AlCl +3H↑
3 2
2Al+2NaOH+2HO===2NaAlO+3H↑
2 2 2
1.等质量的铝与足量的盐酸、氢氧化钠溶液分别反应:
(1)产生H 的物质的量相等。
2
(2)消耗H+、OH-的物质的量之比为n(H+) n(OH-)=3 1。
2.足量的铝分别与等物质的量的HCl和NaOH反应:
∶ ∶
(1)消耗Al的物质的量之比为1 3。
(2)生成H 的物质的量之比为1 3。
2 ∶
3.一定量的铝分别与一定量的盐酸、氢氧化钠溶液反应:
∶
若产生氢气的体积比为 < <1,则必定
(1)铝与盐酸反应时,铝过量而HCl不足。
(2)铝与氢氧化钠溶液反应时,铝不足而NaOH过量。
考向02 通过工艺流程考查铝及其化合物
【例2】(2024·福建泉州·期中)工业上用铝土矿(主要成分为 ,还有少量的 等杂质)
提取氧化铝作冶炼铝的原料,提取的操作过程如下:
下列说法错误的是
A.沉淀Ⅰ主要成分为
B.溶液Ⅱ含有的阴离子主要为
C.溶液Ⅲ中溶质的主要成分为
D.沉淀Ⅲ转化为氧化铝反应是分解反应【答案】C
【分析】铝土矿加入盐酸,氧化铝和氧化铁都可以溶解,二氧化硅不溶解,所以滤渣A为二氧化硅,滤
液甲中加入过量的氢氧化钠,得到氢氧化铁沉淀和偏铝酸钠溶液,滤液乙主要成分为偏铝酸钠,通入过量
的二氧化碳,反应生成碳酸氢钠和氢氧化铝沉淀。
【解析】A.滤渣A为二氧化硅,A正确;
B.滤液乙含有多阴离子主要为偏铝酸根离子和氯离子和氢氧根离子,B正确;
C.滤液丙中主要成分为碳酸氢钠,C错误;
D.氢氧化铝加热分解生成氧化铝和水,为分解反应,D正确;
故选C。
考向03 考查有关铝及其化合物的图像
【例3】(2024·四川成都·期中)实验研究发现,金属与极稀的硝酸反应时,硝酸可被还原为 。现将
一定量的铝粉和铁粉的混合物与 足量很稀的硝酸充分反应,固体完全溶解,反应过程中无气体放出。
反应结束后(忽略溶液体积的变化)将溶液平均分成两份,一份滴加KSCN溶液,一份逐滴加入
溶液。所加 溶液的体积 与产生沉淀的物质的量 关系如图所示。下列说法
正确的是
A.加入KSCN的溶液中无现象
B.原混合物中铝粉的物质的量为
C.根据题目数据,无法计算a点数值
D.原溶液中硝酸浓度为
【答案】D
【分析】0a段没有沉淀生成,说明硝酸过量,发生反应:H++OH-=H2O,可知金属与酸反应中Al、Fe被
氧化为Al3+ 、Fe3+ ;
a-88段产生沉淀,发生反应:Fe3++3OH-=Fe(OH)3↓,Al3++3OH-=Al(OH)3↓;
88-94段消耗NaOH,但沉淀量不变,而金属与硝酸反应过程中无气体放出,由题意可知N元素被还原为
,发生反应: +OH-=NH3H2O;
94-104段沉淀部分溶解,发生反应:Al(OH)3+OH-= 。
【解析】A.根据分析,硝酸过量,产物中有Fe3+ ,加入KSCN溶液会变红,A错误;
B.根据94-104段发生反应:Al(OH)3+OH-= ,消耗的氢氧化钠的物质的量为:(104-94)×10-
3L×5mol/L=0.05mol,根据铝元素守恒,铝粉的物质的量为0.05mol,原混合物中铝粉的物质的量为
0.1mol,B错误;
C.c点溶液中硝酸根刚好生成NaNO3 ,则n(NaNO3)=94×10-3L×5mol/L=0.47mol,a点对应NaOH溶液的体积a= ×103mL=40mL,C错误;
D.由反应过程可知,到加入氢氧化钠为88mL时,溶液中溶质为硝酸钠与硝酸铵。由图可知,88-94段
消耗的氢氧化钠的体积为94mL-88mL=6mL,故该阶段参加反应的氢氧化钠为0.006L×5mol/L=0.03mol,
根据 + OH-=NH3·H2O可知溶液中n( )=0.03ml,由N原子守恒可知n(NH4NO3)=n(
)=0.03mol,根据钠元素守恒可知n(NaNO3)=n(NaOH)=0.088L×5mol/L=0.44mol,根据氮元素守恒原硝酸溶
液中n(HNO3)=n(NaNO3)+2n(NH4NO3)=0.44mol+0.03mol×2=0.5mol,硝酸浓度为 ,D正
确;
故选D。
【对点1】(2024·浙江·模拟预测)铝是生活中重要的金属材料,下列说法正确的是
A. 与 混合固体可用于疏通管道 B.常温下不能与 发生反应
C.铝合金的硬度一定比纯铝小 D.可通过电解熔融 制备金属铝
【答案】A
【解析】A. 与 反应生成氢气, ,可用于疏通管道,A
正确;
B.Al常温下可与O2 反应生成氧化铝,化学方程式为 ,B错误;
C.铝合金的硬度比纯铝大,C错误;
D.铝是活泼性较强的金属,工业上用电解熔融 制备金属铝,D错误;
故选A。
【对点2】(2024·江苏盐城·期中)以铝土矿(主要成分为 ,含 和 等杂质)为原料制备铝
的一种工艺流程如下:
注: 在“碱溶”时转化为铝硅酸钠沉淀
电解时,阳极发生氧化反应
①
下列说法正确的是
②
A.“碱溶”时生成偏铝酸钠的离子方程式为
B.“过滤Ⅰ”的滤渣成分为
C.“反应”中加入 溶液的作用同于通入
D.“电解Ⅰ”中作阳极的石墨易消枆,阳极反应中失电子物质主要是石墨
【答案】C
【分析】铝土矿主要成分为 ,含 和 等杂质,用氢氧化钠溶液溶解, 、 在“碱溶”时转化为铝硅酸钠沉淀,过滤除去 、铝硅酸钠沉淀,滤液为四羟基合铝酸钠溶液,加入碳酸氢钠
溶液生成氢氧化铝沉淀和碳酸钠,灼烧氢氧化铝生成氧化铝,电解熔融氧化铝生成金属铝。
【解析】A.“碱溶”时氧化铝和氢氧化钠反应生成四羟基合铝酸钠,反应的离子方程式为
( ),A错误;
B.“过滤Ⅰ”的滤渣成分为 、铝硅酸钠沉淀,B错误;
C.“反应”中加入 溶液, 和 反应,将 转化为 沉淀,C
正确;
D.石墨惰性电极不参与电极反应,D错误;
故选C。
【对点3】(2024·湖南邵阳·期中)研究实验发现硝酸的浓度越稀,硝酸发生氧化还原反应时,对应还原
产物中氮元素的化合价越低。现有一定量的铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程
中
无气体放出,在反应结束后的溶液中逐滴加入5mol/LNaOH溶液,所加NaOH溶液的体积与产生沉淀的物
质的量关系如图所示,下列说法不正确的是
A.该稀硝酸与铝粉、铁粉反应,其还原产物为硝酸铵
B.c点对应NaOH溶液的体积为40mL
C.b点与a点的差值为0.03mol
D.样品中铝粉和铁粉的物质的量之比为5 3
【答案】C
∶
【分析】铝粉和铁粉的混合物与一定量很稀HNO3 充分反应,被氧化为Al3+ 、Fe3+ ,通过题意,反应始终
没有气体生成,可以得出不会有氮的氧化物生成,又有硝酸的浓度越稀,对应还原产物中氮元素的化合价
越低,可以推测N元素由+5变成了-3价,由图可得硝酸过量,加入氢氧化钠溶液应先与硝酸反应,再生
成沉淀,当沉淀完全后,由图知继续加入氢氧化钠溶液,沉淀量不变,可得与 发生了反应,则随着
NaOH的滴加,发生的反应依次有: , 、
① ②
, , ;b与a的差值为
氢氧化铝的物质的量,由图可知,ef段消耗的氢氧化钠溶液为104mL-94m=10mL,故该阶段参加反应的
③ ④
氢氧化钠为0.01L×5mol/L=0.05mol,根据 可知,Al(OH)3 的物质的量为
0.05mol,根据铝元素守恒,故混合金属中n(Al)=0.05mol,由图可知,de段消耗的氢氧化钠的体积为
94mL-88mL=6mL,故该阶段参加反应的氢氧化钠为0.006L×5mol/L=0.03mol,根据
可知,计算溶液中n( )=0.03ml,根据电子转移守恒有:3n(Fe)+3n(Al)=8n(
),即3n(Fe)+3×0.05mol=8×0.03mol,解得n(Fe)=0.03mol,由反应过程可知,到加入氢氧化钠为88mL时,溶液中溶质为硝酸钠与硝酸铵,n(NH4NO3)=n( )=0.03mol,根据钠元素守恒,可知
n(NaNO3)=n(NaOH)=0.088L×5mol/L=0.44mol,根据氮元素守恒计算原硝酸溶液中
n(HNO3)=n(NaNO3)+2n(NH4NO3)=0.44mol+0.03mol×2=0.5mol,而c点溶液为NaNO3 、NH4NO3 、Fe(NO3)
3 、Al(NO3) 3 ,根据氮元素守恒n(NaNO3)+2n(NH4NO3)+3n[Fe(NO3) 3]+3n[Al(NO3) 3]=n(HNO3),故c点溶液
中n(NaNO3)=0.5mol-0.03mol×2-0.03mol×3-0.05mol×3=0.2mol,故c点加入NaOH的物质的量=0.2mol,以
此分析;
【解析】A.由上述分析可知,稀硝酸与铝粉、铁粉反应,其还原产物为硝酸铵,故A正确;
B.由上述分析可知,c点对应NaOH溶液的体积0.2mol ÷5mol.L=0.04L=40mL,故B正确;
C.由上述分析可知,b与a的差值为n[Al(NO3) 3]=0.05mol,故C错误;
D.由上述分析可知,混合金属中n(Al)=0.05mol、n(Fe)=0.03mol,样品中铝粉和铁粉的物质的量之比为
5:3,故D正确;
故答案为:C。
考法02 镁及其化合物
1.镁的化学性质
(1)与氧气反应: 2Mg + O 2MgO。(发出耀眼的强光,生成白色固体物质)
2
(2)与氮气反应: 3Mg + N MgN。(镁在空气中燃烧得到MgO和MgN 的混合物)
2 3 2 3 2
(3)与盐酸(或硫酸)反应: Mg + 2H + == =Mg 2 + + H ↑。
2
(4)与二氧化碳反应: 2Mg + CO 2MgO + C 。(镁着火不能用CO 灭火)
2 2
(5)与盐溶液反应,如与硫酸铜溶液反应: Mg + Cu 2 + == =Mg 2 + + Cu 。
(6)与水反应: Mg + 2H O Mg(OH) + H ↑。
2 2 2
2.镁的重要化合物
(1)氧化镁:白色粉末状固体,难溶于水,属于碱性氧化物,与盐酸反应的离子方程式为 MgO + 2H +
== =Mg 2 + + H O。
2
(2)氢氧化镁:白色固体,难溶于水,中强碱,与盐酸反应的离子方程式为 Mg(OH) + 2H + == =M g 2 + +
2
2HO。
2
【易错提醒】
氢氧化镁的溶解度小于碳酸镁,能发生反应MgCO +HO Mg(OH) +CO↑,镁元素在水垢中的存在
3 2 2 2
形式是Mg(OH) 。
2
3.从海水中提取镁的流程如图所示:
主要化学反应为
(1)制石灰乳:CaCO CaO + CO ↑ 、 CaO + H O == =Ca(OH) 。
3 2 2 2
(2)沉淀Mg2+: Mg 2 + + Ca(OH) == =Mg(OH) + C a 2 + 。
2 2(3)制备MgCl :Mg(OH) + 2HC l == =MgC l + 2H O 、 MgCl ·6H O MgCl + 6H O。
2 2 2 2 2 2 2 2
(4)电解MgCl :MgCl ( 熔融 ) Mg + Cl ↑。
2 2 2
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)镁在空气中燃烧可生成氧化镁和氮化镁。( )
(2)Mg能从CO 中置换出C。( )
2
(3)电解熔融MgCl 制2.4 g Mg,电路中通过的电子数为0.1N 。( )
2 A
(4)工业上冶炼金属镁也可以采用电解熔融MgO的方法。( )
(5)将Mg加入过量FeCl 溶液中可得Fe。( )
3
(6)加热MgCl 溶液最终可制得MgCl 固体。( )
2 2
(7)Mg表面易被氧化生成氧化膜,保存时一般直接放在塑料袋中或试剂瓶中。( )
(8)镁合金具有密度小、强度高的性质,可用于航空材料。( )
(9)氧化镁是优质的耐火材料。( )
【答案】1.√ 2.√ 3.× 4.× 5.× 6.× 7.√ 8.√ 9.√
考向01 考查镁及其化合物性质
【例1】(2024·山西大同·期末)在给定条件下,下列选项所示的物质间转化均能实现的是
A.
B.
C.
D.
【答案】B
【解析】A.电解熔融的氧化铝制铝而不是氯化铝,A错误;
B.氯化镁与氢氧化钙发生复分解反应生成氢氧化镁,氢氧化镁受热分解生成氧化镁,B正确;
C.铁与氯气反应生成 ,C错误;
D.电解熔融的 制取金属镁,D错误;
故选B。
考向02 通过工艺流程考查镁及其化合物
【例2】(2024·山东泰安·二模)碱式次氯酸镁[MgmClO(OH)n·H2O]微溶于水,不潮解,相对稳定,是一
种有开发价值的无机抗菌剂,以菱镁矿(MgCO3 ,含少量FeCO3)为主要原料,制备碱式次氯酸镁的工艺流
程如图,下列说法正确的是A.流程中酸溶后溶液中只含有Mg2+ 、Fe2+
B.调pH时所选试剂只能是MgCO3
C.过滤1所得的滤渣含有Fe(OH)3
D.“混合”时反应的离子方程式只有:Mg2++ClO-+OH-+H2O=MgClO(OH)·H2O↓
【答案】C
【分析】菱镁矿含少量FeCO3 ,用盐酸溶解,MgCO3 、FeCO3 都和盐酸反应分别生成MgCl2 、FeCl2 ,再加
入过氧化氢将Fe2+ 氧化为Fe3+ ,加入MgO、MgCO3 或Mg(OH)2 调节溶液pH,Fe3+ 使转化为Fe(OH)3 沉淀
过滤除去,滤液为MgCl2 溶液,向MgCl2 溶液中加入NaClO溶液、NaOH溶液得到[MgmClO(OH)n•H2O],
据此分析解题。
【解析】A.流程中酸溶后溶液中含有Mg2+ 、Fe2+ 、H+ ,还有阴离子,A错误;
B.调pH时所选试剂不只是MgCO3 ,MgO或Mg(OH)2 均可,B错误;
C.根据以上分析,过滤1所得的滤渣含有Fe(OH)3 ,C正确;
D.据该工艺流程所制备的物质为碱式次氯酸镁[MgmClO(OH)n·H2O],混合时发生反应的产物不仅是
MgClO(OH)·H2O,还有如Mg2ClO(OH)3•H2O等多种物质,D错误;
故选C。
【对点1】(2024·广东·模拟预测)Mg3N2 常用于制备其它超硬、耐高温的氮化物,实验室通过CuO氧化
NH3 制得N2 ,然后与镁反应得到Mg3N2. 已知Mg+2NH3 Mg(NH2)2+H2 ,Mg3N2 是一种浅黄色粉末,易水
解。下列说法错误的是
A.装置A中分液漏斗中的溶液为浓氨水
B.实验开始时应先点燃C处酒精灯,再点燃E处酒精灯
C.装置D的作用只是干燥N2
D.取反应后装置E所得固体少许,滴入蒸馏水,可检验是否有Mg3N2【答案】C
【分析】该实验主要是N2 与Mg在加热时反应生成Mg3N2 。A中长颈漏斗中是浓氨水,加入烧瓶中遇生
石灰释放NH3 ,B中碱石灰吸收NH3 中的水。在C装置中NH3 与CuO在加热情况下反应生成N2 ,D中浓
硫酸吸收N2 中的水和NH3 后,N2 进入E中与Mg反应。F装置可以防止空气中的CO2 、H2O等进入装置
中
与Mg及Mg3N2 反应。
【解析】A.装置A中分液漏斗中的溶液是浓氨水,流入烧瓶中与CaO接触会产生NH3 ,A正确;
B.实验进行时应先点燃C处的酒精灯,等产生的较纯的N2 进入E中时再点燃E中酒精灯,B正确;
C.装置D中浓硫酸吸收的是N2 中的水蒸气和氨气,因此不只是干燥氮气的作用,C错误;
D.取反应后装置E所得固体少许,滴入蒸馏水, Mg3N2 和水反应生成氢氧化镁和氨气,若闻到刺激性
气味,则有Mg3N2 ,D正确;
故选:C。
【对点2】(2024·安徽安庆·一模)菱镁矿(主要成分为 ,还含有少量 、 )制备 的流
程如图。下列说法正确的是
A.步骤(Ⅰ)得到的滤渣主要成分为 B.步骤(Ⅱ)发生的反应有2个
C.步骤(Ⅲ)操作可在蒸发皿中进行 D.滤液Y中加入足量氨水可得到白色沉淀
【答案】A
【分析】菱镁矿中加入盐酸,SiO2 不与盐酸反应,则滤渣为SiO2 ,滤液X中加入足量NaOH,生成氢氧
化镁沉淀和偏铝酸钠,滤液Y为偏铝酸钠,氢氧化镁灼烧生成氧化镁。
【解析】A.菱镁矿主要成分为 ,还含有少量 、 等,加入足量盐酸,过滤,滤渣是
,A正确;
B.滤液X中含有的阳离子主要有 、 、 ,加入足量 溶液后,发生的反应至少有3个,
B错误;
C.步骤(Ⅲ)灼烧在坩埚中进行,C错误;
D.滤液Y主要成分为 ,加入足量氨水无法生成白色沉淀,D错误;
故答案选A。
1.(2022·浙江舟山·三模)关于镁的性质,下列说法错误的是A.金属镁着火,可以用CO2 灭火 B.镁是一种具有银白色光泽的金属
C.镁可以与热水反应生成氢气 D.镁可以与盐酸剧烈反应生成氢气
【答案】A
【解析】A.镁能够在CO2 中燃烧,生成MgO和C,所以镁条着火不可以用CO2 灭火,A错误;
B.镁是一种银白色、有光泽、质软能导电的金属,B正确;
C.镁与热水反应,生成氢气和氢氧化镁,C正确;
D.镁的活泼性很强,与盐酸剧烈反应生成氯化镁和氢气,D正确;
故选A。
2.(2024·黑龙江哈尔滨·期中)下列物质的转化在给定条件下均能实现的一组是
A. B.
C. D.
【答案】A
【解析】A.铁高温的时候和水蒸气反应生成四氧化三铁和氢气,四氧化三铁和铝可以发生铝热反应生成
单质铁,A正确;
B.氧化铝和盐酸反应生成氯化铝溶液,氯化铝和氨水反应生成氢氧化铝沉淀,B错误;
C.硫在氧气中点燃生成的是二氧化硫不是三氧化硫,三氧化硫和水生成硫酸,C错误;
D.氮气和氧气在高温或放电条件下生成一氧化氮而不是二氧化氮,二氧化氮和水反应生成硝酸和NO,
D错误;
故选A。
3.(2024·浙江·三模)下列“类比合理的是
A. 在足量 中燃烧生成 ,则 在足量 中燃烧生成
B.铜丝在氯气中燃烧生成CuCl2 ,则铁丝在氯气中燃烧生成
C. 与 反应生成 和 ,则 与 反应可能生成 和
D.往 溶液中加入过量氨水生成 沉淀,则往 溶液中加入过量氨水生成 沉淀
【答案】C
【解析】A. 在足量 中燃烧生成 ,而 在足量 中燃烧生成SO2 ,故A错误;
B.氯气具有强氧化性,能够把变价金属氧化为最高价,因此铜丝在氯气中燃烧生成CuCl2 ,铁丝在氯气
中燃烧生成 ,故B错误;
C.由于二氧化碳过量,钠的氧化物能够与二氧化碳反应,所以 与 反应可能生成 和 ,
故C正确;
D.氢氧化铝不溶于过量的氨水,而氢氧化铜能够与过量的氨水反应生成Cu(NH3)4(OH)2 溶液,沉淀溶
解,故D错误;
故选C。
4.(2024·重庆·期中)下列离子在指定溶液中能大量共存的是
A.可与铝反应产生 的溶液中:B.澄清透明的溶液中:
C.新制氯水中:
D.使紫色石蕊变红的溶液:
【答案】B
【解析】A.与铝能产生H2 的溶液可能呈酸性也可能呈碱性,在碱性溶液中: 会生成NH3H2O,镁
离子会产生氢氧化镁沉淀, 在酸性溶液中会生成CO2 ,均不能大量共存, A错误; ∙
B.澄清透明的溶液中: 之间不反应,能够大量共存,B正确;
C.新制氯水中:亚铁离子、碘离子均能被氧化,不能大量共存,C错误;
D.使紫色石蕊溶液呈红色的溶液呈酸性,硅酸根、四羟基合铝酸根均能与 H+ 发生反应,且钡离子和硅
酸根能产生沉淀,不能大量共存, D错误;
答案选B。
5.(2024·福建泉州·期中)下列离子方程式书写正确的是
A.NaAlO2 溶液中通入过量CO2 :AlO +CO2+2H2O=Al(OH)3↓+HCO
B.向AlCl3 溶液中加入过量氨水:Al3++4OH-=AlO +2H2O
C.氯化铁溶液刻蚀铜制印刷电路板:Fe3++Cu=Fe2++Cu2+
D.铜与稀硝酸反应:Cu+4H++2NO =Cu2++2NO2↑+2H2O
【答案】A
【解析】A.NaAlO2 溶液中通入过量CO2 ,生成氢氧化铝和碳酸氢钠,离子方程式正确,A正确;
B.向AlCl3 溶液中加入过量氨水: ,B错误;
C.氯化铁溶液刻蚀铜制印刷电路板:2Fe3++Cu=2Fe2++Cu2+ ,C错误;
D.铜与稀硝酸反应:3Cu+8H++2NO =3Cu2++2NO↑+4H2O,D错误;
故选A。
6.(2024·安徽滁州·一模)部分含Al或含Si物质的价类二维图如下,下列推断正确的是(其中 为阿
伏加德罗常数的数值)
A.将木材浸入到g的水溶液可以防火
B.1mol晶体e中含有共价键的数目为C.肯定存在a→b→c和a→e→f的直接转化
D.d→c和g→f的转化均可通过向溶液中加入足量盐酸来实现
【答案】A
【分析】分析含Al或含Si物质可知,a为Al或Si,b为 ,c为 ,d为 ,e为
,f为H2SiO3 ,g为 ,据此作答。
【解析】A.g的水溶液为 的水溶液, 的水溶液俗称水玻璃,具有黏结力强、耐高温等特
性,可以用作黏合剂和防火剂,故A正确;
B.晶体e为 晶体, 晶体中每个Si原子与4个O原子形成共价键, 含有 ,
故B错误;
C. 不能一步反应生成 , 也不能一步反应生成 ,故C错误;
D.d为 ,向 溶液中加入足量盐酸生成的是AlCl3 溶液,g为 ,向
溶液中加入足量盐酸生成的是H2SiO3 ,故D错误;
故答案选A。
7.(2024·广西贺州·一模)镓( )与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合
物。工业制备镓的流程如图所示。下列推断不合理的是
A.向 溶液中逐滴加入足量稀氨水,先生成沉淀,后沉淀溶解
B.向 和 溶液中通入适量二氧化碳后得到氢氧化铝沉淀,可知酸性:
C.金属镓可以与 溶液反应生成 和
D.步骤二中不能通入过量的 的理由是
【答案】A
【分析】镓(Ga)与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。工业制备镓的流程
如图,分析可知氧化铝和氧化镓都可以与氢氧化钠溶液反应生成盐,并且二氧化碳可以制取氢氧化铝,却
无法与偏镓酸钠反应,可实现铝和镓的分离。
【解析】A.镓( )与铝同主族,曾被称为“类铝”,则其氢氧化物不会溶与弱碱氨水,向GaCl3 溶液中逐
滴加入足量氨水,有Ga(OH)3 沉淀生成,沉淀不溶解,A错误;
B.适量二氧化碳可以制取氢氧化铝,却无法与Na[Ga(OH)4]反应,说明酸性氢氧化铝比氢氧化镓弱,
,B正确;
C.铝能与氢氧化钠反应生成偏铝酸钠和氢气,所以金属镓也可以与NaOH溶液反应生成
和氢气,C正确;D.碳酸溶液为酸性,所以步骤二中不能通入过量的 是因为 会发生反应生成Ga(OH)3
沉淀, ,D正确;
故选A。
8.(2024·海南·一模)物质的性质决定用途。下列两者对应关系不正确的是
A.二氧化氯具有强氧化性,可用作饮用水消毒
B. 溶液呈酸性,可用于腐蚀电路板上的Cu
C. 呈弱碱性,可用于治疗胃酸过多
D. 受热分解,生成高熔点物质和水,常用作塑料的阻燃剂
【答案】B
【解析】A.二氧化氯具有强氧化性,是安全、无毒的绿色消毒剂,常用于饮用水的消毒,故A正确;
B.氯化铁溶液有氧化性,能与铜反应生成氯化亚铁和氯化铜,则氯化铁溶液可用于腐蚀电路板上的铜与
溶液呈酸性无关,故B错误;
C.氢氧化铝呈弱碱性,可与胃酸中的盐酸反应生成氯化铝和水,所以氢氧化铝用于治疗胃酸过多,故C
正确;
D.氢氧化铝受热分解生成的熔点高的氧化铝和水的反应是吸热反应,所以氢氧化铝常用作塑料的阻燃
剂,故D正确;故选B。
9.(2024·山东潍坊·二模)以水泥厂的废料(主要成分为 ,含少量
等杂质)为原料制备 的工艺流程如下:
已知: 下列说法正确的是
A.为提高酸浸速率,可使用浓硫酸 B.试剂X可以是
C.滤渣为 D.操作a所得滤液经处理后可循环利用
【答案】D
【分析】水泥厂的废料(主要成分为MgO,还有少量 等杂质)制取
MgSO4•7H2O,废料加入足量稀硫酸, 都与硫酸反应,转化为对应的硫
酸
盐,SiO2 不与硫酸反应,向反应后溶液中加入次氯酸钠溶液氧化亚铁离子为铁离子,同时使锰离子转化为
MnO2 沉淀,再加入氧化镁等物质调节溶液的pH值,除去锰离子、铁离子、铝离子,过滤,将滤液进行
一系列操作得到MgSO4•7H2O;据此分析解题。
【解析】A.适当升温(或粉碎或搅拌)即可提高浸取速率,不需要使用浓硫酸,故A错误;
B.试剂X为氧化镁或碳酸镁,不能为 ,故B错误;C.滤渣为 、MnO2 ,故C错误;
D.操作a是从溶液中经过一系列过程得到晶体,过滤时溶液中含有硫酸镁,为了提高原料中镁的利用
率,操作a后滤液的处理方法是将操作a后的母液循环利用,故D正确;
故答案选D。
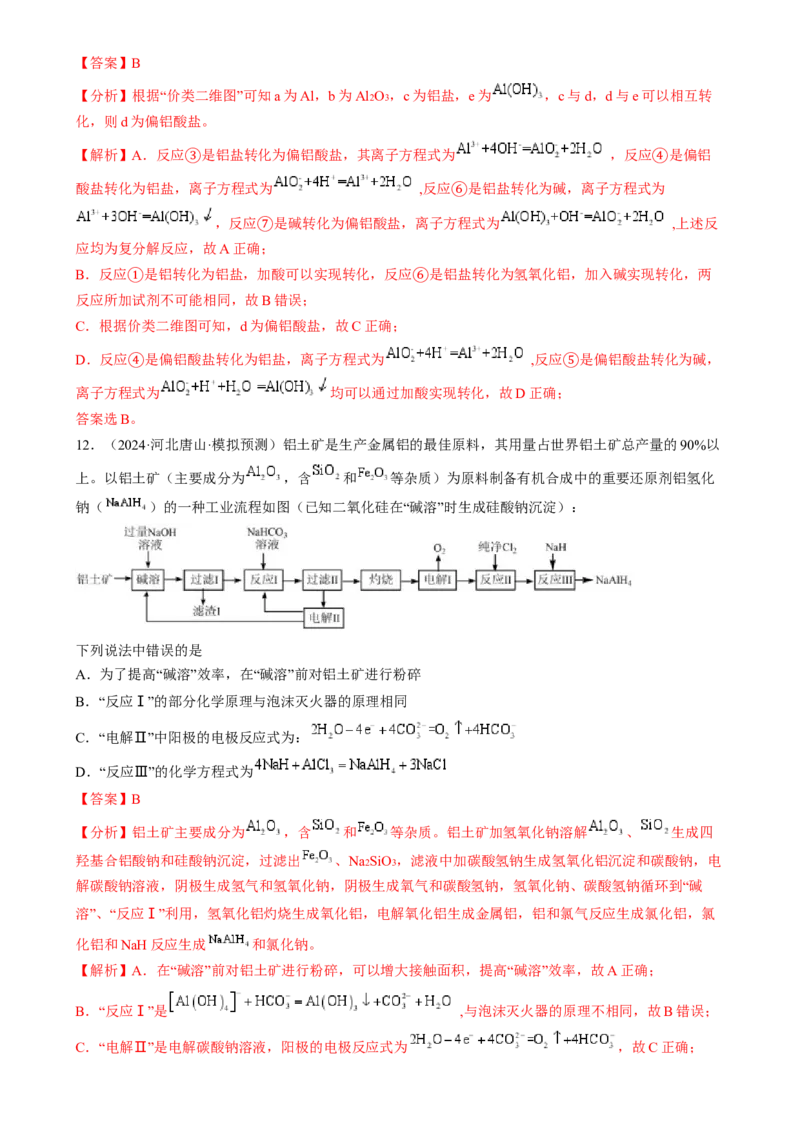
10.(2024·广东佛山·二模)部分含Mg或含Al物质的类别与化合价关系如图所示。下列推断不合理的是
A.a不能与 反应生成d或g
B.b和e均可用于制造耐高温材料
C.可存在a→f→g→e→a的循环转化关系
D.直接加热蒸干c或f溶液无法得到无水氯化物
【答案】A
【分析】由图知,a为Al或Mg,b为MgO,e为Al2O3 ,c为MgCl2 ,f为AlCl3 ,d为Mg(OH)2 ,g为
Al(OH)3 ,据此回答。
【解析】A.Mg能与 在加热条件下反应生成Mg(OH)2 ,A错误;
B.MgO和Al2O3 均可用于制造耐高温材料,B正确;
C.存在Al→AlCl3→Al(OH)3→Al2O3→Al的循环转化关系,C正确;
D.由于MgCl2 或AlCl3 均会水解,生成的氯化氢易挥发,直接加热蒸干MgCl2 或AlCl3 溶液无法得到无水
氯化物,D正确;故选A。
11.(2024·广东广州·模拟预测)“价类”二维图体现了元素的分类观、转化观,下图是 及其部分化合物
的“价类”二维图。下列说法错误的是
A.反应 均属于复分解反应 B.反应 所加试剂可能相同
C.物质的③类④别⑤处⑥“ ⑦ ”代表偏铝酸盐 D.反应①⑥均可以通过加入盐酸实现转化
④⑤【答案】B
【分析】根据“价类二维图”可知a为Al,b为Al2O3 ,c为铝盐,e为 ,c与d,d与e可以相互转
化,则d为偏铝酸盐。
【解析】A.反应 是铝盐转化为偏铝酸盐,其离子方程式为 ,反应 是偏铝
酸盐转化为铝盐,③离子方程式为 ,反应 是铝盐转化为碱,离子方程式为④
,反应 是碱转化为偏铝酸盐,离子方⑥程式为 ,上述反
应均为复分解反应,故A正确;
⑦
B.反应 是铝转化为铝盐,加酸可以实现转化,反应 是铝盐转化为氢氧化铝,加入碱实现转化,两
反应所加试剂不可能相同,故B错误;
① ⑥
C.根据价类二维图可知,d为偏铝酸盐,故C正确;
D.反应 是偏铝酸盐转化为铝盐,离子方程式为 ,反应 是偏铝酸盐转化为碱,
离子方程④式为 均可以通过加酸实现转化,故D正确;⑤
答案选B。
12.(2024·河北唐山·模拟预测)铝土矿是生产金属铝的最佳原料,其用量占世界铝土矿总产量的90%以
上。以铝土矿(主要成分为 ,含 和 等杂质)为原料制备有机合成中的重要还原剂铝氢化
钠( )的一种工业流程如图(已知二氧化硅在“碱溶”时生成硅酸钠沉淀):
下列说法中错误的是
A.为了提高“碱溶”效率,在“碱溶”前对铝土矿进行粉碎
B.“反应Ⅰ”的部分化学原理与泡沫灭火器的原理相同
C.“电解Ⅱ”中阳极的电极反应式为:
D.“反应Ⅲ”的化学方程式为
【答案】B
【分析】铝土矿主要成分为 ,含 和 等杂质。铝土矿加氢氧化钠溶解 、 生成四
羟基合铝酸钠和硅酸钠沉淀,过滤出 、Na2SiO3 ,滤液中加碳酸氢钠生成氢氧化铝沉淀和碳酸钠,电
解碳酸钠溶液,阴极生成氢气和氢氧化钠,阴极生成氧气和碳酸氢钠,氢氧化钠、碳酸氢钠循环到“碱
溶”、“反应Ⅰ”利用,氢氧化铝灼烧生成氧化铝,电解氧化铝生成金属铝,铝和氯气反应生成氯化铝,氯
化铝和NaH反应生成 和氯化钠。
【解析】A.在“碱溶”前对铝土矿进行粉碎,可以增大接触面积,提高“碱溶”效率,故A正确;
B.“反应Ⅰ”是 ,与泡沫灭火器的原理不相同,故B错误;
C.“电解Ⅱ”是电解碳酸钠溶液,阳极的电极反应式为 ,故C正确;D.“反应Ⅲ”是氯化铝和NaH反应生成 和氯化钠,化学方程式为 ,
故D正确;
选B。
13.(2024·重庆·期中)将一定质量的铝粉和铁粉的混合物加入到一定量很稀的硝酸溶液中,充分反应,
反应过程中无气体放出。向反应结束后的溶液中,逐滴加入5mol/L的NaOH溶液,所加NaOH溶液的体
积与产生沉淀的物质的量(n)关系如图所示,下列说法错误的是
A.根据关系图,硝酸被还原成铵盐 B.样品中铝粉和铁粉的物质的量之比为l 1
C.a点对应NaOH溶液的体积为20mL D.原溶液中硝酸的物质的量为0.37mol
∶
【答案】D
【分析】反应始终没有气体生成,可以得出不会有氮的氧化物生成,向反应后溶液溶液中滴加NaOH溶
液,开始没有沉淀生成,可知硝酸过量,故铝和铁被氧化为Al3+ 、Fe3+ ,反应后溶液加入氢氧化钠溶液应
先与硝酸反应,再生成沉淀,当沉淀完全后,由图知继续加入氢氧化钠溶液,沉淀量不变,可得与
发生了反应,则随着NaOH的滴加,发生的反应依次有: H++OH-=H2O, Fe3++3OH-=Fe(OH)3↓、
Al3++3OH-=Al(OH)3↓, +OH-=NH3•H2O, Al(OH①)3+OH-= ,②据此分析解题。
【解析】A.反应始终没有气体生成,可以得出不会有氮的氧化物生成,向反应后溶液溶液中滴加NaOH
③ ④
溶液,开始没有沉淀生成,可知硝酸过量,故铝和铁被氧化为Al3+ 、Fe3+ ,反应后溶液加入氢氧化钠溶液
应先与硝酸反应,再生成沉淀,当沉淀完全后,由图知继续加入氢氧化钠溶液,沉淀量不变,可知与
发生了反应,则硝酸被还原为铵盐(NH4NO3),A正确;
B.cd段消耗NaOH溶液8mL,根据Al(OH)3+OH-=+2H2O可知,n[Al(OH)3]=n(NaOH)=0.008L×5mol/
L=0.04mol,故n(Al)=n[Al(OH)3]=0.04mol,而bc段消耗的氢氧化钠的6mL,根据与 +OH-═NH3•H2O可
知,n( )=n(NaOH)=0.006L×5mol/L=0.03mol,根据电子转移守恒有::3n(Fe)+3n(Al)=8n( ),即
3n(Fe)+3×0.04mol=8×0.03mol,解得n(Fe)=0.04mol,则n(Al):n(Fe)=0.04mol:0.04mol=1:1,B正确;
C.根据电子转移守恒可知Al、Fe提供电子物质的量为8×0.03mol=0.24mol,由电荷守恒可知,ab段消耗
NaOH物质的量为0.24mol,ab段消耗NaOH溶液体积为 =0.048L=48mL,故a点对应NaOH溶液
体积为68mL-48mL=20mL,C正确;
D.加入氢氧化钠溶液为68mL时,溶液中溶质为硝酸钠与硝酸铵,n(NH4NO3)=n( )=0.03mol,根据
Na元素守恒有n(NaNO3)=n(NaOH)=0.068L×0.05mol/L=0.34mol,根据N元素守恒原硝酸溶液中
n(HNO3)=n(NaNO3)+2n(NH4NO3)=0.34mol+0.03mol×2=0.4mol,D错误;
故答案为:D。
14.(2024·浙江金华·期中)将17.9g由Cu、Al、Fe组成的合金溶于足量的NaOH溶液中,合金质量减少了2.7g。另取等质量的合金溶于过量稀 中,生成了6.72LNO(标准状况下),向反应后的溶液中加入
过量的NaOH溶液,则沉淀的质量为
A.22.1g B.25.4g C.33.2g D.30.2g
【答案】B
【解析】将17.9克由Cu、Al、Fe组成的合金溶于足量的NaOH溶液中,只有铝参与反应,则合金质量减
少的2.7克为Al,物质的量为0.1mol,将合金溶于过量稀硝酸中,分别生成Al3+ 、Fe3+ 、Cu2+ 离子,根
据转移电子守恒,金属总共失去电子物质的量等于HNO3 到NO得到的电子总数 ,,其中
0.1mol铝完全反应失去0.3mol电子,则Cu、Fe完全反应失去电子为0.9mol-0.3mol=0.6mol,反应中
Cu、Fe失去电子的物质的量等于生成碱的氢氧根离子的物质的量,则n(OH-)=0.6mol,所以反应后氢氧
化铜、氢氧化铁的质量为17.9g-2.7g+0.6mol×17g/mol=25.4g,答案选B。
15.(2024·山东青岛·一模)锂辉矿(主要成分为LiAlSi2O6)可用低温重构—直接浸出技术制备碳酸锂,同
时得到氧化铝,工艺流程如图。下列说法错误的是
A.“水热反应”为
B.“滤渣1”和“滤渣2”主要成分相同
C.冶炼金属锂和金属铝均可用电解其熔融氯化物的方法
D.流程中不涉及氧化还原反应
【答案】C
【分析】锂辉矿(主要成分为LiAlSi2O6)加NaOH溶液,发生反应生成硅酸锂沉淀、硅酸钠和偏铝酸钠;过
滤出硅酸锂,加硫酸溶解得到硅酸沉淀和硫酸锂溶液,硫酸锂溶液蒸发浓缩后加饱和碳酸钠得到碳酸锂;
含硅酸钠和偏铝酸钠的滤液1加硫酸,生成硫酸铝、硫酸钠和硅酸沉淀,过滤后,滤液中加氨水生成氢氧
化铝沉淀,过滤后煅烧生成氧化铝,据此解答。
【解析】A.“水热反应”中LiAlSi2O6 与NaOH反应生成相应的盐,反应为:
,故A正确;
B.“滤渣1”和“滤渣2”主要成分均为硅酸,故B正确;
C.AlCl3 为共价化合物,冶炼金属铝采用电解熔融氧化铝,故C错误。
D.流程中各步转化过程中均不存在化合价变化,不涉及氧化还原反应,故D正确;
故选:C。
1.(2024·浙江卷)下列说法不正确的是A. 呈两性,不能用于治疗胃酸过多
B. 能与 反应产生 ,可作供氧剂
C. 有还原性,能被氧化成
D. 见光易分解,应保存在棕色试剂瓶中
【答案】A
【解析】A. 呈两性,不溶于水,但可以与胃酸反应生成无毒物质,因此其能用于治疗胃酸过
多,A不正确;
B. 能与 反应产生 ,该反应能安全发生且不生成有毒气体,故 可作供氧剂,B正
确;
C. 有还原性,其中Fe元素的化合价为+2,用适当的氧化剂可以将其氧化成更高价态的 ,C正
确;
D.见光易分解的物质应保存在棕色试剂瓶中; 见光易分解,故其应保存在棕色试剂瓶中,D正
确;
综上所述,本题选A。
2.(2024·广东卷)部分含 或 或 物质的分类与相应化合价关系如图。下列推断合理的是
A.若a在沸水中可生成e,则a→f的反应一定是化合反应
B.在g→f→e→d转化过程中,一定存在物质颜色的变化
C.加热c的饱和溶液,一定会形成能产生丁达尔效应的红棕色分散系
D.若b和d均能与同一物质反应生成c,则组成a的元素一定位于周期表p区
【答案】B
【解析】A.若a在沸水中可生成e,此时a为Mg,e为Mg(OH)
2
,即f为镁盐,a→f的反应有多种,
可能为 ,该反应属于置换反应,可能为 ,该反应属于化合
反应,综上a→f的反应不一定是化合反应,故A错误;
B.e能转化为d,此时e为白色沉淀 ,d为红褐色沉淀 ,说明在g→f→e→d转化过程
中,一定存在物质颜色的变化,故B正确;
C.由题意得,此时能产生丁达尔效应的红棕色分散系为 胶体,c应为铁盐,加热铁盐的饱和溶
液,也有可能直接得到 沉淀,故C错误;
D.假设b为Al2O3 ,即d为 ,c为铝盐,Al2O3 、 与稀盐酸反应均生成铝盐,此时组成a的元素为Al,位于周期表p区;假设b为Fe2O3 ,即d为 ,c为铁盐,Fe2O3 、 与稀盐酸
反应均生成铁盐,此时组成a的元素为Fe,位于周期表d区,故D错误;
故选B。
3.(2023·天津卷)下列常见物质及用途,错误的是
A.氢氧化铝可用于治疗胃酸过多
B.SiO2 可用于制造光导纤维
C.Fe2O3 是铁红,可以用作染料
D.钠起火,可以使用水基灭火器扑灭
【答案】D
【解析】A.胃酸中含有HCl,氢氧化铝可以与HCl反应,能用于治疗胃酸过多,A正确;B.SiO2 具有
良好的光学特性,可用于制造光导纤维,B正确;C.Fe2O3 是一种红色粉末,俗称铁红,常用作红色染
料,C正确;D.钠能与水反应生成易燃性气体氢气,不能使用水基灭火器扑灭,D错误;故选D。
4.(2023·湖南卷)取一定体积的两种试剂进行反应,改变两种试剂的滴加顺序(试剂浓度均为
),反应现象没有明显差别的是
选项 试剂 试剂
① ②
A 氨水 溶液
B 溶液 溶液
C
溶液 酸性 溶液
D 溶液 溶液
【答案】D
【解析】A.向氨水中滴加 溶液并振荡,由于开始时氨水过量,振荡后没有沉淀产生,发生的反应
为 ,继续滴加产生沉淀;向 溶液中滴加氨水并
振荡,开始时生成白色沉淀且沉淀逐渐增多,发生的反应为 ;当
氨水过量后,继续滴加氨水沉淀逐渐减少直至沉淀完全溶解,发生的反应为
,因此,改变两种试剂的滴加顺序后反应现象有明显差别,A不
符合题意;B.向 中滴加 溶液并振荡,由于开始时 过量,振荡后没有沉淀产生,
发生的反应为 ;向 溶液中滴加 并振
荡,开始时生成白色沉淀且沉淀逐渐增多,发生的反应为 ;
当 过量后,继续滴加 沉淀逐渐减少直至沉淀完全溶解,发生的反应为
,因此,改变两种试剂的滴加顺序后反应现象有明显差别,B不符合题
意;C.向 溶液中滴加酸性 溶液并振荡,由于开始时 是过量的, 可以被
完全还原,可以看到紫红色的溶液褪为无色,发生的反应为;向 溶液中滴加酸性 溶液
并振荡,由于开始时 是过量的, 逐渐被 还原,可以看到紫红色的溶液逐渐变浅,
最后变为无色,因此,改变两种试剂的滴加顺序后反应现象有明显差别,C不符合题意;D.向 溶
液中滴加 溶液,溶液立即变为血红色;向 溶液中滴加 溶液,溶液同样立即变为血红
色,因此,改变两种试剂的滴加顺序后反应现象没有明显差别,D符合题意;综上所述,本题选D。
5.(2022·河北卷)NA 是阿伏加德罗常数的值。下列说法正确的是
A.3.9gNa2O2 与足量水反应,转移电子个数为0.1NA
B.1.2gMg在空气中燃烧生成MgO和Mg3N2 ,转移电子个数为0.1NA
C.2.7gAl与足量NaOH溶液反应,生成H2 的个数为0.1NA
D.6.0gSiO2 与足量NaOH溶液反应,所得溶液中SiO 的个数为0.1NA
【答案】B
【解析】A.过氧化钠与水反应生成氢氧化钠和氧气,则3.9g过氧化钠与足量水反应,转移电子个数为
×1×NAmol-1=0.05NA ,故A错误;B.镁在空气中燃烧无论生成氧化镁,还是氮化镁,镁均转化为
镁离子,则1.2gMg在空气中燃烧生成氧化镁和氮化镁时,转移电子个数为 ×2×NAmol-1=0.1NA ,
故B正确;C.铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,则2.7g铝与足量氢氧化钠溶液反应生成氢气
的个数为 × ×NAmol-1=0.15NA ,故C错误;D.二氧化硅与氢氧化钠溶液反应生成硅酸钠和水,
硅酸钠在溶液中发生水解反应,则由原子个数守恒可知,6.0g二氧化硅与足量氢氧化钠溶液反应所得溶液
中硅酸根离子的个数小于 ×NAmol-1=0.1NA ,故D错误;故选B。
6.(2022·浙江卷)下列说法不正确的是
A.晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维
B.高压钠灯发出的黄光透雾能力强、射程远,可用于道路照明
C.氧化铝熔点高,常用于制造耐高温材料
D.用石灰石-石膏法对燃煤烟气进行脱硫,同时可得到石膏
【答案】A
【解析】A.晶体硅的导电性介于导体和绝缘体之间,是良好的半导体材料,可用于制造晶体管、集成电
路等,而二氧化硅常用于制造光导纤维,A错误;B.钠的焰色反应为黄色,可用作透雾能力强的高压钠
灯,B正确;C.耐高温材料应具有高熔点的性质,氧化铝熔点高,可用作耐高温材料,C正确;D.石
灰石的主要成分为碳酸钙,石灰石-石膏法脱硫过程中发生反应:CaCO3 CaO+CO2↑,
SO2+CaCO3=CaSO3+CO2 ,2CaSO3+O2=2CaSO4 ,得到了石膏,D正确;答案选A。
7.(2022·全国卷)能正确表示下列反应的离子方程式为
A.硫化钠溶液和硝酸混合:S2-+2H+=H2S↑
B.明矾溶液与过量氨水混合:Al3++4NH3+2H2O=AlO +4NHC.硅酸钠溶液中通入二氧化碳:SiO +CO2+H2O=HSiO +HCO
D.将等物质的量浓度的Ba(OH)2 和NH4HSO4 溶液以体积比1 2混合:Ba2++2OH-+2H++SO
=BaSO4↓+2H2O
∶
【答案】D
【解析】A.硝酸具有强氧化性,可以将S2- 氧化为S单质,自身根据其浓度大小还原为NO或NO2 ,反应
的离子方程式为4H++2NO +S2-=S↓+2NO2↑+2H2O(浓)或8H++2NO +3S2-=3S↓+2NO↑+4H2O(稀),A错误;
B.明矾在水中可以电离出Al3+ ,可以与氨水电离出的OH- 发生反应生成Al(OH)3 ,但由于氨水的碱性较
弱,生成的Al(OH)3 不能继续与弱碱发生反应,故反应的离子方程式为Al3++3NH3·H2O=Al(OH)3↓+3NH
,B错误;C.硅酸的酸性小于碳酸,向硅酸钠溶液中通入二氧化碳时,生成硅酸沉淀,二氧化碳则根据
其通入的量的多少反应为碳酸根或碳酸氢根,反应的离子方程式为SiO +H2O+CO2=H2SiO3↓+CO (CO2
少量)或SiO +2H2O+2CO2=H2SiO3↓+2HCO (CO2 过量),C错误;D.将等物质的量浓度的Ba(OH)2 与
NH4HSO4 溶液以体积比1:2混合,Ba(OH)2 电离出的OH- 与NH4HSO4 电离出的H+ 反应生成水,Ba(OH)2
电离出的Ba2+ 与NH4HSO4 电离出的SO 反应生成BaSO4 沉淀,反应的离子方程为为Ba2++2OH-+2H++SO
=BaSO4↓+2H2O,D正确;故答案选D。
8.(2022·海南卷)依据下列实验,预测的实验现象正确的是
选项 实验内容 预测的实验现象
A 溶液中滴加NaOH溶液至过量 产生白色沉淀后沉淀消失
B 溶液中滴加KSCN溶液 溶液变血红色
C AgI悬浊液中滴加NaCl溶液至过量 黄色沉淀全部转化为白色沉淀
D 酸性 溶液中滴加乙醇至过量 溶液紫红色褪去
【答案】D
【解析】A.MgCl2 溶液中滴加NaOH溶液至过量,两者发生反应产生白色沉淀,白色沉淀为氢氧化镁,
氢氧化镁为中强碱,其不与过量的NaOH溶液发生反应,因此,沉淀不消失,A不正确;B.FeCl3 溶液中
滴加 KSCN洛液,溶液变血红色,实验室通常用这种方法检验的Fe3+ 存在;FeCl2 溶液中滴加 KSCN洛
液,溶液不变色,B不正确;C.AgI的溶解度远远小于AgCl,因此,向AgI悬浊液中滴加 NaCl溶液至
过量,黄色沉淀不可能全部转化为白色沉淀,C不正确;D.酸性KMnO4 溶液呈紫红色,其具有强氧化
性,而乙醇具有较强的还原性,因此,酸性KMnO4 溶液中滴加乙醇至过量后溶液紫红色褪去,D正确;
综上所述,依据相关实验预测的实验现象正确的是D,本题选D。
9.(2022·湖南卷)铝电解厂烟气净化的一种简单流程如下:
下列说法错误的是( )A.不宜用陶瓷作吸收塔内衬材料
B.采用溶液喷淋法可提高吸收塔内烟气吸收效率
C.合成槽中产物主要有NaAlF 和CO
3 6 2
D.滤液可回收进入吸收塔循环利用
【答案】C
【解析】陶瓷的成分中含有SiO,SiO 能与HF发生反应,因此不宜用陶瓷作吸收塔内衬材料,故A正
2 2
确;采用溶液喷淋法可增大反应物的接触面积,提高吸收塔内烟气吸收效率,故B正确;烟气(含HF)通
入吸收塔,加入过量的碳酸钠,发生反应:NaCO+HF===NaF+NaHCO ,向合成槽中通入
2 3 3
Na[Al(OH)],发生反应:6NaF+Na[Al(OH)]+4NaHCO ===Na AlF↓+4NaCO+4HO,过滤得到
4 4 3 3 6 2 3 2
NaAlF 和含有NaCO 的滤液,所以合成槽内产物主要有NaAlF、NaCO、HO,故C错误;滤液的主
3 6 2 3 3 6 2 3 2
要成分为NaCO,可进入吸收塔循环利用,故D正确。
2 3