文档内容
考点 12 硅及其无机非金属材料
高考对本考点内容的考查主要体现在以下三个方面:(1)结合STSE,以能源、温室效应等为背景,考
查碳(CO、CO)、硅及其重要化合物的性质、用途;(2)结合化学反应原理,考查碳酸、草酸与碱的滴定图
2
像与盐类水解的应用;(3)结合无机化工工艺流程,考查二氧化硅或硅酸盐的性质。
预计2023年高考仍然会结合能源、环保等,以新材料、新工艺为载体,考查碳、硅及其化合物的性质
及应用,以检测考生理论联系实际、运用化学理论解决实际问题的能力和将化学成果应用于生产、生活的
意识。
一、碳及其重要化合物
二、硅及其重要化合物
三、无机非金属材料
碳及其重要化合物
1.碳单质
存在形式有金刚石、石墨、无定形碳、足球烯,它们互为同素异形体。
2.碳的氧化物(CO和CO)
2
(1)一氧化碳的性质及应用
①物理性质:无色无味的气体,难溶于水,能使人中毒的原因是与人体内血红蛋白相结合,因缺氧而
中毒。
②化学性质及应用(写出有关化学方程式)
a.可燃性:2CO+O=====2CO,可作燃料。
2 2
b.还原性:CO还原Fe O 的反应为3CO+Fe O=====2Fe+3CO,可用于冶炼金属。
2 3 2 3 2
(2)CO 在自然界中的循环
2
①CO 的主要来源:大量含碳燃料的燃烧。
2
②自然界消耗CO 的主要反应:
2a.溶于江水、海水中:CO+HOHCO;
2 2 2 3
b.光合作用将CO 转化为O;
2 2
c.岩石的风化:CaCO +HO+CO===Ca(HCO )。
3 2 2 3 2
3.碳酸(H CO)
2 3
弱酸、不稳定。碳酸(H CO)只能在水中存在。HCO 在水中与CO 共存,因此常把CO +HO当碳酸
2 3 2 3 2 2 2
用。
4.碳酸的酸式盐和正盐的比较
(1)在水中的溶解性
①含K+、Na+、NH的正盐易溶于水,其余一般不溶于水;酸式盐均能溶于水。
②一般来说,在相同温度下,难溶性正盐溶解度小于其酸式盐溶解度,如溶解度:
Ca(HCO )>CaCO ;可溶性正盐溶解度大于其酸式盐溶解度,如溶解度:NaCO>NaHCO。
3 2 3 2 3 3
(2)热稳定性
一般来说,热稳定性顺序为正盐>酸式盐>碳酸,如稳定性:NaCO>NaHCO>H CO 。可溶性正盐>难
2 3 3 2 3
溶性正盐,如CaCO 高温分解,而KCO 不易分解。
3 2 3
(3)水溶液酸碱性
物质的量浓度相同时,正盐溶液的pH大于其酸式盐溶液,如pH:NaCO 溶液>NaHCO 溶液。
2 3 3
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)不同碳的物理性质差异是因为含碳量不同( )
(2)碳在氧气中充分燃料是放热反应,而不充分燃烧是吸热反应( )
(3)金刚石、石墨、C 都是由碳原元素组成的单质( )
60
(4)水墨画可长久保存不变色是因为在常温下碳的化学性质不活泼( )
(5)二氧化碳能使紫色石蕊溶液变红,说明二氧化碳具有酸性( )
(6)低碳环保中的“碳”是指二氧化碳( )
(7)石墨转变为金刚石的反应属于氧化还原反应(×)
(8)向空气中排放二氧化碳会形成酸雨(×)
(9)向CaCl 溶液中通入CO 气体,溶液变浑浊,继续通入CO 至过量,浑浊消失(×)
2 2 2
(10)氨化的饱和食盐水中通入足量的CO 气体,会析出晶体(√)
2
答案:(1)× (2)× (3)√ (4)√ (5)× (6)√ (7)× (8)× (9)× (10)√
【典例】
例1 “碳中和”是指CO 的排放总量和减少总量相当。下列措施中促进碳中和最直接有效的是( )
2
A.将重质油裂解为轻质油作为燃料 B.大规模开采可燃冰作为新能源
C.通过清洁煤技术减少煤燃烧污染 D.研发新型催化剂促使CO 转化为甲醇
2
【答案】D【解析】A项,将重质油裂解为轻质油作为燃料,实质是长链烃断裂为短链烃,燃烧后排放的CO 的
2
量并没有改变,A不符合题意;B项,可燃冰是甲烷的结晶水合物,大量开采使用,会产生CO,不利用
2
碳中和,B不符合题意;C项,通过清洁煤技术减少煤燃烧污染,只会减少SO 的排放,但对CO 的排放
2 2
总量无影响,C不符合题意;D项,研发催化剂将CO 还原为甲醇,有利于减少CO 的排放,对促进“碳
2 2
中和”最直接,D正确;故选D。
例2 中国力争在2030年前实现碳达峰、2060年前实现碳中和,关于碳及其化合物,下列说法不正确
的是( )
A.金刚石和石墨是碳的两种不同的单质,二者互称同素异形体
B.在100KPa时,1mol石墨转变为金刚石要吸收1.895kJ的热量,故金刚石比石墨稳定
C.考古时常用于测定文物年代的是碳元素的一种核素14C中,中子数为8
6
D.引起温室效应的气体之一CO 中含极性共价键
2
【答案】B
【解析】A项,金刚石和石墨均是由C元素组成的不同单质,两者互为同素异形体,A正确;B项,
能量越低,物质越稳定,因为在100KPa时,1mol石墨转变为金刚石要吸收1.895kJ的热量,所以可知石墨
比金刚石稳定,B错误;C项,14C 的质子数为6,质量数为14,所以中子数=14-6=8,C正确;D项,
6
CO 可引起温室效应,使全球变暖,其分子中C原子与O原子以共价双键结合,所以含极性共价键,D正
2
确;故选B。
【对点提升】
对点1 第十三届全国人民代表大会第四次会议政府工作报告指出“要扎实做好碳达峰、碳中和各项
工作”,绿色氢能和液态阳光甲醇可助力完成碳中和目标。下列说法正确的是( )
A.CHOH属于电解质
3
B.用焦炭与HO反应是未来较好获取氢能的方法
2
C.H 与CO 反应,每生成1molCH OH时转移4mol电子
2 2 3
D.植树造林、节能减排等有利于实现碳中和
【答案】D
【解析】A项,CHOH属于非电解质,A错误;B项,该工艺需消耗大量的能量,不节能,B错误;
3
C项,每生成1molCH OH时转移6mol电子,C错误;D项,植树造林、节能减排等有利于实现碳中和,D
3
正确;故选D。
对点2 中国努力争取2060年前实现碳中和。利用NaOH溶液喷淋捕捉空气中的CO ,反应过程如
2
图所示。下列说法错误的是( )A.捕捉室中NaOH溶液喷成雾状有利于吸收CO
2
B.环节a中物质分离的基本操作是蒸发结晶
C.反应过程中CaO和NaOH是可循环的物质
D.可用NaCO 溶液代替NaOH溶液捕捉CO
2 3 2
【答案】B
【解析】利用NaOH溶液实现“碳捕获”吸收器中,NaOH溶液用喷淋方式加入,增大反应物之间的
接触面积,充分吸收二氧化碳,环节a中,氧化钙与水反应生成氢氧化钙,碳酸钠与氢氧化钙反应生成碳
酸钙沉淀和氢氧化钠,NaCO 发生反应的化学方程式为NaCO+Ca(OH) =CaCO ↓+2NaOH,CaCO 需从溶
2 3 2 3 2 3 3
液中过滤出来再高温煅烧,生成的CO 循环使用。A项,NaOH溶液喷成雾状,可增大反应接触面积,提
2
高CO 吸收率,A正确;B项,环节a为NaCO 和Ca(OH) 生成CaCO ,需从溶液中过滤出来再高温煅烧,
2 2 3 2 3
故基本操作不是蒸发结晶,B错误;C项,NaOH和CaO在流程中既有消耗,也有生成,可循环利用,C
正确;D项,NaCO 可以和CO 反应,因此可用NaCO 溶液代替NaOH溶液,D正确。故选B。
2 3 2 2 3
【巧学妙记】硅及其重要化合物
1.硅单质
(1)存在
硅单质主要有晶体和无定形两大类。
(2)物理性质
带有金属光泽的灰黑色固体,熔点高,硬度大,有脆性。
(3)化学性质
①常温下不活泼,一般不与其他物质反应,但可以与氟、氢氟酸、碱反应。反应的化学方程式分别为:
与氟:Si+2F===SiF ;
2 4
与氢氟酸:Si+4HF===SiF ↑+2H↑;
4 2
与碱:Si+2NaOH+HO===Na SiO+2H↑。
2 2 3 2
②在加热或者点燃的条件下可以与氢气、氧气、氯气等反应,与氧气反应的化学方程式为 Si+O
2
SiO。
2
2.二氧化硅
(1)存在
自然界中,碳元素既有游离态,又有化合态,而硅元素仅有化合态,主要以氧化物和硅酸盐的形式存
在。天然SiO 有晶体和无定形两种,统称硅石。
2
(2)物理性质
熔点高,硬度大,难溶于水。
(3)结构
SiO 晶体有多种晶型,其基本结构单元为硅氧四面体(如下图甲所示),硅氧四面体通过氧原子相互连
2
接为空间的网状结构(如下图乙所示)。每个硅原子与4个氧原子相连,而每个氧原子与2个硅原子相连,
故SiO 晶体中Si和O的比例为1∶2。
2
(4)化学性质
SiO 为酸性氧化物,是硅酸的酸酐。
2
①)SiO 可以与碱反应,生成硅酸盐,如与氢氧化钠反应的化学方程式为 SiO +2NaOH===Na SiO +
2 2 2 3
HO。
2
②在高温条件下可以与碳酸盐反应,如与碳酸钙反应的化学方程式为 SiO +CaCO =====CaSiO +
2 3 3
CO↑。
2③在高温条件下,能够与碱性氧化物反应,如与氧化钙反应的化学方程式为 SiO +
2
CaO=====CaSiO 。
3
(4)常温下与氢氟酸反应的化学方程式为SiO+4HF===SiF ↑+2HO。
2 4 2
3.硅酸
(1)物理性质
硅酸的溶解度小,新制备的硅酸为透明、胶冻状,干燥硅胶多孔,吸水性和吸附性强。
(2)化学性质
①弱酸性:酸性比碳酸弱,与NaOH溶液反应的化学方程式为:HSiO+2NaOH===Na SiO+2HO。
2 3 2 3 2
②不稳定性:受热易分解,反应的化学方程式为:HSiO SiO+HO。
2 3 2 2
(3)制备:通过可溶性硅酸盐与其他酸反应制得,如 NaSiO 溶液与盐酸反应:NaSiO +
2 3 2 3
2HCl===2NaCl+HSiO(胶体)。
2 3
(4)用途:硅胶可用作干燥剂、催化剂的载体等。
4.硅酸盐
(1)硅酸盐是由硅、氧和金属组成的化合物的总称,是构成地壳岩石的主要成分。
(2)硅酸钠:硅酸钠溶液俗称水玻璃,是无色黏稠液体,常用于制备黏合剂、防腐剂、耐火材料。
(3)硅酸盐写成氧化物形式的顺序:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水,不同氧化物
间以“·”隔开。
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)硅在自然界中只以化合态的形式存在( )
(2)晶体硅熔点高、硬度大,故可用于制作半导体材料( )
(3)Si和SiO 都可用于制造光导纤维( )
2
(4)非金属性:C>Si,则热稳定性:CH>SiH( )
4 4
(5)硅的化学性质不活泼,常温下不与任何物质反应( )
(6)SiO 是酸性氧化物,可溶于强碱(NaOH),不溶于任何酸( )
2
(7)硅酸钠的水溶液俗称“水玻璃”,是一种建筑行业常用的黏合剂(正)
(8)SiO 能与HF反应,因此可用HF刻蚀玻璃( )
2
(9)向NaSiO 溶液中逐滴加入稀盐酸制备硅酸凝胶(√)
2 3
(10)石英是良好的半导体材料,可以制成光电池,将光能直接转化成电能( )
(11)硅是非金属元素,它的单质是灰黑色有金属光泽的固体( )
(12)用二氧化硅制取单质硅的反应中硅元素被氧化( )
(13)加热到一定温度时,硅能与氢气、氧气等非金属发生反应( )
(14)工业上制取粗硅的反应是SiO+C=====Si+CO↑( )
2 2
(15)用二氧化硅制取单质硅时,当生成2.24 L气体(标准状况)时,得到2.8 g硅( )
(16)因为高温时二氧化硅与碳酸钠反应放出二氧化碳,所以硅酸酸性比碳酸强( )
(17)二氧化硅为立体网状结构,其晶体中硅原子和硅氧单键个数之比为1∶2( )答案:(1)√ (2)× (3)× (4)√ (5)× (6)× (7)√ (8)√ (9)√ (10)× (11)√ (12)× (13)√
(14)× (15)× (16)× (17)×
【典例】
例1 东方光源集团公司、中国逸通控股有限公司共同投资35亿元国内最先进的光纤光缆项目,成功
落户安徽滁州市风阳县硅工业园,其一期工程计划于2012年11月竣工。下列有关硅材料的说法正确的是
( )
A.光纤的主要成分是高纯度的单质硅 B.金刚砂的主要成分是二氧化硅
C.28 g硅含有6.02×1023个电子 D.28Si、29Si、30Si是不同的核素
【答案】D
【解析】A项,光纤的主要成分是二氧化硅,A错误;B项,金刚砂的主要成分是碳化硅,B错误;C
项,28 g硅的物质的量是1mol,其中含有14×6.02×1023个电子,C错误;D项,28Si、29Si、30Si的质子数相
同,但中子数不同,是不同的核素,且互为同位素,D正确。
例2 水玻璃(Na SiO 溶液)广泛应用于耐火材料、洗涤剂生产等领域,是一种重要的工业原料。如图
2 3
是用稻壳灰(SiO:65%~70%、C:30%~35%)制取水玻璃的工艺流程:
2
下列说法正确的是( )
A.原材料稻壳灰价格低廉,且副产品活性炭有较高的经济价值
B.操作A与操作B完全相同
C.该流程中硅元素的化合价发生改变
D.反应器中发生的复分解反应为SiO+2NaOH===Na SiO+HO
2 2 3 2
【答案】A
【解析】A项,稻壳灰来源广泛价格低廉,活性碳具有吸附性,有较高的经济价值,A正确;B项,操
作A为过滤,操作B为蒸发浓缩,是两种不同的操作,B错误;C项,二氧化硅中,硅元素的化合价是+4
价,硅酸钠中,硅元素的化合价是+4价,所以该流程中硅元素的化合价没有发生改变,C错误;D项,
复分解反应是指由两种化合物相互交换成分,生成另外两种新的化合物的反应,反应SiO +2NaOH=
2
NaSiO+HO不属于复分解反应,D错误。
2 3 2
【对点提升】
对点1 纯二氧化硅可用下列流程制得.下列说法不正确的是A.X可用作木材防火剂
B.步骤Ⅱ的反应是NaSiO+H SO ═H SiO(胶体)+ Na SO
2 3 2 4 2 3 2 4
C.步骤Ⅱ中的稀硫酸可用CO 来代替
2
D.SiO 既能与盐酸反应,又能与氢氟酸反应,所以SiO 是两性氧化物
2 2
【答案】D
【解析】A项,硅酸钠水溶液具有阻燃性,可用作木材防火剂,A正确;B项,硅酸钠与稀硫酸反应
生成硅酸沉淀,所以步骤II的反应是NaSiO+H SO ═H SiO(胶体)+Na SO ,B正确;C项,碳酸、硫酸的
2 3 2 4 2 3 2 4
酸性都强于硅酸,能够置换硅酸,C正确;D项,SiO 既能和NaOH溶液反应又能和氢氟酸反应,但与氢
2
氟酸反应的生成物不是盐,所以二氧化硅不是两性氧化物,而是酸性氧化物,D不正确。
对点2 高纯度晶硅是典型的无机非金属材料,又称“半导体”材料。它的发现和使用曾引起计算机
的一场“革命”。可以按下列方法制备:
SiO――→Si(粗)――→SiHCl ―――――→Si(纯)
2 3
下列说法不正确的是( )
A.步骤①的化学方程式为:SiO+C=====Si+CO↑
2 2
B.步骤①中每生成1 mol Si,转移4 mol电子
C.高纯硅是制造太阳能电池的常用材料,二氧化硅是制造光导纤维的基本原料
D.SiHCl (沸点33.0 ℃)中含有少量的SiCl (沸点67.6 ℃),通过蒸馏(或分馏)可提纯SiHCl
3 4 3
【答案】A
【解析】A项,二氧化硅高温下与C反应生成CO气体,即步骤①的化学方程式为:SiO +2C=====Si
2
+2CO↑,故A错误;B项,步骤①中Si的化合价降低4,转移电子数为4 mol,故B正确;C项,高纯硅
是半导体,是制造集成电路、太阳能电池的常用材料,二氧化硅是制造光导纤维的基本原料,故 C正确;
D项,沸点相差30 ℃以上的两种液体可以采用蒸馏的方法分离,故D正确。
【巧学妙记】
在设计制备纯硅的实验题中,常遇到的知识点
(1)高温下用碳还原二氧化硅制得粗硅:SiO+2C=====Si(粗)+2CO↑
2
(2)粗硅与干燥HCl气体反应制得SiHCl :Si(粗)+3HCl=====SiHCl +H
3 3 2
(3)粗硅与干燥Cl 反应制得SiCl :Si(粗)+2Cl=====SiCl
2 4 2 4
(4)SiHCl 与过量H 在高温下反应制得纯硅:SiHCl +H=====Si(纯)+3HCl
3 2 3 2
(5)SiCl 与过量H 在高温下反应制得纯硅:SiCl +2H=====Si(纯)+4HCl
4 2 4 2
(6)SiO+2Mg=====2MgO+Si
2
(7)SiHCl 、SiCl 能与水发生反应:SiHCl +3HO===H SiO↓+3HCl+H↑
3 4 3 2 2 3 2
SiCl +3HO===H SiO↓+4HCl
4 2 2 3
(8)SiH 在空气中易自燃:SiH+2O===SiO +2HO
4 4 2 2 2无机非金属材料
1.传统无机非金属材料,如水泥、玻璃、陶瓷等硅酸盐材料。
(1)常见硅酸盐材料比较
水泥 玻璃 陶瓷
生产原料 石灰石、黏土 纯碱、石灰石、石英 黏土
主要设备 水泥回转窑 玻璃窑 陶瓷窑
(2)玻璃生产中的两个重要反应:NaCO +SiO=====NaSiO +CO↑;CaCO +SiO=====CaSiO +
2 3 2 2 3 2 3 2 3
CO↑。
2
2.新型无机非金属材料,如高温结构陶瓷、光导纤维、生物陶瓷、压电陶瓷等。
3.复合材料
(1)概念:将两种或两种以上性质不同的材料经特殊加工而制成的一种新型材料。
(2)组成
①基体:在复合材料中起黏结作用。
②增强体:在复合材料中起骨架作用。
(3)分类
①按基体
②按增强体形状
(4)性能:既保持或发展了原来材料的长处,又能弥补原材料的不足
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)工业生产水泥和玻璃均用到石灰石( )
(2)氮化硅陶瓷和氮化铝陶瓷均为新型无机非金属材料( )
(3)钢化玻璃与普通玻璃的主要成分基本相同( )
(4)玻璃是一种晶体,有较高的熔点( )
(5)水玻璃是一种特殊的玻璃,泡花碱属于碱( )
(6)玻璃钢是以玻璃纤维做增强体、合成树脂做基体的复合材料( )
(7)氮化硅是一种重要的结构陶瓷材料,化学式为Si N( )
3 4
(8)碳化硅(SiC)的硬度大,熔点高,可用于制作高温结构陶瓷和轴承( )
(9)光导纤维是一种新型无机非金属材料,其主要成分为SiO( )
2
(10)水泥、玻璃、青花瓷、水晶、玛瑙都属于硅酸盐工业产品( )
答案:(1)√ (2)√ (3)√ (4) × (5)× (6)√ (7)√ (8)√ (9)√ (10)×
【典例】
例1 下列关于硅酸盐工业的叙述正确的是( )A.普通玻璃的主要成分可以表示为NaO·CaO·6SiO ,说明玻璃为纯净物
2 2
B.陶瓷、玻璃、水泥都属于硅酸盐产品
C.制玻璃、水泥时都用到了石灰石和黏土
D.制玻璃的过程中发生了反应:NaCO+SiO=====NaSiO+CO↑,说明酸性:HSiO>H CO
2 3 2 2 3 2 2 3 2 3
【答案】B
【解析】普通玻璃的主要成分可以表示为NaO·CaO·6SiO ,还含有其他杂质,因此玻璃属于混合物,
2 2
A错误;陶瓷、玻璃、水泥都属于传统的硅酸盐产品,B正确;制造玻璃的主要原料是石灰石、纯碱和石
英,制造水泥的主要原料是石灰石、黏土和辅助原料,C错误;反应NaCO+SiO=====NaSiO+CO↑,
2 3 2 2 3 2
不是在溶液中进行的,利用的是难挥发性酸制备易挥发性酸原理,事实上碳酸的酸性强于硅酸的酸性,在
溶液中碳酸可以制备硅酸,D错误。
例2 《天工开物》记载:“凡埏泥造瓦,掘地二尺余,择取无砂粘土而为之”,“凡坯既成,干燥
之后,则堆积窖中燃薪举火”,“浇水转釉(主要为青色),与造砖同法”。下列说法错误的是( )
A.粘土是制作砖瓦和陶瓷的主要原料
B.“燃薪举火”使粘土发生复杂的物理化学变化
C.沙子和粘土的主要成分均为硅酸盐
D.烧制后自然冷却成红瓦,浇水冷却成青瓦
【解析】制作砖瓦和陶瓷的主要原料是粘土,故A错误;,粘土的主要成分均为硅酸盐,灼烧使粘土
发生复杂的物理化学变化,故B正确;沙子的主要成分是二氧化硅,粘土的主要成分均为硅酸盐,故C错
误;浇水转釉(主要为青色),与造砖同法,所以烧制后自然冷却成红瓦,浇水冷却成青瓦,故D正确。
【答案】C
【对点提升】
对点1 “九秋风露越窑开,夺得千峰翠色来”是赞誉越窑秘色青瓷的诗句,描绘我国古代精美的青
瓷工艺品。玻璃、水泥和陶瓷均为硅酸盐制品,下列有关说法中正确的是( )
A.玻璃是人类最早使用的硅酸盐制品
B.制水泥的原料为纯碱、石灰石和石英
C.硅酸盐制品的性质稳定、熔点较高
D.沙子和黏土的主要成分均为硅酸盐
【答案】C
【解析】陶瓷是人类最早使用的硅酸盐制品,A项错误;纯碱、石灰石和石英是制玻璃的原料,而制
水泥的原料是黏土和石灰石,B项错误;硅酸盐制品性质稳定、熔点高,C项正确;沙子的主要成分是
SiO,黏土的主要成分是硅酸盐,D项错误。
2
对点2 宋代五大名窑分别为:钧窑、汝窑、官窑、定窑、哥窑。其中钧窑以“入窑一色,出窑万
彩”的神奇窑变著称。下列关于陶瓷的说法不正确的是( )
A.窑变是高温下釉料中的金属化合物发生氧化还原反应导致的颜色变化B.氧化铝陶瓷属于新型无机非金属材料
C.高品质的瓷器晶莹剔透,属于纯净物
D.陶瓷属于硅酸盐材料,耐酸碱腐蚀,但是不能用来盛装氢氟酸
【答案】C
【解析】不同的金属氧化物颜色可能不同,在高温下,釉料中的金属化合物发生氧化还原反应导致的
颜色变化称为窑变,故A正确;新型无机非金属材料主要有先进陶瓷、非晶体材料、人工晶体、无机涂层,
无机纤维等,氧化铝陶瓷属于新型无机非金属材料,故 B正确;瓷器的原料主要是黏土烧结而成,瓷器中
含有多种硅酸盐和二氧化硅,是混合物,故C错误;HF能与二氧化硅反应,陶瓷的成分是硅酸盐和二氧
化硅,所以陶瓷不能用来盛装氢氟酸,故D正确。
【巧学妙记】
陶瓷 普通玻璃 普通水泥
纯碱(Na CO)、石灰石 主要原料:石灰石、黏土
原料 黏土 2 3
(CaCO 3 )、石英砂(SiO 2 ) 辅助原料:适量的石膏
设备 陶瓷窑 玻璃熔炉 水泥回转窑
硅酸三钙(3CaO·SiO )、硅酸二钙
主要 硅酸钠(Na SiO)、硅酸钙 2
成分复杂 2 3 (2CaO·SiO )、铝酸三钙
成分 (CaSiO 3 )、二氧化硅(SiO 2 ) (3CaO·Al O 2 )
2 3
抗氧化、抗酸 玻璃是非晶体,称为玻璃态物
具有水硬性,与水掺和搅拌并静置
特点 碱腐蚀、耐高 质,无固定熔点,在某一温度
后,很容易凝固变硬
温、绝缘 范围内软化可加工成制品
建筑材料、绝
缘材料、日用 建筑材料、光学仪器、各种器
用途 大量用于建筑和水利工程
器皿、卫生洁 皿、制造玻璃纤维
具
1.下列关于硅的说法不正确的是( )
A.硅是非金属元素,晶体硅是灰黑色有金属光泽的固体
B.硅的导电性能介于金属和绝缘体之间,是良好的半导体材料
C.硅的化学性质不活泼,常温下不与任何物质发生反应
D.加热到一定温度时,硅能与氯气、氧气等非金属单质反应
【答案】C
【解析】硅的化学性质不活泼,但常温下仍能与氟气、氢氟酸、NaOH溶液等发生反应,加热至一定
温度时,硅能与氯气、氧气等发生反应。
2.中国是瓷器的故乡,下列关于陶瓷的说法正确的是( )
A. 高品质的白瓷晶莹剔透,属于纯净物B. 瓷器中含有大量的金属元素,因此陶瓷属于金属材料
C. 氮化硅陶瓷属于传统无机非金属材料
D. “窑变”是高温下釉料中的金属化合物发生氧化还原反应导致颜色的变化
【答案】D
【解析】A项,瓷器是主要原料黏土烧结而成,瓷器中含有多种硅酸盐,是混合物,A错误;B项,
尽管瓷器中含有大量的金属元素,但是陶瓷不属于金属材料,因为其中的金属元素是以化合态存在的。陶
瓷属于无机非金属材料,B错误;C项,氮化硅陶瓷属于新型无机非金属材料,是高温结构材料,可用于
制造陶瓷发动机的受热面,C错误;D项,不同的金属氧化物颜色可能不同,在高温下,釉料中的金属化
合物发生氧化还原反应导致颜色发生变化,D正确;故选D。
3.下列关于硅材料的说法不正确的是( )
A.钢化玻璃与普通玻璃的主要成分基本相同
B.制普通玻璃的原料是石灰石、纯碱和石英砂
C.陶瓷是人类应用很早的硅酸盐材料
D.水玻璃是纯净物,可用于生产黏合剂和防火剂
【答案】D
【解析】A项,钢化玻璃就是将普通退火玻璃先切割成要求尺寸,然后加热到接近软化点的700度左
右,再进行快速均匀的冷却而得到的玻璃,故钢化玻璃与普通玻璃的主要成分基本相同,A正确;B项,
玻璃是传统硅酸盐产品,制普通玻璃的原料主要是纯碱、石灰石和石英,故B正确;C项,陶瓷是传统无
机非金属材料,是人类应用很早的硅酸盐材料,故C正确;D项,水玻璃为硅酸钠的水溶液,属于混合物,
故D错误。故选D。
4.我国具有独立知识产权的电脑芯片“龙芯一号”的问世,填补了我国计算机制造史上的一项空白。
下列对晶体硅的有关叙述正确的是( )
A. 晶体硅的结构与金刚石类似
B. 晶体硅的化学性质不活泼,常温下不与任何物质发生反应
C. 晶体硅是一种良好的半导体材料,但是它提炼工艺复杂,价格昂贵
D. 晶体硅具有金属光泽,故它属于金属材料,可以导电
【答案】A
【解析】A项,晶体硅为正四面体结构,与金刚石类似,A正确;B项,晶体硅常温下可以与氢氟酸
反应,B错误;C项,晶体硅是一种良好的半导体材料,但是它提炼工艺不复杂,价格不高,已经被普及
使用,C错误;D项,晶体硅有金属光泽,可以导电,但它属于非金属材料,D错误;故选A。
5.在20世纪90年代末,科学家发现碳有新的单质形态C 存在。后来人们又相继得到了C 、C 、
60 70 76C 、C 、C 等另外一些球碳分子。21世纪初,科学家又发现了管状碳分子和洋葱状碳分子,大大丰富了
84 90 94
碳元素单质的家族。下列有关碳元素单质的说法错误的是
A.金刚石和石墨的熔点肯定比C 高
60
B.熔点:C <C <C
60 70 90
C.球碳分子、管状碳分子和洋葱状碳分子都是分子晶体,都是碳的同素异形体
D.金刚石以非分子形式的粒子存在,属于原子晶体;C 、C 、管状碳分子和洋葱状碳分子以分子形
60 70
式的粒子存在,属于分子晶体;这些碳单质不互为同素异形体
【答案】D
【解析】A项,金刚石属于原子晶体,石墨属于混合晶体,C 属于分子晶体,因此金刚石和石墨的熔
60
点肯定要比C 高,故A正确;B项,分子晶体的相对分子质量越大,熔点越高,因此熔点:C <C <
60 60 70
C ,故B正确;C项,球碳分子、管状碳分子和洋葱状碳分子都是碳元素形成的不同单质,所以均为碳的
90
同素异形体,故C正确;D项,金刚石属于原子晶体,不存在分子;C 、C 、管状碳分子和洋葱状碳分
60 70
子都是分子晶体,以分子形式存在;都是碳元素形成的不同单质,互为同素异形体,故D错误;故选D。
6.中国在探索太空,开发深海,建设世界第一流的高铁、桥梁、码头,5G技术联通世界等方面取得
了举世瞩目的成就,它们与化学有着密切联系,下列说法正确的是( )
A.中国天眼的“眼眶”是钢铁结成的圈梁,属于新型无机非金属材料
B.为打造生态文明建设,我国近年来大力发展核电、光电、风电、水电,电能属于一次能源
C.我国提出网络强国战略,光缆线路总长超过三千万公里,光缆的主要成分是二氧化硅
D.“神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶瓷的主要成分是硅酸盐
【答案】C
【解析】A项,中国天眼的“眼眶”,索网结构是FAST主动反射面的主要支撑结构,不是新型无机
非金属材料,故A错误; B项,电能不是一次能源,属于二次能源,故B错。
C项,二氧化硅具有良好的光学特性,是制造光缆的主要原料,故 C正确;D项,高温结构陶瓷包括
氮化硅陶瓷,氮化硼陶瓷,碳化硼陶瓷,故D 错误; 故选C
7.硅是构成无机非金属材料的一种主要元素,下列有关硅及其化合物的叙述错误的是( )
A.氮化硅陶瓷是一种高温结构陶瓷,其化学式为Si N
3 4
B.高纯硅可以制成计算机、通信设备等的芯片C.硅可以用来生产新型无机非金属材料——光导纤维
D.二氧化硅为立体网状结构,每个硅原子结合4个氧原子
【答案】C
【详解】A项,氮化硅陶瓷是一种高温结构陶瓷,氮化硅中各元素的原子最外层达到8电子稳定结构,
Si原子最外层电子数为4,N原子最外层电子数为5,要形成8电子稳定结构,则二者个数比值为3∶4,
其化学式为Si N,故A正确;B项,高纯硅具有良好的半导体性能,可以制成计算机、通信设备等的芯片,
3 4
故B正确;C项,光导纤维的主要成分是二氧化硅,属于新型无机非金属材料,故C错误;D项,二氧化
硅为原子晶体,为立体网状结构,其晶体中每个硅原子结合4个氧原子,每个氧原子结合2个硅原子,硅
原子和氧原子个数之比为1∶2,故D正确;故选C。
8.纯二氧化硅可用下列流程制得.下列说法不正确的是( )
A.X可用作木材防火剂
B.步骤Ⅱ的反应是NaSiO+H SO ═H SiO(胶体)+ Na SO
2 3 2 4 2 3 2 4
C.步骤Ⅱ中的稀硫酸可用CO 来代替
2
D.SiO 既能与盐酸反应,又能与氢氟酸反应,所以SiO 是两性氧化物
2 2
【答案】D
【解析】A项,硅酸钠水溶液具有阻燃性,可用作木材防火剂,A正确;B项,硅酸钠与稀硫酸反应
生成硅酸,所以步骤II的反应是NaSiO+H SO ═H SiO(胶体)+Na SO ,B正确;C项,碳酸、硫酸的酸性
2 3 2 4 2 3 2 4
都强于硅酸,能够与硅酸钠溶液反应生成硅酸,C正确;D项,SiO 既能和NaOH溶液反应又能和氢氟酸
2
反应,但与氢氟酸反应的生成物不是盐,所以二氧化硅不是两性氧化物,而是酸性氧化物,D不正确;故
选D。
9.硅是带来人类文明的重要元素之一,从传统材料到信息材料的发展过程中创造了一个又一个奇迹。
(1)新型陶瓷Si N 的熔点高、硬度大、化学性质稳定。工业上可以采用化学气相沉积法,在 H 的保护
3 4 2
下 , 使 SiCl 与 N 反 应 生 成 Si N 沉 积 在 石 墨 表 面 , 写 出 该 反 应 的 化 学 方 程 式 :
4 2 3 4
________________________________________________________________________。
(2)一种工业用硅(含少量钾、钠、铁、铜的氧化物),已知硅的熔点是1 420 ℃,高温下氧气及水蒸气
能明显腐蚀氮化硅。一种合成氮化硅的主要工艺流程如下:①净化N 和H 时,铜屑的作用是______________,硅胶的作用是________________。
2 2
②在氮化炉中发生反应3SiO(s)+2N(g)===Si N(s)+3O(g) ΔH=-727.5 kJ·mol-1,开始时,严格控
2 2 3 4 2
制氮气的流速以控制温度的原因是__________________;体系中要通入适量的氢气是为了
___________________________________________________________。
③X可能是__________________(填“盐酸”“硝酸”“硫酸”或“氢氟酸”)。
(3)工业上可以通过如图所示的流程制取纯硅:
①整个制备过程必须严格控制无水无氧。SiHCl 遇水剧烈反应,写出该反应的化学方程式:
3
__________________________________________________________。
②假设每一轮次制备1 mol纯硅,且生产过程中硅元素没有损失,反应Ⅰ中HCl的利用率为90%,反
应Ⅱ中 H 的利用率为 93.75%。则在第二轮次的生产中,补充投入 HCl 和 H 的物质的量之比是
2 2
______________。
【答案】(1)3SiCl +2N+6H===Si N+12HCl
4 2 2 3 4
(2)①除去原料气中的氧气 除去生成的水蒸气
②该反应是放热反应,防止局部过热,导致硅熔化成团,阻碍与N 的接触 将体系中的氧气转化为水
2
蒸气,而易被除去(或将整个体系中空气排尽) ③硝酸
(3)①SiHCl +3HO===H SiO↓+3HCl+H↑ ②5∶1
3 2 2 3 2
【解析】(1)根据原子个数守恒可写出化学方程式 3SiCl +2N +6H===Si N +12HCl。(2)①由于氧气
4 2 2 3 4
和水蒸气都能腐蚀氮化硅,而氮气和氢气中含有水蒸气和氧气,所以铜屑的作用是除去氧气,硅胶的作用
是除去水蒸气。②因为该反应是放热反应,如果温度过高,局部过热,会导致硅熔化成团,阻碍与 N 的接
2
触;通入氢气能将体系中的氧气转化为水蒸气,而易被除去。③由于工业用硅中含有铜的氧化物,在反应
中氧化铜能被还原生成铜,因此要除去铜应该选择硝酸,盐酸和硫酸不能溶解铜,氢氟酸能腐蚀氮化硅。
(3)①SiHCl 遇水剧烈反应生成HSiO 、HCl和氢气:SiHCl +3HO===H SiO↓+3HCl+H↑。②反应生成
3 2 3 3 2 2 3 2
1 mol纯硅需补充HCl(-3) mol,需补充H(-1) mol,补充HCl与H 的物质的量之比为5∶1。
2 2
10.水泥是重要的建筑材料,硅酸盐水泥主要为硅酸二钙(2CaO·SiO )、硅酸三钙(3CaO ·SiO )、铝酸
2 2
三钙(3CaO·Al O)。铁铝酸四钙(4CaO·Al O·Fe O)和氧化镁等的混合物。《水泥化学分析方法》中用
2 3 2 3 2 3
EDTA(一种常用作滴定金属离子含量的有机物)滴定法测定水泥样品中钙、镁的含量。其过程如图所示:
已知:相关金属离
子浓度为0.1mol/L时,形成氢氧化物沉淀的pH范围如表:金属离子 Mg2+ Ca2+ Al3+ Fe3+
开始沉淀的pH 11 13.5 3.5 2
完全沉淀的pH 13 >14 4.5 3.5
回答下列问题:
(1)工业制水泥的主要原料是黏土和______(填名称)。
(2)步骤①中选择用银坩埚而不用瓷坩埚,其理由是_____.滤渣的主要成分为_____。(填化学式)。
(3)步骤③中加入的酒石酸钠和三乙醇胺作为掩蔽剂,可掩蔽杂质离子的干扰,在该过程中,主要掩蔽
的离子有_____。 掩蔽剂需要在调pH前加入,若在碱性溶液中则起不到掩蔽作用,试从要掩蔽的离子性
质分析原因:_______。
(4)步骤④和⑤中,调pH时,最好选用试剂_____(填序号)。
A.氨水 B.MgO C.CaCO
3
(5)水泥样品中的钙的含量通过步骤④滴定结果可计算得出;而步骤⑤滴定的是钙、镁总量,所以测定
镁的含量准确性还依赖于步骤④。当溶液pH大于12时,会生成硅酸钙沉淀,所以若滴定前,溶液中还有
少量的硅酸,则需加入适量氟化钾,以消除硅酸的干扰。若未加氟化钾,残留的硅酸会使镁含量测定结果
______(填“偏高”“偏低”或“无影响”)。
(6)镁含量的测定还受水泥试样中一氧化锰含量的影响,当一氧化锰含量小于0.5%时,干扰不明显,
可忽略不计;但大于0.5%时,还需要再测出一氧化锰含量。一氧化锰的测定是在硫酸介质中,用高碘酸钾
将其氧化为高锰酸根离子,进行测量。写出该过程中反应的离子方程式:______(该反应中的一种产物可以
作为食盐的添加剂)。
【答案】(1)石灰石 氢
(2)氧化钠会与二氧化硅反应,腐蚀瓷坩埚 HSiO
2 3
(3)Al3+和Fe3+ 碱性溶液中,Al3+和Fe3+会生成Al(OH) 沉淀和Fe(OH) 沉淀
3 3
(4)A (5)偏高 (6)2MnO+5IO -+H O=2 MnO-+5IO -+2H+
4 2 4 3
【解析】(1)工业制水泥的主要原料是黏土和石灰石;(2)瓷坩埚中含有二氧化硅,加热熔融时氢氧化钠
和二氧化硅反应,会腐蚀瓷坩埚;由分析可知,加入足量盐酸酸化后,过滤得到硅酸滤渣;(3)由题意可知,
步骤③中加入的酒石酸钠和三乙醇胺作为掩蔽剂,掩蔽铁离子和铝离子,防止加入EDTA时对钙、镁含量
测定的干扰;在碱性溶液中,铁离子和铝离子会转化为氢氧化铁沉淀和氢氧化铝沉淀,则在调溶液pH前
加入掩蔽剂,起不到掩蔽作用;(4)调节溶液pH时,若加入氧化镁和碳酸钙,会使溶液中钙离子和镁离子
的量增大,影响测定结果,所以调节溶液pH的试剂最好为氨水,故答案为A;(5)由题意可知,当溶液pH
大于12时,会生成硅酸钙沉淀,若滴定前不加入适量氟化钾消除硅酸的干扰,会导致测得钙离子的量偏低,计算出的镁离子含量偏高;(6)由题意可知,酸性条件下,高碘酸钾与一氧化锰发生氧化还原反应生成碘酸
钾和高锰酸,反应的离子方程式为2MnO+5IO -+H O=2 MnO-+5IO -+2H+。
4 2 4 3
1.(2022·广东省高三模拟预测)广东一直是我国对外交流的重要窗口,馆藏文物是其历史见证。下列
文物主要由硅酸盐制成的是( )
文物
选项 A.南宋鎏金饰品 B.蒜头纹银盒 C.广彩瓷咖啡杯 D.铜镀金钟座
【答案】C
【解析】A项,鎏金饰品是用金汞合金制成的金泥涂饰器物的表面,经过烘烤,汞蒸发而金固结于器
物上的一种传统工艺,其中不含硅酸盐,故A项不符合题意;B项,蒜头纹银盒中主要成分为金属银,其
中不含硅酸盐,故B项不符合题意;C项,广彩瓷咖啡杯是由黏土等硅酸盐产品烧制而成,其主要成分为
硅酸盐,故C项符合题意;D项,铜镀金钟座是铜和金等制得而成,其中不含硅酸盐,故D项不符合题意;
故选C。
2.(2022·北京市第一六一中学三模)改革开放40年,我国取得了很多世界瞩目的科技成果,下列说法
不正确的是( )
B.用到石墨烯,是碳原 C.用到的氮化硅陶瓷
A.用到钛合金,22号钛 D.传输信息用的光纤
子紧密堆积成单层二维蜂 是新型无机非金属材
元素属于过渡元素 材料是硅
窝状晶格结构的新材料 料
【答案】D
【解析】A项,钛元素的原子序数为22,位于元素周期表第四周期IVB族,属于过渡元素,故A正确;
B项,石墨烯是碳原子紧密堆积成单层二维蜂窝状晶格结构的新材料,故B正确;C项,氮化硅陶瓷是性能优良的新型无机非金属材料,故C正确;D项,光纤材料的主要成分是二氧化硅,故D错误;故选D。
3.(2022·广东省三模)北京冬奥会系列设计充满了化学知识。下列说法错误的是( )
A B C D
光纤主要成分是二氧化 石墨烯是有机高分 头盔具有外壳硬、内壳软、
该制冰过程是物理过程
硅 子材料 防护性能好的特性
【答案】C
【解析】A项,所谓光导纤维,就是依靠光在线缆中进行内全反射从而达到用光进行载体传输信息的
介质,光纤主要成分是二氧化硅,故A正确;B项,干冰升华时吸热,该过程属于物理变化,故B正确;
C项,石墨烯是无机非金属材料,故C错误;D项,碳纤维及一些高分子化合物具有硬、强度大、防护性
能优等特点,头盔具有外壳硬、内壳软、防护性能好的特性,故D正确;故选C。
4.(2022·广东省佛山市高三第二次教学质量监测)文物是传承文化的重要载体,下列主要成分不是硅
酸盐的文物是( )
简牍 陶彩绘女舞俑 清雍正款霁红釉瓷碗 萧何月下追韩信图梅瓶
A B C D
【答案】A
【解析】A项,简牍主要成分为植物纤维,A符合题意;B项,陶彩绘女舞俑,陶制品为硅酸盐材料,
B不符合题意;;D项,梅瓶也是瓷器,为硅酸盐材料,D不符合题意;故选A。
5.(2022·上海市二模)“碳中和”是指CO 排放总量和减少总量相当。下列措施对实现“碳中和”没有
2帮助的是( )
A.植树造林 B.风力发电 C.燃煤脱硫 D.绿色出行
【答案】C
【解析】A项,植树造林可以吸收二氧化碳,减少二氧化碳总量,A项正确;B项,风力发电代替部
分火力发电,可减少煤炭的燃烧,从而减少二氧化碳排放量,B项正确;C项,燃煤脱硫,只能减少二氧
化硫的排放,无法减少C燃烧释放的二氧化碳,C项错误;D项,绿色出行可以减少汽车等尾气排放的二
氧化碳,D项正确;故选C。
6.(2022·山东省高三模拟预测)下列有关说法与碳达峰、碳中和无关的是( )
A.北京冬奥火炬使用氢燃料 B.我国科学家以CO 为原料合成淀粉
2
C.化石燃料脱硫 D.种植“碳中和林”
【答案】C
【解析】A项,使用氢燃料,可以减少化石燃料的使用,减少CO 的排放,有利于降低空气中CO 的
2 2
含量,与碳中和、碳达峰有关,A不符合题意;B项,以CO 为原料合成淀粉,有利于降低空气中CO 的
2 2
含量,与碳中和、碳达峰有关,B不符合题意;C项,化石燃料脱硫,不能减少CO 的排放,与碳中和、
2
碳达峰无关,C符合题意;D项,种植“碳中和林”,有利于降低空气中CO 的含量,与碳中和、碳达峰
2
有关,D不符合题意;故选C。
7.(2022·海南省高三学业考试)我国宣布力争到2060年前实现“碳中和”目标。“碳中和” 是指CO
2
的排放总量和减少总量相当,下列做法不利于实现“碳中和”的是( )
A.大量使用煤炭 B.将CO 再生转化成资源
2
C.开发利用核能 D.人工光合作用消耗CO
2
【答案】A
【解析】A项,大量使用煤炭,会增加二氧化碳的排放量,A符合题意;B项,将CO 再生转化成资
2
源,实现资源化利用,能减少空气中二氧化碳的含量,与碳中和目标实现有关,B不符合题意;C项,开
发利用核能,可以减少化石能源的使用,减少二氧化碳的排放,有利于实现“碳中和”,C不符合题意;
D项,人工光合作用消耗CO,可以减少二氧化碳的总量,D不符合题意;故选A。
2
8.(2022•·河北省邯郸市高三模拟考试)下列关于硼、硅及其化合物的说法中错误的是( )
A.可用HBO 溶液来中和溅在皮肤上的碱液
3 3
B.Si与HF的反应中体现了HF的还原性
C.B O 熔融时可以与多种碱性氧化物反应
2 3
D.NaSiO 溶液可用作木材防火剂和黏合剂
2 3
【答案】B【解析】A项,HBO 酸性较弱,可中和溅在皮肤上的碱液,A正确;B项,Si与HF的反应,HF体
3 3
现的是氧化性,B错误;C项,B O 是酸性氧化物,熔融时可以与多种碱性氧化物反应,C正确;D项,
2 3
NaSiO 溶液可用作木材防火剂和黏合剂,D正确。故选B。
2 3
9.(2022·湖北省黄冈中学三模)2022年4月16日,神舟十三号载人飞船返回舱在东风着陆场成功着陆,
三名航天员平安凯旋。下列说法正确的是( )
A.具有耐高温和高度密封性的返回舱舷窗玻璃属于传统无机非金属材料
B.返回舱表面的烧蚀材料由玻璃纤维与合成树脂复合而成,属于新型无机非金属材料
C.烧蚀材料应具有高熔点、高沸点、难分解的特性,从而保护返回舱的安全
D.返回舱次外层的“避火衣”热容量大、熔点高,由钛合金制成,属于金属材料
【答案】D
【解析】A项,耐高温和高度密封性的玻璃属于新型无机非金属材料,普通玻璃属于传统无机非金属
材料,A项错误;B项,玻璃纤维与合成树脂复合而成,属于复合材料,B项错误;C项,烧蚀材料应具
有较低熔点、较低沸点、易分解的特性,从而保护返回舱的安全,C项错误;D项,钛合金热容量大、熔
点高,属于金属材料,D项正确;故选D。
10.(2022·河北省石家庄市部分学校高三模拟考试)生产生活中的各种“玻璃”的说法正确的是( )
A.钢化玻璃和普通玻璃成分不相同,但都属于硅酸盐产品
B.有机玻璃的主要成分聚甲基丙烯酸甲酯属于天然有机高分子材料
C.“水玻璃”的主要成分是硅酸钠的水溶液,可用作矿物胶
D.石英玻璃熔点高、硬度大,可制作加热NaOH、NaCO 等固体的仪器
2 3
【答案】C
【解析】A项,钢化玻璃是将普通玻璃高温后骤降温度得到,二者成分相同,都属于硅酸盐产品;A
错误;B项,有机玻璃属于有机合成高分子材料,B错误;C项,“水玻璃”的主要成分是硅酸钠的水溶
液,可以用作矿物胶,C正确;D项,石英玻璃主要成分是二氧化硅,属于酸性氧化物,会与NaOH、
NaCO 等碱性物质发生反应,所以不能制作加热NaOH、NaCO 等固体的仪器,D错误;故选C。
2 3 2 3
11.(2022·河北省衡水中学一模)无机非金属材料在生产生活中应用广泛。下列说法错误的是( )
A.玻璃纤维用于高强度复合材料,其主要成分为玻璃B.陶瓷是一种常见硅酸盐材料,可以用陶瓷坩埚熔融纯碱
C.碳纳米材料是一类新型无机非金属材料,其中石墨烯具有导电性
D.碳化硅俗称金刚砂,可用作砂纸、砂轮的磨料
【答案】B
【解析】A项,玻璃纤维是纤维状的玻璃,其主要成分为玻璃,常用于高强度复合材料,故A正确;
B项,陶瓷中的硅酸盐在高温条件下能与纯碱反应,故B错误;C项,碳纳米材料的主要成分为碳,属于
新型无机非金属材料,石墨烯具有石墨的层状结构,具有导电性,故C正确;D项,碳化硅为共价晶体,
具有高硬度,可用作砂纸、砂轮的磨料,故D正确;故选B。
12.(2022·河北省邯郸市二模)近年来中国的航天技术发展迅速,天宫、天和、天舟、巡天、问天、梦
天、天问、神舟等等体现了中国的强大科技力量,下列说法不正确的是( )
A.为航天器量身定制的柔性三结砷化镓太阳电池阵首次在“天和”号使用,砷化镓属于半导体
B.“天宫”空间站使用石墨烯存储器,所用材料石墨烯与金刚石互为同分异构体
C.“天问一号”火星车使用热控保温材料----纳米气凝胶,可产生丁达尔效应
D.“神州十三号”飞船返回舱外面是一层耐高温的陶瓷材料,属于无机非金属材料
【答案】B
【解析】A项,砷化镓是良好的半导体材料,故A正确; B项,石墨烯与金刚石都是由碳元素构成的
不同单质,属于同素异形体,故B错误;C项,新型纳米气凝胶做热控材料,气凝胶是分散在空气中,分
散剂是气体,可产生丁达尔效应,故C正确;D项,氮化硼陶瓷基材料属于新型无机非金属材料,故D正
确;故选B。
13.(2022·河南省濮阳市高三模拟)2022年2月在北京举办的冬季奥运会中,使用了许多功能各异的材
料,下列有关材料的描述中不正确的是( )
A.陶瓷、玻璃、水泥属于传统的无机非金属材料
B.石墨烯、富勒烯和碳纳米管属于新型有机非金属材料
C.硅是应用最为广泛的半导体材料
D.通讯中使用的光导纤维,主要成分为SiO
2
【答案】B
【解析】A项,玻璃、陶瓷、水泥的主要成分是硅酸盐类,都属于传统的无机非金属材料,A正确;
B项,碳纳米管、富勒烯、石墨烯都是新型无机非金属材料,B不正确;C项,晶体硅导电性介于导体与
绝缘体之间,是应用最广泛的良好的半导体材料,C正确;D项,光导纤维的主要成分是二氧化硅,D正
确;故选B。
14.(2022·广东省珠海市第二中学高三模拟)中国科技改变世界。下列说法错误的是( )A.“天机芯”是全球首款异构融合类脑计算芯片,其主要成分和光导纤维相同
B.“天问一号”火星车使用热控保温材料纳米气凝胶,可产生丁达尔效应
C.“雷霆之星”速滑服采用银离子抗菌技术,可有效防护细菌侵入
D.“天和”核心舱电推进系统中的腔体采用的氮化硼陶瓷属于新型无机非金属材料
【答案】A
【解析】A项,光导纤维是用二氧化硅生产的,通信容量大,抗干扰性能好,传输信号不易衰减,能
有效提高通信效率。而芯片利用了高纯硅的半导体性能广泛应用于信息技术和新能源技术等领域,A错误;
B项,热控保温材料纳米气凝胶的粒径大小在1nm-100nm间,此分散系为胶体,可产生丁达尔效应,B正
确;C项,银离子为重金属离子,能使蛋白质变性,有杀菌消毒的作用,故可用于抗菌技术,防护细菌侵
入,C正确;D项,氮化硼陶瓷具有多种优良性能,可用做高温、高压、绝缘、散热部件、航天航空业中
的热屏蔽材料,属于新型无机非金属材料, D正确;故选A。
15.(2022·天津市和平区三模)制造芯片用到高纯硅,用SiHCl (沸点:31.85℃,SiHCl 遇水会剧烈反
3 3
应,易自燃)与过量H 在1100~1200℃反应制备高纯硅的装置如图所示(夹持装置和尾气处理装置略去),下
2
列说法不正确的是( )
A.整个实验的关键是控温、检查装置气密性和排尽装置中的空气
B.装置II、III中依次盛装的是浓HSO 、温度高于32℃的温水
2 4
C.实验时,先打开装有稀硫酸仪器的活塞,收集尾气验纯,再预热装置IV石英管
D.尾气处理可直接通入NaOH溶液中
【答案】D
【解析】由实验装置可知,I中Zn与稀硫酸反应生成氢气,II中浓硫酸干燥氢气,Ⅲ中气化的SiHCl
3
与过量H 混合,Ⅳ中高温下反应硅,且SiHCl 遇水发生SiHCl +3H O═H SiO+H ↑+3HCl。A项,SiHCl 的
2 3 3 2 2 3 2 3
沸点为31.85°C,且易自燃,因而整个实验的关键是控温、检查装置气密性和排尽装置中的空气,故A正
确;B项,装置Ⅱ中浓HSO 可干燥氢气,Ⅲ中盛装温度高于32℃的温水,目的是使滴入烧瓶中的SiHCl
2 4 3
气化,与氢气反应,故B正确;C项,实验时应先打开装有稀硫酸仪器的活塞制取氢气,用氢气将装置内
的空气排出,收集尾气验纯,再预热装置Ⅳ石英管,防止氢气不纯加热易爆炸,故C正确;D项,SiHCl
3与氢气在1100~1200°C反应制备高纯硅,因而处理尾气时,因该在通入NaOH溶液前加上防倒吸装置,故
D错误;故选D。
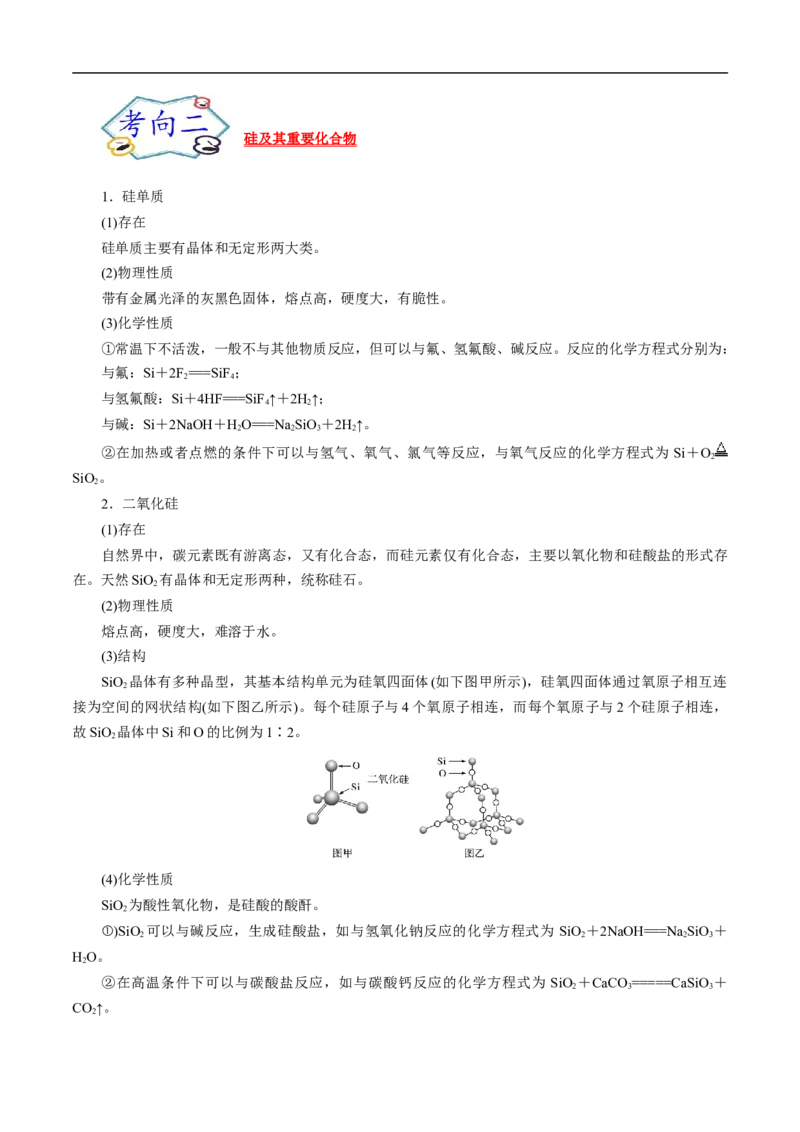
16.(2022·山东师范大学附中模拟预测)部分含碳物质的分类与相应碳元素的化合价关系如图所示。下
列说法错误的是( )
A.固态p可做制冷剂用于人工降雨
B.p转化为r可通过化合反应来实现
C.m转化为n或o的反应均释放能量
D.n的一种同素异形体中既存在共价键也存在范德华力
【答案】C
【解析】依据价类二维图可知:m为甲烷、n为碳单质、o为CO、p为CO、r为碳酸盐。A项,p为
2
二氧化碳,可做制冷剂用于人工降雨,A项正确;B项,二氧化碳与氧化钙反应生成盐碳酸钙,是化合反
应实现,B项正确;C项,甲烷转化为二氧化碳是放热反应,C项错误;D项,碳有多种同素异形体,如
金刚石、石墨等,石墨既存在共价键也存在范德华力,D项正确;故选C。
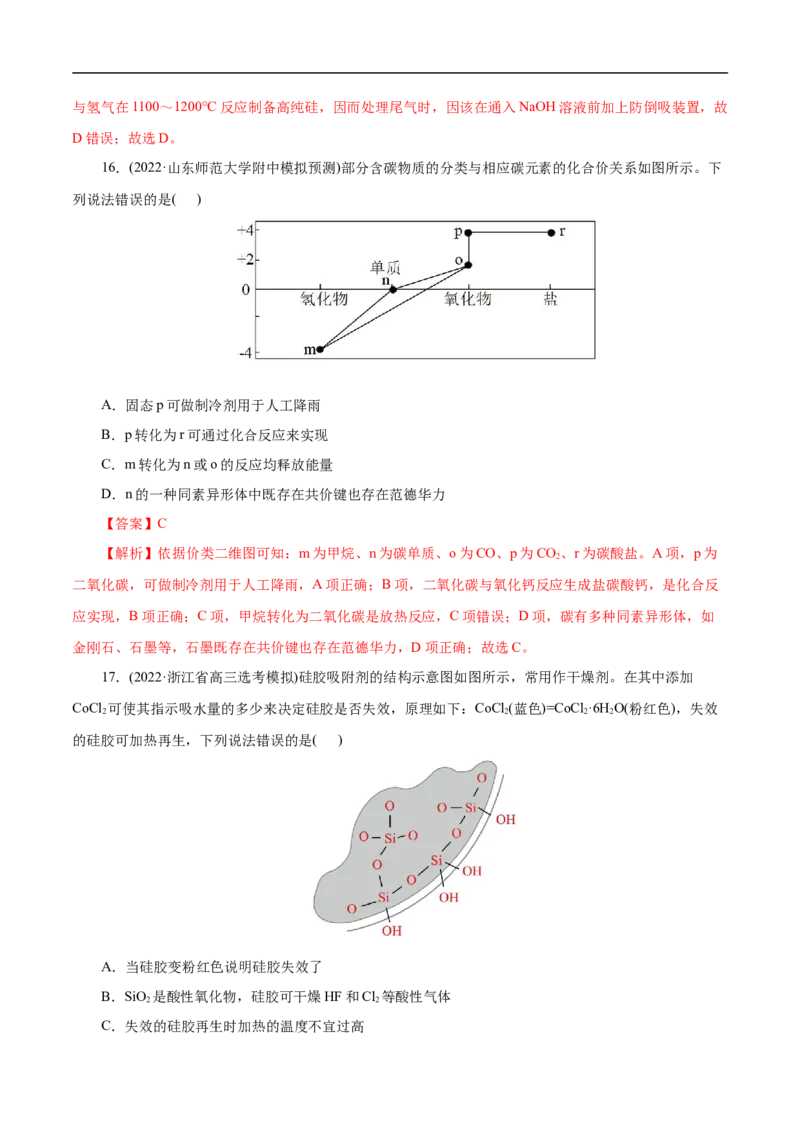
17.(2022·浙江省高三选考模拟)硅胶吸附剂的结构示意图如图所示,常用作干燥剂。在其中添加
CoCl 可使其指示吸水量的多少来决定硅胶是否失效,原理如下:CoCl (蓝色)=CoCl ·6H O(粉红色),失效
2 2 2 2
的硅胶可加热再生,下列说法错误的是( )
A.当硅胶变粉红色说明硅胶失效了
B.SiO 是酸性氧化物,硅胶可干燥HF和Cl 等酸性气体
2 2
C.失效的硅胶再生时加热的温度不宜过高D.当硅胶遇到大量的水分子时,与硅羟基形成了过多氢键从而失去吸附力
【答案】B
【解析】A项,由题中信息可知,硅胶吸水后,会变成蓝色的CoCl ·6H O(粉红色),故变成粉红色后
2 2
则说明硅胶失效了,A正确;B项,二氧化硅可以和HF反应,故硅胶不能干燥HF,B错误;C项,温度
过高会因显色剂逐步氧化而失去显色作用,C正确;D项,由硅胶结构可知,硅胶用作干燥剂,是通过硅
羟基和水分子之间形成氢键而达到吸水的目的,故当硅胶遇到大量的水分子时,与硅羟基形成了过多氢键
从而失去吸附力,D正确;故选B。
18.(2022·北京市十一学校三模)AX 四面体(T )在无机化合物中很常见。T 按图所示方式相连,可形成
4 1 1
一系列“超四面体”(T 、T…),下列说法正确的是( )
2 3
A.超四面体系列的各物质最简式相同
B.AX 每个面都是正三角形,键角为
4
C.SiO、SiC、SiCl 等硅的化合物均可形成超四面体系列
2 4
D.AX 四面体形成的无限三维结构对应的晶体可能为共价晶体
4
【答案】D
【解析】A项,T、T 和T 的化学式分别为AX 、AX 和A X ,故超四面体系列的各物质最简式不
1 2 3 4 4 10 10 20
相同,A错误;B项,AX 是正四面体结构,每个面都是正三角形,但是键角为 ,B错误;C项,
4
观察“超四面体”(T 、T…)结构图,不难发现A为中心原子,与四个X连接,应为硅、锗等原子;而X
2 3
为配位原子,可以与两个A原子相连,应为氧、硫等原子,表明SiO、SiC可形成超四面体系列,SiCl 不
2 4
可以形成超四面体系列,C错误;D项,共价晶体的微观空间中没有分子,可无限延伸,AX 四面体形成
4
的无限三维结构对应的晶体可能为共价晶体,D正确;故选D。
19.(2022·上海市南洋模范中学高三等级考试模拟预测)硅是构成矿物和岩石的主要成分,单质硅及其
化合物具有广泛的用途。某些硅酸盐具有筛选分子的功能,一种硅酸盐的组成为:MO·R O·2SiO·nH O,
2 2 3 2 2
已知元素M、R均位于元素周期表的第3周期。两元素原子的质子数之和为24。(1)该硅酸盐中同周期元素原子半径由大到小的顺序为____________;
(2)常温下,不能与R单质发生反应的是_______(选填序号);
A.CuCl 溶液 B.Fe O C.浓硫酸 D.NaCO 溶液
2 2 3 2 3
(3)写出M、R两种元素的最高价氧化物对应的水化物反应的离子方程式_______。
(4) 氮化硅(Si N)陶瓷材料硬度大、熔点高。Si N 晶体中只有极性共价键,则氮原子的化合价为
3 4 3 4
_______。
(5)C N 的结构与Si N 相似。请比较二者熔点高低并说明理由:_______。
3 4 3 4
(6)可由下列反应制得Si N,配平该反应并标出电子转移的数目和方向:_______。
3 4
_______SiO+_______C+_______N _______Si N+_______CO
2 2 3 4
(7)如果上述反应在10L的密闭容器中进行,一段时间后测得气体密度增加了2.8g/L,则制得的Si N
3 4
质量为_______。
【答案】(1) r(Na)>r(Al)>r(Si) (2)bd
(3)OH-+Al(OH) =AlO-+2HO (4)−3
3 2 2
(5)C N 熔点比Si N 熔点高,原因为两者都是原子晶体,碳原子半径比硅原子半径小,键长短,键能
3 4 3 4
大,因此C N 熔点比Si N 熔点高
3 4 3 4
(6)
(7)35g
【解析】一种硅酸盐的组成为:MO·R O·2SiO·nH O,已知元素M、R均位于元素周期表的第3周期,
2 2 3 2 2
两元素原子的质子数之和为24,M为+1价,R为+3价,则说明M为Na,R为Al。(1)该硅酸盐中同周期
元素是Na、Al、Si,根据同周期原子半径逐渐减小,则原子半径由大到小的顺序为r(Na)>r(Al)>r(Si);
(2)常温下,铝与氯化铜反应生成氯化铝和铜单质,铝与氧化铁常温不反应,铝常温下与浓硫酸发生钝化反
应,铝常温下与碳酸钠不反应,因此不能与R单质发生反应的是bd;(3)M、R两种元素的最高价氧化物对
应的水化物分别为氢氧化钠和氢氧化铝,两者反应的离子方程式OH-+Al(OH) =AlO-+2HO;(4)Si N
3 2 2 3 4
晶体中只有极性共价键,氮非金属性比硅强,硅为+4价,根据化合物为电中性,则氮原子的化合价为
−3;(5)氮化硅(Si N)陶瓷材料硬度大、熔点高。C N 的结构与Si N 相似,说明两者都是原子晶体,碳原
3 4 3 4 3 4
子半径比硅原子半径小,键长短,键能大,则C N 熔点比Si N 熔点高; (6)碳化合价由0价变为+2价,
3 4 3 4
氮化合价由0价变为−3价,则碳升高2个价态,Si N 降低12个价态,因此碳系数配6,Si N 系数配1,
3 4 3 4根据硅和氮守恒配SiO 系数为3,N 系数为2,再根据碳守恒配CO系数为6,则为3SiO+6C+2N
2 2 2 2
1Si N+6CO,其电子转移为 ;(7)根据反应方程式3SiO+6C+2N
3 4 2 2
1Si N+6CO分析得到气体质量增加112g,则生成1mol Si N 即140g,如果上述反应在10L的密闭容器中进
3 4 3 4
行,一段时间后测得气体密度增加了2.8g/L,则气体质量增加了28g,则制得的Si N 质量为
3 4
。
1.【2022·浙江省6月选考】下列说法不正确的是( )
A.晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维
B.高压钠灯发出的黄光透雾能力强、射程远,可用于道路照明
C.氧化铝熔点高,常用于制造耐高温材料
D.用石灰石-石膏法对燃煤烟气进行脱硫,同时可得到石膏
【答案】A
【解析】A项,晶体硅的导电性介于导体和绝缘体之间,是良好的半导体材料,可用于制造晶体管、
集成电路等,而二氧化硅常用于制造光导纤维,A错误;B项,钠的焰色反应为黄色,可用作透雾能力强
的高压钠灯,B正确;C项,耐高温材料应具有高熔点的性质,氧化铝熔点高,可用作耐高温材料,C正
确;D项,石灰石的主要成分为碳酸钙,石灰石-石膏法脱硫过程中发生反应:CaCO CaO+CO ↑,
3 2
SO +CaCO =CaSO +CO ,2CaSO+O =2CaSO ,得到了石膏,D正确;故选A。
2 3 3 2 3 2 4
2.【2021•浙江1月选考】铝硅酸盐型分子筛中有许多笼状空穴和通道(如图),其骨架的基本结构单元
是硅氧四面体和铝氧四面体,化学组成可表示为M[(AlO )·(SiO)]·zHO(M代表金属离子)。
a 2 x 2 y 2下列推测不正确的是( )
A.常采用水玻璃、偏铝酸钠在强酸溶液中反应后结晶制得分子筛
B.若a=x/2,则M为二价阳离子
C.调节y/x(硅铝比)的值,可以改变分子筛骨架的热稳定性
D.分子筛中的笼状空穴和通道,可用于筛分分子
【答案】A
【解析】A项,偏铝酸钠在强酸性溶液中不能稳定存在容易形成Al3+,不可以利用偏铝酸钠在强酸性
溶液中制备分子筛,A错误;B项,设M的化合价为m,则根据正负化合价代数和为0计算,m×
+x×(-1)=0,解得m=+2,B正确;C项,调节硅铝比可以改变分子筛的空间结构,从而改变分子筛的稳定
性,C正确;D项,调节硅铝比可以调节分子筛的孔径,根据分子筛孔径的大小可以筛分不同大小的分子,
D正确;故选A。
3.【2020•浙江7月选考】下列说法不正确的是( )
A.高压钠灯可用于道路照明
B.SiO 可用来制造光导纤维
2
C.工业上可采用高温冶炼黄铜矿的方法获得粗铜
D.BaCO 不溶于水,可用作医疗上检查肠胃的钡餐
3
【答案】D
【解析】A项,高压钠灯发出的黄光射程远、透雾能力强,所以高压钠灯用于道路照明,故A正确;
B项,二氧化硅传导光的能力非常强,用来制造光导纤维,故B正确;C项,黄铜矿高温煅烧生成粗铜、
氧化亚铁和二氧化硫,故C正确;D项,碳酸钡不溶于水,但溶于酸,碳酸钡在胃酸中溶解生成的钡离子
为重金属离子,有毒,不能用于钡餐,钡餐用硫酸钡,故D错误;故选D。
4.(2020•浙江7月选考)Ca SiO 是硅酸盐水泥的重要成分之一,其相关性质的说法不正确的是( )
3 5
A.可发生反应:Ca SiO+4NH Cl CaSiO +2CaCl +4NH ↑+2HO
3 5 4 3 2 3 2
B.具有吸水性,需要密封保存C.能与SO 反应生成新盐
2
D.与足量盐酸作用,所得固体产物主要为SiO
2
【答案】D
【解析】将Ca SiO 改写为氧化物形式后的化学式为:3CaO·SiO ,性质也可与NaSiO 相比较。A项,
3 5 2 2 3
Ca SiO 与NH Cl反应的方程式为:Ca SiO+4NHCl CaSiO +2CaCl +4NH↑+2H O,A正确;B项,CaO
3 5 4 3 5 4 3 2 3 2
能与水反应,所以需要密封保存,B正确;C项,亚硫酸的酸性比硅酸强,当二氧化硫通入到Ca SiO 溶液
3 5
时,发生反应:3SO +H O+ Ca SiO=3 CaSO+H SiO,C正确;D项,盐酸的酸性比硅酸强,当盐酸与
2 2 3 5 3 2 3
Ca SiO 反应时,发生反应:6HCl+ Ca SiO=3CaCl +H SiO+2H O,D不正确;故选D。
3 5 3 5 2 2 3 2
5.【2020•浙江7月选考】Ca SiO 是硅酸盐水泥的重要成分之一,其相关性质的说法不正确的是
3 5
( )
A.可发生反应:Ca SiO+4NH Cl CaSiO +2CaCl +4NH ↑+2HO
3 5 4 3 2 3 2
B.具有吸水性,需要密封保存
C.能与SO 反应生成新盐
2
D.与足量盐酸作用,所得固体产物主要为SiO
2
【答案】D
【解析】将Ca SiO 改写为氧化物形式后的化学式为:3CaO·SiO ,性质也可与NaSiO 相比较。A项,
3 5 2 2 3
Ca SiO 与NH Cl反应的方程式为:Ca SiO+4NHCl CaSiO +2CaCl +4NH↑+2H O,A正确;B项,CaO
3 5 4 3 5 4 3 2 3 2
能与水反应,所以需要密封保存,B正确;C项,亚硫酸的酸性比硅酸强,当二氧化硫通入到Ca SiO 溶液
3 5
时,发生反应:3SO +H O+ Ca SiO=3 CaSO+H SiO,C正确;D项,盐酸的酸性比硅酸强,当盐酸与
2 2 3 5 3 2 3
Ca SiO 反应时,发生反应:6HCl+ Ca SiO=3CaCl +H SiO+2H O,D不正确;故选D。
3 5 3 5 2 2 3 2
6.【2019•浙江4月选考】在温热气候条件下,浅海地区有厚层的石灰石沉积,而深海地区却很少。
下列解析不正确的是( )
A.与深海地区相比,浅海地区水温较高,有利于游离的CO 增多、石灰石沉积
2
B.与浅海地区相比,深海地区压强大,石灰石岩层易被CO 溶解,沉积少
2
C.深海地区石灰石岩层的溶解反应为:CaCO (s)+HO(l)+CO(aq) Ca(HCO )(aq)
3 2 2 3 2
D.海水呈弱酸性,大气中CO 浓度增加,会导致海水中CO浓度增大
2
【答案】D
【解析】石灰岩的形成是CaCO 的沉积结果,海水中溶解一定量的CO,因此CaCO 与CO,HO之
3 2 3 2 2
间存在着下列平衡:CaCO (s)+CO(g)+HO(l) Ca(HCO )(aq)。A.海水中CO 的溶解度随温度的升高而减
3 2 2 3 2 2
小,随压力的增大而增大,在浅海地区,海水⇌层压力较小,同时水温比较高,因而CO 的浓度较小,即游
2
离的CO 增多,根据平衡移动原理,上述平衡向生成CaCO 方向移动,产生石灰石沉积,A项正确;B.
2 3与A恰恰相反,石灰石岩层易被CO 溶解,沉积少,B项正确;C.在深海地区中,上述平衡向右移动,
2
且倾向很大,故溶解反应为CaCO (s)+HO(l)+CO(aq)=Ca(HCO )(aq),C项正确;D. 海水温度一定时,
3 2 2 3 2
大气中CO 浓度增加,海水中溶解的CO 随之增大,导致CO2-转化为HCO -,CO2-浓度降低,D项错误。
2 2 3 3 3
故选D。
7.【2019•北京卷】下列我国科研成果所涉及材料中,主要成分为同主族元素形成的无机非金属材料
的是( )
A.4.03米大口径碳化硅 B.2022年冬奥会聚氨酯 C.能屏蔽电磁波的碳包 D.“玉兔二号”钛
反射镜 速滑服 覆银纳米线 合金筛网轮
【答案】A
【解析】A项,碳化硅(SiC)是由碳元素和硅元素组成的无机非金属材料,且碳元素与硅元素均位于元
素周期表第IVA族,故A符合题意;B项,聚氨酯为有机高分子化合物,故B不符合题意;C项,碳包覆
银纳米材料中银为金属元素,故C不符合题意;D项,钛合金为金属材料。
8.【2019·全国Ⅰ卷】陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的
关系。下列说法错误的是
A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁
B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成
C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐
D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点
【答案】A
【解析】A项,氧化铁为棕红色固体,瓷器的青色不可能来自氧化铁,故A错误;B项,兵马俑是陶制
品,陶制品是由粘土或含有粘土的混合物经混炼、成形、煅烧而制成的,故B正确;C项,瓷的主要原料
是取之于自然界的硅酸盐矿物,陶瓷的主要成分是硅酸盐,与水泥、玻璃等同属硅酸盐产品,故 C正确;
D项,瓷的主要成分是硅酸盐,硅酸盐的化学性质不活泼,具有不与酸或碱反应、抗氧化的特点,故 D正
确。故选A。