文档内容
1.3年真题考点分布
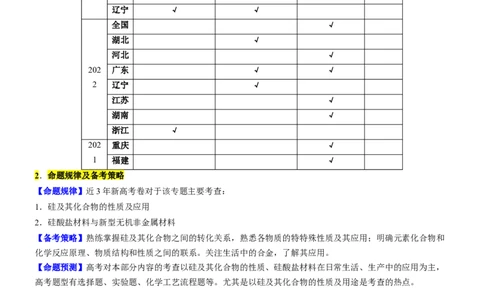
考点分布
年
卷区 二氧化硅的性质及用
份 硅的制备、性质及用途 硅酸盐性质及用途 综合应用
途
江苏
广东 √ √
202
山东 √
3
湖北 √
辽宁 √ √
全国 √
湖北 √
河北 √
202 广东 √ √
2 辽宁 √
江苏 √
湖南 √
浙江 √
202 重庆 √
1 福建 √
2.命题规律及备考策略
【命题规律】近3年新高考卷对于该专题主要考查:
1.硅及其化合物的性质及应用
2.硅酸盐材料与新型无机非金属材料
【备考策略】熟练掌握硅及其化合物之间的转化关系,熟悉各物质的特特殊性质及其应用;明确元素化合物和
化学反应原理、物质结构和性质之间的联系。关注生活中的合金,了解其应用。
【命题预测】高考对本部分内容的考查以硅及其化合物的性质、硅酸盐材料在日常生活、生产中的应用为主,
高考题型有选择题、实验题、化学工艺流程题等。尤其是以硅及其化合物的性质及用途是考查的热点。考法 1 硅和二氧化硅
1、硅
(1)原子和晶体结构:硅元素的原子序数为14,基态原子的简化电子排布式为[Ne] 3s23p2,核外电子的空间运动
状态有7种,不成对电子数有2种;单晶硅为_________晶体,晶体中每个Si原子以sp3杂化,分别与4个相邻
的Si 原子形成4个σ键,Si原子的配位数为4,晶体中最小的环是6元环,1个环中平均含有0.5个Si原子,含
Si-Si键数为1。
(2)物理性质:晶体硅为原子晶体,灰黑色、有金属光泽、硬度大而脆、熔沸点高,导电性介于导体和绝缘体
之间,是常用的半导体材料。金刚石、晶体硅、碳化硅中熔点从高到低的顺序是金刚石、碳化硅、晶体硅。
(3)化学性质:常温下化学性质不活泼,只能跟F、HF和NaOH溶液反应,在高温条件下,单质硅能与O 和
2 2
Cl 等非金属单质反应。
2
条件 化学反应 化学方程式
跟F 反应 ___________________________
2
常温 跟HF反应 ___________________________
跟NaOH溶液反应 ___________________________
高温 跟O 反应 ___________________________
2
跟Cl 反应 ___________________________
2
(4)用途:太阳能电池、计算机芯片、半导体材料、制作特种钢及合金等。
(5)制备:自然界中无游离态的硅,工业上,用C在高温下还原SiO 可制得粗硅,有关反应的化学方程式:
2
高温 高温 高温
SiO+2C Si(粗)+2CO↑,Si(粗)+2Cl SiCl ,SiCl +2H Si(纯)+4HCl。
2 2 4 4 2
2、二氧化硅
(1)空间结构:二氧化硅是直接由原子构成的_________晶体,晶体中Si原子均以sp3杂化,分别与4个O原
子成键,每个O原子与2个Si原子成键,晶体中的最小环为12元环,其中有6个Si原子和6个O原子,含有
12个Si-O键;每个Si原子被_________个环共有,每个O原子被6个环共有,每个Si-O键被6个环共有,Si原
子数与O原子数之比为1:2。
(2)物理性质:熔点高,硬度大,不溶于水。
(3)化学性质:SiO 常温下化学性质很不活泼,不与水、酸反应(_________除外),能与强碱溶液、氢氟酸
2
反应,高温条件下可以与碱性氧化物反应。
化学反应 化学方程式 相关应用
与强碱反应 SiO+2NaOH=NaSiO+HO SiO 能与强碱溶液生成的硅酸钠具有粘性,所以
2 2 3 2 2
不能用带磨口玻璃塞试剂瓶存放碱性溶液,避免
NaSiO 将瓶塞和试剂瓶粘住,打不开,碱性溶液
2 3
存放应用橡皮塞
与氢氟酸反应 __________________ 利用此反应,氢氟酸能刻蚀玻璃;氢氟酸不能用
玻璃试剂瓶存放,应用塑料瓶
与碱性氧化物反应 高温
SiO
2
+CaO CaSiO与某些盐类反应 高温 之所以能够如此反应,原因是高温条件下,产物
SiO 2 +CaCO 3 CaSiO 3 +CO 2 ↑ CO 容易从反应体系中逃逸,使反应向正方面进
2
行
高温
SiO
2
+Na
2
CO
3
Na
2
SiO
3
+CO
2
↑
(4)用途:石英可用于制作石英表和石英玻璃;石英砂常用作制薄玻璃和建筑材料;水晶常用来制造电子部件、
光学仪器、工艺品和眼镜片等;玛瑙用于制造精密仪器轴承、耐磨器皿和装饰品;SiO 被用于制造高性能的现
2
代通讯材料——_________。
【典例1】(2023·枣阳市第一高级中学模拟预测)硅及其化合物的应用范围很广。下列说法正确的是( )
A.硅是人类将太阳能转换为电能的常用材料
B.粗硅制备单晶硅不涉及氧化还原反应
C.反应Si+2NaOH+HO===Na SiO+2H↑中,Si为氧化剂
2 2 3 2
D.硅能与氢氟酸反应,则硅也可以与盐酸反应
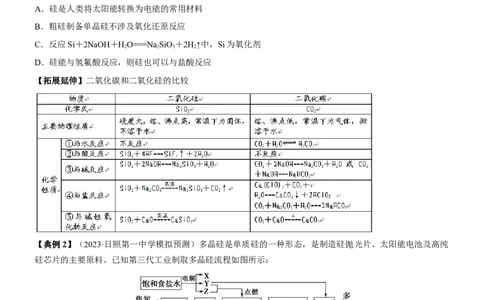
【拓展延伸】二氧化碳和二氧化硅的比较
【典例2】(2023·日照第一中学模拟预测)多晶硅是单质硅的一种形态,是制造硅抛光片、太阳能电池及高纯
硅芯片的主要原料。已知第三代工业制取多晶硅流程如图所示:
下列说法错误的是( )
A.Y、Z分别为H、Cl
2 2
B.制取粗硅的过程中焦炭与石英会发生副反应生成碳化硅,在该副反应中,氧化剂与还原剂的物质的量之比
为1∶1
C.SiHCl 极易水解,其完全水解的产物为HSiO、H、HCl,据此推测SiHCl 中硅元素的化合价为+4
3 2 3 2 3
D.Y与SiHCl 制备多晶硅的反应属于置换反应
31.(2023·广东梅州·统考三模)下列叙述Ⅰ和Ⅱ均正确且有因果关系的是
选项 叙述Ⅰ 叙述Ⅱ
A 具有氧化性 在葡萄酒酿制过程中添加适量
B 断裂 分子中的 键需要吸收热量 工业上用液氨作制冷剂
C 氢氟酸可与 反应得到 二氧化硅是一种两性氧化物
D 蔗糖遇浓硫酸变黑,同时产生有刺激性气味的气体 浓硫酸具有脱水性和强氧化性
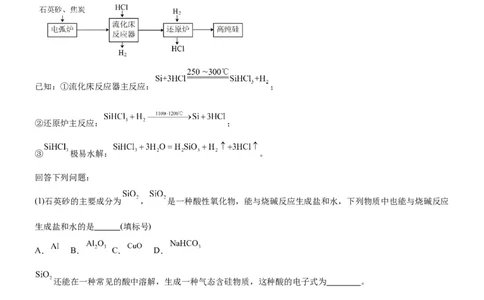
2.(2023·辽宁·校联考二模)高纯硅是制作光伏电池的关键材料,如图是一种生产高纯硅的工艺流程示意图:
已知:①流化床反应器主反应: ;
②还原炉主反应: ;
③ 极易水解: 。
回答下列问题:
(1)石英砂的主要成分为 , 是一种酸性氧化物,能与烧碱反应生成盐和水,下列物质中也能与烧碱反应
生成盐和水的是 (填标号)
A. B. C. D.
还能在一种常见的酸中溶解,生成一种气态含硅物质,这种酸的电子式为 。
(2)电弧炉中生成粗硅,反应的化学方程式为 。若电弧炉中焦炭过量,还会有 生成,石英砂和
焦炭生成 的反应中,氧化剂和还原剂的物质的量之比为 。
(3)整个操作流程都需隔绝空气,原因是 (答出两条即可)。
(4)流化床反应器中除 外,还可能发生副反应,生成其他含硅化合物(如 、 、 等),可
以用分馏的方法加以分离,该操作方法的理论依据是 。
(5)上述操作流程中可以循环利用的物质是 。
3.(2023·福建龙岩·统考三模)硅在地壳中含量丰富,晶体硅与硅化物等新材料在现代工业领域作用巨大。回
答下列问题:(1)下列属于硅原子激发态的电子排布式有 (填标号,下同),其中能量较高的是 。
a.1s22s22p63s23p2 b.1s22s22p63s13p3 c.1s22s22p63s13p2 d.1s22s22p63s13p24s1
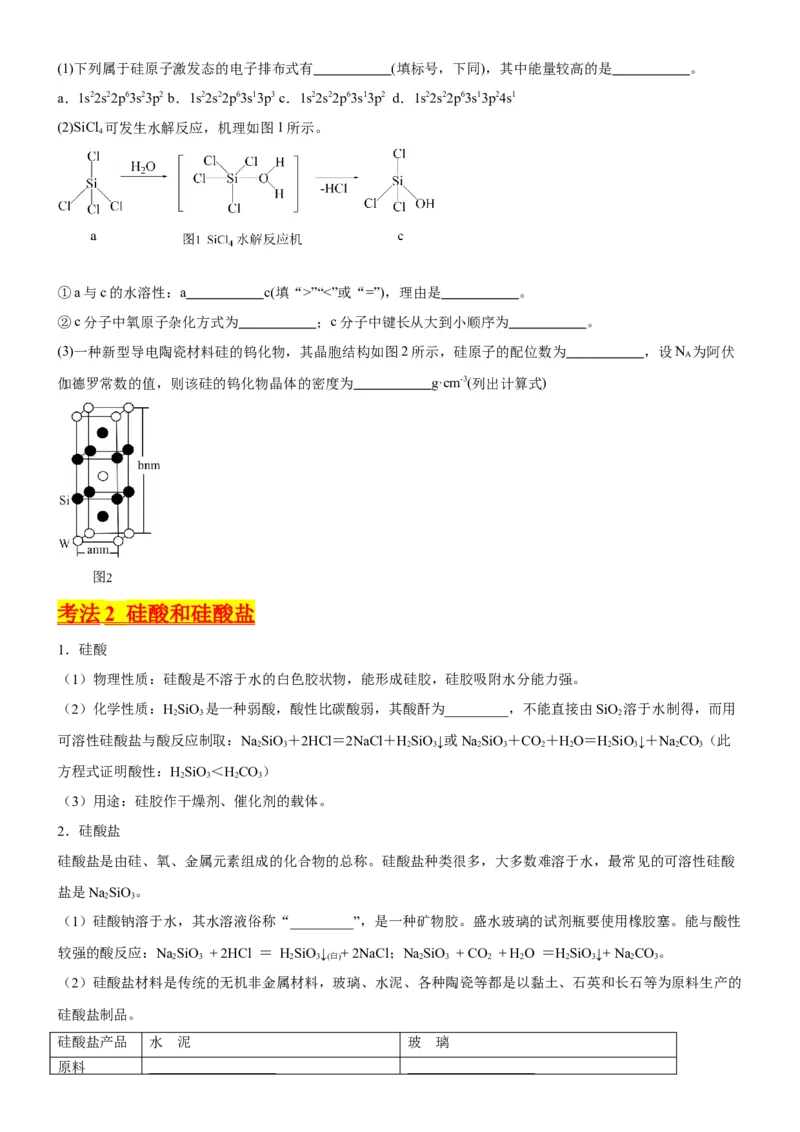
(2)SiCl 可发生水解反应,机理如图1所示。
4
①a与c的水溶性:a c(填“>”“<”或“=”),理由是 。
②c分子中氧原子杂化方式为 ;c分子中键长从大到小顺序为 。
(3)一种新型导电陶瓷材料硅的钨化物,其晶胞结构如图2所示,硅原子的配位数为 ,设N 为阿伏
A
伽德罗常数的值,则该硅的钨化物晶体的密度为 g·cm-3(列出计算式)
考法 2 硅酸和硅酸盐
1.硅酸
(1)物理性质:硅酸是不溶于水的白色胶状物,能形成硅胶,硅胶吸附水分能力强。
(2)化学性质:HSiO 是一种弱酸,酸性比碳酸弱,其酸酐为_________,不能直接由SiO 溶于水制得,而用
2 3 2
可溶性硅酸盐与酸反应制取:NaSiO+2HCl=2NaCl+HSiO↓或NaSiO+CO+HO=HSiO↓+NaCO(此
2 3 2 3 2 3 2 2 2 3 2 3
方程式证明酸性:HSiO<HCO)
2 3 2 3
(3)用途:硅胶作干燥剂、催化剂的载体。
2.硅酸盐
硅酸盐是由硅、氧、金属元素组成的化合物的总称。硅酸盐种类很多,大多数难溶于水,最常见的可溶性硅酸
盐是NaSiO。
2 3
(1)硅酸钠溶于水,其水溶液俗称“_________”,是一种矿物胶。盛水玻璃的试剂瓶要使用橡胶塞。能与酸性
较强的酸反应:NaSiO + 2HCl = HSiO↓ + 2NaCl;NaSiO + CO + H O =HSiO↓+ Na CO。
2 3 2 3 (白) 2 3 2 2 2 3 2 3
(2)硅酸盐材料是传统的无机非金属材料,玻璃、水泥、各种陶瓷等都是以黏土、石英和长石等为原料生产的
硅酸盐制品。
硅酸盐产品 水 泥 玻 璃
原料 __________________ __________________反应原理 发生复杂的物理化学变化 SiO + Na CO NaSiO + CO↑
2 2 3 2 3 2
SiO + CaCO CaSiO + CO↑
2 3 3 2
主要设备 水泥回转窑 玻璃窑
主要成分 3CaO·SiO 、2CaO·SiO 、3CaO·Al O NaSiO、CaSiO 、SiO
2 2 2 3 2 3 3 2
反应条件 高温 高温
陶瓷生产的一般过程:混合→成型→干燥→烧结→冷却→陶瓷,随着现代科学技术的发展,一些具有特殊结构、
特殊功能的新型无机非金属材料如高温结构陶瓷、生物陶瓷、压电陶瓷等相继被生产出来。
【典例4】(2023年青岛一中高三月考) 南海一号博物馆,又称广东海上丝绸之路博物馆,位于广东阳江市海陵
岛试验开发区的“十里银滩”上,其建筑特色鲜明,设计创意独特,紧扣海的主题,体现了海洋文化与南方建
筑风格的柔美组合。下列相关说法正确的是( )
A.展柜使用的钢化玻璃,其主要成分只有SiO
2
B.墙体使用的砖瓦、水泥是硅酸盐制品
C.陈列的元青花瓷的原料有高岭土[AlSi O(OH) ],也可以表示为Al O·SiO·H O
2 2 5 4 2 3 2 2
D.展示的青铜器上有一层绿色物质,此绿色物质可能是碱式碳酸铜,它不溶于盐酸
【拓展延伸】硅及其化合物性质的“反常”
(1)碳族元素的主要化合价一般是+2、+4价,而硅常见的是+4价。
(2)硅的还原性比碳强,而碳在高温下却能从SiO 中还原出硅。
2
(3)非金属单质与强碱反应一般不生成氢气,而硅却能与强碱溶液反应产生氢气。
(4)非金属单质一般不与非氧化性酸反应,而硅不但能与氢氟酸反应,而且还有H 生成(类似于较活泼金属与酸
2
的置换反应),Si+4HF===SiF ↑+2H↑。
4 2
(5)SiO 是HSiO 的酸酐,但它不溶于水,不能直接将它与水作用制备HSiO。
2 2 3 2 3
(6)非金属氧化物的熔、沸点一般较低,但SiO 的熔、沸点却很高。
2
(7)酸性氧化物一般不与酸作用,但SiO 却能与氢氟酸作用。SiO+4HF===SiF ↑+2HO。
2 2 4 2
(8)无机酸一般易溶于水,而HSiO 却难溶于水。
2 3
(9)因HCO 的酸性强于HSiO,所以在NaSiO 溶液中通入CO 能发生下列反应:NaSiO+CO+
2 3 2 3 2 3 2 2 3 2
HO===H SiO↓+NaCO,但在高温下NaCO+SiO=====NaSiO+CO↑也能发生。
2 2 3 2 3 2 3 2 2 3 2
(10)Na SiO 的水溶液俗称水玻璃,但它与玻璃的成分不相同;硅酸钠水溶液(即水玻璃)称为泡花碱,但它却是
2 3
盐溶液(存放的试剂瓶不能用玻璃塞),并不是碱溶液。
【典例5】(2023·顺德一中高三月考)Ca SiO 是硅酸盐水泥的重要成分之一,其相关性质的说法不正确的是(
3 5
)
A.可发生反应:Ca SiO+4NH Cl=====CaSiO +2CaCl +4NH ↑+2HO
3 5 4 3 2 3 2B.具有吸水性,需要密封保存
C.能与SO 反应生成新盐
2
D.与足量盐酸作用,所得固体产物主要为SiO
2
1.(2023·浙江·校联考二模)NaSiO 应用广泛,下列说法不正确的是
2 3
A.Si元素位于周期表p区B. NaSiO 属于强电解质
2 3
C. NaSiO 的水溶液俗称水玻璃D.存放 NaSiO 溶液的试剂瓶可以用玻璃塞
2 3 2 3
2.(2023·北京海淀·北京市十一学校校考三模)硅酸盐是地壳岩石的主要成分,在硅酸盐中,四面体 (如
图甲为俯视投影图)通过共用顶角氧原子可形成六元环(图乙)、无限单链状(图丙)、无限双链状(图丁)等多种结构。
石棉是由钙、镁离子以离子数 的比例与单链状硅酸根离子形成的一种硅酸盐。
下列说法不正确的是
A.大多数硅酸盐材料硬度高与硅氧四面体结构有关
B.六元环的硅酸盐阴离子化学式
C.石棉的化学式为
D.双链状硅酸盐中硅氧原子数之比为
3.(2023·江西新余·新余市第一中学校考模拟预测)某实验小组设计了如下装置对焦炭还原二氧化硅的气体产
物的成分进行探究。
已知:PdCl 溶液可用于检验CO,反应的化学方程式为CO + PdCl + H O = CO + 2HCl + Pd(产生黑色金属钯
2 2 2 2
粉末,使溶液变浑浊)。
(1)实验时要通入足够长时间的N,其原因是 。
2
(2)装置B的作用是 。(3)装置C、D中所盛试剂分别为 、 ,若装置C、D中溶液均变浑浊,且经检测两气体产物的物质的量
相等,则该反应的化学方程式为 。
(4)该装置的缺点是 。
(5)设计实验证明碳酸的酸性比硅酸的强: 。
【基础过关】
1.(2023·广东梅州·统考三模)中华文化源远流长、博大精深。博物馆馆藏文物是中华文化的重要代表。下列
文物主要是由硅酸盐材料制成的是
A. 西汉素纱禅衣 B. 溪山行旅图
C. 东汉青铜奔马 D. 新石器时代鸡形陶壶
2.(2021·广东揭阳·普宁市第二中学校考模拟预测)2020年11月10日08时12分,我国“奋斗者”号载人潜
水器在马里亚纳海沟成功坐底,坐底深度10909米,创造了中国载人深潜的新纪录。下列关于“奋斗者”号的
说法中错误的是
A.为了承受万米海压,载人舱所用Ti-62A材料是由我国自主研制的新型钛合金材料,具有强度高、韧性好的
特点
B.载人潜水器下水时要携带两组压载铁,在重力牵引下潜入海洋深处,铁是黑色金属
C.浮力材料是成千上万个纳米级空心玻璃微球,其主要成分与玛瑙、刚玉、硅胶相同
D.“奋斗者”号的上百块单体锂电池,模块的间隙中充满了油,不可用水代替油
3.(2023·江西宜春·江西省宜丰中学校考模拟预测)《流浪地球2》向观众展示了太空电梯、行星发动机、超
级计算机550W等超前的科技幻想,探讨了数字生命、人工智能等科技伦理问题。它们与化学有着密切联系,
下列说法不正确的是
A.我国“硅—石墨烯—锗高速晶体管”技术获重大突破,C、Si、Ge都是主族元素
B.我国提出网络强国战略,光纤线路总长超过三千万公里,光纤的主要成分是SiO
2
C.新型陶瓷碳化硅(SiC)可作耐高温结构材料
D.富勒烯、石墨烯都是含碳化合物4.(2023·河北·模拟预测)原始瓷是中国乃至世界出现最早且初步具有瓷器特征的一种器物。考古工作者对某
原始瓷文物分析发现,其中含有石英颗粒,还有一定量的莫来石( , )等。下列说法正确
的是
A.石英的主要成分 由大量的硅氧四面体基本单元构成
B.瓷器质地均匀,硬度高,是纯净物
C.莫来石的主要成分为氧化物
D.瓷器烧制前后颜色不同的现象称为“窑变”,“窑变”属于物理变化
5.(2023·福建泉州·泉州五中校考一模)航天科技的发展与化学密切相关。2013年12月15日,“玉兔号”成
为我国登陆月球的第一辆月球车。2022年11月29日,神舟十五号载人飞船成功发射,首次实现6名航天员太
空会师。中国航天科技集团计划2023年安排60余次宇航发射任务。
下列说法中错误的是
A.碳化硅 可用作宇宙飞船的耐热材料
B.肼 可作火箭燃料,可用 作氧化剂
C.二氧化硅可用作航天器太阳能电池板的材料
D.电解水产生氧气是宇航员供氧的主要来源
6.(2023·福建福州·统考模拟预测) 法生产多晶硅的流程如下。下列说法错误的是
A.合成1反应中 作氧化剂
B.合成2的反应为:
C.上述流程说明 可溶于D.净化、热解中生成的多晶硅为还原产物
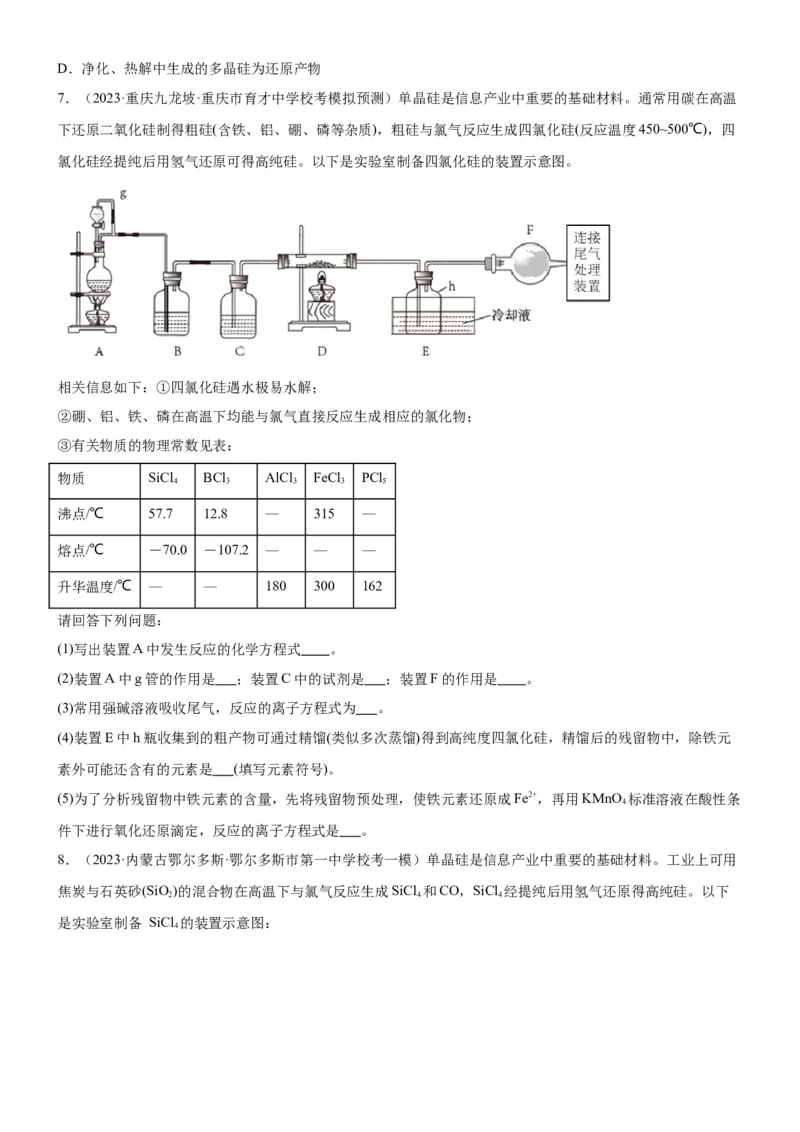
7.(2023·重庆九龙坡·重庆市育才中学校考模拟预测)单晶硅是信息产业中重要的基础材料。通常用碳在高温
下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500℃),四
氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
相关信息如下:①四氯化硅遇水极易水解;
②硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
③有关物质的物理常数见表:
物质 SiCl BCl AlCl FeCl PCl
4 3 3 3 5
沸点/℃ 57.7 12.8 — 315 —
熔点/℃ -70.0 -107.2 — — —
升华温度/℃ — — 180 300 162
请回答下列问题:
(1)写出装置A中发生反应的化学方程式 。
(2)装置A中g管的作用是 ;装置C中的试剂是 ;装置F的作用是 。
(3)常用强碱溶液吸收尾气,反应的离子方程式为 。
(4)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除铁元
素外可能还含有的元素是 (填写元素符号)。
(5)为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO 标准溶液在酸性条
4
件下进行氧化还原滴定,反应的离子方程式是 。
8.(2023·内蒙古鄂尔多斯·鄂尔多斯市第一中学校考一模)单晶硅是信息产业中重要的基础材料。工业上可用
焦炭与石英砂(SiO)的混合物在高温下与氯气反应生成SiCl 和CO,SiCl 经提纯后用氢气还原得高纯硅。以下
2 4 4
是实验室制备 SiCl 的装置示意图:
4实验过程中,石英砂中的铁、铝等杂质也能转化为相应氯化物,SiCl 、AlCl 、FeCl 遇水均易水解,有关物质
4 3 3
的物理常数见下表:
物质 SiCl AlCl FeCl
4 3 3
沸点/℃ 57.7 — 315
熔点/℃ -70.0 — —
升华温度/℃ — 180 300
(1)装置B中的试剂是 ,装置 D 中制备SiCl 的化学方程式是 。
4
(2) D、E 间导管短且粗的作用是 。
(3)G中吸收尾气一段时间后,吸收液中肯定存在OH-、Cl-和SO 2-,请设计实验,探究该吸收液中可能存在的其
4
他酸根离子(忽略空气中CO 的影响)。
2
【提出假设】假设1:只有SO 2-;假设2:既无SO 2-也无ClO-;假设3: 。
3 3
【设计方案进行实验】可供选择的实验试剂有:3 mol/L H SO 、1 mol/L NaOH、0.01 mol/LKMnO 、溴水、淀
2 4 4
粉-KI、品红等溶液。
取少量吸收液于试管中,滴加 3 mol/L H SO 至溶液呈酸性,然后将所得溶液分置于a、b、c三支试管中,分
2 4
别进行下列实验。请完成下表:
序
操作 可能出现的现象 结论
号
若溶液褪色 则假设1成立
① 向a试管中滴加几滴 溶液
若溶液不褪色 则假设2或3成立
若溶液褪色 则假设1或3成立
② 向b试管中滴加几滴 溶液
若溶液不褪色 假设2成立
③ 向c试管中滴加几滴 溶液 假设3成立
【能力提升】
1.(2023·广东珠海·珠海市第一中学校考模拟预测)广东省博物馆馆藏集岭南文物之大成,汇聚诸多种类于一
体,下列文物不含硅酸盐材料的是A.清康熙宜兴紫砂象生瓜 B.明万历款黄釉五彩双龙 D.南朝波斯鎏金
C.清起降款青花船形碟
形壶 纹盘 器
2.(2023·湖北黄冈·黄冈中学校考三模)ChatGPT是史上月活用户增长最快的消费者应用。下列说法中不正确
的是
A.硅晶片是生产芯片的基础材料
B.芯片制造中的“光刻技术”是利用光敏树脂在曝光条件下成像,该过程涉及化学变化
C.硅在自然界中主要以单质形式存在
D.硅是应用最广泛的半导体材料
3.(2023·安徽芜湖·统考二模)化学与生活、科技、社会发展息息相关。下列说法正确的是
A.“天宫”空间站使用聚乳酸材料餐具,聚乳酸是化合物
B.富勒烯与石墨烯用途广泛,它们都属于新型无机非金属材料
C.冬奥场馆建筑使用碲化镉发电玻璃,碲和镉均属于主族元素
D.中国承建的卡塔尔首座光伏电站中的光伏材料为高纯度二氧化硅
4.(2023·湖北武汉·统考模拟预测)湖北钟祥出土的“四爱图梅瓶”是一种青花瓷器。下列说法错误的是
A.陶瓷烧制的过程为物理变化 B.传统陶瓷可用作绝缘材料
C.制作陶瓷的原料为铝硅酸盐 D.陶瓷稳定性较强且耐腐蚀
5.(2023·四川乐山·统考三模)我国科学家分析月壤成分发现含有X、Y、Z、W、M五种主族元素,其原子序
数依次增大且都不大于20,Y、Z、W同周期且Z、M同主族;X与W形成的化合物是光导纤维的基本原料,
在潜水艇中YX 可以用作供氧剂。下列说法正确的是
2 2
A.离子半径的大小顺序:Z>Y>X
B.最简单气态氢化物稳定性X>W
C.最高价氧化物对应水化物碱性Y>Z>M
D.工业上用电解ZX来制备Z的单质
6.(2023·广东潮州·统考二模)提纯粗硅时可通过反应 获取晶体硅。下列说法正确的
是
A. 晶体中含有 非极性键
B.基态 原子的轨道表示式C. 的空间填充模型为
D. 的电子式为
7.(2023·海南海口·海南中学校考三模)Ⅰ.高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它
的发现和使用曾引起计算机的一场“革命”。它可以按下列方法制备:
(1)写出步骤①的化学方程式:_________。
(2)步骤②经过冷凝得到的SiHCl (沸点33.0 ℃)中含有少量的SiCl (沸点57.6 ℃)和HCl(沸点-84.7 ℃),提纯
3 4
SiHCl 的主要化学操作的名称是______;SiHCl 和SiCl 一样,遇水可发生剧烈水解,已知SiHCl 水解会生成两
3 3 4 3
种气态产物,试写出其水解的化学方程式:________。
Ⅱ.白炭黑(SiO·H O)广泛应用于橡胶、涂料、印刷等行业,可用蛇纹石[主要成分为Mg(Si O )(OH) ]来制取,
2 2 6 4 10 8
其主要工艺流程如图所示:
(3)蛇纹石用氧化物形式可表示为_________________。
(4)碱浸时,为提高其中硅酸盐的浸取率,除采用合适的液固比和循环浸取外,还可采用的方法:
①___________;②____________(任举两种)。
(5)过滤1得到的滤液的主要成分是___________________。
(6)滤液与盐酸反应的主要离子方程式为________________。
(7)洗涤时,如何证明产品已洗涤干净?______________。
8.(2023·兴宁一中高三月考)高纯硅被誉为“信息革命的催化剂”。某小组模拟工业上用SiHCl 与H 在
3 2
1357K的条件下制备高纯硅,实验装置如图所示(部分加热及夹持装置略去):
已知:①SiHCl 的沸点为33.0℃,密度为1.34g·cm-3;易溶于有机溶剂;能与HO剧烈反应;在空气中易被氧
3 2
化;
②CaCl +xCH CHOH→CaCl ·xCHCHOH;
2 3 2 2 3 2
③银氨溶液中存在:[Ag(NH)]++2H O Ag++2NH·H O。
3 2 2 3 2回答下列问题:
(1)装置B中试剂宜选择____(填字母,单选)。
a.碱石灰b.无水氯化钙c.五氧化二磷d.硅胶
(2)实验操作步骤有:
①加热装置D至1357K;
②关闭K;
1
③加热装置C,打开K,滴加VmLSiHCl ;
2 3
④关闭K;
2
⑤打开K,向安全漏斗中加入足量乙醇,装置A中反应一段时间。
1
正确的操作顺序为___(填序号)。
(3)E中CCl 的作用是防倒吸和___。
4
(4)石英管中发生反应的化学方程式为___。
(5)本实验制得高纯硅a g,则SiHCl 的利用率为___(只列计算式)。实验结束后,有同学认为根据高纯硅与消耗
3
钠或乙醇的量也可以计算SiHCl 的利用率,这种观点___(填“是”或“否”)正确。
3
【真题感知】
1.(2023·广东·统考高考真题)“高山流水觅知音”。下列中国古乐器中,主要由硅酸盐材料制成的是
A.九霄环佩木古琴 B.裴李岗文化骨笛 C.商朝后期陶埙 D.曾侯乙青铜编钟
2.(2023·广东·统考高考真题)建设美丽乡村,守护中华家园,衣食住行皆化学。下列说法正确的是
A.千家万户通光纤,光纤的主要材质为 B.乡村公路铺沥青,沥青属于天然无机材料
C.美容扮靓迎佳节,化妆品中的甘油难溶于水 D.均衡膳食助健康,主食中的淀粉可水解为葡萄糖
3.(2022·河北·高考真题)定窑是宋代五大名窑之一,其生产的白瓷闻名于世。下列说法正确的是A.传统陶瓷是典型的绝缘材料 B.陶瓷主要成分为 和
C.陶瓷烧制的过程为物理变化 D.白瓷的白色是因铁含量较高
4.(2023·湖北·统考高考真题)工业制备高纯硅的主要过程如下:
石英砂 粗硅 高纯硅
下列说法错误的是
A.制备粗硅的反应方程式为
B.1molSi含Si-Si键的数目约为
C.原料气HCl和 应充分去除水和氧气
D.生成 的反应为熵减过程
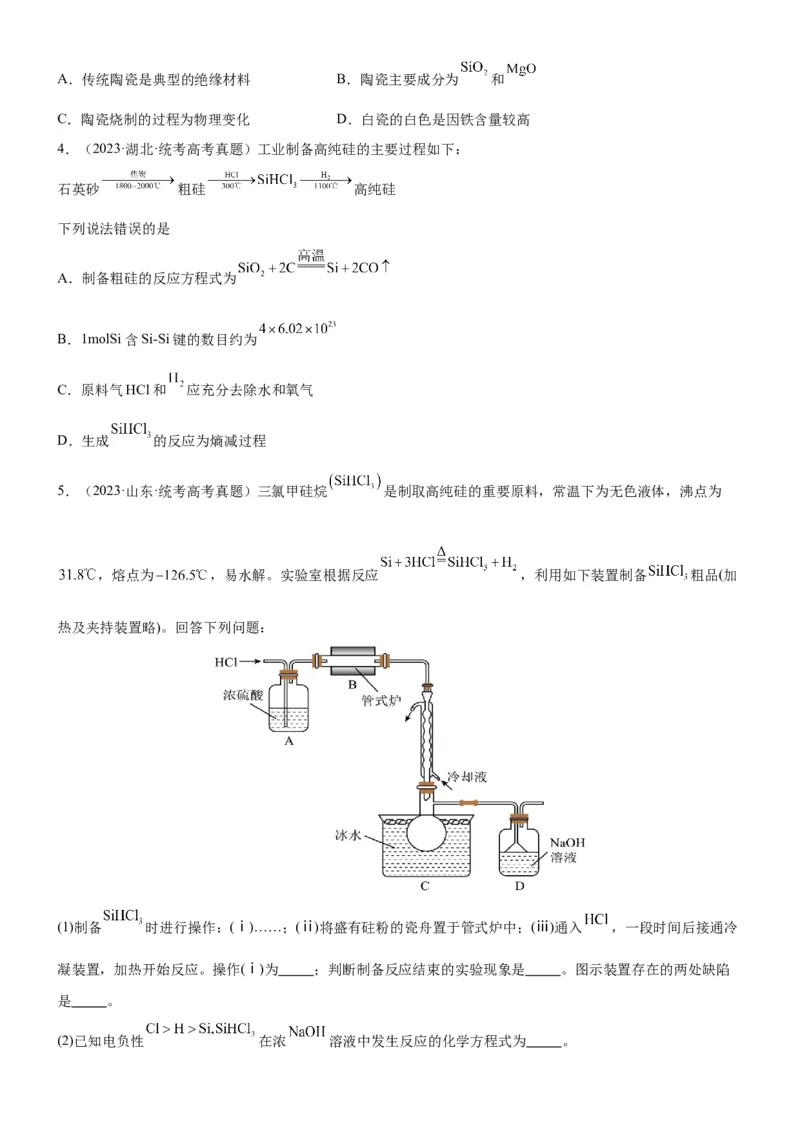
5.(2023·山东·统考高考真题)三氯甲硅烷 是制取高纯硅的重要原料,常温下为无色液体,沸点为
,熔点为 ,易水解。实验室根据反应 ,利用如下装置制备 粗品(加
热及夹持装置略)。回答下列问题:
(1)制备 时进行操作:(ⅰ)……;(ⅱ)将盛有砫粉的瓷舟置于管式炉中;(ⅲ)通入 ,一段时间后接通冷
凝装置,加热开始反应。操作(ⅰ)为 ;判断制备反应结束的实验现象是 。图示装置存在的两处缺陷
是 。
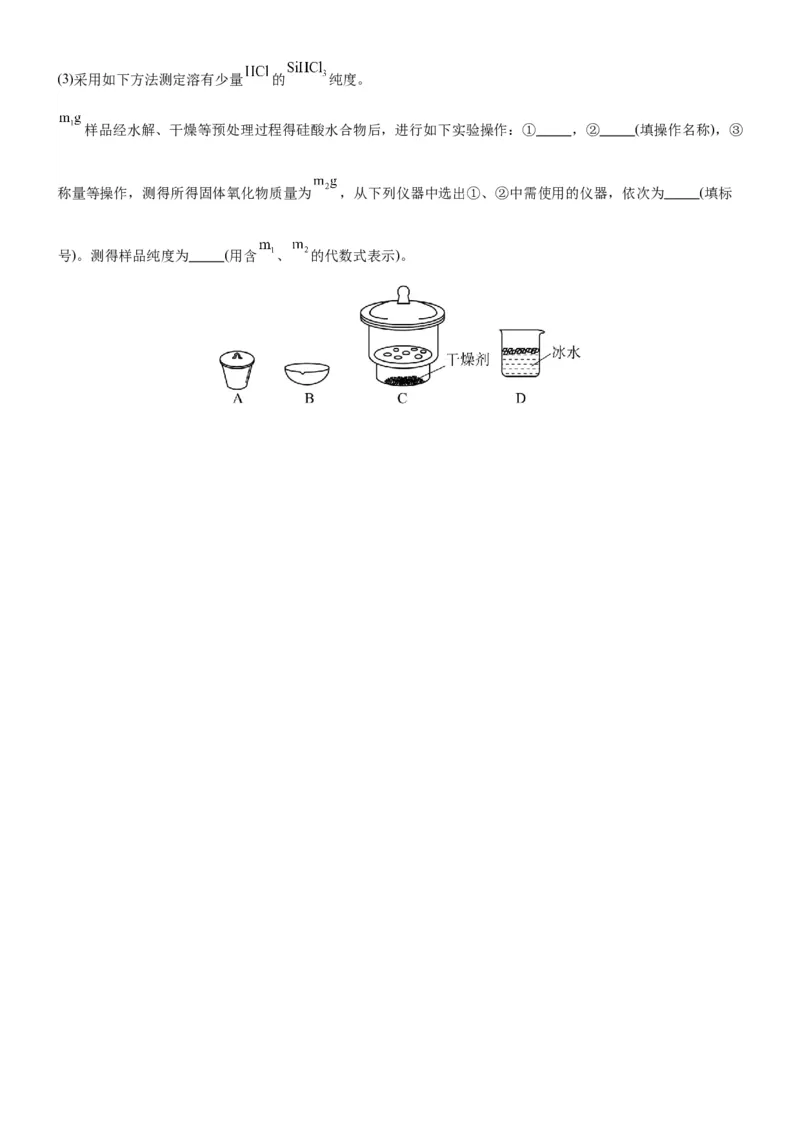
(2)已知电负性 在浓 溶液中发生反应的化学方程式为 。(3)采用如下方法测定溶有少量 的 纯度。
样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:① ,② (填操作名称),③
称量等操作,测得所得固体氧化物质量为 ,从下列仪器中选出①、②中需使用的仪器,依次为 (填标
号)。测得样品纯度为 (用含 、 的代数式表示)。