文档内容
考点 20 晶体结构与性质
目录
.............................................................................................................................................1
1.高考真题考点分布...................................................................................................................................1
2.命题规律及备考策略...............................................................................................................................1
.............................................................................................................................................2
考法01 晶体与晶胞...................................................................................................................................2
考法02 晶体的类型、结构与性质...........................................................................................................4
考法03 配合物与超分子...........................................................................................................................9
...........................................................................................................................................10
1.高考真题考点分布
考点内容 考点分布
2024·山东卷,3分;2024·浙江卷,3分;2024·安徽卷,3分;2024·甘肃卷,3
分;
2023·江苏卷,3分;2023·湖北卷,3分;2023·重庆卷,3分;2023山东卷5题,3
晶体的性质
分;2023北京卷1题,3分;2023全国新课标卷9题,6分;2022山东卷5题,2
分;
2022湖北卷7题,3分;
2024·辽宁卷,3分;2024·湖北卷,3分;2024·辽宁卷,3分;2024·新课标卷,6
配合物与超分子 分;
2024·浙江卷,3分;2023·湖南卷,3分;2022·江苏卷,3分;
2.命题规律及备考策略
【命题规律】
高频考点从近几年全国高考试题来看,晶体类型的判断、晶胞的计算、晶体密度、边长、半径、参数等相
关计算仍是高考命题的热点。
【备考策略】【命题预测】
预计2025年高考会以新的情境载体考查有关晶体类型判断、四种晶体的区别、晶体的结构特点以及晶胞的
相关计算等知识,题目难度一般适中。
考法01 晶体与晶胞
1.物质的聚集状态
(1)物质的聚集状态除了固态、液态、气态,还有 、非晶态以及介乎晶态和非晶态之间的塑晶态、液
晶态等。
(2)等离子体和液晶
①等离子体:由电子、阳离子和电中性粒子组成的整体上 的物质聚集体。具有良好的导电性和流动
性。
②液晶:介于 和 之间的物质状态。既具有液体的 、黏度、形变性等,又具有晶体的
、光学性质等。
2.晶体与非晶体
晶体 非晶体
结构特征 结构微粒 排列 结构微粒
自范性
性质特征 熔点
异同表现
二者区别 间接方法 看是否有固定的
方法 科学方法 对固体进行 实验
3.获得晶体的三条途径
(1)熔融态物质凝固。
(2)气态物质冷却不经液态直接凝固(凝华)。
(3)溶质从溶液中析出。
4.晶胞
(1)晶胞:晶胞是描述晶体结构的基本单元。
(2)晶体中晶胞的排列——无隙并置①无隙:相邻晶胞之间没有任何 。
②并置:所有晶胞 排列、 相同。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)冰和碘晶体中相互作用力相同( )
(2)凡有规则外形的固体一定是晶体( )
(3)固体SiO 一定是晶体( )
2
(4)缺角的NaCl晶体在饱和NaCl溶液中会慢慢变为完美的立方体块( )
(5)晶胞是晶体中最小的“平行六面体”( )
(6)区分晶体和非晶体最可靠的方法是对固体进行X射线衍射实验( )
(7)晶体内部的微粒按一定规律周期性排列( )
(8)晶胞是晶体中最小的“平行六面体” ( )
(9)区分晶体和非晶体最可靠的方法是对固体进行X-射线衍射实验( )
(10)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过X射线衍射方法区分晶体、准
晶体和非晶体( )
考向01 考查物质聚集状态的多样性
【例1】(2024·江西景德镇·模拟)下列有关物质特殊聚集状态与结构的说法不正确的是( )
A.液晶中分子的长轴取向一致,表现出类似晶体的各向异性
B.等离子体是一种特殊的气体,由阳离子和电子两部分构成
C.纯物质有固定的熔点,但其晶体颗粒尺寸在纳米量级时也可能发生变化
D.超分子内部的分子间一般通过非共价键或分子间作用力结合成聚集体
考向02 考查晶体与非晶体
【例1】(2024·河北衡水·质检)下列物质中前者为晶体,后者为非晶体的是( )
A.白磷、蓝矾 B.陶瓷、塑料
C.碘、橡胶 D.食盐、蔗糖
【对点1】(2024·山东东营·模拟)水的状态除了气、液和固态外,还有玻璃态。它是由液态水急速冷却到
165 K时形成的。玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,下列有关玻
璃态水的叙述正确的是( )
A.水由液态变为玻璃态,体积缩小
B.水由液态变为玻璃态,体积膨胀
C.玻璃态是水的一种特殊状态
D.在玻璃态水的X射线图谱上有分立的斑点或明锐的衍射峰
【对点2】(2024·广东深圳·二模)晶体是一类非常重要的材料,在很多领域都有广泛的应用。我国现已能够拉制出直径为300毫米的大直径硅单晶,晶体硅大量用于电子产业。下列对晶体硅的叙述中正确的是(
)
A.形成晶体硅的速率越大越好
B.晶体硅没有固定的熔、沸点
C.可用X射线衍射实验来鉴别晶体硅和玻璃
D.晶体硅的形成与晶体的自范性有关,而与各向异性无关
考法02 晶体的类型、结构与性质
1.四类晶体的比较
类型
分子晶体 共价晶体 金属晶体 离子晶体
比较
构成粒子
粒子间的相互
作用力
硬度 较 很 有的很大,有的很小 较
熔、沸点 较 很 有的很高,有的很低 较
难溶于任何 大多易溶于水等极
溶解性 相似相溶 难溶于常见溶剂
溶剂 性溶剂中
一般不导电,溶 一般不具有 晶体不导电,水溶
导电、传热性 电和热的良导体
于水后有的导电 导电性 液或熔融态导电
2.常见晶体结构模型
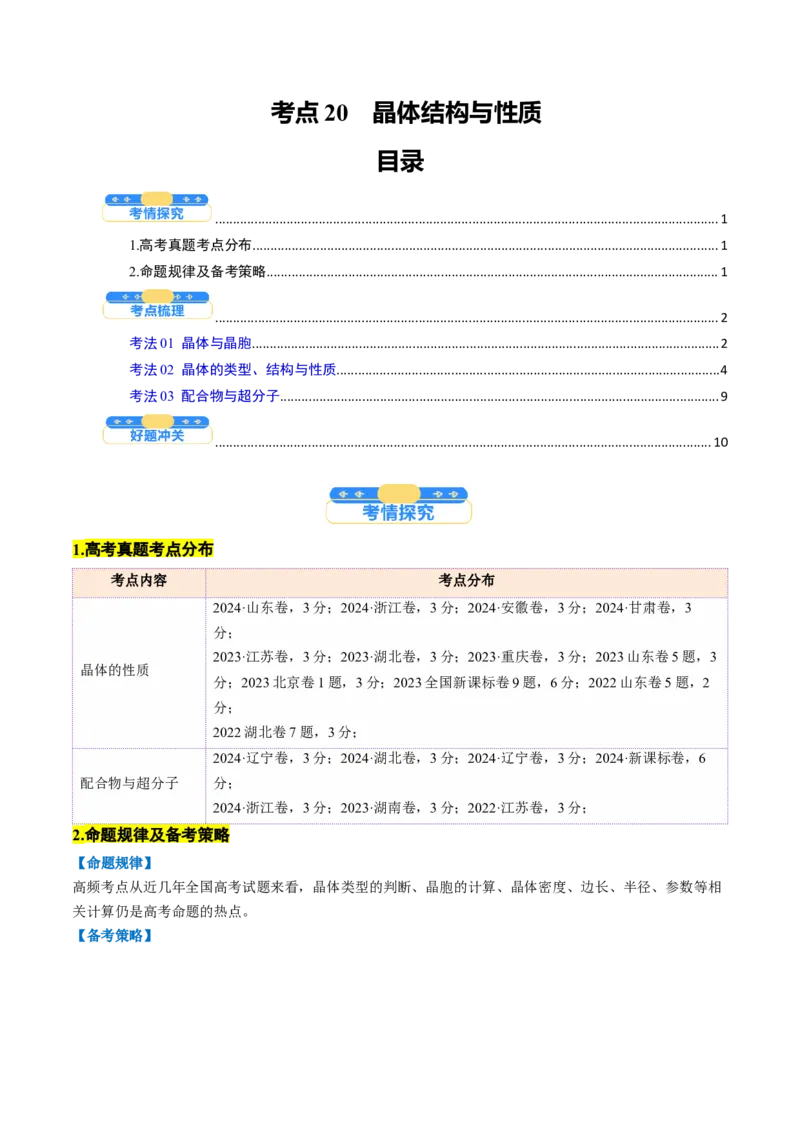
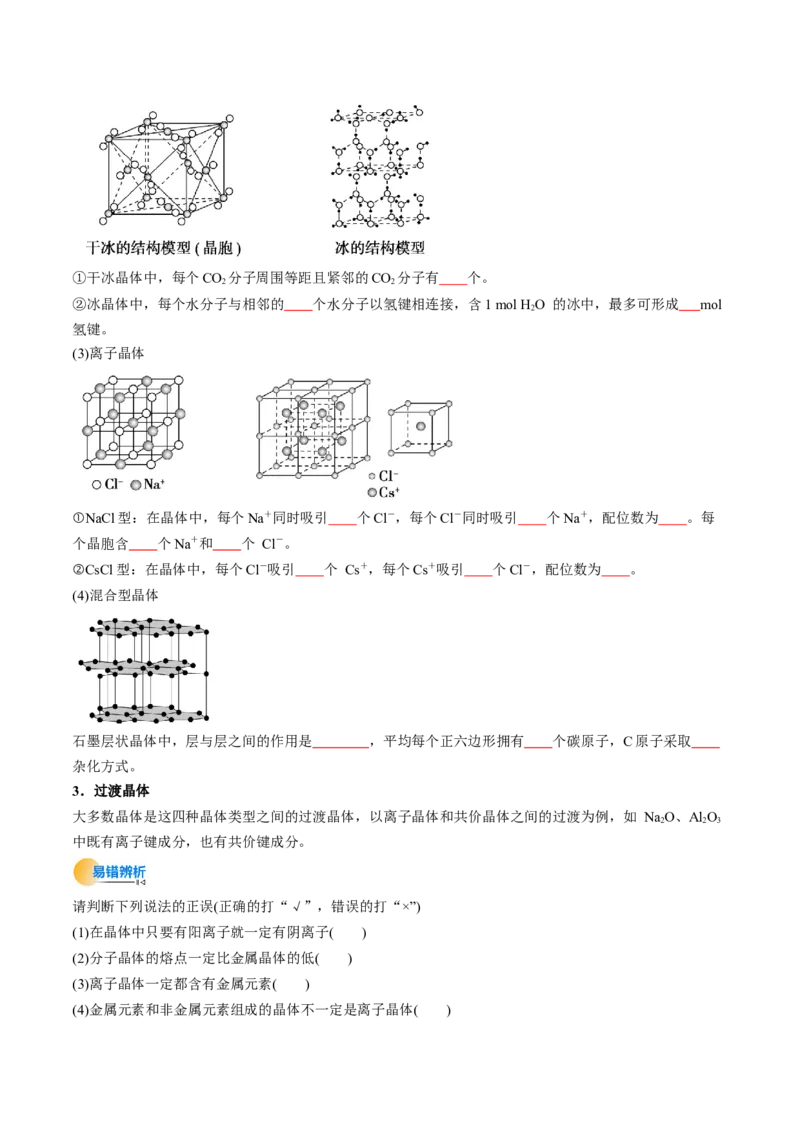
(1)共价晶体
①金刚石晶体中,每个C与相邻 个C形成共价键,C—C—C夹角是 ,最小的环是 元环。含有
1 mol C的金刚石中,形成的共价键是 mol。
②SiO 晶体中,每个Si原子与 个O原子成键,每个O原子与 个硅原子形成共价键,最小的环
2
是 元环,在“硅氧”四面体中,处于中心的是 原子,1 mol SiO 晶体中含有 mol Si—O
2
键。
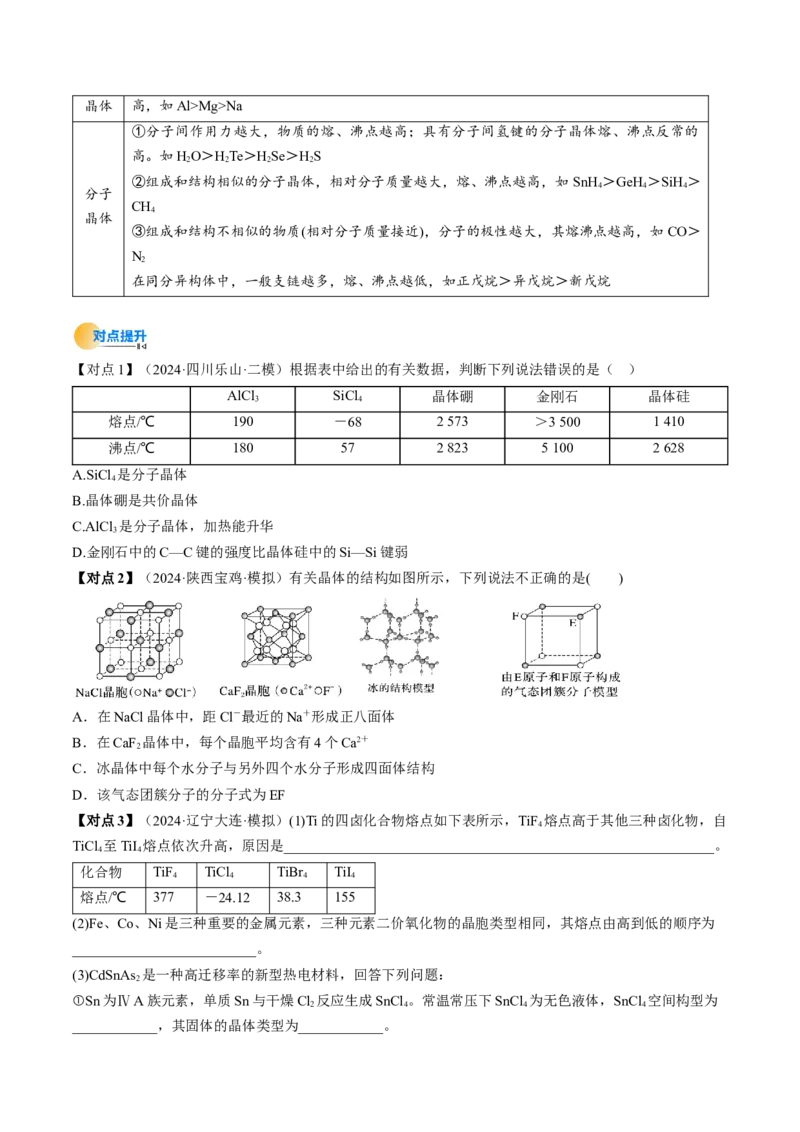
(2)分子晶体①干冰晶体中,每个CO 分子周围等距且紧邻的CO 分子有 个。
2 2
②冰晶体中,每个水分子与相邻的 个水分子以氢键相连接,含1 mol H O 的冰中,最多可形成 mol
2
氢键。
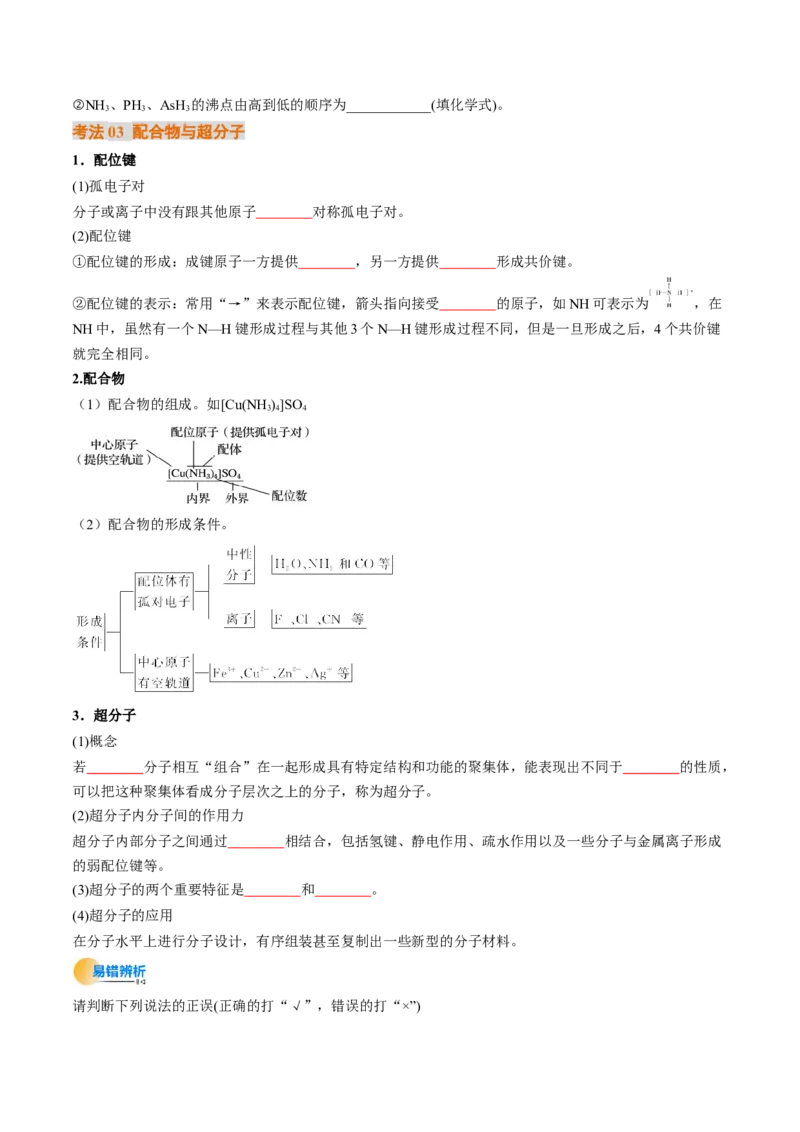
(3)离子晶体
①NaCl型:在晶体中,每个Na+同时吸引 个Cl-,每个Cl-同时吸引 个Na+,配位数为 。每
个晶胞含 个Na+和 个 Cl-。
②CsCl型:在晶体中,每个Cl-吸引 个 Cs+,每个Cs+吸引 个Cl-,配位数为 。
(4)混合型晶体
石墨层状晶体中,层与层之间的作用是 ,平均每个正六边形拥有 个碳原子,C原子采取
杂化方式。
3.过渡晶体
大多数晶体是这四种晶体类型之间的过渡晶体,以离子晶体和共价晶体之间的过渡为例,如 NaO、Al O
2 2 3
中既有离子键成分,也有共价键成分。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)在晶体中只要有阳离子就一定有阴离子( )
(2)分子晶体的熔点一定比金属晶体的低( )
(3)离子晶体一定都含有金属元素( )
(4)金属元素和非金属元素组成的晶体不一定是离子晶体( )(5)1 mol金刚石和1 mol SiO 中含有的共价键数目均为4N ( )
2 A
(6)氯化钠晶体中,每个Na+周围距离相等且最近的Na+共有6个( )
(7)冰中包含的作用力有范德华力、氢键和共价键( )
(8)离子晶体一定都含有金属元素( )
(9)金属元素和非金属元素组成的晶体不一定是离子晶体( )
(10)冰和固体碘晶体中相互作用力相同( )
考向01 考查晶体类型的判断
【例1】(2024·湖南常德·一模)下列有关晶体类型的判断正确的是( )
A SiI :熔点120.5 ℃,沸点271.5 ℃ 共价晶体
4
B B:熔点2 300 ℃,沸点2 550 ℃,硬度大 金属晶体
C 锑:熔点630.74 ℃,沸点1 750 ℃,晶体导电 共价晶体
D FeCl :熔点282 ℃,易溶于水,也易溶于有机溶剂 分子晶体
3
考向02 考查晶体的结构
【例2】(2024·四川乐山·二模)下列有关晶体结构的叙述中错误的是( )
A.金刚石的网状结构中,最小的环上有6个碳原子
B.分子晶体熔化时,不破坏共价键;共价晶体熔化时,破坏共价键
C.在金属铜的晶体中,由于存在自由电子,因此铜能导电
D.在氯化铯晶体中,每个氯离子周围最近且距离相等的氯离子有8个
考向03 考查晶体熔、沸点高低的比较
【例3】(2024·四川乐山·二模)硅、锗(Ge)及其化合物广泛应用于光电材料领域。回答下列问题:
(1)晶体硅和碳化硅熔点较高的是________(填化学式)。
(2)硅和卤素单质反应可以得到SiX,SiX 的熔、沸点如下表:
4 4
SiF SiCl SiBr SiI
4 4 4 4
熔点/K 183.0 203.2 278.6 393.7
沸点/K 187.2 330.8 427.2 560.7
0 ℃时,SiF、SiCl 、SiBr 、SiI 呈液态的是________(填化学式),沸点依次升高的原因是
4 4 4 4
__________________________________________________________________。
【思维建模】物质熔、沸点高低比较规律
一般情况下,原子晶体>离子晶体>分子晶体,如:金刚石>NaCl>Cl ;金属晶体>分子晶体,如:
2
Na>Cl 。(金属晶体熔、沸点有的很高,如钨、铂等,有的则很低,如汞等)
2
原子
→→,如:金刚石>石英>晶体硅
晶体
离子 一般地说,阴阳离子的电荷数越多,离子半径越小,离子键越强,晶格能越大,熔、沸点就
晶体 越高。如:MgO>MgCl ,NaCl>CsCl
2
金属 金属离子半径越小,离子所带电荷数越多,其形成的金属键越强,金属单质的熔、沸点就越晶体 高,如Al>Mg>Na
①分子间作用力越大,物质的熔、沸点越高;具有分子间氢键的分子晶体熔、沸点反常的
高。如HO>HTe>HSe>HS
2 2 2 2
②组成和结构相似的分子晶体,相对分子质量越大,熔、沸点越高,如 SnH >GeH >SiH>
4 4 4
分子
CH
4
晶体
③组成和结构不相似的物质(相对分子质量接近),分子的极性越大,其熔沸点越高,如CO>
N
2
在同分异构体中,一般支链越多,熔、沸点越低,如正戊烷>异戊烷>新戊烷
【对点1】(2024·四川乐山·二模)根据表中给出的有关数据,判断下列说法错误的是( )
AlCl SiCl 晶体硼 金刚石 晶体硅
3 4
熔点/℃ 190 -68 2 573 >3 500 1 410
沸点/℃ 180 57 2 823 5 100 2 628
A.SiCl 是分子晶体
4
B.晶体硼是共价晶体
C.AlCl 是分子晶体,加热能升华
3
D.金刚石中的C—C键的强度比晶体硅中的Si—Si键弱
【对点2】(2024·陕西宝鸡·模拟)有关晶体的结构如图所示,下列说法不正确的是( )
A.在NaCl晶体中,距Cl-最近的Na+形成正八面体
B.在CaF 晶体中,每个晶胞平均含有4个Ca2+
2
C.冰晶体中每个水分子与另外四个水分子形成四面体结构
D.该气态团簇分子的分子式为EF
【对点3】(2024·辽宁大连·模拟)(1)Ti的四卤化合物熔点如下表所示,TiF 熔点高于其他三种卤化物,自
4
TiCl 至TiI 熔点依次升高,原因是_____________________________________________________________。
4 4
化合物 TiF TiCl TiBr TiI
4 4 4 4
熔点/℃ 377 -24.12 38.3 155
(2)Fe、Co、Ni是三种重要的金属元素,三种元素二价氧化物的晶胞类型相同,其熔点由高到低的顺序为
__________________________。
(3)CdSnAs 是一种高迁移率的新型热电材料,回答下列问题:
2
①Sn为ⅣA族元素,单质Sn与干燥Cl 反应生成SnCl 。常温常压下SnCl 为无色液体,SnCl 空间构型为
2 4 4 4
____________,其固体的晶体类型为____________。②NH 、PH 、AsH 的沸点由高到低的顺序为____________(填化学式)。
3 3 3
考法03 配合物与超分子
1.配位键
(1)孤电子对
分子或离子中没有跟其他原子 对称孤电子对。
(2)配位键
①配位键的形成:成键原子一方提供 ,另一方提供 形成共价键。
②配位键的表示:常用“→”来表示配位键,箭头指向接受 的原子,如NH可表示为 ,在
NH中,虽然有一个N—H键形成过程与其他3个N—H键形成过程不同,但是一旦形成之后,4个共价键
就完全相同。
2.配合物
(1)配合物的组成。如[Cu(NH )]SO
3 4 4
(2)配合物的形成条件。
3.超分子
(1)概念
若 分子相互“组合”在一起形成具有特定结构和功能的聚集体,能表现出不同于 的性质,
可以把这种聚集体看成分子层次之上的分子,称为超分子。
(2)超分子内分子间的作用力
超分子内部分子之间通过 相结合,包括氢键、静电作用、疏水作用以及一些分子与金属离子形成
的弱配位键等。
(3)超分子的两个重要特征是 和 。
(4)超分子的应用
在分子水平上进行分子设计,有序组装甚至复制出一些新型的分子材料。
请判断下列说法的正误(正确的打“√”,错误的打“×”)(1)配位键实质上是一种特殊的共价键( )
(2)提供孤电子对的微粒既可以是分子,也可以是离子( )
(3)有配位键的化合物就是配位化合物( )
(4)配位化合物都很稳定( )
(5)在配合物[Co(NH )Cl]Cl 中的Cl-均可与AgNO 反应生成AgCl沉淀( )
3 5 2 3
(6)Ni(CO) 是配合物,它是由中心原子与配体构成的( )
4
考向01 考查配合物
【例1】(2024·河北邢台·一模)Zn(OH) 溶于氨水可生成可溶性配合物[Zn(NH )](OH) ,下列说法正确的
2 3 4 2
是( )
A.根据上述信息可推导出氢氧化锌为两性氢氧化物
B.该配合物中只有离子键和配位键
C.形成该配合物的离子方程式为:Zn(OH) +4NH ===[Zn(NH)]2++2OH-
2 3 3 4
D.该配合离子中由NH 提供空轨道,Zn2+提供电子对
3
考向02 考查超分子
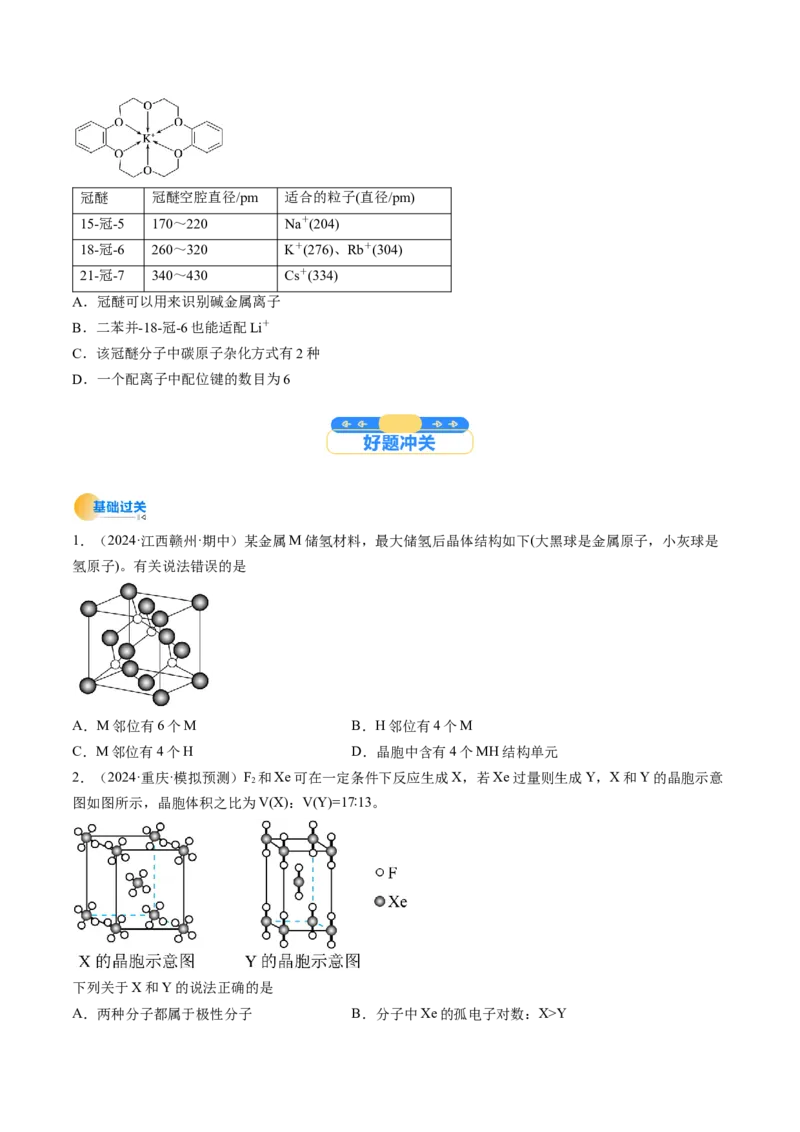
【例2】(2024·安徽亳州·二模)利用超分子可分离C 和C 。将C 、C 混合物加入一种空腔大小适配
60 70 60 70
C 的“杯酚”中进行分离的流程如图。下列说法错误的是( )
60
A.第一电离能:CYC.两种晶体都属于分子晶体 D.晶体密度:X>Y
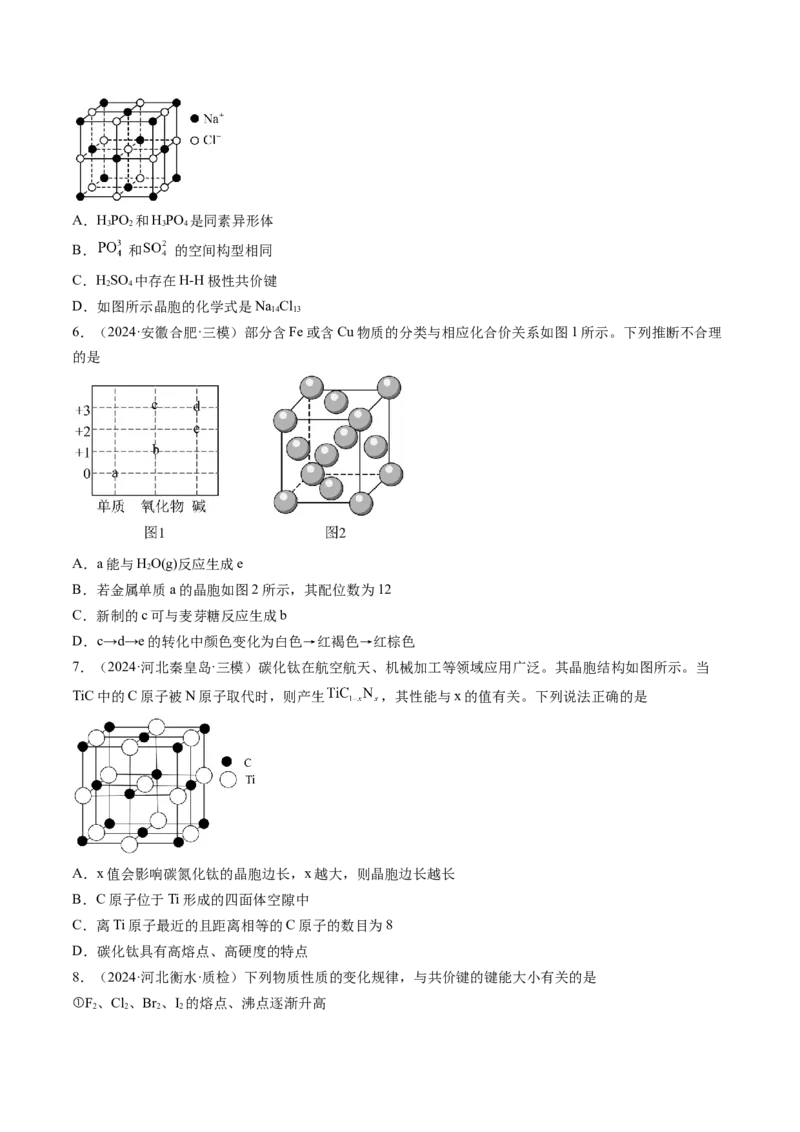
3.(2024·重庆·期中)有关晶体的结构如图所示,下列说法不正确的是
○ ● 晶胞(● )
冰的结构模型 由E原子和F原子构成的气态团簇分子模型
A.在NaCl晶体中,距 最近的 形成正八面体
B.在 晶胞中, 的配位数为4
C.冰晶体中每个水分子与另外四个水分子形成四面体结构
D.该气态团簇分子的分子式为EF
4.(2024·黑龙江大庆·模拟预测)有关晶体的结构如下图所示。下列说法错误的是
A.在 晶体中,每个晶胞平均占有4个
B.在金刚石晶体中,碳原子与碳碳键个数之比为
C.在 晶体中,阴阳离子的总个数为
D.由E原子和F原子构成的气态团簇分子的分子式为EF或FE
5.(2024·江苏盐城·期中)下列说法正确的是A.HPO 和HPO 是同素异形体
3 2 3 4
B. 和 的空间构型相同
C.HSO 中存在H-H极性共价键
2 4
D.如图所示晶胞的化学式是Na Cl
14 13
6.(2024·安徽合肥·三模)部分含Fe或含Cu物质的分类与相应化合价关系如图1所示。下列推断不合理
的是
A.a能与HO(g)反应生成e
2
B.若金属单质a的晶胞如图2所示,其配位数为12
C.新制的c可与麦芽糖反应生成b
D.c→d→e的转化中颜色变化为白色→红褐色→红棕色
7.(2024·河北秦皇岛·三模)碳化钛在航空航天、机械加工等领域应用广泛。其晶胞结构如图所示。当
TiC中的C原子被N原子取代时,则产生 ,其性能与x的值有关。下列说法正确的是
A.x值会影响碳氮化钛的晶胞边长,x越大,则晶胞边长越长
B.C原子位于Ti形成的四面体空隙中
C.离Ti原子最近的且距离相等的C原子的数目为8
D.碳化钛具有高熔点、高硬度的特点
8.(2024·河北衡水·质检)下列物质性质的变化规律,与共价键的键能大小有关的是
①F、Cl、Br 、I 的熔点、沸点逐渐升高
2 2 2 2②HF、HCl、HBr、HI的热稳定性依次减弱
③金刚石的硬度、熔点、沸点都高于晶体硅
④H O的沸点高于HS的沸点
2 2
A.①② B.②③ C.①④ D.②④
9.(2024··辽宁大连·期中)氯化钠的一种晶胞结构如图所示,下列有关氯化钠的说法正确的是
A.该晶胞结构中有6个Na+和6个Cl-
B.Na+的配位数为4
C.117g氯化钠中有2molNaCl分子
D.将晶胞沿体对角线AB作投影,CD两原子的投影将相互重合
10.(2024·江苏苏州·期中)石墨烯是从石墨材料中剥离出来,由碳原子组成的只有一层原子厚度的二维
晶体。下列关于石墨与石墨烯的说法正确的是
A.从石墨中剥离石墨烯需要破坏化学键
B.石墨中的碳原子采取sp3杂化
C.石墨属于混合型晶体,层与层之间存在分子间作用力;层内碳原子间存在共价键,石墨能导电,存在
金属键
D.石墨烯中平均每个六元碳环含有3个碳原子
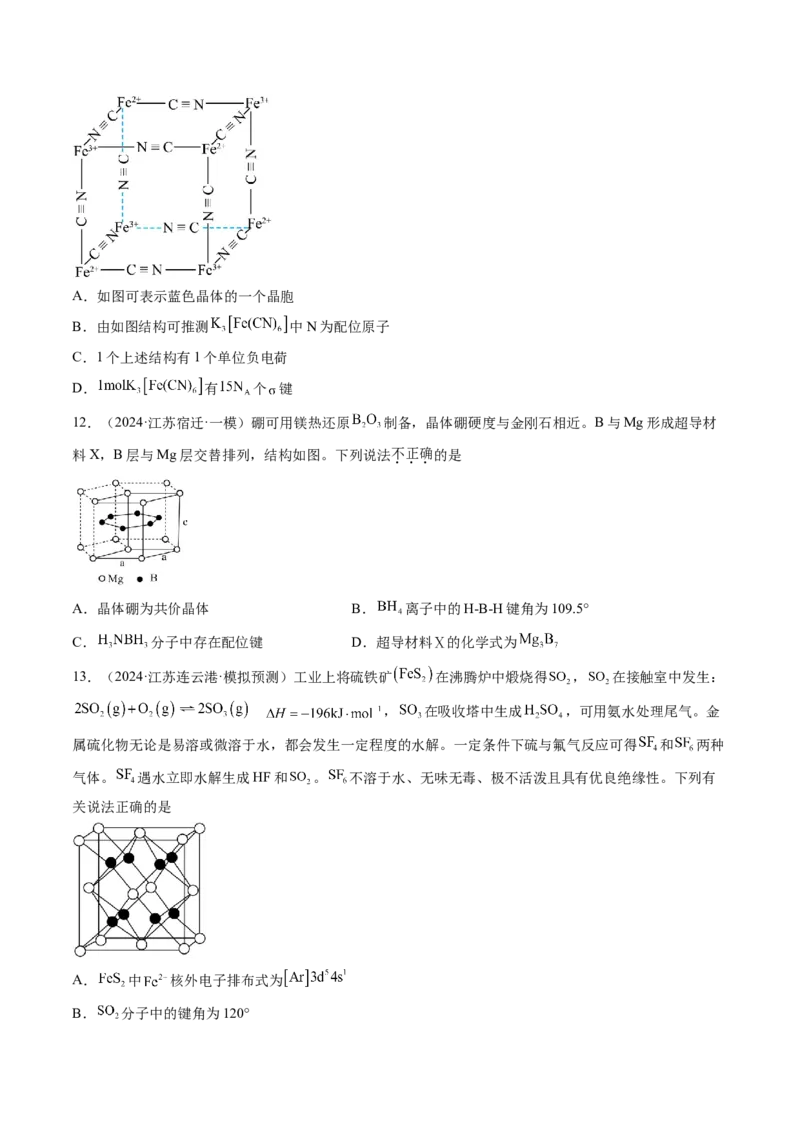
11.(2024·四川成都·模拟预测)常用于检验 的试剂为 ,反应生成的蓝色沉淀其晶体中基
本单元的部分结构如图。下列说法正确的是A.如图可表示蓝色晶体的一个晶胞
B.由如图结构可推测 中N为配位原子
C.1个上述结构有1个单位负电荷
D. 有 个 键
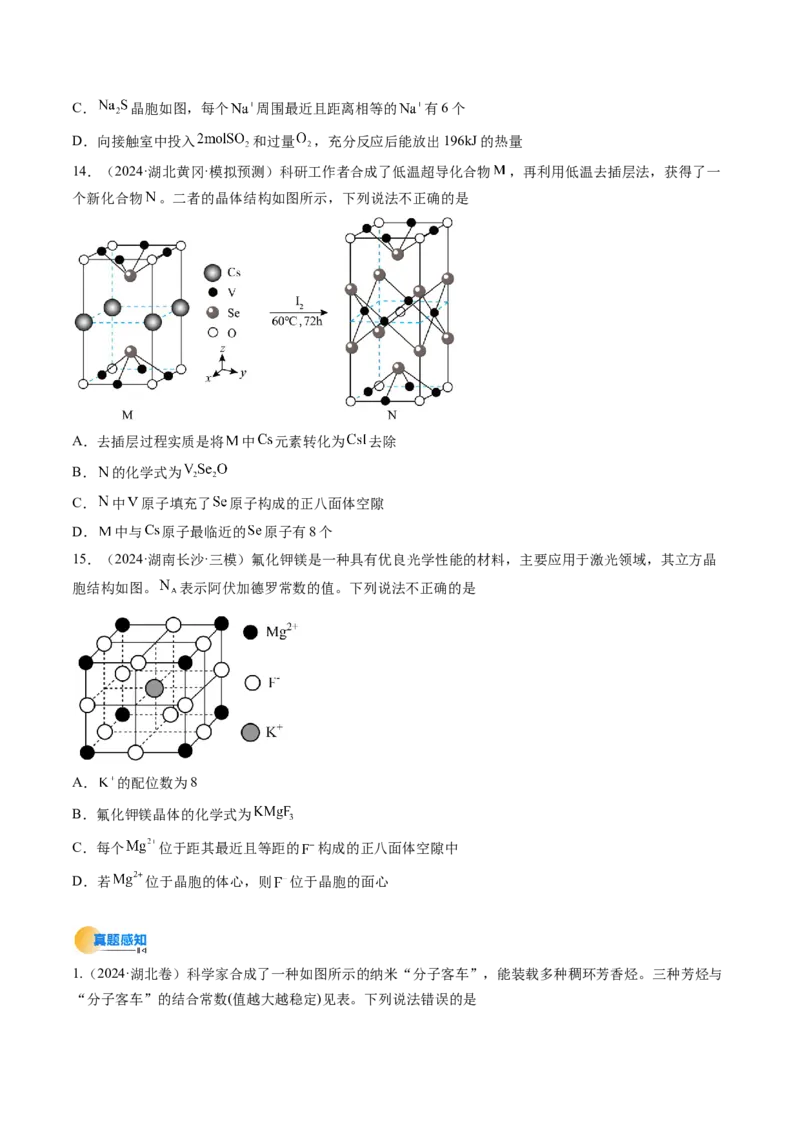
12.(2024·江苏宿迁·一模)硼可用镁热还原 制备,晶体硼硬度与金刚石相近。B与Mg形成超导材
料X,B层与Mg层交替排列,结构如图。下列说法不正确的是
A.晶体硼为共价晶体 B. 离子中的H-B-H键角为109.5°
C. 分子中存在配位键 D.超导材料Ⅹ的化学式为
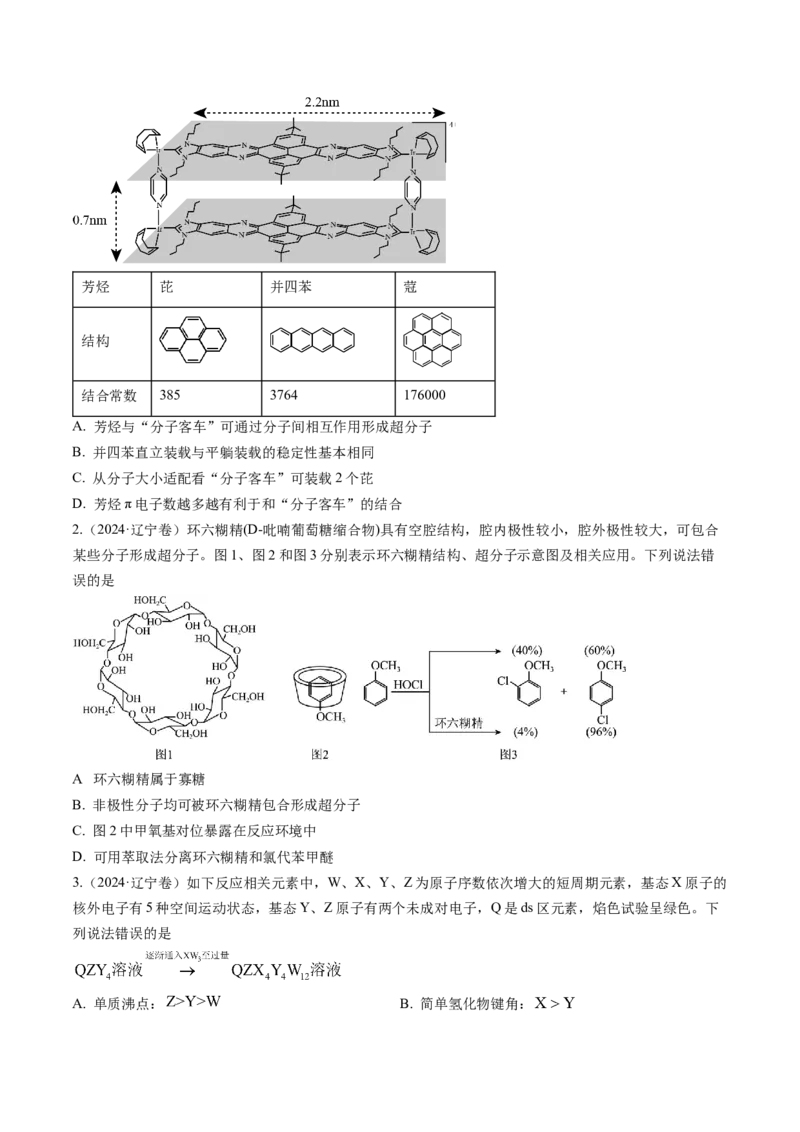
13.(2024·江苏连云港·模拟预测)工业上将硫铁矿 在沸腾炉中煅烧得 , 在接触室中发生:
, 在吸收塔中生成 ,可用氨水处理尾气。金
属硫化物无论是易溶或微溶于水,都会发生一定程度的水解。一定条件下硫与氟气反应可得 和 两种
气体。 遇水立即水解生成HF和 。 不溶于水、无味无毒、极不活泼且具有优良绝缘性。下列有
关说法正确的是
A. 中 核外电子排布式为
B. 分子中的键角为120°C. 晶胞如图,每个 周围最近且距离相等的 有6个
D.向接触室中投入 和过量 ,充分反应后能放出196kJ的热量
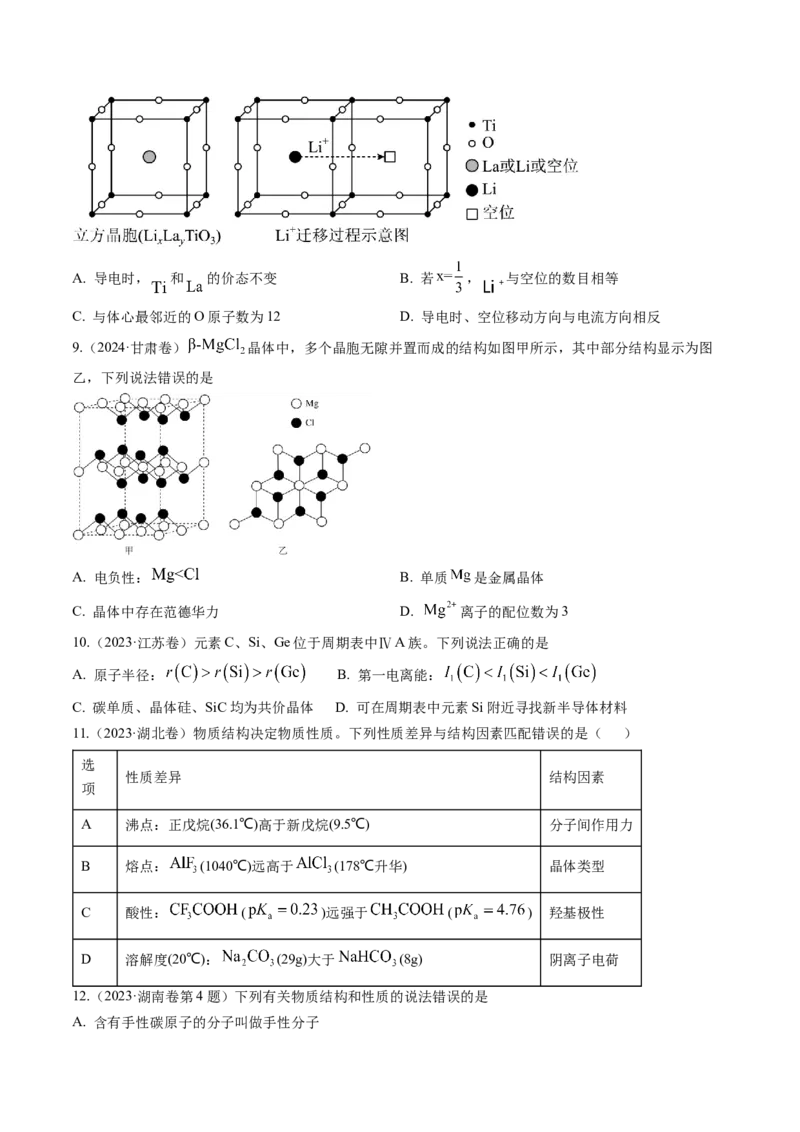
14.(2024·湖北黄冈·模拟预测)科研工作者合成了低温超导化合物 ,再利用低温去插层法,获得了一
个新化合物 。二者的晶体结构如图所示,下列说法不正确的是
A.去插层过程实质是将 中 元素转化为 去除
B. 的化学式为
C. 中 原子填充了 原子构成的正八面体空隙
D. 中与 原子最临近的 原子有8个
15.(2024·湖南长沙·三模)氟化钾镁是一种具有优良光学性能的材料,主要应用于激光领域,其立方晶
胞结构如图。 表示阿伏加德罗常数的值。下列说法不正确的是
A. 的配位数为8
B.氟化钾镁晶体的化学式为
C.每个 位于距其最近且等距的 构成的正八面体空隙中
D.若 位于晶胞的体心,则 位于晶胞的面心
1.(2024·湖北卷)科学家合成了一种如图所示的纳米“分子客车”,能装载多种稠环芳香烃。三种芳烃与
“分子客车”的结合常数(值越大越稳定)见表。下列说法错误的是芳烃 芘 并四苯 蒄
结构
结合常数 385 3764 176000
A. 芳烃与“分子客车”可通过分子间相互作用形成超分子
B. 并四苯直立装载与平躺装载的稳定性基本相同
C. 从分子大小适配看“分子客车”可装载2个芘
D. 芳烃π电子数越多越有利于和“分子客车”的结合
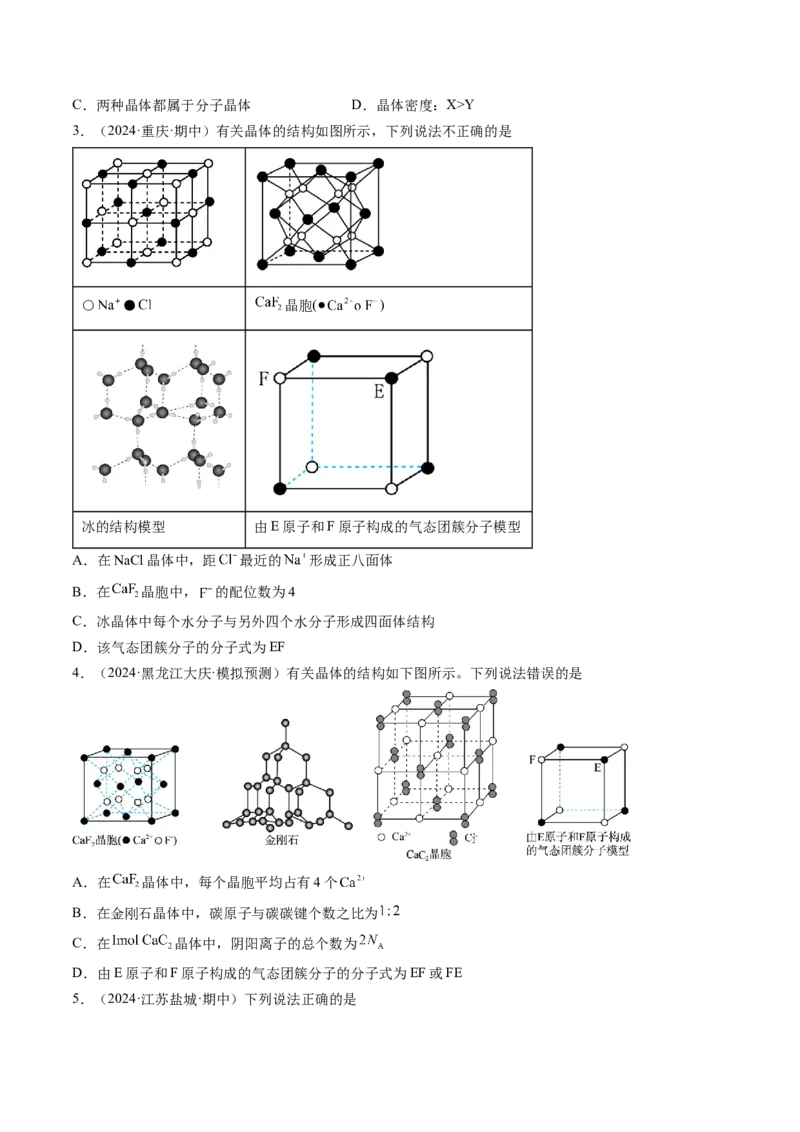
2.(2024·辽宁卷)环六糊精(D-吡喃葡萄糖缩合物)具有空腔结构,腔内极性较小,腔外极性较大,可包合
某些分子形成超分子。图1、图2和图3分别表示环六糊精结构、超分子示意图及相关应用。下列说法错
误的是
.
A 环六糊精属于寡糖
B. 非极性分子均可被环六糊精包合形成超分子
C. 图2中甲氧基对位暴露在反应环境中
D. 可用萃取法分离环六糊精和氯代苯甲醚
3.(2024·辽宁卷)如下反应相关元素中,W、X、Y、Z为原子序数依次增大的短周期元素,基态X原子的
核外电子有5种空间运动状态,基态Y、Z原子有两个未成对电子,Q是ds区元素,焰色试验呈绿色。下
列说法错误的是
A. 单质沸点: B. 简单氢化物键角:C. 反应过程中有蓝色沉淀产生 D. 是配合物,配位原子是Y
4.(2024·山东卷)下列物质均为共价晶体且成键结构相似,其中熔点最低的是
A. 金刚石(C) B. 单晶硅( ) C. 金刚砂( ) D. 氮化硼( ,立方相)
5.(2024·新课标卷)我国科学家最近研究的一种无机盐 纳米药物具有高效的细胞内亚铁离
子捕获和抗氧化能力。W、X、Y、Z的原子序数依次增加,且W、X、Y属于不同族的短周期元素。W的
外层电子数是其内层电子数的2倍,X和Y的第一电离能都比左右相邻元素的高。Z的M层未成对电子数
为4。下列叙述错误的是
A. W、X、Y、Z四种元素的单质中Z的熔点最高
B. 在X的简单氢化物中X原子轨道杂化类型为
C. Y的氢氧化物难溶于NaCl溶液,可以溶于 溶液
D. 中 提供电子对与 形成配位键
6.(2024·浙江卷)物质微观结构决定宏观性质,进而影响用途。下列结构或性质不能解释其用途的是
选
结构或性质 用途
项
A 石墨呈层状结构,层间以范德华力结合 石墨可用作润滑剂
B 具有氧化性 可用作漂白剂
C 聚丙烯酸钠( )中含有亲水基团 聚丙烯酸钠可用于制备高吸水性树脂
冠醚18-冠-6空腔直径( )与 直径(
冠醚18-冠-6可识别 ,能增大 在有机
D
)接近 溶剂中的溶解度
7.(2024·浙江卷)X、Y、Z、M四种主族元素,原子序数依次增大,分别位于三个不同短周期,Y与M同
主族,Y与Z核电荷数相差2,Z的原子最外层电子数是内层电子数的3倍。下列说法不正确的是
A. 键角: B. 分子的极性:
C. 共价晶体熔点: D. 热稳定性:
8.(2024·安徽卷)研究人员制备了一种具有锂离子通道的导电氧化物( ),其立方晶胞和导电
时 迁移过程如下图所示。已知该氧化物中 为 价, 为 价。下列说法错误的是A. 导电时, 和 的价态不变 B. 若 , 与空位的数目相等
C. 与体心最邻近的O原子数为12 D. 导电时、空位移动方向与电流方向相反
9.(2024·甘肃卷) 晶体中,多个晶胞无隙并置而成的结构如图甲所示,其中部分结构显示为图
乙,下列说法错误的是
A. 电负性: B. 单质 是金属晶体
C. 晶体中存在范德华力 D. 离子的配位数为3
10.(2023·江苏卷)元素C、Si、Ge位于周期表中ⅣA族。下列说法正确的是
A. 原子半径: B. 第一电离能:
C. 碳单质、晶体硅、SiC均为共价晶体 D. 可在周期表中元素Si附近寻找新半导体材料
11.(2023·湖北卷)物质结构决定物质性质。下列性质差异与结构因素匹配错误的是( )
选
性质差异 结构因素
项
A 沸点:正戊烷(36.1℃)高于新戊烷(9.5℃) 分子间作用力
B 熔点: (1040℃)远高于 (178℃升华) 晶体类型
C 酸性: ( )远强于 ( ) 羟基极性
D 溶解度(20℃): (29g)大于 (8g) 阴离子电荷
12.(2023·湖南卷第4题)下列有关物质结构和性质的说法错误的是
A. 含有手性碳原子的分子叫做手性分子B. 邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点
C. 酰胺在酸或碱存在并加热的条件下可发生水解反应
D. 冠醚(18-冠-6)的空穴与K+尺寸适配,两者能通过弱相互作用形成超分子
13.(2023·重庆卷第9题)配合物[MA L]的分子结构以及分子在晶胞中的位置如图所示,下列说法错误的
2 2
是
A. 中心原子的配位数是4 B. 晶胞中配合物分子的数目为2
C. 晶体中相邻分子间存在范德华力 D. 该晶体属于混合型晶体
14.(2023·北京,1)中国科学家首次成功制得大面积单晶石墨炔,是碳材料科学的一大进步。
下列关于金刚石、石墨、石墨炔的说法正确的是( )
A.三种物质中均有碳碳原子间的σ键
B.三种物质中的碳原子都是sp3杂化
C.三种物质的晶体类型相同
D.三种物质均能导电
15.(2023·山东,5)石墨与F 在450 ℃反应,石墨层间插入F得到层状结构化合物(CF),该物质仍具润滑
2 x
性,其单层局部结构如图所示。下列关于该化合物的说法正确的是( )
A.与石墨相比,(CF) 导电性增强
x
B.与石墨相比,(CF) 抗氧化性增强
x
C.(CF) 中C—C的键长比C—F短
x
D.1 mol (CF) 中含有2x mol共价单键
x
16.(2022·江苏卷)下列说法正确的是A. 金刚石与石墨烯中的 夹角都为
B. 、 都是由极性键构成的非极性分子
C. 锗原子( )基态核外电子排布式为
D. ⅣA族元素单质的晶体类型相同
17.(2022•山东卷)AlN、GaN属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在
键、 键。下列说法错误的是( )
A. 的熔点高于 B.晶体中所有化学键均为极性键
C.晶体中所有原子均采取sp3杂化 D.晶体中所有原子的配位数均相同
18.(2022·湖北,7)C 在高温高压下可转变为具有一定导电性、高硬度的非晶态碳玻璃。下列关于该碳玻
60
璃的说法错误的是( )
A.具有自范性
B.与C 互为同素异形体
60
C.含有sp3杂化的碳原子
D.化学性质与金刚石有差异
19.(2022·山东卷) 、 属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在
键、 键。下列说法错误的是
A. 的熔点高于 B. 晶体中所有化学键均为极性键
C. 晶体中所有原子均采取 杂化 D. 晶体中所有原子的配位数均相同