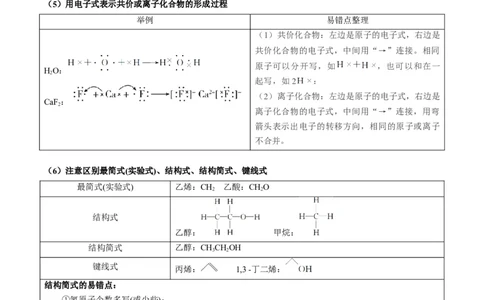
文档内容
重难点 02 化学用语
►命题趋势►解题策略►真题回眸►限时检测
考向一 原子结构用语的书写及判断
考向二 分子结构用语的书写及判断
化学用语 考向三 共价微粒结构式书写及判断
考向四 微粒电子式的书写及判断
考向五 微粒间的相互关系
化学用语题型主要以选择题的形式呈现,整体难度不大,但是考察得非常细。因此,要求考生在复习
的时候,注意把握不同化学用语之间的区别,注意特殊性。预计在2024年高考中,化学用语的考查内容主
要包括物质组成和结构的各种图示,化学反应的各种表达式等。其中结构示意图、核外电子排布式、结构
式、球棍或比例模型、核素表示方法等仍是高频考点。复习时要特别关注以下几点:
①区分化学式和实验式的概念。
②结构式和结构简式的区别。
③易错物质的电子式的书写。
③球棍模型和填充模型的区别。
另外,要特别关注杂化轨道重叠的图示表达、电子云图的表达、VSEPR模型的图示表达、配位化合
物结构的书写等。
【策略1】掌握常用的图式及注意事项
(1)核素(原子或离子)符号
举例 易错点整理
C、Cl、Cl-、Mg2+
(1)左上角错写成中子数;
(2)左上角漏写质量数。
(2)核反应方程表示
举例 易错点整理
资料整理【淘宝店铺:向阳百分百】(1)核聚变、核裂变属于核反应,不是化学变化。
钋209的α衰变:Po→Pb+He
(2)核反应遵循的两守恒:
查德威克发现中子:Be+He→C+n
①反应前后质量数之和不变。
铀核裂变反应:U+n→Kr+Ba+3n
②反应前后质子数之和不变。
(3)原子(离子)结构示意图
举例 易错点整理
(1)最外层电子数写错,即原子的结构示意图与离子的结构示意图混
淆;
(2)核电荷数与相对原子质量混淆,如氮元素的核电荷数错误的写成
Cl: S2-:
+14等。
(4)电子式
举例 易错点整理
电子式书写的常见错误:
a、漏写未参与成键的电子,如:
。
b、化合物类型不清楚,漏写或多写[ ]及错写电荷数,如:
, 正 确 应 为
。
c、书写不规范,错写共用电子对,如:
CO 的 电 子 式 为 , 不 能 写 成
2
;N 的电子式为 ,不能写成
2
。
d、原子结合顺序写错,如:
HClO的电子式为 。
e、复杂阳离子与简单阳离子混淆不清,如:
Na+电子式的正确表示应为Na+,误写成 ;
资料整理【淘宝店铺:向阳百分百】NH电子式的正确表示应为 ,误写成NH。
f、不考虑AB 型离子化合物中2个B是分开写还是一起写,如:
2
CaBr 、CaC 的电子式分别为 、
2 2
。
(5)用电子式表示共价或离子化合物的形成过程
举例 易错点整理
(1)共价化合物:左边是原子的电子式,右边是
共价化合物的电子式,中间用“→”连接。相同
原子可以分开写,如 ,也可以和在一
HO:
2
起写,如2 :
(2)离子化合物:左边是原子的电子式,右边是
CaF :
2
离子化合物的电子式,中间用“→”连接,用弯
箭头表示出电子的转移方向,相同的原子或离子
不合并。
(6)注意区别最简式(实验式)、结构式、结构简式、键线式
最简式(实验式) 乙烯:CH 乙酸:CHO
2 2
结构式
乙醇: 甲烷:
结构简式 乙醇:CHCHOH
3 2
键线式
丙烯: 1,3 -丁二烯:
结构简式的易错点:
①氢原子个数多写(或少些);
②官能团的书写必须注意规范性,例如碳碳双键为“ ”,而不能写成“C===C”,碳碳三键
为“ ”,而不能写成“ ”,醛基应为“—CHO”,而不能写成“—COH”。
③写成结构式或分子式;
④相对位置关系写错,
键线式书写要注意的几个问题:
①一般表示3个及以上碳原子的有机物。
资料整理【淘宝店铺:向阳百分百】②只忽略C—H键,其余的化学键不能忽略。
③必须表示出 、—C≡C—等官能团。
④碳、氢原子不标注,其余原子必须标注(含羟基、醛基和羧基中氢原子)。
(7)注意区别球棍模型和比例模型
球棍模型
(1)注意原子的相对大小
CH: 乙烯:
4
(2)注意微粒的空间构型
比例(填充)模型
CH: 乙烯:
4
(8)原子核外电子的排布表示方法
表示方法 以铁原子为例
电子排布式 1s22s22p63s23p63d64s2
简化电子排布式 [Ar]3d64s2
价电子(外围电子、特征电
3d64s2
子)排布式
最外层电子排布式 4s2
M层电子排布式 3s23p63d6
最高能级电子排布式 3d6
电子排布图(轨道表示式)
价电子排布图
易错点整理:
(1)电子排布式
①原子的核外电子排布式的书写:首先明确原子的核外电子数,然后根据构造原理按顺序填充电子并
检查是否符合洪特规则特例,最后将相同能层的能级写在一起。如Cu:1s22s22p63s23p63d104s1。
②离子核外电子排布式的书写方法:先写出基态原子的核外电子排布式,再失去电子或补充电子(基
态原子失去电子时总是优先失去最外层电子),即得到相应阳离子或阴离子的核外电子排布式。
电子排布式能直观地反映核外电子的能层、能级和各能级上的电子数,但不能表示原子核的情况,
也不能表示各个电子的运动状态。
(2)简化电子排布式
一般用“[稀有气体]+价层电子”的形式表示。如Cu:[Ar]3d104s1。但31号元素(Ga)及以后的主族p
区元素书写简化电子排布式时除价层电子外还应加上nd10,如 As:[Ar]3d104s24p3。
33
(3)价层电子排布式
对于主族元素和0族元素,写出最外层电子排布式即可;对于过渡金属元素,其价层电子排布式一
资料整理【淘宝店铺:向阳百分百】般符合(n-1)d1~10ns1~2(n≥4)。价层电子排布式能反映基态原子的能层数和参与成键的电子数以及最外层电
子数。
(4)电子排布图(轨道表示式)
核外电子排布图能直观地反映出原子的核外电子的自旋情况以及成对的电子对数和未成对电子数。
(9)原子轨道模型
符号 s p d
球形 纺锤形(哑铃形) 花瓣形
电子云形
状
(10)杂化轨道模型
杂化方式 sp sp2 sp3
杂化轨道构型
【策略2】熟练等电子微粒的快速寻找方法
(1)寻找10电子微粒和18电子微粒的方法
①10电子微粒:以Ne为核心,推断同周期的非金属元素的化合物和下一周期的金属元素的化合物。
②18电子微粒:以Ar为核心,推断同周期的非金属元素的化合物和下一周期的金属元素的化合物。
CH—CH、HN—NH、HO—OH、F—F、F—CH 、CH—OH……
3 3 2 2 3 3
(2)记忆其他等电子微粒
“2电子”的粒子:He、H-、Li+、Be2+、H。
2
资料整理【淘宝店铺:向阳百分百】“9电子”的粒子:—F、—OH、—NH 、—CH(取代基)。
2 3
“14电子”的粒子:Si、N、CO。
2
“16电子”粒子:S、O、C H、HCHO。
2 2 4
考向一 原子结构用语的书写及判断
1.(22·23上·浙江·高考真题)下列表示不正确的是
A.乙炔的结构简式HC≡CH B.KOH的电子式
C.乙烷的球棍模型: D.氯离子的结构示意图:
【答案】C
【详解】A.乙炔中碳碳之间为三键,故结构简式HC≡CH,选项A正确;
B.KOH为离子化合物,故电子式为 ,选项B正确;
C. 为乙烷的比例模型,不是球棍模型,选项C错误;
D.氯离子的核电荷数是17,电子数为18,氯离子的结构示意图为 ,选项D正确;
故答案是C。
2.(21·22下·浙江·高考真题)下列表示正确的是
A.乙醛的结构简式: B. 丁烯的键线式:
C. 的结构示意图: D.过氧化钠的电子式:
【答案】D
【详解】A.乙醛含醛基,其结构简式为:CHCHO,A错误;
3
B.2-丁烯的结构简式为CHCH=CHCH ,键线式为: ,B错误;
3 3
C.硫的原子序数为16,硫原子最外层有6个电子,得2个电子形成硫离子,硫离子的结构示意图为:
,C错误;
D.过氧化钠为离子化合物,含离子键和氧氧非极性共价键,其电子式为: ,D正确;
资料整理【淘宝店铺:向阳百分百】答案选D。
3.(20·21下·重庆·高考真题)次磷酸根( )的球棍模型如图所示,下列说法错误的是
A.P的原子结构示意图为: B.次磷酸根的电子式为:
C.次磷酸根的结构式为: D.次磷酸分子式为:HPO
3 2
【答案】B
【详解】A.P是15号元素,质子数为15,核外电子数为15,原子结构示意图为: ,A正确;
B.次磷酸根中其中一个O与P原子共用2对电子对,正确的电子式为: ,B错误;
C.由次磷酸根( )的球棍模型,可得次磷酸根的结构式为: ,C正确;
D.次磷酸根为 ,次磷酸为一元弱酸,则次磷酸分子式为:HPO ,D正确;
3 2
故选:B。
考向二 分子结构用语的书写及判断
4.(22·23下·江苏·高考真题)反应 应用于石油开采。下列说法正确
的是
A. 的电子式为 B. 中N元素的化合价为+5
C. 分子中存在 键 D. 为非极性分子
【答案】C
【详解】A. 的电子式为 ,A错误;
B. 中N元素的化合价为+3,B错误;
资料整理【淘宝店铺:向阳百分百】C. 分子中存在 键,C正确;
D. 为V形分子,分子中正负电荷中心未重合,为极性分子,D错误。
故选C。
5.(22·23下·浙江·高考真题)下列化学用语表示正确的是
A. 分子的球棍模型:
B. 的价层电子对互斥模型:
C. 的电子式:
D. 的名称:3−甲基戊烷
【答案】D
【详解】A. 分子是“V”形结构,因此该图不是 分子的球棍模型,故A错误;
B. 中心原子价层电子对数为 ,其价层电子对互斥模型为平面三角形,故B错
误;
C. 是离子化合物,其电子式: ,故C错误;
D. 的结构简式为 ,其名称为3−甲基戊烷,故D正确。
综上所述,答案为D。
6.(22·23下·湖南·高考真题)下列化学用语表述错误的是
A.HClO的电子式:
B.中子数为10的氧原子: O
C.NH 分子的VSEPR模型:
3
D.基态N原子的价层电子排布图:
【答案】C
【详解】A.HClO中O元素呈负化合价,在结构中得到H和Cl共用的电子,因此HClO的电子式为
,A正确;
B.中子数为10,质子数为8的O原子其相对原子质量为10+8=18,其原子表示为 O,B正确;
C.根据VSEPR模型计算,NH 分子中有1对孤电子对,N还连接有3和H原子,因此NH 的VSEPR模型
3 3
为四面体型,C错误;
资料整理【淘宝店铺:向阳百分百】D.基态N原子的价层电子排布为2s22p3,其电子排布图为 ,D正确;
故答案选C。
考向三 共价微粒结构式书写及判断
7.(21·22·北京·高考真题)下列化学用语或图示表达不正确的是
A.乙炔的结构简式:
B.顺 丁烯的分子结构模型:
C.基态 原子的价层电子的轨道表示式:
D. 的电子式:
【答案】C
【详解】A.乙炔中含有碳碳三键,其结构简式为 ,A项正确;
B.顺 丁烯中两个甲基位于双键同侧,其结构模型为 ,B项正确;
C.基态 原子的价层电子排布式为3s23p2,其轨道表示式为 ,C项错误;
D. 是离子化合物,其电子式为 ,D项正确;
答案选C。
8.(22·23下·北京·高考真题)下列化学用语或图示表达正确的是
A. 的电子式为
B. 的VSEPR模型为
C. 电子云图为
D.基态 原子的价层电子轨道表示式为
资料整理【淘宝店铺:向阳百分百】【答案】C
【详解】A.氯化钠是离子化合物,其电子式是 ,A项错误;
B.氨分子的VSEPR模型是四面体结构,B项错误:
C.p能级电子云是哑铃(纺锤)形,C项正确;
D.基态铬原子的价层电子轨道表示式是 ,D项错误;
故选C。
9.(22·23·浙江·高考真题)下列化学用语表示正确的是
A.中子数为18的氯原子:
B.碳的基态原子轨道表示式:
C. 的空间结构: (平面三角形)
D. 的形成过程:
【答案】C
【详解】A.质量数=质子数+中子数,质量数标注于元素符号左上角,质子数标注于左下角,中子数为18
的氯原子的质量数为17+18=35,核素符号为 ,故A错误;
B.基态碳原子的核外电子排布式为1s22s22p2,根据洪特规则,2p轨道上的2个电子应该分别在2个轨道
上,且自旋方向相同,轨道表示式: ,故B错误;
C.BF 的中心原子B原子孤电子对数= =0,价层电子对数=3,空间构型为平面三角形,空间结构模型
3
为: ,故C正确;
D.HCl是共价化合物,不存在电子得失,其形成过程应为 ,故D错误;
故选:C。
考向四 微粒电子式的书写及判断
10.(20·21·北京·高考真题)下列化学用语或图示表达不正确的是
A.N 的结构式:N≡N B.Na+的结构示意图:
2
资料整理【淘宝店铺:向阳百分百】C.溴乙烷的分子模型: D.CO 的电子式:
2
【答案】D
【详解】A.N 分子中N原子间是三键,结构式:N≡N,正确;
2
B.Na+的结构示意图: ,正确;
C.溴乙烷的分子模型: ,正确;
D.CO 的电子式: ,错误;
2
故选D。
11.(21·22上·浙江·高考真题)下列表示正确的是
A.甲醛的电子式 B.乙烯的球棍模型
C.2-甲基戊烷的键线式 D.甲酸乙酯的结构简式CHCOOCH
3 3
【答案】B
【详解】A.O原子最外层有6个电子,故甲醛的电子式为 ,A错误;
B.乙烯中碳原子之间以双键形式存在,乙烯的球棍模型为 ,B正确;
C.2-甲基戊烷的键线式为 ,C错误;
D.甲酸乙酯甲酸和乙醇酯化得到,故甲酸乙酯的结构简式为HCOOCH CH,D错误;
2 3
故答案选B。
12.(20·21·江苏·高考真题)反应Cl+2NaOH=NaClO+NaCl+H O可用于制备含氯消毒剂。下列说法正确
2 2
的是
A.Cl 是极性分子
2
B.NaOH的电子式为
C.NaClO既含离子键又含共价键
D.Cl-与Na+具有相同的电子层结构
【答案】C
【详解】A.氯气分子结构对称,正负电荷中心重合,为非极性分子,A错误;
B.NaOH为离子化合物,电子式为 ,B错误;
C.NaClO含有钠离子和次氯酸根形成的离子键,含有O原子和Cl原子形成的共价键,C正确;
D.Cl-有3层电子,Na+有2层电子,D错误;
资料整理【淘宝店铺:向阳百分百】综上所述答案为C。
考向五 微粒间的相互关系
13.(21·22·天津·高考真题)下列叙述错误的是
A. 是极性分子
B. 原子的中子数为10
C. 与 互为同素异形体
D. 和 互为同系物
【答案】D
【详解】A. 是“V”形结构,不是中心对称,属于极性分子,故A正确;
B. 原子的中子数18−8=10,故B正确;
C. 与 是氧元素形成的不同单质,两者互为同素异形体,故C正确;
D. 属于酚, 属于醇,两者结构不相似,因此两者不互为同系物,故D错误。
综上所述,答案为D。
14.(21·22下·浙江·高考真题)下列说法不正确的是
A.乙醇和丙三醇互为同系物
B. 和 互为同位素
C. 和 互为同素异形体
D.丙酮( )和环氧丙烷( )互为同分异构体
【答案】A
【详解】A.结构相似,组成上相差若干个CH 原子团的有机化合物为同系物,乙醇(CHCHOH)是饱和一
2 3 2
元醇,丙三醇是饱和三元醇,两者所含官能团数目不同,不互为同系物,A错误;
B.质子数相同、中子数不同的同种元素互为同位素,35Cl的质子数为17,中子数为18,37Cl的质子数为
17,中子数为20,两者质子数相同、中子数不同,互为同位素,B正确;
C.由同种元素组成的不同的单质互为同素异形体,O 和O 是由氧元素组成的不同的单质,两者互为同素
2 3
异形体,C正确;
D.分子式相同、结构不同的化合物互为同分异构体,丙酮和环氧丙烷的分子式相同、结构不同,两者互
为同分异构体,D正确;
答案选A。
15.(20·21下·浙江·高考真题)下列说法正确的是
A. C 和C 互为同位素 B. C H 和C H 互为同系物
60 70 2 6 6 14
C. CO和CO 互为同素异形体 D.CHCOOH和CHOOCH是同一种物质
2 3 3
资料整理【淘宝店铺:向阳百分百】【答案】B
【详解】A.同种元素的不同种核素互称同位素,C 和C 为C元素的两种不同单质,不能互称同位素,
60 70
A错误;
B.C H 和C H 均为烷烃,二者结构类似,分子组成上相差4个CH 基团,二者互为同系物,B正确;
2 6 6 14 2
C.同种元素的不同种单质互称同素异形体,CO和CO 为C元素的两种不同氧化物,二者不是单质,不能
2
互称同素异形体,C错误;
D.两种物质的结构不同,不是同一种物质,二者互称同分异构体,D错误;
故答案选B。
(建议用时:25分钟)
1.(22·23上·台州·一模)下列说法正确的是
A. 、 、 互为同素异形体
B.HCHO和 最简式相同
C. 和 互为同分异构体
D.正丁烷和环己烷互为同系物
【答案】B
【详解】A.H、D、T 都是同位素形成的不同单质,属于同一种物质,不属于同素异形体,故A错误;
2 2 2
B.HCHO与C H O 的最简式都是CHO,故B正确;
6 12 6 2
C.HCOOCH 与CHOCHO的分子式相同,但结构也是相同的,属于同一种物质,不属于同分异构体,故
3 3
C错误;
D.正丁烷的分子式为C H ,环己烷的分子式为C H ,二者分子结构不同,不属于同系物,故D错误;
4 10 6 12
故本题选B。
2.(22·23上·浙江·一模)下列化学用语表述正确的是
A. 的球棍模型:
B.NaCl晶体的晶胞:
C.丁二烯的键线式:
D.基态Cr原子的价层电子轨道式:
【答案】D
【详解】A.该模型为 的空间充填模型而非球棍模型,A错误;
资料整理【淘宝店铺:向阳百分百】B.晶胞要求是“无隙并置”,B选项给出的立方体平移一个单位后,顶点并不能重叠,所以不是NaCl的
晶胞,B错误;
C.丁二烯的键线式为 ,C错误;
D.Cr是第24号元素,价电子排布式为 。根据洪特规则,基态原子中,填入简并轨道的电子总是
先单独分占,且自旋平行,所以Cr的3d能级的电子分占简并轨道且自旋平行,但4s与3d不是简并轨道,
自旋方向不一定平行,D正确;
故选:D。
3.(22·23·大连·模拟预测)下列化学用语错误的是
A. 的VSEPR模型:
B.基态 原子的价电子轨道表示式:
C. 的电子式:
D. 在水溶液中的电离方程式:
【答案】D
【详解】A.水的孤电子对为 =2,所以其VSEPR模型: ,A正确;
B.基态 原子的价电子排布式为3s23p5,所以其轨道表示式: ,B正确;
C.二氧化碳中各原子满足8电子稳定状态,所以中心碳原子与氧原子分别共用两对电子对,CO 的电子式:
2
,C正确;
D. 在水溶液中完全电离生成钾离子、氢离子和硫酸氢根离子,所以其电离方程式为:
,D错误;
故选D。
4.(22·23上·保山·一模)下列化学用语表示不正确的是
A. 的结构示意图:
B.KCl形成过程:
C.乙炔的球棍模型:
D.中子数为6的氮原子:
资料整理【淘宝店铺:向阳百分百】【答案】B
【详解】A.氯元素的原子序数为17,氯离子结构示意图为 ,A正确;
B.氯化钾为离子化合物,形成过程可表示为 ,B错误;
C.乙炔中含有碳碳三键,其球棍模型: ,C正确;
D.中子数为6的氮原子: ,D正确;
故选B。
5.(22·23下·上海·模拟预测)对于反应 ,以下说法正确的是
A.HCl的电子式为 B. 的空间构型为三角锥形
C. 中只含有离子键 D. 的最外层电子排布式是
【答案】B
【详解】A.HCl是共价化合物,电子式为 ,故A错误;
B. 的空间构型为三角锥形,故B正确;
C. 中含有离子键和共价键,故C错误;
D. 的最外层电子达到了8电子稳定结构,排布式是 ,故D错误;
故选B。
6.(22·23上·浙江·一模)下列说法正确的是
A. 互为同位素
B. 互为同素异形体
C.C H 与C H 一定互为同系物
2 4 4 8
D.甘氨酸(H NCH COOH)与硝基乙烷(C HNO )互为同分异构体
2 2 2 5 2
【答案】D
【详解】A.同位素为同种元素的不同核素, 是单质不是核素,故A错误;
B.同素异形体的分析对象为单质,而 为离子,与单质不能互为同素异形体,故B错误;
C.C H 可能为烯烃或环烷烃,若为环烷烃时不能与乙烯互为同系物,故C错误;
4 8
D.硝基乙烷与甘氨酸的分子式均为C HNO ,但结构不同,互为同分异构体,故D正确;
2 5 2
故选D。
7.(22·23下·辽宁·模拟预测)实验室利用 制备 的原理是
。下列有关叙述错误的是
资料整理【淘宝店铺:向阳百分百】A.基态 的价层电子排布式为
B. 的结构式为
C. 的电子式为
D. 的球棍模型为
【答案】D
【详解】A.Co是27号元素,基态Co的价层电子排布式为 ,则基态 的价层电子排布式为 ,
故A正确;
B. 的结构式为 ,故B正确;
C. 是离子化合物,电子式为 ,故C正确;
D. 的球棍模型为 ,故D错误;
故选D。
8.(22·23·鞍山·模拟预测)下列关于物质的结构或性质描述正确的是
A. 的空间填充模型:
B.基态As原子的简化电子排布式为
C. 的水解方程式为:
D.第二周期元素中,基态原子第一电离能比O大的元素共有3种
【答案】D
【详解】A. 的空间结构为正四面体, 是平面结构,A错误;
B.基态As原子的简化电子排布式为 ,B错误;
C. 为 的电离方程式, 的水解方程式为:
,C错误;
D.第二周期元素中,基态原子第一电离能比O大的元素有 共3种,D正确;
故选D。
资料整理【淘宝店铺:向阳百分百】9.(22·23下·滨海新·三模)下列化学用语或图示不正确的是
A.甲醛和乙酸的实验式均为:CHO
2
B.自由基 的电子式:
C.反-2-丁烯的分子的球棍模型:
D.HCl分子中σ键的形成:
【答案】C
【详解】A.甲醛(HCHO)和乙酸(CHCOOH)的实验式均为:CHO,A正确;
3 2
B.自由基I的最外层有7个电子,故电子式: ,B正确;
⋅
C. 为顺-2-丁烯的分子的球棍模型,C错误;
D.σ键为头碰头方式重叠,HCl分子中σ键的形成: ,D正确;
故答案为:C。
10.(22·23下·海南·一模)化合物ClF 可用作燃烧剂、推进剂中的氧化剂、高温金属的切割油等,能与
3
NH 发生反应: 。下列叙述正确的是
3
A. 的电子式为
B.上述反应产生 时,转移
C. 键的键长比 键的键长短
D. 晶体中存在离子键、 键、配位键
【答案】D
【详解】A.NH 是共价化合物,其电子式为 ,A错误;
3
B.分析反应 可知,该反应过程中转移电子为6e-,故上述反应产生1molCl
2
时,转移6mole-,B错误;
C.已知Cl的原子半径大于F的原子半径,故 键的键长比 键的键长长,C错误;
D.NH F晶体中存在 和F-之间的离子键、 内部的N-H均为 键,还存在一个N→H配位键,D
4
正确;
资料整理【淘宝店铺:向阳百分百】故答案为:D。
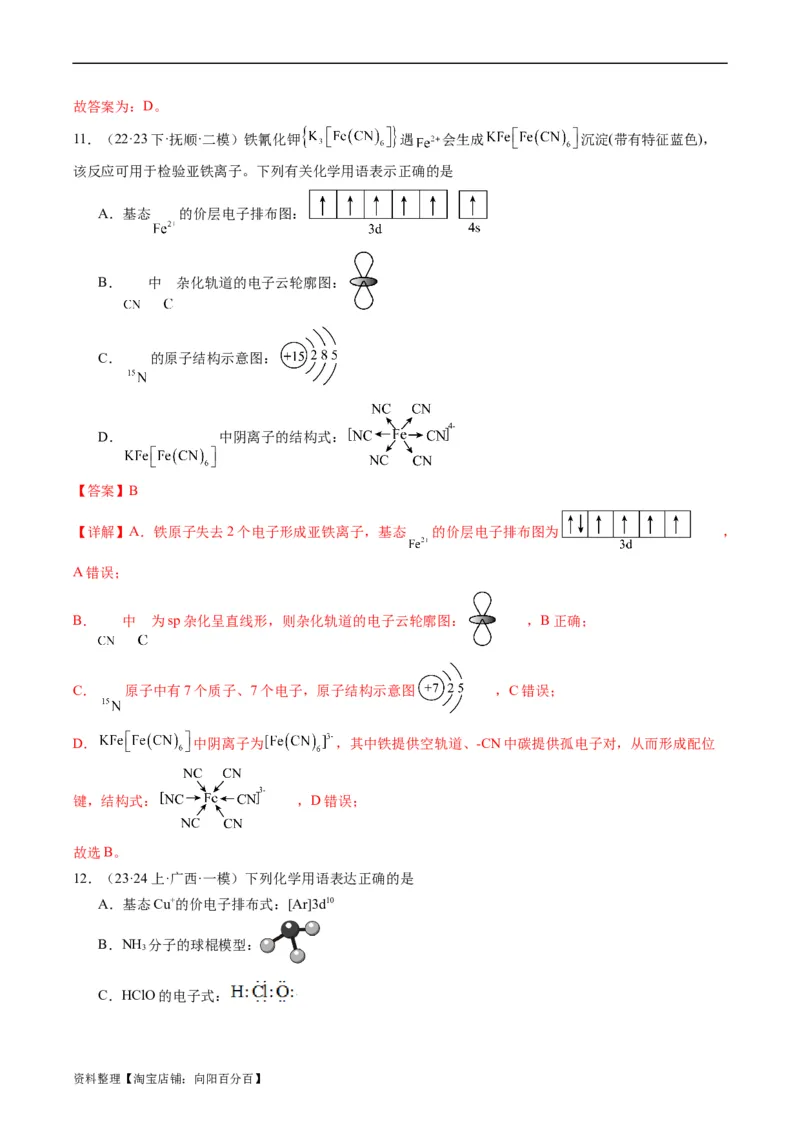
11.(22·23下·抚顺·二模)铁氰化钾 遇 会生成 沉淀(带有特征蓝色),
该反应可用于检验亚铁离子。下列有关化学用语表示正确的是
A.基态 的价层电子排布图:
B. 中 杂化轨道的电子云轮廓图:
C. 的原子结构示意图:
D. 中阴离子的结构式:
【答案】B
【详解】A.铁原子失去2个电子形成亚铁离子,基态 的价层电子排布图为 ,
A错误;
B. 中 为sp杂化呈直线形,则杂化轨道的电子云轮廓图: ,B正确;
C. 原子中有7个质子、7个电子,原子结构示意图 ,C错误;
D. 中阴离子为 ,其中铁提供空轨道、-CN中碳提供孤电子对,从而形成配位
键,结构式: ,D错误;
故选B。
12.(23·24上·广西·一模)下列化学用语表达正确的是
A.基态Cu+的价电子排布式:[Ar]3d10
B.NH 分子的球棍模型:
3
C.HClO的电子式:
资料整理【淘宝店铺:向阳百分百】D.质量数为238、中子数为146的铀(U)原子: U
【答案】B
【详解】A.Cu为29号元素,其电子排布式为1s22s22p63s23p63d104s1,基态Cu+的价电子排布式:3d10,故
A错误;
B.氨分子为三角锥结构,氨气分子的球棍模型为: ,故B正确;
C.HClO的结构式为H-O-Cl,电子式是 ,故C错误;
D.质量数为238、中子数为146的铀(U)原子,质子数等于238-146=92,该原子表示为: ,故D错误。
答案选B。
13.(22·23下·淮安·模拟预测) 可发生水解反应 ,下列说法正确的是
A. 分子空间构型为三角锥型
B. 的VSEPR模
C.质量数为35、中子数为18的Cl原子,
D.用电子式表示 的形成过程:
【答案】A
【详解】A. 中氮原子形成了3个σ键,有1对孤电子对,价层电子对数为4,其空间构型为:三角
锥形,A正确;
B. 中氧原子形成了2个σ键,有2对孤电子对,价层电子对数为4,其VSEPR模型为四面体型,B
错误;
C.质量数为35、中子数为18的Cl原子, ,C错误;
D.水为共价化合物,则用电子式表示 的形成过程为: ,D错误;
故选A。
14.(23·24上·湛江·模拟预测)下列化学用语或图示表达正确的是
A.金刚石的晶体结构:
资料整理【淘宝店铺:向阳百分百】B.基态溴原子电子占据最高能级的电子云轮廓图:
C. 的空间填充模型:
D. 的电子式:
【答案】A
【详解】A.金刚石的晶胞中一个碳原子与其他四个碳原子构成正四面体,选项A正确;
B.基态溴原子电子占据的最高能级是p能级,电子云轮廓图是哑铃形,选项B错误;
C. 的空间结构是正四面体,不是平面结构,选项C错误;
D. 的电子式中碳原子周围是6个电子,选项D错误;
答案选A。
15.(23·24上·郴州·一模)下列有关化学用语的表示错误的是
A.原子核内有8个中子的碳原子: C
B.基态Ga原子的简化电子排布式为[Ar]4s24p1
C.CO 的空间结构为:平面三角形
D.HCl分子中σ键的形成:
【答案】B
【详解】A.原子核内有8个中子的碳原子表示为: C,A正确;
B.基态Ga原子的简化电子排布式为[Ar]3d104s24p1,B错误;
C.CO 中价层对数为3,无孤对电子,故空间构型为平面三角形,C正确;
D.HCl分子中σ键的形成为: ,D正确;
故选B。
16.(22·23下·梅州·三模)下列化学用语的表示不正确的是
A.中子数为2的氢核素:
B. 的电子式:
资料整理【淘宝店铺:向阳百分百】C.基态铬原子的价电子排布式:
D. 的空间结构模型:
【答案】C
【详解】A.该氢核素的质子数为1、中子数为2,其质量数为3,A项正确;
B. 是共价化合物,电子式为 ,B项正确;
C.基态铬原子的电子排布式为 ,其价电子排布式是 ,C项错误;
D. 的价层电子对数为3+ (4+2-3×2)=3,无孤电子对,其空间结构为平面三角形,D项正确;
故选C。
17.(22·23下·浙江·二模)下列表示不正确的是
A.苯的实验式:
B. 共价键电子云轮廓图:
C.己烷共有4种同分异构体,它们的熔点、沸点各不相同
D.聚合物( )可由单体 和 加聚制得
【答案】C
【详解】A.苯的分子式:C H,其实验式: ,故A正确;
6 6
B. 中H、Cl原子轨道头碰头形成 键,共价键电子云轮廓图: ,故B正确;
C.己烷共有5种同分异构体,故C错误;
D.单体 和 可以发生加聚反应,生成 ,故D正
确;
答案选C。
18.(23·24上·大庆·模拟预测)下列化学用语表达正确的是
A.碳的基态原子的轨道表示式:
B.甲烷分子和四氯化碳分子的空间填充模型均为:
C.CHCH(CH )CHCOOH 的名称:2-甲基丁酸
3 3 2
资料整理【淘宝店铺:向阳百分百】D.CHOH分子中,碳原子与氧原子之间的共价键: sp3 p 键
3
【答案】A
【详解】A.碳的基态原子电子排布式为1s22s22p2,轨道表示式: ,故A正确;
B.甲烷分子和四氯化碳分子都是正四面体形,但原子半径:Cl>C>H,该模型不能表示四氯化碳分子的空
间填充模型,故B错误;
C.CHCH(CH )CHCOOH中羧基碳为1号碳,甲基在3号碳原子上,命名为:3-甲基丁酸,故C错误;
3 3 2
D.CHOH分子中C原子杂化方式为sp3杂化,O原子杂化方式也是sp3杂化,碳原子与氧原子之间的共价
3
键:sp3-sp3σ键,故D错误;
故选A。
19.(22·23上·金华·模拟预测)化学用语是学习化学的重要工具,以下化学用语表述正确的是
A. 的空间填充模型:
B.HClO分子的VSEPR模型:直线形
C.基态 的价电子轨道表示式:
D.1,3-丁二烯的键线式:
【答案】D
【详解】A. 的球棍模型为: ,A错误;
B.HClO分子的中心原子为氧原子,有两个孤对电子,故VSEPR模型为V形,B错误;
C.图示为基态Mn的价电子轨道表示式,基态Mn原子失去电子变成基态 ,需失去最外层4s轨道的
电子,C错误;
D.1,3-丁二烯的结构简式为:CH=CH-CH=CH ,键线式: ,D正确;
2 2
故选D。
20.(23·24上·温州·一模)下列化学用语表示正确的是
A.溴的简化电子排布式:
B.1-丁醇的键线式:
C. 形成的 键模型:
D.水的VSEPR模型:
【答案】D
资料整理【淘宝店铺:向阳百分百】【详解】A.溴位于周期表中第4周期第ⅤⅡA族,核外电子数35,电子排布式为 ,选项
A错误;
B.1-丁醇的键线式为 ,而 为1-丙醇,选项B错误;
C. 形成的 键模型: ,选项C错误;
D.HO中价层电子对个数=2+ =4,且含有2个孤电子对,所以HO的VSEPR模型为四面体
2 2
,选项D正确;
答案选D。
资料整理【淘宝店铺:向阳百分百】资料整理【淘宝店铺:向阳百分百】