文档内容
课堂检测·素养达标
1.对电解质概念理解正确的是 ( )
A.在水溶液或熔融状态下能导电的物质
B.凡在水中能生成离子因而能导电的物质
C.氧化钠溶于水能电离生成钠离子和氢氧根离子,尽管氧化钠是化合物,其水溶
液能导电,但溶液中的氢氧根离子并非氧化钠本身电离,因而氧化钠是非电解质
D.在水溶液里或熔融状态下本身能电离出阳离子和阴离子,因而能导电的化合
物
2.(教材改编)下列物质中属于能导电的电解质的是 ( )
A.KNO 固体 B.石墨
3
C.熔融的MgCl D.NaCl溶液
2
【补偿训练】
下列物质既不是电解质,又不是非电解质的是 ( )
A.NaHSO B.Cu(OH)
4 2
C.O D.HCl
23.喝电解质饮料对人体有好处,尤其在锻炼时更为明显。电解质是人体维持适
当功能必需的,但它们会通过汗水流失。在剧烈运动或过热出汗后,及时补充电
解质对保持健康很重要。
酸、碱、盐是从电离特点上对电解质的分类。下列关于酸、碱、盐的说法错误
的是 ( )
A.酸、碱、盐都是电解质,电解质只有酸、碱、盐
B.电离时生成的阴离子全部是OH-的化合物才可能是碱
C.电离时生成的阳离子全部是H+的化合物才可能是酸
D.只要电离时能生成金属阳离子和酸根阴离子的化合物就是盐
4.下列电离方程式书写正确的是 ( )
A.MgSO Mg+2+S
4
B.Ba(OH) Ba2++OH-
2
C.KCl K++Cl-
D.Ca(NO ) Ca2++2(N )
3 25.下列关于纯净物、混合物、电解质和非电解质的正确组合是
( )
纯净物 混合物 电解质 非电解质
A 浓盐酸 天然气 硫酸 干冰
B 氢氧化钡 蔗糖溶液 硫酸钡 三氧化硫
C 胆矾 石灰水 KOH 碳酸钙
D 硫酸 铝合金 氯化钠 氢气
6.判断下列物质在相应条件下能否电离,不能电离的说明理由,能电离的写出电
离方程式。
(1)液态HCl:________, ________________________。
(2)熔融状态下的NaCl:________,____________________。
(3)高温熔化后的单质铁:________,_______________________。
(4)固体KOH:________,___________________________。
【补偿训练】
NaHSO 通常为晶体,易溶于水,它溶于水时电离出三种不同的离子,溶液显
4
酸性。NaHSO 受热熔化时只能电离出两种不同离子。试回答下列问题:
4
(1)NaHSO 在水中和熔融状态下的电离有什么不同?(用电离方程式表示)
4
_________________________________________________________
(2)NaHSO 在物质分类中属于哪一类物质?能否与Zn反应生成氢气?
4
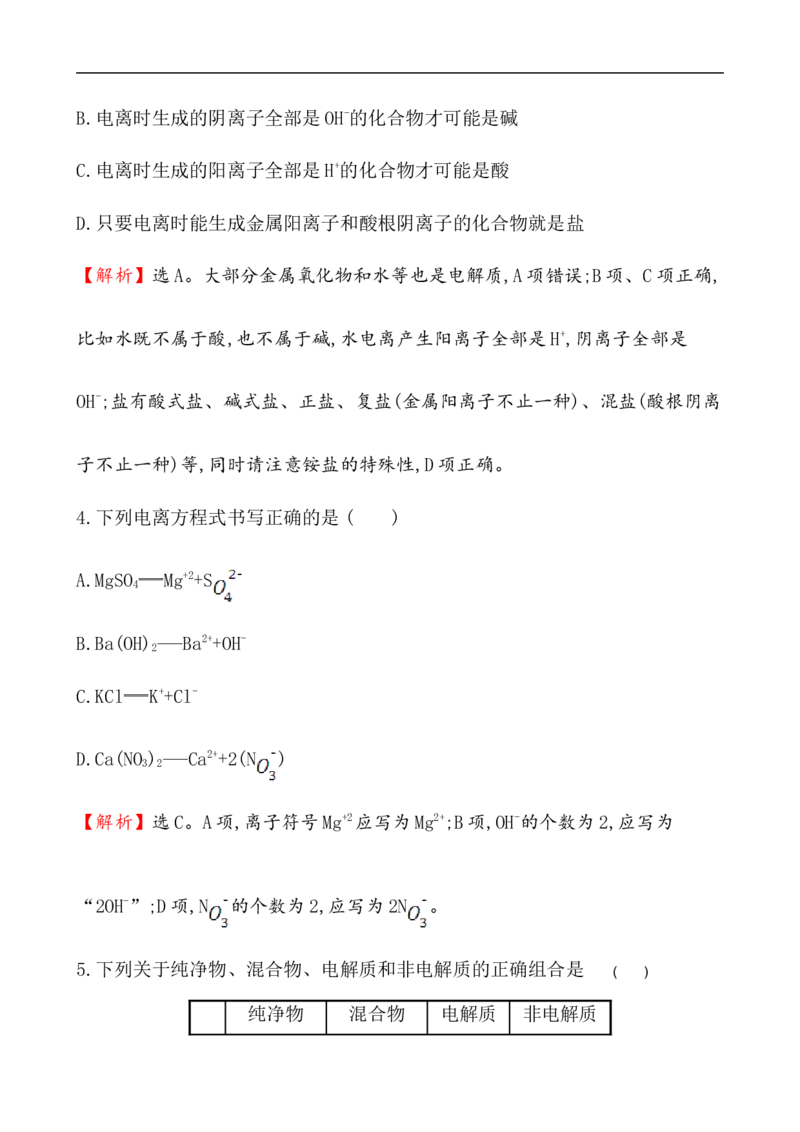
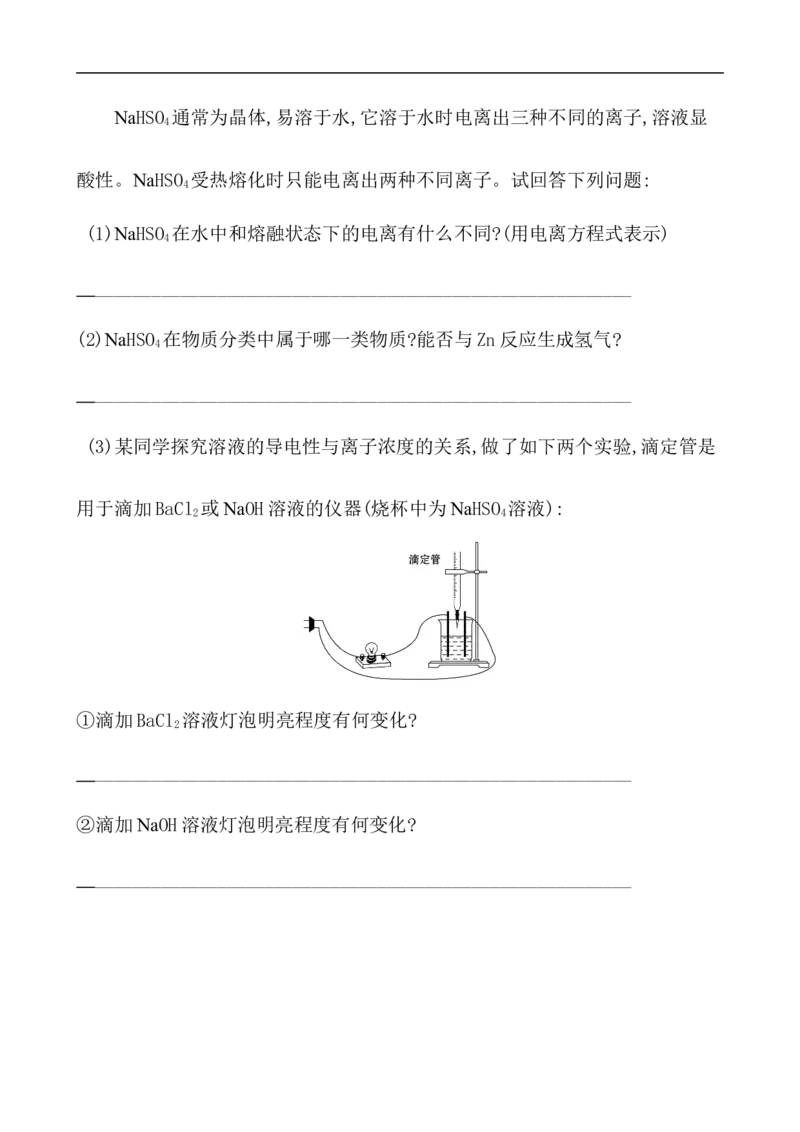
_________________________________________________________(3)某同学探究溶液的导电性与离子浓度的关系,做了如下两个实验,滴定管是
用于滴加BaCl 或NaOH溶液的仪器(烧杯中为NaHSO 溶液):
2 4
①滴加BaCl 溶液灯泡明亮程度有何变化?
2
_________________________________________________________
②滴加NaOH溶液灯泡明亮程度有何变化?
_________________________________________________________课堂检测·素养达标
1.对电解质概念理解正确的是 ( )
A.在水溶液或熔融状态下能导电的物质
B.凡在水中能生成离子因而能导电的物质
C.氧化钠溶于水能电离生成钠离子和氢氧根离子,尽管氧化钠是化合物,其水溶
液能导电,但溶液中的氢氧根离子并非氧化钠本身电离,因而氧化钠是非电解质
D.在水溶液里或熔融状态下本身能电离出阳离子和阴离子,因而能导电的化合
物
【解析】选D。A项中未说明该物质是化合物还是单质,说法不严密,错误;B项
未说明在水中生成的离子是化合物本身产生的,故不能成为判断电解质的依据,
错误;C项氧化钠属于离子化合物,本身就是由离子构成的,溶于水时因能与水反
应生成Na+和OH-,但氧化钠在熔融状态下能导电,因此,氧化钠是电解质,错误。
2.(教材改编)下列物质中属于能导电的电解质的是 ( )
A.KNO 固体 B.石墨
3
C.熔融的MgCl D.NaCl溶液
2【解析】选C。KNO 固体属于电解质但不导电,A错误;石墨虽然导电,但属于单
3
质,B错误;熔融的MgCl 属于电解质且能导电,C正确; NaCl溶液能导电,但属于
2
混合物,D错误。
【补偿训练】
下列物质既不是电解质,又不是非电解质的是 ( )
A.NaHSO B.Cu(OH)
4 2
C.O D.HCl
2
【解析】选C。O 为单质,既不是电解质,也不是非电解质。
2
3.喝电解质饮料对人体有好处,尤其在锻炼时更为明显。电解质是人体维持适
当功能必需的,但它们会通过汗水流失。在剧烈运动或过热出汗后,及时补充电
解质对保持健康很重要。
酸、碱、盐是从电离特点上对电解质的分类。下列关于酸、碱、盐的说法错误
的是 ( )
A.酸、碱、盐都是电解质,电解质只有酸、碱、盐B.电离时生成的阴离子全部是OH-的化合物才可能是碱
C.电离时生成的阳离子全部是H+的化合物才可能是酸
D.只要电离时能生成金属阳离子和酸根阴离子的化合物就是盐
【解析】选A。大部分金属氧化物和水等也是电解质,A项错误;B项、C项正确,
比如水既不属于酸,也不属于碱,水电离产生阳离子全部是H+,阴离子全部是
OH-;盐有酸式盐、碱式盐、正盐、复盐(金属阳离子不止一种)、混盐(酸根阴离
子不止一种)等,同时请注意铵盐的特殊性,D项正确。
4.下列电离方程式书写正确的是 ( )
A.MgSO Mg+2+S
4
B.Ba(OH) Ba2++OH-
2
C.KCl K++Cl-
D.Ca(NO ) Ca2++2(N )
3 2
【解析】选C。A项,离子符号Mg+2应写为Mg2+;B项,OH-的个数为2,应写为
“2OH-”;D项,N 的个数为2,应写为2N 。
5.下列关于纯净物、混合物、电解质和非电解质的正确组合是
( )
纯净物 混合物 电解质 非电解质A 浓盐酸 天然气 硫酸 干冰
B 氢氧化钡 蔗糖溶液 硫酸钡 三氧化硫
C 胆矾 石灰水 KOH 碳酸钙
D 硫酸 铝合金 氯化钠 氢气
【解析】选B。A项,浓盐酸是HCl的水溶液,属于混合物;C项,碳酸钙属于电解
质;D项,氢气既不是电解质也不是非电解质。
6.判断下列物质在相应条件下能否电离,不能电离的说明理由,能电离的写出电
离方程式。
(1)液态HCl:________, ________________________。
(2)熔融状态下的NaCl:________,____________________。
(3)高温熔化后的单质铁:________,_______________________。
(4)固体KOH:________,___________________________。
【解析】HCl在液态时不电离;NaCl在熔融状态下可以电离;Fe是单质,任何条
件下都不电离;KOH在固态时不电离。
答案:(1)不能 液态HCl以分子形式存在,不电离
(2)能 NaCl(熔融) Na++Cl-
(3)不能 Fe是金属单质,通过自由电子而导电
(4)不能 KOH在固态时离子运动受到束缚
【补偿训练】NaHSO 通常为晶体,易溶于水,它溶于水时电离出三种不同的离子,溶液显
4
酸性。NaHSO 受热熔化时只能电离出两种不同离子。试回答下列问题:
4
(1)NaHSO 在水中和熔融状态下的电离有什么不同?(用电离方程式表示)
4
_________________________________________________________
(2)NaHSO 在物质分类中属于哪一类物质?能否与Zn反应生成氢气?
4
_________________________________________________________
(3)某同学探究溶液的导电性与离子浓度的关系,做了如下两个实验,滴定管是
用于滴加BaCl 或NaOH溶液的仪器(烧杯中为NaHSO 溶液):
2 4
①滴加BaCl 溶液灯泡明亮程度有何变化?
2
_________________________________________________________
②滴加NaOH溶液灯泡明亮程度有何变化?
_________________________________________________________【解析】NaHSO 溶于水电离出三种离子,且呈酸性,则它电离出的离子是Na+、
4
H+、S ;它受热熔化时只能电离出两种离子,分别是Na+和HS ;由其电离情况
知,NaHSO 既是盐又是电解质,不属于酸,NaHSO 溶液中有H+,能与Zn反应生成
4 4
H 。
2
答案:(1)NaHSO Na++H++S
4
NaHSO (熔融) Na++HS
4
(2) NaHSO 属于酸式盐类物质,NaHSO 溶液能与Zn反应生成氢气。
4 4
(3)①变暗。BaCl 与NaHSO 溶液中的S 反应生成BaSO 沉淀,使离子浓度减
2 4 4
小,导电性减弱。
②变暗。NaOH与NaHSO 溶液中的H+反应生成水,使离子浓度减小,导电性减弱。
4