文档内容
物质的量(1)
重难点 题型 分值
1. 理解摩尔(mol)是物质的量的基本单位,可用于进
行简单的化学计算。
2. 了解物质的量的单位——摩尔(mol)、摩尔质量、
重点 气体摩尔体积、阿伏加德罗常数的含义。
3. 能根据物质的量与微粒(原子、分子、离子等)数 选 择 与
10-14分
目、气体体积(标准状况下)之间的相互关系进行有关 填空
计算。
能根据物质的量与微粒(原子、分子、离子等)数目、
难点 气体体积(标准状况下)之间的相互关系进行有关计
算。
第1页核心知识点一:
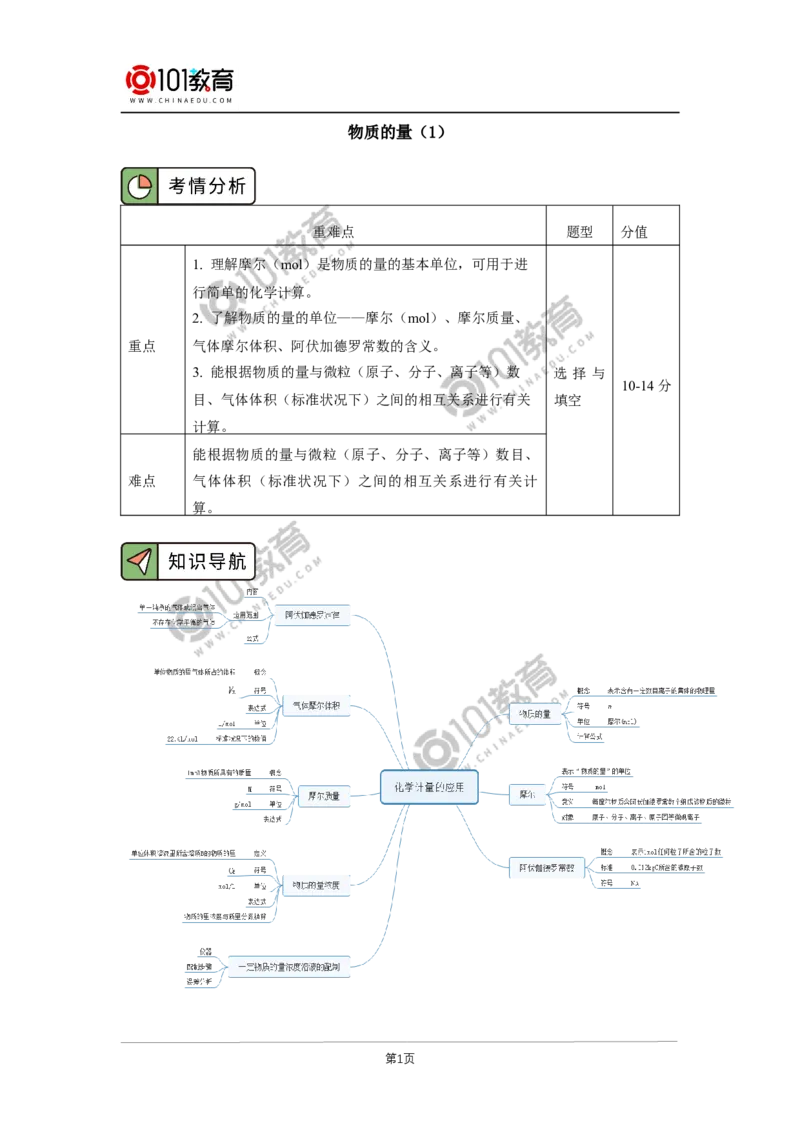
一、物质的量、阿伏加德罗常数
1. 物质的量
①物质的量是表示含有一定数目粒子的集合体的物理量,用符号n 表示。
②物质的量的单位——摩尔
2. 应用物质的量具有的问题
①物质的量是一个整体,不可拆开
②物质的量仅用于计量微观粒子(分子、原子、离子、电子、中子、质子等),不适
用于宏观物质。
③摩尔不是物理量,只是物质的量的这个物理量的单位。
④物质的量描叙的对象搜粒子的集体,但没有限定是何种粒子集体,因此,我们在使
用摩尔表示物质的量时,要指明粒子(分子、原子、粒子、质子、电子等)的种类。
使用物质的量时要用化学式指明粒子种类或其组合,不用该粒子的中文名称,应表示
为:1molH
⑤物质的量的数值可以是整数,也可以是小数。
思考:已知:一个碳原子的质量为1. 993 ×10−23g,求0. 012kg12C中所含的碳原子数?
3. 阿伏加德罗常数
(1)已知1个12C的实际质量为1.993 3×10-23 g,则12 g 12C所含碳原子个数约为6.
02×10 23 ,碳原子的物质的量为 1 摩尔 。
(2)阿伏加德罗常数的基准量为 0. 012_kg_ 12 C 中所含的原子个数 ,近似值为 6.
02×10 23 。
(3)阿伏加德罗常数是1摩尔任何粒子的粒子数,符号是N ,单位是 mol - 1 。
A
N
N
(4)物质的量、阿伏加德罗常数与粒子数之间的关系:n= A 。
4. 阿伏加德罗常数的理解及应用
(1)阿伏加德罗常数是指1 mol任何粒子的粒子数,这里的粒子指同种粒子,如1
mol O 中的分子数为N ,而1 mol O 中的氧原子数为2N 。
2 A 2 A
(2)阿伏加德罗常数有单位(mol-1),是一个准确值,而6. 02×1023无单位,是一个
第2页纯数值。阿伏加德罗常数与6. 02×1023的关系就像π与3. 14的关系,6. 02×1023是阿伏加德
罗常数的近似值,计算时通常使用这个近似值,而在叙述或定义“摩尔”的概念时要用
“阿伏加德罗常数”来表示。
(3)考查一定物质的量的物质中含有多少粒子(分子、原子、质子、电子等),注意
看清粒子的种类,常涉及稀有气体He、Ne等单原子分子,N 、O 等双原子分子及O 等多
2 2 3
原子分子。
二、摩尔质量
1. 摩尔质量
2. 摩尔质量概念的理解
(1)等值性:摩尔质量以g·mol-1作单位时,在数值上与其相对分子质量或相对原子
质量相等。
(2)确定性:对于指定的物质来说,其摩尔质量的值是一个定值,不随物质的物质的
量的多少而改变。
3. 摩尔质量的归纳总结
(1)摩尔质量——“四性”
①等值性:摩尔质量以g·mol-1作单位时,在数值上与其相对分子质量或相对原子质量
相等。
②近似性:由于电子的质量非常微小,所以离子的摩尔质量以g·mol-1为单位时,其数
值近似等于相对原子质量,如Na和Na+的摩尔质量都为23 g·mol-1。
③确定性:对于指定的物质来说,其摩尔质量的值是一个定值,不随物质的物质的量
的多少而改变。
④混合性:对于混合物来说,只要其组成一定,1 mol该混合物的质量就是该混合物的
平均摩尔质量。
(2)物质的量的相关概念比较
概念 含义 注意事项
物质的量 衡量一定数目微观粒子集合 ①表示的是微观粒子的集合体多少,不是
第3页宏观物质的数量,是一个整体,不可拆
分;
体多少的物理量:n
②“物质的量”是联系宏观物质和微观粒
子的桥梁
①因其所代表的数量巨大,只能用来描述
①物质的量的单位:mol; 具体的微观粒子,表示宏观物质没意义;
摩尔 ②基准:0. 012 kg 12C所含 ②用“mol”衡量微观粒子时,必须用化学
的碳原子数为1 mol 式指明粒子的种类,如“1 mol O”“2 mol
2−
O”“1. 5 mol SO4 ”
2
①N 是一个实验值,现取6. 02×1023作计
A
阿伏加德罗 1 mol微观粒子的粒子数,符
算依据;
常数 号:N
A
②N 的单位:mol-1
A
①单位物质的量的物质所具
①适用于任何一种微观粒子;
有的质量;
摩尔质量 ②纯净物和混合物都有摩尔质量,混合物
②符号:M;
的摩尔质量一般称为平均摩尔质量
③单位:g/mol或g·mol-1
三、关于物质的量的简单计算
1. 基本关系式
N
N
(1)n= A (n表示物质的量,N表示粒子数)。关系式中N 的单位是 mol - 1 。
A
m
n
(2)M= (M为摩尔质量,m为物质的质量)。
在M、n和m中,已知任意两项求第三项;若 M的单位是 g·mol - 1 时,则m的单位是
g。
2. 恒等关系式
N m N m
N M N M
由基本关系式n= A 和n= 可得恒等关系式: A = 。在N、N 、m、M中,
A
已知任意三项可求第四项。一般情况下,N 、M是已知的,则N与m可互求。
A
核心知识点二:
一、气体摩尔体积
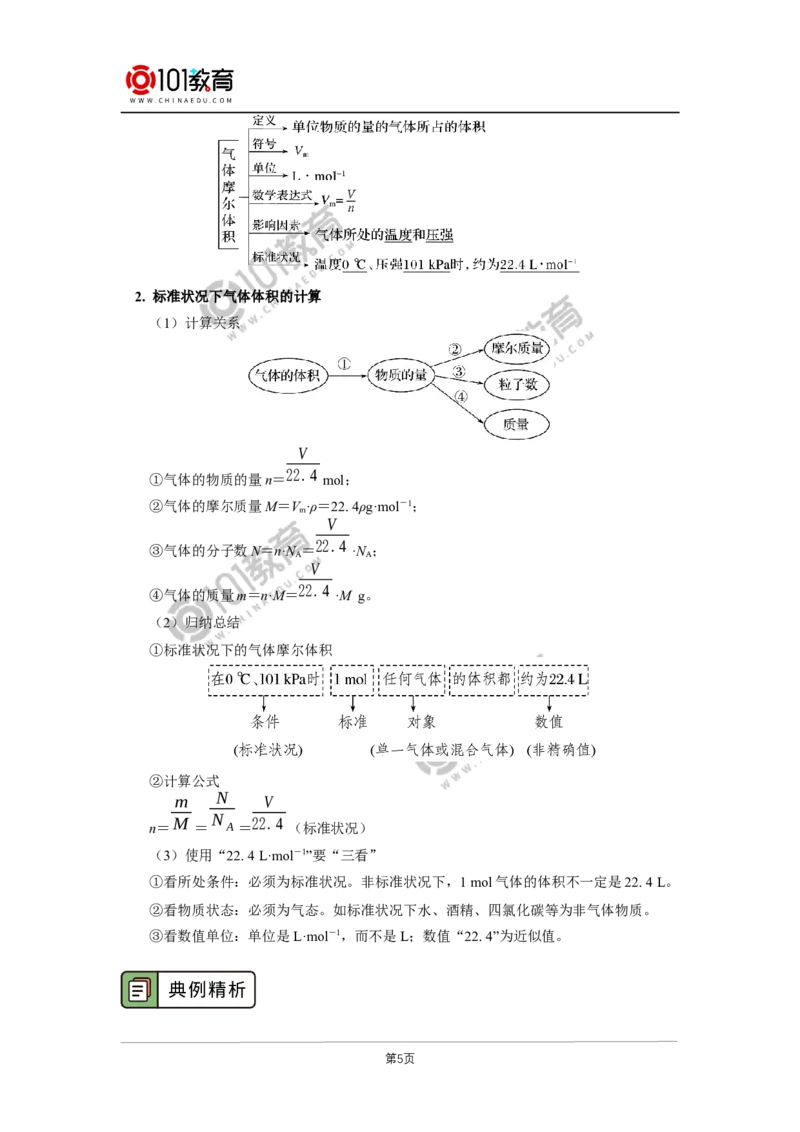
1. 气体摩尔体积
第4页2. 标准状况下气体体积的计算
(1)计算关系
V
22.4
①气体的物质的量n= mol;
②气体的摩尔质量M=V ·ρ=22. 4ρg·mol-1;
m
V
22.4
③气体的分子数N=n·N = ·N ;
A A
V
22.4
④气体的质量m=n·M= ·M g。
(2)归纳总结
①标准状况下的气体摩尔体积
②计算公式
m N V
M N 22.4
n= = A = (标准状况)
(3)使用“22. 4 L·mol-1”要“三看”
①看所处条件:必须为标准状况。非标准状况下,1 mol气体的体积不一定是22. 4 L。
②看物质状态:必须为气态。如标准状况下水、酒精、四氯化碳等为非气体物质。
③看数值单位:单位是L·mol-1,而不是L;数值“22. 4”为近似值。
第5页核心知识点一:
N 是阿伏加德罗常数的值,下列说法不正确的是( )
A
A. 1molH O含有10N 个电子
2 A
B. 2. 5molHe含有5N 个质子
A
C. 6. 02×1022个HSO 在溶液中可电离出N 个H+
2 4 A
D. 1molFe与盐酸完全反应,可以失去2N 个电子
A
【答案】C
【解析】A. 1个HO含有10个电子,1molH O含有10N 个电子
2 2 A
B. 1个He含有2个质子,2. 5molHe含有5N 个质子
A
C. 1个HSO 在溶液中可电离出2个H+,6. 02×1022个HSO 在溶液中可电离出0. 2N
2 4 2 4 A
个H+
D. 1个lFe与盐酸完全反应,可以失去2个电子,1molFe与盐酸完全反应,可以失去
2N 个电子
A
【考点】关于物质的量、阿伏加德罗常数的应用
已知m克二氧化硫气体中所含有的分子数约为3. 01×1022,则m为( )
A. 3. 2g B. 6. 4g C. 9. 6g D. 无法计算
【答案】A
【解析】n=N/N ,所以n=0. 05mol;m=n×M=0. 05mol×64g/mol=3. 2g
A
【考点】物质的量与阿伏伽德罗常数、摩尔质量的相关计算
核心知识点二:
下列说法正确的是( )
A. 32 g O 占有的体积约为22. 4 L
2
B. 22. 4 L N 含有阿伏加德罗常数个氮分子
2
C. 在标准状况下,22. 4 L水的质量约为18g
D. 22g二氧化碳与标准状况下11. 2LHCl含有相同的分子数
【答案】D
【解析】A. 不是在标况下
B. 不在标况下
第6页C. 在标准状况下,水为液体
D. 22g二氧化碳是0. 5mol,与标准状况下11. 2LHCl物质的量也是0. 5mol
【考点】气体的摩尔体积
同温同压下,在两个容积相同的容器中,一个盛有C H 气体,另一个盛有N 和CO的
2 4 2
混合气体。两容器内的气体一定具有相同的( )
①分子数②密度③质量④质子数⑤原子数⑥电子数
A. ①③④ B. ①②⑤ C. ③④⑥ D. ①②③
【答案】D
【解析】①在同温同压下,相同体积的任何气体含有相同的分子数,C H 与N 和CO
2 4 2
的总分子数目相同,正确;②N 和CO的相对分子质量都是28,故混合气体平均相对分子
2
质量为28,C H 的相对分子质量为28,同温同压下,气体密度之比等于相对分子质量之比,
2 4
故两容器内气体的密度相等,正确;③N 、CO和C H 的摩尔质量都是28g/mol,C H 的
2 2 4 2 4
物质的量与N、CO的总物质的量相等时,质量一定相等,正确。④N、CO分子中的质子
2 2
数均为14,C H 分子中的质子数是16,故C H 分子数目与N、CO的总分子数相等时,质
2 4 2 4 2
子数一定不相等,错误;⑤N 、CO是双原子分子,C H 是6原子分子,故C H 分子数目
2 2 4 2 4
与N 、CO的总分子数相等时,原子数一定不相等,错误。⑥N 、CO中的电子数为均为
2 2
14,
C H 分子中的电子数是16,故C H 分子数目与N 、CO的总分子数相等时,电子数一
2 4 2 4 2
定不相等,错误。
【考点】气体摩尔体积使用的注意事项
在标准状况下:①6. 72LCH ,② 3. 01×1023个HCl分子,③13. 6gHS,④0.
4 2
2molNH 。下列对这四种气体的关系从大到小表达不正确的是( )
3
A. 体积:②>③>①>④
B. 密度:②>③>④>①
C. 质量:②>③>④>①
D. 氢原子的个数:①>④>③>②
【答案】D
【解析】①n(CH )=0. 3mol,②n(HCl)=0. 5mol,③n(HS)=0. 4mol,④0.
4 2
2molNH 。
3
第7页A对,相同状况下,气体的物质的量越大,则体积越大,故体积大小为②>③>①>
④
B对,相同状况下,气体摩尔体积相同,根据密度与其摩尔质量成正比,故密度大小
为密度:②>③>④>①
C对,①m(CH )=4. 8g,②m(HCl)=18. 25g,③m(HS)=13. 6g,④m(NH )
4 2 3
=3. 4g。
故质量:②>③>④>①
D错,①n(H)=1. 2mol,②n(H)=0. 5mol,③n(H)=0. 8mol,④n(H)=0.
6mol。
氢原子的个数:①>③>④>②
(答题时间:25分钟)
一、选择题:本题包括12小题,每小题4分,共48分。
1. 下列叙述正确的是( )
①2 mol铁原子 ②1 mol Fe3+ ③0. 5 mol氧
④0. 5 mol 氮气 ⑤氨的摩尔质量是17 g
A. ①③④ B. ①②④⑤ C. ①②④ D. 都正确
2. 1. 6 g某物质中含有6. 02×1022个分子,则该物质的相对分子质量为( )
A. 16 B. 64 C. 32 D. 96
3. 下列物质中含分子数最多的是( )
A. 1. 204×1023个CO 分子
2
B. 0. 6 mol CO
C. 32 g SO
2
D. 1. 6 g H
2
4. 相同质量的SO 和SO ,它们之间的关系是( )
2 3
A. 所含硫原子的物质的量之比为1∶1
B. 氧原子的物质的量之比为3∶2
C. 氧元素的质量比为5∶6
D. 硫元素的质量比为4∶5
5. 在标准状况下,与32 g O 的体积相等的N( )
2 2
A. 质量为14 g
B. 分子数为6. 02×1024
第8页C. 体积为22. 4 L
D. 物质的量为2 mol
6. 相同条件下,等物质的量的两种气体一定满足( )
A. 体积均为22. 4 L
B. 具有相同的体积
C. 是双原子组成的分子
D. 所含原子数目相同
7. 有以下物质:
①6 g H ②0. 5 mol CO ③1. 204×1024个HCl分子 ④147 g H SO ⑤4 ℃时27
2 2 2 4
mL水
(1)它们的物质的量最大的是________。(填序号,下同)
(2)所含分子数最多的是________。
(3)所含原子数最多的是________。
(4)质量最小的是________。
8. 在标准状况下,有33 g二氧化碳、0. 5 mol氢气和5. 6 L氮气三种气体。
(1)其中物质的量最大的是________,质量最小的是________;
(2)物质所含分子数目最多的是________,所含原子数目最少的是________;
(3)物质所占体积最大的是________,这三种气体的体积比为________。
第9页1. 答案:C
【解析】使用摩尔时必须指明微粒的名称,①、②、④正确,③中指代不明确,⑤摩
尔质量的单位是“g/mol”,故选C。
2. 答案:A
【解析】物质的摩尔质量在以g·mol-1为单位时,在数值上等于它的相对分子(或原
子)质量,因而只要求出该物质的摩尔质量即可。由题可知该物质的物质的量 n=0. 1
m 1.6g
n 0.1mol
mol,所以M= = =16 g·mol-1。所以相对分子质量为16。
3. 答案:D
N 1.204×1023
【解析】n(CO)=
N
A =
6.02×1023mol−1
=0. 2 mol;
2
n(CO)=0. 6 mol;
32g
64g⋅mol−1
n(SO )= =0. 5 mol;
2
1.6g
2g⋅mol−1
n(H)= =0. 8 mol。
2
4. 答案:C
1 1
64 80
【解析】相同质量的SO 和SO 的物质的量之比为 ∶ =5∶4,则硫原子的物质
2 3
的量之比为5∶4,硫元素的质量之比也为5∶4,故A、D两项错误;氧原子的物质的量之
比为(5×2)∶(4×3)=5∶6,质量之比亦为5∶6,故C项正确,B项错误。
5. 答案:C
32g
32g⋅mol−1
【解析】:n(O )= =1 mol,V(O )=22. 4 L,因此n(N )=1
2 2 2
mol,m(N)=28 g,N(N)=6. 02×1023,V(N)=22. 4 L。
2 2 2
6. 答案:B
【解析】相同条件(同温、同压)下,相同体积的气体具有相同的分子数(即相同的
物质的量),则具有相同物质的量的气体必具有相同的体积。
7. 答案:(1)① (2)① (3)④ (4)①
6g
2g⋅mol−1
【解析】各物质的物质的量分别为:n(H )= =3 mol,n(CO )=0. 5
2 2
1.204×1023 147g
mol,n(HCl)=
6.02×1023mol−1
=2 mol,n(HSO )=
98g⋅mol−1
=1. 5 mol,n
2 4
第10页27mL×1g⋅cm−3
18g⋅mol−1
(HO)= =1. 5 mol。故①物质的量最大,分子数最多;①~⑤中原子
2
的物质的量依次为6 mol、1. 5 mol、4 mol、10. 5 mol、4. 5 mol,故④中原子数最多;各物
质的质量依次为m(H )=6 g,m(CO )=0. 5 mol×44 g·mol-1=22 g,m(HCl)=2
2 2
mol×36. 5 g·mol-1=73 g,m(HSO )=147 g,m(HO)=27 g,故①的质量最小。
2 4 2
8. 答案:(1)CO H
2 2
(2)CO N
2 2
(3)CO V(CO)∶V(H)∶V(N)=3∶2∶1
2 2 2 2
33g
【解析】(1)n(CO)=
44g⋅mol−1
=0. 75 mol,
2
5.6L
n(N)=
22.4L⋅mol−1
=0. 25 mol,
2
m(H)=0. 5 mol×2 g·mol-1=1 g,
2
m(N)=0. 25 mol×28 g·mol-1=7 g。
2
(2)物质的量最大的气体分子数最多;CO 、H 、N 中原子的物质的量依次为0. 75
2 2 2
mol×3=2. 25 mol、0. 5 mol×2=1 mol、0. 25 mol×2=0. 5 mol。
(3)物质的量最大的气体体积最大;V(CO )∶V(H )∶V(N )=n(CO )∶n
2 2 2 2
(H)∶n(N)=0. 75∶0. 5∶0. 25=3∶2∶1。
2 2
第11页